
1
PATOFIZJOLOGIA
ZABURZEŃ PROLIFERACJI
KOMÓREK
2
W dojrzałym organizmie
(narządzie, tkance) panuje
równowaga między proliferacją a
ubytkiem komórek
3
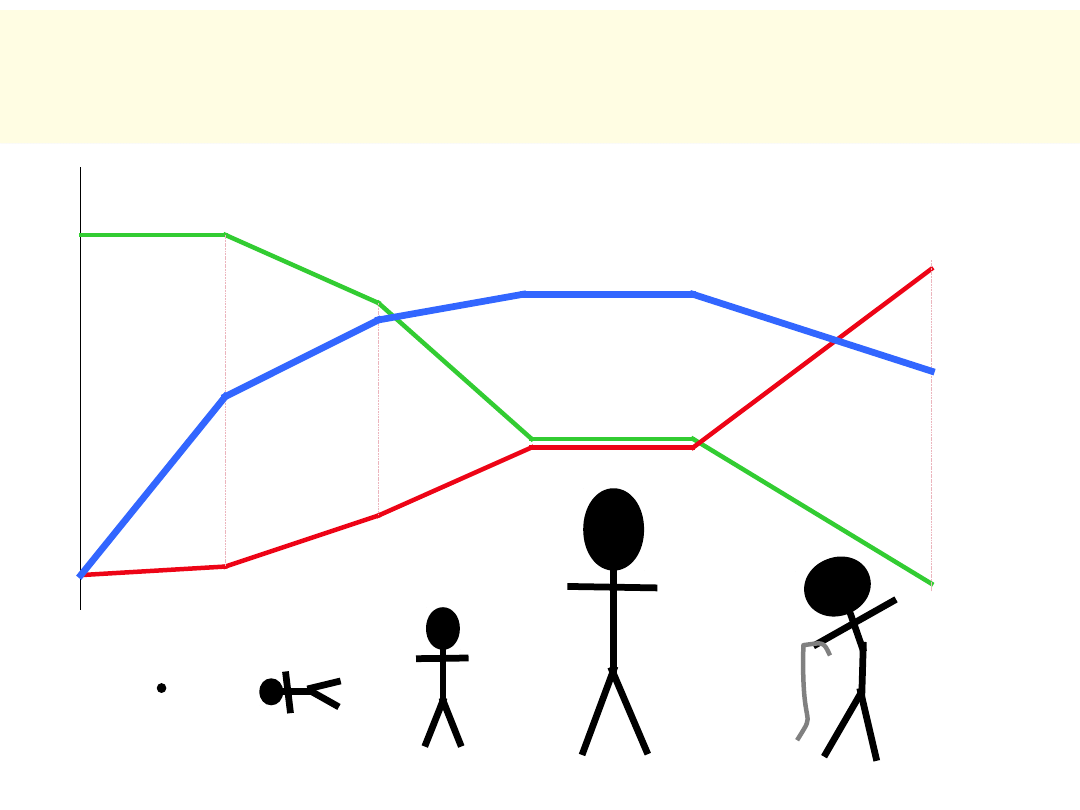
Szybkość i natężenie proliferacji i eliminacji
komórek w organizmie zmienia się
L
ic
zb
a
k
o
m
ó
re
k
p
o
w
s
ta
ją
c
y
c
h
i
tr
a
c
o
n
y
c
h
w
j
e
d
n
o
s
tc
e
c
z
a
s
u
proliferacja
eliminacja
całkowita
liczba komórek
4
W optymalnych warunkach komórki zdolne
do podziału dzielą się bardzo szybko…
średnio 1-2 razy na dobę…
ale…

5
Co to znaczy „optymalne
warunki”?
• Zapotrzebowanie
na nowe komórki
• Wzrost organizmu (do okresu dojrzałości)
• Reakcja na stymulację
• Wysiłek fizyczny
• Praca umysłowa
• Odpowiedź immunologiczna
• Obecność odpowiednich
czynników wzrostowych
• Zdolność komórek do reakcji na cz.w.
• Prawidłowa transdukcja sygnałów
• Właściwości
środowiska
• Podłoże (białka macierzy międzyklomórkowej)
• Substancje odżywcze
• Tlen
• Brak błędów w samych komórkach (DNA)
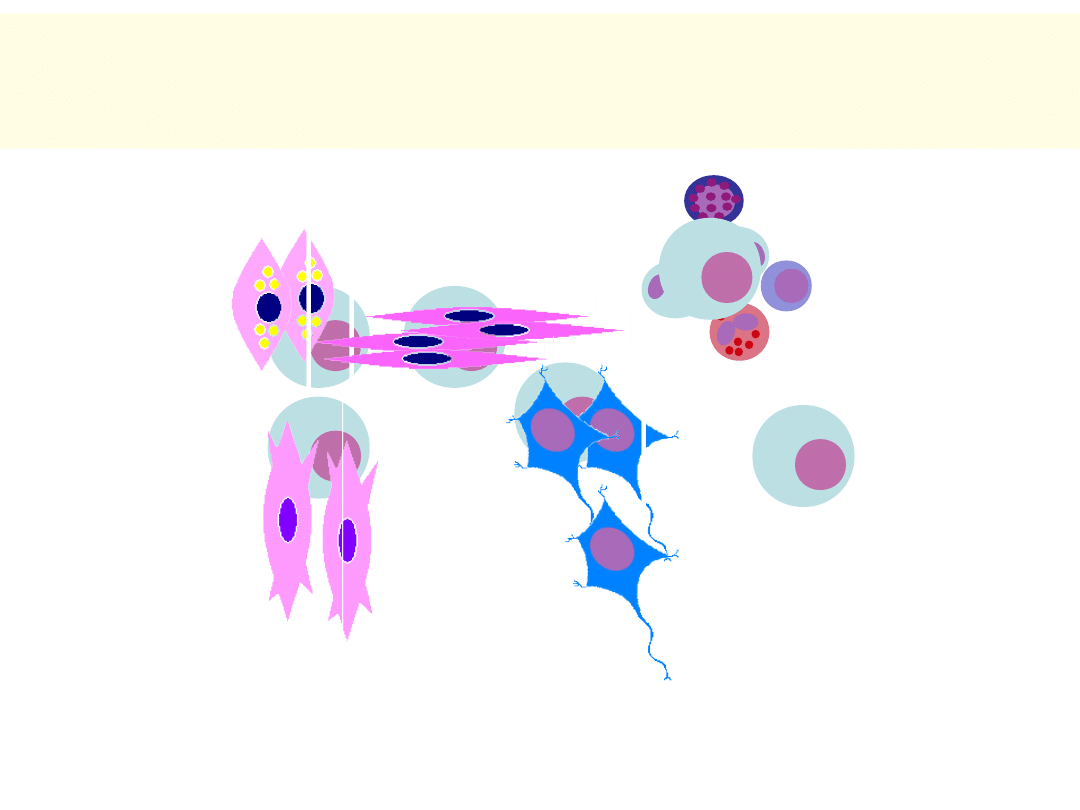
6
Tylko nieliczne komórki w tkankach dzielą
się stale; większość ulega różnicowaniu
Prawidłowe różnicowanie wymaga: odpowiednich czynników wzrostu
(np. interleukiny!), kontaktu z innymi komórkami, białkami podłoża
KOMÓRKA PNIA

7
Niepotrzebne, uszkodzone lub zużyte
komórki ulegają eliminacji i są
zastępowane przez nowe:
…bez zmiany wielkości/objętości tkanki lub
narządu.
PROLIFERACJA = APOPTOZA + NEKROZA
8
Przewaga śmierci komórek nad proliferacją
prowadzi do zaniku i reorganizacji tkanki….
PROLIFERACJA < APOPTOZA + NEKROZA
Przyczyny:
czynniki toksyczne
endogenne czynniki hamujące proliferację, np. IL-
10, TGFβ
nadmierna indukcja apoptozy
niedobór substancji pokarmowych
niedobór czynników wzrostowych
obniżona/zniesiona reaktywność na cz.w.

9
Konsekwencje niedoborów proliferacji
komórek:
• Zaburzenia wzrostu narządu/tkanki np. :
• Karłowatość
• Niedorozwój (hipo- lub aplazja) narządu
• Utrudnione gojenie się ran i innych
ubytków tkankowych
• Zaburzenia czynności „ze zużycia” (niezależnie od
wieku osobniczego)
• Marskość wątroby, nerki
• Wtórne niedobory endokrynologiczne
• Niedobory immunologiczne
• Starzenie się (także przedwczesne)

10
Przewaga proliferacji komórek nad ich
eliminacją prowadzi do rozwoju
nowotworów
Przyczyny:
nadmierna, niekontrolowana proliferacja
brak lub obniżenie apoptozy
Uwaga
: szybki wzrost nowotworów nie wynika ze skrócenia cyklu komórkowego,
tylko z większej liczby (PROPORCJI) proliferujących komórek [
WYSOKI
INDEKS MITOTYCZNY
] i (względnej)
przewagi proliferacji nad apoptozą
PROLIFERACJA >> APOPTOZA + NEKROZA

11
NOWOTWORY - Pojęcia
podstawowe:
• Nowotwór to NIEKONTROLOWANY rozplem
(namnażanie, proliferacja) populacji
komórek PRZEKRACZAJĄCY
ZAPOTRZEBOWANIE tkanki/organizmu
• Nowotwór składa się z komórek o:
• zaburzonej dynamice proliferacji
• niewłaściwym stopniu zróżnicowania (np. raki)
• niewłaściwej lokalizacji (przerzuty nowotworowe)
• niewłaściwej organizacji tkankowej (np. potworniaki)
• Nowotwór może powstać z każdego typu
komórek zdolnych do podziału
• Nowotwory łagodne a złośliwe

12
Przyczyny nowotworów
• Czynniki środowiskowe – 85% mutacji
kancerogennych
• Czynniki genetyczne – pozostałe 15 %
• Zróżnicowane rozmieszczenie czynników
środowiskowych i/lub różnice genetyczne
między populacjami zamieszkującymi różne
regiony geograficzne zróżnicowanie
częstości występowania nowotworów

13
Przyczyny nowotworów
• Podłożem powstawania i rozwoju
nowotworów są mutacje genów,
których produkty uczestniczą w
inicjowaniu, przebiegu i kontroli
procesu proliferacji –
PROTOONKOGENÓW
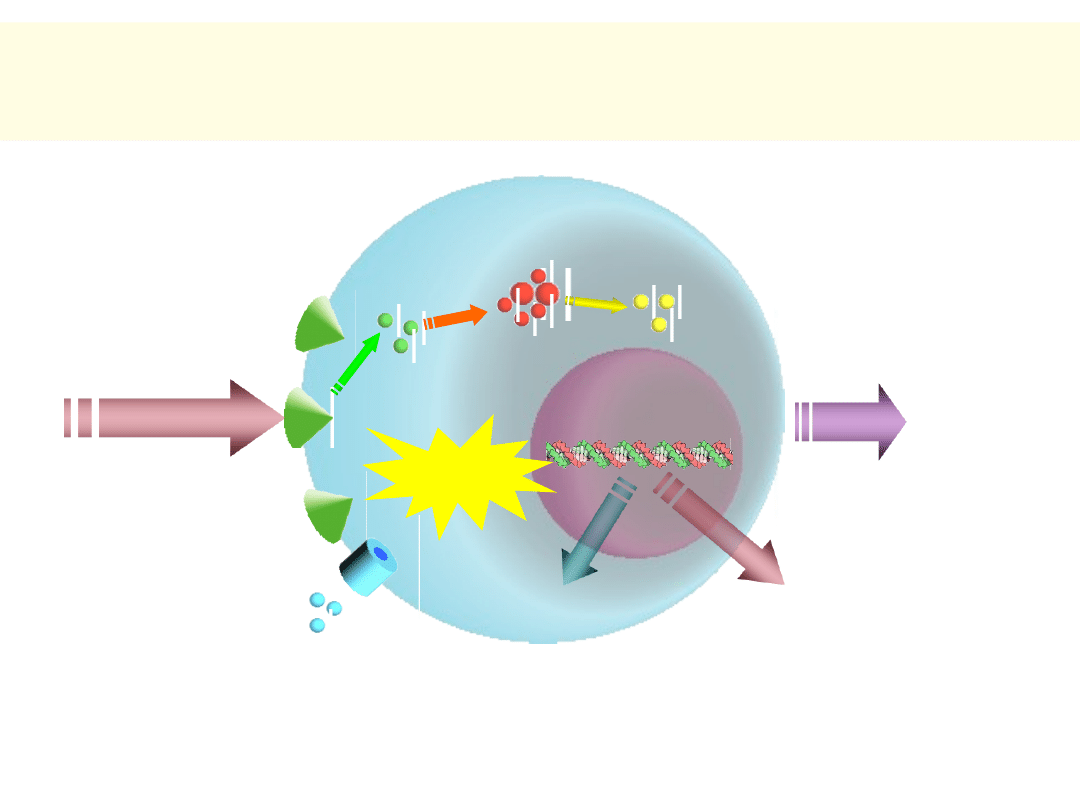
14
HORMON
Schemat działania hormonów
peptydowych
RECEPTOR
BŁONOWY
TRANSDUKCJA SYGNAŁU !
2
o
PRZEKAŹNIKI
KASKADA KINAZ
CZYNNIKI
TRANSKRYPCYJNE
SYNTEZA
BIAŁEK
Ca
2+
ZMIANY
METABOLICZNE
REPLIKACJA DNA
I PODZIAŁ
NOWY SYGNAŁ
(UWALNIANIE
HORMONU,
MEDIATORA)

15
Protoonkogeny
• DEFINICJA: geny kodujące białka biorące
udział w przebiegu procesów prowadzących
do podziału komórki
• Grupy protoonkogenów:
– Geny receptorów powierzchniowych (hormonów –
np. estrogenów), czynników wzrostu (np. EGF),
cytokin
– Geny czynników wzrostu, hormonów, cytokin…
– Geny czynników transdukcji sygnału i
transkrypcyjnych, np. : H-ras, Ki-ras, c-myc, c-fos,
c-jun, src…
– Geny cyklin i kinaz zależnych od cyklin
16
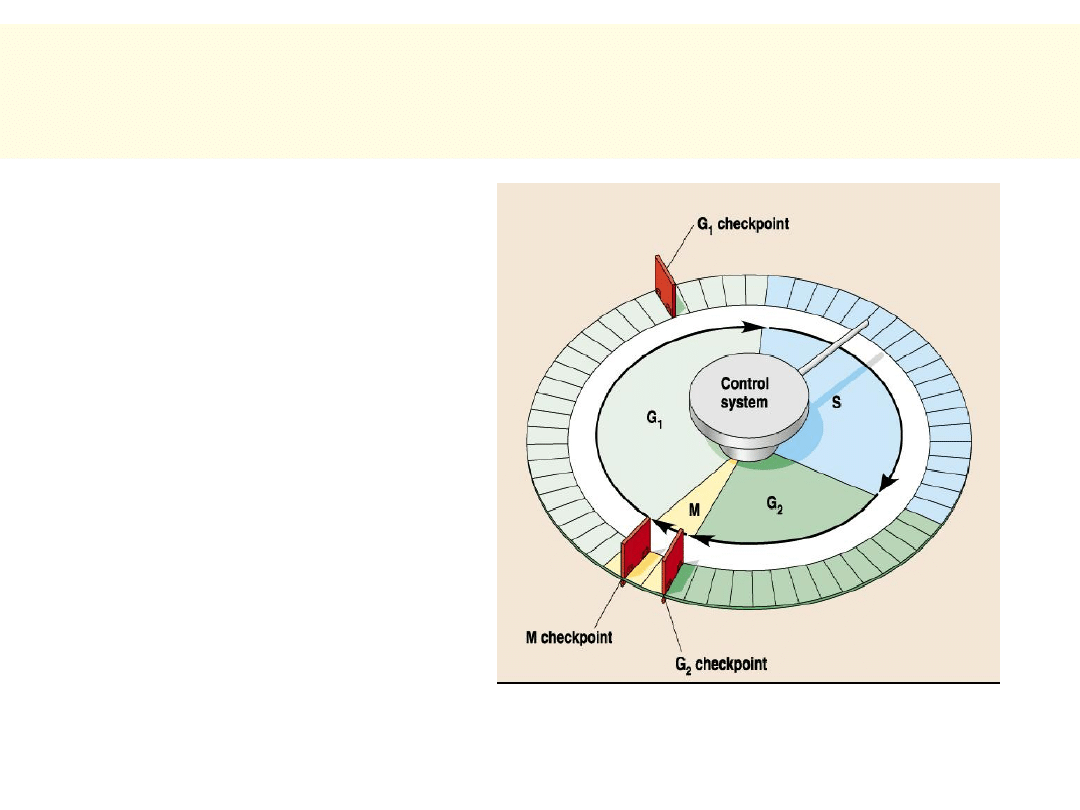
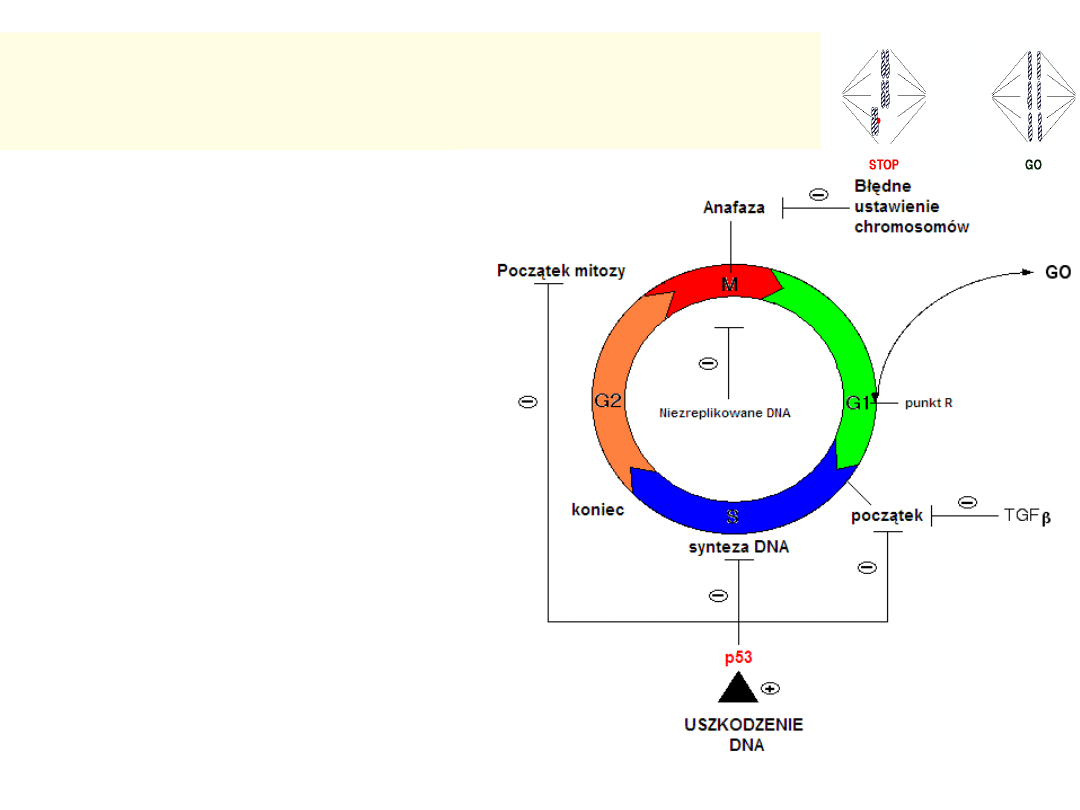
Prawidłowa kontrola nad
proliferacją komórek zależy:
• W komórkach
przygotowujących się
do podziału (faza G0)
od:
– wykrywania błędów w
DNA i ich reperacji
– inicjacji apoptozy w
przypadku niemożności
naprawienia mutacji
– oceny długości telomerów
• W trakcie cyklu
podziałowego od:
– Decyzji o kontynuacji lub
zatrzymaniu cyklu w
„punktach kontrolnych”
– Prawidłowego rytmu
syntezy i degradacji
protoonkogenów, a
zwłaszcza cyklin
17
Antyonkogeny
• Geny kodujące
białka hamujące
podział komórki,
np.:
• p53, Rb
• Białka
kontrolujące
apoptozę (np.
FasL, kaspazy,
Bid…)
• Inhibitory kinaz
zależnych od
cyklin (cdk) – np.
p21
waf/cip
, p16
INK4
, p27…
18
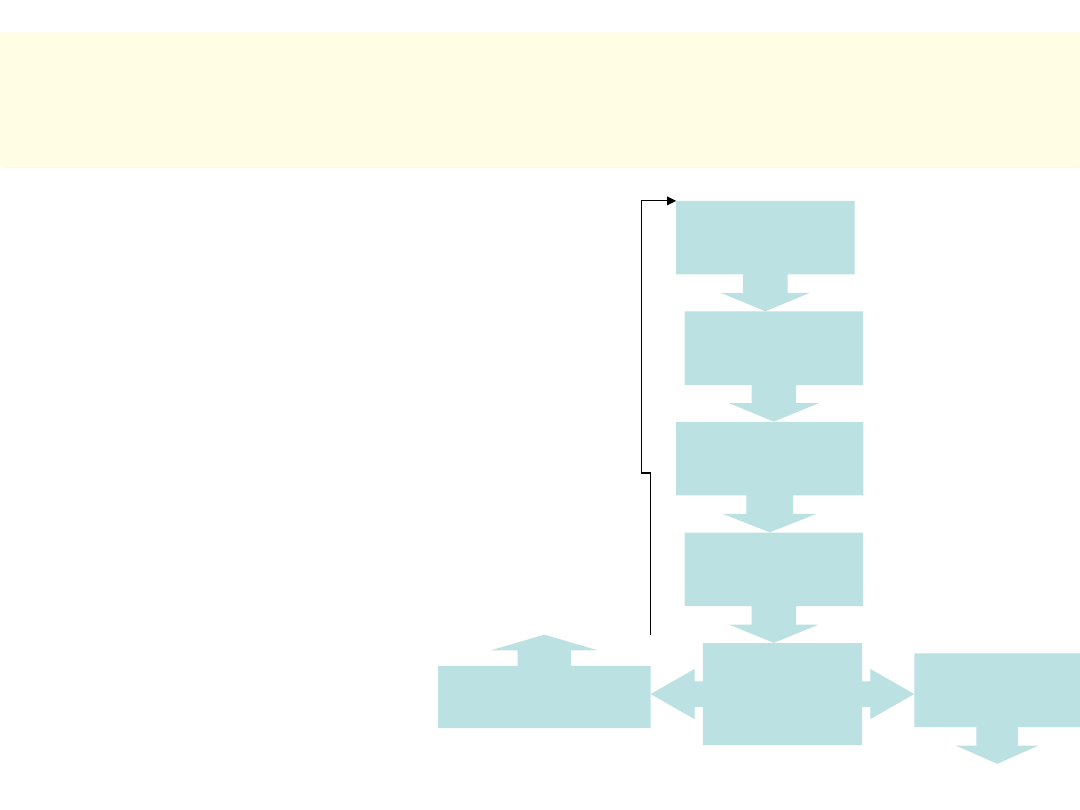
p53 i „kontrola genomu”
• Aktywacja w odpowiedzi
na defekt DNA
• Czynnik transkrypcyjny
dla genów p21
WAF/CIP
, c-
myc i mutatorów.
• Mutacje p53:
• gromadzenie p53
mut
• brak zatrzymania
proliferacji
• brak apoptozy
• proliferacja komórek
z uszkodzonym DNA
Uszkodzenie
DNA
Aktywacja
p53
Synteza p21…
Zatrzymanie
cyklu
Naprawa
DNA
+
-
PROLIFERACJA
APOPTOZA
19
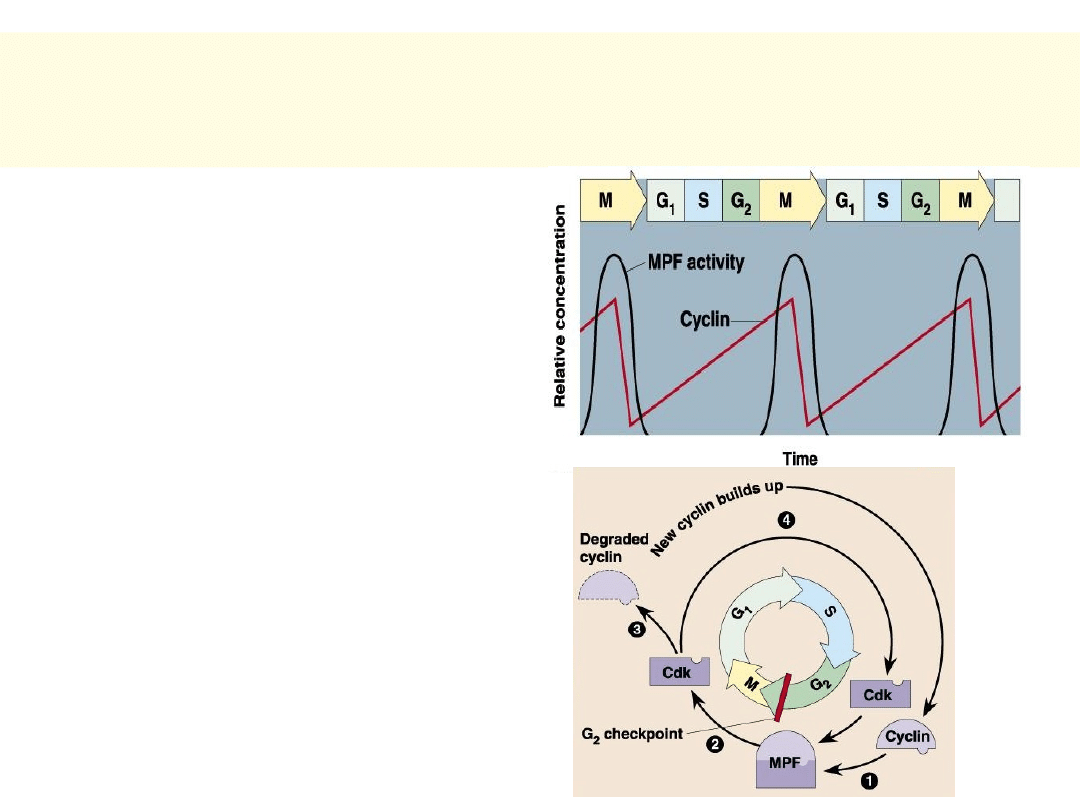
Cykliny były jednymi z pierwszych
odkrytych (proto)onkogenów
• Pojawianie się i
zanikanie cyklin (A-F)
decyduje o rozpoczęciu
i kontynuacji cyklu
komórkowego
• Trwała aktywność
kompleksu cyklina/cdk
nadmierna
proliferacja (np.
gruczolak przytarczyc –
mutacja cykliny D1)

20
ONKOGENY
• Zmutowane protoonkogeny…
• Analogi protoonkogenów pochodzące
z wirusów onkogennych, np.:
• V-ras,
• V-myc…
…których aktywność warunkuje
niekontrolowaną proliferację
komórek nowotworowych

21
Przykłady mutacji onkogennych
• Punktowe:
• H-ras (rak pęcherza, okrężnicy, trzustki)
• Geny enzymów reperujących DNA (mutatorów)
• Translokacje:
• Chromosom Filadelfia („krótki 22”; t9,22) hybrydowe białko
kinazowe BCR/Abl (białaczka szpikowa)
• Chłoniak Burkitta (t8,14 w limfocytach B) – c-myc
• Amplifikacje
– wzrost liczby kopii (onko)genu
• N-myc w neuroblastoma
• Erb-2 (homolog receptora EGF) w raku okrężnicy, sutka,
jajników i in.
• Cykliny D (raki sutka, przełyku, okrężnicy, wątroby; białaczki)
• Kinaza CDK4 (czerniak, mięsaki, glioblastoma)
• P-glikoproteina (mdr1) – nowotwory lekooporne

22
Kancerogeny 1
• Chemiczne, m.in.:
• Aflatoksyny (Aspergillus flavus)
• Benzo(a)piren [1300 ton/rok
uwalniane do atmosfery w wyniku
spalania węgla, ropy, grillowania…]
• Węglowodory policykliczne [np.
epoksydy w wędzonym mięsie]
• Aminy aromatyczne i barwniki
azowe [środki spożywcze]
• Nitrozaminy [peklowane mięso]
• Jony Ni
2+
, Pb
2+
, Cd2+, Co
2+
Aspergillus flavus
na orzeszku ziemnym
Konidiofory Aspergillus

23
• Fizyczne, np. :
– Promieniowanie cieplne:
• pęknięcia DNA spowodowane ruchami Browna –
10
5
/komórkę /dobę
• rak wargi u palaczy fajki
– Promieniowanie jonizujące:
• UV (rak podstawnokomórkowy naskórka – około 10
6
przypadków rocznie; czerniak złośliwy,
• gamma, X – białaczki, osteosarcoma
– Azbest: nowotwory płuc (mesothelioma
malignum)
• kopalnie,
• izolacja termiczna budynków
Kancerogeny 2

24
• Biologiczne, np. :
– DNA-wirusy – bezpośrednia integracja do genomu:
• Brodawczaki (herpeswirus HPV typ 1,2,4,7) i raki (wirus
HPV typ 16, 18, 31, 33, 51) – białka wirusa blokują p53, pRb
• Wirus Epsteina-Barra (EBV) – chłoniak Burkitta (mutacja v-
myc w limfocytach B) i inne; około 70% populacji
eksponowane na wirusa [przeciwciała]
• Wirus zapalenia watroby B (HBV)
• Herpesvirus mięsaka Kaposi’ego (KSHV)
– RNA-wirusy – integracja po odwrotnej transkrypcji:
• Wirus zapalenia wątroby C (HCV) – przyczyna 50% ostrych
zapaleń wątroby marskość hepatoma
• HTLV-1 – białaczki i chłoniaki z limfocytów T, powinowactwo
do CD4+
– Bakterie?
• Helicobacter pylori – raki żołądka, chłoniaki jelit?
Kancerogeny 3
25
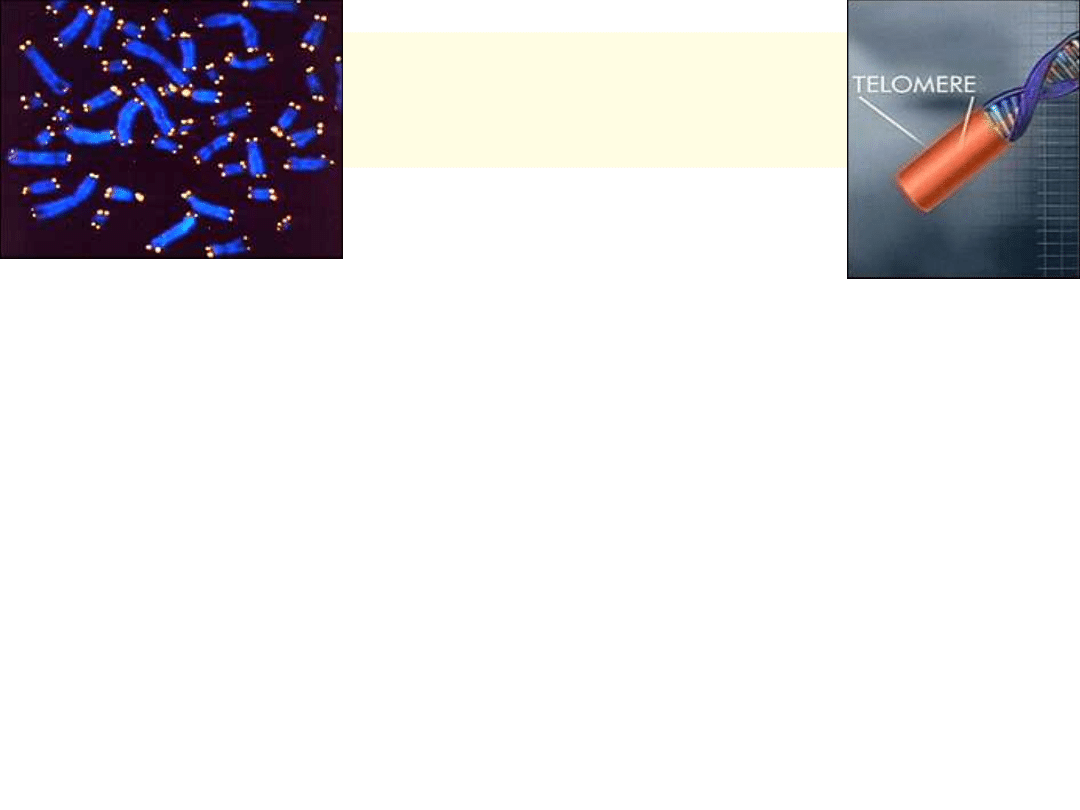
Telomery
Na końcach chromosomów, powtórzenia
sekwencji TTAGGG
Ochrona chromosomów przed degeneracją
i fuzją końców
Pry każdym podziale komórki dochodzi do
skracania telomerów starzenie komórek
26
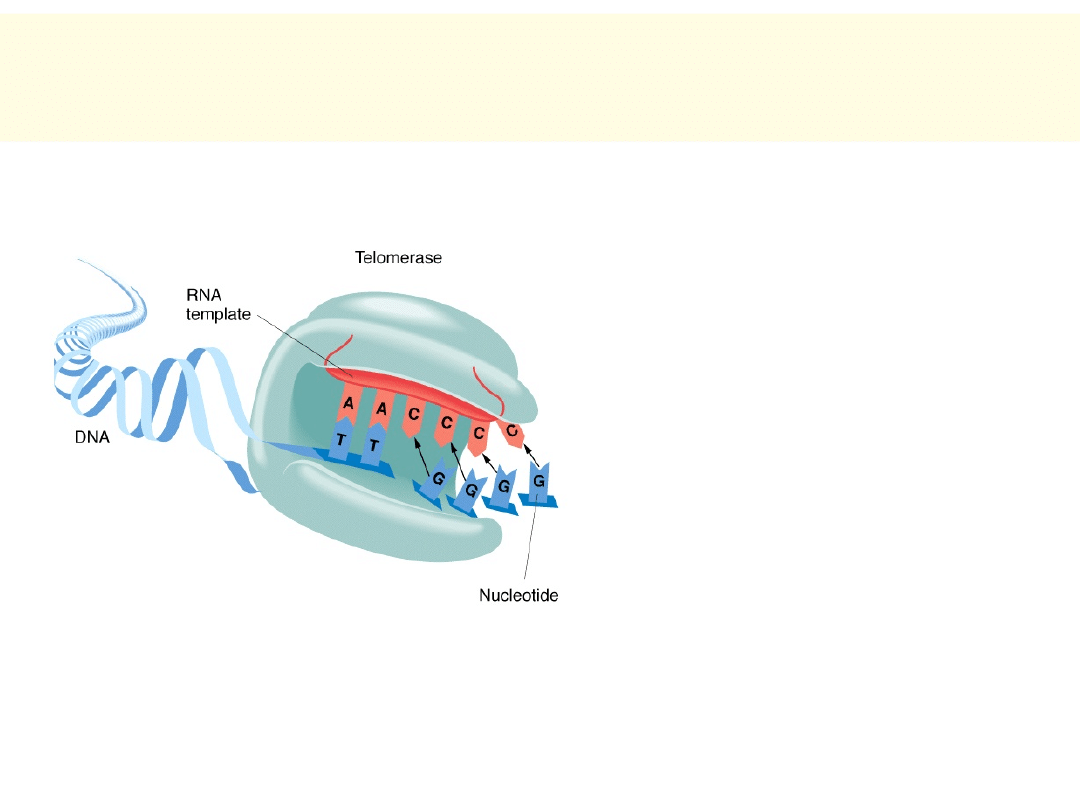
Telomeraza: enzym, który zapobiega
starzeniu się komórek i…
Odtwarza brakujące
fragmenty DNA
Jest aktywny w
komórkach pnia, ale nie
w komórkach
zróżnicowanych
…reaktywacja w
komórkach
zróżnicowanych prowadzi
do ich unieśmiertelnienia
i przemiany
nowotworowej
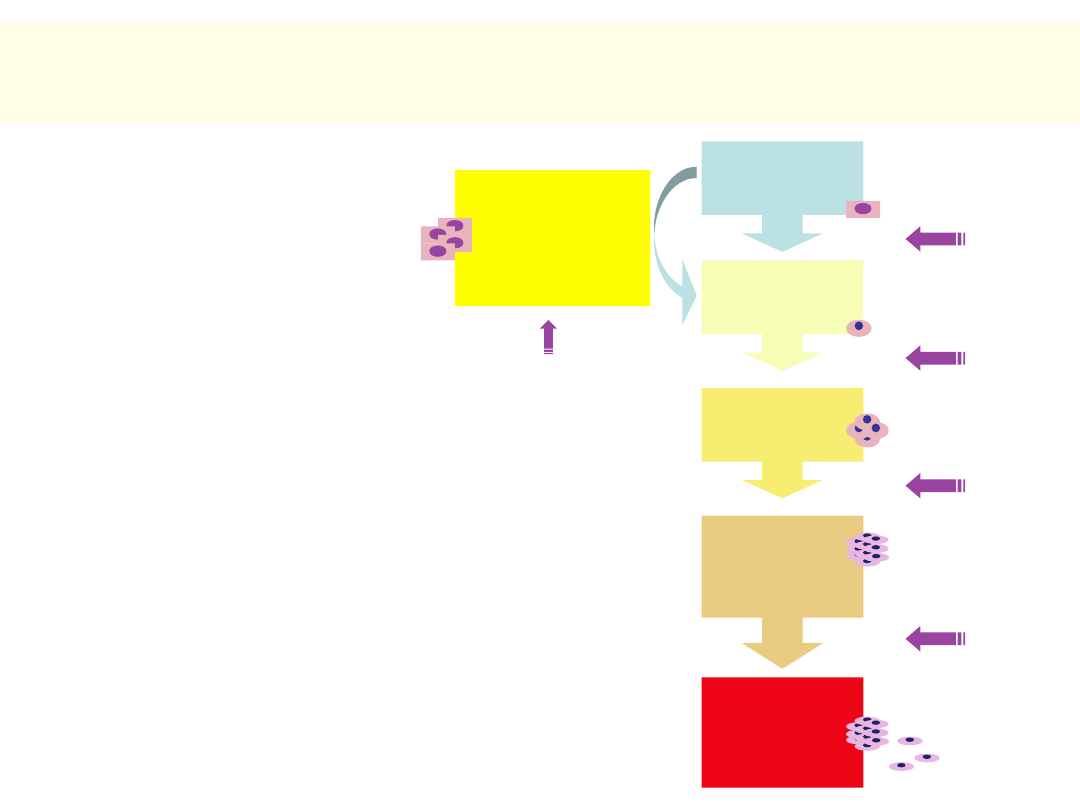
27
Rak
miejscowo
naciekający
Rozwój nowotworów
Inicjacja
(pierwotne, nieodwracalne
uszkodzenie DNA
protoonkogenu)
Stan przednowotworowy
Promocja (selekcja,
proliferacja, obniżenie
kontroli immunologicznej
Nowotwór łagodny
Progresja (dodatkowe
mutacje) Nowotwór
złośliwy
Prawidłowa
śluzówka
Mały
gruczolak
Duży
gruczolak
Rak
inwazyjny
(przerzuty)
Nadmierna
proliferacja
(rodzinna
polipowatość)
Mutacje:
APC
MCC
del 5q
C-myc
Ki-ras
p53
del 17p
del 18q
LICZNE
Mutacja APC
Przykład:
gruczolakorak
jelita grubego

28
Wielość mutacji potrzebnych do
powstania nowotworu złośliwego
to:
• Zwykle długi czas rozwoju do wykrycia
• Zależny od rodzaju pierwotnej mutacji
» Mutacje p53, genów mutatorów i aparatu naprawy
DNA szybka progresja
• Małe prawdopodobieństwo tego samego
„zestawu” mutacji w zaawansowanych
nowotworach tego samego typu
• Różny przebieg
• Różna wrażliwość na chemioterapię

29
Propagacja nowotworów złośliwych
następuje poprzez
:
• Naciekanie
(inwazję) otaczających tkanek
• Przerzutowanie
drogą naczyń limfatycznych
(limfogenne) do węzłów chłonnych (RAKI)
• Przerzutowanie
drogą naczyń krwionośnych
(hematogenne) do kompatybilnych
tkanek/narządów (RAKI i MIĘSAKI)
• Rozsiew
w obrębie jam ciała (np. w jamie
otrzewnej – rak jajnika, w opłucnej – mesothelioma)
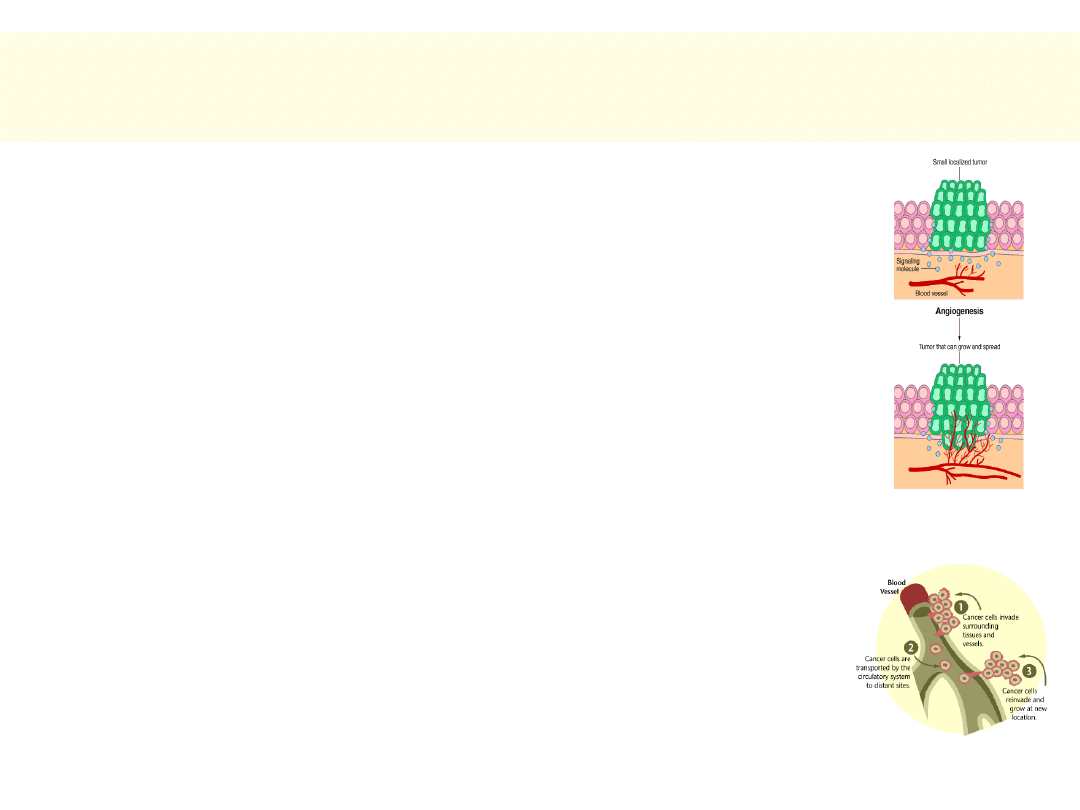
30
Warunki propagacji nowotworów
złośliwych
• Słabe połączenia międzykomórkowe
• Luźne podścielisko
• Mały stopień włóknienia
• Sekrecja enzymów proteolitycznych
– Kolagenazy
– Proteazy (np. MMP)
– Hialuronidazy
• Rozbudowane unaczynienie krwionośne
i limfatyczne
• Sekrecja czynników angiogenetycznych
UWAGA: komórki nowotworowe mogą być obecne w naczyniach
już w stadium przedklinicznym nowotworów!
Angiogeneza

31
Tolerancja immunologiczna wobec
nowotworu – warunek rozrostu
• Przyczyny:
• Zaburzenia antygenowości komórek nowotworowych
– utrata HLA
– antygeny rakowo-płodowe (karcynoembrionalne, CEA),
– α-fetoproteina
• Sekrecja cytokin supresorowych (TGF-β)
• Sekrecja hormonów immunosupresyjnych (sterydy,
ACTH)
• Przeciwciała blokujące antygeny nowotworowe
(„maskujące”)
• AIDS
• Podeszły wiek (zmniejszona czynność układu
odpornościowego).

32
Konsekwencje nowotworów – dlaczego
giniemy?
• Efekt masy guza – ucisk na życiowo ważny narząd:
• drogi pokarmowe - zagłodzenie
• nerwy – niedowład, porażenie (OUN – wgłobienie)
• naczynia – zawał, niedokrwienie
• Lokalne zniszczenie tkanki – inwazja lub liza powierzchni
nabłonkowych lub naczyń:
• proces zapalny
• krwawienia i krwotoki
• infekcje
• Wypieranie tkanki prawidłowej (białaczki, szpiczaki)
• Niedokrwistość
• Niedobory odpornościowe
• Zaburzenia krzepliwości krwi
• Wyniszczenie:
• obniżony pobór kalorii
• zużycie zasobów metabolicznych przez nowotwór
• zmiana metabolizmu (TNF)
• zatrucie produktami rozpadu guza

33
Aktywność hormonalna
nowotworów
• Nowotwory narządów dokrewnych
• Gigantyzm, akromegalia (guz komórek kwasochłonnych PPPM)
• Mlekotok (prolactinoma)
• Hiperinsulinemia/szoki insulinowe (wyspiak)
• Kryzysy nadciśnieniowe (pheochromocytoma)
• Hiperkalcemia, kalcynoza (gruczolak przytarczyc)
• Raki produkujące hormony:
• ACTH – rak owsianokomórkowy
• Erytropoetyna – rak jasnokomórkowy nerki
• Analogi PTH – raki płaskonabłonkowe
• Hiperkalcemia jako objaw towarzyszący
nowotworom:
• Nasilona osteoliza – przerzuty do kości
• działanie PTH i jego analogów
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
Wyszukiwarka
Podobne podstrony:
W02b Patofizjologia zaburzeń proliferacji komórek
06 Patofizjologia zaburzeń proliferacji komórek
Wykład 3 Patofizjologia zaburzeń proliferacji komórek
W08 Patofizjologia zaburzeń gospodarki węglowodanowej
Wykład 5 Patofizjologia zaburzeń odporności AIDS2
Patofizjologia zaburze ä jonowych
PATOFIZJOLOGIA ZABURZEŃ IMMUNOLOGICZNYCH, Wykłady
Patofizjologia, patofizjoIV, ZABURZENIA DIUREZY- diureza dobowa czyli ilosc moczu wydalana w ciagu d
Patofizjologia, patofizjoIV, ZABURZENIA DIUREZY- diureza dobowa czyli ilosc moczu wydalana w ciagu d
Określanie żywotności i proliferacji komórek metodami spektrofotometrycznymi
W04b Patofizjologia zaburzeń odporności
Patofizjologia zaburzeń odporności 1
W04c Patofizjologia zaburzeń odporności
Patofizjologia, Zaburzenia rytmu serca2, Zaburzenie rytmu serca:Przyczyny: 1)dyselektrolitemia (hipo
4 Ćwiczenia Patofizjologia zaburzeń krzepnięcia krwi1
W4 Patofizjologia zaburzeń oddechowych., Wykłady
Patofizjologia zaburzeń czynności podwzógrza, Patofizjologia
więcej podobnych podstron