
Dr n. med. Ewa Ziarko
Dr n. med. Ewa Ziarko
Pracownia Teorii i Podstaw Pielęgniarstwa
Pracownia Teorii i Podstaw Pielęgniarstwa
Instytut Pielęgniarstwa i Położnictwa
Instytut Pielęgniarstwa i Położnictwa
WNoZ CM UJ
WNoZ CM UJ
TECHNIKA POBIERANIA MATERIAŁU
TECHNIKA POBIERANIA MATERIAŁU
DO BADAŃ
DO BADAŃ
ZAPOBIEGANIE ZAKAŻENIOM
ZAPOBIEGANIE ZAKAŻENIOM
SZPITALNYM
SZPITALNYM

„
„
Jeżeli lekarz nie widzi na swoim oddziale zakażeń
Jeżeli lekarz nie widzi na swoim oddziale zakażeń
szpitalnych, powinien tylko szerzej otworzyć oczy”
szpitalnych, powinien tylko szerzej otworzyć oczy”
Sir Robert
Sir Robert
Williams
Williams
„
„
Oprócz cierpień, jakie sprawia to chorym,
Oprócz cierpień, jakie sprawia to chorym,
zakażenia szpitalne są dla szpitali bolesnym
zakażenia szpitalne są dla szpitali bolesnym
uderzeniem po kieszeni”
uderzeniem po kieszeni”
Sir Wilson
Sir Wilson
Jameson
Jameson

WHO stwierdza pojawianie się zakażeń
WHO stwierdza pojawianie się zakażeń
szpitalnych u około 9% wszystkich
szpitalnych u około 9% wszystkich
hospitalizowanych pacjentów
hospitalizowanych pacjentów
.
.
W Stanach Zjednoczonych 5%
W Stanach Zjednoczonych 5%
W Belgii 9%
W Belgii 9%
W Niemczech 6,9%
W Niemczech 6,9%
W Polsce rzeczywista częstość występowania
W Polsce rzeczywista częstość występowania
zakażeń nie jest znana
zakażeń nie jest znana
Inne dane mówią, że w Polsce częstość zakażeń
Inne dane mówią, że w Polsce częstość zakażeń
szpitalnych wynosi 15% wszystkich zakażeń;
szpitalnych wynosi 15% wszystkich zakażeń;
rocznie z ich powodu umiera ok. 10 000 pacjentów.
rocznie z ich powodu umiera ok. 10 000 pacjentów.

W Stanach Zjednoczonych najczęstsze zakażenia
W Stanach Zjednoczonych najczęstsze zakażenia
szpitalne dotyczą:
szpitalne dotyczą:
- infekcji układu moczowego 39%
- infekcji układu moczowego 39%
- zapalenia płuc 18%
- zapalenia płuc 18%
- zakażeń rany pooperacyjnej 17%
- zakażeń rany pooperacyjnej 17%
- krwi 7%
- krwi 7%
Według raportu europejskiego
Według raportu europejskiego
główne zagrożenia
główne zagrożenia
dla chorych z
dla chorych z
oddziałów zabiegowych
oddziałów zabiegowych
stanowią:
stanowią:
- zakażenia dróg moczowych 31-48%
- zakażenia dróg moczowych 31-48%
- zakażenia ran pooperacyjnych 28-31%
- zakażenia ran pooperacyjnych 28-31%
- infekcje układu oddechowego 18% (duża śmiertelność)
- infekcje układu oddechowego 18% (duża śmiertelność)

Według raportu europejskiego
Według raportu europejskiego
główne zagrożenia
główne zagrożenia
dla chorych
dla chorych
z
z
oddziałów niezabiegowych
oddziałów niezabiegowych
to:
to:
- zakażenia dróg moczowych 42%
- zakażenia dróg moczowych 42%
- zakażenia dróg oddechowych 24%
- zakażenia dróg oddechowych 24%
Według raportu europejskiego zakażenia szpitalne
Według raportu europejskiego zakażenia szpitalne
są
są
bezpośrednią przyczyną zgonów u 3%
bezpośrednią przyczyną zgonów u 3%
chorych hospitalizowanych, a pośrednią u
chorych hospitalizowanych, a pośrednią u
8,3%.
8,3%.

Parlament Europejski decyzją z 22. 12. 1999r. powołał
Parlament Europejski decyzją z 22. 12. 1999r. powołał
Europejskie Centrum Epidemiologiczne
Europejskie Centrum Epidemiologiczne
Ustawa o chorobach zakaźnych i zakażeniach z 2001r.
Ustawa o chorobach zakaźnych i zakażeniach z 2001r.
wprowadza definicję zakażenia szpitalnego, wymusza
wprowadza definicję zakażenia szpitalnego, wymusza
zorganizowany, nowoczesny nadzór nad zakażeniami
zorganizowany, nowoczesny nadzór nad zakażeniami
szpitalnymi.
szpitalnymi.

„
„
Zakażenie związane z pobytem chorego w szpitalu,
Zakażenie związane z pobytem chorego w szpitalu,
które powstaje lub rozwija się w czasie hospitalizacji
które powstaje lub rozwija się w czasie hospitalizacji
pacjenta (albo po opuszczeniu szpitala), a które nie
pacjenta (albo po opuszczeniu szpitala), a które nie
było w okresie inkubacji w chwili przyjęcia,
było w okresie inkubacji w chwili przyjęcia,
rozpoznane klinicznie i potwierdzone laboratoryjnie
rozpoznane klinicznie i potwierdzone laboratoryjnie
jest
jest
zakażeniem szpitalnym
zakażeniem szpitalnym
niezależnie od tego,
niezależnie od tego,
czy czynnik etiologiczny (drobnoustrój), który je
czy czynnik etiologiczny (drobnoustrój), który je
wywołał jest pochodzenia endogennego
wywołał jest pochodzenia endogennego
(autogennego) czy egzogennego”.
(autogennego) czy egzogennego”.
Lowbury 1981 za Nosowską
Lowbury 1981 za Nosowską
1999
1999

Czynniki ryzyka zakażeń szpitalnych
Czynniki ryzyka zakażeń szpitalnych
:
:
związane z gospodarzem (choroba, wiek,
związane z gospodarzem (choroba, wiek,
niedożywienie, otyłość, niedobory witamin i
niedożywienie, otyłość, niedobory witamin i
pierwiastków śladowych, niedokrwistość, choroby
pierwiastków śladowych, niedokrwistość, choroby
współistniejące: cukrzyca, miażdżyca, choroby
współistniejące: cukrzyca, miażdżyca, choroby
nowotworowe, zakażenie wirusem HIV, wrodzone
nowotworowe, zakażenie wirusem HIV, wrodzone
defekty immunologiczne, chemioterapia, radioterapia,
defekty immunologiczne, chemioterapia, radioterapia,
rany, otwarte złamania, ochłodzenie organizmu)
rany, otwarte złamania, ochłodzenie organizmu)
związane z drobnoustrojem (rodzaj, zaraźliwość,
związane z drobnoustrojem (rodzaj, zaraźliwość,
zjadliwość, wrażliwość na chemioterapeutyki)
zjadliwość, wrażliwość na chemioterapeutyki)
związane ze szpitalem (wyposażenie, dezynfekcja,
związane ze szpitalem (wyposażenie, dezynfekcja,
sterylizacja, mycie rąk, sprzątanie), zabiegami
sterylizacja, mycie rąk, sprzątanie), zabiegami
diagnostycznymi, leczniczymi, pielęgnacyjnymi,
diagnostycznymi, leczniczymi, pielęgnacyjnymi,
czasem hospitalizacji
czasem hospitalizacji

Czynniki etiologiczne zakażeń szpitalnych
Czynniki etiologiczne zakażeń szpitalnych
:
:
1. wirusy:
1. wirusy:
- wywołujące zapalenia górnych dróg oddechowych i przewodu
- wywołujące zapalenia górnych dróg oddechowych i przewodu
pokarmowego (np.. wirus grypy, paragrypy, rota, odry, różyczki, świnki)
pokarmowego (np.. wirus grypy, paragrypy, rota, odry, różyczki, świnki)
- wywołujące zakażenia przenoszone przez krew (wirusy zapalenia
- wywołujące zakażenia przenoszone przez krew (wirusy zapalenia
wątroby typu B,C, D, G, wirus HIV)
wątroby typu B,C, D, G, wirus HIV)
- z rodziny Herpesviridae (wirus cytomegalii - CMV, varicella-zoster –
- z rodziny Herpesviridae (wirus cytomegalii - CMV, varicella-zoster –
HVZ, herpes simplex – HSV –wirus opryszczki zwykłej, Epsteina-Barr –
HVZ, herpes simplex – HSV –wirus opryszczki zwykłej, Epsteina-Barr –
EBV, które ujawniają się u pacjentów ze zmniejszoną odpornością
EBV, które ujawniają się u pacjentów ze zmniejszoną odpornością
2
2
.
.
bakterie:
bakterie:
- Staphylococcus aureus, Staphylococcus epidermidis (szczepy oporne
- Staphylococcus aureus, Staphylococcus epidermidis (szczepy oporne
na metycylinę), Enterococcus faecalis, Escherichia coli, Proteus,
na metycylinę), Enterococcus faecalis, Escherichia coli, Proteus,
Klebsiella, Enterobacter, Pseudomonas aeruginosa, Clostridium difficile
Klebsiella, Enterobacter, Pseudomonas aeruginosa, Clostridium difficile
3. grzyby:
3. grzyby:
drożdżaki z rodzaju Candida, grzyby pleśniowe z rodzaju
drożdżaki z rodzaju Candida, grzyby pleśniowe z rodzaju
Aspergillus
Aspergillus
4. pierwotniaki i robaki
4. pierwotniaki i robaki
(owsica)
(owsica)

Drobnoustroje odporne na wysuszenie to:
Drobnoustroje odporne na wysuszenie to:
-
Staphylococcus aureus
Staphylococcus aureus
-
Enterococcus
Enterococcus
-
Mycobacterium tuberculosis
Mycobacterium tuberculosis
-
Niektóre grzyby
Niektóre grzyby

Drobnoustroje wykazujące zdolność
Drobnoustroje wykazujące zdolność
rozmnażania w środowisku wilgotnym:
rozmnażania w środowisku wilgotnym:
- Pałeczki Gram-ujemne, np. Pseudomonas (woda
- Pałeczki Gram-ujemne, np. Pseudomonas (woda
destylowana, roztwory środków dezynfekcyjnych,
destylowana, roztwory środków dezynfekcyjnych,
umywalki)
umywalki)

Drogi szerzenia się zakażeń szpitalnych
Drogi szerzenia się zakażeń szpitalnych
:
:
a) bezpośrednie,
a) bezpośrednie,
np. ręce personelu
np. ręce personelu
b) pośrednie
b) pośrednie
:
:
- powietrzno-kropelkowa
- powietrzno-kropelkowa
- wodno-pokarmowa
- wodno-pokarmowa
- skażone narzędzia i urządzenia, np. krwią
- skażone narzędzia i urządzenia, np. krwią

Zapobieganie i zwalczanie zakażeń szpitalnych:
Zapobieganie i zwalczanie zakażeń szpitalnych:
- higiena szpitalna
- higiena szpitalna
(codzienne czyszczenie, sprzątanie
(codzienne czyszczenie, sprzątanie
pomieszczeń i sprzętów,
pomieszczeń i sprzętów,
prawidłowa dezynfekcja
prawidłowa dezynfekcja
miejsc,
miejsc,
sprzętów, aparatury, narzędzi, usuwanie i utylizacja odpadów
sprzętów, aparatury, narzędzi, usuwanie i utylizacja odpadów
szpitalnych,
szpitalnych,
prawidłowo prowadzone i skutecznie
prawidłowo prowadzone i skutecznie
kontrolowane procesy sterylizacji
kontrolowane procesy sterylizacji
, przestrzeganie higieny
, przestrzeganie higieny
osobistej pacjentów, właściwe postępowanie z brudną
osobistej pacjentów, właściwe postępowanie z brudną
bielizną,
bielizną,
używanie rękawiczek, mycie i dezynfekcja rąk
używanie rękawiczek, mycie i dezynfekcja rąk
przez personel)
przez personel)
- zabezpieczenie wrót zakażenia (skuteczna antyseptyka
- zabezpieczenie wrót zakażenia (skuteczna antyseptyka
skóry chorego przed zabiegami inwazyjnymi, skuteczna
skóry chorego przed zabiegami inwazyjnymi, skuteczna
dekontaminacja narzędzi,
dekontaminacja narzędzi,
prawidłowe przygotowanie
prawidłowe przygotowanie
zespołu operacyjnego i bloku zabiegowego, opieka nad raną
zespołu operacyjnego i bloku zabiegowego, opieka nad raną
operacyjną i miejscem wkłucia)
operacyjną i miejscem wkłucia)
- Komitet Kontroli Zakażeń Szpitalnych, Zespół Kontroli
- Komitet Kontroli Zakażeń Szpitalnych, Zespół Kontroli
Zakażeń Szpitalnych
Zakażeń Szpitalnych

DEKONTAMINACJA
DEKONTAMINACJA
to proces usuwania lub zabicia drobnoustrojów,
to proces usuwania lub zabicia drobnoustrojów,
doprowadzający do tego, że materiały stają się
doprowadzający do tego, że materiały stają się
bezpieczne dla zdrowia. Obejmuje:
bezpieczne dla zdrowia. Obejmuje:
-
oczyszczanie
oczyszczanie
-
dezynfekcję
dezynfekcję
-
sterylizację
sterylizację

Dekontaminacja rąk
Dekontaminacja rąk
obejmuje mycie:
obejmuje mycie:
-
Socjalne (zwykłe, codzienne)
Socjalne (zwykłe, codzienne)
-
Higieniczne
Higieniczne
-
Chirurgiczne
Chirurgiczne

Dezynfekcja
Dezynfekcja
to proces zmniejszający liczbę patogennych
to proces zmniejszający liczbę patogennych
drobnoustrojów znajdujących się na przedmiotach
drobnoustrojów znajdujących się na przedmiotach
bądź skórze do poziomu, który nie zagraża zdrowiu
bądź skórze do poziomu, który nie zagraża zdrowiu
ludzi; to proces prowadzący do
ludzi; to proces prowadzący do
zabicia głównie form
zabicia głównie form
wegetatywnych bakterii.
wegetatywnych bakterii.
Dezynfekcji podlegają
Dezynfekcji podlegają
narzędzia i sprzęt, które mają bezpośredni
narzędzia i sprzęt, które mają bezpośredni
kontakt z
kontakt z
nieuszkodzoną powierzchnią skóry.
nieuszkodzoną powierzchnią skóry.

Dezynfekcja wysokiego poziomu
Dezynfekcja wysokiego poziomu
to proces prowadzący do zabicia
to proces prowadzący do zabicia
nie tylko wrażliwych
nie tylko wrażliwych
form wegetatywnych: bakterii, grzybów, wirusów ale
form wegetatywnych: bakterii, grzybów, wirusów ale
także prątków gruźlicy i enterowirusów
także prątków gruźlicy i enterowirusów
przy użyciu
przy użyciu
preparatów dezynfekcyjnych o szerokim spektrum
preparatów dezynfekcyjnych o szerokim spektrum
działania. Tej dezynfekcji podlegają narzędzia i sprzęt,
działania. Tej dezynfekcji podlegają narzędzia i sprzęt,
który nie może być sterylizowany ze względów
który nie może być sterylizowany ze względów
technicznych, a ma
technicznych, a ma
kontakt z nieuszkodzonymi
kontakt z nieuszkodzonymi
błonami śluzowymi.
błonami śluzowymi.

Sterylizacja
Sterylizacja
to proces, w wyniku którego całkowitemu zniszczeniu
to proces, w wyniku którego całkowitemu zniszczeniu
ulegają
ulegają
wszystkie patogenne drobnoustroje, ich formy
wszystkie patogenne drobnoustroje, ich formy
wegetatywne i przetrwalnikowe (spory, zarodniki).
wegetatywne i przetrwalnikowe (spory, zarodniki).
Sterylizacji podlegają narzędzia i sprzęt, który ma
Sterylizacji podlegają narzędzia i sprzęt, który ma
kontakt z uszkodzonymi tkankami lub narusza
kontakt z uszkodzonymi tkankami lub narusza
ciągłość powłok ciała.
ciągłość powłok ciała.

Aseptyka
Aseptyka
to postępowanie polegające na posługiwaniu się
to postępowanie polegające na posługiwaniu się
materiałem i narzędziami wyjałowionymi (sterylnymi).
materiałem i narzędziami wyjałowionymi (sterylnymi).
Antyseptyka
Antyseptyka
to postępowanie polegające na wstrzymaniu rozwoju
to postępowanie polegające na wstrzymaniu rozwoju
bakterii lub ich niszczeniu przez stosowanie
bakterii lub ich niszczeniu przez stosowanie
chemicznych środków antyseptycznych.
chemicznych środków antyseptycznych.

Zasady aseptyki:
Zasady aseptyki:
Przy wykonywaniu zabiegów aseptycznych (jałowych)
Przy wykonywaniu zabiegów aseptycznych (jałowych)
należy:
należy:
- umyć higienicznie ręce przed i po zabiegu
- umyć higienicznie ręce przed i po zabiegu
- założyć rękawiczki jednorazowego użytku (czyste lub
- założyć rękawiczki jednorazowego użytku (czyste lub
jałowe)
jałowe)
- posługiwać się jałowymi narzędziami (najlepiej sprzętem
- posługiwać się jałowymi narzędziami (najlepiej sprzętem
jednorazowego użytku) i jałowym materiałem
jednorazowego użytku) i jałowym materiałem
opatrunkowym
opatrunkowym
- sprzęt jednorazowego użytku przechowywać w
- sprzęt jednorazowego użytku przechowywać w
oryginalnych pojemnikach, np. kartonach
oryginalnych pojemnikach, np. kartonach
- przygotowując sprzęt do zabiegu należy sprawdzić: datę
- przygotowując sprzęt do zabiegu należy sprawdzić: datę
upływu gwarancji, szczelność opakowania; opakowanie
upływu gwarancji, szczelność opakowania; opakowanie
otwierać tak, aby sprzętu nie zainfekować
otwierać tak, aby sprzętu nie zainfekować

- sprzęt wielokrotnego użytku wyjmować odpowiednio długimi, jałowymi
- sprzęt wielokrotnego użytku wyjmować odpowiednio długimi, jałowymi
narzędziami, przechowywanymi w sposób jałowy; jeśli stosuje się
narzędziami, przechowywanymi w sposób jałowy; jeśli stosuje się
pakiety nie ma potrzeby używania, np. pęset „podających”
pakiety nie ma potrzeby używania, np. pęset „podających”
- wszystkie narzędzia i materiał opatrunkowy nieużyty podczas zabiegu
- wszystkie narzędzia i materiał opatrunkowy nieużyty podczas zabiegu
należy wyjałowić ponownie
należy wyjałowić ponownie
- miejsce (pole zabiegu) przemyć środkiem antyseptycznym, z
- miejsce (pole zabiegu) przemyć środkiem antyseptycznym, z
zachowaniem kierunku, czasu kolejności mycia, dostosowanym do
zachowaniem kierunku, czasu kolejności mycia, dostosowanym do
rodzaju środka
rodzaju środka
- uważać, aby jałowym sprzętem nie dotykać przedmiotów znajdujących
- uważać, aby jałowym sprzętem nie dotykać przedmiotów znajdujących
się poza polem działania, w przypadku zakażenia – sprzęt wymienić
się poza polem działania, w przypadku zakażenia – sprzęt wymienić
- po zakończonym zabiegu używany sprzęt wielokrotnego użytku
- po zakończonym zabiegu używany sprzęt wielokrotnego użytku
umieścić w płynie dezynfekcyjnym, sprzęt jednorazowego użytku w
umieścić w płynie dezynfekcyjnym, sprzęt jednorazowego użytku w
pojemnikach na odpady, a zużyty materiał opatrunkowy włożyć do
pojemnikach na odpady, a zużyty materiał opatrunkowy włożyć do
foliowego worka i przeznaczyć do spalenia
foliowego worka i przeznaczyć do spalenia
- sprzęt dezynfekować zgodnie z aktualnie obowiązującą instrukcją
- sprzęt dezynfekować zgodnie z aktualnie obowiązującą instrukcją
stosowania środków dezynfekcyjnych.
stosowania środków dezynfekcyjnych.
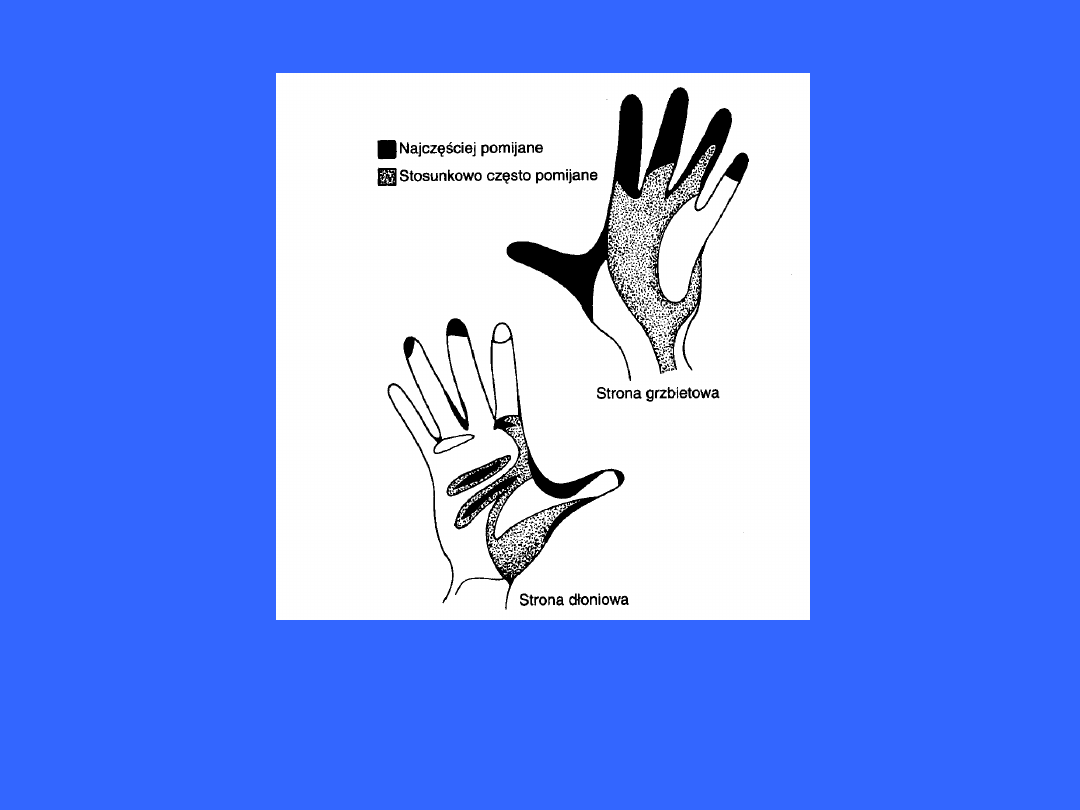
Obszary dłoni najczęściej pomijane podczas mycia rąk
Obszary dłoni najczęściej pomijane podczas mycia rąk

Wskazania do codziennego (zwykłego) mycia
Wskazania do codziennego (zwykłego) mycia
rąk
rąk
, które
, które
usuwa większość drobnoustrojów
usuwa większość drobnoustrojów
przejściowych z niezbyt zabrudzonych rąk
przejściowych z niezbyt zabrudzonych rąk
:
:
- przed jedzeniem
- przed jedzeniem
- przed rozpoczęciem pracy
- przed rozpoczęciem pracy
- po czynnościach biurowych, gospodarczych
- po czynnościach biurowych, gospodarczych
- po wyjściu z toalety
- po wyjściu z toalety
-
po długich przerwach w pracy
po długich przerwach w pracy
3-5 ml preparatu myjącego, mycie energiczne, 10-15
3-5 ml preparatu myjącego, mycie energiczne, 10-15
sek, technika Ayliffe
sek, technika Ayliffe

Wskazania do higienicznego mycia rąk
Wskazania do higienicznego mycia rąk
, które
, które
eliminuje wszystkie drobnoustroje przejściowe i
eliminuje wszystkie drobnoustroje przejściowe i
częściowo stałe
częściowo stałe
:
:
- przed wykonaniem i po wykonaniu inwazyjnych
- przed wykonaniem i po wykonaniu inwazyjnych
zabiegów (iniekcje, pobranie krwi, cewnikowanie,
zabiegów (iniekcje, pobranie krwi, cewnikowanie,
opatrunki, punkcje)
opatrunki, punkcje)
- przed i po pielęgnacji chorego, np. kąpiel, ścielenie łóżka
- przed i po pielęgnacji chorego, np. kąpiel, ścielenie łóżka
- przed i po dotknięciu ran, cewników naczyniowych,
- przed i po dotknięciu ran, cewników naczyniowych,
moczowych, drenów, sond
moczowych, drenów, sond
- przed i po zabiegach diagnostycznych, leczniczych,
- przed i po zabiegach diagnostycznych, leczniczych,
pielęgnacyjnych, rehabilitacyjnych przebiegających z
pielęgnacyjnych, rehabilitacyjnych przebiegających z
użyciem niejałowych rękawiczek jednorazowego użytku
użyciem niejałowych rękawiczek jednorazowego użytku

-
-
przed założeniem jałowych rękawiczek i po ich
przed założeniem jałowych rękawiczek i po ich
zdjęciu
zdjęciu
- po kontakcie z krwią, płynami ustrojowymi,
- po kontakcie z krwią, płynami ustrojowymi,
wydalinami, wydzielinami chorego
wydalinami, wydzielinami chorego
- po opuszczeniu boksów izolujących chorych zakaźnie
- po opuszczeniu boksów izolujących chorych zakaźnie
- po zdjęciu maski chirurgicznej, po użyciu chusteczki
- po zdjęciu maski chirurgicznej, po użyciu chusteczki
do nosa, po kaszlu lub kichaniu w dłonie
do nosa, po kaszlu lub kichaniu w dłonie
-
przed wejściem do sali operacyjnej, gabinetu
przed wejściem do sali operacyjnej, gabinetu
zabiegowego, przed pracą z jałowym materiałem
zabiegowego, przed pracą z jałowym materiałem
3-5 ml preparatu myjącego,
3-5 ml preparatu myjącego,
mycie higieniczne
mycie higieniczne
, 30-60
, 30-60
sek, technika Ayliffe
sek, technika Ayliffe
3-5 ml alkoholowego preparatu antyseptycznego,
3-5 ml alkoholowego preparatu antyseptycznego,
dezynfekcja higieniczna
dezynfekcja higieniczna
, 30-60 sek, technika Ayliffe
, 30-60 sek, technika Ayliffe
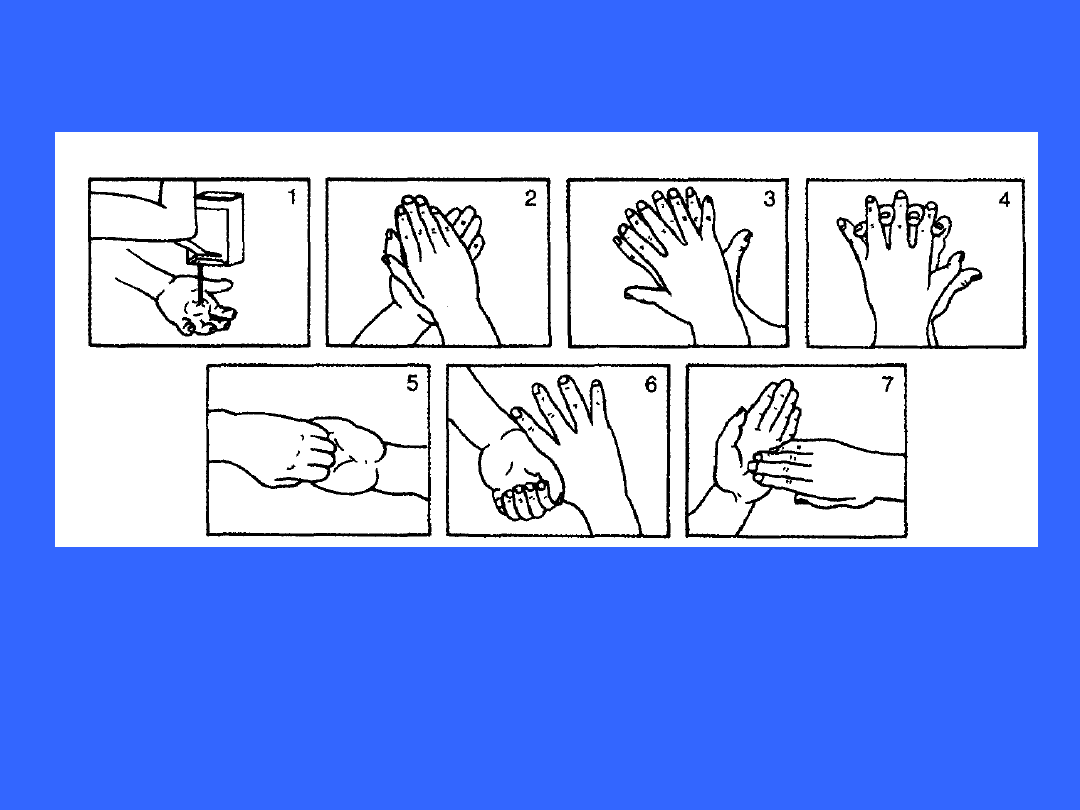
Technika Ayliffe
Technika Ayliffe
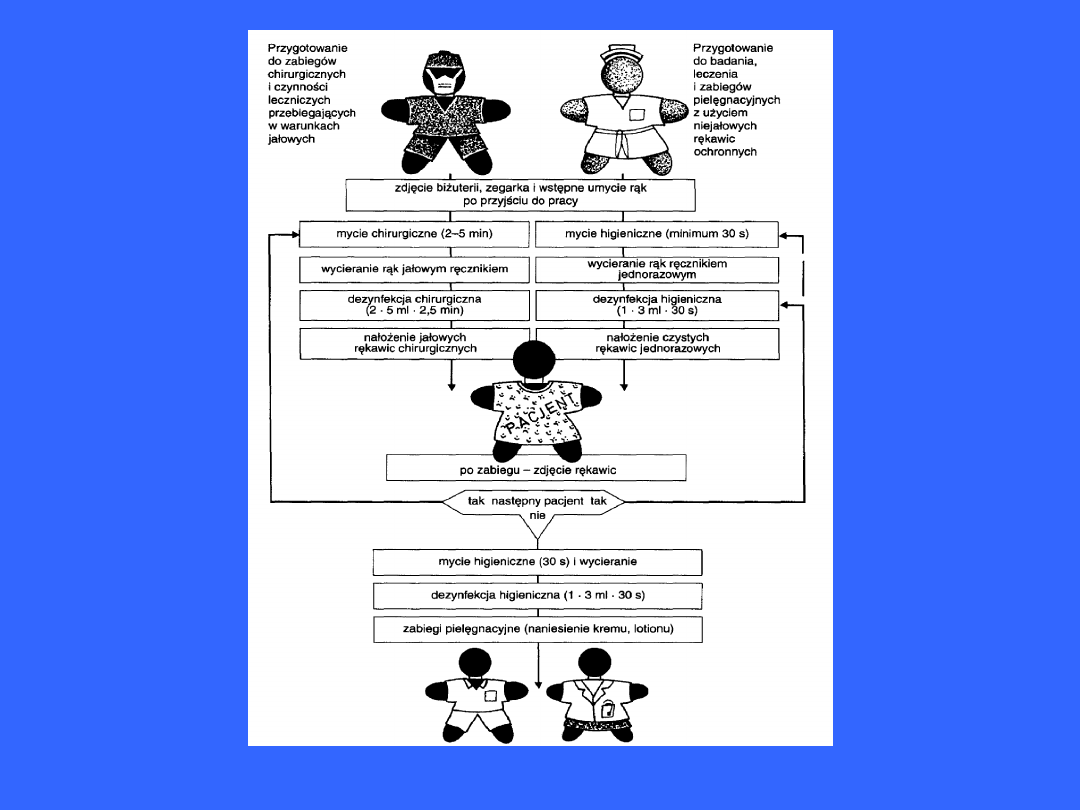
Schemat higienicznego mycia rąk
Schemat higienicznego mycia rąk

Higiena rąk – zasady ogólne
Higiena rąk – zasady ogólne
obetnij krótko paznokcie
obetnij krótko paznokcie
nie wycinaj skórek
nie wycinaj skórek
nie zakładaj w pracy pierścionków i obrączki
nie zakładaj w pracy pierścionków i obrączki
nie noś sztucznych lub lakierowanych paznokci
nie noś sztucznych lub lakierowanych paznokci
nie pracuj w odzieży z długim rękawem, zrezygnuj
nie pracuj w odzieży z długim rękawem, zrezygnuj
także z noszenia w pracy zegarka lub bransoletki
także z noszenia w pracy zegarka lub bransoletki
myj ręce bieżącą wodą
myj ręce bieżącą wodą
zmocz ręce przed nałożeniem preparatu myjącego
zmocz ręce przed nałożeniem preparatu myjącego
dokładnie osuszaj ręce przed dezynfekcją
dokładnie osuszaj ręce przed dezynfekcją
zakręcaj kurek przy użyciu suchego ręcznika
zakręcaj kurek przy użyciu suchego ręcznika
jednorazowego
jednorazowego

Proces dezynfekcji dzielimy na:
Proces dezynfekcji dzielimy na:
- dezynfekcję przed sterylizacją
- dezynfekcję przed sterylizacją
- dezynfekcję sprzętu, który nie musi być jałowy, a
- dezynfekcję sprzętu, który nie musi być jałowy, a
powinien być bezpieczny dla chorego
powinien być bezpieczny dla chorego

Proces dezynfekcji możemy przeprowadzić, stosując
Proces dezynfekcji możemy przeprowadzić, stosując
metody
metody
:
:
-
-
fizyczne (nietermiczne):
fizyczne (nietermiczne):
promieniowanie nadfioletowe,
promieniowanie nadfioletowe,
ultradźwięki i filtracja do odkażania roztworów i powietrza
ultradźwięki i filtracja do odkażania roztworów i powietrza
- termiczne:
- termiczne:
a) ciepło suche
a) ciepło suche
b) ciepło wilgotne:
b) ciepło wilgotne:
-
-
pasteryzacja
pasteryzacja
- ogrzanie płynu w temperaturze 65
- ogrzanie płynu w temperaturze 65
0
0
C przez 30
C przez 30
min. lub w temperaturze 75
min. lub w temperaturze 75
0
0
C przez 10 min., np. do odkażania
C przez 10 min., np. do odkażania
mleka (Brucellae, Salmonellae, prątki gruźlicy).
mleka (Brucellae, Salmonellae, prątki gruźlicy).
- dekoktacja
- dekoktacja
– proces niszczenia drobnoustrojów przez działanie
– proces niszczenia drobnoustrojów przez działanie
wrzącej wody lub pary wodnej w normalnym ciśnieniu przez 15-
wrzącej wody lub pary wodnej w normalnym ciśnieniu przez 15-
20 minut. Giną formy wegetatywne.
20 minut. Giną formy wegetatywne.

-
-
tyndalizacja
tyndalizacja
– niszczenie drobnoustrojów bieżącą parą wodną w
– niszczenie drobnoustrojów bieżącą parą wodną w
czasie 30 minut poprzez powtarzanie zabiegu w odstępach co
czasie 30 minut poprzez powtarzanie zabiegu w odstępach co
24 godz. Przeprowadzana jest w aparatach Kocha, niszczy
24 godz. Przeprowadzana jest w aparatach Kocha, niszczy
spory bakteryjne.
spory bakteryjne.
-
-
gotowanie
gotowanie
– w temperaturze 100
– w temperaturze 100
0
0
C przez 10-30 min., eliminuje
C przez 10-30 min., eliminuje
większość form wegetatywnych bakterii i wirusów, z wyjątkiem
większość form wegetatywnych bakterii i wirusów, z wyjątkiem
wirusa żółtaczki zakaźnej i spor (przetrwalników) bakteryjnych.
wirusa żółtaczki zakaźnej i spor (przetrwalników) bakteryjnych.
-
-
wyparzanie wodą
wyparzanie wodą
o temperaturze 100
o temperaturze 100
0
0
C pozwala na
C pozwala na
zmniejszenie liczby drobnoustrojów.
zmniejszenie liczby drobnoustrojów.
-
-
para wodna przy normalnym ciśnieniu atmosferycznym
para wodna przy normalnym ciśnieniu atmosferycznym
o
o
temperaturze 100
temperaturze 100
0
0
C jest środkiem bakteriobójczym o szerokich
C jest środkiem bakteriobójczym o szerokich
możliwościach stosowania w warunkach szpitalnych.
możliwościach stosowania w warunkach szpitalnych.
-
-
para wodna w nadciśnieniu
para wodna w nadciśnieniu
ma zastosowanie w autoklawach
ma zastosowanie w autoklawach
grawitacyjnych, służy do unieszkodliwiania posiewów
grawitacyjnych, służy do unieszkodliwiania posiewów
bakteryjnych, zużytego sprzętu jednorazowego, odpadów
bakteryjnych, zużytego sprzętu jednorazowego, odpadów
zakaźnych.
zakaźnych.
Ten proces nie spełnia standardów sterylizacji.
Ten proces nie spełnia standardów sterylizacji.

Sprzęt medyczny do dezynfekcji termicznej:
Sprzęt medyczny do dezynfekcji termicznej:
-
-
dezynfektory termiczne
dezynfektory termiczne
do kuchni mlecznej (mycie
do kuchni mlecznej (mycie
butelek)
butelek)
-
-
laboratoryjne myjnie dezynfektory
laboratoryjne myjnie dezynfektory
(mycie kolb,
(mycie kolb,
probówek, pipet)
probówek, pipet)
-
-
płuczki dezynfektory
płuczki dezynfektory
(opróżnianie, mycie, dezynfekcja
(opróżnianie, mycie, dezynfekcja
basenów, kaczek, misek, ssaków)
basenów, kaczek, misek, ssaków)
-
-
myjnie parowe
myjnie parowe
(urządzenia do mycia i dezynfekcji
(urządzenia do mycia i dezynfekcji
powierzchni)
powierzchni)
-
-
mechaniczne myjnie dezynfektory
mechaniczne myjnie dezynfektory
(mycie i dezynfekcja
(mycie i dezynfekcja
narzędzi chirurgicznych, sprzętu anestezjologicznego,
narzędzi chirurgicznych, sprzętu anestezjologicznego,
sprzętu o skomplikowanej budowie)
sprzętu o skomplikowanej budowie)

- termiczno-chemiczne
- termiczno-chemiczne
-automatyczne dezynfektory termiczno-chemiczne
-automatyczne dezynfektory termiczno-chemiczne
pozwalają na
pozwalają na
obniżenie temperatury przez użycie chemicznych preparatów,
obniżenie temperatury przez użycie chemicznych preparatów,
które działają w temp. 60
które działają w temp. 60
0
0
C przez 10 min. w zakresie
C przez 10 min. w zakresie
bakteriobójczym (B), grzybobójczym (F), prątkobójczym (Tbc),
bakteriobójczym (B), grzybobójczym (F), prątkobójczym (Tbc),
wirusobójczym (V). Służą do dezynfekcji endoskopów miękkich
wirusobójczym (V). Służą do dezynfekcji endoskopów miękkich
(próba szczelności i drożności, mycie i czyszczenie, dezynfekcja
(próba szczelności i drożności, mycie i czyszczenie, dezynfekcja
właściwa, płukanie sterylną wodą i suszenie urządzenia); cykl
właściwa, płukanie sterylną wodą i suszenie urządzenia); cykl
trwa około 30 minut.
trwa około 30 minut.
-
-
myjnie ultradźwiękowe
myjnie ultradźwiękowe
do urządzeń laparoskopowych, które
do urządzeń laparoskopowych, które
wykorzystują preparaty myjąco -dezynfekcyjne, w temperaturze
wykorzystują preparaty myjąco -dezynfekcyjne, w temperaturze
60
60
0
0
C.
C.
-komory dezynfekcyjne
-komory dezynfekcyjne
do dezynfekcji np. materacy, kocy,
do dezynfekcji np. materacy, kocy,
poduszek, lóżek, sprzętu ortopedycznego, rehabilitacyjnego.
poduszek, lóżek, sprzętu ortopedycznego, rehabilitacyjnego.

- chemiczne -
- chemiczne -
polegają na zastosowaniu
polegają na zastosowaniu
chemicznych substancji inaktywujących
chemicznych substancji inaktywujących
drobnoustroje.
drobnoustroje.
Chemiczne preparaty pozwalają na
Chemiczne preparaty pozwalają na
dezynfekcj
dezynfekcj
ę
ę
:
:
- powierzchni szpitalnych (podłóg, ścian, glazury,
- powierzchni szpitalnych (podłóg, ścian, glazury,
terakoty, stolików)
terakoty, stolików)
- narzędzi medycznych i aparatury medycznej
- narzędzi medycznych i aparatury medycznej
- sprzętu medycznego (łóżek, przyborów)
- sprzętu medycznego (łóżek, przyborów)
- bielizny szpitalnej
- bielizny szpitalnej
- wydalin, odpadów zakaźnych.
- wydalin, odpadów zakaźnych.

Wybrane preparaty do
Wybrane preparaty do
dezynfekcji narzędzi
dezynfekcji narzędzi
zaopiniowane przez PZH:
zaopiniowane przez PZH:
Aldesan E+aktywator,
Aldesan E+aktywator,
nierozcieńczony, 10 min (B, F, V), 1h (B, Tbc, F, V),
nierozcieńczony, 10 min (B, F, V), 1h (B, Tbc, F, V),
10h (B, Tbc, F, V, S)
10h (B, Tbc, F, V, S)
Cidex
Cidex
Lysoformin 3000,
Lysoformin 3000,
2% 15 min (B, V)
2% 15 min (B, V)
Virkon,
Virkon,
2% 10 min (B, V)
2% 10 min (B, V)
Septo DN
Septo DN
, 1% (urządzenia myjąco – dezynfekujące), 5 min, 60
, 1% (urządzenia myjąco – dezynfekujące), 5 min, 60
0
0
C (B, Tbc, F,
C (B, Tbc, F,
V)
V)
Wybrane preparaty do
Wybrane preparaty do
dezynfekcji powierzchni
dezynfekcji powierzchni
zaopiniowane przez PZH:
zaopiniowane przez PZH:
Chloramina T
Chloramina T
, 5% (powierzchnie zanieczyszczone substancjami
, 5% (powierzchnie zanieczyszczone substancjami
organicznymi), 15 min (B, V)
organicznymi), 15 min (B, V)
Alkohol etylowy
Alkohol etylowy
, 70-80%, 10 min (B, V)
, 70-80%, 10 min (B, V)
Incidur Spray
Incidur Spray
, stężony, 10 min. (B, F, V)
, stężony, 10 min. (B, F, V)
I
I
ncidin Liquid
ncidin Liquid
Spray
Spray
, stężony, 15 min.
, stężony, 15 min.
(B, F)
(B, F)
Aldesan E+ aktywator
Aldesan E+ aktywator
, stężony, 10 min (B, F, V)
, stężony, 10 min (B, F, V)
Lysoformin 3000
Lysoformin 3000
, 1%, 15 min (B, F)
, 1%, 15 min (B, F)

Chemiczne preparaty o wysokim rozcieńczeniu –
Chemiczne preparaty o wysokim rozcieńczeniu –
określane są mianem preparatów (środków)
określane są mianem preparatów (środków)
antyseptycznych
antyseptycznych
,
,
stosowane są na:
stosowane są na:
-
-
rany
rany
(Rivanol 0,1%, 1:1000 KMNO
(Rivanol 0,1%, 1:1000 KMNO
4
4
)
)
- błony śluzowe (Rivanol 0,1%, 1:10 000 KMNO
- błony śluzowe (Rivanol 0,1%, 1:10 000 KMNO
4
4
, Skinsept
, Skinsept
mucosa, Skinsept oral)
mucosa, Skinsept oral)
- skórę (Dodesept, Softasept N-spray, Skinsept Color/Pur-
- skórę (Dodesept, Softasept N-spray, Skinsept Color/Pur-
spray,)
spray,)
- skórę rąk (AHD 2000 Sterisol, Skinman, Spitaderm,
- skórę rąk (AHD 2000 Sterisol, Skinman, Spitaderm,
Biotensid); przed wymagają umycia w: Skinsept soap,
Biotensid); przed wymagają umycia w: Skinsept soap,
Sterisol gel, Seraman, Manisoft; po dezynfekcji wymagają
Sterisol gel, Seraman, Manisoft; po dezynfekcji wymagają
pielęgnacji: Sterisol hudlotion, Silonda, Silonda lipid.
pielęgnacji: Sterisol hudlotion, Silonda, Silonda lipid.

Preparaty dezynfekcyjne zawierają różne substancje
Preparaty dezynfekcyjne zawierają różne substancje
aktywne inaktywujące drobnoustroje:
aktywne inaktywujące drobnoustroje:
- aldehydy (formalina, aldehyd glutarowy)
- aldehydy (formalina, aldehyd glutarowy)
- alkohole (alifatyczne, aryloalifatyczne)
- alkohole (alifatyczne, aryloalifatyczne)
- chlorowce (chlor, jod, podchloryn sodu, chloraminy)
- chlorowce (chlor, jod, podchloryn sodu, chloraminy)
- pochodne biguanidyny (chlorheksydyna)
- pochodne biguanidyny (chlorheksydyna)
- związki fenolu (bifenole)
- związki fenolu (bifenole)
- kationowe związki powierzchniowo czynne (amfolity)
- kationowe związki powierzchniowo czynne (amfolity)
- związki utleniające (nadmanganiany).
- związki utleniające (nadmanganiany).

Wady dezynfekcji chemicznej:
Wady dezynfekcji chemicznej:
- szkodliwe działanie na personel, pacjentów,
- szkodliwe działanie na personel, pacjentów,
środowisko
środowisko
- wytwarzanie oporności drobnoustrojów na preparaty
- wytwarzanie oporności drobnoustrojów na preparaty
- trudność w ocenie skuteczności dezynfekcji
- trudność w ocenie skuteczności dezynfekcji
- niszczenie sprzętu (korozja, matowienie,
- niszczenie sprzętu (korozja, matowienie,
przebarwienia, pękanie)
przebarwienia, pękanie)
- szkodliwe działanie źle dobranego preparatu np.
- szkodliwe działanie źle dobranego preparatu np.
formaldehyd i guma.
formaldehyd i guma.

Zasady sporządzania roztworów roboczych do
Zasady sporządzania roztworów roboczych do
dezynfekcji chemicznej (
dezynfekcji chemicznej (
Komunikat MZiOS Dz. U.
Komunikat MZiOS Dz. U.
nr 11 z 1996r.)
nr 11 z 1996r.)
1
1
.
. nie wolno stosować do dezynfekcji powierzchni,
sprzętu medycznego z gumy i tworzyw sztucznych,
mającego
bezpośredni
kontakt
z
tkankami
(endoskopy) lub układem oddechowym (sprzęt
anestezjologiczny)
preparatów
zawierających
formaldehyd

2. w przypadku stosowania preparatów zawierających
aldehyd glutarowy jego stężenie nie może
przekraczać 0,2% w roztworach użytkowych,
dezynfekcję tym preparatem można przeprowadzać
wyłącznie
w
pomieszczeniach
z
prawidłową
wentylacją, w miejscach pobytu ludzi jednorazowo
można dezynfekować tym preparatem małe
powierzchnie (ok. 2m
2
), gdy dezynfekowane są
większe, pomieszczenie może być udostępnione
pacjentom,
personelowi
po
dokładnym
wywietrzeniu; preparaty z aldehydem glutarowym w
urządzeniach spryskujących mogą być stosowane
tylko do dezynfekcji trudno dostępnych powierzchni

3.
3. do dezynfekcji powierzchni stosuje się preparaty
skutecznie działające w czasie 15 min., preparaty
wymagające czasu dłuższego niż 15 min. stosuje się
do dezynfekcji sprzętu i przedmiotów, które można
zanurzyć lub wypełnić płynem
4. powierzchnie wolne od zanieczyszczeń organicznych
dezynfekuje
się
preparatami
bakteriobójczymi,
powierzchnie
zanieczyszczone
substancjami
organicznymi, np. krwią – preparatami bakterio- i
wirusobójczymi
(wskazane
prątkobójcze
i
grzybobójcze); plamy krwi trzeba zasypać preparatem
lub zalać roztworem o szybkim działaniu, po
zalecanym czasie materiał usunąć (traktując go jako
zakaźny), powierzchnie ponownie zdezynfekować i
umyć

6
6
. po zakończeniu procesu należy dokładnie
. po zakończeniu procesu należy dokładnie
wypłukać narzędzia wodą (przegotowaną-w
wypłukać narzędzia wodą (przegotowaną-w
przypadku działania dezynfekcyjnego, sterylną-
przypadku działania dezynfekcyjnego, sterylną-
działania sporobójczego)
działania sporobójczego)
7
7
. roztwory użytkowe należy przygotowywać w
. roztwory użytkowe należy przygotowywać w
wyznaczonym do tego pomieszczeniu zamkniętym,
wyznaczonym do tego pomieszczeniu zamkniętym,
niedostępnym dla osób niepowołanych, ze sprawnie
niedostępnym dla osób niepowołanych, ze sprawnie
działająca wentylacją, stosując środki ochrony
działająca wentylacją, stosując środki ochrony
osobistej: rękawiczki z lateksu, a przy preparatach
osobistej: rękawiczki z lateksu, a przy preparatach
zawierających aldehyd glutarowy i alkohol
zawierających aldehyd glutarowy i alkohol
izopropylowy z tworzyw butadienowo-styrenowych,
izopropylowy z tworzyw butadienowo-styrenowych,
winylowych oraz fartuchy, okulary
winylowych oraz fartuchy, okulary

8
8
. roztwory należy sporządzać codzienne, chyba że
. roztwory należy sporządzać codzienne, chyba że
istnieje możliwość kontroli stężenia substancji
istnieje możliwość kontroli stężenia substancji
czynnej to rzadziej, najdłuższy okres przechowywania
czynnej to rzadziej, najdłuższy okres przechowywania
roztworu w pojemniku zamkniętym nie może
roztworu w pojemniku zamkniętym nie może
przekraczać 7 dni; do przygotowania roztworów
przekraczać 7 dni; do przygotowania roztworów
preparatów przeznaczonych do dezynfekcji narzędzi
preparatów przeznaczonych do dezynfekcji narzędzi
lekarskich należy używać jałowej wody destylowanej,
lekarskich należy używać jałowej wody destylowanej,
do dezynfekcji powierzchni i przedmiotów jałowej
do dezynfekcji powierzchni i przedmiotów jałowej
wody twardej lub kierować się zaleceniami
wody twardej lub kierować się zaleceniami
producenta; nie wolno dopełniać naczyń
producenta; nie wolno dopełniać naczyń
zawierających częściowo zużyty roztwór; naczynia po
zawierających częściowo zużyty roztwór; naczynia po
zużytym roztworze należy wysterylizować lub
zużytym roztworze należy wysterylizować lub
zdezynfekować termicznie lub umyć i zdezynfekować;
zdezynfekować termicznie lub umyć i zdezynfekować;

osoba sporządzająca roztwór oznacza na pojemniku
osoba sporządzająca roztwór oznacza na pojemniku
nazwę preparatu, stężenie, datę i składa swój podpis;
nazwę preparatu, stężenie, datę i składa swój podpis;
stężenie roztworu musi być dostosowane do
stężenie roztworu musi być dostosowane do
zagrożenia i możliwości zastosowania wymaganego
zagrożenia i możliwości zastosowania wymaganego
czasu dezynfekcji; należy dążyć do stosowania
czasu dezynfekcji; należy dążyć do stosowania
najniższego z koniecznych stężeń roztworu;
najniższego z koniecznych stężeń roztworu;
preparaty dezynfekcyjne przechowywać w
preparaty dezynfekcyjne przechowywać w
oryginalnych opakowaniach; zabrania się używania
oryginalnych opakowaniach; zabrania się używania
preparatów dezynfekcyjnych w urządzeniach
preparatów dezynfekcyjnych w urządzeniach
rozpylających w oddziałach gruźliczych
rozpylających w oddziałach gruźliczych
9
9
. preparaty wymagające połączenia z aktywatorem nie
. preparaty wymagające połączenia z aktywatorem nie
mogą być używane dłużej jak 14 dni; na opakowaniu
mogą być używane dłużej jak 14 dni; na opakowaniu
należy zaznaczyć datę wsypania aktywatora.
należy zaznaczyć datę wsypania aktywatora.

Idealny preparat dezynfekcyjny
Idealny preparat dezynfekcyjny
- natychmiastowe działanie w niskim stężeniu na szeroki
- natychmiastowe działanie w niskim stężeniu na szeroki
zakres drobnoustrojów, bez wywoływania wzrostu ich
zakres drobnoustrojów, bez wywoływania wzrostu ich
oporności
oporności
- dobra biodegradacja, brak toksycznego działania, brak
- dobra biodegradacja, brak toksycznego działania, brak
zapachu
zapachu
- duża trwałość koncentratu i roztworów użytkowych
- duża trwałość koncentratu i roztworów użytkowych
- dobra rozpuszczalność w wodzie
- dobra rozpuszczalność w wodzie
- wysoka tolerancja na wodę twardą i substancje
- wysoka tolerancja na wodę twardą i substancje
organiczne
organiczne
- brak działania korodującego
- brak działania korodującego
- brak barwy i drażniącego działania na skórę
- brak barwy i drażniącego działania na skórę
- niska cena.
- niska cena.

Postępowanie z narzędziami medycznymi (z
Postępowanie z narzędziami medycznymi (z
wyjątkiem endoskopów) po zabiegu na
wyjątkiem endoskopów) po zabiegu na
oddziale (w laboratorium):
oddziale (w laboratorium):
-
dezynfekcja,
dezynfekcja,
-
mycie mechaniczne, ręczne lub ultradźwiękowe,
mycie mechaniczne, ręczne lub ultradźwiękowe,
-
płukanie,
płukanie,
-
suszenie,
suszenie,
-
kontrola techniczna,
kontrola techniczna,
-
pakowanie,
pakowanie,
-
wyjaławianie.
wyjaławianie.

Postępowanie ze sprzętem wielokrotnego użytku –
Postępowanie ze sprzętem wielokrotnego użytku –
endoskopy po użyciu:
endoskopy po użyciu:
oczyścić ze śluzu
oczyścić ze śluzu
umyć
umyć
zdezynfekować
zdezynfekować
wypłukać
wypłukać
wysuszyć
wysuszyć
zapakować
zapakować

Metody sterylizacji:
Metody sterylizacji:
a) gorąca sterylizacja
a) gorąca sterylizacja
:
:
- sterylizacja suchym gorącym powietrzem
- sterylizacja suchym gorącym powietrzem
(wyroby szklane,
(wyroby szklane,
porcelanowe, metalowe, oleje, wosk, gliceryna, pudry) w
porcelanowe, metalowe, oleje, wosk, gliceryna, pudry) w
sterylizatorach na suche gorące powietrze (wyjaławiacze
sterylizatorach na suche gorące powietrze (wyjaławiacze
elektryczne)
elektryczne)
1. dla urządzeń z wymuszonym obiegiem powietrza:
1. dla urządzeń z wymuszonym obiegiem powietrza:
- 160
- 160
0
0
C; 120 min.
C; 120 min.
- 180
- 180
0
0
C; 45 min
C; 45 min
- 200
- 200
0
0
C; 30 min
C; 30 min
2. dla urządzeń bez wymuszonego obiegu powietrza:
2. dla urządzeń bez wymuszonego obiegu powietrza:
- 160
- 160
0
0
C; 150 min
C; 150 min
- 180
- 180
0
0
C; 60 min
C; 60 min

- sterylizacja parą wodną w nadciśnieniu
- sterylizacja parą wodną w nadciśnieniu
(bielizna, materiał
(bielizna, materiał
opatrunkowy, narzędzia, rękawice, materiały gumowe, tworzywa
opatrunkowy, narzędzia, rękawice, materiały gumowe, tworzywa
sztuczne, woda, płyny infuzyjne, unieszkodliwianie posiewów
sztuczne, woda, płyny infuzyjne, unieszkodliwianie posiewów
mikrobiologicznych i zużytego sprzętu jednorazowego użytku) w
mikrobiologicznych i zużytego sprzętu jednorazowego użytku) w
autoklawach
autoklawach
- temperatura 121
- temperatura 121
0
0
C, 1 atm, 15 min
C, 1 atm, 15 min
- temperatura 134
- temperatura 134
0
0
C, 2 atm, 5,3 min
C, 2 atm, 5,3 min
metoda grawitacyjna
metoda grawitacyjna
(powietrze usuwane jest ze zbiornika
(powietrze usuwane jest ze zbiornika
ciśnieniowego przez wypieranie go nasyconą parą)
ciśnieniowego przez wypieranie go nasyconą parą)
metoda próżniowa
metoda próżniowa
(powietrze usuwa się z komory za pomocą
(powietrze usuwa się z komory za pomocą
pomp próżniowych, a następnie wprowadzana jest para wodna w
pomp próżniowych, a następnie wprowadzana jest para wodna w
nadciśnieniu; usunięcie pary i suszenie wsadu osiąga się przez
nadciśnieniu; usunięcie pary i suszenie wsadu osiąga się przez
wytworzenie próżni po wstępnym wyrównaniu ciśnienia)
wytworzenie próżni po wstępnym wyrównaniu ciśnienia)

b.
b.
zimna sterylizacja
zimna sterylizacja
:
:
- sterylizacja radiacyjna
- sterylizacja radiacyjna
na skalę przemysłową (materiały
na skalę przemysłową (materiały
opatrunkowe, bielizna operacyjna jednorazowego
opatrunkowe, bielizna operacyjna jednorazowego
użytku, leki, implanty, sprzęt jednorazowego użytku:
użytku, leki, implanty, sprzęt jednorazowego użytku:
strzykawki, igły, cewniki, sondy, aparaty do transfuzji);
strzykawki, igły, cewniki, sondy, aparaty do transfuzji);
nie można sprzętu resterylizować
nie można sprzętu resterylizować
-
sterylizacja tlenkiem etylenu (TE
sterylizacja tlenkiem etylenu (TE
): urządzenia optyczne,
): urządzenia optyczne,
elektryczne, respiratory, urządzenia sztucznej nerki; na
elektryczne, respiratory, urządzenia sztucznej nerki; na
skale przemysłową i w warunkach szpitalnych (artykuły
skale przemysłową i w warunkach szpitalnych (artykuły
wielokrotnego użytku z tworzyw sztucznych). Stężenie
wielokrotnego użytku z tworzyw sztucznych). Stężenie
TE 750 mg/l, temp. 50+- 8
TE 750 mg/l, temp. 50+- 8
0
0
C, wilgotność 40%, czas 4
C, wilgotność 40%, czas 4
godz.
godz.

Pomieszczenia dobrze wentylowane (6-10 wymian
Pomieszczenia dobrze wentylowane (6-10 wymian
powietrza na godzinę), nie wolno zatrudniać przy
powietrza na godzinę), nie wolno zatrudniać przy
obsłudze kobiet ciężarnych (działanie karcinogenne,
obsłudze kobiet ciężarnych (działanie karcinogenne,
mutagenne), gaz trujący od stężenia 0,5 ppm, zaś
mutagenne), gaz trujący od stężenia 0,5 ppm, zaś
wyczuwalny powonieniem przy 30-50 ppm (w
wyczuwalny powonieniem przy 30-50 ppm (w
pomieszczeniach do sterylizacji nie wolno przechowywać
pomieszczeniach do sterylizacji nie wolno przechowywać
płynów w pojemnikach plastikowych, kwiatów).
płynów w pojemnikach plastikowych, kwiatów).
Wymaga
Wymaga
degazacji
degazacji
w specjalnych pomieszczeniach lub z
w specjalnych pomieszczeniach lub z
użyciem aeratorów (60
użyciem aeratorów (60
0
0
C, obieg filtrowanego powietrza).
C, obieg filtrowanego powietrza).
7 dni wietrzenia przedmiotów z tworzyw sztucznych w
7 dni wietrzenia przedmiotów z tworzyw sztucznych w
temperaturze pokojowej, 12 godzin w komorach
temperaturze pokojowej, 12 godzin w komorach
areacyjnych.
areacyjnych.

c)
c)
sterylizacja niskotemperaturowa
sterylizacja niskotemperaturowa
- sterylizacja formaldehydowa (F):
- sterylizacja formaldehydowa (F):
rozruszniki serca,
rozruszniki serca,
endoskopy, elementy optyki. 4,5 godz., 48
endoskopy, elementy optyki. 4,5 godz., 48
0
0
C lub
C lub
55
55
0
0
C.
C.
-
-
sterylizacja plazmowa (nadtlenek wodoru):
sterylizacja plazmowa (nadtlenek wodoru):
przedmioty medyczne wrażliwe na temperaturę
przedmioty medyczne wrażliwe na temperaturę
;
;
50
50
0
0
C
C
,
,
1,5 godz.
1,5 godz.
- sterylizacja kwasem nadoctowym:
- sterylizacja kwasem nadoctowym:
endoskopy, sprzęt
endoskopy, sprzęt
anestezjologiczny, 50-55
anestezjologiczny, 50-55
0
0
C, 30 min.
C, 30 min.

Sterylizator na suche gorące powietrze z
Sterylizator na suche gorące powietrze z
wymuszonym obiegiem powietrza
wymuszonym obiegiem powietrza

Sterylizarotor 15 Vacum pojemność 15 l do
Sterylizarotor 15 Vacum pojemność 15 l do
sterylizacji nasyconą parą wodną opakowanych i
sterylizacji nasyconą parą wodną opakowanych i
nieopakowanych
nieopakowanych

Sterylizator parowy
Sterylizator parowy
SECUREX
SECUREX


Kontrola sterylizacji:
Kontrola sterylizacji:
wskaźniki fizyczne
wskaźniki fizyczne
(termometry, manometry,
(termometry, manometry,
wskaźniki czasu, kontrolki świetlne)
wskaźniki czasu, kontrolki świetlne)
wskaźniki chemiczne
wskaźniki chemiczne
:
:
STEAM – sterylizacja parą wodną
STEAM – sterylizacja parą wodną
DRY – sterylizacja suchym gorącym powietrzem
DRY – sterylizacja suchym gorącym powietrzem
EO - sterylizacja tlenkiem etylenu
EO - sterylizacja tlenkiem etylenu
IRRAD – sterylizacja promieniowaniem jonizującym
IRRAD – sterylizacja promieniowaniem jonizującym
FORM – sterylizacja formaldehydem
FORM – sterylizacja formaldehydem

Wskaźniki chemiczne do kontroli sterylizacji para wodną w
Wskaźniki chemiczne do kontroli sterylizacji para wodną w
nadciśnieniu:
nadciśnieniu:
1. Taśma kontrolna (
1. Taśma kontrolna (
ukośne linie zmieniają barwę z białej na szarą)
ukośne linie zmieniają barwę z białej na szarą)
2. Wskaźnik emulacyjny TST (
2. Wskaźnik emulacyjny TST (
pasek zmienia barwę
pasek zmienia barwę
z żółtej na
z żółtej na
fioletową)
fioletową)
Wskaźniki do kontroli sterylizacji suchym gorącym
Wskaźniki do kontroli sterylizacji suchym gorącym
powietrzem:
powietrzem:
1. Taśma kontrolna (
1. Taśma kontrolna (
znaki w kształcie litery V zmieniają się z
znaki w kształcie litery V zmieniają się z
zielonej na brunatną)
zielonej na brunatną)
2. Rurki Browne’a typu 5 (
2. Rurki Browne’a typu 5 (
zmiana barwy z czerwonej na zieloną)
zmiana barwy z czerwonej na zieloną)
Wskaźniki chemiczne do kontroli sterylizacji tlenkiem
Wskaźniki chemiczne do kontroli sterylizacji tlenkiem
etylenu:
etylenu:
1. Taśma kontrolna (
1. Taśma kontrolna (
brązowe napisy „gas” zmieniają się na zielone)
brązowe napisy „gas” zmieniają się na zielone)
2. Test paskowy EOp (
2. Test paskowy EOp (
zmiana koloru czerwonego na zielony)
zmiana koloru czerwonego na zielony)

Wskaźniki chemiczne do kontroli sterylizacji formaldehydem:
Wskaźniki chemiczne do kontroli sterylizacji formaldehydem:
1. Groszek samoprzylepny (
1. Groszek samoprzylepny (
zmiana barwy z niebieskiej na żółtą)
zmiana barwy z niebieskiej na żółtą)
2. Test paskowy (
2. Test paskowy (
zmiana barwy z niebieskiej na zieloną).
zmiana barwy z niebieskiej na zieloną).
wskaźniki biologiczne:
wskaźniki biologiczne:
1. Sporal S (
1. Sporal S (
sterylizacja suchym gorącym powietrzem, krążki bibuły
sterylizacja suchym gorącym powietrzem, krążki bibuły
przenieść na pożywkę i inkubować 7 dni)
przenieść na pożywkę i inkubować 7 dni)
2. Sporal A
2. Sporal A
(sterylizacja para wodną, bibułowy pasek inkubuje się na
(sterylizacja para wodną, bibułowy pasek inkubuje się na
pożywce 14 dni)
pożywce 14 dni)
3. Biologiczny test fiolkowy (
3. Biologiczny test fiolkowy (
sterylizacja parą wodną, po 8, 12, 18,
sterylizacja parą wodną, po 8, 12, 18,
24, 48 godz. odczytuje się wynik, zmiana koloru na żółty to
24, 48 godz. odczytuje się wynik, zmiana koloru na żółty to
nieskuteczna sterylizacja)
nieskuteczna sterylizacja)
4. Test do kontroli skuteczności sterylizacji tlenkiem etylenu
4. Test do kontroli skuteczności sterylizacji tlenkiem etylenu
(test fiolkowy, odczyt po 48 godz, nieskuteczny proces to zmiana
(test fiolkowy, odczyt po 48 godz, nieskuteczny proces to zmiana
koloru pożywki na żółty)
koloru pożywki na żółty)
5. Test do kontroli skuteczności sterylizacji formaldehydowej
5. Test do kontroli skuteczności sterylizacji formaldehydowej
(
(
test bibułowy lub fiolkowy)
test bibułowy lub fiolkowy)

Wg zaleceń WHO, PZH proces sterylizacji
Wg zaleceń WHO, PZH proces sterylizacji
każdorazowo powinien być kontrolowany
każdorazowo powinien być kontrolowany
wskaźnikami fizycznymi i chemicznymi; w
wskaźnikami fizycznymi i chemicznymi; w
przypadku sterylizacji tlenkiem etylenu każdy
przypadku sterylizacji tlenkiem etylenu każdy
proces powinien być kontrolowany
proces powinien być kontrolowany
biologicznie; w pozostałych sposobach
biologicznie; w pozostałych sposobach
sterylizacji kontrola wskaźnikami
sterylizacji kontrola wskaźnikami
biologicznymi powinna odbywać się okresowo
biologicznymi powinna odbywać się okresowo
(raz w tygodniu, najrzadziej raz w miesiącu, a
(raz w tygodniu, najrzadziej raz w miesiącu, a
wg PZH raz na kwartał)
wg PZH raz na kwartał)



Rodzaje opakowań sterylizacyjnych:
Rodzaje opakowań sterylizacyjnych:
a) pojemniki wielokrotnego użytku (
a) pojemniki wielokrotnego użytku (
pojemniki
pojemniki
sterylizacyjne z filtrem
sterylizacyjne z filtrem
jednorazowym lub
jednorazowym lub
wielorazowym,
wielorazowym,
pojemniki sterylizacyjne z zaworem,
pojemniki sterylizacyjne z zaworem,
siatki sterylizacyjne
siatki sterylizacyjne
) do sterylizacji w
) do sterylizacji w
autoklawach
autoklawach
:
:
narzędzi chirurgicznych, bielizny operacyjnej,
narzędzi chirurgicznych, bielizny operacyjnej,
rękawiczek chirurgicznych, szkła laboratoryjnego)
rękawiczek chirurgicznych, szkła laboratoryjnego)
b)
b)
jednorazowe opakowania
jednorazowe opakowania
specjalistyczne do
specjalistyczne do
sterylizacji
sterylizacji
suchym gorącym powietrzem, parą wodną
suchym gorącym powietrzem, parą wodną
w nadciśnieniu, tlenkiem etylenu, metodą radiacyjną,
w nadciśnieniu, tlenkiem etylenu, metodą radiacyjną,
plazmową, formaldehydem
plazmową, formaldehydem
. Zaliczamy do nich:
. Zaliczamy do nich:

- włókniny - do pakietowania przy dużym ciężarze tac
- włókniny - do pakietowania przy dużym ciężarze tac
- papier krepowany (sterylizacyjny). Należy stosować podwójną
- papier krepowany (sterylizacyjny). Należy stosować podwójną
warstwę opakowań: papier i włóknina lub dwie warstwy
warstwę opakowań: papier i włóknina lub dwie warstwy
papieru.
papieru.
- rękawy foliowe (TYVEK, zamykane zgrzewarką – do sterylizacji
- rękawy foliowe (TYVEK, zamykane zgrzewarką – do sterylizacji
plazmowej, nie nadają się do sterylizacji parowej, ulegają
plazmowej, nie nadają się do sterylizacji parowej, ulegają
topnieniu
topnieniu
- rękawy (torebki) papierowo-foliowe (WIPAK): zgrzewarka
- rękawy (torebki) papierowo-foliowe (WIPAK): zgrzewarka
impulsowa do sterylizacji suchym gorącym powietrzem,
impulsowa do sterylizacji suchym gorącym powietrzem,
zgrzewarka rolkowa lub impulsowa do sterylizacji parowej i
zgrzewarka rolkowa lub impulsowa do sterylizacji parowej i
gazowej. Są dostępne samozamykające, jednostronnie
gazowej. Są dostępne samozamykające, jednostronnie
przezroczyste torebki. Rękawy (torebki) należy wypełniać do
przezroczyste torebki. Rękawy (torebki) należy wypełniać do
3/4 objętości.
3/4 objętości.
- torebki osłonowe.
- torebki osłonowe.

Okres przechowywania narzędzi medycznych
Okres przechowywania narzędzi medycznych
opakowanych w
opakowanych w
:
:
- torebki papierowe zamykane zgrzewarką – 4 tygodnie
- torebki papierowe zamykane zgrzewarką – 4 tygodnie
-
rękawy papierowo-foliowe zamykane zgrzewarką: pojedyncza
rękawy papierowo-foliowe zamykane zgrzewarką: pojedyncza
torba – 6 miesięcy, dwie torby jedna w drugiej indywidualnie
torba – 6 miesięcy, dwie torby jedna w drugiej indywidualnie
zgrzane – 12 miesięcy, opakowanie dodatkowo umieszczone w
zgrzane – 12 miesięcy, opakowanie dodatkowo umieszczone w
torebce osłonowej – 5 lat
torebce osłonowej – 5 lat
-
pojemniki sterylizacyjne z filtrem 1 miesiąc,
pojemniki sterylizacyjne z filtrem 1 miesiąc,
-
pojemniki sterylizacyjne z zaworem 6 miesięcy.
pojemniki sterylizacyjne z zaworem 6 miesięcy.
Przechowywać w pomieszczeniach suchych, czystych, z dala od
Przechowywać w pomieszczeniach suchych, czystych, z dala od
promieni słonecznych, w temp. 18-22
promieni słonecznych, w temp. 18-22
0
0
C, w szafach
C, w szafach
zamkniętych. Nie narażać na przesuwanie, przenoszenie,
zamkniętych. Nie narażać na przesuwanie, przenoszenie,
uszkodzenia mechaniczne.
uszkodzenia mechaniczne.


Uniwersalne środki ostrożności w zapobieganiu
Uniwersalne środki ostrożności w zapobieganiu
przenoszenia HIV/HBV/HCV:
przenoszenia HIV/HBV/HCV:
przestrzegać zasad aseptyki
przestrzegać zasad aseptyki
przestrzegać zasad antyseptyki
przestrzegać zasad antyseptyki
przestrzegać mycia rąk
przestrzegać mycia rąk
stosować mechaniczne środki ostrożności
stosować mechaniczne środki ostrożności
właściwie postępować ze sprzętem i materiałem
właściwie postępować ze sprzętem i materiałem
jednorazowego użytku (szczególnie z igłami, ostrymi
jednorazowego użytku (szczególnie z igłami, ostrymi
narzędziami)
narzędziami)
właściwie postępować ze sprzętem wielokrotnego użytku
właściwie postępować ze sprzętem wielokrotnego użytku
właściwie postępować przy uszkodzonej skórze i błonach
właściwie postępować przy uszkodzonej skórze i błonach
śluzowych
śluzowych
właściwie postępować przy rozlaniu krwi
właściwie postępować przy rozlaniu krwi

właściwie transportować krew i inne materiały do badań
właściwie transportować krew i inne materiały do badań
analitycznych
analitycznych
właściwie postępować przy usuwaniu odpadów
właściwie postępować przy usuwaniu odpadów
przestrzegać zasad obowiązujących przy przetaczaniu
przestrzegać zasad obowiązujących przy przetaczaniu
krwi lub środków krwiopochodnych, prowadzeniu
krwi lub środków krwiopochodnych, prowadzeniu
sztucznego oddychania
sztucznego oddychania
właściwie postępować z bielizną, na której są ślady krwi
właściwie postępować z bielizną, na której są ślady krwi
lub innych płynów ustrojowych
lub innych płynów ustrojowych
eliminować z pracy pośpiech, niedbalstwo, złą
eliminować z pracy pośpiech, niedbalstwo, złą
organizację pracy
organizację pracy
monitorować zakażenia na terenie zakładów opieki
monitorować zakażenia na terenie zakładów opieki
zdrowotnej
zdrowotnej
zapewnić dostateczna ilość sprzętu jednorazowego
zapewnić dostateczna ilość sprzętu jednorazowego
użytku.
użytku.

HIV
HIV
HBV
HBV
Dawka zakażająca krwi: 0.1 ml 0.00004
Dawka zakażająca krwi: 0.1 ml 0.00004
ml
ml
Prawdopodobieństwo zakażenia 0.4% 20%
Prawdopodobieństwo zakażenia 0.4% 20%
Wrażliwość na temperaturę 56
Wrażliwość na temperaturę 56
0
0
C 120
C 120
0
0
C
C
Wrażliwość na związki chemiczne wrażliwy na
Wrażliwość na związki chemiczne wrażliwy na
niektóre
niektóre
Czynne uodparnianie brak
Czynne uodparnianie brak
ENGERIX-B
ENGERIX-B

ZAKAŹNE PŁYNY USTROJOWE
ZAKAŹNE PŁYNY USTROJOWE
KREW
KREW
INNY POTENCJALNIE INFEKCYJNY MATERIAŁ (IPIM):
INNY POTENCJALNIE INFEKCYJNY MATERIAŁ (IPIM):
-
Nasienie
Nasienie
-
Wydzielina z pochwy
Wydzielina z pochwy
-
Płyn mózgowo-rdzeniowy, owodniowy, z opłucnej, otrzewnej,
Płyn mózgowo-rdzeniowy, owodniowy, z opłucnej, otrzewnej,
osierdzia, stawowy
osierdzia, stawowy
-
Żółć, mleko kobiece
Żółć, mleko kobiece
-
Ślina w czasie zabiegów dentystycznych
Ślina w czasie zabiegów dentystycznych
-
Każdy płyn ustrojowy zawierający domieszkę krwi
Każdy płyn ustrojowy zawierający domieszkę krwi
-
Tkanki lub narządy pobierane od pacjenta.
Tkanki lub narządy pobierane od pacjenta.
NIEZAKAŹNE PŁYNY USTROJOWE: stolec, mocz, ślina, łzy, pot.
NIEZAKAŹNE PŁYNY USTROJOWE: stolec, mocz, ślina, łzy, pot.
To również otarcia naskórka powyżej 24 godz., „stare rany” powyżej
To również otarcia naskórka powyżej 24 godz., „stare rany” powyżej
3 dni.
3 dni.

RODZAJE EKSPOZYCJI NA ZAKAŻENIE HIV
RODZAJE EKSPOZYCJI NA ZAKAŻENIE HIV
-
Wątpliwa
Wątpliwa
– profilaktyka poekspozycyjna nie
– profilaktyka poekspozycyjna nie
oferowana.
oferowana.
-
Prawdopodobna
Prawdopodobna
- profilaktyka poekspozycyjna
- profilaktyka poekspozycyjna
oferowana
oferowana
-
Wyraźna
Wyraźna
- profilaktyka poekspozycyjna zawsze
- profilaktyka poekspozycyjna zawsze
oferowana
oferowana
-
Masywna
Masywna
- profilaktyka poekspozycyjna zawsze
- profilaktyka poekspozycyjna zawsze
oferowana
oferowana

POSTĘPOWANIE PO EKSPOZYCJI na materiał zawierający HIV
POSTĘPOWANIE PO EKSPOZYCJI na materiał zawierający HIV
:
:
1.
1.
Natychmiast usunąć krew lub IPIM, umyć ranę ciepłą wodą z
Natychmiast usunąć krew lub IPIM, umyć ranę ciepłą wodą z
mydłem, pozwolić na swobodny wypływ krwi z rany,
mydłem, pozwolić na swobodny wypływ krwi z rany,
zdezynfekować obszar rany 2x, zabezpieczyć ranę opatrunkiem
zdezynfekować obszar rany 2x, zabezpieczyć ranę opatrunkiem
wodoszczelnym, oczy spłukać 0.9% NaCL lub bieżącą wodą,
wodoszczelnym, oczy spłukać 0.9% NaCL lub bieżącą wodą,
wypluć krew lub IPIM z jamy ustnej, przepłukać kilkanaście razy
wypluć krew lub IPIM z jamy ustnej, przepłukać kilkanaście razy
wodą jamę ustną
wodą jamę ustną
2.
2.
Dokonać oceny ryzyka zakażenia
Dokonać oceny ryzyka zakażenia
3.
3.
Oznaczyć w surowicy krwi przeciwciała anty-HIV, antygen HBs,
Oznaczyć w surowicy krwi przeciwciała anty-HIV, antygen HBs,
przeciwciała anty-HCV
przeciwciała anty-HCV
4.
4.
Odnotować okoliczności ekspozycji w protokole powypadkowym,
Odnotować okoliczności ekspozycji w protokole powypadkowym,
raporcie pielęgniarskim, zgłosić przełożonemu
raporcie pielęgniarskim, zgłosić przełożonemu
5.
5.
Powiadomić lekarza odpowiedzialnego za postępowanie
Powiadomić lekarza odpowiedzialnego za postępowanie
poekspozycyjne
poekspozycyjne
6.
6.
Rozważyć podanie leków antyretrowirusowych, omówić styl
Rozważyć podanie leków antyretrowirusowych, omówić styl
życia
życia

7. Rozpocząć podawanie leków bezpośrednio po
7. Rozpocząć podawanie leków bezpośrednio po
ekspozycji (optymalny czas 2-4 godzin, nie później
ekspozycji (optymalny czas 2-4 godzin, nie później
jak 48 godzin)
jak 48 godzin)
8. Kontrola przeciwciał anty-HIV, antygenu HBs,
8. Kontrola przeciwciał anty-HIV, antygenu HBs,
przeciwciał anty-HCV po 6 tygodniach, 3 i 6
przeciwciał anty-HCV po 6 tygodniach, 3 i 6
miesiącach
miesiącach
9. Kontrola co 7 dni w trakcie leczenia
9. Kontrola co 7 dni w trakcie leczenia
antyretrowirusowego morfologii krwi,
antyretrowirusowego morfologii krwi,
aminotransferaz, mocznika, kreatyniny, amylazy w
aminotransferaz, mocznika, kreatyniny, amylazy w
surowicy krwi.
surowicy krwi.

POSTĘPOWANIE PO EKSPOZYCJI na materiał
POSTĘPOWANIE PO EKSPOZYCJI na materiał
zawierający HBV:
zawierający HBV:
Jest zależne od wyniku badania na antygen HBs i
Jest zależne od wyniku badania na antygen HBs i
ewentualnych szczepień otrzymanych w przeszłości
ewentualnych szczepień otrzymanych w przeszłości
przez osobę eksponowaną
przez osobę eksponowaną
Osoba zakażona HBV (HBsAg+):
Osoba zakażona HBV (HBsAg+):
bez immunoglobuliny
bez immunoglobuliny
i szczepionki
i szczepionki
Osoba nie zakażona, nie szczepiona przeciw WZW B
Osoba nie zakażona, nie szczepiona przeciw WZW B
:
:
immunoglobulina anty HBs, szczepionka 3 dawki
immunoglobulina anty HBs, szczepionka 3 dawki
Osoba szczepiona przeciw WZW B do 36 miesięcy
Osoba szczepiona przeciw WZW B do 36 miesięcy
: nic
: nic
Osoba szczepiona przeciw WZW B ponad 36 miesięcy
Osoba szczepiona przeciw WZW B ponad 36 miesięcy
:
:
immunoglobulina anty-HBs, szczepionka 1 dawka
immunoglobulina anty-HBs, szczepionka 1 dawka

Znany jest poziom przeciwciał anty-HBs:
Znany jest poziom przeciwciał anty-HBs:
-
Powyżej 100IU/l
Powyżej 100IU/l
– bez immunoglobuliny i szczepionki
– bez immunoglobuliny i szczepionki
-
Od 100 do 10 IU/l
Od 100 do 10 IU/l
– immunoglobulina nie, 1 dawka
– immunoglobulina nie, 1 dawka
szczepionki
szczepionki
-
Poniżej 10 IU/l
Poniżej 10 IU/l
– immunoglobulina, 3 dawki
– immunoglobulina, 3 dawki
szczepionki
szczepionki
Jeżeli osoba eksponowana nie jest zakażona HBV w
Jeżeli osoba eksponowana nie jest zakażona HBV w
momencie ekspozycji, powinna być zbadana
momencie ekspozycji, powinna być zbadana
ponownie po 3 i 6 miesiącach.
ponownie po 3 i 6 miesiącach.

Literatura:
Literatura:
Ciuruś M.J.: Zapobieganie zakażeniom w gabinetach
Ciuruś M.J.: Zapobieganie zakażeniom w gabinetach
zabiegowych a jakość usług medycznych. Adi, Łódź 1999.
zabiegowych a jakość usług medycznych. Adi, Łódź 1999.
Dzierżanowska D., Jeliasiewicz J. (red.): Zakażenia szpitalne. A-
Dzierżanowska D., Jeliasiewicz J. (red.): Zakażenia szpitalne. A-
medica press, Bielsko Biała 1999.
medica press, Bielsko Biała 1999.
Nosowska K.: Podstawy sterylizacji i dezynfekcji w zwalczaniu
Nosowska K.: Podstawy sterylizacji i dezynfekcji w zwalczaniu
zakażeń szpitalnych. Czelej, Lublin 1999.
zakażeń szpitalnych. Czelej, Lublin 1999.
Piegdoń G., Rzewuska I., Pękacki J.: Wybrane zagadnienia z
Piegdoń G., Rzewuska I., Pękacki J.: Wybrane zagadnienia z
tematyki zakażeń szpitalnych. Auxilium, Warszawa 1996.
tematyki zakażeń szpitalnych. Auxilium, Warszawa 1996.
Postępowanie zapobiegawcze i diagnostyczne w przypadku
Postępowanie zapobiegawcze i diagnostyczne w przypadku
zakażenia HIV i zachorowania na AIDS – zalecenia dla
zakażenia HIV i zachorowania na AIDS – zalecenia dla
pracowników medycznych. Krajowe Biuro Koordynacyjne ds.
pracowników medycznych. Krajowe Biuro Koordynacyjne ds.
Zapobiegania AIDS. Warszawa 1996.
Zapobiegania AIDS. Warszawa 1996.

DZIĘKUJĘ ZA UWAGĘ
DZIĘKUJĘ ZA UWAGĘ
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
Wyszukiwarka
Podobne podstrony:
Pobieranie materiałów do badań
POBIERANIE MATERIALOW DO BADAN MIKROBIOLOGICZNYCH ppt
pobieranie materiału d do badań
pobieranie materiału do badań
Pobieranie materiału do badań biologicznych, Ratownicto Medyczne, MIKROBIOLOGIA
pobieranie materialu do badań morfologicznych wyklady
Pobieranie materiałów do badań
POBIERANIE MATERIALOW DO BADAN MIKROBIOLOGICZNYCH ppt
Pobieranie materiałów do badań
Pobieranie materiału do badań laboratoryjnych
POBIERANIE I PRZECHOWYWANIE MATERIAŁÓW DO BADAŃ wiRUSOLOGICZNYCH prezentacja
pobieranie i przesyłanie materiałów do badań mikrobiologicznych, mikrobiologia
Pobieranie i przesyłanie materiału do badań, UM Wrocław - Stomatologia, Mikrobiologia i mikrobiolog
POBIERANIE I PRZECHOWYWANIE MATERIAŁÓW DO BADAŃ wiRUSOLOGICZNYCH prezentacja
Badanie cytologiczne i histopatologiczne Zasady prawidłowego pobierania, opisywania i przesyłania ma
Podstawa programowa z techniki, szkoła, Materiały do techniki(technika)
genetyka cw 9 materiał do badan
Nakłucie tętnicy, Studia - materiały, Analityka ogólna i techniki pobierania materiału
I wykład analityka ogólna i techniki pobierania materiału, Analityka Medyczna UMB, III, Analityka Og
więcej podobnych podstron