
WODÓR
Ar
Al
Rn
Ga
N
e
Na
Be
Kr
Xe
B
In
H
e
Li
Mg
K
Rb
Cs
Fr
Ca
Sr
Ba
Ra
Sc
Y
La-Lu
Ac-Lr
Ti
Zr
Hf
Rf
V
Nb
Ta
Db
Cr
Mo
W
Sg
Mn
Tc
Re
Bh
Fe
Ru
Os
Hs
Co
Rh
Ir
Mt
Ni
Pd
Pt
Cu
Ag
Au
Zn
Cd
Hg Tl
C N O
F
Si P
S Cl
Br
I
At
Ge
Sn
Pb
As
Sb
Bi Po
Se
Te
Lantanowce
Tb
Gd
Eu
Pm
La
Sm
Yb
Pr
Ce
Tm
Er
Ho
Nd
Dy
Lu
Aktynowce
Bk
Cm
Am
Np
Ac
Pu
Pa
Th
Md
Fm
Es
U
Df
No Lr
H
H H H
H H H H H
H H H H H H H H H HH
H
H
H
H
H
H
H
H
H
H
H
H
?
H
?
H
?
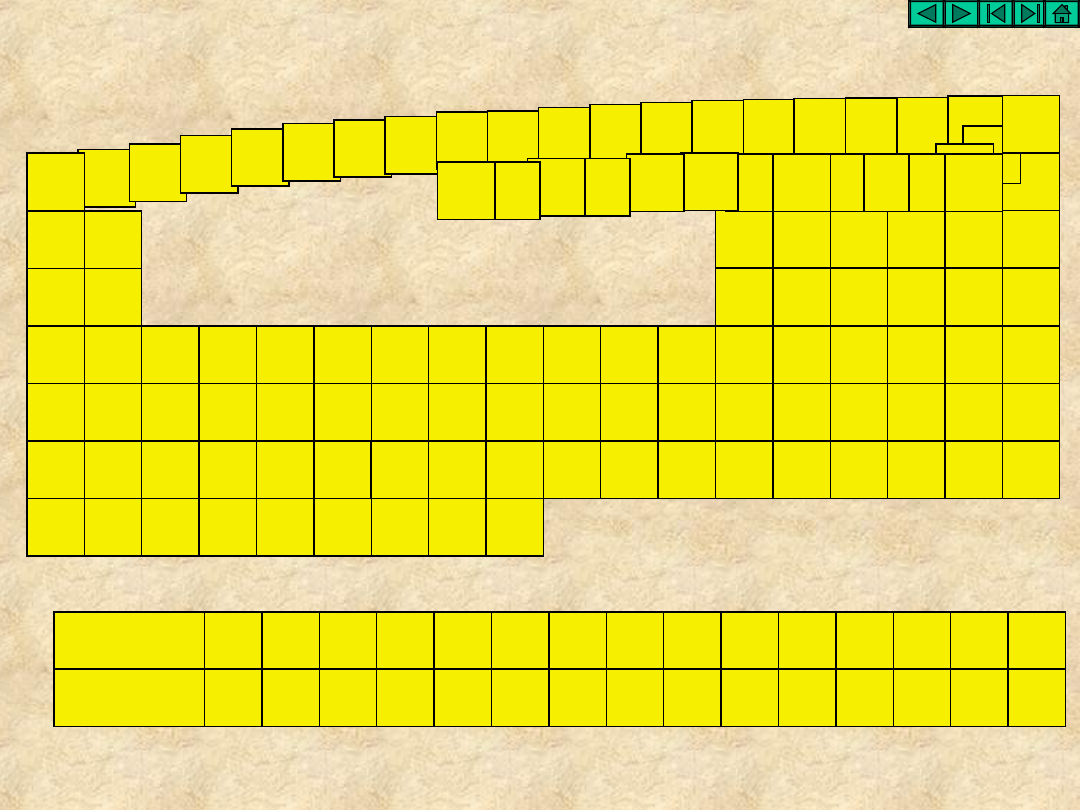
Miejsce wodoru w układzie okresowym
?
H
Al
Ga
Na
Be
B
In
Li
Mg
K
Rb
Cs
Ca
Sr
Ba
Sc
Y
La
Ti
Zr
Hf
V
Nb
Ta
Cr
Mo
W
Mn
Tc
Re
Fe
Ru
Os
Co
Rh
Ir
Ni
Pd
Pt
Cu
Ag
Au
Zn
Cd
Hg Tl
C N O
F
Si P
S Cl
Br
I
At
Ge
Sn
Pb
As
Sb
Bi Po
Se
Te
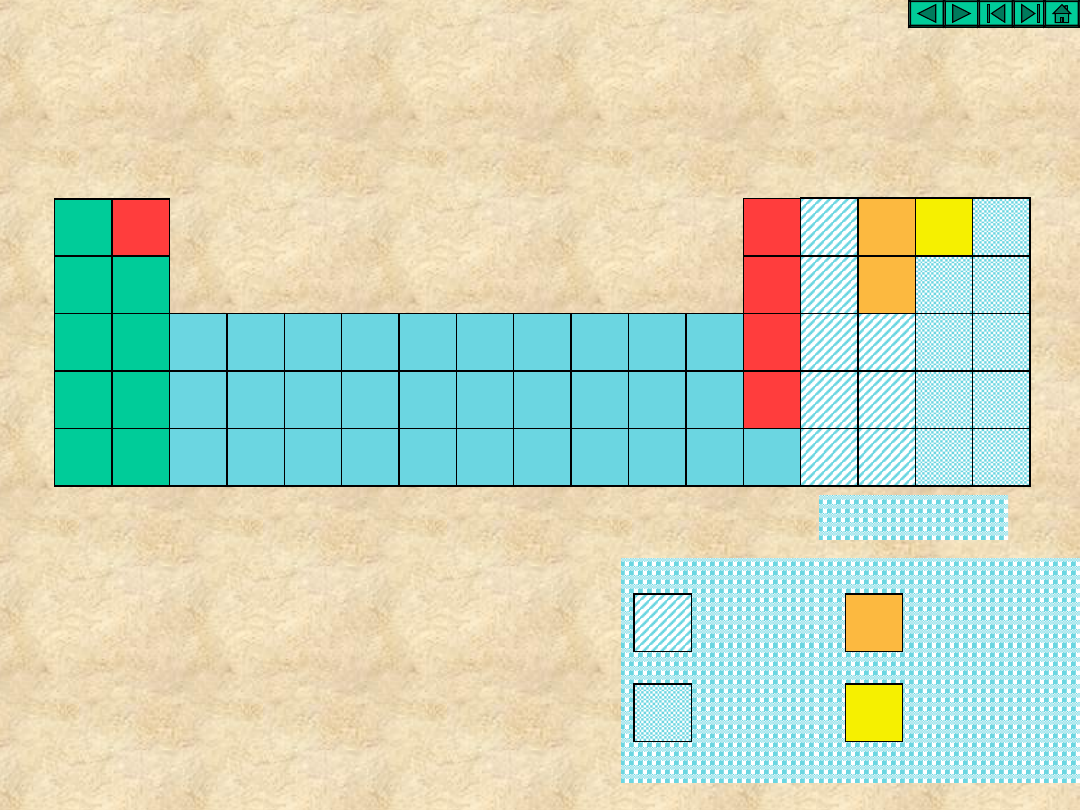
Klasyfikacja wodorków
MHMH
2
RH
4
RH
3
H
2
XHX
solne
obojętne
kwasowe
zasadowe
amfoteryczne
polimery z mostkami wodorowymi
metaliczne
molekularne
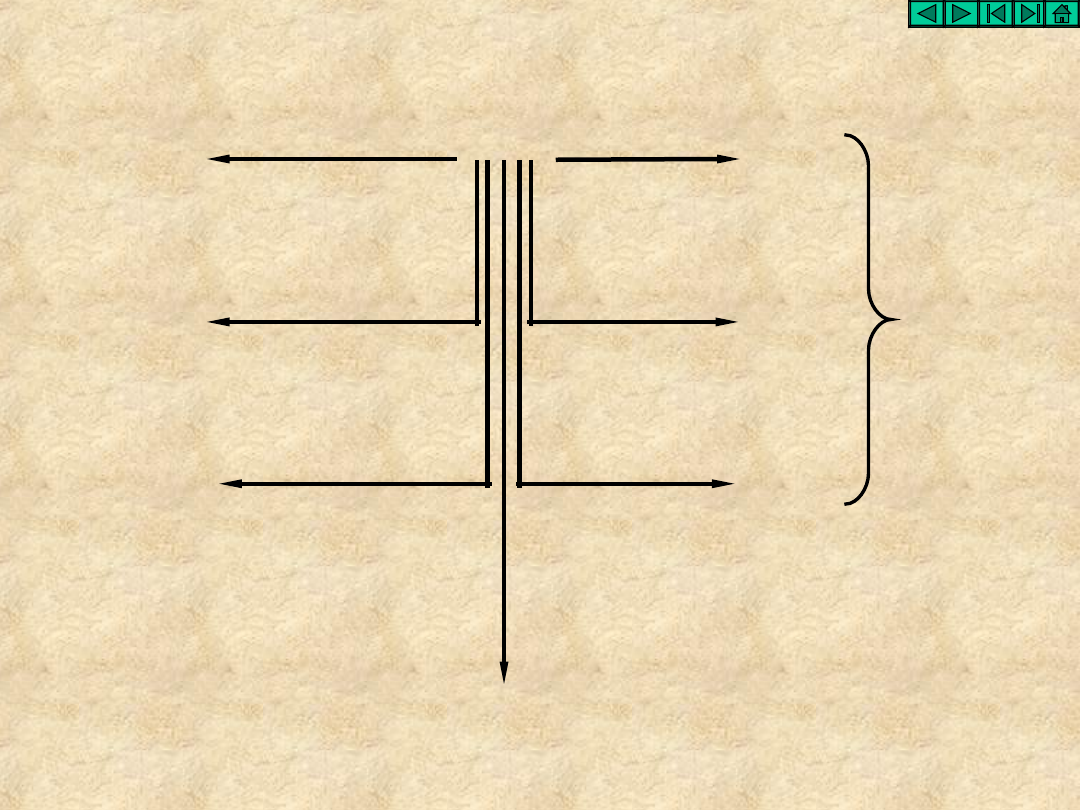
Właściwości chemiczne wodoru
H
2
fluorowce
tlenowce
azotowce
HX
H
2
X
H
3
X
litowce,
c. berylowce
tlenki
metali
nienasycone
węglowodory
(kat.)
tym
łatwiej
im
lżejszy
niemetal
wodorki
solne
metale
nasycone
węglowodory
CO, kat., wys. temperatura
CH
3
OH lub CH
4
, C
2
H
6
, benzyna syntetyczna
+ wiele innych substancji organicznych
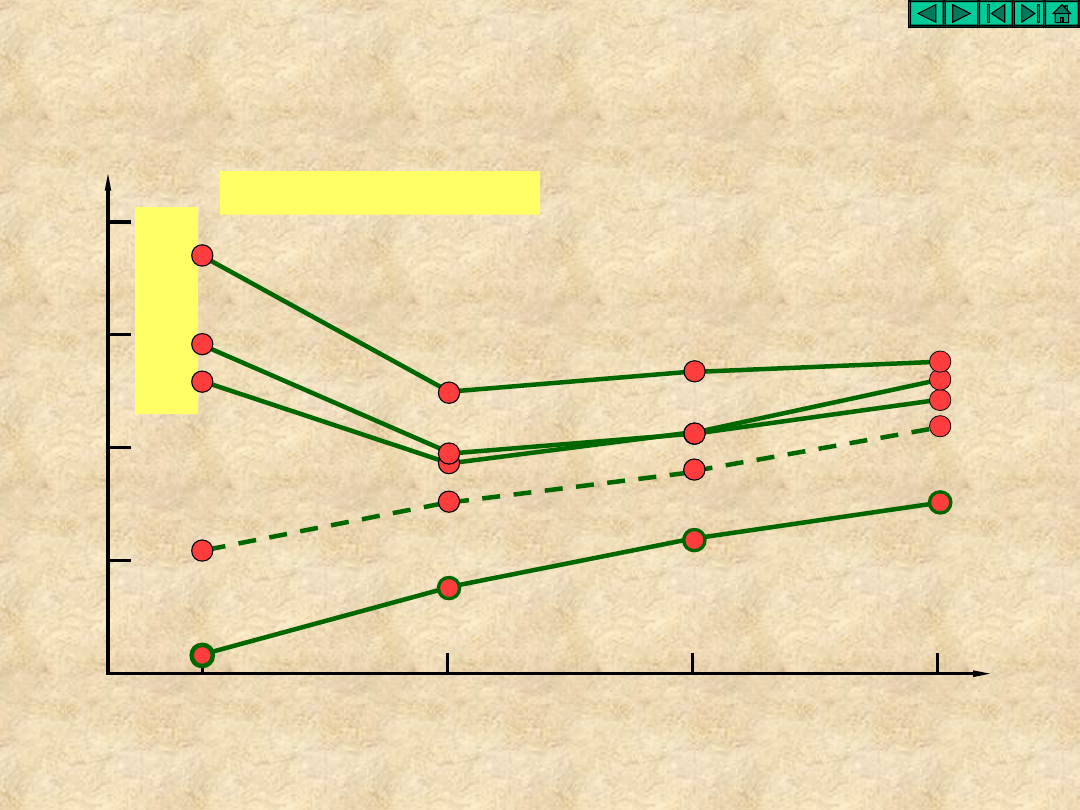
numer okresu
2
3
4
5
100
200
300
400
K
Ne
CH
4
NH
3
HF
H
2
O
H
2
S
H
2
Se
H
2
Te
HCl
AsH
3
SbH
3
PH
3
HBr
HI
SiH
4
GeH
4
SnH
4
Ar
Kr
Xe
Właściwości wodorków molekularnych
Temperatury
wrzenia
wiązania wodorowe

HELOWCE
Ar
Al
Rn
H
Ga
N
e
Na
Be
Kr
Xe
B
In
H
e
Li
Mg
K
Rb
Cs
Fr
Ca
Sr
Ba
Ra
Sc
Y
La-Lu
Ac-Lr
Ti
Zr
Hf
Rf
V
Nb
Ta
Db
Cr
Mo
W
Sg
Mn
Tc
Re
Bh
Fe
Ru
Os
Hs
Co
Rh
Ir
Mt
Ni
Pd
Pt
Cu
Ag
Au
Zn
Cd
Hg Tl
C N O
F
Si P
S Cl
Br
I
At
Ge
Sn
Pb
As
Sb
Bi Po
Se
Te
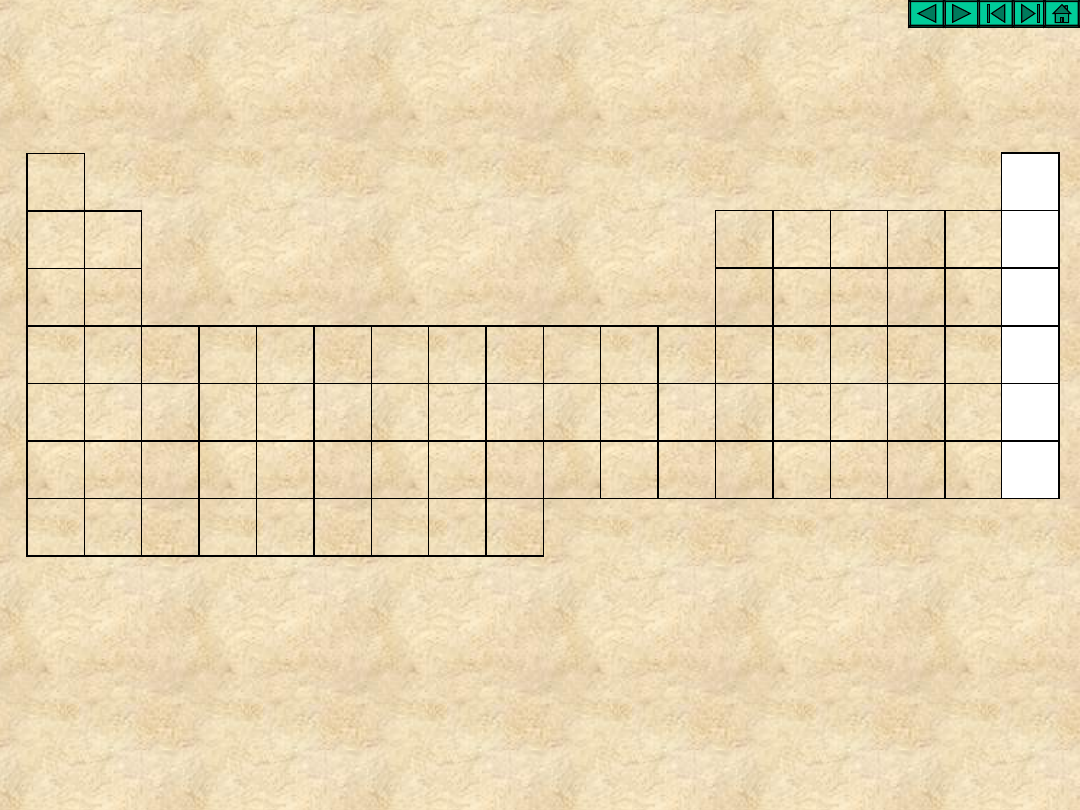
[poprzedni helowiec] ns
2
(n-2)f
14
(n-1)d
10
np
6
konfiguracja elektronowa:
Helowce w układzie okresowym
Właściwości fizyczne helowców
T
t
(K)
T
w
(K)
He
Ne
Ar
Kr
Xe
Rn
0,9(25A)
4,2
24
84 116 161 202
27
87 120 166 208
Q
top.
(kJ/mol)
Q
par.
(kJ/mol)
I (eV)
0,01380,3261,1091,5062,05 3,35
0,092 1,846,2769,66513,6817,99
24,6 21,6 15,8 14,0 12,1 10,8
wąski zakres
temperatur dla
istnienia cieczy
wyjątkowo
małe
największe w
okresie
w pełni symetryczny rozkład
elektronów walencyjnych
właściwoś
ci
fizyczne
konfigur
acja
0,9
0,9
0,9
0,9
0,9
0,9
0,9
0,9
0,9
4,2
4,2
4,2
4,2
4,2
4,2
4,2
4,2

gaz
ciecz II
ciecz I
ciało stałe
P
T
linia
Anomalne właściwości fizyczne helu

Związki helowców
stopień
utlenieni
a
wzór
wyglą
d
symet
ria
trwał
ość
bezbarwne
kryształy
bezbarwne
kryształy
bezbarwne
kryształy
ciecz i para żółte
bezbarwne
kryształy
kryształy żółte
ciecz bezbarwna
bezbarwne
kryształy
2
XeF
2
KrF
2
XeF
4
XeF
6
KrF
4
(RnF
4
?)
Cs
2
XeF
7
Cs
2
XeF
8
XeOF
4
XeO
3
4
6
liniow
a
kwadr
at
oktaedr
zniekształ
cony
piramida
kwadr.
piramida
trygon.
tt. 140
0
C
wybuch
owy
tt. 114
0
C
subl.300
0
C
tt.
47,7
0
C
subl.300
0
C
tt. -
28
0
C
trwałe do
400
0
C
wybucho
wy
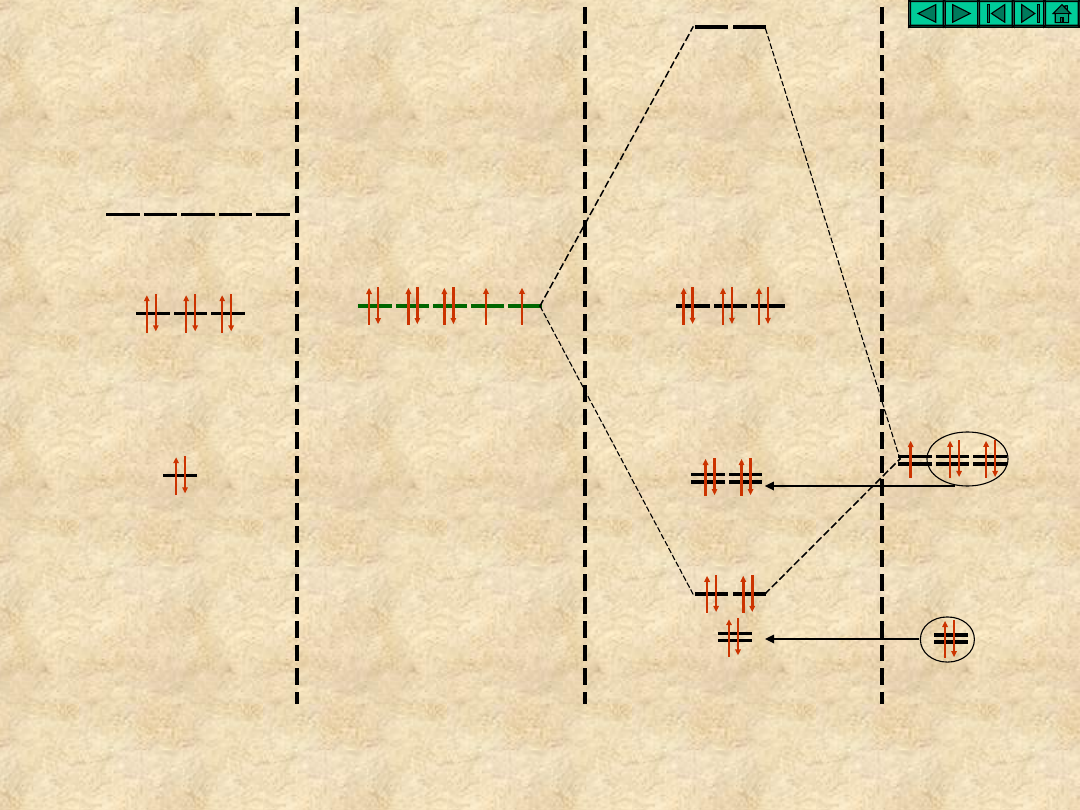
sp
3
d
Xe
stan
walencyjny
XeF
2
2F
5p
5s
5d
2s
2p
*
t
p
tp
t
1
t
2
t
3
t
1
t
2
t
3
t
4
t
5
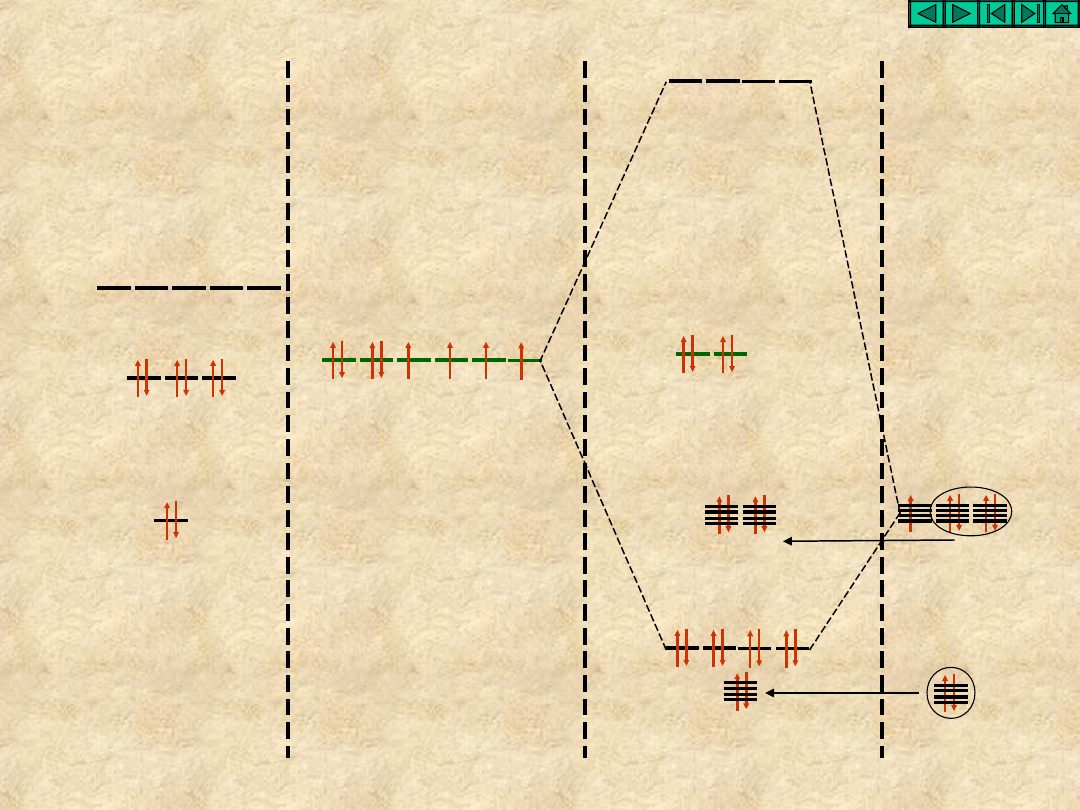
sp
3
d
2
stan
walencyjny
XeF
4
4F
Xe
5p
5s
5d
*
tp
tp
2p
2s
t
1
t
2
t
1
t
2
t
3
t
4
t
5
t
6
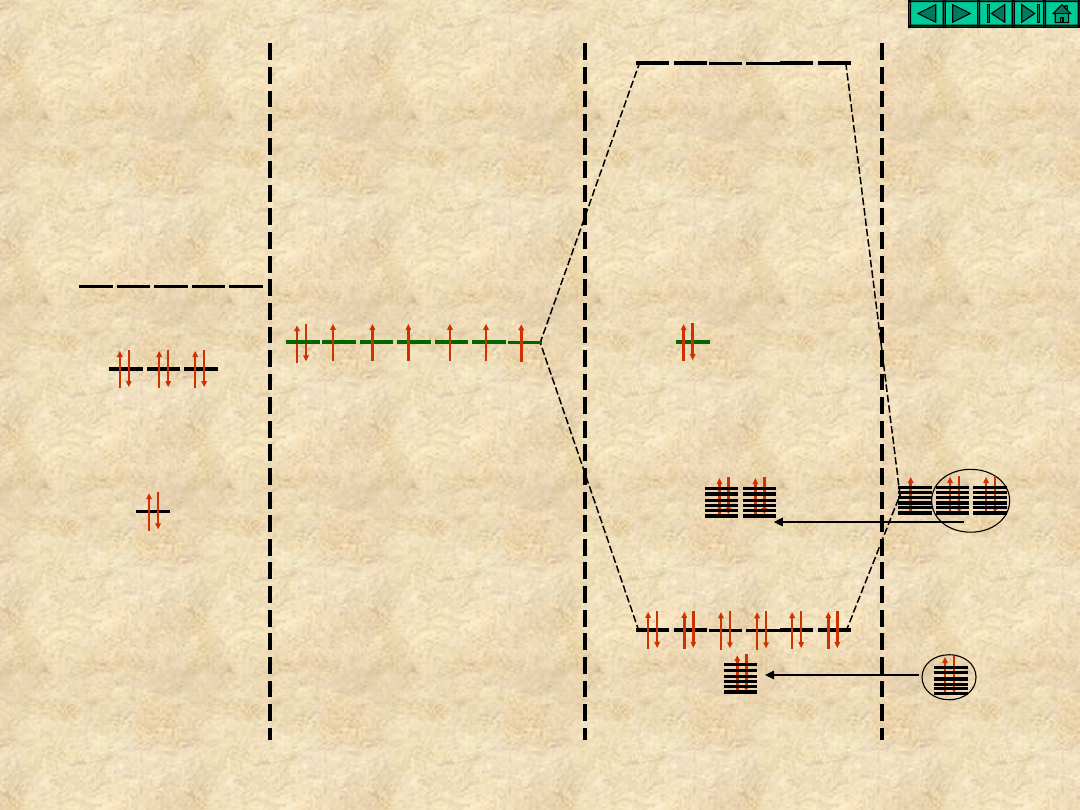
sp
3
d
3
stan
walencyjny
XeF
6
6F
Xe
5p
5s
5d
*
tp
tp
t
1
2p
2s
t
1
t
2
t
3
t
4
t
5
t
6
t
7
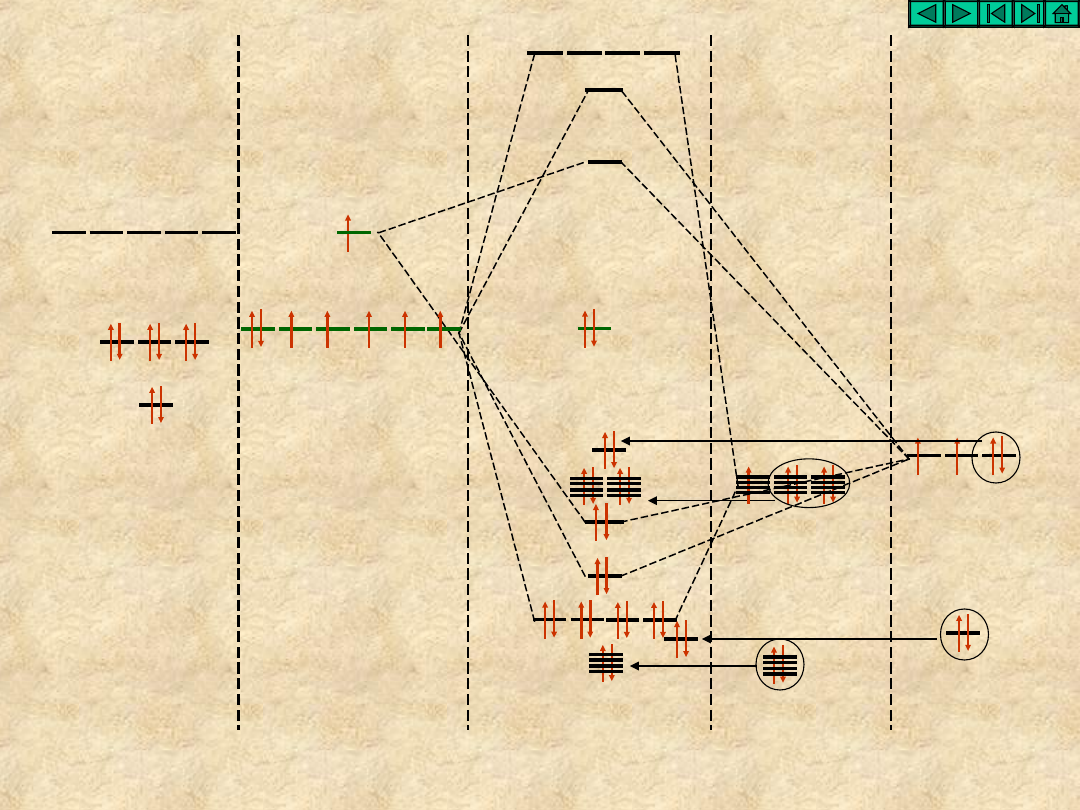
sp
3
d
2
Xe
stan
walencyjny
XeOF
4
4F
2p
2p
2s
tp
*
t
p
t
1
5s
5d
5p
2s
O
pd
*
pd
*
tp
tp
LH = 5 + 1 = 6
WP = ½(8 –2 –4) = 1
t
1
t
2
t
3
t
4
t
5
t
6
5d
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
Wyszukiwarka
Podobne podstrony:
Wodór technologia2
Helowce i ich związki
3 Helowce
12-helowceTECH, Materiały PG, Nieorgana
SPRAWOZDANIE wodór
troche teorii, HELOWCE
ZGAZOWAIE, WODÓR
geografia klimat, Atmosfera : azot (78%), tlen 21%, argon 0,9%, inne 0,1% (neon, hel, krypton, wodór
Wodór
2 wodór
04-Wodór TECH, Materiały PG, Nieorgana
wodór, 08. MEDYCYNA, 1.Analityka medyczna, I rok, Chemia ogólna i nieorganiczna, Inne
helowce
jak zmetalizowac wodor
więcej podobnych podstron