
Środki stosowane
w chorobach
infekcyjnych

WSTĘP

Definicje
• Środkami stosowanymi w schorzeniach
infekcyjnych są substancje chemiczne,
które mogą zabijać mikroorganizmy lub
hamować ich wzrost.
• Antybiotyki to rozpuszczalne związki, które
są otrzymywane z pewnych
mikroorganizmów i mają zdolność
hamowania rozwoju innych
mikroorganizmów.

Rodzaje schorzeń infekcyjnych i
ich leczenie
• Zakażenia bakteryjne są w większości przypadków łatwe w
leczeniu za pomocą wielu środków. Niektóre leki
przeciwbakteryjne działają bakteriostatycznie, tzn. hamują
wzrost wrażliwych na nie bakterii. Inne natomiast są
prawdziwie bakteriobójcze, tzn. zabijają wrażliwe szczepy
bakteryjne.
• Zakażenia grzybicze, w przeciwieństwie do bakteryjnych, są
na ogół oporne na chemioterapię, w związku z czym liczba
przydatnych środków przeciwgrzybiczych jest nieco
ograniczona. Zakażenia grzybicze występują często jako
nadkażenia, tzn. nakładające się na pierwotną infekcję
zakażenia wtórne, będące skutkiem zmian flory bakteryjnej
organizmu gospodarza (np. w wyniku terapii
przeciwbakteryjnej).

• Zakażenia prątkami w przeszłości często wymagały leczenia w
wyspecjalizowanych ośrodkach; obecnie nie jest to konieczne.
–
Gruźlica jest jednym z niewielu schorzeń wymagających leczenia
kombinacją leków przeciwbakteryjnych; zapobiega to rozwojowi
opornych szczepów zakażającego mikroorganizmu.
– Trąd jest schorzeniem, którego przebieg został w istotny sposób
zmieniony przez chemioterapię.
–
Zakażenia prątkami atypowymi (np. grupą Mycobacterium
avium) spotyka się, podobnie jak gruźlicę, u pacjentów z nabytym
zespołem upośledzenia odporności (AIDS).
• Robaczyce. Zakażeniu nimi ulega około miliarda ludzi rocznie, a
częstość zachorowań na nie wzrasta w miarę rozszerzania terenów
upraw ziemi i zwiększania się częstości podróżowania. Pojawienie się
nowych, wysoce selektywnych środków przeciwrobaczych
spowodowało wycofanie starszych leków, stosowanych dawniej w
parazytologii.

• Zakażenia pierwotniakowe, takie jak amebiazy i
trypanosomatozy, są leczone rozmaitymi środkami.
Metronidazol działa bezpośrednio rzęsistkobójczo, a także
jest stosowany w terapii kilku innych zakażeń
pierwotniakowych.
• Zakażenia wirusowe są trudne do leczenia, ponieważ
wirusy są pasożytami wewnątrzkomórkowymi,
korzystającymi w sposób czynny ze szlaków metabolicznych
gospodarza. Niewiele środków farmakologicznych jest
wystarczająco selektywnych. aby mogły unieszkodliwić
wirusa bez uszkodzenia komórki gospodarza.

Ogólne zasady terapii
przeciwinfekcyjnej
• Wybór właściwego środka przeciwinfekcyjnego
– Jeśli to jest możliwe, należy przed podjęciem terapii
przeciwinfekcyjnej zidentyfikować organizm będący przyczyną
zakażenia.
• Stan ogólny pacjenta może wymagać terapii empirycznej jeszcze przed określeniem
rodzaju organizmu wywołującego zakażenie.
•
W takiej sytuacji często stosuje się terapię „parasolową". Wybiera się środek o
szerokim zakresie działania lub kombinację środków, która jest skuteczna wobec
czynników chorobotwórczych będących najbardziej prawdopodobną przyczyną
zakażenia.
– Jeśli istnieje odpowiedni test laboratoryjny, należy określić wrażliwość
drobnoustrojów na działanie czynników przeciwinfekcyjnych.
– Do czynników mających wpływ na wybór środka przeciwinfekcyjnego
lub jego dawkowanie należą:
wiek pacjenta,
wydolność wątroby i wydolność nerek,
ewentualna ciąża,
umiejscowienie zakażenia.

• Drogi podawania leku
– Podanie doustne jest stosowane w łagodnych
zakażeniach.
• Jest szczególnie przydatne w lecznictwie otwartym.
• Zastosowany środek musi być wchłaniany z przewodu pokarmowego.
• Jeżeli pożywienie utrudnia wchłanianie, istotna jest odpowiednia
pora
po
dania leku.
– Podanie pozajelitowe stosuje się w leczeniu groźnych
zakażeń, szczególnie jeżeli leczenie wymaga dużych
stężeń leku w surowicy krwi.
– Podanie podtwardówkowe jest stosowane w
zakażeniach opon mózgowo-rdzeniowych, w sytuacji gdy
właściwy lek nie przenika przez barierę krew-mózg.

• Terapia wielolekowa środkami przeciwinfekcyjnymi
• Leczenie co najmniej dwoma (często trzema) środkami
przeciwinfekcyjnymi
ma
różne zadania:
zapewnia szeroki zakres działania (np. gdy zakażenie jest
spowodowane przez więcej mikroorganizmów niż jeden);
jest stosowane w leczeniu wstępnym (ślepym), gdy pacjent
jest w stanie ciężkim, a wyniki posiewów mikrobiologicznych są
jeszcze nie ustalone;
daje synergizm działania w sytuacji, gdy drobnoustroje nie są
skutecznie
eli
minowane w wyniku zastosowania jednego środka,
np. w enterokokowym zapaleniu wsierdzia stosuje się
jednocześnie penicylinę i aminoglikozyd, ponieważ skutek ich
łącznego działania jest większy niż suma efektów niezależnie
działających leków;
zapobiega niebezpieczeństwu powstania lekooporności
podczas leczenia gruźlicy.

• Niewłaściwie zastosowana
kombinacja leków może doprowadzić
do:
antagonizmu między jednocześnie
zastosowanymi środkami przeciw
drobnoustrojom,
wzrostu liczby lub nasilenia reakcji
niepożądanych,
wzrostu kosztów leczenia

ŚRODKI
STOSOWANE
W
LECZENIU
ZAKAŻEŃ
BAKTERYJNYCH

A.
Sulfonamidy
• Budowa
chemiczna
• Sulfonamidy są pochodnymi
amidu
kwasu sulfanilowego
(sulfanilamidu).
• Różne pochodne powstają przez podstawienie grupy amidowej
ugrupowania
sulfonamidowego.
• Mechanizm działania
• Sulfonamidy
uniemożliwiają
wbudowanie
kwasu
paraaminobenzoesowego (PABA) w kwas
foliowy,
który w formie
zredukowanej
jest
konieczny do biosyn
tezy
nukleotydów
purynowych jako przenośnik grupy jednowęglowej.
• Bakteriami wrażliwymi na sulfonamidy są
te,
które potrzebują
PABA, ponieważ nie
są
zdolne do bezpośredniego korzystania
z
egzogennego
kwasu foliowego.
• Komórki ludzkie korzystają
z
egzogennych zasobów kwasu
foliowego, brak PABA nie upośledza więc ich funkcji życiowych.

• Zakres działania
farmakologicznego
• Sulfonamidy działają na wiele bakterii Gram-dodatnich
z
Streptococcus
pyogenes
grupy A i
Streptococcus
pneumonice
włącznie.
• Wiele bakterii Gram-ujemnych jest opornych na
działanie sulfonamidów, lecz niektóre, takie jak
Haemophilus
influenzie,
Escherichia
coli
(drobnoustroje
naj
częściej
wywołujące
zakażenia
układu
moczowego),
Shigella, Yersinia enterocolitica
i
Proteus mirabilis często
są
wrażliwe
na
ich działanie.
• Do innych wrażliwych na sulfonamidy
mikroorganizmów należą: Bacillus anthracis,
Nocardia,
Actinomyces i
Chlamydia trachomatis, wywołujące
kolejno:
jag
licę, ziarniniaka wenerycznego i wtrętowe
zapalenie spojówek.

• Preparaty. Powszechnie stosowanymi sulfonamidami są
m.in.:
• Trimetoprim-sulfametoksazol (kotrimoksazol
[Biseptol, Groseptol])
Trimetoprim i sulfametoksazol hamują dwa różne etapy
metabolizmu
kwasu
foliowego.
Trimetoprim jest wysoce selektywnym inhibitorem
reduktazy kwasu
dihyd
rofoliowego niższych organizmów.
W skojarzeniu, leki te działają synergistycznie.
Skojarzenie to jest skuteczne w leczeniu zapalenia płuc
wywołanego
przez
Pneumocystis carinii, oportunistycznego
zakażenia występującego u pacjentów z AIDS.
• Sulfisoksazol (sulfafurazol [Amidoxal])
• Sulfadiazyna
Obecnie w leczeniu zakażeń układu moczowego jest rzadziej
stosowana.
Jest skuteczna w leczeniu nokardiozy.
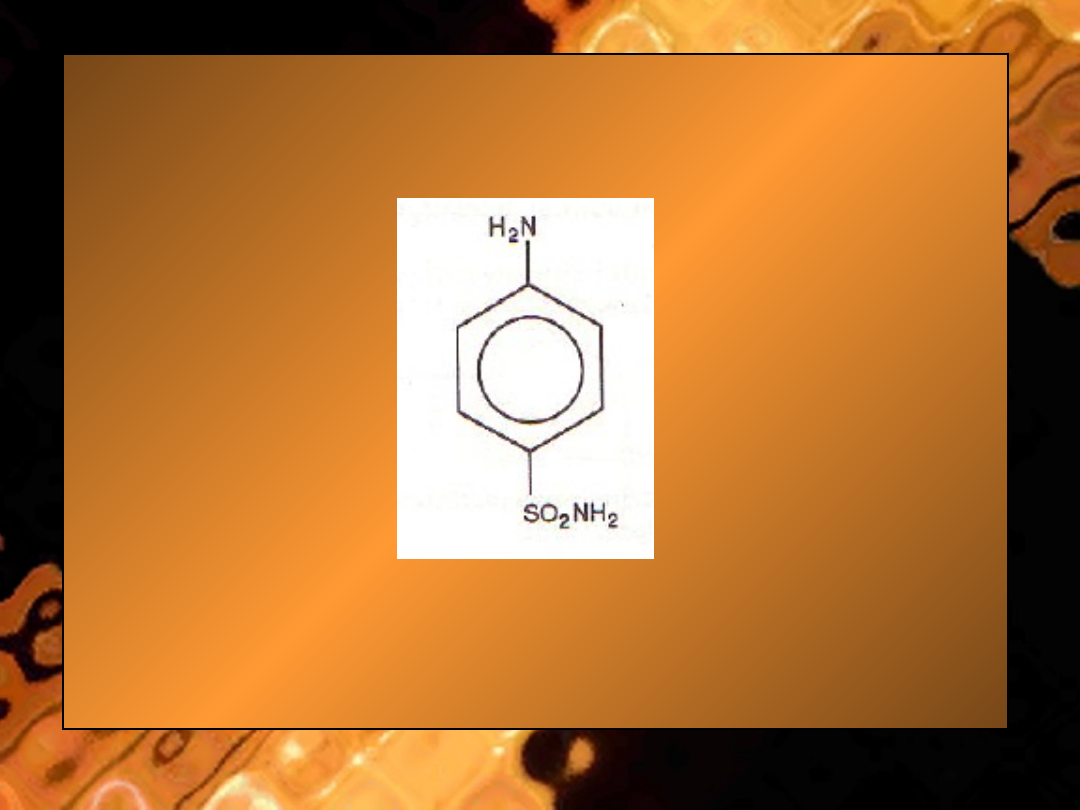
• Ryc.
Sulfanilamid

B. Antybiotyki ß-laktamowe
• Wiadomości ogólne
– Budowa chemiczna
Pierścień ß-laktamowy jest czteroczłonowym
pierścieniem, w którym wiąząnie amidowe łączy grupę
karbonylową i azot.
Obecność pierścienia
ß
-laktamowego jest cechą
charakterystyczną budowy antybiotyków
ß
-
laktamowych.
– Mechanizm działania. Antybiotyki
ß
-laktamowe
działają bakteriobójczo.
Antybiotyki te hamują aktywność podstawowych
enzymów syntezy ściany komórkowej bakterii.
Wydaje się, że aktywują również jeden lub kilka
enzymów autolitycznych ściany komórkowej,
doprowadzając do lizy komórki bakteryjnej.

• Oporność bakterii
ß
-laktamazy, enzymy wytwarzane przez dużą grupę
bakterii, inaktywują antybiotyk, hydrolizując
pierścień
ß
-laktamowy. Penicylinaza i
cefalosporynaza są
ß
-laktamazami o dużej
swoistości wobec substratu.
Przez nabycie plazmidów lub czynników R
(oporności), będących nośnikami kodu genetycznego
dla
ß
-laktamazy, początkowo wrażliwe szczepy
bakteryjne stają się oporne na konkretny antybiotyk.
Penicyliny i inne antybiotyki
ß
-laktamowe różnią się
wrażliwością na
ß
-laktamazy.
Inhibitory
ß
-laktamaz są substancjami mogącymi
nieodwracalnie połączyć się z
ß
-laktamazą
bakteryjną i spowodować jej inaktywację.

Klasyfikacja
• Do grupy antybiotyków
ß
-
1aktamowych zaliczamy:
penicyliny,
cefalosporyny,
imipenem,
aztreonam.

• 1. Penicyliny
•
Budowa chemiczna
Struktura penicylin składa się z pierścienia tiazolidynowego połączonego z
pierścieniem -laktamowym, do którego jest dołączony łańcuch boczny.
Wszystkie penicyliny są pochodnymi kwasu 6-amino-penicylanowego.
Poszczególne penicyliny różnią się budową łańcucha bocznego.
•
Mechanizm działania
Penicyliny hamują syntezę bakteryjnej ściany komórkowej i są zaliczane do
środków bakteriobójczych.
Wiążą i inaktywują transpeptydazę, która w normalnych warunkach jest
odpowiedzialna za powstanie wiązań krzyżowych w liniowych łańcuchach
glikopeptydowych ściany komórki bakteryjnej. Utrata sztywności ściany
komórkowej przy normalnym wysokim wewnątrzkomórkowym ciśnieniu
osmotycznym jest przyczyną lizy bakteryjnej błony komórkowej.
•
Oporność bakteryjna
Penicylinaza jest -laktamazą wytwarzaną przez wiele bakterii. Może ona
hydrolizować pierścień -laktamowy penicylin i przekształcać go w kwas
penicyloilowy, substancję pozbawioną aktywności przeciwbakteryjnej.
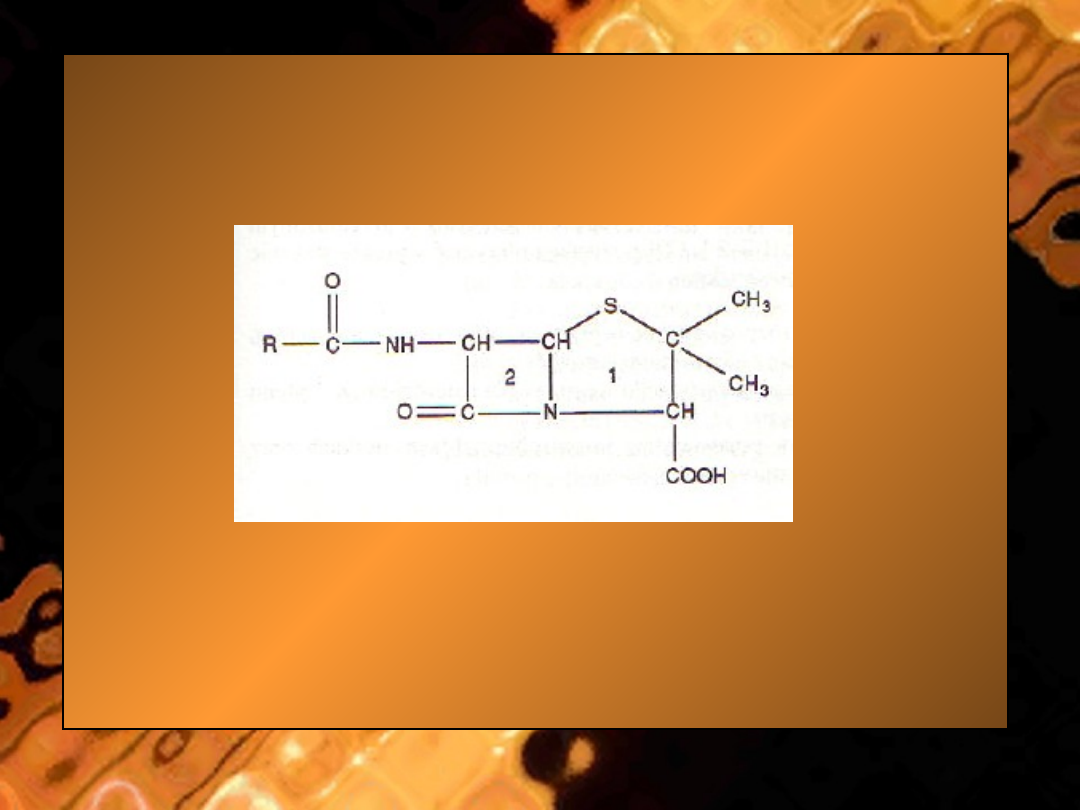
• Ryc. 12-2. Budowa penicylin: R - łańcuch boczny; 1
- pierścień tiazolidynowy; 2 - pierścień ,3- -
laktamowy

•Tabela. Klasyfikacja penicylin

Do mikroorganizmów zdolnych do
wytwarzania penicylinazy zaliczamy:
Staphylococcus aureus,
Bacillus species,
Bacterioides species,
E. coli,
Proteus species,
Pseudomonas aeruginosa,
Mycobacterium tuberculosis.

• Penicyliny G i V
– Wchłanianie
• Podanie doustne
Z powodu inaktywacji penicyliny G przez sok żołądkowy
tylko
30% dawki doustnej jest
wchłanianych
z
dwunastnicy.
Penicylina V jest bardziej stabilna
w
środowisku kwaśnym; równoważna dawka
doustna osiąga stężenie w surowicy
2-5
razy większe niż osiągane w razie
zastosowania penicyliny G.
Penicyliny G
i
V powinny
być
podawane -
z
powodu
wpływu
pożywienia na wchłanianie
- przynajmniej godzinę przed
posił
kiem i 2-3 godziny po nim.
Maksymalne stężenie w surowicy występuje 30-60 minut po
poda
niu.
• Podanie podskórne lub domięśniowe
Po wstrzyknięciu
krystalicznej
penicyliny G maksymalne
stężenie
w
surowicy występuje
po
15
minutach, następnie szybko opada.
Jednoczesne podanie probenecydu wydłuża eliminację
penicylin z organizmu, ponieważ
probenecyd blokuje transport penicylin
w cewkach bliższych nerek. Preparaty
penicylino
przedłużonym
działaniu pozwalają utrzymać wysokie
stężenie
penicylin
w
surowicy krwi.
• Wydalanie
60-90% domięśniowej dawki penicyliny G jest wydalanych w ciągu godziny.
Drogą nerkową jest eliminowanych aż do 99% leku; około 90% przez
sekrecję
kanalikową i 10% przez filtrację kłębkową.

• Działania farmakologiczne i
zastosowanie kliniczne.
Poszczególne typy penicylin różnią się
zakresem działania i stopniem
skuteczności wobec różnych szczepów
bakterii. W zasadzie, jeżeli tylko jest to
możliwe, powinna być określana
wrażliwość mikrobiologiczna.

•
Zakażenia ziarniakami Gram-dodatnimi (paciorkowcami, gronkowcami).
Penicyliny G i V są bardzo aktywne wobec wielu szczepów ziarniaków Gram-dodatnich.
–
Zakażenia wywołane przez S. pneumonice (zakażenia pneumokokowe)
Penicyliny G lub V są lekami pierwszego rzutu w leczeniu pneumokokowego zapalenia płuc.
W pneumokokowym zapaleniu opon mózgowo-rdzeniowych penicylina G jest podawana
zazwyczaj dożylnie. Czasami stosuje się podanie podtwardówkowe, lecz komplikacją tego
rodzaju terapii mogą być zapalenie pajęczynówki i encefalopatia.
Do innych zakażeń paciorkowcowych, względem których penicylina G jest lekiem
pierwszego rzutu, należą: ropne zapalenie stawów, zapalenie wyrostka sutkowego, zapalenie
wsierdzia i zapalenie szpiku kostnego.
–
Inne zakażenia paciorkowcowe, głównie związane z S. pyogenes grupy A, które są wrażliwe na
działanie penicylin G i V
Paciorkowcowe zapalenie gardła i szkarlatyna reagują na doustne leczenie penicyliną V
Poprawa kliniczna następuje szybko, w ciągu 2-4 dni.
Zapalenie ucha środkowego wywołane przez S. pyogenes także poddaje się leczeniu po
zastosowaniu penicyliny V
Do innych zakażeń paciorkowcowych wrażliwych na leczenie penicyliną G należą: zapalenie
wsierdzia, zapalenie stawów i opon mózgowo-rdzeniowych.
–
Zakażenia gronkowcowe wrażliwe na penicylinę G powinny być nią leczone, ponieważ jest ona
bardziej aktywna niż penicyliny oporne na penicylinazę.
Około 20% szczepów S. aureus jest jednak opornych na penicylinę, ponieważ produkują
penicylinazę.
W tego typu zakażeniach bardzo skuteczne są penicyliny penicylinazooporne: oksacylina,
kloksacylina, metycylina i nafcylina.

• Zakażenia
ziarniakami
Gram-ujemnymi
(meningokokowe, gonokokowe) dobrze reagują na
leczenie penicyliną G i V.
W zakażeniach gonokokowych ceftriakson jest
uważany za lek pierwszego rzutu, ponieważ szczepy
bakteryjne stają się coraz bardziej oporne na leczenie
penicyliną G.
W leczeniu zakażeń szczepami penicylinoopornymi
stosuje się penicylinę prokainową, ampicylinę lub
amoksacylinę, zazwyczaj wraz z probenecydem.
– Kiła.
Leczenie penicyliną G jest najbardziej
skuteczne we wszystkich stadiach choroby, ponieważ
Treponema pallidum jest bardzo wrażliwe na ten
lek.

• Zakażenia
innymi
drobnoustrojami
wrażliwymi
na
penicylinę G
Penicylina G jest aktywna wobec wielu beztlenowców jamy ustnej. Z tego
powodu w dalszym ciągu stosuje się ją w leczeniu zakażeń tkanek miękkich
jamy ustnej, zębów, płuc, spowodowanych drobnoustrojami będącymi typową
florą tej okolicy.
Penicylina G jest także lekiem z wyboru w leczeniu zgorzeli gazowej
(zazwyczaj wywołanej przez Clostridium). Jednakże zakażenia podprzeponowe
bakteriami beztlenowymi (np. wywołane przez Bacteroides fragilis) są na ogół
oporne na penicyliny, z wyjątkiem tzw. penicylin antypseudomonas.
Większość szczepów Corynebacterium diphtheriae jest wrażliwa na penicylinę
G, stosowaną w leczeniu zarówno ostrego stanu, jak i nosicielstwa błonicy.
Penicylina G jest także lekiem z wyboru w leczeniu:
• wąglika (większość szczepów B. anthracis jest wrażliwa na penicylinę),
• promienicy,
• listeriozy.

• Penicyliny o szerokim zakresie działania - ampicylina,
amoksycylina i ich różne pochodne (np. bakampicylina,
piwampicylina, hetacylina) - są aktywne wobec Gram-
dodatnich drobnoustrojów niektórych szczepów E. coli, H.
influenzae, Salmonella i Shigella oraz niektórych gatunków
Proteus. Jeśli szczepy bakteryjne są wrażliwe na ampicylinę
i amoksycylinę, to antybiotyki te są stosowane w leczeniu:
niektórych form rzeżączki,
zapalenia zatok i ucha środkowego wywołanych przez
H. influenzae. pneumokoki lub S. pyogenes,
zakażeń układu moczowego wywołanych przez E. coli
lub P. mirabilis,
zapaleń opon mózgowo-rdzeniowych wywołanych
przez meningokoki. H. influenzae lub paciorkowce.

•
Penicyliny „antypseudomonas" są stosowane głównie w leczeniu
poważnych zakażeń (bakteriemii, pneumonii, zakażeń pooparzeniowych)
wywołanych przez drobnoustroje Gram-ujemne, szczególnie P aeruginosa,
Proteus indolododatni i Enterobacter
–
Karbenicylina i tikarcylina mają zakres działania podobny do ampicyliny, a
ponadto są aktywne wobec indolododatnich gatunków Proteus i Pseudomonas.
Tikarcylina jest wobec P. aeruginosa 2-4 razy bardziej aktywna niż karbenicylina
i
jest zalecana w leczeniu groźnych zakażeń wywołanych przez Pseudomonas.
Pochodna karbenicyliny - indanyl karbenicyliny (karyndacylina [Geopen]) -
gromadzi się szybko w moczu, stanowi więc skuteczną terapię zakażeń układu
moczowego spowodowanych przez indolododatnie gatunki Proteus i Pseudomonas.
–
Azlocylina
[Securopen],
mezlocylina
[Baypen]
i
piperacylina
[Piperacillinum, Pipril]
są
wspólnie określane jako ureidopenicyliny.
Azlocylina i piperacylina są dziesięciokrotnie aktywniejsze wobec Pseudomonas niż
karbenicylina.
Mezlocylina i piperacylina przewyższają karbenicylinę aktywnością wobec pałeczek
Klebsiella.
– Penicyliny z grupy „antypseudomonas" często
są
stosowane wraz z
gentamycyną, amikacyną lub tobramycyną w stanach zagrożenia życia
będących skutkiem zakażenia Pseudomonas.

• Połączenia
penicylin z inhibitorami
ß
-laktamaz
–
Kwas klawulanowy,
mający budowę podobną do penicylin, jest inhibitorem
ß
-laktamaz.
•
Kwas klawulanowy poszerza zakres przeciwbakteryjnego działania antybiotyków
ß
-
laktamowych
przez nieodwracalne wiązanie, a tym samym unieczynnianie wielu bakteryjnych
ß
-laktamaz.
Rozszerza on
aktywność amoksycyliny wobec
szczepów
wytwarzających
ß
-laktamazy: H. influenzae;
E
coli;
odmian Proteus; Klebsiella pneumoniae; Staphylococcus epidermidis
i
Staphylococcus
saprophyticus, a także S. aureus
i
Branhamella catarrhalis. Roszerza także aktywność
in
vitro
tikarcyliny na ogromną, różnorodną grupę drobnoustrojów Gram-ujemnych, Gram-dodatnich i
beztlenowców.
•
Połączenie amoksycyliny
i
kwasu
klawulanowego
[Augmentin]
jest
stosowane
w
terapii zakażeń
spowodowanych przez następujące szczepy wytwarzające P-Iaktamazy: H.
influenzae,
B. catarrhalis,
S. aureus, E. coli, Klebsiella
i
Enterobacter.
•
Kombinacja
tikarcyliny
i kwasu
klawulanowego jest
stosowana
w te
rapii zakażeń wywołanych
przez szczepy wytwarzające P-Iaktamazy: Klebsiella, E. coli, S. aureus, Pseudomonas, H. influenzae,
Citrobacter, Enterobacter doicie
i
Serratia marcescens.
–
Sulbaktam
jest
sulfonem
kwasu
penicylinowego
o
ograniczonej
aktywności
przeciwbakteryjnej.
Jego główne
działanie polega na inaktywacji bakteryjnej
ß
-Iaktamazy,
dzięki czemu zwiększa się zakres działania przeciwbakteryjnego ampicyliny.
•
Rozszerza on aktywność
ampicyliny
in vitro na następujące szczepy wytwarzające P-Iaktamazy: H.
influenzae, E. coli, Proteus species, K. pneumoniae, S.
aureus,
S. epidermidis, B. catarrhalis,
Enterobacter
aerogenes,
Acinetobacter calcoaceticus,
Neisseria
oraz na
wiele
beztlenowców z B.
fragilis
włącznie.
• Połączenie
ampicyliny i sulbaktamu
jest skuteczne
w
leczeniu zakażeń jamy brzusznej
i
zakażeń
ginekologicznych.

• Preparaty
i ich
podawanie
– Formy
rozpuszczalne
penicylin G
i
V
Penicylina
G
(benzylopenicylina)
w
postaci soli sodowej
i
potasowej
jest
stosowana domięśniowo
i
dożylnie.
Penicylina
V (penicylina fenoksymetylowa) występuje
w
formie rozpusz
czalnej,
opornej
na działanie
kwasów. Stosuje
się
ją
doustnie.
– Formy
o przedłużonym działaniu
są
nierozpuszczalnymi
solami, które opóźniają wchłanianie penicylin
z
miejsca
podania, zapewniając 12-14 godzinny czas ich działania. Do
preparatów tych, stosowanych tylko domięśniowo, należą:
penicylina prokainowa,
penicylina benzatynowa [Debecylina] lek ten jest słabo
rozpuszczalny. jego skuteczne stężenie
we
krwi utrzymuje się
często
przez tydzień).

– Penicyliny oporne na penicylinazę
• Metycylina
Lek ten ma jedną dwudziestą aktywności penicyliny G.
Z powodu złego wchłaniania
z
przewodu pokarmowego nie jest
podawana doustnie.
• Oksacylina
Lek ten jest stabilny w środowisku kwaśnym, dlatego może być
podawany zarówno doustnie, jak
i
dożylnie lub domięśniowo.
W dużym stopniu
wiąże się z
białkami krwi.
Jest do
8 razy
bardziej aktywna niż metycylina.
• Kloksacylina [Syntarpen]
ma właściwości farmakologiczne i farmakokinetyczne podobne
do oksacyliny.
• Nafcylina
może
być
podawana doustnie, dożylnie
i
domięśniowo.
• Dikloksacylina
jest wysoce skuteczna po podaniu doustnym; jest bardzo
oporna na penicylinazę i
na
hydrolizę w środowisku kwaśnym.

– Penicyliny o szerokim zakresie działania
Ampicylina jest podawana doustnie, dożylnie i domięśniowo. Jest
stabil
na
w
środowisku kwaśnym, ale unieczynniana przez penicylinazę.
Amoksycylina jest podawana doustnie.
W surowicy krwi
osiąga wyższe
stężenia niż ampicylina.
Uważa się, że powikłania biegunkowe wywołuje rzadziej
niż
ampicylina.
– Penicyliny „antypseudomonas"
Azlocylinę podaje się dożylnie.
Karbenicylina, tikarcylina, mezlocylina i piperacylina
są
podawane
dożylnie lub domięśniowo.
Indanyl karbenicyliny (karyndacylina) jest podawany doustnie; jest
sta
bilny w środowisku kwaśnym.
– Połączenia penicylin z inhibitorami -laktamaz
Amoksycylinę z kwasem klawulanowym [Augmentin] podaje
się
doustnie.
Tikarcylina z kwasem klawulanowym [Timentin] jest podawana
dożylnie.
Ampicylina z sulbaktamem [Unasyn] jest podawana dożylnie i
do
mięśniowo.

• Działania niepożądane
• Reakcje nadwrażliwości na penicyliny występują u
5-20%
chorych otrzymujących ten lek.
– Wszystkie formy penicylin mogą być
przyczyną
reakcji
nad
wrażliwości. Alergia może się pojawić bez uprzedniego
leczniczego podania penicyliny.
• Reakcje nawracające i nadwrażliwość krzyżowa
– Występowanie u
chorego
reakcji uczuleniowej na pewien rodzaj
penicyliny
stwarza
duże niebezpieczeństwo wystąpienia reakcji
uczuleniowej po zastosowaniu zarówno tej samej penicyliny, jak i
jakiejkolwiek innej.
• Inne objawy niepożądane
–
Działanie drażniące na przewód pokarmowy występuje najczęściej
podczas podawania doustnych preparatów penicylin; przykładem jest
biegunka związana z podawaniem ampicyliny.
– Działanie nefrotoksyczne występuje bardzo rzadko; pojawia
się
zazwyczaj tylko u chorych
z
upośledzoną czynnością nerek.
– Nadkażenia wynikające
z
zaburzeń równowagi flory jelitowej

• 3. Cefalosporyny
– Budowa chemiczna
Cefalosporyny
są
pochodnymi kwasu 7-aminocefalosporynowe
go,
mającymi
budowę zbliżoną do budowy penicylin.
Mają 6-członowy pierścień zawierający siarkę, przyłączony do pierścienia
ß
-laktamowego.
Są stosunkowo stabilne w środowisku słabych kwasów.
–
Klasyfikacja.
Cefalosporyny dzieli
się
najczęściej na „generacje", co
w
przybliżeniu określa
również
chronologię
ich
powstawania
oraz
zakres
ich
działania
przeciwbakteryjnego.
– Mechanizm działania.
Cefalosporyny, podobnie jak penicyliny, hamują rozwój
ściany
komórkowej
bakterii i są uznawane za bakteriobójcze.
– Oporność
bakterii
Cefalosporyny
są
wysoce oporne na penicylinazę.
Niektóre bakterie wytwarzają laktamazç nazywaną cefalosporynaza. Działa ona
na jądro cefalosporyn i niszczy ich aktywność
przeciwbakteryjne.
Jednakże wiele
cefalosporyn jest odpornych na działanie tych
enzymów.

•Tabela. Klasyfikacja
cefalosporyn
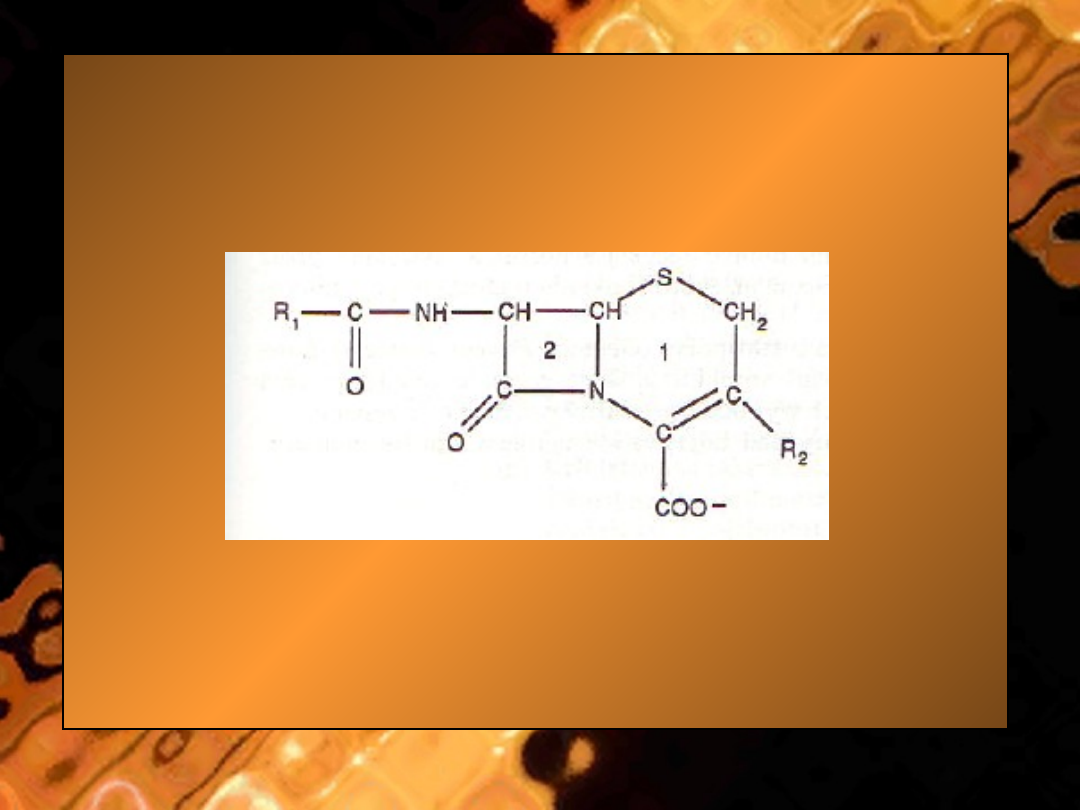
• Ryc. Budowa cefalosporyn: 1 -
pierścień
zawierający siarkę; 2
-
pierścień

•
Działanie farmakologiczne. Wszystkie cefalosporyny są aktywne wobec
większości
ziarniaków
Gram-dodatnich,
m.in.
gronkowców
wytwarzających penicylinazę, i wielu pałeczek Gram-ujemnych.
Cefalosporyny na ogół nie są aktywu: wobec enterokoków.
•
Zastosowanie kliniczne
Cefalosporynami
leczy
się
skutecznie
schorzenia
wywołane
przez
penicilinowraż1iwy i penicylinooporny S. aureus, takie jak zakażenia skóry,
zapalenie szpiku kostnego, zapalenie wsierdzia.
W zakażeniach K. pneumonice cefalosporyny są stosowane jako leki wyboru.
Leki te są stosowane z powodzeniem w leczeniu paciorkowcowych zapalań
płuc i zakażeń wywołanych przez S. pyogenes.
Niektóre stosowane pozajelitowo cefalosporyny są skuteczne w terapii
schorzeń gonokokowych opornych na leczenie innymi środkami.
Na terapię cefalosporynami dobrze reagują schorzenia wywołane przez różne
bakterie Gram-ujemne, m.in. choroby układu oddechowego i moczowego.
Poszerzony zakres działania cefalosporyn obejmuje Proteus, B. fragilis,
Emerobacter, a także Pseudomonas. Środki te są skuteczne w leczeniu
zapalenia opon mózgowo-rdzeniowych wywołanego wrażliwymi na nie
szczepami.
• Profilaktyczna terapia cefalosporynami odgrywa ważną rolę w
redukowaniu liczby zakażeń okołooperacyjnych.

• Cefalosporyny pierwszej generacji
nie są aktywne wobec
indolododatnich gatunków Proteus, Pseudomonas, Serratia, Enterobacter i B. fragilis.
– Cefalotyna [Keflin]
Nie jest dobrze wchłaniana z przewodu pokarmowego.
Podaje się ją zazwyczaj dożylnie. Wstrzyknięcia domięśniowe są bolesne.
– Cefazolina [Kefzol, Cefamezin]
Nie wchłania się dobrze z przewodu pokarmowego. Jest podawana dożylnie lub
domięśniowo.
Około 80% leku wiąże się odwracalnie z białkami surowicy, co w znaczny sposób przedłuża
okres półtrwania.
– Cefaleksyna [Keflex, Oracefi]
Jest dobrze wchłaniana z przewodu pokarmowego, ponieważ jest stabilna w środowisku
kwaśnym.
Jest dostępna w sprzedaży w postaci doustnych kapsułek, zawiesin i kropli pediatrycznych.
– Cefradyna [Sefril]
• Posiada właściwości podobne do cefaleksyny. Może być podawana doustnie, dożylnie lub
domięśniowo
.
– Cefadroksyl [Duracef]
• Podawany doustnie odpowiednikiem cefaleksyny. Stosuje się go w leczeniu zakażeń układu
moczowego.

• Cefalosporyny drugiej generacji
– Cefamandol [Mandol]
Jest to cefalosporyna o poszerzonym zakresie działania, aktywna wobec indolododatnich gatunków
Proteus i wytwarzającego -laktamazy H. influenzae.
Podaje się go wyłącznie pozajelitowo.
– Cefoksytyna [Mefoxin]
Jest to cefalosporyna o poszerzonym zakresie działania, aktywna wobec indolododatnich gatunków
Proteus i B. fragilis. Jest słabiej aktywna wobec zarazków Gram-dodatnich. Podaje się ją pozajelitowo.
–
Cefaklor [Alfacet, Ceclor]
•
Posiada działanie podobne do działania cefaleksyny, a ponadto jest skuteczny wobec H. influenzae
wytwarzającego -laktamazy. Podaje się go doustnie.
– Cefonicyd
Cefonicyd ma zakres działania podobny do zakresu działania cefamandolu.
Jego przedłużony okres półtrwania pozwala na stosowanie go raz na dobę. Jest podawany pozajelitowo.
–
Cefuroksym [Zinnat, Zinacef, Cinnat, Biofuroksym]
•
Jest cefalosporyną o szerszym zakresie działania, skuteczną w leczeniu groźnych zakażeń wywołanych
przez H. influenzae, a szczególnie układu oddechowego i zapaleń ucha środkowego. Jest dostępny w
preparatach do podawania pozajelitowego i doustnego.
– Ceforanid
• Posiada budowę podobną do cefamandolu, lecz cechuje go mniejsza aktywność wobec H. influenzae.
Jest podawany pozajelitowo.

Cefalosporyny trzeciej generacji
– Cefotaksym [Tarcefoksym, Claforan], ceftizoksym,
ceftriakson
[Longa
ceph, Rocephin]
Te stosunkowo nowe, półsyntetyczne cefalosporyny mają
większą
siłę
działania niż leki macierzyste.
Są podawane pozajelitowo.
Z powodu długiego okresu półtrwania ceftriakson może być
poda
wany raz na dobę. Jest on szczególnie przydatny w leczeniu
za
każeń
wywołanych
szczepami
Neisseria
gonorrhoeae
wytwarzający
mi penicylinazę.
– Cefoperazon [Cefobid] i ceftazydym [Fortum, Kefadim, Biofort]
Cechuje
większa niż inne cefalosporyny trzeciej generacji
aktywność
wobec
P. aeruginosa, lecz mniejsza skuteczność
wobec innych mikroorganizmów.
– Cefiksym
jest skuteczny wobec szczepów H. influenzae
wytwarzających
-
laktamazę. Może być podawany doustnie raz na dobę.

• Działania niepożądane
– Reakcje uczuleniowe występują mniej więcej u 5%
chorych leczonych cefalosporynami.
– Uszkodzenie nerek może wystąpić, chociaż rzadko, w
następstwie podawania normalnych dawek
cefalosporyn.
– Po podaniu pozajelitowym może pojawić się tkankowe,
miejscowe działanie drażniące. Podanie dożylne może
być przyczyną zapalenia ży1.
– Jako następstwa leczenia cefalosporynami mogą
pojawić się nadkażenia spowodowane bakteriami
Gram-ujemnymi lub drożdżami.

• 4. Imipenem
jest antybiotykiem -laktamowym, pochodną tienamycyny. Mechanizm jego
działania, podobnie jak innych antybiotyków -laktamowych, polega na zaburzaniu syntezy ściany komórki
bakteryjnej. Jest lekiem bakteriobójczym.
–
Farmakokinetyka
Imipenem [Conet] jest podawany wraz z cylastatyną [Tienam], inhibitorem dihydropeptydazy,
enzymu otwierającego jego pierścień -laktamowy w cewkach nerkowych i zapobiegającego
powstawaniu związków potencjalnie nefrotoksycznych.
Osoczowy okres półtrwania procesu eliminacji zarówno imipenemu, jak i cylastatyny wynosi około
godziny.
–
Działania farmakologiczne.
Ze wszystkich antybiotyków -1aktarnowych Imipenem ma najszerszy zakres
dzialania.
Jest aktywny wobec ziarniaków zarówno Gram-dodatnich, jak i Gram-ujemnych (z wyjątkiem
gronkowców metycylinoopornych), wobec Entercbacteriaceae, P aeruginosa i bakterii
beztlenowych, włącznie z B. fragilis.
Szczepy gonokoków i H. influenzae oporne zarówno na penicylinę, jak i ampicylinę, są wrażliwe na
Imipenem.
– Zastosowanie kliniczne
–
Imipenem jest stosowany wyłącznie w leczeniu groźnych zakażeń wewnątrzszpitalnych szczepami
wrażliwymi na ten antybiotyk. Podaje się go dożylnie.
Jest stosowany w zakażeniach układu moczowego, oddechowego, skóry i tkanek miękkich.
Jest skuteczny w leczeniu zapaleń szpiku kostnego, septycznego zapalenia stawów, bakteriemii,
zakażeń ginekologicznych i zakażeń jamy brzusznej.
–
Ustalona jest skuteczność imipenemu w leczeniu gronkowcowego zapalenia wsierdzia. Jest on natomiast
nieużyteczny w leczeniu zakażeń OUN.

• 5. Aztreonam
[Azactam]
Aztreonam należy do monobaktamów. W przeciwieństwie do
penicylin i cefalosporyn, mających dwucykliczny układ -laktamowy, ma układ monocykliczny.
– Mechanizm działania
Podobnie jak inne antybiotyki -laktamowe aztreonam zaburza syntezę
ścia
ny komórki
bakterii.
Jego aktywność przeciwbakteryjna wynika z dużego powinowactwa do
bak
teryjnej proteiny 3,
wiążącej penicyliny.
– Farmakokinetyka
Po podaniu domięśniowym biodostępność wynosi
100%.
Okres półtrwania w surowicy krwi wynosi 1,7 godziny.
– Działanie farmakologiczne
Aztreonam jest bardzo oporny na działanie -laktamaz.
Jest bardzo aktywny wobec tlenowych bakterii Gram-ujemnych
(z
P aeruginosa i ze szczepami
H. influenzae wytwarzającymi penicylinazę oraz
z
gonokokami włącznie).
Ma słabą aktywność wobec ziarniaków Gram-dodatnich i bakterii beztlenowych.
– Zastosowanie kliniczne
Aztreonam może być stosowany zamiast aminoglikozydów w leczeniu zakażeń układu
moczowego, zakażeń dolnych dróg oddechowych, skóry
i
tkanek miękkich. Ponadto jest
skuteczny w leczeniu zapaleń szpiku kostnego,
rzeżączki,
zakażeń ginekologicznych i jamy
brzusznej wywołanych wrażliwymi drobnoustrojami chorobotwórczymi.
Z powodu wąskiego zakresu działania aztreonam często
jest
łączony z innymi środkami
przeciwbakteryjnymi.
Aztreonam podaje
się
pozajelitowo.

• Budowa chemiczna
– Aminoglikozydy są związkami zawierającymi charakterystyczne
aminocukry, przyłączone wiązaniem aminoglikozydowym do układu
heksozy.
– Są to związki wielokationowe; stopień ich polaryzacji odpowiada za
właściwości farmakokinetyczne.
• Mechanizm działania
– Aminoglikozydy hamują syntezę białka przez bezpośrednie
oddziaływanie na rybosomy bakterii.
Zaburzają, w procesie inicjującym syntezę białka, prawidłowe przyłączani,:
informacyjnego RNA do rybosomu.
Powodują także błędne odczytanie kodu genetycznego, wskutek czego
zwalniają syntezę białka lub powodują syntezę białek nieprawidłowych.
– Aminoglikozydy mają także właściwość uszkadzania bakteryjnej błony
komórkowej.
– Żadne znane mechanizmy działania aminoglikozydów nie tłumaczą
jednak w sposób wystarczający ich szybkiego efektu bakteriobójczego.
C. Aminoglikozydy

• Farmakokinetyka
• Z powodu struktury wielokationowej wszystkie aminoglikozydy
słabo
wchłania
ją się po podaniu doustnym.
• Są szybko wchłaniane po podaniu domięśniowymi podskórnym.
• Wszystkie aminoglikozydy są bardziej aktywne w środowisku
zasadowym
• Oporność bakterii
może wynikać
z
działania enzymów
bakteryjnych
inaktywują
cych cząsteczkę aminoglikozydu.
• Plazmidy i czynniki R (oporności) przenoszą kod genetyczny
tych enzymów. Dlategoteż liczne szczepy bakterii, wrażliwe
początkowo na
aminoglikozydy.
stają się na nie oporne.
• Mechanizm ten może również prowadzić do zaniku działania
synergistycznego, między antybiotykami -laktamowymi i
aminoglikozydami wobec
emerokoków
• Zdarza się oporność krzyżowa między antybiotykami
aminoglikozydowymi.

• 5. Działania farmakologiczne
– Streptomycyna
• duże stężenia streptomycyny działają bakteriobójczo; małe stężenia bakteriostatycznie, jest aktywna wobec
organizmów wywołujących dżumę Yersinia pestis),
a
także w kombinacji
z penicyliną
wobec Gram-dodatnich
enterokoków i
paciorkow
ców. In vivo streptomycyna tłumi rozwój prątków gruźlicy
M tuberculosis
–
Neomycyna
•
działa skutecznie wobec wielu gatunków Gram-ujemnych, a także jest aktywna wobec
szeregu
Gram-dodatnich
bakterii (np. S. aureus) i
M tuberculosis
Paciorko
wce są na ogół niewrażliwe na neomycynę.
– Gentamycyna [Gentamicin, Gentaforj
• działa bakteriobójczo wobec różnych Gram-ujemnych mikroorganizmów z gatunkami indolododatnimi
Proteus,
Pseudomonas i Serratia włącznie. Niektóre szczepy Staphylococcus mogą być wrażliwe na gentamycynę.
– Tobramycyna [Tobrex, Brulamycin, Nebcin, Obracin]
• ma zakres działania przeciwbakteryjnego podobny do zakresu działania gentamycyny, lecz może być nieco
bardziej aktywna
wobec
Pseudomonas.
– Amikacyna [Amikacin, Amikin, Biodacin]
• także ma zakres działania zbliżony do gentamycyny, lecz stosuje
się
ją na ogół wyłącznie do leczenia zakażeń
bakteriami opornymi na gentamycynę oraz M tuberculosis
– Netylmycyna
• ma
zakres
działania podobny do zakresu działania amikacyny
i
może być skuteczna wobec bakterii opornych
na gentamycynę.
– Kanamycyna
• ma w porównaniu
z
gentamycyną znacznie węższy
zakres
działania stosowana przy M tuberculosis

• Zastosowanie kliniczne
– a. Streptomycyna
• Streptomycyną, zazwyczaj w kombinacji z penicyliną G, leczy się podostre zapalenie
wsierdzia spowodowane przez paciorkowca zieleniejącego, rzadko jest stosowana
w
monoterapii
z
powodu
częstego
rozwoju oporności bakteryjnej.
•
Jakkolwiek streptomycyna nie ma już zastosowania
w
monoterapii gruźlicy płuc, jest często
łączona z innymi środkami w celu leczenia groźnych postaci tej choroby.
– Gentamycyna,
tobramycyna, amikacyna
i netylmycyna [Netromycin, Guardocin]
•
Wiele zakażeń może być
z
powodzeniem leczonych tymi środkami, lecz toksyczność
ogranicza ich zastosowanie do zagrażających życiu zakażeń
wy
wołanych przez: P
aeruginosa, Serratia, Enterobacter i Klebsiella, gronkowce
wrażliwe na gentamycynę.
•
Środki
te są
czasami używane jako składnik wstępnej, „ślepej terapii"
groźnych
zakażeń
o
nieznanej etiologii. W zakażeniach tych podaje
się
penicylinazooporne penicyliny lub
cefalosporyny w kombinacji
z
aminoglikozydami, np.
z
gentamycyną.
–
Neomycyna.
•
Z powodu poważnych objawów toksycznych występujących po podaniu systemowym jest
ona najczęściej używana jako maść dermatologiczna lub oczna. Ponadto neomycyna może
być stosowana doustnie przed zabiegami chirurgicznymi jamy brzusznej lub w leczeniu
śpiączki wątrobowej.
– Kanamycyna
• również została w większości przypadków zastąpiona mniej toksycznymi i bardziej
skutecznymi lekami.

– Preparaty i
ich
podawanie
• Streptomycyna
• Najczęstszą drogą podawania jest iniekcja domięśniowa, w celu zapobiegania
rozwojowi oporności bakteryjnej
terapię
streptomycyną rzadko stosuje się dłużej niż
10 dni (z wyjątkiem leczenia gruźlicy
i
podostrego zapalenia wsierdzia).
• Gentamycyna
• Lek ten może być podawany domięśniowo, dożylnie lub pod postacią maści czy kremu.
•
Tobramycyna, amikacyna i netylmycyna
są podawane domięśniowo lub dożylnie.
• Kanamycyna
może być podawana domięśniowo, dożylnie lub (w celu działania
miejscowego, w przewodzie pokarmowym) doustnie.
•
Neomycyna
•
Lek ten jest dostępny w postaci kremów, maści, aerozoli, sam lub w
mie
szankach
z
polimyksynami, bacytracyną i
z
innymi antybiotykami oraz kortykosteroidami.
• Jest dostępna także w formie preparatu do podawania doustnego (w zakażeniach
przewodu pokarmowego)
i
pozajelitowego, jakkolwiek rzadko jest stosowana
pozajelitowo.
–
Działania niepożądane
•
Wszystkie aminoglikozydy mają wąski indeks terapeutyczny, ograniczający ich
pozajelitowe zastosowanie.
• Ototoksyczność i nefrotoksyczność są najpoważniejszymi objawami niepożądanymi
terapii.

D. Tetracykliny
• Budowa chemiczna. Tetracykliny
i związki im pokrewne są pochodnymi
policyklicznego naftacenokarboksyamidu.
• Mechanizm działania
Tetracykliny działają głównie bakteriostatycznie hamując syntezę białek przez
wiązanie
się z
podjednostką 30 S rybosomu.
Tetracykliny oddziałują na komórki zarówno eukariotyczne, jak i prokariotyczne,
lecz obecność aktywnego transportu w komórce drobnoustroju najwyraźniej ułatwia
przenikanie tetracyklin przez jego błony komórkowe.
• Oporność bakterii
Bakterie Gram-dodatnie często stają
się
oporne na tetracykliny, co
w
znacznym
stopniu ogranicza przydatność tych leków.
Występuje całkowita oporność krzyżowa między poszczególnymi preparatami
tetracyklin.
• Dzialania farmakoiogiczne
Tetracykliny działają aktywnie na
wiele
bakterii Gram-dodatnich i Gram-ujemnych.
Tetracykliny są skuteczne wobec Mycoplasma, Borrelia, Chlamydia i riketsji.
Są stosowane jako leki drugiego rzutu w schorzeniach wywołanych przez gatunki
Leptospira i Treponema.
W dużych stężeniach tetracykliny hamują wzrost pierwotniaków Entamoeba
histolytica.
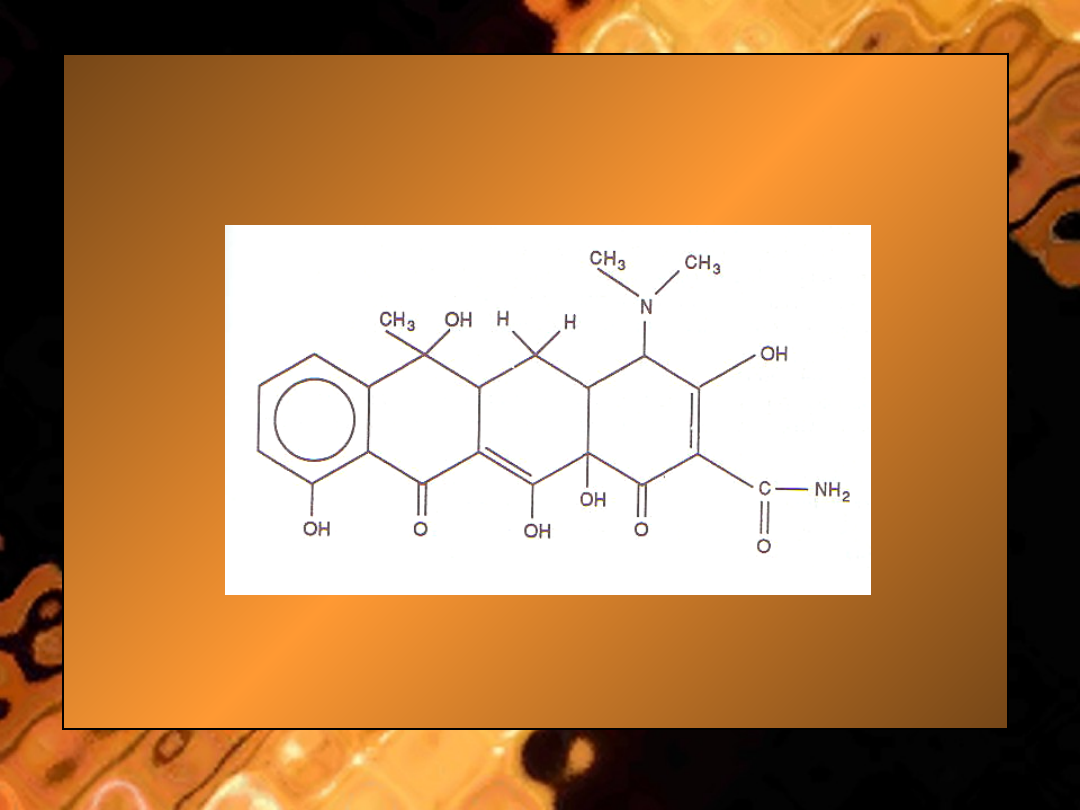
• Ryc.
Tetracyklina

– Zastosowanie kliniczne
Zastosowanie tetracyklin w leczeniu chorób infekcyjnych maleje w związku ze wzrastającą na nie opornością
bakterii i wprowadzaniem do leczenia nowych. skuteczniejszych środków przeciw drobnoustrojom.
• Za pomocą tetracyklin są leczone następujące schorzenia:
(1) zakażenia riketsjami (w których są lekami z wyboru), obejmujące:
gorączkę plamistą Gór Skalistych,
dur plamisty, chorobę Brilla,
tyfus mysi i chorobę tsutsugamushi (japońską gorączkę rzeczną),
zakażenie Rikettsia akari (przebiegające z wysypką),
gorączkę Q;
(2) zakażenia chlamydiami, powodujące:
ziarniniaka wenerycznego,
chorobę papuzią,
wtrętowe zapalenie spojówek,
jaglicę;
(3) zakażenia bakteriami z rodzaju Mycoplasma;
(4) zakażenia pałeczkami:
brucelozy,
cholery,
Shigella i Salmonella (niektórymi)

(5) zakażenia weneryczne:
rzeżączka,
kiła,
wrzód miękki (weneryczny),
ziarniniak pachwinowy (weneryczny),
chlamydiowe zapalenie cewki moczowej i szyjki macicy
(6) amebiaza.
• Choroba z Lyme, wielosystemowe zaburzenie o charakterze
zapalnym, jest spowodowane przez krętek Borrelia burgdorferi
przenoszony przez kleszcze. Doustne podawanie tetracykliny lub
doksycykliny przez 10-20 dni skraca czas trwania objawów
chorobowych i zapobiega rozwojowi poważniejszych nastçpstxk
choroby.
• Tetracykliny mogą być z powodzeniem stosowane w leczeniu
trądzika.

– Preparaty i drogi ich podawania
Tetracykliny są dostępne w preparatach do podawania doustnego, dożylnego i
domięśniowego. Mogą być także podawane miejscowo, również jako krople okulistyczne.
• Do grupy tetracyklin należą:
chlorotetracyklina
oksytetracyklina
tetracyklina
demeklocyklina. W porównaniu z innymi tetracyklinami lek ten utrzymuje
się w surowicy krwi dłużej i w wyższych stężeniach.
Metacyklina [Rondomycin]. Lek ten jest bardzo szybko wchłaniany.
Minocyklina. Obecność pokarmu i jonów wapnia nie wpływa na
wchłanianie tego leku.
Doksycyklina [Vibramycin]. Po pierwszym dniu leczenia doksycyklina
może być podawana raz na dobę
.
• W przeciwieństwie do innych tetracyklin 90% leku jest wydalanych z kałem:
dlatego nie kumuluje się on w surowicy krwi u pacjentów z zaburzoną
czynnością nerek. Jest to więc jedna z najbezpieczniejszych tetracyklin,
możliwych do zastosowania w leczeniu zakażeń pozanerkowych u tych chorych.

• Działania niepożądane
•
Mogą wystąpić reakcje nadwrażliwości pod postacią zarówno wysypek
skórnych, jak i gorączki polekowej. Powszechna jest w grupie tetracyklin alergia
krzyżowa.
•
Podczas doustnego podawania tetracyklin dość często występują objawy
podrażnienia przewodu pokarmowego.
•
Dożylne podawanie tetracyklin może być przyczyną zakrzepowego zapalenia żył
z powodu działania miejscowo drażniącego. Wstrzyknięcia domięśniowe są
bolesne, powodują miejscowe podrażnienie, a wchłanianie jest słabe.
•
Duże dawki tetracyklin mogą być przyczyną zaburzeń czynności wątroby.
Niebezpieczeństwo powstania tego powikłania nasila się w trakcie ciąży.
•
Zażycie przeterminowanych i rozłożonych tetracyklin może być przyczyną
powstania zespołu Fanconiego (dysfunkcji cewek nerkowych wiodącej do
niewydolności nerek).
•
Tetracykliny mogą podwyższać ciśnienie wewnątrzczaszkowe, szczególnie u
niemowląt.

Działania niepożądane
– Podawanie tetracyklin dzieciom może doprowadzić do
powstania żółto-brązowego przebarwienia zębów i
zaburzeń wzrostu kośćca.
Tetracykliny odkładają się w zębach i w kościach wskutek
właściwości chelatujących, tworząc związki tetracykliny z
ortofosforanem wapnia.
Stopień przebarwienia zębów zależy od dawki całkowitej
tetracyklin i czasu trwania terapii.
Ryzyko powstania przebarwień zębów wzrasta, gdy
tetracykliny są podawane niemowlętom przed
pojawieniem się pierwszych zębów.
Jednakże przebarwienia zębów stałych mogą powstać,
jeżeli tetracykliny były podawane dzieciom w wieku od 2
miesięcy do 7 lat, czyli w okresie kalcyfikacji zębów.
Podawanie tetracyklin w trakcie ciąży może spowodować
przebarwienia zębów u potomstwa.

E. Chloramfenikol
Budowa chemiczna. Chloramfenikol jest pochodną nitrobenzenu.
Mechanizm działania
Chloramfenikol hamuje syntezę białek przez wiązanie się
z
podjednostką 50 S rybosomu,
podobnie jak antybiotyki makrolidowe i klindamycyna.
Lek ten działa głównie bakteriostatycznie, chociaż wobec niektórych szczepóNN może
działać bakteriobójczo
.
Farmakokinetyka
Chloramfenikol szybko wchłania
się z
przewodu pokarmowego.
Jest rozprowadzany w płynach organizmu
i
osiąga stężenia terapeutyczne w płynie mózgowo-
rdzeniowym. Przenika także do żółci, mleka
i
cieczy wodnistej gałki ocznej.
Chloramfenikol jest metabolizowny w wątrobie
z
udziałem transferazy glukuronowej.
Jego metabolity są wydalane do moczu
.
Działania
farmakologiczne
Chloramfenikol ma względnie
szeroki
zakres działania, obejmujący m.in.:
wiele organizmów Gram-ujemnych (np. jest bakteriobójczy wobec H. influ
enzie),
bakterie beztlenowe, takie jak gatunki Bacteroides (np. B.
fragilis),
niektóre szczepy Streptococcus i Staphylococcus (przy dużych stężeniach antybiotyku),
gatunki drobnoustrojów
z
rodzaju Clostridium, Chlamydia, Mycoplasma,
riketsje, których wzrost jest hamowany przez chloramfenikol.
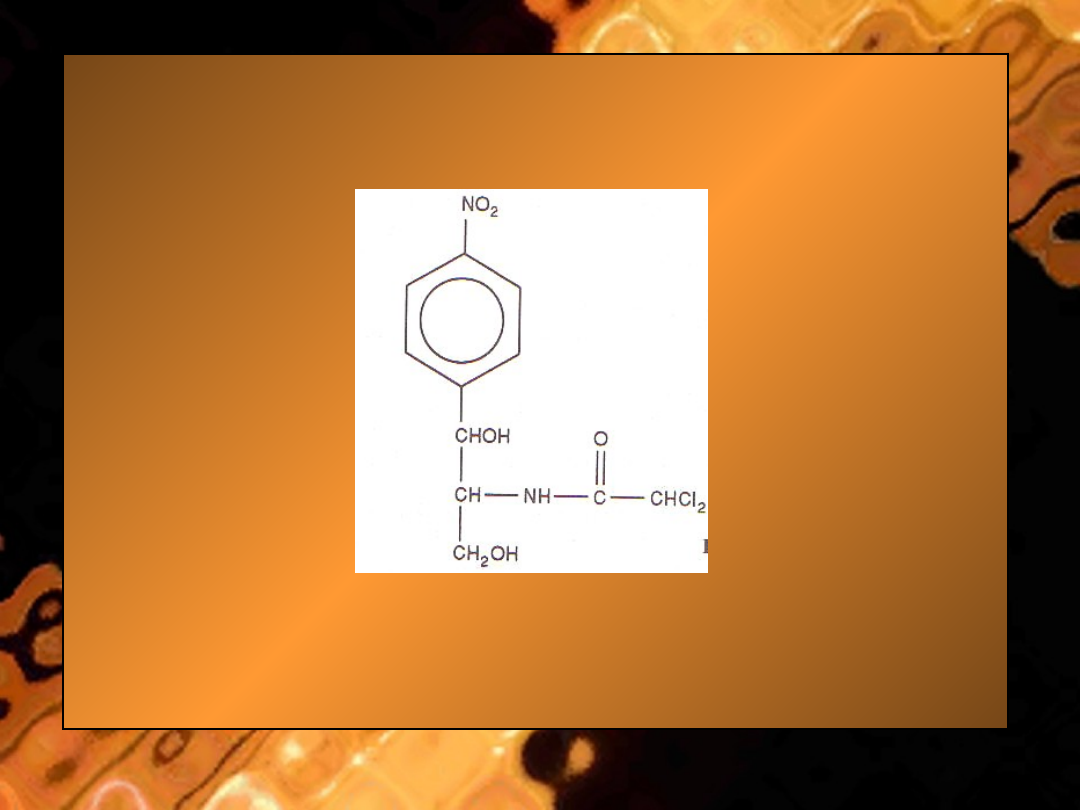
• Ryc.
Chloramfenikol

•
Zastosowanie kliniczne. Potencjalnie silne działania toksyczne ograniczają
zastosowanie chloramfenikolu do tych zakażeń, które nie mogą być skutecznie
leczone innymi antybiotykami. Jeżeli inny środek przeciwinfekcyjny jest tak
samo skuteczny jak chloramfenikol, a przy tym potencjalnie mniej toksyczny, to
powinien być zastosowany zamiast chloramfenikolu.
Chloramfenikol jest lekiem z wyboru w leczeniu duru brzusznego.
Bakteryjne zapalenie opon mózgowo-rdzeniowych wywołane przez H. influenzae
może być skutecznie leczone chloramfenikolem. U dzieci polecane jest w
początkowym okresie terapii łączenie chloramfenikolu z ampicyliną.
Większość zakażeń bakteriami beztlenowymi reaguje na leczenie chloramfenikolem.
Zakażenia riketsjami i brucelozą mogą być leczone chloramfenikolem; jednakże
preferowanymi środkami są tetracykliny.
• Preparaty i ich podawanie
Chloramfenikol i jego sól palmitynową podaje się doustnie.
Chloramfenikol w postaci bursztyniam sodu jest podawany dożylnie [Chlorocid]. Nie
ma on działania przeciwbakteryjnego, zanim nie zostanie zhydrolizowany do
chloramfenikolu. Osiąga stężenie maksymalne w ciągu godziny.
Dostępne są także roztwory i maści [Detreomycyna] do stosowania w okulistyce.

E Erytromycyna, klindamycyna i
wankomycyna
•
Budowa chemiczna
Erytromycyna jest antybiotykiem makrolidowym. Makrolidy zawierają pierścień laktonowy
i jedną lub więcej cząsteczek dezoksycukru.
Klindamycyna [Klimicin,DalacinC]jest7-dezoksy,7-chloropochodn41ekumacie‑
rzystego, linkomycyny [Lincocin, Cillimycin, Neloren], którą zasadniczo zastąpiła.
Wankomycyna jest złożonym glikopeptydem.
•
Mechanizm działania
Erytromycyna i klindamycyna hamują syntezę białek, łącząc się z podjednostką 50S
rybosomu wrażliwego mikroorganizmu: działają one zazwyczaj bakteriostatycznie, lecz w
pewnych warunkach mogą być bakteriobójcze.
Wankomycyna hamuje syntezę bakteryjnej ściany komórkowej. W przeciwieństwie więc do
erytromycyny i klindamycyny jest oczywiście bakteriobójcza.
•
Działanie farmakologiczne
–
Erytromycyna
Jest aktywna wobec bakterii Gram-dodatnich, z niektórymi szczepami S. aureus, opornymi
na leczenie penicyliną G włącznie.
Wrażliwe na erytromycynę są gatunki Neisserria, niektóre szczepy H. influenzam,
Bordetella, Legionella, Treponema i Mycoplasma.
–
Klindamycyna
Klindamycyna jest aktywna wobec:bakterii Gram-dodatnich i beztlenowych paciorkowców,
wielu innych bakterii beztlenowych, szczególnie B. fragilis.
–
Wankomycyna działa głównie na bakterie Gram-dodatnie.
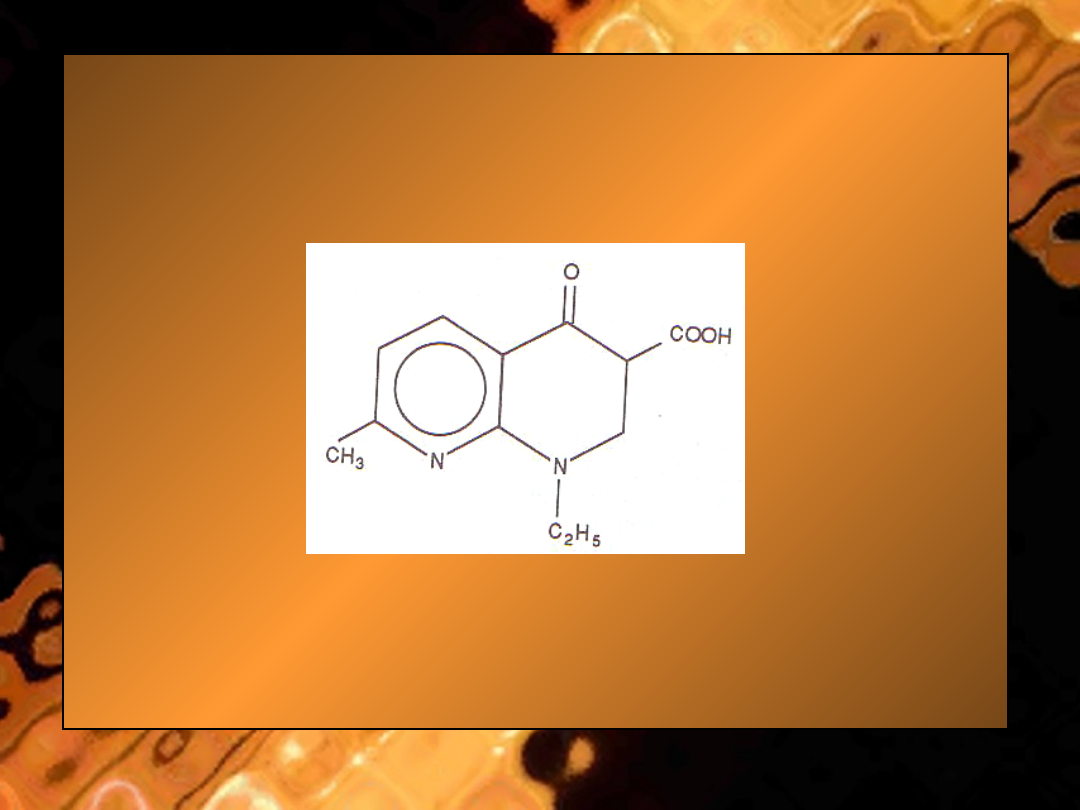
• Ryc. Kwas nalidyksowy

– G. Chinolony
•
Budowa chemiczna. Norfloksacyna i cyprofloksacyna są fluorochinolonami. Te
nowsze syntetyczne środki przeciw drobnoustrojom mają budowę zbliżoną do
starszego chinolonu - kwasu nalidyksowego.
• Mechanizm działania. Chinolony działają na gyrazę DNA - enzym biorący udział w
replikacji DNA. Jest to szybkie działanie bakteriobójcze.
• Oporność bakterii. Oporność na fluorochinolony nie rozwija się tak szybko jak
oporność na kwas nalidyksowy.
• Farmakokinetyka
Po podaniu doustnym norfloksacyna [Nolicin] i cyprofloksacyna [Ciprobay, Ciprinol]
szybko wchłaniają się z przewodu pokarmowego.
Okres półtrwania wynosi 3-4 godziny.
Oba leki są częściowo metabolizowane przez wątrobę.
• Działania farmakologiczne
Norfloksacyna i cyprofloksacyna działają na wiele bakterii Gram-dodatnich i Gram-
ujemnych. Ponadto cyprofloksacyna jest aktywna wobec niektórych prątków. Są bardzo
aktywne wobec gonokoków.
Norfloksacyna i cyprofloksacyna działają na prawie wszystkie zarazki wywołujące
zakażenia układu moczowego.
cyprofloksacyna jest wysoce aktywna wobec bakterii będących przyczyną zapalenia jelit i
wobec gronkowców, w tym także opornych na metycylinę.

ŚRODKI
STOSOWANE W
LECZENIU
ZAKAŻEŃ
GRZYBICZYCH

A. Nystatyna
• Budowa chemiczna.
Nystatyna jest antybiotykiem polienowym.
• Mechanizm działania
• Lek działa grzybostatycznie i grzybobójcze.
•
Przyłącza się do steroli, szczególnie ergosterolu, występującego w dużych ilościach w błonie
komórki grzybów i drożdży. Wydaje się, że w wyniku tego połączenia w obrębie błony
powstają kanały, przez które małe cząstki przenikają na zewnątrz komórki.
• Farmakokinetyka
• Nystatyna nie jest wchłaniana w uchwytnych ilościach z przewodu pokarmowego.
• Nie wchłania się ze skóry i błon śluzowych.
• Nie jest podawana pozajelitowo.
• Jest słabo rozpuszczalna i rozpada się gwałtownie w środowisku wodnym.
• Zastosowanie kliniczne
• Nystatyna jest używana do leczenia zakażeń skóry, błon śluzowych i przewodu
pokarmowego wywołanych przez Candida.
• Pleśniawka (kandydiaza jamy ustnej) i zapalenie pochwy są leczone miejscowo, w
zakażeniach przewodu pokarmowego nystatyna jest podawana doustnie.
• Preparaty.
• Nystatyna jest dostępna jako maść, zawiesina do stosowania doustnego, tabletki doustne, krople i zasypka.
• Działania niepożądane.
• Po podaniu doustnym sporadycznie występują zaburzenia żołądkowe-jelitowe.

B. Amfoterycyna B [Fungizone]
• Budowa chemiczna.
Lek ten jest antybiotykiem polienowym.
• Mechanizm działania
jest taki sam jak nystatyny.
•
Farmakokinetyka
Amfoterycyna B jest słabo wchłaniana z przewodu pokarmowego.
Okres półtrwania po podaniu dożylnym wynosi około 24 godzin.
• Działania farmakologiczne
Amfoterycyna B jest środkiem przeciwgrzybiczym o szerokim zakresie działania.
Wrażliwe na nią są: Histoplasma capsulatum, Cryptococcus neoformans, Coccidioides
immitis, Candida, Blastomyces dermatitidis oraz niektóre szczepy Aspergillus i
Sporotrichum.
Stężenie amfoterycyny B decyduje o jej działaniu grzybostatycznym lub grzybobójczym.
• Preparaty
Do iniekcji dożylnych dostępna jest amfoterycyny B w postaci zliofilizowanego proszku.
Amfoterycyna B występuje także w postaci preparatów do stosowania miejscowego w
leczeniu skórnej i śluzówkowej postaci kandydiazy.
• Działania niepożądane.
Wszyscy chorzy poddawani leczeniu amfoterycyną B powinni być
hospitalizowani przynajmniej w początkowym okresie terapii.
Mogą wystąpić reakcje nadwrażliwości.
Po podaniu dożylnym często pojawiają się gorączka, dreszcze, bóle głowy; zaburzenia
żołądkowe-jelitowe. Zazwyczaj, w miarę trwania terapii amfoterycyną B. pacjenci tolerują
lek coraz lepiej.
Występują także zakrzepowe zapalenia żył w trakcie terapii dożylnej.

C. Gryzeofulwina [Gricin]
• Budowa chemiczna.
Lek ten jest wytwarzany przez Penicilliitm griseofulvum. Jest słabo rozpuszczalny w
wodzie.
• Mechanizm działania.
Dokładny mechanizm działania nie jest poznany. Prawdopodobnie gryzeofulwina łączy się z
polimeryzującymi nićmi wrzeciona, rozrywając wrzeciono mitotyczne. Działa grzybostatycznie.
Farmakokinetyka.
Gryzeofulwina po podaniu doustnym jest wchłaniana z górnej części jelita cienkiego.
Większość leku wydala się w formie nie zmienionej z kałem.
• Działania farmakologiczne.
Gryzeofulwina jest aktywna wobec grzybów skórnych z Microsporum, Epidermophyton i szczepami
Trichophyton włącznie. Nie
działa
na drożdże.
•
Zastosowanie kliniczne.
Z powodu dużego powinowactwa do keratyny gryzeofulwina jest używana do leczenia grzybiczych
schorzeń skóry, włosów, paznokci, grzybicy skóry owłosionej, stóp, podudzi, tułowia i grzybicy
obrączkowatej. Podaje się ją doustnie. Stosowanie miejscowe jest mało skuteczne.
• Preparaty.
Gryzeofulwina,
jest
dostępna w postaci tabletek, kapsułek i zawiesin do podawania doustnego.
• Działania niepożądane.
Szerokie stosowanie gryzeofulwiny wykazało jej stosunkowo małą toksyczność.
Wśród możliwych objawów niepożądanych występują: bóle głowy, zaburzenia neurologiczne, podrażnienia
przewodu pokarmowego, reakcje skórne z pokrzywką i nadwrażliwością na światło włącznie.

D. Flucytozyna [Ancotil]
• Budowa chemiczna.
Lek ten jest fluoropirymidyną.
• Mechanizm działania.
Flucytozyna jest przetwarzana wewnątrz komórki grzyba (lecz nie w komórce gospodarza) w 5-
fluorouracyl - antagonistę metabolicznego, który doprowadza do hamowania syntetazy
tymidylowej.
• Farmakokinetyka.
Flucytozyna jest dobrze wchłaniana z przewodu pokarmowego i szeroko rozprowadzana w
organizmie. Przenika nawet do płynu mózgowo-rdzeniowego.
Jest wydalana do moczu, głównie w postaci nie zmetabolizowanej.
• Działanie farmakologiczne.
Lek jest aktywny wobec C. neoformans. Działa na niektóre szczepy Candida, ze szczepami
Candida albicans włącznie.
Jednakże w trakcie terapii C albicans może stać się oporna na flucytozynę.
• Zastosowanie kliniczne .
Jakkolwiek flucytozyna nie jest tak skuteczna jak amfoterycyna B, jest jednak mniej toksyczna i
może być podawana drogą doustną. Jest stosowana w leczeniu ogólnoustrojowych zakażeń
wywołanych przez C albicans i C neoformans (Cryptococcus meningitidis).
Najczęściej stosuje się ją w kombinacji z amfoterycyną B.
• Preparaty.
Flucytozyna jest dostępna w postaci kapsułek do podawania doustnego.
• Działania niepożądane
. śmiertelna w skutkach depresja szpiku, zaburzenia żołądkowe-jelitowe,
wysypki skórne, zaburzenia czynności wątroby.

E. Ketokonazol [Nizoral, Oronazol]
• Budowa chemiczna.
Ketokonazol jest podstawioną pochodną imidazolu.
• Mechanizm działania
.
Ketokonazol zmienia przepuszczalność błony komórkowej przez blokowanie syntezy
ergosterolu - głównego sterolu komórki grzyba.
• Farmakokinetyka
Ketokonazol jest wchłaniany z przewodu pokarmowego. Maksymalne stężenie w
surowicy występuje po upływie 1-2 godzin od podania doustnego.
Aby lek mógł dobrze się rozpuścić, powinien się znajdować w środowisku kwaśnym.
Dlatego środki podwyższające pH środowiska przewodu pokarmowego mogą
zmniejszać biodostępność ketokonazolu.
• Działanie farmakologiczne i zastosowanie kliniczne
Ketokonazol
jest
skuteczny
w
leczeniu
blastomykozy,
kokcydioidomykozy,
histoplazmozy, parakokcydioidomykozy, przewlekłej kandydiazy skóry i błon śluzowych
oraz opornych zakażeń grzybiczych skóry.
Ketokonazol działa wolniej niż inne, dostępne środki przeciwgrzybicze, wymaga więc
długiego okresu podawania. W związku z tym jest mniej użyteczny w leczeniu ciężkich
i ostrych zakażeń ogólnoustrojowych.
Słabo przenika do płynu mózgowo-rdzeniowego, dlatego też nie jest zalecany do
leczenia zapalenia grzybiczego opon mózgowych.
• Preparaty.
Ketokonazol występuje w formie tabletek do podawania doustnego.
• Działania niepożądane.
Najczęściej występującymi objawami niepożądanymi są
nudności i wymioty. Rzadziej występują reakcje nadwrażliwości (pokrzywka i anafilaksja).

E Flukonazol [Diflucan]
• Budowa chemiczna.
Lek jest bis-triazolem.
• Mechanizm działania.
Hamuje enzymy związane z cytochromem P-450, blokując
syntezę ergosterolu.
• Farmakokinetyka
Flukonazol jest rozpuszczalny w wodzie lepiej niż ketokonazol i charakteryzuje
się dużą biodostępnością.
Maksymalne stężenie w surowicy występuje po upływie 1-2 godzin od podania. a
okres półtrwania wynosi 30 godzin.
Jest wydalany w postaci nie zmienionej z moczem.
• Działanie farmakologiczne i zastosowanie kliniczne
Flukonazol jest aktywny wobec szeregu ogólnoustrojowych patogenów
grzybiczych z Aspergillus, B. dermatitidis, C. albicans, C. neoformans, C immitis i
H. capsulatum włącznie.
Jest skuteczny w leczeniu kandydiazy jamy ustnej, gardła i przełyku, groźnych
ogólnoustrojowych zakażeń kandydiazowych i kryptokokowego zapalenia opon.
• Preparaty.
Flukonazol może być podawany doustnie i dożylnie.
• Działania niepożądane
Jest mniej toksyczny od amfoterycyny B i flucytozyny i tolerowany przez chorych
lepiej niż ketokonazol.
Podawanie flukonazolu powinno być przerwane u chorych z postępującą
dysfunkcją wątroby.

G. Naftyfina
• Budowa chemiczna. Ten syntetyczny środek przeciwgrzybiczy
jest alliloaminą.
• Mechanizm działania.
• Naftyfina zwalnia syntezę ergosterolu, istotnego składnika grzybiczej
błony komórkowej, przez hamowanie enzymu epoksydazy - skwalenu
.
• Działanie farmakologiczne i zastosowanie kliniczne
• In vitro naftyfina działa grzybobójcze na grzyby zakażające
skórę i
grzybostatycznie na drożdżaki, np. C albicans.
• W leczeniu znalazła zastosowanie w terapii grzybicy stóp, podudzi i
tułowia. Nie działa ani w grzybiczych zakażeniach włosów, ani w
zakażeniach paznokci.
• Preparaty i ich podawanie.
• Naftyfina jest dostępna pod postacią 1% kremu do
stosowania miejscowego.
• Działania niepożądane.
• Opisano uczucie parzenia skóry, nadmierną suchość,
zaczerwienienie i świąd.

H. Mikonazol [Daktarin, Gyno-Femidazol] i
klotrimazol [Fungizid]
• Są to pochodne imidazolowe, stosowane głównie miejscowo.
Hamują one wzrost powszechnie występujących grzybów skórnych -
drożdżaków, ze szczepami Trichophyton, Epidermophyton floccosum, C.
albicans i Malassezia furfurwłącznie.
Są stosowane w leczeniu grzybic i innych zakażeń skóry wywołanych
przez organizmy podatne na lek, a także w leczeniu kandydiazy warg
sromowych i pochwy.
• Mikonazol występuje także jako preparat do podawania
pozajelitowego stosowany w leczeniu ciężkich ogólnoustrojowych
zakażeń grzybiczych, takich jak kandydiaza, kokcydioidomykoza i
kryptokokoza. Jednakże toksyczność leku zmniejsza jego
przydatność i ogranicza jego skuteczność.

I. Haloprogina i tolnaftat
• Tolnaftat jest skuteczny w leczeniu większości grzybic
skóry powodowanych przez Trichophyton rubrum i
Microsporum canis, lecz nie działa na Candida.
• Haloprogina działa grzybobójcze wobec
Epidermophyton, Pityrosporum, Microsporum,
Trichophyton i Candida.
• W przeciwieństwie do tolnaftatu - nietoksycznego i nie
wywołującego reakcji alergicznych - haloprogina może
powodować świąd, pokrzywki i zaognienie skóry w
miejscu stosowania.

ŚRODKI
STOSOWANE W
LECZENIU
ZAKAŻEŃ
PIERWOTNIAKOWY
CH

Metronidazol
.
Jest
lekiem
bardzo
skutecznym
w
leczeniu
zakażeń
pierwotniakowych, z rzęsistkowicą, inwazjami Giardia lamblia-i amebiazą wywołaną
przez E. histolytica włącznie. Jest także aktywny w terapii zakażeń bakteriami
beztlenowymi (np. wywołanymi przez szczepy Bacteroides).
Diloksanid (diklofurazol) działa pełzakobójczo. Stosuje się go w leczeniu
bezobjawowych nosicieli cyst ameby.
Suramina jest niemetalicznym, wieloanionowym związkiem stosowanym w leczeniu
afrykańskiej trypanosomatozy (inwazji świdrowców) zarówno we wczesnym, jak i
zaawansowanym stadium choroby. Jest także bardzo skuteczna w leczeniu
onchocerkozy, lecz została w dużym stopniu zastąpiona mniej toksyczną
iwermektyną.
Nifurtymoks jest lekiem stosowanym w leczeniu południowoamerykańskiej
trypanosomatozy
Styboglukonian, związek antymonowy, jest lekiem z wyboru do leczenia
leiszmaniozy.
Pentamidyna. Pentamidyna jest skuteczna w leczeniu wczesnych postaci
afrykańskiej trypanosomatozy oraz w profilaktyce i leczeniu zapalenia płuc
wywołanego przez P carinii. To ostatnie schorzenie jest oportunistycznym
zakażeniem występującym u chorych z AIDS. pentamidyna może być bardzo
skuteczna u chorych, u których terapia związkami antymonowymi jest nieskuteczna.

•
Chlorochina [Arechin] jest lekiem z wyboru do leczenia niepowikłanej, ostrej
malarii wywołanej przez którykolwiek z mikroorganizmów Plasmodium (z
wyjątkiem postaci opornych) oraz stosowanym w celach profilaktycznych podczas
pobytu w rejonach endemicznych.
•
Prymachina jest stosowana do leczenia i zapobiegania nawrotom malarii
wywołanej przez Plasmodium vivax i Plasmodium ovale po opuszczeniu rejonów
endemicznych Jest podawana wraz z chlorochiną lub z innym lekiem
przeciwzimniczym.
•
Pirymetamina [Daraprim] i sulfadoksyna są stosowane zamiennie w
profilaktyce i leczeniu zakażeń wywołanych przez oporne na chlorochinę szczepy
Plasmodiumfalciparum. Kombinacja pirymetaminy z sulfadoksyną jest dostępna
jako [Fansidar].
•
Chinina
–
Siarczan chininy podawany doustnie jest skuteczny w leczeniu ostrych,
nieskomplikowanych ataków malarii wywołanych przez oporne na
chlorochinę szczepy Plasmodium falciparum.
–
Dwuchlorowodorek chininy, podawany pozajelitowo, jest stosowany w
leczeniu ciężkich schorzeń spowodowanych przez oporne na chlorochinę
szczepy P. falciparum.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
Wyszukiwarka
Podobne podstrony:
chemioterapia zakazeń bakteryjnychskrócona
CHEMIOTERAPEUTYKI W CHOROBACH BAKTERYJNYCH
CHEMIOTERAPIA ZAKAŻEŃ BAKTERYJNYCH, GUMed, Medycyna, Mikrobiologia, Mikrobiologia, Mikrobiologia
FARMAKOLOGIA, 03 Chemioterapia chorób bakteryjnych
chemioterapia zakazen bakteryjnychskrocona
chemioterapia zakazeń bakteryjnychskrócona
CHEMIOTERAPEUTYKI W CHOROBACH BAKTERYJNYCH
Metody oceny wraliwoci bakterii na antybiotyli i chemioterapetyki, mikrobiologia
prelekcja z chemioterapeutykow
Bakterie spiralne do druk
choroby wirus i bakter ukł odd Bo
Ogólne zasady chemioterapi, 2013i
Kopia Chemioterapia2
Leczenie uzupełniające nowotworów narządu rodnego chemioterapia, radioterapia
Bakterie 2
Szkol Lampy bakteriobójcze
Chemioterapia przeciwbakteryjna ogólna
Bakterie w biotech
więcej podobnych podstron