
C
2
H
5
OH

Właściwości fizykochemiczne alkoholu
etylowego:
- Ciecz bezbarwna, lotna, rozpuszczająca się
w wodzie
- Temperatura wrzenia: 78 ºC
- Ciężar właściwy: 0,79
- Ciecz łatwopalna
Otrzymywanie:
1. Syntetycznie
2. metodą biochemiczną z cukrów prostych
oraz złożonych,
które przedtem poddawane są wstępnej
hydrolizie
za pomocą enzymów

Oznaczanie alkoholu w materiale
biologicznym:
1.
Metoda Widmarka
–metoda niespecyficzna (metanol,
etanol, wyższe alkohole alifatyczne oznacza sumarycznie)
2.
Metoda enzymatyczna
ADH – metoda wystarczająco
specyficzna (oznacza sumarycznie alkohol etylowy i wyższe
alkohole alifatyczne). W metodzie tej wykorzystano
pierwszą część reakcji metabolizującej alkohol etylowy w
ustroju. Dodany do krwi semikarbazyd blokuje reakcję na
etapie aldehydu. W warunkach przeprowadzanej analizy nie
oznaczymy alkoholu metylowego. Do określenia stężenia
alkoholu etylowego wykorzystuje się pomiar przyrostu
absorbancji przy 340 nm.
3.
Metody immunologiczne
: EMIT (immunoenzymatyczna) i
FPIA (met. immunofluorescencji w świetle
spolaryzowanym). W metodach tych wykorzystano zjawisko
konkurencji między antygenem oznaczanym a antygenem
oznakowanym o ograniczoną ilość miejsc na
specyficznych przeciwciałach. W metodzie EMIT
znacznikiem jest enzym, aktywny jedynie w stanie wolnym,
a w metodzie FPIA znacznikiem jest cząsteczka
fluoryzująca. Metody niespecyficzne.

T
/m
in
A
B
C
A. Alkohol izopropylowy
B. Alkohol etylowy
C. Alkohol metylowy
Chromatogram roztworów wzorcowych alkoholi
4. Metoda chromatografii gazowej (GC, GLC).
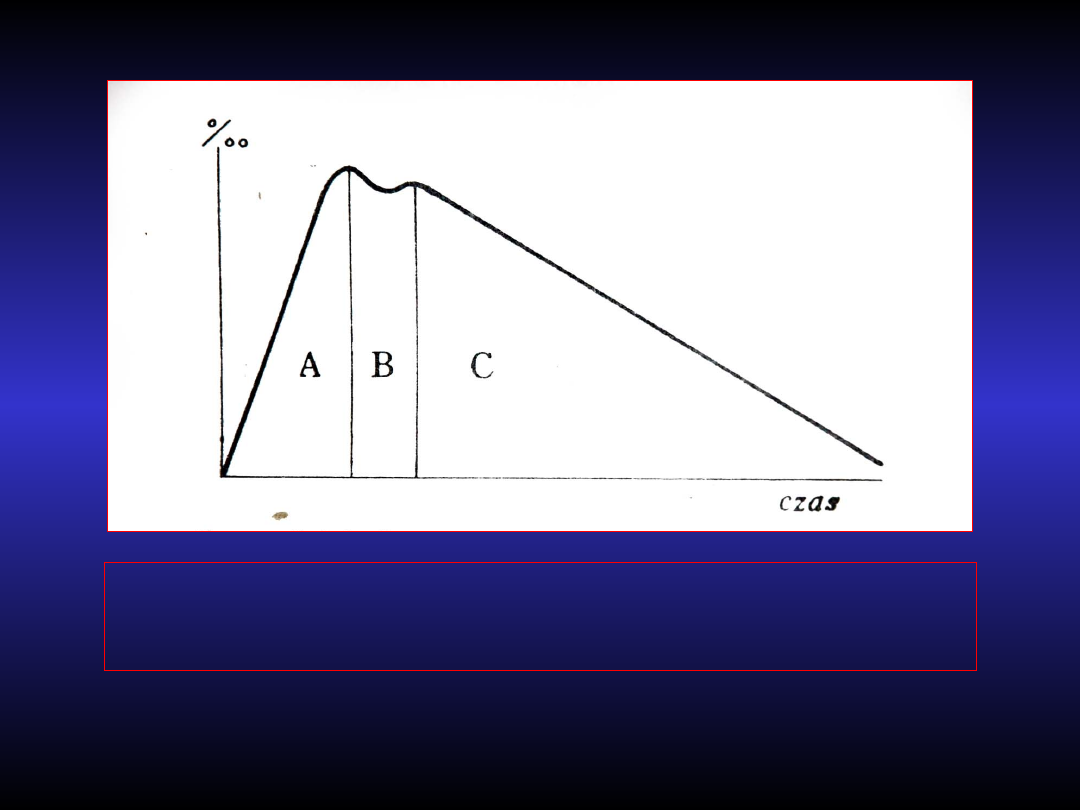
Krzywa alkoholemii
A. Resorpcja
B. Faza ustalenia równowagi
C. Faza eliminacji i wydalanie w postaci niezmienionej.
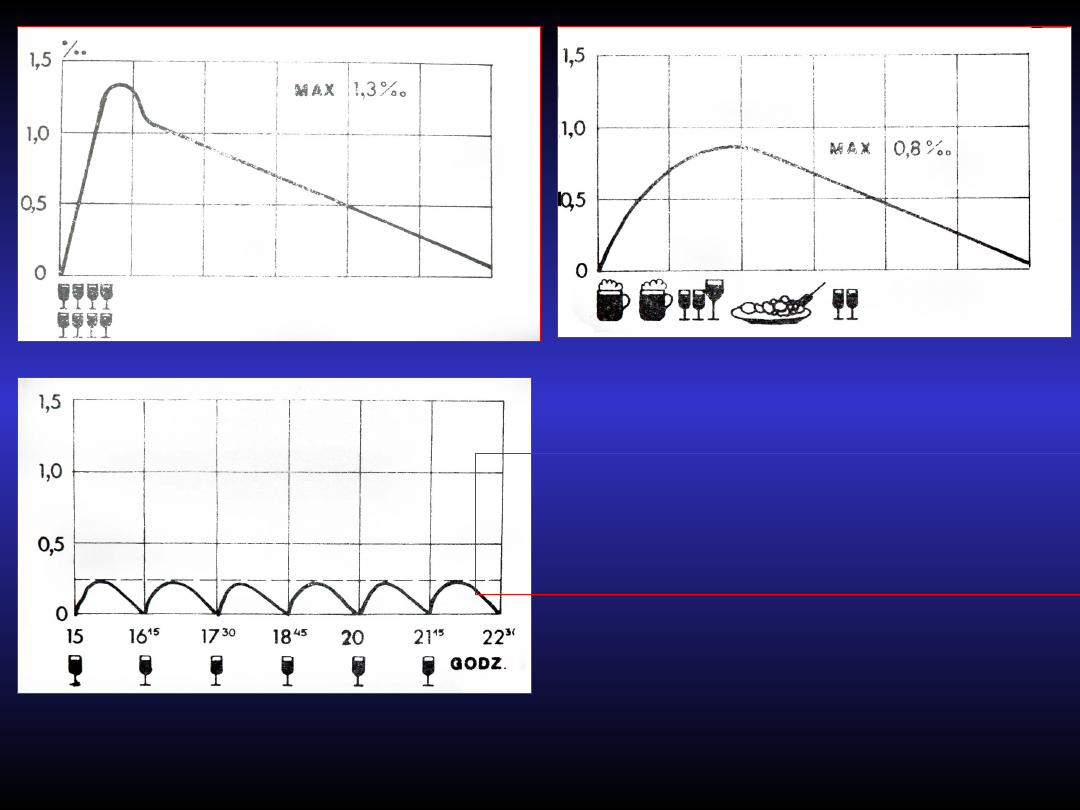
A
B
C
Krzywe alkoholemii
A. Na pusty żołądek
B. Przy posiłku
C. Przy konsumpcji rozciągniętej w czasie

5. Badanie powietrza wydychanego
Aparatura: Alcotesty, Alkomaty
Wg prawa Henry-Daltona:
stężenie alkoholu we krwi 1
---------------------------------------------------------------------- = ----------
stężenia alkoholu w powietrzu pęcherzyków płucnych 2100

Pobranie krwi na zawartość alkoholu
etylowego (osoba żywa)
- Żyła łokciowa - odkażenie związkami nie
redukujacymi: (riwanol, woda utleniona,
sublimat)
Nie wolno używać do odkażenia: alkoholi, eteru,
benzyny, chloroformu
Badanie materiału sekcyjnego:
- Krew z żyły udowej (pobranie krwi z serca może
dać wynik zawyżony na skutek pośmiertnej
dyfuzji alkoholu przez ściany żołądka i jelita)
- płyn z gałki ocznej (ciałko szkliste)
- płyn z ucha wewnętrznego (perylimfa)
- płyn mózgowo-rdzeniowy
- mięsień z kończyn dolnych
- maź stawowa
- mocz

Rachunek retrospektywny
Pozwala na wsteczne obliczenie stężenia alkoholu w czasie
wypadku, w sytuacji gdy pobranie próbki krwi miało miejsce w
kilka godzin po zdarzeniu.
C wyp. = C pobranie + β x t
0,07 < β < 0,28 ‰/h
0,1 < β < 0,2 ‰/h
( 7-8,4 g /h)

Współczynnik eliminacji obejmuje:
- utlenianie metaboliczne
- wydalanie z moczem, potem i powietrzem
wydychanym
- Liniowa zależność: od 0,5 ‰ do 2,0 ‰
- Zależy przede wszystkim od ciężaru ciała i
własności
osobniczych a także od
stężenia alkoholu.

Warunki niezbędne do przeprowadzenia
obliczeń retrospektywnych:
1. oznaczone stężenie alkoholu > 0,4
‰
2. między wypadkiem a pobraniem nie
powinno upłynąć więcej niż 5 godzin
3. wypadek i pobranie krwi powinno
mieć miejsce w fazie eliminacji

Indywidualny współczynnik eliminacji :
Można określić wtedy , gdy krew będzie pobierana
w odstępach czasowych (co najmniej trzykrotnie) co da
nam możliwość obliczenia indywidualnego współczynnika
eliminacji . Pozwoli nam to także jednoznacznie określić
fazę w jakiej znajdował się alkohol w tym czasie.

Rachunek prospektywny
Pozwala na szacunkowe obliczenie
stężenia alkoholu na podstawie ilości
alkoholu spożytego.
A= p
x
c
x
r
A – ilość alkoholu spożytego w przeliczeniu na czysty
spirytus
p – ciężar ciała
r - współczynnik rozmieszczenia, określa średni
stosunek
stężenia alkoholu w całym ustroju do stężenia
we krwi
zależy od ilości tkanki tłuszczowej (budowy
ciała) oraz
płci 0,6 < r < 1,0
c - stężenie alkoholu we krwi w promillach
dla mężczyzn średni r - 0,7
dla kobiet średni r - 0,6

n-propylowy
izo-propylowy
CH
3
CH
2
CH
2
OH t.w. 97,2°C
(CH
3
)
2
CHOH t.w. 82,3°C
15% metabolizuje do acetonu
OBJAWY ZATRUCIA
• depresja OUN
• nudności
• krwawe wymioty
ALKOHOLE
PROPYLOWE

LECZENIE
•
płukanie żołądka
• hemodializa
• podanie glukozy
• wyrównanie zaburzeń
elektrolitowych
• podtrzymywanie ciśnienia krwi

ALKOHOLE BUTYLOWE
1-butanol
pierwszorzędowy
izobutylowy 2-
metylo-1propanol
2-butanol
2-metylo-2propanol
(alkohol butylowy
trzeciorzędowy
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CHCH
2
OH
CH
3
CH
3
CHCH
2
CH
3
OH
CH
3
CH
3
C
CH
3
OH

ALKOHOLE BUTYLOWE
Zastosowanie: rozpuszczalniki lakierów nitrocelulozowych
Biotransformacja: aldehydy, kwasy karboksylowe, CO
2
i H
2
O
Wydalanie: nerki, płuca
Zatrucia ostre: depresja OUN, śpiączka, zatrzymanie akcji serca
Leczenie: analogicznie jak w przypadku alkoholi propylowych

Glikol etylenowy
15-100 g dawka śmiertelna
(100 ml płynu Borygo)
Objawy zatrucia:
1. 30 minut –12 godzin : faza narkotyczna i objawów
żołądkowo-jelitowych, objawy podobne do upojenia
alkoholem etylowym, bóle i zawroty głowy , kwasica
metaboliczna.
2. 12 –24 godzin – niewydolność układu krążenia i
oddychania,
narastająca kwasica oddechowa,
nasilenie objawów uszkodzenia
OUN. Może wystąpić
obrzęk płuc . W ciężkich przypadkach rozwija się
odoskrzelowe zapalenie płuc , które z współistniejącą
niewydolnością krążenia może doprowadzić do śmierci
3. 24-72 godzin – faza nerkowa : charakterystyczne bóle
w okolicy lędźwiowej, małomocz, bezmocz. W moczu o
niskim ciężarze właściwym występuje białko, krwinki i
kryształy szczawianu wapnia. Wzrost stężenia potasu,
mocznika i kreatyniny. Obniżeniu ulega pH, rezerwa
alkaliczna i stężenie wapnia.
4. Śmierć w początkowym okresie związana jest z
uszkodzeniem mózgui niewydolnością krążenia,
później z niewydolnością nerek
O O O COOH
CH
2
OH C CH
2
OHCOOH C C
H H OH COOH
Aldehyd glikolowy kwas glikolowy Kwas glioksalowy Kwas
szczawiowy
CH
2
OH
Glikol
CH
2
OH
O
O
C C
H
H
Glioksal
CO
2 +
H
2
O

L E C Z E N I E :
1. płukanie żołądka
2. zwalczanie kwasicy metabolicznej
3. zwalczanie zaburzeń krążeniowo
oddechowych
4. hemodializa lub dializa otrzewnowa
5. alkohol etylowy w 5-15 % roztworze
izotonicznym chlorku sodowego
( 10 – 20 g alkoholu etylowego na
dobę) lub roztworze glukozy
6. zwalczanie hipocalcemii
(podawanie calcium chloratum )

Opis
metody
Tab. 1.W a r u n k i a n a
l i z y
Aparat Chrom-5 z integratorem C-I – 100
W a r i a n t I
W a r i a n t II
Kolumna szklana dł. 3,5 m
Wypełnienie: 10 % Carbowax 20
M/Chromosorb
WAW - DMCS, 100/120 mesh
Temperatura kolumny: 160º C
Temperatura odparowalnika:
220ºC
Temperatura detektora: 240ºC
Gaz nośny: przepływ 30-40 ml/min.
Kolumna szklana dł. 3,5 m
Wypełnienie: Tenax
Temperatura kolumny: 160 º C
Temperatura odparowalnika :
210ºC
Temperatura detektora: 220ºC
Gaz nośny : azot przepływ 30-40
ml/min

Czasy retencji uzyskane dla glikolu etylenowego, propylenowego
i metabolitów glikolu.
Substancja
badana
Czas retencji w minutach
Carbowax
Tenax
Aldehyd
glikolowy
1,35
1,67
Kwas
glioksalowy
1,25
0,84
Kwas
glikolowy
2,0
4,74
Glioksal
1,70
2,90
Glikol
etylenowy
3,50
4,01
Glikol
propylenowy
4,42
2,91
Alkohol
etylowy
0,75
0,84
1,3-
Butanediol
7,50
9,14
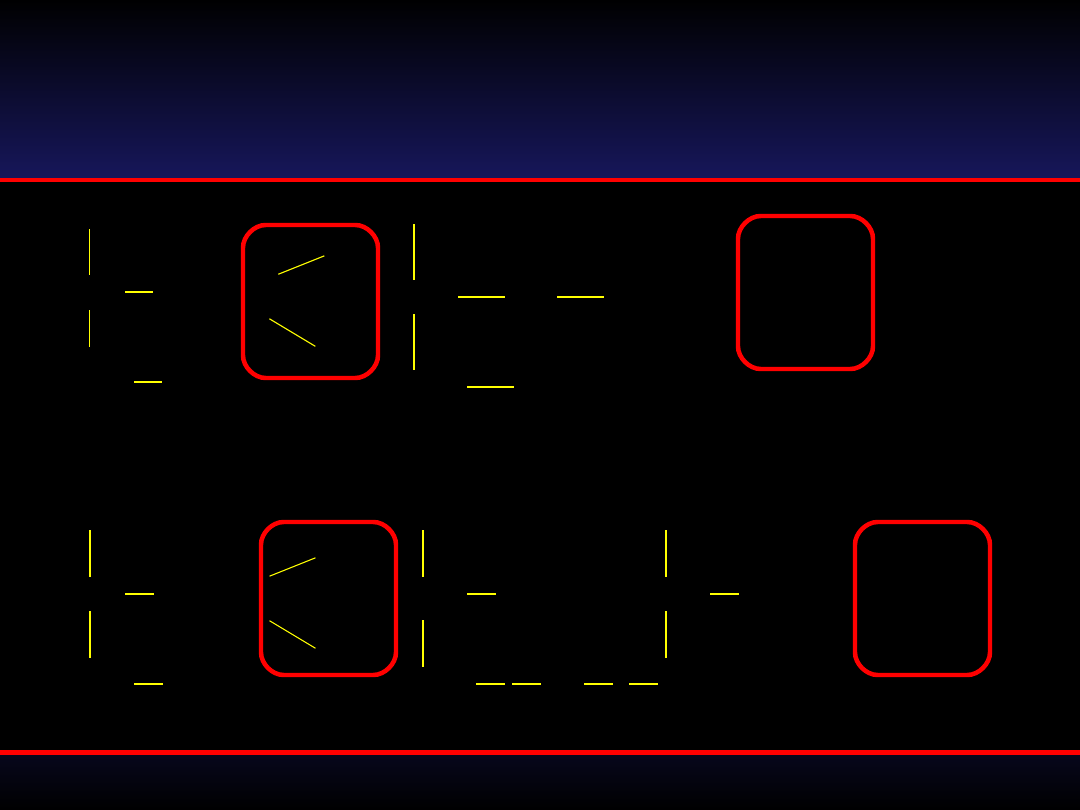
DZIAŁANIE DIMERKAPROLU W
ZATRUCIACH RTĘCIĄ
CH
2
OH CH
2
OH
S HS
CH SH + Hg CH SH Hg +
S HS
CH
2
SH CH
2
SH
Dimerkaprol (BAL)
CH
2
OH CH
2
OH CH
2
OH
S HS
CH SH + Hg CH SH CH SH +
S HS
CH
2
SH CH
2
S Hg S CH
2
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
Wyszukiwarka
Podobne podstrony:
Zatrucie Alkoholem Etylowym i Innymi Alkoholami
Ostre zatrucie alkoholem etylowym
DZIAŁANIE BIOLOGICZNE ALKOHOLU ETYLOWEGO, Farmacja, Farmakologia(1), Etanol i Metanol
Działanie alkoholu etylowego Ślosarek, Pawliński gr 7B
Alkohol etylowy a organizm człowieka2
alkohol etylowy
zatrucie alkoholem etylowtym
Zatrucie alkoholem etylowym, pierwsza pomoc
alkohol etylowy2, Rat med rok 2, Toksykologia
Alkohol etylowy, Chemia
ZESPOŁY?STYNENCYJNE Alkohol etylowy MR
Oznaczanie gęstości i procentowej zawartości alkoholu etylowego w różnych mieszaninach alkoholu w wo
Alkohol etylowy, Rat med rok 2, Toksykologia
poziomy alkohol etylowy
Alkohol etylowy
Zatrucie Alkoholem Etylowym i Innymi Alkoholami
Alkohol etylowy
więcej podobnych podstron