74 Â
WIAT
N
AUKI
Listopad 1996
WCZESNE WYKRYWANIE
K
obieta zg∏asza si´ do lekarza,
kiedy wyczuje zgrubienie w
piersi. Doktor stwierdza guz
i sprawa zaczyna si´ toczyç dobrze zna-
nym trybem. Biopsja potwierdza dia-
gnoz´ raka piersi. Ordynuje si´ zabieg
chirurgiczny uzupe∏niony radio- i che-
mioterapià. Tego typu historia cz´sto
koƒczy si´ tragicznie tylko dlatego, ˝e
nowotwór zosta∏ wykryty dopiero
wówczas, gdy spowodowa∏ wystàpie-
nie widocznych objawów.
Wielu ludzi nauczy∏o si´ rozpozna-
waç wczesne objawy raka dzi´ki wska-
zówkom zawartym w programie samo-
kontroli propagowanym przez Ameri-
can Cancer Society. Kiedy jednak wy-
st´pujà objawy – zwykle ból, krwawie-
nie z narzàdu czy te˝ wyczuwalne zgru-
bienie – nowotwory cz´sto majà ju˝ ca∏-
kiem znaczne rozmiary. Pomimo za-
biegu chirurgicznego, polegajàcego na
usuni´ciu guza, wiele zaawansowanych
postaci raka ulega wznowie lub staje si´
êród∏em przerzutów, co mo˝e dopro-
wadziç do zgonu pacjenta. Natomiast
nowotwory we wczesnych stadiach ma-
jà mniejsze mo˝liwoÊci rozsiania i z
wi´kszym prawdopodobieƒstwem mo-
gà zostaç ca∏kowicie usuni´te.
Dokonujàca si´ rewolucja w biologii
molekularnej i w naszym rozumieniu ge-
netyki nowotworów przyczyni∏a si´ do
opracowania serii obiecujàcych testów
umo˝liwiajàcych zarówno ocen´ ryzyka
zachorowania danej osoby, jak i wykry-
cie raka we wczesnym stadium, kiedy za-
bieg chirurgiczny jest w pe∏ni skuteczny.
Dzi´ki nowym strategiom opracowuje
si´ najlepsze dla danego pacjenta formy
chemioterapii oraz ustala prawdopo-
dobieƒstwo nawrotu nowotworu po za-
biegu chirurgicznym. W miejsce metod
inwazyjnych (biopsji) wprowadza si´ te-
sty, które mogà byç przeprowadzone na
ma∏ej próbce moczu lub kropli krwi.
Mimo ˝e od d∏u˝szego czasu wielkim
zainteresowaniem cieszà si´ nowe spo-
soby leczenia, takie jak terapia genowa,
wielu z nas wierzy, ˝e w nadchodzàcych
latach najwi´cej istnieƒ ludzkich uratuje
wczesne wykrywanie oraz wprowa-
dzenie systematycznych badaƒ kontrol-
nych, co umo˝liwi zastosowanie ju˝ ist-
niejàcych metod terapeutycznych we
w∏aÊciwym momencie.
Dziedzictwo genetyczne
Tak jak w przypadku wielu innych
chorób sk∏onnoÊç do zachorowania na
dany nowotwór mo˝e byç dziedziczna.
Mutacje w specyficznych genach prze-
kazanych dzieciom przez rodziców de-
terminujà podatnoÊç na liczne nowo-
twory, na przyk∏ad raka piersi, jelita
grubego, czerniaki oraz inne, rzadsze
ich rodzaje. Obecnie opracowuje si´ pro-
ste testy przeprowadzane na próbce
krwi, które umo˝liwiajà znalezienie mu-
tacji w dwóch znanych genach podat-
noÊci na raka piersi (BRCA1 i BRCA2).
Pomogà one oceniç ryzyko wczesnego
wystàpienia tego nowotworu. JeÊli ko-
bieta jest nosicielkà mutacji w którymÊ
z tych genów, musi si´ liczyç z wi´k-
szym ryzykiem (choç nie pewnoÊcià)
rozwoju raka piersi, zwykle przed 40
rokiem ˝ycia. (M´˝czyêni z takimi mu-
tacjami sà równie˝ bardziej zagro˝eni
rakiem piersi i prawdopodobnie rakiem
prostaty.)
JeÊli natomiast kobieta nie ma takich
mutacji, ryzyko wystàpienia u niej raka
piersi nie powinno byç wy˝sze ni˝ w ca-
∏ej populacji (choruje jedna na osiem
kobiet w USA). Testy te pozwolà leka-
rzom na uwa˝niejszà obserwacj´ cz∏on-
ków rodzin obcià˝onych genetycznie. A
rozpocz´te wczeÊniej badania kontrolne
za pomocà mammografii lub innych kon-
wencjonalnych metod diagnostycznych
pomogà wtedy w wykryciu raka we
wczesnym stadium. Poniewa˝ niewielki
odsetek nowotworów, jak sàdzimy, ma
pod∏o˝e dziedziczne (oko∏o 10%), testy
majà wi´c wartoÊç w przypadku rodzin
o zwi´kszonym ryzyku zachorowania
na raka. Poza dost´pnymi ju˝ testami
genetycznymi wykrywajàcymi predys-
pozycje do raka piersi opracowano rów-
nie˝ inne, na przyk∏ad podatnoÊci na ra-
ka jelita grubego.
Wraz z mo˝liwoÊcià okreÊlenia osob-
niczego ryzyka zachorowania na raka
na dziesi´ciolecia przed prawdopodob-
nym wystàpieniem choroby pojawi∏o
si´ wiele kwestii natury spo∏ecznej i psy-
Post´py
w wykrywaniu raka
Testy genetyczne pomogà uratowaç
wi´cej istnieƒ ludzich ni˝ nowa generacja leków
David Sidransky
ELI REICHMAN

Â
WIAT
N
AUKI
Listopad 1996 75
chologicznej. Ustawodawcy rozpocz´li
ju˝ prac´ nad przepisami prawnymi za-
pobiegajàcymi dyskryminacji osób,
które majà takie zmutowane geny, przez
firmy ubezpieczeniowe. ÂwiadomoÊç
dziedzictwa genetycznego mo˝e staç si´
du˝ym obcià˝eniem psychicznym, za-
równo dla obarczonego nim cz∏owieka,
jak i jego rodziny. Nawet krewni, któ-
rzy nie sà nosicielami takich mutacji,
doÊwiadczajà poczucia winy [ramka na
stronie 77].
Zanim testy wejdà do powszechnej
praktyki, oprócz problemów natury
spo∏ecznej trzeba b´dzie pokonaç wie-
le przeszkód technicznych. Pomimo
du˝ego post´pu w technikach gene-
tycznych opracowanie w pe∏ni wia-
rygodnych testów wykrywajàcych wszy-
stkie mutacje zwiàzane z procesem no-
wotworzenia ciàgle jeszcze jest wyzwa-
niem dla naukowców. JeÊli test nie b´-
dzie wykrywa∏ mutacji, niektóre przy-
padki nie zostanà zauwa˝one. Ka˝dy
nowo opracowany test musi byç nie tyl-
ko dok∏adny, lecz tak˝e ma pomóc w
zwi´kszaniu szansy prze˝ycia. Do-
tychczas nie uda∏o si´ tego osiàgnàç.
Niektórzy krytycy twierdzà, ˝e cz´ste
badania kontrolne podejmowane po
stwierdzeniu dodatniego wyniku testu
– na przyk∏ad rutynowa mammografia
– nie zawsze prowadzi do wykrycia no-
wotworu wystarczajàco wczeÊnie, by
zwi´kszyç szanse chorego na wylecze-
nie. Jednak dane pochodzàce z badaƒ
rodzin obcià˝onych zwi´kszonym ry-
zykiem nowotworu jelita grubego do-
wodzà, ˝e Êcis∏y nadzór i podawanie
zwiàzków chemicznych zapobiegajà-
cych nowotworom, a w niektórych wy-
padkach usuni´cie jelita grubego, mogà
znacznie zmniejszyç umieralnoÊç.
Okazuje si´, ˝e usuni´cie narzàdu ta-
kiego jak jelito grube czy pierÊ nie za-
wsze jest post´powaniem wystarczajà-
co zapobiegawczym. Po mastektomii
mo˝e pozostaç cz´Êç tkanki nowotworo-
wej sutka, chocia˝ prawdopodobieƒ-
stwo nawrotu choroby jest mniejsze.
Niedoskona∏oÊç testów oceniajàcych po-
datnoÊç na chorob´ nowotworowà
uzmys∏awia potrzeb´ opracowania lep-
szych strategii wczeÊniejszego wykry-
wania nowotworu – w stadium, gdy jest
ca∏kiem ma∏y lub gdy dopiero zaczyna
nabieraç cech nowotworu z∏oÊliwego.
Lepsze sposoby wykrywania powinny
pomóc nie tylko rodzinom z wrodzonà
podatnoÊcià na choroby nowotworowe,
ale i ca∏ej populacji.
Niezale˝nie od tego, czy zmiany gene-
tyczne sà wrodzone, jak w rakach rodzin-
nych, czy nabyte, nowotwór jest zawsze
wynikiem uszkodzeƒ w DNA – noÊniku
informacji genetycznej. Zanim komórki
stanà si´ agresywnie z∏oÊliwe – tzn. dzie-
làc si´ w sposób nie kontrolowany, za-
cznà naciekaç inne tkanki i dokonywaç
przerzutów – muszà doznaç uszkodzeƒ
w wielu genach zwiàzanych z nowotwo-
rami [patrz: Robert A. Weinberg, „Jak po-
wstaje rak?”, strona 32].
Sondy molekularne
Dzi´ki coraz lepszemu rozumieniu
przyczyn i rozwoju tej choroby wiemy
ju˝, ˝e niewielkie zgrupowania komó-
rek przednowotworowych (ciàgle jesz-
cze uwa˝anych za ∏agodne, ale zmie-
rzajàce do zrakowacenia), jak równie˝
komórki wczesnych postaci nowotwo-
ru cz´sto majà ju˝ ∏atwo wykrywalne
zmiany genetyczne. Mo˝e to byç pod-
stawà do opracowania nowego rodza-
ju testów.
Stosowane obecnie analizy cytologicz-
ne – na przyk∏ad badanie pod mikro-
skopem rozmazu metodà Papanicolau
– cz´sto nie wystarczajà do zidentyfiko-
wania niewielkiej grupy zmienionych
komórek jedynie na podstawie ich
kszta∏tu i wielkoÊci. Natomiast dzi´ki
analizie DNA mo˝na wykryç nieliczne
zmutowane komórki, które z∏uszczy∏y
si´ z wczesnej postaci nowotworu do
p∏ynów ustrojowych, takich jak mocz,
plwocina czy nawet wydzielina z bro-
dawki piersiowej. Metoda zwana ∏aƒ-
cuchowà reakcjà polimerazy (PCR – po-
lymerase chain reaction) pozwala na
utworzenie ponad miliona kopii frag-
mentu pojedynczej nici DNA obecnego
w komórce przednowotworowej lub no-
wotworowej. Ta technologia „moleku-
larnego namna˝ania” pozwala na prze-
prowadzenie testu z próbkà tak ma∏à
jak kropla p∏ynu ustrojowego.
Powielonego w ten sposób DNA u˝y-
wa si´ nast´pnie do hybrydyzacji: tzn.
po rozdzieleniu jego nici dodaje sond´
genetycznà, którà jest równie˝ jednoni-
ciowy DNA, zawierajàcy mutacj´ cha-
rakterystycznà dla komórek danego ty-
pu nowotworu. Ka˝dy DNA z próbki
p∏ynu ustrojowego, który ma takà samà
mutacj´, zwià˝e si´ (zhybrydyzuje) z son-
dà oznakowanà barwnikiem fluorescen-
cyjnym lub materia∏em radioaktywnym
[ramka na stronach 78-79].
Wiele z analiz DNA majàcych na ce-
lu wykrywanie nowotworów wykona-
no w moim laboratorium w Johns Hop-
kins University School of Medicine.
Stosujàc metody molekularne, wraz z ko-
legami wykry∏em mutacje genetyczne
charakterystyczne dla raka p∏uca w ko-
mórkach znajdowanych w plwocinie, dla
raka p´cherza – wyst´pujàcych w mo-
czu i dla raka jelita grubego – w kale. Kil-
ka lat temu nasz zespó∏ wykaza∏ mu-
tacje w onkogenie ras w komórkach
obecnych w kale pacjentów z polipami
jelita grubego (naroÊlami b´dàcymi pre-
kursorami raka). Mutacje takie zna-
jdowano tak˝e u pacjentów z rakiem
jelita grubego.
Obserwacje te doprowadzi∏y do za-
krojonych na szerszà skal´ prób klinicz-
nych, których celem jest okreÊlenie, czy
identyfikacja mutacji w genie ras w ka-
le mo˝e staç si´ podstawowà strategià
badaƒ przesiewowych. Test taki pozwa-
la∏by na wykrycie polipa, zanim uwi-
doczni go kolonoskopia (badanie jelita
za pomocà wziernika). Usuni´cie polipa
znacznie zmniejszy∏oby ryzyko rozwo-
ju nowotworu u pacjenta.
Test wykrywajàcy mutacje w genie
ras zapewne stanie si´ rutynà w labora-
toriach medycznych w ciàgu kilku naj-
bli˝szych lat. Jednak˝e taki rodzaj ana-
lizy genetycznej mo˝e okazaç si´ zbyt
d∏ugotrwa∏y i kosztowny przy poszu-
kiwaniu wielu mutacji, które zdarzajà
si´ w niektórych genach. ˚eby znaleêç
poszczególne mutacje, trzeba bowiem
u˝ywaç oddzielnych sond. Inne pode-
jÊcie, pozwalajàce na znalezienie komó-
rek nowotworowych, opiera si´ na fak-
cie, ˝e w DNA istniejà powtarzajàce si´
sekwencje, zwane mikrosatelitami. Po-
niewa˝ nie niosà one ˝adnych niezb´d-
nych komórce informacji, czasami na-
PODATNOÂå NA NOWOTWORY daje si´
czasami wykryç dzi´ki testom genetycznym.
Naukowcy z Johns Hopkins University
School of Medicine szukajà wÊród genów
rodziny Lueder z Omaha (Nebraska) mutacji
w szczególny sposób zwiàzanej z rakiem
jelita grubego, a byç mo˝e tak˝e z rakami
dróg moczowych. Geny te zlokalizowane sà
na trzech ró˝nych chromosomach (kolor
szary widoczny na diagramie).
CHROMOSOM 2
CHROMOSOM 3
CHROMOSOM 7
TOMO NARASHIMA
zywane sà „Êmieciowym DNA”. Sek-
wencje mikrosatelitarne sà jednak nie-
zwykle cenne dla diagnostyków nowo-
tworowych, a tak˝e dla specjalistów me-
dycyny sàdowej, którzy na ich podsta-
wie opracowali metody zwane „zdejmo-
waniem odcisków palców” DNA (DNA
fingerprinting) – te same, które wzbu-
dzi∏y tak ogromne emocje podczas pro-
cesu O. J. Simpsona.
Sekwencje mikrosatelitarne rozpro-
szone w DNA ka˝dego chromosomu
powoli udowadniajà swojà wartoÊç
w diagnostyce nowotworowej. Nieobec-
noÊç jakiegoÊ zgrupowania sekwencji
mikrosatelitarnych Êwiadczy o delecji
(wypadni´ciu) danego regionu chromo-
somu. Inna jego wielkoÊç tak˝e jest
oznakà zmian genetycznych.
Podczas jednej ze wst´pnych prób kli-
nicznych przeprowadzonych na ma∏à
skal´ w Johns Hopkins University
School of Medicine szukaliÊmy zmian
w sekwencjach mikrosatelitarnych DNA
wyizolowanego z komórek zawartych
w moczu pacjentów podejrzanych o ra-
ka p´cherza. ZnaleêliÊmy je dzi´ki po-
równaniu DNA wykrytego w moczu
z DNA krwi. Komórki raka p´cherza
z∏uszczajà si´ do moczu, nie przedosta-
jà si´ natomiast do krwi. Badanie krwi
jest wi´c w takim eksperymencie próbà
kontrolnà.
U 19 z 20 pacjentów znaleêliÊmy zmia-
ny w mikrosatelitarnym DNA, wskazu-
jàce na brak ca∏ego regionu chromoso-
mu. Wykryto je tak˝e w DNA izolo-
wanym z biopsji nowotworu tych pa-
cjentów. U ludzi, którzy nie byli chorzy
na raka, nie znaleêliÊmy ˝adnych niepra-
wid∏owoÊci w sekwencjach mikrosateli-
tarnych. Chocia˝ test zawiód∏ w jednym
przypadku, 95-procentowy wspó∏czyn-
nik wykrywalnoÊci wypada korzystnie
w porównaniu z wynikami uzyskiwa-
nymi w mniej skomplikowanej technice
diagnostycznej – rozmazie cytologicz-
nym metodà Papanicolau w przypadku
raka szyjki macicy.
Prostota i niewielkie koszty testu mi-
krosatelitarnego stanowià o jego prze-
wadze nad testem wykrywajàcym mu-
tacje specyficzne, takie jak na przyk∏ad
w genie ras. W praktyce testowanie mi-
krosatelitów mo˝e byç w pe∏ni zauto-
matyzowane; technik b´dzie potrzebo-
wa∏ jedynie kropli moczu i krwi. Po
naciÊni´ciu guzika aparat do PCR po-
wieli DNA z próbek moczu, by znaleêç
wzór mikrosatelitarny Êwiadczàcy o
obecnoÊci komórek raka p´cherza. Obe-
cnie przeprowadzana jest du˝a próba
kliniczna majàca potwierdziç nasze
wst´pne wyniki. Pozostaje jednak do
sprawdzenia, czy badanie mikrosateli-
tów oka˝e si´ metodà wystarczajàco
skutecznà przy wykrywaniu innych ty-
pów nowotworów.
Odmienna strategia wczesnego wy-
krywania nowotworów koncentruje si´
na monitorowaniu poziomu bia∏ek, któ-
re sà albo produktem zmutowanego ge-
nu, albo konsekwencjà unikalnej bio-
chemii komórki nowotworowej. Jako
przyk∏ad mo˝na podaç znajdowane we
krwi chorego na raka prostaty bia∏ko PSA
(prostate-specific antigen) [patrz: Ge-
rald E. Hanks i Peter T. Scardino, „Rak
prostaty: czy badania przesiewowe ma-
jà sens?”, strona 83]. Test na PSA odgry-
wa istotnà rol´ w monitorowaniu roz-
woju raka prostaty: wysoki poziom tego
bia∏ka Êwiadczy o nawrocie nowotwo-
ru, lecz mo˝e byç te˝ dobrym narz´-
dziem wczesnego diagnozowania. Wie-
lu lekarzy zacz´∏o go stosowaç w celu
wykrycia raka prostaty.
Markery enzymatyczne
Niezwykle obiecujàcy z punktu wi-
dzenia wykrywania i badaƒ kontrolnych
wydaje si´ prosty test bia∏kowy poszu-
kujàcy aktywnoÊci enzymu zwanego te-
lomerazà. Telomeraza jest zaanga˝owa-
na w odtwarzanie telomerów, seg-
mentów na koƒcu chromosomów, któ-
re przy ka˝dym podziale komórki ule-
gajà skróceniu. Skrócenie telomerów po-
ni˝ej pewnej okreÊlonej d∏ugoÊci sta-
nowi dla komórki sygna∏ do samoza-
g∏ady. Mechanizm ten prawdopodob-
nie umo˝liwia organizmowi eliminacj´
starzejàcych si´ komórek. W wi´kszo-
Êci normalnych komórek nie ma telo-
merazy. W komórkach nowotworowych
jest ona aktywna i przeciwdzia∏a skraca-
niu telomerów. W konsekwencji komór-
ki nowotworowe nie obumierajà.
Poniewa˝ enzym ten rzadko wyst´-
puje w komórkach normalnych, mo˝e
s∏u˝yç jako marker sygnalizujàcy obec-
noÊç komórek nowotworowych. Teore-
tycznie badanie przesiewowe na obec-
noÊç telomerazy mo˝e si´ okazaç ogólnà
strategià wykrywania wszelkich komó-
rek nowotworowych w p∏ynach ustro-
jowych i tkankach. Firma Geron z Men-
lo Park (Kalifornia) rozpocz´∏a opraco-
wywanie testu na aktywnoÊç telomerazo-
wà, opierajàc si´ na badaniach Jerry’ego
W. Shaya z University of Texas South-
western Medical Center i Carol Greider
z Cold Spring Harbor Laboratory.
Obecnie prace nad testami bia∏kowy-
mi sà bardziej zaawansowane ni˝
76 Â
WIAT
N
AUKI
Listopad 1996
WCZESNE WYKRYWANIE
Niektóre zespo∏y rodzinnych nowotworów
MARIA SUTTON
Zespó∏*
Nowotwory
Gen
Koszt testu**
Czerniaki Czerniak, MTS1/p16
400–600
dolarów
rodzinne
trzustki
(supresor transformacji
nowotworowej)
Dziedziczny
Piersi, jajnika
BRCA 1
400–2000 dolarów
rak piersi
i inne
(supresor transformacji
i jajnika
nowotworowej)
Dziedziczny
Piersi i inne
BRCA 2
400–2000 dolarów
rak piersi
(supresor transformacji
nowotworowej)
Rak jelita grubego
Jelita grubego,
MSH2, MLH1,
400–2000 dolarów
na pod∏o˝u
macicy i inne
PMS1 i PMS2
niepolipowatoÊci
(supresory transformacji
nowotworowej)
Li-Fraumeni
Mózgu, mi´saki
p53
500–700 dolarów
i inne
(supresor transformacji
nowotworowej)
Zespó∏
Rdzeniasty rak
RET
350–500 dolarów
nowotworów
tarczycy i inne
(onkogen)
w uk∏adzie
dokrewnym
* Zespó∏ mo˝e zawieraç kilka typów nowotworów
** Koszty zale˝à od liczby potrzebnych testów

poszukiwania markerów genetycznych.
Wiele z tych testów nie spe∏ni∏o jednak
pok∏adanych w nich nadziei, gdy˝ zbyt
cz´sto dajà one fa∏szywe wyniki. Dlate-
go ostatnio po∏o˝ono nacisk na procesy
zachodzàce w materiale genetycznym.
Poza wczesnym wykryciem wa˝na
jest równie˝ ocena, jak szybko dany ro-
dzaj nowotworu b´dzie rós∏ i si´ rozsie-
wa∏. Ocena ta – nazywana stopniem kli-
nicznego zaawansowania (staging) – jest
czynnikiem decydujàcym przy okreÊla-
niu, jakiemu rodzajowi terapii zostanie
poddany pacjent po wykonaniu zabie-
gu chirurgicznego – napromienianiu czy
chemioterapii. Przed podj´ciem decyzji
lekarze badajà fragmenty tkanki w ce-
lu sprawdzenia, czy ca∏y guz zosta∏ usu-
ni´ty. Poniewa˝ komórki nowotworo-
we mogà tak˝e naciekaç najbli˝sze
w´z∏y ch∏onne, okreÊlenie stopnia kli-
nicznego zaawansowania raka wyma-
ga ustalenia liczby zaj´tych w´z∏ów.
Lekarze od dawna zdawali sobie
spraw´, ˝e standardowe podejÊcie do
okreÊlania stopnia klinicznego zaawan-
sowania, czyli identyfikacji zmienionych
komórek pod mikroskopem Êwietlnym,
cz´sto nie pozwala wykryç niewielkich
grup komórek nowotworowych. Ostat-
Â
WIAT
N
AUKI
Listopad 1996 77
M
o˝liwoÊç odnalezienia wrodzonych mutacji genetycznych,
zwi´kszajàcych predyspozycje osobnicze do zachorowania
na raka, wywo∏a∏a burzliwe dyskusje w Êrodowisku medycznym.
W latach osiemdziesiàtych naukowcy zidentyfikowali pierwszy
marker podatnoÊci na raka, czyli mutacj´ genowà, która jest przy-
czynà siatkówczaka (retinoblastoma) – nowotworu oka. Dopiero
jednak odkrycie w pierwszej po∏owie lat dziewi´çdziesiàtych ge-
nów zaanga˝owanych w powstawanie raka piersi – i nast´pnie
opracowanie testów okreÊlajàcych stopieƒ podatnoÊci na t´ cho-
rob´ – podda∏y ten problem pod publicznà dyskusj´. Znaczenie wy-
krycia genów podatnoÊci na raka piersi nie dotyczy wy∏àcznie tej
choroby, poniewa˝ predysponujà one zarówno m´˝czyzn, jak
i kobiety do ró˝nych innych nowotworów, od raka jajnika do (praw-
dopodobnie) raka prostaty.
WàtpliwoÊci zarówno etyków, jak i lekarzy koncentrujà si´ wo-
kó∏ niejednoznacznej wartoÊci testów. JeÊli test wyka˝e obecnoÊç
mutacji genetycznej u kobiety, której krewni chorowali na raka
piersi, ryzyko, ale nie pewnoÊç, wystàpienia choroby wynosi 85%.
Jednak˝e w przypadku kobiet, których ˝adni krewni nie chorowa-
li na raka piersi, jest ono nieznane.
Przeprowadziwszy testy, kobieta nadal stoi wobec trudnej decy-
zji, co robiç dalej. Wynik ujemny wskazujàcy na brak wrodzonego
defektu genetycznego mo˝e daç jej nieuzasadnione poczucie bez-
pieczeƒstwa. Poniewa˝ 85% nowotworów nie ma pod∏o˝a dzie-
dzicznego, grozi jej nadal zachorowanie na niedziedziczne typy te-
go nowotworu. Mo˝e mieç tak˝e wrodzonà mutacj´, która prowadzi
do choroby, a nie zosta∏a jeszcze zidentyfikowana przez badaczy.
Dodatni wynik testu równie˝ nie jest jednoznaczny. Zwi´ksze-
nie cz´stoÊci badaƒ kontrolnych mo˝e bowiem nie wystarczaç:
badanie mammograficzne nie zawsze wykrywa raka. Profilaktyczne
usuni´cie obu piersi te˝ nie daje gwarancji, ˝e nowotwór nie roz-
winie si´ w tkance pozostawionej po zabiegu chirurgicznym.
Krytyków testu niepokoi mo˝liwoÊç wykorzystania takich infor-
macji przez firmy ubezpieczeniowe i przez pracodawców. W kil-
ku stanach wydano ju˝ ustawy zapobiegajàce pos∏ugiwaniu si´ da-
nymi genetycznymi i dyskryminacji pacjenta przy ubezpieczeniach
zdrowotnych. Co wi´cej, podobna ustawa przeprowadzana jest
obecnie w Kongresie USA. Dopóki niektóre z tych problemów nie
zostanà rozwiàzane, National Breast Cancer Coalition, American
Society of Human Genetics i National Advisory Council for Hu-
man Genome Research zalecajà, aby testy te stosowano jedy-
nie w prowadzonych ju˝ badaniach naukowych.
Run na przeprowadzanie takich testów poza oÊrodkami ba-
dawczymi ju˝ si´ jednak rozpoczà∏. Jedna z klinik – Genetics and
I.V.F. Institute w Fairfax (Wirginia), kierowana przez Josepha H.
Ullmana – oferuje test na mutacj´ wyst´pujàcà ze zwi´kszonà
cz´stoÊcià wÊród ˚ydówek aszkenazyjskich. Dwie firmy – Myriad
Genetics i OncorMed – opracowa∏y bardziej wszechstronne te-
sty, wykrywajàce wi´kszà liczb´ mutacji w obu znanych genach
podatnoÊci na raka piersi – BRCA1 i BRCA2. Oczekuje si´, ˝e
wejdà one do praktyki klinicznej w ciàgu najbli˝szych kilku lat.
Opór Êrodowiska lekarskiego wobec takich testów przepro-
wadzanych w klinikach nie tylko w ramach badaƒ naukowych za-
czyna s∏abnàç. W majowym numerze Journal of Clinical Oncolo-
gy
American Society of Clinical Oncology wy∏ama∏o si´ z szeregu
zalecajàc, aby testy takie by∏y dost´pne dla ka˝dego, w którego
rodzinie wystàpi∏y przypadki raka piersi. Zwolennicy testów sà
przekonani, ˝e ignorowanie dost´pnych danych o obcià˝eniu ge-
netycznym zwi´ksza zagro˝enie pacjenta. Ich zdaniem dwuznacz-
noÊci i niepokoje towarzyszàce tej metodzie mo˝na usunàç dzi´-
ki w∏aÊciwemu doradztwu. David Sidransky, autor powy˝szego
artyku∏u, podziela ten poglàd. Jako pracownik Johns Hopkins Uni-
versity School of Medicine i doradca naukowy OncorMed pod-
kreÊla, ˝e nawet bez sprawdzenia genetycznej podatnoÊci na
choroby nowotworowe ciàg∏a kontrola pacjentów o wysokim ry-
zyku zachorowania na raka jelita grubego doprowadzi∏a do znacz-
nego obni˝enia umieralnoÊci na t´ chorob´.
Sidransky doradza, aby kobiety, u których stwierdzono wy-
st´powanie mutacji w genach podatnoÊci na raka piersi, poddawa∏y
si´ systematycznym badaniom kontrolnym oraz by spoÊród nich
wybierano osoby uczestniczàce w próbach klinicznych nowych
zwiàzków chemioprofilaktycznych. Przyznaje, ˝e ÊwiadomoÊç
wyst´powania mutacji jest dla pacjentki i jej rodziny silnym stresem.
Jednak˝e jego zdaniem jest to problem „bez porównania mniej-
szy ni˝ groêba zachorowania na raka piersi i Êmierç z powodu
przerzutów”.
Inni zainteresowani nie podzielajà pewnoÊci Sidransky’ego.
Francis S. Collins, który prowadzi National Center for Human Ge-
nome Research, by∏ jednym ze wspó∏autorów repliki skierowanej
do Journal of Clinical Oncology. „JesteÊmy zaniepokojeni – g∏osi
oÊwiadczenie – ˝e mo˝liwoÊç stwierdzenia dziedzicznej podatnoÊci
na nowotwory, jakà dajà testy, nie idzie w parze z mo˝liwoÊcià
zaproponowania pacjentom zarówno najlepszego rodzaju tera-
pii, jak doradztwa i edukacji u∏atwiajàcych podj´cie decyzji ˝ycio-
wych oraz ochron´ przed ró˝nymi formami dyskryminacji.” Col-
lins przedstawi∏ t´ opini´ w imieniu rzàdowo-prywatnej organizacji
National Action Plan on Breast Cancer.
Collins radzi wszystkim, którzy chcà poznaç swoje dziedzictwo
genetyczne, by wzi´li udzia∏ w badaniach organizowanych
przez Narodowà Sieç Genetyki Nowotworów (National Cancer
Genetics Network) powsta∏à niedawno przy National Cancer In-
stitute. Uczestniczàc w takich badaniach dowiedzà si´ o swoich
ewentualnych obcià˝eniach dziedzicznych. Sieç ta pomaga pacjen-
tom i ich lekarzom radziç sobie z wyjàtkowo trudnym proble-
mem – ÊwiadomoÊcià, ˝e ma si´ groênà mutacj´
genetycznà.
Gary Stix
Czy za wczeÊnie na testy genetyczne?
BRCA1
CHROMOSOM 17
TOMO NARASHIMA

nio nasz zespó∏ z Johns Hopkins wyko-
rzysta∏ technologi´ molekularnà do wy-
szukiwania niewykrywalnych klasycz-
nymi metodami komórek nowotworo-
wych u pacjentów z rakiem g∏oÊni
oraz innymi nowotworami g∏owy i szyi.
Pomimo radykalnych zabiegów chirur-
gicznych guzy te cz´sto ulegajà wzno-
wie w tym samym miejscu. W pilota˝o-
wym eksperymencie przebadaliÊmy
pacjentów, których komórki nowotwo-
rowe nosi∏y mutacje w genie p53. Pro-
dukt prawid∏owego genu p53, zwane-
go tak˝e genem supresorowym, hamuje
nie kontrolowany rozrost komórek; gdy
gen ulega mutacji, komórka wchodzi na
drog´ transformacji nowotworowej.
SkonstruowaliÊmy sond´ molekular-
nà dla p53, której u˝yliÊmy do badania
w´z∏ów ch∏onnych i tkanki sàsiadujàcej
z guzem po rzekomo ca∏kowitym jego
usuni´ciu. W ponad po∏owie przypad-
ków stwierdziliÊmy, ˝e co najmniej je-
den obszar tkanki otaczajàcej nowotwór
– choç badanie mikroskopowe nie wy-
kazywa∏o zmian – zawiera komórki nio-
sàce t´ samà mutacj´ w genie p53 co
usuni´ty guz. Komórki nowotworowe,
rozproszone w tkance otaczajàcej w´-
z∏y ch∏onne, pozosta∏y pomimo chirur-
gicznego usuni´cia guza pierwotnego.
U pacjentów, u których test na muta-
cje w p53 wypad∏ dodatnio, cz´sto ob-
serwowaliÊmy wznow´ w tym samym
obszarze, gdzie uprzednio wykazano
obecnoÊç komórek nowotworowych. Na-
tomiast w grupie pacjentów, u których
po zabiegu chirurgicznym test wypad∏
ujemnie – nie zaobserwowano ˝adnego
przypadku choroby. Inni badacze tak˝e
zidentyfikowali te mutacje w w´z∏ach
ch∏onnych pacjentów z rakiem jelita.
Marker molekularny taki jak gen p53
mo˝e równie˝ s∏u˝yç do oceny reakcji
organizmu na ró˝ne formy chemiotera-
pii. Prawid∏owà funkcjà produktu genu
p53 jest wykrycie uszkodzeƒ genetycz-
nych i uruchomienie procesów napraw-
czych. Gdy uszkodzenia sà zbyt powa˝-
ne, produkt genu p53 wymusza na ko-
mórce Êmierç samobójczà (apoptoz´).
Wiele rodzajów chemioterapii powodu-
je powa˝ne uszkodzenia w materiale ge-
netycznym komórki, co zwykle induku-
je apoptoz´ zale˝nà od p53. Jednak taki
nowotwór, w którym gen p53 uleg∏ de-
lecji lub produkt zmutowanego genu jest
nieaktywny, mo˝e nie reagowaç na pew-
ne formy konwencjonalnej chemiotera-
pii. W raku piersi rozwa˝ane sà obecnie
inne rodzaje chemioterapii, na przyk∏ad
wykorzystujàca taksol. U pacjentów, któ-
rych komórki nowotworowe nie zawie-
rajà funkcjonalnego p53, zwiàzek ten
doprowadza do ich Êmierci przez apop-
toz´ w inny sposób.
Aby wykorzystaç w pe∏ni potencja∏
zawarty w genetycznych metodach
wykrywania i nadzorowania, nie wy-
starczy jedynie wykazaç obecnoÊci zmu-
towanego genu. Trzeba ponadto od-
naleêç miejsce tej niewielkiej kolonii
komórek zmienionych nowotworowo,
aby mo˝na je by∏o wszystkie usunàç.
Post´p w technikach obrazowania – za
pomocà rezonansu magnetycznego lub
tomografii komputerowej – powinien
pomóc w wykryciu zmian patologicz-
nych. Przy badaniu pacjenta metody te
mogà byç uzupe∏nione „obrazowaniem
biologicznym”. Sà to techniki, które
78 Â
WIAT
N
AUKI
Listopad 1996
WCZESNE WYKRYWANIE
Diagnoza postawiona Hubertowi H.
Humphreyowi 27 lat po jego Êmierci
Wyjàtek z listu Muriel Humphrey Brown,
wdowy po Hubercie H. Humphreyu, w którym wyrazi∏a
zgod´, by Johns Hopkins Medical Center wykorzysta∏
próbki tkanek jej zmar∏ego m´˝a do celów medycznych.
Ta decyzja, jak powiedzia∏a,
jest na pewno zgodna z jego wolà.
„Wierz´, ˝e Hubert chcia∏by w∏aÊnie tego; to trzyma∏o go
przy ˝yciu, chcieliÊmy, aby te próbki zosta∏y zachowane po to,
by mo˝na je by∏o zbadaç w przyszloÊci. Wraz z Hubertem
wyznawaliÊmy filozofi´, która pomog∏a nam przetrwaç ró˝ne
ci´˝kie chwile. PowtarzaliÊmy sobie: «Wszystko, co nas
spotyka, dzieje si´ w dobrym celu.» Cz´sto potrzeba wiele czasu,
by zrozumieç dlaczego. Przez wiele lat ˝alu i gniewu nie
umia∏am pogodziç tej naszej filozofii z jego cierpieniem
i Êmiercià. Byç mo˝e teraz znalaz∏am odpowiedê.”
N
owoczesna diagnostyka molekularna ujawni∏a swà pot´g´ w
1994 roku, gdy w Johns Hopkins University School of Medicine
nasz zespó∏ naukowy zdiagnozowa∏ raka p´cherza na podstawie
próbki moczu Huberta H. Humphreya pobranej 27 lat wczeÊniej. By∏
to klasyczny przypadek choroby nowotworowej potwierdzajàcy potrze-
b´ wczesnego wykrywania raka. W 1967 roku Humphrey zauwa˝y∏
w swoim moczu obecnoÊç krwi. Lekarze przeprowadzili wiele testów,
szukajàc nieprawid∏owych komórek w moczu. Nie potrafili jednak ich
wykryç i jednoznacznie stwierdziç raka. Nie zastosowano wi´c w∏a-
Êciwej terapii. Kilka lat póêniej, w 1976 roku, gdy postawiono prawi-
d∏owà diagnoz´, Humphrey przeszed∏ radioterapi´ i radykalnà chirur-
gi´. Niestety, zmar∏ z powodu nawrotu choroby.
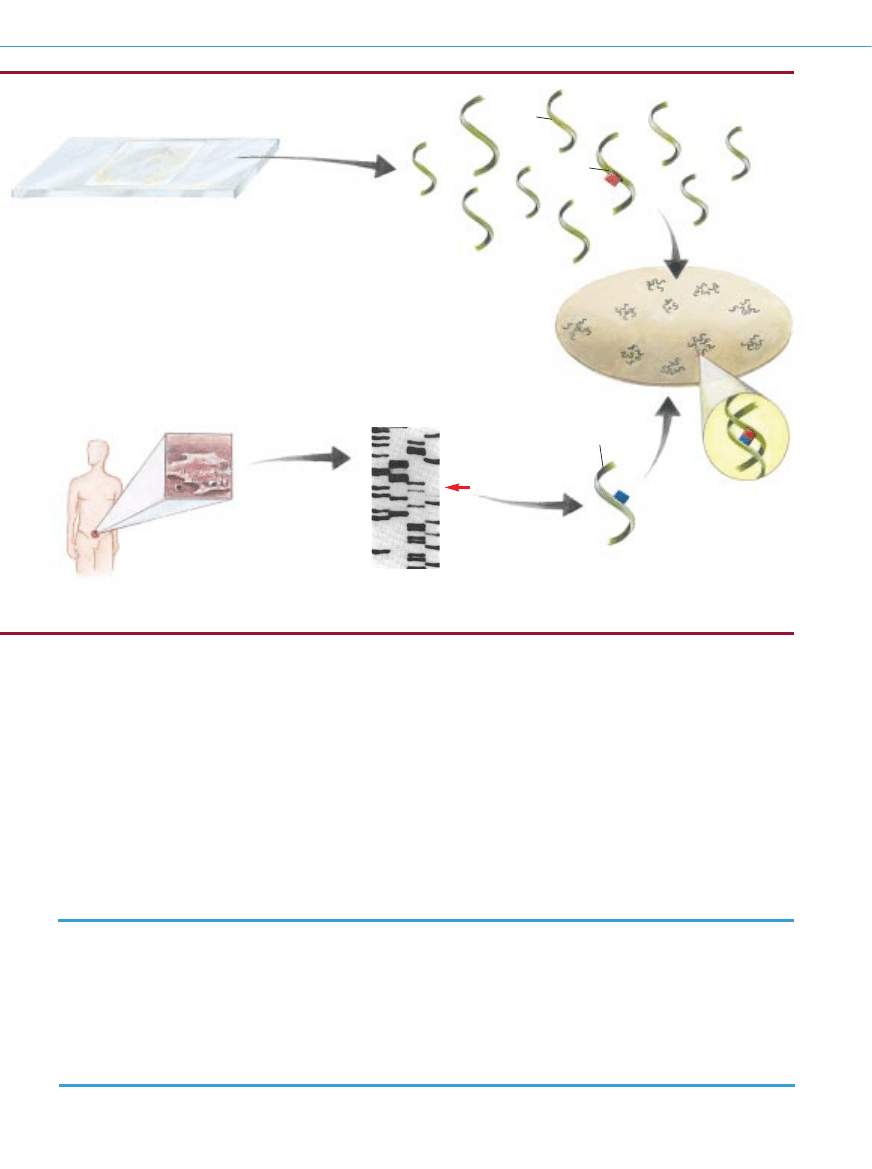
Otrzymawszy od Muriel Humphrey Brown zgod´ na wykorzysta-
nie próbki moczu pobranego w 1967 roku i próbki usuni´tego po la-
tach nowotworu, Ralph H. Hruban, Peter van der Riet, Yener S. Ero-
zan i ja przeprowadziliÊmy eksperyment (diagram obok).
Obecnie wiadomo, ˝e pewne mutacje w genie p53 sà znakiem roz-
poznawczym raka p´cherza. ChcieliÊmy jednak sprawdziç, czy takà
samà mutacj´ da∏oby si´ wykryç wiele lat wczeÊniej w próbce moczu
wiceprezydenta. Aby si´ o tym przekonaç, musieliÊmy najpierw stwier-
dziç obecnoÊç mutacji w guzie (na dole diagramu). Z tkanki nowotwo-
rowej wyekstrahowaliÊmy i namno˝yliÊmy DNA, a nast´pnie okre-
ÊliliÊmy kolejnoÊç nukleotydów fragmentu zawierajàcego gen p53.
Sekwencjonowanie ujawni∏o mutacj´ punktowà – adenina zosta∏a
tam zastàpiona tyminà. Nast´pnie zsyntetyzowaliÊmy jednoniciowà
sond´ rozpoznajàcà DNA z takà samà mutacjà. Sond´ wyznakowa-
no materia∏em radioaktywnym.
Niezale˝nie od tego za pomocà ∏aƒcuchowej reakcji polimerazy
(PCR) otrzymaliÊmy fragmenty kopii DNA genu p53 z próbki moczu
(u góry)
. DNA wprowadziliÊmy do genomu bakterii. Kolonie bakterii
przenieÊliÊmy nast´pnie na nylonowà membran´, a potem rozdzie-
liliÊmy nici DNA, by umo˝liwiç im parowanie z odpowiednià sondà. Gdy
dodaliÊmy sond´, zhybrydyzowa∏a ona z tym fragmentem DNA,
który zawiera∏ mutacj´ (skrajnie z prawej) co Êwiadczy∏o, ˝e w prób-
ce moczu pobranej od Humphreya w 1967 roku rzeczywiÊcie by∏y
komórki nowotworowe.
AP/WIDE WORLD PHOTOS
umo˝liwiajà rejestracj´ promieniowania
pochodzàcego ze specyficznie groma-
dzàcych si´ w komórkach guza nisko-
znakowanych zwiàzków radioaktyw-
nych lub fluorescencyjnych podawa-
nych doustnie.
Pomimo korzyÊci p∏ynàcych z zasto-
sowania diagnostyki molekularnej wi´k-
szoÊç wspomnianych w tym artykule ba-
daƒ ciàgle jeszcze znajduje si´ w stadium
poczàtkowym i czeka na ostatecznà we-
ryfikacj´ w du˝ych próbach klinicznych.
Mam jednak nadziej´, ˝e w ciàgu najbli˝-
szych 5 lat diagnostyka molekularna –
wraz z odpowiednimi strategiami okre-
Êlania stopnia klinicznego zaawansowa-
nia i ustalania w∏aÊciwej terapii – stanie
si´ cz´Êcià rutynowego badania lekar-
skiego wi´kszoÊci ludzi w USA.
Prawdopodobnie nigdy nie b´dziemy
dysponowaç jednym testem pozwalajà-
cym wykryç wszystkie rodzaje nowo-
tworów, ka˝dy bowiem ma swój w∏asny
„podpis molekularny”, a wi´c wymaga
testu opracowanego specjalnie dla nie-
go. Jednak te same zmiany genetyczne,
które prowadzà do powstania raka, mo-
gà si´ okazaç jego najs∏abszym punktem.
Potrafimy ju˝ wyobraziç sobie, ˝e w
przysz∏oÊci niewielka próbka krwi, in-
nych tkanek lub ró˝nych p∏ynów ustro-
jowych b´dzie ujawniaç obecnoÊç nowe-
go lub pochodzàcego z przerzutów no-
wotworu – p∏uca, piersi, jelita lub innych
narzàdów – w czasie umo˝liwiajàcym je-
go ca∏kowite zniszczenie. Czu∏oÊç tych
testów mo˝e znacznie zmieniç nasz
stosunek do chorób nowotworowych.
Zdiagnozowanie raka, zamiast parali˝o-
waç nas ze strachu przed nieuniknionà
tragedià, oznaczaç b´dzie, ˝e choroba
zosta∏a wykryta we wczesnej fazie i
zostanie wyleczona.
T∏umaczyli
Janusz A. Siedlecki i Ma∏gorzata Siedlecka
Â
WIAT
N
AUKI
Listopad 1996 79
Informacja o autorze
DAVID SIDRANSKY pracuje w Johns Hopkins Uni-
versity School of Medicine jako profesor nadzwyczaj-
ny onkologii i otolaryngologii (specjalnoÊç chirurgia
g∏owy i szyi) w zakresie medycyny komórkowej i mo-
lekularnej. Kieruje tak˝e grupà naukowà zajmujàcà si´
nowotworami g∏owy i szyi. Jest równie˝ redaktorem
Predictive Oncology, Clinical Cancer Research i Cancer
Research. Wspó∏pracuje stale z firmà Oncor. Tytu∏ dok-
tora medycyny otrzyma∏ w 1984 roku w Baylor Colle-
ge of Medicine w Houston.
Literatura uzupe∏niajàca
MOLECULAR BIOLOGY AND THE EARLY DETECTION OF CARCINOMA OF THE BLADDER – THE CA-
SE OF HUBERT H. HUMPHREY
. R. H. Hruban, P. van der Riet, Y. S. Erozan i D. Sidran-
sky, New England Journal of Medicine, vol. 330, nr 18, ss. 1276-1278, 5 V 1994.
MOLECULAR SCREENING: HOW LONG CAN WE AFFORD TO WAIT?
David Sidransky, Journal of
the National Cancer Institute, vol. 86, nr 13, ss. 955-956, 6 VII 1994.
DISCOVERY, TRANSFER AND DIFFUSION OF TECHNOLOGIES FOR THE DETECTION OF GENETIC DI-
SORDERS: POLICY IMPLICATIONS.
N. A. Holtzman, International Journal of Technology
Assessment in Health Care, vol. 10, nr 4, ss. 562-572, 1994.
EMOTIONAL AND BEHAVIORAL RESPONSES TO GENETIC TESTING FOR SUSCEPTIBILITY TO CANCER.
Caryn Lerman i Robert T. Croyle, Oncology, vol. 10, nr 2, ss. 191-199, II/1996.
Przygotowanie szkie∏ka z rozmazem z próbki moczu
Huberta Humphreya pobranej w 1967 roku
Powielanie DNA
za pomocà reakcji
∏aƒcuchowej polimerazy
NORMALNY
DNA
ZMUTOWANY
DNA
Przeniesienie DNA
na nylonowà membran´
Sonda wià˝e si´
ze zmutowanym DNA
Sonda dla
zmutowanego DNA
Konstrukcja sondy
do wykrywania
mutacji
˚el wykazujàcy obecnoÊç
mutacji w genie p53
(czerwona strza∏ka)
Oczyszczanie DNA
i zsekwencjonowanie
genu p53
Próbka z nowotworu
pobranego od Humphreya
podczas chirurgicznego
usuni´cia p´cherza w 1976 roku
W podobny sposób opracowuje si´ testy, które w przysz∏oÊci b´dà u˝ywane w oÊrod-
kach klinicznych do wykrywania nowotworów. Odpowiednie sondy rozpoznajàce ko-
mórki nowotworowe mogà byç wykorzystane do badaƒ moczu lub krwi.
Przypadek Humphreya jest najlepszym Êwiadectwem potencja∏u diagnostycznego,
jaki tkwi w podejÊciach molekularnych, gdy zawodzà inne metody diagnostyczne. Wcze-
sne rozpoznanie pozwoli∏oby wykonaç zabieg chirurgiczny na tyle szybko, ˝e uratowa-
∏oby mu to ˝ycie.
Kto wie, czy nie wp∏yn´∏oby to na polityk´ Êwiatowà. Humphrey móg∏ zmieniç wcze-
Êniejszà decyzj´ i przystàpiç do wyborów prezydenckich, które w 1968 roku wygra∏
Richard M. Nixon. – D.S.
JOHNS HOPKINS UNIVERSITY SCHOOL OF MEDICINE
(radiograf)
; JENNIFER CHRISTIANSEN
(rysunki)
Wyszukiwarka
Podobne podstrony:
199611 jak powstaje rak
199611 postepy w leczeniu raka
199611 wczesne wykrywanie
RAK PIERSI WYKRYWANIE CZY OSZUKIWANIE
199611 rak prostaty czy badania
199611 rak w polsce
GMO metody wykrywania 2
epidemiologia, czynniki ryzyka rola pielegniarki rak piersi szkola, nauczyciel
RAK P UC
ZATRUCIA ZASADY POSTĘPOWANIA
Postępowanie u osób nieprzytomnych
rak pecherza
więcej podobnych podstron