
88 Â
WIAT
N
AUKI
Listopad 1996
DOSKONALENIE DZISIEJSZYCH TERAPII
C
z´sto marzymy o wynalezieniu
lekarstwa na raka, tak jakby do-
tkni´ci nim ludzie nigdy nie po-
wracali do zdrowia. Tymczasem znako-
mita wi´kszoÊç z∏oÊliwych nowotworów
skóry i oko∏o po∏owy nowotworów na-
rzàdów wewn´trznych jest dziÊ ca∏ko-
wicie uleczalna. Powszechne w spo∏e-
czeƒstwie pragnienie lekarstwa na raka
to raczej odbicie uzasadnionego nieza-
dowolenia z obecnie stosowanych me-
tod. Cz´sto majà one bowiem tak szko-
dliwe dzia∏ania uboczne, ˝e ca∏kowicie
niweczone sà korzyÊci wynikajàce z le-
czenia. W wielu rodzajach raka metody
te okazujà si´ równie˝ niesku-
teczne. Smutna rze-
czywistoÊç
zmusza wi´c lekarzy do cytowania pa-
cjentom statystyk prze˝ycia w miejsce
solennej obietnicy wyleczenia.
W przysz∏oÊci sytuacja byç mo˝e
zmieni si´ na lepszà. Leki przeciwno-
wotworowe powinny bardziej przypo-
minaç dzia∏aniem antybiotyki przepi-
sywane w przypadku chorób zakaê-
nych, a metody lecznicze stanà si´ bez-
pieczne, skuteczne i wybiórcze; ograni-
czà si´ do komórek nowotworowych
i nie b´dà pociàgaç za sobà dzia∏aƒ
ubocznych. Co najwa˝niejsze, b´dà kon-
sekwentnie przywracaç pacjenta do
pierwotnego stanu zdrowia. Poczynio-
no ju˝ pewne kroki ku stwo-
rzeniu idealnych leków,
lecz realizacja tych am-
bitnych zamierzeƒ wymaga od naukow-
ców g∏´bszego poznania mechanizmów
le˝àcych u pod∏o˝a ró˝nych postaci no-
wotworów z∏oÊliwych.
Obecne sposoby leczenia
Rak nie jest jednà chorobà; mianem
tym okreÊla si´ du˝à grup´ bardzo ró˝-
nych schorzeƒ, które ∏àczà pewne istot-
ne cechy charakterystyczne. Trzy wspól-
ne cechy wszystkich nowotworów z∏o-
Êliwych sà przyczynami ich najbardziej
niszczàcego dzia∏ania. Pierwszà i najbar-
dziej fundamentalnà w∏aÊciwoÊcià tkan-
ki nowotworowej jest jej ciàg∏e powi´k-
szanie si´ (cz´sto w∏aÊnie to powoduje
objawy u pacjenta) dzi´ki zdolnoÊci ko-
mórek nowotworowych do nieskoƒczo-
nej liczby podzia∏ów. Nast´pnà – nacie-
kanie sàsiednich zdrowych tkanek przez
nowotwór, ÊciÊle zwiàzane z tym nie
kontrolowanym podzia∏em i wzrostem
komórek. I w koƒcu – tworzenie prze-
rzutów, najbardziej z∏owieszcza cecha
raka, czyli jego zdolnoÊç do rozprzestrze-
niania si´ w organizmie. Wówczas to ko-
mórki nowotworowe odrywajà si´ od
guza pierwotnego i w´drujà z krwià
w uk∏adzie krà˝enia, docierajàc do od-
leg∏ych miejsc i tworzàc tam kolonie.
Wi´kszoÊç obecnych sposobów leczenia
nowotworów z∏oÊliwych ma na celu
zwalczanie nie kontrolowanego wzro-
stu, naciekania sàsiadujàcych narzàdów
i powstawania przerzutów odleg∏ych.
Najstarszà metodà zwalczania nowo-
tworów z∏oÊliwych i nadal najpowszech-
Post´py
w leczeniu raka
Za pomocà chirurgii, radioterapii i chemioterapii
mo˝na obecnie wyleczyç wiele nowotworów z∏oÊliwych.
Metody przysz∏oÊci b´dà jeszcze skuteczniejsze
Samuel Hellman i Everett E. Vokes
a
b
c
Leczenie nowotworów
promieniowaniem
KLINICZNE AKCELERATORY LINIOWE
dajà wiàzk´ promieniowania rentgenow-
skiego o du˝ym nat´˝eniu. Chocia˝ jej
energia bywa ogromna, te nowoczesne
urzàdzenia majà na tyle zwartà budow´,
˝e bez najmniejszego k∏opotu mo˝na ni-
mi manewrowaç wokó∏ pacjenta.
NAÂWIETLANIE GUZA za pomocà obra-
cajàcego si´ akceleratora liniowego. Zmia-
na toru przejÊcia wiàzki promieni X inten-
syfikuje napromienienie guza i dzi´ki temu
minimalizuje uszkodzenia otaczajàcych
go zdrowych tkanek.
Za zgodà VARIAN ONCOLOGY SYSTEMS
ANDREW CHRISTIE
Slim Films
Â
WIAT
N
AUKI
Listopad 1996 89
niej stosowanà jest operacja. Chirurgicz-
ne usuni´cie guza to metoda zarówno
szybka, jak i skuteczna i w∏aÊnie jej za-
wdzi´czamy najwi´kszà liczb´ wyleczeƒ.
Chirurgia jest tak˝e tà metodà, która da-
je mo˝liwoÊç potwierdzenia, ˝e guz zo-
sta∏ ca∏kowicie wyci´ty: patolog na pod-
stawie ogl´dzin mo˝e bowiem oceniç,
czy wraz z guzem uda∏o si´ usunàç rów-
nie˝ pierwszà warstw´ nie zmienionych
nowotworowo komórek.
Niestety, ten rodzaj terapii ma te˝ kil-
ka istotnych mankamentów. Usuni´cie
masy guza widocznej dla chirurga sa-
mo w sobie nie gwarantuje zlikwido-
wania mikroskopijnych nacieków, tak
charakterystycznych dla nowotworów
z∏oÊliwych. Aby objàç ten inwazyjny
brzeg nowotworu, chirurg musi niekie-
dy wyciàç du˝à cz´Êç zdrowej tkanki.
Mo˝e to powa˝nie wp∏ynàç na funkcjo-
nowanie pacjenta, a tak˝e na jego wy-
glàd. Niekiedy nowotwór atakuje na-
rzàdy niezb´dne do ˝ycia, których nie
sposób usunàç. Nawet gdy operacja jest
wykonalna – rozleg∏e zabiegi (i zwiàza-
ne z tym znieczulenie ogólne) nieod-
∏àcznie traumatyzujà pacjenta. Jednak-
˝e najbardziej istotnym ograniczeniem
chirurgii jest jej bezradnoÊç wobec no-
wotworu, który wytworzy∏ ju˝ przerzu-
ty do innych miejsc organizmu.
W wielu przypadkach zamiast chi-
rurgii wybiera si´ wi´c radioterapi´. Po-
lega ona na zastosowaniu silnego pro-
mieniowania rentgenowskiego lub
gamma (zarówno z zewnàtrz, jak i w
niektórych przypadkach z wszczepio-
nego miniaturowego êród∏a radioak-
tywnego) do naÊwietlenia tkanki nowo-
tworowej. Leczenie radiacyjne powo-
duje uszkodzenie genomu komórki no-
wotworowej, wystarczajàce do jej zabi-
cia albo do indukcji procesu samobój-
stwa komórkowego, zwanego apoptozà.
(Apoptoza jest procesem swoistym dla
komórek ssaków i szczególnie istotnym
w okresie rozwoju zarodkowego, gdy
wytworzone struktury, takie jak np.
skrzela, zanikajà, poniewa˝ ich komór-
ki ulegajà programowanej Êmierci.)
Poniewa˝ prawid∏owe tkanki toleru-
jà ekspozycj´ na promieniowanie znacz-
nie lepiej ni˝ komórki nowotworowe,
metoda ta pozwala zachowaç struktury
anatomiczne otaczajàce guz nowotwo-
rowy i leczy raka, nie upoÊledzajàc funk-
cji organizmu. W nowotworze z∏oÊliwym
szyjki macicy, we wczesnych stadiach
choroby Hodgkina, czyli ziarnicy z∏oÊli-
wej, czy w raku prostaty radioterapia da-
je dobre wyniki. Jest równie˝ niezwykle
istotna w leczeniu nowotworów krtani,
bo nie zaburza zdolnoÊci mówienia.
Radioterpia oprócz tego, ˝e oszcz´-
dza prawid∏owe tkanki, ma te˝ inne za-
lety w porównaniu z chirurgicznym
usuni´ciem nowotworu. Przyk∏adowo,
stosujàc promieniowanie mo˝na znisz-
czyç mikroskopijne nacieki nowotwo-
ru, które skalpel móg∏ ominàç. Radio-
terapia jest te˝ rozwiàzaniem bezpiecz-
niejszym dla starszych, s∏abszych bio-
logicznie pacjentów, dla których zabieg
operacyjny stanowi∏by zbyt wielkie ob-
cià˝enie. Chorzy leczeni tà metodà zwy-
kle poddawani sà codziennym napro-
mienieniom przez okres 5–8 tygodni bez
koniecznoÊci hospitalizacji.
Pomimo tych wielu zalet radioterapia
niekiedy nie wystarcza, poniewa˝ tak jak
leczenie chirurgiczne nie zawsze usuwa
wszystkie komórki nowotworowe guza.
Podobnie jak zabieg chirurgiczny nie jest
ona mo˝liwa w przypadku szerokiego
rozsiewu nowotworowego, który w koƒ-
cu prowadzi do powstania guzów w
wielu miejscach cia∏a. (Napromienienie
ca∏ego organizmu du˝ymi dawkami
umo˝liwiajàcymi zabicie rozsianych ko-
mórek nowotworowych niszczy bowiem
delikatne tkanki niezb´dne do ˝ycia.) W
takim przypadku trzeba stosowaç che-
mioterapi´, czyli ogólnoustrojowe poda-
wanie leków przeciwnowotworowych,
które krà˝à w organizmie wraz z krwià.
W chwili obecnej stosuje si´ wiele ró˝-
nych leków przeciwnowotworowych,
a nowe sà ciàgle odkrywane i testowa-
ne. Typowe leki chemioterapeutyczne
dzia∏ajà na komórki ludzkie w podobny
sposób jak antybiotyki na komórki bak-
teryjne. Uniemo˝liwiajà ich namna˝anie,
zak∏ócajàc zdolnoÊç do replikacji DNA.
Wydaje si´, przynajmniej w kilku przy-
padkach, ˝e (podobnie jak radioterapia)
indukujà one apoptoz´ w komórkach
nowotworowych.
Pierwsze chemioterapeutyki opraco-
wane w latach czterdziestych naszego
wieku zwykle okazywa∏y si´ niewystar-
czajàce, gdy podawano je oddzielnie,
a nawet kolejno po sobie. Dopiero w la-
tach szeÊçdziesiàtych lekarze odkryli,
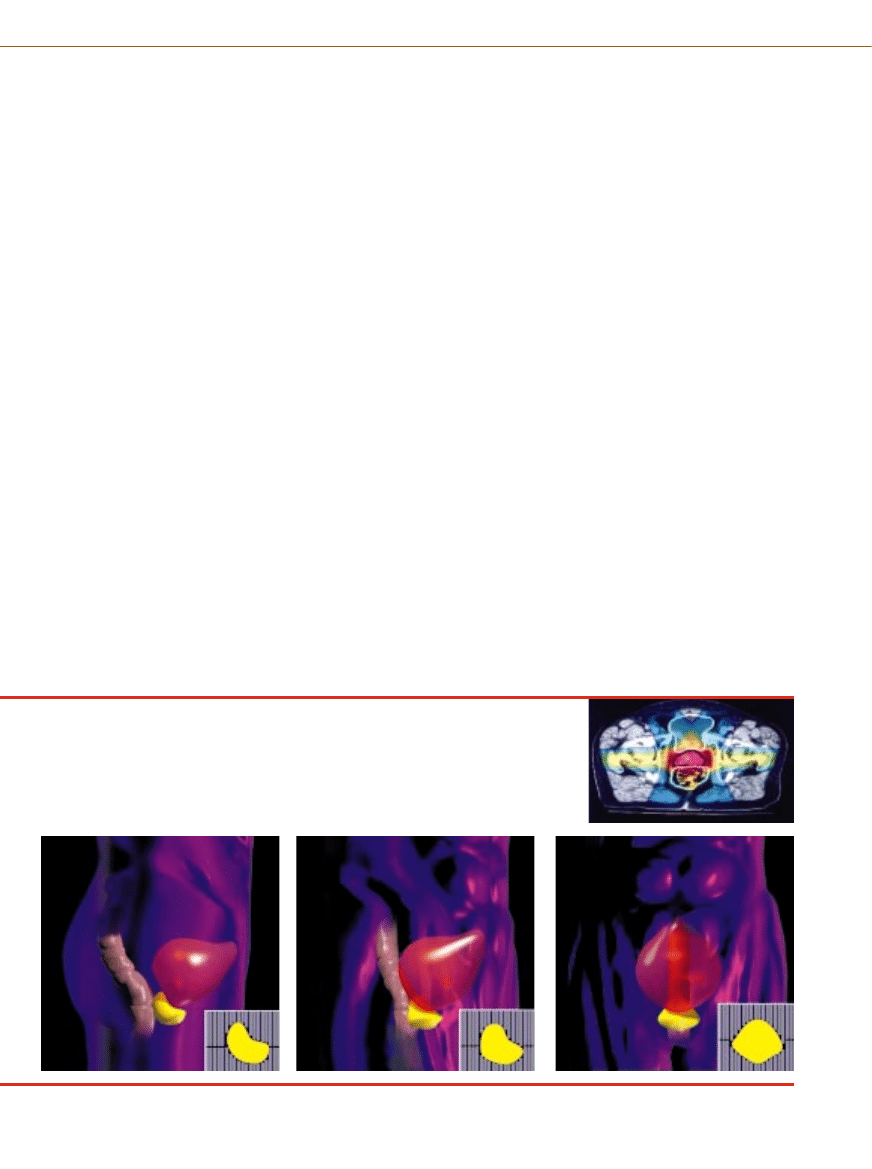
W RADIOTERAPII KONFORMACYJNEJ kszta∏t i kierunek wiàzki promieniowania rentgenowskiego stale zmienia si´
w czasie. Na przyk∏ad przy leczeniu napromienieniem raka prostaty kszta∏t wiàzki ulega zmianie (˝ó∏ty) w zale˝noÊci
od tego, czy skierowana jest ona z boku (a), z ukosa (b) czy z przodu (c). Sàsiadujàce narzàdy, takie jak jelito grube
(ró˝owy) i p´cherz (czerwony) nie sà wtedy niepotrzebnie napromieniane. W niektórych urzàdzeniach sterowany kom-
puterem mechanizm kszta∏tuje wiàzk´ (wstawki poni˝ej) poprzez regulowanie po∏o˝enia zestawu metalowych palców
w szczelinie akceleratora. Dzi´ki temu wiàzka zostaje zogniskowana dok∏adnie w tym miejscu, które wyznaczono na pod-
stawie tomografii komputerowej (czarny obrys z prawej).
a
b
c
ANDREW CHRISTIE
Slim Films
SAMUEL HELLMAN
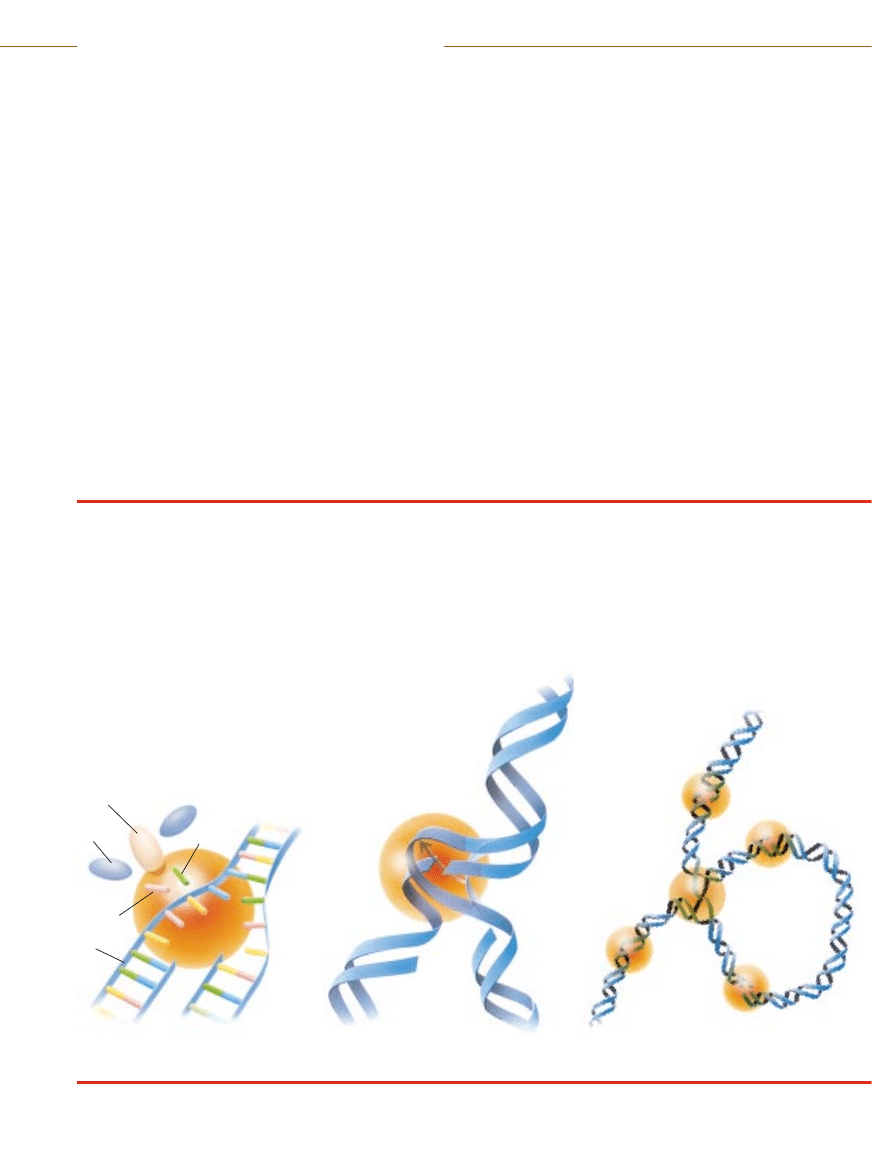
CZYNNIKI ALKILUJÑCE
Pewne zwiàzki (pomaraƒczowy) tworzà
wiàzania chemiczne z poszczególnymi ele-
mentami budulcowymi DNA, powodujàc
w ten sposób defekty w normalnej podwój-
nohelikalnej strukturze czàsteczki DNA.
Mogà to byç przerwy lub niew∏aÊciwe po-
∏àczenia w niciach czy pomi´dzy niçmi.
Je˝eli uszkodzenia te nie
zostanà naprawione
przez odpowiednie
mechanizmy ko-
mórkowe, to
wywo∏ajà
apoptoz´.
INHIBITORY TOPOIZOMERAZY
Replikacja materia∏u genetycznego komórki
wymaga rozdzielenia dwóch nici sk∏adowych
helisy DNA. Pomocne sà w tym zwykle spe-
cjalne enzymy, topoizomerazy, które na mo-
ment rozcinajà jednà z nici, pozwalajà drugiej
przejÊç przez wytworzonà przerw´, a po-
tem ∏àczà rozdzielone koƒce. Leki,
które hamujà zdolnoÊç enzymów
topoizomerazowych do ∏àcze-
nia rozdzielonych nici, spra-
wiajà, ˝e podczas podzia∏u
w DNA powstajà trwa∏e
przerwy, co powoduje
apoptoz´.
˝e chemioterapia bywa cz´sto skutecz-
na, gdy podaje si´ kilka leków naraz.
Obecnie wiele nowotworów, takich jak
bia∏aczki, ch∏oniaki i nowotwory jàdra
z powodzeniem leczy si´ chemiotera-
pià wielolekowà. Jest to szczególnie
istotne, gdy˝ nowotwory te cz´sto doty-
kajà ludzi m∏odych, którym wyleczenie
mo˝e zapewniç znacznie wi´cej lat ˝y-
cia ni˝ wi´kszoÊci chorych na nowotwo-
ry. Niestety, najcz´Êciej spotykanych no-
wotworów (np. piersi, p∏uca, jelita gru-
bego i prostaty) zazwyczaj nie udaje si´
wyleczyç wy∏àcznie chemioterapià. W
tych przypadkach chemioterapia jest
jednym z elementów programu lecze-
nia skojarzonego, obejmujàcego rów-
nie˝ chirurgi´ i radioterapi´.
Dost´pne chemioterapeutyki cz´sto
zawodzà, poniewa˝ zabijajà wiele zdro-
wych komórek, powodujàc powa˝ne
skutki uboczne, co ogranicza dawk´ le-
ku, jakà lekarz mo˝e podaç. Uszkodze-
nie szybko namna˝ajàcych si´ komórek,
na przyk∏ad szpiku kostnego, powodu-
je anemi´, niezdolnoÊç do zwalczania
infekcji i sk∏onnoÊç do krwawieƒ we-
wn´trznych, co wynika z niemo˝noÊci
wytworzenia przez organizm chorego
odpowiedniej iloÊci czerwonych i bia-
∏ych krwinek i p∏ytek krwi (komórek od-
powiedzialnych za jej krzepni´cie). In-
nymi skutkami ubocznymi chemiote-
rapii sà biegunki, nudnoÊci, wymioty
i utrata w∏osów. Zdarzajà si´ przypadki,
˝e leki te uszkadzajà uk∏ad nerwowy.
Chocia˝ post´p w strategiach majà-
cych na celu usuni´cie tych niepo˝à-
danych objawów jest doÊç szybki, to jed-
nak chemioterapia w swojej obecnej
postaci zdradza jeszcze innà podstawo-
wà s∏aboÊç. Podobnie jak bakterie opor-
ne na antybiotyki pewne nowotwory
mogà prze˝yç mimo dzia∏ania leków
przeciwnowotworych. Niektóre nie re-
agujà na chemioterapi´ od poczàtku,
a inne stajà si´ oporne na powtarzane
leczenie. Jest to problem szczególnie
wa˝ny, gdy˝ komórki nowotworowe
potrafià staç si´ oporne na dzia∏anie
wielu leków ju˝ po podaniu tylko jedne-
go z nich.
Inny rodzaj leczenia mo˝liwy w przy-
padku niektórych nowotworów omija
wiele problemów zwiàzanych z chemio-
terapià. Metoda ta polega na manipula-
cji uk∏adem hormonalnym organizmu.
Sutek oraz prostata sà gruczo∏ami regu-
lowanymi przez hormony p∏ciowe, tak
˝e nowotwory tych narzàdów równie˝
mogà na nie reagowaç. T´ wra˝liwoÊç
wykorzystuje si´ praktycznie: lekarze po-
dajà kobietom chorym na raka piersi an-
tyestrogeny, a m´˝czyznom cierpiàcym
na raka prostaty – leki zapewniajàce tzw.
blokad´ androgenowà.
Tego typu terapia hormonalna ma sto-
sunkowo niewiele skutków ubocznych,
poniewa˝ jej dzia∏anie ogranicza si´ do
tkanek posiadajàcych receptory dla spe-
cyficznych hormonów. Mo˝na jednak
stosowaç jà wy∏àcznie w przypadku no-
wotworów tych tkanek. Nawet wówczas
okazuje si´ jednak nie zawsze skutecz-
na, poniewa˝ nowotwory piersi i prosta-
90 Â
WIAT
N
AUKI
Listopad 1996
DOSKONALENIE DZISIEJSZYCH TERAPII
ANTYMETABOLITY
Niektóre substancje przeciwnowotworowe
dzia∏ajà jako fa∏szywe substraty w reak-
cjach biochemicznych ˝ywych komórek.
Jednym z g∏ównych leków tego typu jest
metotreksat – chemiczny analog kwasu
foliowego. Dzia∏anie metotreksatu polega
m.in. na wiàzaniu si´ z enzymem (poma-
raƒczowy)
bioràcym udzia∏ w przemianie
kwasu foliowego do dwóch elementów bu-
dulcowych DNA – adeniny i guaniny. Lek
ten zapobiega podzia∏om komórkowym,
upoÊledzajàc zdolnoÊci komórki do tworze-
nia nowego DNA.
Przyk∏ady: metotreksat, fluorouracyl,
gemcytabina
Przyk∏ady: doksorubicyna, CPT-11
Przyk∏ady: cyklofosfamid, chlorambucyl
METOTREKSAT
KWAS
FOLIOWY
ADENINA
GUANINA
DNA
Rodziny leków chemioterapeutycznych
ty mogà zawieraç komórki niezale˝ne od
hormonów, które wcià˝ b´dà si´ niebez-
piecznie namna˝aç.
¸àczenie ró˝nych terapii
Ju˝ w momencie rozpoznania lekarze
potrafià okreÊliç faz´ rozwoju wi´kszo-
Êci nowotworów litych. Ogólnie za pier-
wszy stopieƒ klinicznego zaawansowa-
nia nowotworu uznaje si´ niewielkich
rozmiarów guzy, które nie rozprzestrze-
ni∏y si´ do w´z∏ów ch∏onnych. Stopieƒ
drugi i trzeci to wi´ksze guzy pierwotne
(atakujàce w´z∏y ch∏onne). W stopniu
czwartym choroba rozprzestrzenia si´
w ca∏ym organizmie pod postacià stwier-
dzanych klinicznie przerzutów odleg∏ych.
Do zwalczania nowotworów we
wczesnych stadiach zaawansowania, tj.
guzów in situ lub w okolicznych w´z∏ach
ch∏onnych, lekarze stosujà zabieg chi-
rurgiczny lub radioterapi´. W przypad-
ku chorych, u których stwierdzono no-
wotwór w czwartym stopniu zaawan-
Â
WIAT
N
AUKI
Listopad 1996 91
sowania klinicznego, rokowanie jest
zazwyczaj niekorzystne, a opieka me-
dyczna ma na celu zmniejszenie nasi-
lenia objawów choroby i przed∏u˝enie
˝ycia. (W takich przypadkach stosuje
si´ z powodzeniem zwykle chemiotera-
pi´.) Leczenie poÊrednich stadiów za-
awansowania trudno usystematyzowaç,
zw∏aszcza ˝e w tych przypadkach meto-
dy zmieniajà si´ najszybciej. Chorych z
nowotworami w stadiach poÊrednich
mo˝na cz´sto ca∏kowicie wyleczyç dzi´-
ki usuni´ciu z ich organizmu wszelkich
Êladów nowotworu. Jednak˝e wielu pa-
cjentów doÊwiadczy jedynie czasowej
remisji choroby, poniewa˝ mikroskopij-
ne nacieki nowotworu (komórki nowo-
tworowe obecne, lecz nie wykryte) z
czasem zacznà rozwijaç si´ poza jakà-
kolwiek kontrolà.
W przypadku chorych na nowotwo-
ry w poÊrednich stadiach zaawansowa-
nia lekarze coraz cz´Êciej stosujà po∏à-
czenie ró˝nych metod, tzw. leczenie
skojarzone. Wymaga ono udzia∏u spe-
cjalistów z ró˝nych dziedzin medycy-
ny – onkologów, chirurgów, patologów
i radiologów – a koordynacja tej wspó∏-
pracy cz´sto stanowi powa˝ny problem
logistyczny.
Zwykle ∏àczy si´ zabieg chirurgiczny
lub radioterpi´ z uzupe∏niajàcà chemio-
terapià. Najlepszym bodaj tego przyk∏a-
dem jest obecny sposób leczenia raka
piersi. Chirurgiczne usuni´cie guza wraz
z niewielkà warstwà otaczajàcych go
tkanek (zabieg zwany tumorektomià)
po∏àczone z radioterapià i chemioterapià
zwi´ksza liczb´ wyleczeƒ z nowotwo-
ru i w wielu przypadkach sprawia, ˝e
mastektomia nie jest konieczna. Podob-
nie jest w przypadku nowotworu jelita
grubego, niektórych nowotworów ko-
Êci i tkanek mi´kkich.
Nowszy sposób leczenia skojarzone-
go – chemioterapia indukcyjna – pole-
ga na zastosowaniu najpierw chemiote-
rapii, a dopiero potem leczenia chirur-
gicznego lub radioterapeutycznego. Pro-
cedura ta pozwala onkologom oceniç
skutecznoÊç zastosowanej chemiotera-
pii poprzez obserwowanie szybkoÊci
zmniejszania si´ ogniska pierwotnego
nowotworu.
Chemioterapia indukcyjna czyni real-
nym mo˝liwie najszybsze rozpocz´cie
leczenia mikroprzerzutów komórek no-
wotworowych rozsianych po ca∏ym orga-
nizmie. W niektórych przypadkach taka
poprzedzajàca zabieg operacyjny che-
mioterapia mo˝e zmniejszyç lub ca∏ko-
wicie wyeliminowaç koniecznoÊç usu-
ni´cia ca∏ego narzàdu. Na przyk∏ad cho-
rych cierpiàcych na zaawansowane po-
stacie nowotworów g∏owy i szyi trady-
cyjnie leczy si´ chirurgicznie bàdê napro-
mienianiem, lecz w wielu przypadkach
dzia∏ania te nie przynoszà korzystnych
efektów. Czasami zostajà oni pozbawie-
ni mo˝liwoÊci mówienia. Chemioterapia
indukcyjna z nast´powym napromienia-
niem zmian nowotworowych daje zbli˝o-
ne wskaêniki prze˝yç ca∏kowitych, nie
powodujàc tak ogromnego kalectwa.
Z podobnym powodzeniem zastosowa-
no ju˝ chemioterapi´ indukcyjnà w le-
czeniu nowotworów p∏uca i p´cherza
moczowego. W tym ostatnim przypadku
pozwala ona zachowaç narzàd. Induk-
cyjna hormonoterapia z nast´powym le-
czeniem operacyjnym lub radioterapià
jest równie˝ doÊç skuteczna w leczeniu
raka prostaty.
Chemio- lub hormonoterapi´ mo˝na
tak˝e stosowaç w tym samym czasie co
leczenie chirurgiczne lub napromienia-
nie. PodejÊcie to zwane jednoczasowà
chemioradioterapià jest nieocenione
zw∏aszcza w leczeniu nowotworów,
o których wiadomo, ˝e sam zabieg chi-
rurgiczny bàdê napromienianie niewie-
le by pomog∏y (tj. leczenie nie niszczy
nowotworu w ca∏oÊci ani nie zapobie-
ga wczeÊniejszemu powstaniu przerzu-
tów odleg∏ych). Wykazano na przyk∏ad,
˝e leczenie raka prze∏yku jest skutecz-
niejsze w przypadku zastosowania jed-
noczasowej chemioradioterapii ni˝ sa-
mej radioterapii. Uzupe∏nienie o che-
mioterapi´ zmniejsza w tych przypad-
kach ryzyko wznowy miejscowej i wy-
stàpienia przerzutów odleg∏ych.
Coraz powszechniejsze stajà si´ nowe
metody chirurgiczne polegajàce na wyko-
nywaniu ma∏ych ci´ç i wprowadzaniu
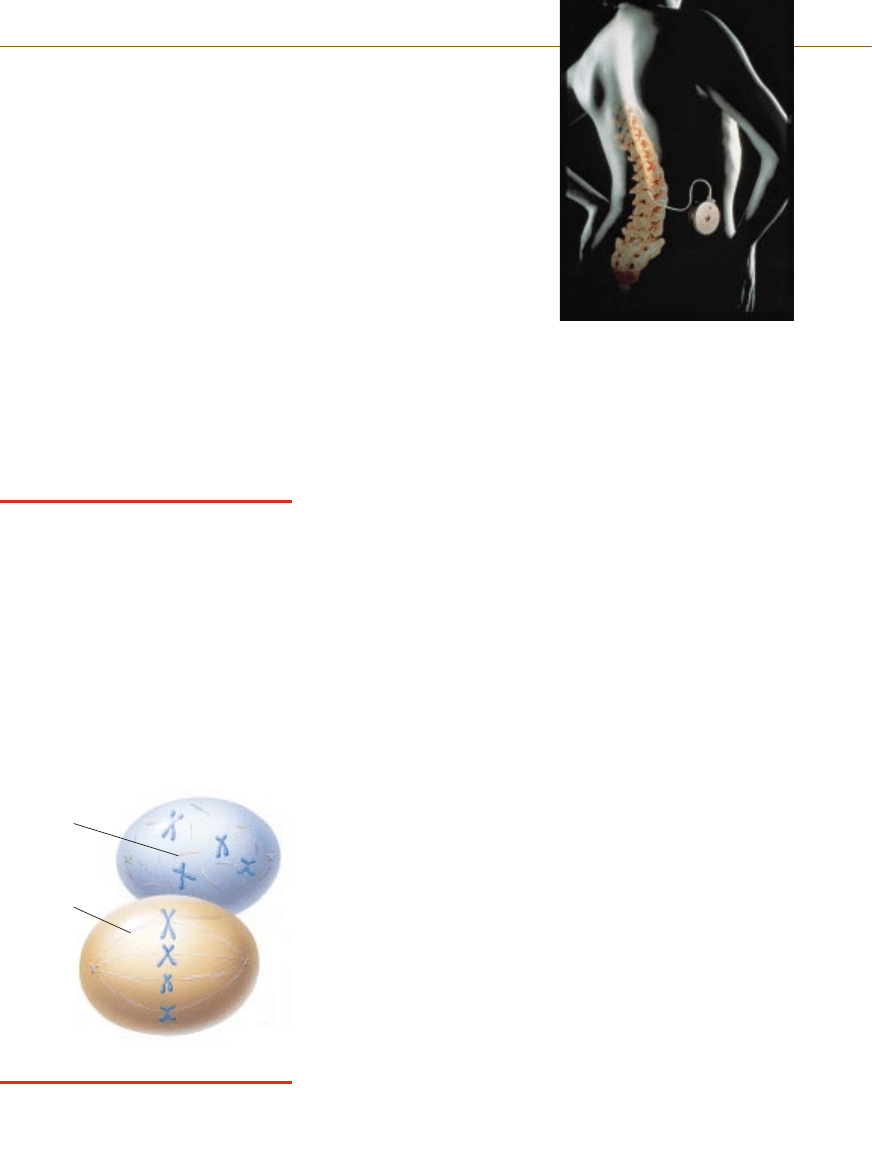
ALKALOIDY ROÂLINNE
Niektóre substancje pochodzàce z roÊlin zapo-
biegajà podzia∏om komórkowym, wià˝àc si´
z bia∏kiem tubulinà. Tubulina formuje mikrotu-
bularne w∏ókna pomagajàce skoordynowaç po-
dzia∏ komórkowy. W∏ókna te ciàgnà zdupliko-
wane chromosomy do przeciwleg∏ych koƒców
macierzystej komórki, dzi´ki czemu ka˝da ko-
mórka potomna otrzymuje pe∏en zestaw ma-
teria∏u genetycznego. Leki, które wp∏ywajà na
procesy powstawania lub rozpadu w∏ókien
tubulinowych, mogà zapobiec podzia∏om
komórkowym.
Przyk∏ady: winblastyna, winorelbina,
paklitaksel, docetaksel.
ROZERWANE
W¸ÓKNO
NORMALNE
W¸ÓKNO
WSZCZEPIALNE POMPY INFUZYJNE
umieszczane pod skórà brzucha lub w klat-
ce piersiowej pacjenta pozwalajà na ciàg∏e po-
dawanie leków chemioterapeutycznych lub
narkotyków, pomagajàc w ten sposób w ∏ago-
dzeniu chronicznego bólu nowotworowego.
Za zgodà MEDTRONIC, INC.
TOMO NARASHIMA

specjalnych instrumentów pozwalajà-
cych chirurgom widzieç i operowaç g∏´-
boko we wn´trzu cia∏a pacjenta. Oszcz´-
dzajà one choremu urazu powodowa-
nego przez tradycyjny zabieg operacyjny.
Jednak˝e z pewnoÊcià najwi´kszy prze-
∏om w leczeniu nowotworów przyniosà
post´py w radio- i chemioterapii, zwi´k-
szajàce skutecznoÊç tych metod w zabi-
janiu komórek nowotworowych bez
trwa∏ego uszkadzania zdrowych tkanek.
Niektóre metody wymagajà jeszcze wie-
lu lat badaƒ, zanim zostanà dopuszczo-
ne do rutynowego leczenia chorych, lecz
inne wydajà si´ bliskie powszechnego
zastosowania.
Perspektywy na przysz∏oÊç
Szybko rozwijajàca si´ radioterapia
umo˝liwi lekarzom indywidualne przy-
stosowanie leczenia do konkretnego
przypadku chorobowego. W szczegól-
noÊci post´p technologiczny pozwala
w chwili obecnej na manipulowanie ze-
wn´trznà wiàzkà promieniowania, tak
by skierowaç jà na guz, nie uszkadzajàc
zdrowych otaczajàcych go tkanek. Tech-
niki takie nazywa si´ radioterapià kon-
formacyjnà (conformal radiotherapy),
poniewa˝ wiàzka promieniowania do-
pasowuje si´ ÊciÊle do kszta∏tu guza.
Radioterapia konformacyjna wyko-
rzystuje wiele zaawansowanych tech-
nik. Po pierwsze, trzeba uzyskaç trój-
wymiarowy obraz guza za pomocà to-
mografii komputerowej (z u˝yciem pro-
mieni X) lub magnetycznego rezonan-
su jàdrowego. Informacja ta zostaje za-
pisana cyfrowo, s∏u˝àc jako podstawa
do opracowania szczegó∏owego planu
leczenia, który okreÊla kierunek i kszta∏t
wiàzki (oraz nasilenie i czas trwania na-
promieniania). Taki program maksyma-
lizuje dawk´ promieniowania poch∏a-
nianà przez guz przy jednoczesnym
zminimalizowaniu ekspozycji otaczajà-
cych tkanek. Nast´pnie pacjent pod kon-
trolà komputera zostaje napromienio-
ny za pomocà akceleratora liniowego –
wzgl´dnie ma∏ego urzàdzenia, które
mo˝e wytwarzaç promienie X o du˝ym
nat´˝eniu i którym ∏atwo daje si´ ma-
newrowaç wokó∏ pacjenta.
Radioterapia konformacyjna pozwa-
la zespo∏owi lekarzy, radioterapeutów
i fizyków na bezpieczne podwy˝szenie
dawki promieniowania poch∏anianego
przez guz prostaty (a wi´c i prawdo-
podobieƒstwa jego wyleczenia) bez
zwi´kszania (w praktyce czasem nawet
umo˝liwia zmniejszenie) uszkodzenia
tkanek nie obj´tych procesem nowotwo-
rowym. Technik´ t´ stosuje si´ tak˝e do
eksperymentalnego leczenia nowo-
tworów gdzie indziej zlokalizowanych,
a nawet w przypadkach istnienia nie-
wielkiej liczby przerzutów.
Innà powstajàcà dopiero odmianà ra-
dioterapii konformacyjnej jest metoda
napromieniania guzów mózgu z wy-
korzystaniem specjalnej ramy przy-
twierdzanej bezpoÊrednio do czaszki
pacjenta. Naprowadzajàc êród∏o pro-
mieniowania rentgenowskiego osadzo-
ne w sztywnej ramie, technicy mogà
bardzo precyzyjnie ukierunkowaç wiàz-
k´ podczas ka˝dej sesji terapeutycznej.
Promieniowanie rentgenowskie i gam-
ma to podstawa radioterapii, ale skutecz-
ne w naÊwietlaniu sà tak˝e wiàzki pro-
tonów czy neutronów. Protony ∏atwiej
ni˝ promienie X skierowaç na guz, neu-
trony zaÊ majà silniejsze dzia∏anie prze-
ciwnowotworowe. Przysz∏oÊç poka˝e,
jak skuteczne sà te czàstki, ale dost´pne
ju˝ dane Êwiadczà o niez∏ych rezultatach.
Protony na przyk∏ad leczà niewielkie gu-
zy rdzenia le˝àce w sàsiedztwie struk-
tur niezb´dnych do ˝ycia, z kolei neu-
trony – nowotwory z∏oÊliwe Êlinianek.
Post´py w chemioterapii nadejdà
wraz z erà nowych leków. Interesujàce
nowe Êrodki przeciwnowotworowe za-
stosowane ostatnio w praktyce klinicz-
nej obejmujà taksany wyodr´bnione z ci-
sów, skuteczne w leczeniu zaawanso-
wanego raka jajnika i raka piersi [patrz:
K. C. Nicolaou, Rodney K. Guy i Pierre
Potier; „Taksoidy: nowy or´˝ w walce
z rakiem”; Âwiat Nauki, wrzesieƒ 1996].
Z kolei tzw. pochodne kamptotekano-
we budzà nadziej´ w leczeniu raka je-
lita grubego i raka p∏uca. Mechanizm
dzia∏ania obu tych rodzajów leków jest
inny ni˝ dotychczasowych chemiotera-
peutyków. Tak˝e zmiany w sposobach
podawania chemioterapeutyków mogà
spowodowaç wi´kszà liczb´ wyleczeƒ.
Na przyk∏ad zastosowanie implanto-
wanych pomp infuzyjnych wprowadza-
jàcych leki bezpoÊrednio do krwiobiegu
zapewnia d∏u˝szà ekspozycj´ guza na
lek w okresie wzrostu i wra˝liwoÊci no-
wotworu na dany zwiàzek, dajàc lep-
sze wyniki leczenia.
Niektóre wysi∏ki zmierzajàce do po-
prawienia skutecznoÊci chemioterapii
koncentrujà si´ na przeciwdzia∏aniu
opornoÊci komórek nowotworowych na
leki. Inne metody leczenia, w chwili
obecnej jeszcze teoretyczne, polega∏yby
na uniemo˝liwianiu unaczynienia si´
guza lub na pobudzaniu uk∏adu odpor-
noÊciowego do zwalczania nowotworu
[patrz: Terapie jutra, strona 107]. W faz´
prób klinicznych wchodzà tak˝e nowe
leki – czynniki ró˝nicowania. Zwiàzki
92 Â
WIAT
N
AUKI
Listopad 1996
DOSKONALENIE DZISIEJSZYCH TERAPII
Za zgodà MAYO CLINIC; PETER SAMEK
Slim Films
OPERACJA JELITA GRUBEGO wymaga pe∏nego otwarcia jamy brzusznej pacjenta, a wi´c
zwykle du˝ego ci´cia. Metoda laparoskopowa umo˝liwia dziÊ mniej urazowe operowanie
raka tego narzàdu. Lekarze z Mayo Clinic i kilku innych oÊrodków testujà obecnie t´ metod´
w badaniach klinicznych
(z lewej). Instrumenty chirurgiczne wprowadza si´ przez ma∏e
otwory w pow∏okach brzusznych
(drugie od lewej). Obserwujàc na ekranie obraz wn´trza
nadmuchanej jamy brzusznej pacjenta, chirurdzy wycinajà fragment jelita od strony Êcia-
ny brzusznej
(na prawo od Êrodka). Mogà wtedy przez ma∏y otwór wydobyç t´ cz´Êç jelita
na zewnàtrz i usunàç fragment z naciekiem nowotworowym
(skrajnie z prawej).

te zamiast zabijaç komórki nowotworo-
we powodujà ich ostateczne ró˝nicowa-
nie. Tracà one wtedy zdolnoÊç do po-
dzia∏u i podejmujà jednà funkcj´, po-
dobnie jak inne prawid∏owe komórki
organizmu. Czynniki ró˝nicowania
umo˝liwiajà znacznie mniej toksycznà
chemioterapi´ ni˝ obecne leki, które za-
bijajà komórki.
W ostatnich latach lekarze poczynili
olbrzymie post´py w zmniejszaniu tok-
sycznych dzia∏aƒ ubocznych i ulepsza-
niu terapii os∏aniajàcej pacjentów leczo-
nych chemioterapià. Na przyk∏ad nowe
silniejsze leki przeciwwymiotne przy-
noszà tym chorym znacznà ulg´. Z uwa-
gi na fakt, ˝e chemioterapia z regu∏y
uszkadza szybko dzielàce si´ komórki
wyÊcie∏ajàce przewód pokarmowy, bie-
gunka i nadwra˝liwoÊç Êluzówki jamy
ustnej sà jej cz´stymi objawami ubocz-
nymi. Byç mo˝e wkrótce dost´pne sta-
nà si´ leki stymulujàce wzrost i napra-
w´ komórek wyÊcie∏ajàcych przewód
pokarmowy, co pozwoli wp∏ywaç na
przyczyn´ toksycznych oddzia∏ywaƒ
chemioterapeutyków, a nie tylko ich
skutków.
Od pewnego czasu trwajà badania
nad ró˝nymi czynnikami wzrostu zdol-
nymi stymulowaç komórki prekursoro-
we krwi w szpiku kostnym do szybszej
jego odnowy po chemioterapii. Leki
zwi´kszajàce na przyk∏ad produkcj´ leu-
kocytów chronià pacjentów przed wie-
loma skomplikowanymi infekcjami. Je-
den z opracowywanych obecnie Êrod-
ków pobudza szpik kostny do produk-
cji p∏ytek krwi, niezb´dnych do jej
krzepni´cia. Ponadto w terapii nowo-
tworów nie poddajàcych si´ leczeniu
konwencjonalnymi dawkami leków co-
raz cz´Êciej stosuje si´ wysokie dawki,
w czasie gdy komórki prekursorowe sà
magazynowane poza organizmem pa-
cjenta [patrz: Karen Antman, „Kiedy
przeszczepiaç szpik”, strona 94].
Trudno te˝ nie doceniaç znaczenia,
jakie w zwi´kszaniu odsetka wyleczeƒ
ma wczesne rozpoznanie raka, które po-
zwala leczyç guz mniejszy, mniej agre-
sywny i mniej sk∏onny do dawania prze-
rzutów. Lekarze poczynili ogromne
post´py w wykorzystaniu technik ob-
razowania przy rozpoznawaniu guzów.
Wspó∏czesne rozumienie genetycznych
mechanizmów nowotworzenia dostar-
cza Êrodków do testowania wrodzonej
podatnoÊci na niektóre rodzaje raka, do
ostrzegania w pewnych przypadkach
o ich wystàpieniu i do szacowania stop-
nia ich z∏oÊliwoÊci.
Leczenie naprawd´ definitywne
Wi´ksza cz´Êç tego numeru poÊwi´-
cona jest post´pom wiedzy o moleku-
larnych i genetycznych podstawach no-
wotworów. Zapewne zaowocuje ona
w koƒcu opracowaniem bardziej sku-
tecznych metod leczenia raka i w re-
zultacie strategià profilaktyki nowo-
tworów. W bli˝szej przysz∏oÊci lekarze
zapewne zacznà wykorzystywaç mar-
kery genetyczne i molekularne do oce-
ny z∏oÊliwoÊci nowotworów i prawdo-
podobieƒstwa ich reakcji na ró˝ne
rodzaje leczenia.
Nowy rozdzia∏ w leczeniu nowotwo-
rów otwiera terapia genowa. Wraz z ko-
legami z University of Chicago próbuje-
my po∏àczyç radioterapi´ i terapi´
genowà, czyli wykorzystaç wiàzk´ pro-
mieniowania do inicjacji (w okreÊlonych
punktach ludzkiego cia∏a) produkcji bia-
∏ek toksycznych dla komórek nowotwo-
rowych. Ten raczej niezwyk∏y rezultat
uda∏o si´ nam uzyskaç u zwierzàt do-
Êwiadczalnych dzi´ki wprowadzeniu
do tkanki nowotworowej genu „indu-
kowanego promieniowaniem”, czyli ge-
nu tak przetworzonego metodami in-
˝ynierii genetycznej, by si´ uaktywnia∏
(tj. powodowa∏ wytwarzanie kodowa-
nego przez siebie bia∏ka) tylko pod
wp∏ywem promieniowania. Technika
ta – zwana miejscowà terapià genowà
(regional gene therapy) – mog∏aby zna-
czàco zwi´kszyç skutecznoÊç i specy-
ficznoÊç radioterapii w leczeniu nowo-
tworów; wkrótce wejdzie ona w faz´
prób klinicznych.
Wojna w po∏owie wygrana
Badania nad zwalczaniem raka cz´-
sto porównywane sà do dzia∏aƒ wojen-
nych. Chocia˝ analogia ta bywa niekie-
dy mylàca, to jednak we w∏aÊciwym
Êwietle przedstawia obecnà sytuacj´ na-
ukowców. Podczas II wojny Êwiatowej,
przed làdowaniem w Normandii, alian-
ci odnieÊli znaczne sukcesy, choç praw-
dziwa ofensywa jeszcze si´ wtedy nie
rozpocz´∏a. Patrzàc na map´, mo˝na sà-
dziç, ˝e wojenne zwyci´stwa w Afryce
i we W∏oszech by∏y minimalne. Ale
w okresie tym osiàgni´to ju˝ nadzwy-
czajne post´py w uzbrojeniu, wyszko-
leniu ˝o∏nierzy i mo˝liwoÊciach prze-
rzucenia ich do Europy Zachodniej.
Chocia˝ w leczeniu raka nastàpi∏ ju˝
pewien post´p, to jednak sukcesy te
niewiele mówià o niezwyk∏ym rozwoju
narz´dzi, które badacze i klinicyÊci ma-
jà ju˝ w zasi´gu r´ku. W tej chwili trud-
no przewidzieç, jak przydatne oka˝à si´
poszczególne odkrycia, ale wszystkie ra-
zem przyniosà z pewnoÊcià korzyÊç pa-
cjentom. Nasze oczekiwania muszà byç
jednak realistyczne. Prosta, uniwersalna
metoda, skuteczna we wszystkich typach
nowotworów, chocia˝ mo˝liwa, w naj-
bli˝szej przysz∏oÊci jest niezwykle ma∏o
prawdopodobna. Jednak szeroki wa-
chlarz specyficznych i mniej toksycznych
metod leczenia wydaje si´ bardziej do-
st´pny, ni˝ wi´kszoÊç osób sàdzi.
T∏umaczy∏
Maciej Chwaliƒski
Â
WIAT
N
AUKI
Listopad 1996 93
Informacja o autorach
SAMUEL HELLMAN i EVERETT E. VOKES sà profesorami w Zak∏adzie Radioterapii i Onkolo-
gii Komórkowej University of Chicago. Zanim przyjecha∏ do Chicago w 1988 roku, Hellman pra-
cowa∏ w Nowym Jorku. By∏ dyrektorem ds. klinicznych w Memorial Sloan-Kettering Cancer Cen-
ter oraz profesorem onkologii radiacyjnej w Cornell University Medical College. Vokes ukoƒczy∏
medycyn´ na Uniwersytecie w Bonn. Nast´pnie odby∏ sta˝ internistyczny w Bonn i Chicago, rezy-
dentur´ w University of Southern California Los Angeles County Hospital, a nast´pnie w 1983 ro-
ku uzyska∏ stypendium z hematologii i onkologii w Chicago. Cztery lata póêniej zosta∏ tam
profesorem i w chwili obecnej jest dyrektorem ds. klinicznych uniwersyteckiego centrum nowo-
tworowego. Hellman i Vokes sà autorami licznych publikacji na temat leczenia nowotworów,
prowadzà te˝ wyk∏ady.
Literatura uzupe∏niajàca
MULTIDRUG RESISTANCE IN CANCER
. Norbert
Kartner i Victor Ling, Scientific American,
vol. 260, nr 3, ss. 26-33, III/1989.
CANCER:PRINCIPLES AND PRACTICE OF ONCO-
LOGY
. Wyd. IV. Red. V. T. DeVita, Jr., S.
Hellman i S. A. Rosenberg; J. B. Lippin-
cott, 1993.
BIOLOGIC THERAPY OF CANCER
. Wyd. II. Red.
V. T. DeVita, Jr., S. Hellman i S. A. Ro-
senberg; J. B. Lippincott, 1995.
Wyszukiwarka
Podobne podstrony:
Postępowanie w przypadkach niedoboru estrogenów u kobiet po leczeniu raka piersi
03 0000 003 02 Leczenie raka piersi trastuzumabem
03 0000 001 02 Leczenie raka piersi docetakselem
03 0000 002 02 Leczenie raka piersi kapecytabina
Koksyby Postęp w leczeniu bólu i zapalenia w chorobie zwyrodnieniowej stawów (osteoartrozie)
KWALIFIKACJA I LECZENIE RAKA KRTANI
Chirurgiczne leczenie raka płuca (Lublin 2007)
Zaburzenia głosu po leczeniu raka krtani
DCA W LECZENIU RAKA
Leczenie raka kapsaicyna, @P PROD. KTÓRE CHRONIĄ PRZED RAKIEM @, Rak i terapia
03 0000 007 02 Leczenie raka jajnika topotekanem
Leczenie raka jonami krzemu
Lekarstwo na raka(1), LECZENIE RAKA alternatywne metody
Leczenie raka z pomocą wody o zwiększonej ilości deuteru
Leczenie raka jonami krzemu
Leczenie raka!!! – KAPSYCYNA, Zdrowie
Postepy w leczeniu zywieniowym, podstawy pielęgniarstwa
więcej podobnych podstron