Dorota Dziuba,
Piotr Duży,
Robert Fajger,
gr. L-2,
Analiza Instrumentalna.
Ćwiczenie nr 7.
OZNACZANIE ZAWARTOŚCI METALI W ROZTWORACH WODNYCH METODĄ SPEKTROSKOPII ABSORPCJI ATOMOWEJ AAS.
Absorpcyjna spektrometria atomowa jest metodą analityczną opartą na zjawisku absorpcji promieniowania elektromagnetycznego przez wolne atomy. Stosujemy tzw. plazmę niskotemperaturową 1000-4000K, w której większość substancji ulega dysocjacji i w wyniku powstają wolne atomy. Badane atomy wprowadza się do środowiska absorbującego w postaci roztworu. Wolne atomy otrzymuje się z roztworu przez doprowadzenie energii. Liczba wolnych atomów w plazmie jest proporcjonalna do stężenia:
N = rc
Linie atomowe zarówno absorpcyjne, jak i emisyjne, mają kształt krzywych Gaussa, a charakteryzuje je intensywność i szerokość w połowie wysokości. szerokość linii można wyrazić wzorem:
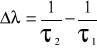
w którym τ1 oznacza czas życia stanu podstawowego, τ2 jest czasem życia stanu wzbudzonego. W praktyce obserwujemy zawsze poszerzenie linii widmowych. Na poszerzenie wpływają własności plazmy: temperatura, ciśnienie, pole elektrycznemagnetyczne. Absorbancja w AAS jest zależna od liczby wolnych atomów w środowisku absorbującym.
Celem ćwiczenia jest ilościowe oznaczenie zawartości miedzi w roztworach wodnych metodą krzywej wzorcowej z wykorzystaniem absorpcyjnej spektroskopii atomowej.
Odczynniki i aparatura:
mianowany roztwór wodny Cu(NO3)2 zawierający 1g metalu/dm3,
1n HNO3,
1n NaOH,
woda redestylowana,
kolbki miarowe o pojemności 100 cm3, 3 sztuki,
biureta 20 cm3,
mikrobiureta,
pipeta,
zlewka o pojemności 100 cm3,
papierki wskaźnikowe,
spektrometr AAS.
2. Wykonanie ćwiczenia:
Używając przygotowanego wcześniej mianowanego roztworu miedzi o stężeniu 1 g Cu/dm3 przygotowano roztwór o stężeniu 100 mg Cu/dm3 pobierając 10 cm3 roztworu pierwotnego i przenosząc go do kolbki o pojemności 100 cm3 .Uzupełniono kolbkę wodą destylowaną do kreski.
Sporządzono sześć roztworów w kolbkach o pojemności 50 cm3 zawierających następujące ilości miedzi:
1 mg Cu/dm3 ,
5 mg Cu/dm3 ,
10 mg Cu/dm3 ,
15 mg Cu/dm3 ,
20 mg Cu/dm3 ,
30 mg Cu/dm3 ,
wykorzystując do tego celu wcześniej przygotowany roztwór miedzi o stężeniu 100 mg Cu/dm3 i pobierając odpowiednio 0.5, 2.5, 5, 7.5, 10 i 15 cm3 tego roztworu. Do każdej kolbki dodano 0,25 cm3 30% roztworu HNO3 w celu uzyskania pH w granicach 2-3. Roztwór miedzi o stężeniu 1 g Cu/dm3 zadano wcześniej 3 cm3 stężonego roztworu HNO3 .
przygotowanie spektrometru do pracy:
•włączyć wentylację pomieszczenia,
•ustawić przy pomocy reduktora ciśnienie acetylenu w instalacji zasilającej aparat na poziomie 1,35 atm, a powietrza 3,5 atm,
•włączyć spektrometr i zapalić palnik przyciskiem START,
•włączyć zasilanie lamp z katodą wnękową przy pomocy potencjometrów i wyregulować prąd żarzenia na ok. 6,5 mA,
•wyregulować przy pomocy pokręteł regulujących przepływ acetylenu na poziomie 120 l/h i powietrza na 530 l/h,
wykonanie analizy:
•ustawić odpowiednią do oznaczanego miedzi lampę w osi optycznej aparatu, •wyregulować prąd żarzenia lampy do odpowiedniej wartości 6,5 mA,
•ustawić szczelinę aparatu na 10 nm i długości fali analizatora na 324,75 nm, aż do uzyskania maksymalnego wychylania prądu detektora,
•wyzerować wskaźnik absorbancji przyrządu przy zasilaniu palnika wodą redestylowaną,
•zanurzyć kapilarę zasilającą palnik w zlewce wypełnionej kolejno roztworami o odpowiednich stężeniach.
Na podstawie zmierzonej absorbancji dla każdej próbki z miedzią wyznaczono absorbancję średnią Aśr, odchylenie standardowe S i błąd oznaczenia %bł dla otrzymanych wyników korzystając z następujących zależności:
![]()
![]()
![]()
![]()
![]()
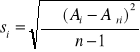
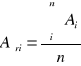
![]()
![]()
![]()
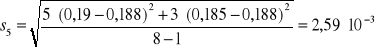
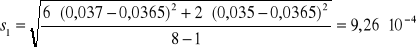
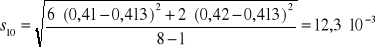
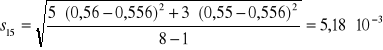
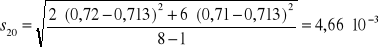
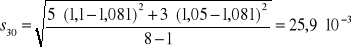
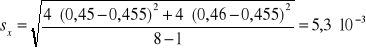
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Odczytana wartość nieznanego stężenia miedzi w roztworze wyznaczona na podstawie wykresy A = f(c) wynosi 12,5 mg/dm3.
Lp. |
Stęzenie miedzi w roztworze |
Absorbancja |
Absorbancja średnia |
Odchylenie standardowe dla absorbancji |
|
Lp. |
Stęzenie miedzi w roztworze |
Absorbancja |
Absorbancja średnia |
Odchylenie standardowe dla absorbancji |
1 |
1 |
0,037 |
0,0365 |
0,000926 |
|
5 |
20 |
0,71 |
0,713 |
0,00466 |
|
|
0,037 |
|
|
|
|
|
0,72 |
|
|
|
|
0,035 |
|
|
|
|
|
0,71 |
|
|
|
|
0,035 |
|
|
|
|
|
0,71 |
|
|
|
|
0,037 |
|
|
|
|
|
0,72 |
|
|
|
|
0,037 |
|
|
|
|
|
0,71 |
|
|
|
|
0,037 |
|
|
|
|
|
0,71 |
|
|
|
|
0,037 |
|
|
|
|
|
0,71 |
|
|
2 |
5 |
0,19 |
0,188 |
0,00259 |
|
6 |
30 |
1,05 |
1,081 |
0,0259 |
|
|
0,185 |
|
|
|
|
|
1,1 |
|
|
|
|
0,19 |
|
|
|
|
|
1,1 |
|
|
|
|
0,19 |
|
|
|
|
|
1,1 |
|
|
|
|
0,185 |
|
|
|
|
|
1,05 |
|
|
|
|
0,185 |
|
|
|
|
|
1,05 |
|
|
|
|
0,19 |
|
|
|
|
|
1,1 |
|
|
|
|
0,19 |
|
|
|
|
|
1,1 |
|
|
3 |
10 |
0,42 |
0,413 |
0,00123 |
|
7 |
x |
0,45 |
0,455 |
0,0053 |
|
|
0,41 |
|
|
|
|
|
0,46 |
|
|
|
|
0,41 |
|
|
|
|
|
0,45 |
|
|
|
|
0,41 |
|
|
|
|
|
0,46 |
|
|
|
|
0,42 |
|
|
|
|
|
0,45 |
|
|
|
|
0,41 |
|
|
|
|
|
0,46 |
|
|
|
|
0,41 |
|
|
|
|
|
0,46 |
|
|
|
|
0,41 |
|
|
|
|
|
0,45 |
|
|
4 |
15 |
0,56 |
0,556 |
0,00518 |
|
|
|
|
|
|
|
|
0,55 |
|
|
|
|
|
|
|
|
|
|
0,56 |
|
|
|
|
|
|
|
|
|
|
0,55 |
|
|
|
|
|
|
|
|
|
|
0,55 |
|
|
|
|
|
|
|
|
|
|
0,56 |
|
|
|
|
|
|
|
|
|
|
0,56 |
|
|
|
|
|
|
|
|
|
|
0,56 |
|
|
|
|
|
|
|
|
Dyskusja wyników:
1. Krzywa wyznaczona doświadczalnie w pełni pokrywa się z krzywą teoretyczną. Oznacza to, że spełnione jest prawo absorpcji mówiące, że absorbancja jest proporcjonalna do grubości warstwy absorbującej, jeśli wiązka promieniowania monochromatycznego przechodzi przez jednorodny ośrodek absorbujący, przy czym w spektroskopii absorpcji atomowej absorbancja zależy od liczby wolnych atomów w środowisku absorbującym.![]()
Średni błąd pomiarów wynosi:
![]()
co stanowi dopuszczalną granicę błędu. Zatem wartość nieznanego stężenia miedzi wyznaczoną metodą krzywej wzorcowej można uważać za dokładną. Tak mała wartość błędu pomiaru świadczy o dużej precyzyjności metody absorpcji spektroskopii atomowej AAS.
3. Dwa punkty odbiegają znacznie położeniem od punktów znajdujących się na prostej A = f(c), co sprawia, że poprowadzenie krzywej uwzględniając wszystkie punkty zwiększy błąd odczytu wartości stężenia miedzi.
![]()
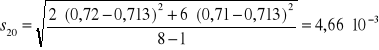
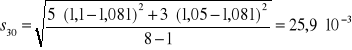
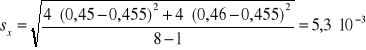
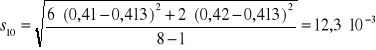
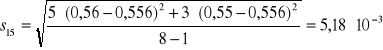
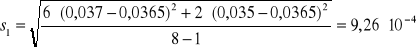
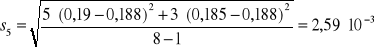
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
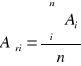
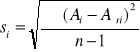
![]()
![]()
![]()
Wyszukiwarka
Podobne podstrony:
ćw 4 Profil podłużny cieku
biofiza cw 31
Kinezyterapia ćw synergistyczne
Cw 1 ! komorki
Pedagogika ćw Dydaktyka
Cw 3 patologie wybrane aspekty
Cw 7 IMMUNOLOGIA TRANSPLANTACYJNA
Cw Ancyl strong
Cw 1 Zdrowie i choroba 2009
Rehabilitacja medyczna prezentacja ćw I
ćw 2b
Ćw 3 Elektorforeza Bzducha
ćw 3 Projektowanie drenowania
ćw 3 dla studentów
więcej podobnych podstron