Spin
Z momentem pędu elektronu w atomie (lub cząsteczce), podobnie jak z momentem pędu każdego innego ładunku, związany jest pewien moment magnetyczny. Okazuje się, że w mechanice kwantowej, nawet w sytuacji, gdy moment pędu (orbitalny) elektronu jest równy zeru (jak np. dla elektronu opisywanego orbitalem typu s), elektron wykazuje pewien własny moment pędu (o innej naturze).
Tego rodzaju moment pędu, tzw. wewnętrzny moment pędu, nazywamy spinem.
Konsekwencją faktu, że elektron posiada określony spin (kręt) jest pojawienie się magnetycznego momentu elektronu.
Spinem nazywamy dodatkowy wewnętrzny moment pędu, który nie jest związany z ruchem orbitalnym elektronu.
Początkowo podejrzewano, że spin elektronu wynika z ruchu obrotowego elektronu wokół własnej osi (stąd angielskie słowo „spin” i polskie słowo „kręt”). Okazuje się jednak, że gdyby spin elektronu wynikał rzeczywiście z ruchu wirowego elektronu (wokół własnej osi), elektron musiałby obracać się z prędkością 300 razy większą od prędkości światła, co jak wiadomo ze szczególnej teorii względności Einsteina, jest niemożliwe.
Wniosek: spin elektronu nie ma odpowiednika w fizyce klasycznej
Spin (czyli spinowy moment pędu) ma charakterystykę podobną w sensie matematycznym do orbitalnego momentu pędu elektronu.
A zatem:
Spinowy moment pędu (S), podobnie jak orbitalny moment pędu (M) jest wielkością wektorową: S=i∙Sx+j∙Sy+k∙Sz
Zgodnie z zasadą nieokreśloności Heisenberga, możliwe jest jednoczesne wyznaczenie (pomiar) kwadratu całkowitego spinu (S2) oraz składowej zetowej spinu (Sz).
Podobnie jest dla orbitalnego momentu pędu, dla którego możemy jednocześnie wyznaczyć tylko kwadrat długości (M2) i jedną składową (umownie: zetową) Mz.
Rzut wektora spinu na wyróżnioną oś układu współrzędnych wynosi msħ (podobnie jak rzut wektora M na pewną oś wynosi mħ).
Rzut wektora spinu na wyróżnioną oś układu wynosi zawsze +½ ħ albo -½ ħ (czyli ms=½ lub ms= -½).
Kwadrat spinu elektronu jest zawsze równy ¾ ħ2, natomiast kwadrat orbitalnego momentu pędu wynosi l(l+1)ħ2.
Przez analogię do orbitalnego momentu pędu, kwadrat spinu zapisujemy jako ½∙(½+1)ħ albo s∙(s+1)ħ
(gdzie s=½).
Wprowadzamy zatem dla elektronu w atomie dwie nowe (dodatkowe) liczby kwantowe, które określają jego spin:
magnetyczną spinową liczbę kwantową ms (odpowiednik magnetycznej liczby kwantowej m), oraz
spinową liczbę kwantową s (odpowiednik orbitalnej liczby kwantowej l).
Dopuszczalne wartości liczb kwantowych s i ms :
s=½ ms=±½
Stan elektronu w atomie jest zatem opisywany zestawem pięciu liczb kwantowych: n, l, m, s, ms
Ponieważ jednak wartość liczby kwantowej s wynosi dla elektronu zawsze ½, podawanie tej liczby nie jest konieczne (tylko dla elektronu!).
Wniosek: opis stanu elektronu za pomocą funkcji falowej ψnlm(r,θ,φ) nie jest wystarczający i dlatego wprowadzamy jeszcze funkcję spinową σ, która zależy od liczb kwantowych s i ms i dla której argumentem jest tzw. współrzędna spinowa.
Ponieważ s=½, zamiast pisać σsms zapisujemy w skrócie σms
Ponadto, ponieważ ms=±½, możliwe są jedynie dwie funkcje spinowe: σ½ oraz σ-½
Wobec tego stosujemy zapis α (dla σ½) oraz β (dla σ-½).
σ½ ≡ α σ-½ ≡ β
Czyli:
Jeżeli wartość spinowej magnetycznej liczby kwantowej ms
wynosi ½ mówimy, że elektron opisywany jest spinową funkcją α.
Podobnie, jeżeli wartość spinowej magnetycznej liczby kwantowej ms wynosi -½ mówimy, że elektron opisywany jest spinową funkcją β.
Możemy zatem zapisać dwa dodatkowe równania własne dla atomu wodoru:
![]()
![]()
Po zamianie symboli i wprowadzeniu s=½ mamy dla kwadratu spinu
![]()
oraz ![]()
natomiast dla składowej zetowej wektora spinu:
![]()
oraz ![]()
Pełny opis elektronu w atomie jest dany przez iloczyn funkcji ψnlm(r,θ,φ) (zależącej od współrzędnych przestrzennych) oraz funkcji σsms (zależącej od współrzędnej spinowej).
Funkcję ψnlm(r,θ,φ) nazywamy przestrzenną funkcją falową albo orbitalem.
Funkcję σsms nazywamy spinową funkcją falową.
Iloczyn funkcji przestrzennej ψ i funkcji spinowej σ nazywamy spinorbitalem. A zatem spinorbital φ jest dany przez wyrażenie:
φnlmsms = ψnlm(r,θ,φ)∙ σsms
Ponieważ z jednego orbitala ψ można uzyskać dwa spinorbitale:
ψ∙α oraz ψ∙β, mówimy często o „orbitalach alfa” (czyli ψ∙α) lub „orbitalach beta” (czyli ψ∙β).
Elektron opisywany spinową funkcją α oznaczamy przez ↑
natomiast elektron opisywany spinową funkcją β przez ↓
Orbital oznaczamy zazwyczaj symbolem □
Warto pamiętać, że nie tylko elektrony obdarzone są spinem. Spin posiadają również np. neutrony oraz jądra atomowe (co jest wykorzystywane w różnych dziedzinach chemii, fizyki i medycyny).
Spin w układach wieloelektronowych
W układach gdzie występuje więcej niż jeden elektron, liczby kwantowe związane ze spinem zapisujemy przez analogię jako
S oraz Ms. Mówimy wówczas o całkowitym wektorze spinu (dotyczącym jednocześnie wszystkich elektronów).
Liczba S dla układu wieloelektronowego wynika z różnicy między elektronami opisywanymi funkcją α i funkcją β.
Jeżeli np. tyle samo elektronów w układzie opisywanych jest funkcjami α i β, to całkowity spin S wynosi 0.
Jeżeli różnica wynosi 1 (np. mamy trzy elektrony α i dwa β lub odwrotnie), to całkowity spin S wynosi ½.
Jeżeli różnica wynosi 2 (np. mamy trzy elektrony β i jeden α lub odwrotnie), to całkowity spin S wynosi 1 (... i tak dalej).
Liczbę Ms dla układu wieloelektronowego obliczamy poprzez
sumowanie (po wszystkich elektronach) liczb ms
Multipletowość układu określamy obliczając wartość 2∙S+1.
Np. dla S=0 , multipletowość wynosi 1 (gdyż 2∙0+1=1)
Mówimy wówczas o stanie singletowym.
Dla S=½ , multipletowość wynosi 2 (gdyż 2∙½+1=2)
Mówimy wówczas o stanie dubletowym.
Dla S=1 , multipletowość wynosi 3 (gdyż 2∙1+1=3)
Mówimy wówczas o stanie trypletowym.
Dla S=1½ , multipletowość wynosi 4 (gdyż 2∙1½+1=4)
Mówimy wówczas o stanie kwartetowym. (... i tak dalej).
Multipletowość nazywamy degeneracją spinową, gdyż określa ona ile jest możliwych wartości rzutu wektora całkowitego spinu (na określony kierunek w przestrzeni). Jeżeli całkowity spin określa liczba kwantowa S to mamy właśnie 2S+1 możliwych wartości rzutu.
Oczywiście dla układu jednoelektronowego, mamy S=s=½, czyli będzie to zawsze stan o multipletowości 2 (stan dubletowy, dublet).
Operatory związane ze spinem
Ponieważ spin nie ma odpowiednika w fizyce klasycznej, operatorów spinu nie można utworzyć w oparciu o reguły Jordana.
Dlatego, konstruujemy je (na zasadzie postulatu) w taki sposób, aby obliczane wartości średnie składowej zetowej oraz kwadratu wektora spinu były zgodne z doświadczeniem:
Pamiętając, że spin jest wektorem: S=i∙Sx+j∙Sy+k∙Sz
definiujemy następujące operatory składowych spinu (poprzez podanie w jaki sposób działają one na funkcje spinowe α i β) :
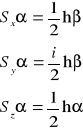
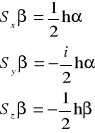
Przybliżenie Borna-Oppenheimera
Atom wodoru (jony wodoropodobne) - najbardziej skomplikowane układy, dla których równanie Schrödingera można rozwiązać w sposób dokładny.
Przybliżenie Borna-Oppenheimera zakłada, że jądra atomowe są „nieskończenie ciężkie”, czego konsekwencją jest to, że funkcja falowa cząsteczki jest iloczynem funkcji elektronowej (zależnej parametrycznie od położenia jąder) i funkcji falowej jądrowej.
A zatem, rozwiązujemy problem własny dla funkcji zależącej od położenia elektronów, dla zadanego (zamrożonego) położenia jąder. Uzasadnienie: wobec niewielkiej masy elektronów w porównaniu z masą jąder, rozkład elektronów w cząsteczce zależy w przybliżeniu od chwilowego rozkładu jąder, natomiast nie zależy on od ruchu jąder.
Hamiltonian elektronowy
Na podstawie przybliżenia BO można zdefiniować tzw. hamiltonian elektronowy:
![]()
gdzie Tel oznacza energię kinetyczną elektronów, Uj-el jest energią potencjalną oddziaływania elektronów z jądrami (przyciąganie kulombowskie), Uel-el jest energią potencjalną wzajemnego oddziaływania elektronów (odpychanie kulombowskie), Uj-j jest energią potencjalną wzajemnego oddziaływania jąder (odpychanie kulombowskie).
Hamiltonian elektronowy w porównaniu z pełnym hamiltonianem nie zawiera członu Tj odpowiadającego za energię kinetyczną jąder.
Przybliżenie BO jest powszechnie stosowane we współczesnej chemii kwantowej.
Energia elektronowa
Wartość własna (energia) w równaniu Schrödingera z hamiltonianem elektronowym (tzw. elektronowe równanie Schrödingera) nazywana jest energią elektronową (Eel).
![]()
Po rozwiązaniu powyższego równania i uzyskaniu Eel (dla określonej konfiguracji jąder) możemy otrzymać energię całkowitą E poprzez dodanie do Eel członu odpowiadającego odpychaniu międzyjądrowemu.
Przybliżenie jednoelektronowe
Po wprowadzeniu przybliżenia BO mamy do czynienia z zagadnieniem własnym ![]()
. Jest ono jednak w dalszym ciągu zbyt skomplikowane i niezbędne jest wprowadzenie kolejnego przybliżenia, opartego na modelu cząstek niezależnych.
W przybliżeniu jednoelektronowym każdemu elektronowi w atomie (lub cząsteczce) przyporządkowujemy jednoelektronową funkcję falową nazywaną spinorbitalem.
W tym ujęciu, ruch każdego z elektronów rozpatrujemy niezależnie.
Zakaz Pauliego (pierwsze sformułowanie)
W układzie wieloelektronowym nie może być dwóch elektronów znajdujących się w jednakowym stanie.
Alternatywnie:
Żadne dwa elektrony nie mogą być opisane takim samym spinorbitalem (czyli takim samym zespołem liczb kwantowych określających spinorbital).
Metoda Hartree - iloczynowa funkcja falowa
A zatem, np. dla układu trzech elektronów (atom litu) mielibyśmy pełną funkcję falową ψ=φ1(1)∙φ2(2)∙φ3(3) , gdzie φk(k) oznacza k-ty spinorbital opisujący ruch k-tego elektronu (czyli zależący od współrzędnych k-tego elektronu).
Założenie iloczynowej funkcji falowej (niepoprawne) jest intuicyjne i wynika z tego, że prawdopodobieństwo zdarzeń niezależnych jest równe iloczynowi prawdopodobieństw.
Na iloczynowej funkcji falowej oparta była stosowana w przeszłości metoda Hartree.
Wada metody Hartree: postać funkcji falowej jest sprzeczna z zasadą nieodróżnialności cząstek identycznych (pamiętamy, że funkcja opisująca układ elektronów musi być antysymetryczna względem permutacji elektronów). Funkcja iloczynowa nie wykazuje natomiast żadnej symetrii względem permutacji elektronów (patrz ćwiczenia).
Wyznacznik Slatera
Okazuje się, że wyznacznikowa funkcja falowa posiada odpowiednią symetrię (tzn. jest antysymetryczna względem permutacji elektronów), jak również ma inne, wygodne własności.
Wyznacznik zbudowany ze spinorbitali, który można następnie rozwinąć w antysymetryczną funkcję falową, nazywamy wyznacznikiem Slatera
Wyznacznik Slatera dla układu n-elektronowego:
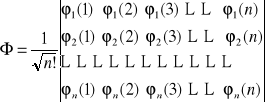
(sposób konstrukcji wyznacznika Slatera dla dowolnej konfiguracji elektronowej - patrz ćwiczenia).
Np. dla układu dwuelektronowego, wyznacznik jest bardzo prosty:
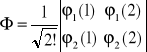
i można go rozwinąć otrzymując funkcję:
![]()
Własności funkcji wyznacznikowej
Poprawna symetria względem permutacji elektronów (antysymetryczność) - uzasadnienie: zamiana (permutacja) dwóch elektronów byłaby równoważna zamianie kolumn wyznacznika, co jak wiadomo z algebry liniowej, powoduje zmianę znaku.
Unormowanie - uzasadnienie: współczynnik 1/√n! zapewnia unormowanie funkcji wyznacznikowej.
Spełnianie zakazu Pauliego - uzasadnienie: jeżeli mielibyśmy dwa elektrony opisywane tym samym orbitalem, to dwa wiersze wyznacznika byłyby jednakowe, czyli wyznacznik byłby równy zeru (co wynika z własności matematycznych wyznacznika). Funkcja falowa równa tożsamościowo zeru jest niemożliwa, gdyż oznaczałoby to, że opisywany układ nie istnieje.
Przybliżenie jednoelektronowe - stanowi podstawę spojrzenia na strukturę elektronową atomów i molekuł, na nim opierają się takie pojęcia jak: orbitale, konfiguracja elektronowa, powłokowy model atomu, energie orbitalne, itp.
Zakaz Pauliego (drugie sformułowanie)
Dwa elektrony nie mogą znajdować się w tym samym miejscu przestrzeni konfiguracyjno-spinowej (czyli w tym samym miejscu przestrzeni konfiguracyjnej (x,y,z) i spinowej (ten sam spin: ↑ lub ↓).
Całka kulombowska J, całka wymienna K i całka rdzeniowa I
Rozwiązanie równania Schrödingera z hamiltonianem elektronowym (w przybliżeniu BO i w przybliżeniu jedno-elektronowym) prowadzi m.in. do trzech rodzajów całek, które pojawiają się w wyrażeniu na energię elektronową:
Całka Jpq, nazywana całką kulombowską:
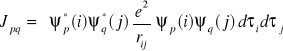
Całka Kpq, nazywana całką wymienną:
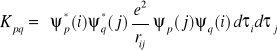
Całka Ip, nazywana całką rdzeniową:
![]()
Definicje tych całek będą wykorzystane przy omawianiu
metody Hartree-Focka.
Konfiguracje elektronowe atomów
Konfiguracją elektronową nazywamy przyporządkowanie elektronów określonym poziomom energetycznym.
Patrz podręcznik Kołosa, rozdział 8:
(i) energie orbitalne, (ii) powłoki i podpowłoki elektronowe, (iii) układy zamkniętopowłokowe, (iv) układy otwartopowłokowe, (v) reguły Hunda.
Termy atomowe i molekularne
Termami atomowymi (molekularnymi) nazywamy rzeczywiste (obserwowane w spektroskopii) poziomy energetyczne atomu (molekuły).
Wyznaczanie termów atomowych dla danej konfiguracji elektronowej - patrz ćwiczenia oraz podręcznik Kołosa (rozdział 9)
87
Wyszukiwarka
Podobne podstrony:
wykladChK-03, Chemia UŁ, teoretyczna wykład
wykladChK-10, Chemia UŁ, teoretyczna wykład
wykladChK-11, Chemia UŁ, teoretyczna wykład
wykladChK-15, Chemia UŁ, teoretyczna wykład
wykladChK-12, Chemia UŁ, teoretyczna wykład
wykladChK-13, Chemia UŁ, teoretyczna wykład
wykladChK-14, Chemia UŁ, teoretyczna wykład
wykladChK-04, Chemia UŁ, teoretyczna wykład
wykladChK-09, Chemia UŁ, teoretyczna wykład
wykladChK-05, Chemia UŁ, teoretyczna wykład
wykladChK-01, Chemia UŁ, teoretyczna wykład
wykladChK-02, Chemia UŁ, teoretyczna wykład
wyklad 1 1 2008, CHEMIA UŁ, 3 rok, Fizyczna, różne
równowagi protolityczne aminokwasów, CHEMIA UŁ, 3 rok, Biochemia
Cwiczenie 6a, Chemia UŁ, Elektrochemia
sciaga I koło, CHEMIA UŁ, 4 rok, Krystalografia
krystalografia kolokwium I LAB, CHEMIA UŁ, 4 rok, Krystalografia
Kryształki lab ściąga, CHEMIA UŁ, 4 rok, Krystalografia
więcej podobnych podstron