CHROMATOGRAFIA GAZOWA.
CG - 1 - oznaczanie THM - ów w wodzie
Celem ćwiczenia jest ilościowe oznaczanie stężenia trihalogenometanów - chloroformu, bromodichlorometanu, chlorodibromometanu i bromoformu w próbkach wody wodociągowej.
Aparatura i odczynniki.
1) Chromatograf gazowy wyposażony w następujące elementy:
-dozownik
-detektor
-komputer
2) Mikrostrzykawka Hamiltona 1ul.
3)Probówki miarowe 15 ml ze szlifem + korki
4)Pipety Moh'ra 10 ml i 1 ml
5)Pentan do chromatografii gazowej
Wykonanie ćwiczenia:
1.Pobranie prób z sieci wodociągowej
Próbki wody wodociągowej pobiera się do butelek około 0.5 l w dniu wykonywania ćwiczenia. Przed napełnieniem butelki należy na kilka minut odkręcić kran i odczekać (4 - 5 minut) aż woda została w rurach wodociągowych spłynie. Butelkę napełnić tak, aby nie było w niej powietrza i szczelnie zamknąć.
2. Przygotowanie próbek do analizy:
a)za pomocą pipety pobrać z każdej butelki po 10 ml wody wodociągowej i przenieść do probówek miarowych.
b)do każdej probówki z próbką wody wodociągowej dodać po 1 ml pentanu i zamknąć szczelnie korkiem.
3. Ekstrakcja pentanem
a)intensywnie wytrząsać probówkę przez około minutę
b)pozostawić probówkę w statywie w celu rozdzielenia warstw.
4. Nastrzyk próbki i rejestracja chromatogramu:
a)po rozdzieleniu warstwy organicznej pobrać za pomocą mikropipety 1 ul warstwy pentalu.
b)wprowadzić igłę strzykawki do komory dozownika i wykonać nastrzyk, jednocześnie wcisnąć klawisz Start na panelu sterowania , rejestracja chromatogramu odbywa się w pełni automatycznie i jest sterowana przez komputer.
c)strzykawkę pozostawić na około 3 minuty w komorze dozownika obserwując rejestrowany chromatogram
d)po zakończeniu analizy automatycznie wywoływana jest procedura przygotowująca chromatograf do kolejnej analizy.
ADSORPCJA
A -1..
Wyznaczanie izotermy adsorpcji dla układu ciecz - ciało stałe
Celem cwiczenia jest wyznaczenie izotermy adsorpcji Freundlicha kwasu octowego na węglu aktywnym.
Zadanie sprowadza się do wyznaczenia doswiadczalnego współczynników k i 1/n w równaniu Freundlicha dla konkretnego węgla aktywnego. Należy ustalić zależność ilości zaadsorbowanego kwasu na jednostkę masy, w zależności od stężenia tego kwasu.
Wykonanie ćwiczenia:
W kolbach miarowych o pojemności 100 cm należy sporządzić 6 roztworów kwasu octowego o następujących stężeniach: 0.3; 0.25;0.2;0.15;0.1;0.05 mol/ dm3 w ilości po 100 cm3 każdego (korzystając z roztworu kwasu octowego o stężeniu 0.5 mol/ dm3). Otrzymane roztwory mianuje się roztworem NaOH o c= 0.1 mol/dm3 wobec fenoloftaleiny jako wskaźnika. W tym celu należy odmierzyć 10 cm3 roztworu kwasu octowego o danym stężeniu do suchej kolby stożkowej i miareczkować dwukrotnie. Analogicznie wykonać miareczkowanie pozostałych roztworów kwasu octowego.
Korzystając z wagi technicznej a następnie analitycznej należy dokładnie odważyć na folii aluminiowej 6 odważek wegla (po około 2 g każda). Nastepnie odważki wegla wsypać kolejno do 6 kolbek ze szlifem. Później do tych kolbek należy dodać po 50 cm3 każdego z przygotowanych roztworów kwasu octowego. Kolbki zamknąć szczelnie korkiem i zawartość wytrząsać przez około 10 minut na wytrząsarce. Otrzymane zawiesiny przesączyć, z każdego przesączu pobrać do miareczkowania próbki o objetości 10 cm3, celem oznaczenia stężenia równowagowego kwasu octowego (niezaadsorbowanego). Wszystkie miareczkowania wykonać podwójnie.
Opracowanie wyników:
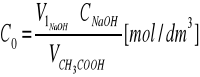
Z róznicy stężeń przed i po adsorpcji należy obliczyć X, to jest liczbę miligramów zaadsorbowanego kwasu octowego na węglu aktywnym.
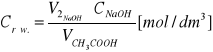
![]()
V1, V2 - objetości zasady zużyte na miareczkowanie
VCH3COOH - objetośc próbki kwasu octowego 10 cm3
Vkw. - objętośc kwasu zużyta do adsorpcji (0.05 dm3)
60 - M kwasu octowego
Wyszukiwarka
Podobne podstrony:
Wprowadzenie do 44 ch fiz, Studia PŁ, Ochrona Środowiska, Chemia, fizyczna, laborki, wszy, Ch f, bon
Ch w2 13.10 (Naprawiony), Studia (Geologia,GZMIW UAM), I rok, Chemia
Ch w9 8.12, Studia (Geologia,GZMIW UAM), I rok, Chemia
CH.F.L9, Studia, Politechnika
I.CH.kolokwiumB, Nieorganiczna, chemia2, Arkusze powtórzeniowe, Pobieranie1, studia 1.2, testy (Bato
Ch w8 1.12, Studia (Geologia,GZMIW UAM), I rok, Chemia
Ch w1 6.10, Studia (Geologia,GZMIW UAM), I rok, Chemia
I.CH.kolokwium, Nieorganiczna, chemia2, Arkusze powtórzeniowe, Pobieranie1, studia 1.2, testy (Baton
Ch, studia, PK - WIŚ -UCZ, Semestr I, Chemia
Ch w10 15.12, Studia (Geologia,GZMIW UAM), I rok, Chemia
Chemia srod pytania i odp, Studia, Ch. Środowiska
CH.F.L.24, Studia, Politechnika
Ch w4 10.11, Studia (Geologia,GZMIW UAM), I rok, Chemia
Ch w3 27.10, Studia (Geologia,GZMIW UAM), I rok, Chemia
CH.F.Li.5, Studia, Politechnika
Ch w6 19.11, Studia (Geologia,GZMIW UAM), I rok, Chemia
CH.F.L.22, Studia, Politechnika
Ch w7 24.11, Studia (Geologia,GZMIW UAM), I rok, Chemia
więcej podobnych podstron