Robert Maniura
Sprawozdanie z ćwiczenia nr 21: Wyznaczanie masy cząsteczkowej metodą ebuliometryczną.
1. Wstęp teoretyczny:
Pośród rozlicznych właściwości roztworów istnieje jedna ich grupa, której wspólną cechą jest ich zależność od liczby cząsteczek (moli) substancji rozpuszczonej. Do tych, koligatywnych, właściwości roztworów zaliczamy: obniżenie temperatury krzepnięcia roztworu w stosunku do czystego rozpuszczalnika, podwyższenie temperatury wrzenia roztworu w stosunku do czystego rozpuszczalnika oraz ciśnienie osmotyczne roztworów. Właściwości te wynikają z faktu, że w procesie tworzenia roztworu obniża się jego entalpia swobodna.
Rozważmy przykładowo zjawisko zmiany temperatury krzepnięcia substancji przez dodatek substancji rozpuszczonej. Metoda fizykochemiczna oparta na tym zjawisku nosi nazwę kriometrii.
Niech roztwór dwuskładnikowy o składzie (x1, x2) w stanie ciekłym ma temperaturę początkową Tp, gdzie x1 oznacza ułamek molowy rozpuszczalnika. Przy obniżaniu temperatury, w temperaturze Tk rozpocznie się wydzielanie z roztworu czystego rozpuszczalnika. Zgodnie z regułą faz Gibbsa, liczba stopni swobody (n) w tym dwuskładnikowym ( = 2) i dwufazowym ( = 2) układzie wynosi 2:
n = - + 2 = 2
Jednym z nich jest ciśnienie, drugim zaś temperatura lub skład. Ponieważ ciśnienie jest ustalone (p = const) zatem jedynym stopniem swobody jest temperatura lub skład. Te dwa parametry nie mogą więc być niezależne - musi istnieć równanie podające zależność temperatury krzepnięcia od składu roztworu. Znajdźmy to równanie.
Potencjał chemiczny wydzielającego się w temperaturze Tk czystego rozpuszczalnika jest równy standardowemu potencjałowi chemicznemu w tej temperaturze:
![]()
Potencjał chemiczny rozpuszczalnika w roztworze (faza ciekła) zależy od jego aktywności a1:
![]()
W stanie równowagi te potencjały chemiczne są sobie równe:
![]()
lub ![]()
Różnica (![]()
) jest równa zmianie entalpii swobodnej krystalizacji jednego mola czystego rozpuszczalnika Gk w temperaturze Tk:
![]()
Zgodnie z II zasadą termodynamiki:
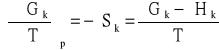
(1)
zaś różniczkując powyższe równanie obustronnie względem temperatury mamy:
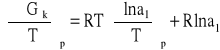
(2)
Przyrównanie prawych stron równań (1)i (2) prowadzi do zależności:
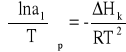
(3)
w której Hk oznacza zmianę entalpii w procesie krystalizacji 1 mola rozpuszczalnika.
Całkowanie równania (3) uzależnione jest od zakresu temperatur. Dla temperatur Tk niezbyt odległych od temperatury krystalizacji czystego rozpuszczalnika To, można przyjąć entalpię krystalizacji Hk za wielkość stałą, niezależną od temperatury. Przy takim założeniu całkowanie równania (3) począwszy od temperatury krystalizacji czystego rozpuszczalnika To (w której a1 = 1) do temperatury krystalizacji roztworu Tk (w której aktywność rozpuszczalnika w roztworze wynosi a1) prowadzi kolejno:
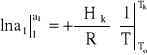
(4)
do równania:
![]()
(5)
Jeżeli roztwór jest ponadto dostatecznie rozcieńczony, to aktywność rozpuszczalnika można zastąpić przez jego ułamek molowy x1, a ponieważ:
x1 = 1 - x2
zatem dla małych wartości x2:
-lnx1 = -ln(1 - x2) = x2
gdzie x2 jest ułamkiem molowym substancji rozpuszczonej:
![]()
(6)
W równaniu tym m1 i m2 oznaczają masy rozpuszczalnika i substancji rozpuszczonej, zaś M1 i M2 odpowiednie masy cząsteczkowe. Zatem równanie (5) przyjmie postać:
![]()
(7)
Wyrażając stężenie roztworu w skali molarności m [mol/l000 g] rozpuszczalnika mamy:
![]()
(8)
a stąd i z równania (6):
![]()
(9)
Oznaczając obniżenie temperatury krzepnięcia roztworu w stosunku do temperatury krzepnięcia czystego rozpuszczalnika przez Tk:
Tk = To - Tk
oraz przyjmując, że:
![]()
otrzymujemy z równań (7) i (9):
Tk = Kkm (10)
gdzie stała Kk zwana stałą kriometryczną zawiera wszystkie wielkości stałe:
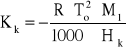
(11)
Znak „-„ w równaniu na stalą krioskopową pochodzi stąd, że w rozważaniach posłużono się entalpią krystalizacji, a nie jak zwykle ciepłem topnienia (Hk < 0).
![]()
(12)
Stała kriometryczna jest równa obniżeniu temperatury krzepnięcia roztworu zawierającego w 1000 g rozpuszczalnika 1 mol substancji rozpuszczonej. Jest to wielkość charakterystyczna dla rozpuszczalnika.
Przyjęte założenia ograniczają stosowalność równania (10) jedynie do roztworów rozcieńczonych. Przy roztworach bardziej stężonych założenia te należy odrzucić.
Zgodnie z prawem Kirchhoffa entalpię krystalizacji rozpuszczalnika w temperaturze krzepnięcia roztworu Tk należy przedstawić za pomocą równania:
Hk = Ho + Cp(Tk - To) = Ho - Cp*Tk (13)
w którym Ho oznacza entalpię krystalizacji rozpuszczalnika w temperaturze krystalizacji czystego rozpuszczalnika To, zaś Cp jest różnicą ciepeł molowych stałego i ciekłego rozpuszczalnika. Wprowadzając równanie (13) dorównania (5) oraz rezygnując z przybliżenia ![]()
otrzymuje się:
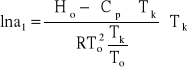
(14)
Utrzymując założenie o idealnym zachowaniu rozpuszczalnika można równanie (14) doprowadzić do postaci:
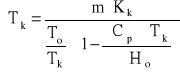
(15)
w której mianownik określa poprawkę w stosunku do równania (10). Jeżeli Tk jest rzędu 2 - 3°, to błąd wynikający z nieuwzględnienia wyrażenia w mianowniku nie przekracza 1 - 2 %.
Podstawowe równanie kriometrii (10) spełnione jest jedynie przez idealne roztwory nieelektrolitów. W rozcieńczonych roztworach mocnych elektrolitów w miejsce molarności we wzorze (10) należy stosować iloczyn l*m, gdzie l jest liczbą jonów tworzących się w wyniku dysocjacji cząsteczki elektrolitu. W rozcieńczonych roztworach słabych elektrolitów należy uwzględnić dysocjację; w miejsce stężenia molarnego -dla słabego elektrolitu binarnego - należy wstawić wartość m(1 + ), gdzie jest stopniem dysocjacji.
W bardziej stężonych roztworach elektrolitów należy uwzględnić współczynniki aktywności.
Termodynamiczną konsekwencją procesu tworzenia roztworu (dodania substancji rozpuszczonej do rozpuszczalnika) jest spadek entalpii swobodnej roztworu. Spadek entalpii swobodnej prowadzi w przypadku roztworów doskonałych i większości roztworów rzeczywistych do obniżenia prężności par rozpuszczalnika nad roztworem w stosunku do prężności par nad czystym rozpuszczalnikiem. Konsekwencją tego zjawiska jest obniżanie temperatury krzepnięcia roztworu w stosunku do temperatury krzepnięcia czystego rozpuszczalnika, a także podwyższanie temperatury wrzenia roztworu w stosunku do temperatury wrzenia czystego rozpuszczalnika. Na zjawisku podwyższania temperatury wrzenia roztworu oparta jest fizykochemiczna metoda badawcza zwana ebuliometrią.
Podobnie jak w kriometrii, wielkość podwyższenia temperatury wrzenia w ebuliometrii (Tw) związana jest ze stężeniem roztworu (m). Rozważanie analogiczne, jak przy wyprowadzeniu równania (10) prowadzi do równania:
Tw = KEm (16)
Stała ebuliometryczna KE występująca w tym równaniu określona jest równaniem analogicznym do (11):
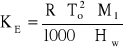
(17)
w którym To jest odpowiednio temperaturą wrzenia czystego rozpuszczalnika, zaś Hw molowym ciepłem parowania. Stała ebuliometryczna podająca podwyższenie temperatury wrzenia obserwowane dla roztworu 1 molarnego, jest - podobnie jak stała kriometryczna wielkością charakterystyczną dla rozpuszczalnika i niezależną od rodzaju substancji rozpuszczonej.
Zastrzeżenia czynione przy wyprowadzaniu równania (10) słuszne są także dla podstawowego równania ebuliometrii (17).
2. Opracowanie wyników:
Masy próbek obliczam z następującej zależności:
![]()
gdzie: ms - masa substancji; mpk - masa kolby z naważką substancji; mk - masa pustej kolby.
naważka I: ms = 54,3815 - 51,3645 = 3,017 g
naważka II: ms = 53,3608 - 51,8085 = 1,5523 g
naważka III: ms = 49,2515 - 47,1826 = 2,0689 g
naważka IV: ms = 48,9855 - 46,8677 = 2,1178 g
Równanie termistora jest następujące:
![]()
z równania termistora można obliczyć temperaturę wrzenia rozpuszczalnika i roztworów (![]()
= -9,2872 ± 0,0571; b = -3573,2239 ± 21,2883):
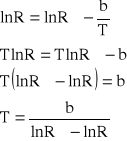
Temperatura wrzenia (R = 1,371 k) dla czystego rozpuszczalnika (H2O) wynosi: Twrz.(w) = 372,10 K.
Temperatura wrzenia (R = 1,361 k) dla roztworu z naważką I wynosi: Twrz.(1) = 372,39 K.
Temperatura wrzenia (R = 1,355 k) dla roztworu z naważką I, II i III wynosi: Twrz.(2) = 372,56 K.
Temperatura wrzenia (R = 1,352 k) dla roztworu z naważką I, II, III i IV wynosi: Twrz.(3) = 372,65 K.
Molarność badanych roztworów i masa molowa substancji:
Molarność roztworów obliczyć można z następującej zależności:
![]()
gdzie: Tw - przyrost temperatury wrzenia (Tw = Twrz.(x) - Twrz.(w); x - oznacza odpowiedni pomiar: 1, 2, 3); KE - stała ebuliometryczna wody (KE = 0,521 [K*kg/mol]); m - molarność roztworu.
Masa molowa substancji:
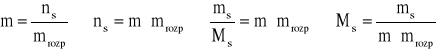
gdzie: m - molarność roztworu; ns - liczba moli substancji; mrozp - masa rozpuszczalnika [kg]; ms - masa substancji w roztworze [g]; Ms - masa molowa substancji.
Pomiar |
Masa substancji w roztworze ms [g] |
Przyrost temperatury Tw [K] |
Molarność roztworu [mol/kg] |
Masa molowa [g/mol] |
1 |
naważka I ms = 3,017 |
0,29 |
0,5566 |
54,20 |
2 |
naważka I + II + III ms = 6,6382 |
0,46 |
0,8829 |
75,19 |
3 |
naważka I + II + III + IV ms = 8,756 |
0,55 |
1,0557 |
82,94 |
Średnia masa molowa substancji wynosi 70,78 [g/mol]
W przypadku małej liczby pomiarów średnia może różnić się dość znacznie od wartości prawdziwej. Dlatego wygodniej jest wtedy określić przedział, w którym wartość rzeczywista znajduje się z dużym prawdopodobieństwem. Taki przedział nazywamy przedziałem ufności. Wyznaczam przedział ufności dla prawdopodobieństwa 95% (p = 0,95 ; α = 0,05)
μ = X + t * s
gdzie: X - średnia arytmetyczna; t - wartość funkcji Studenta, wartość współczynnika „t” dla prawdopodobieństwa 95% (dla 3 pomiarów), t = 4,303 dla K = n - 1 = 2
s - odchylenie standardowe średniej arytmetycznej, obliczane ze wzoru:
s = 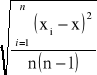
gdzie: xi - kolejne wyniki; x - średnia arytmetyczna wyników; n - ilość wyników (n=5).
s = 8,39 ![]()
Masa molowa substancji wynosi 70,78 ± 36,1 [g/mol]
Porównanie z wartością tablicową: masa molowa tiomocznika wynosi 76,1226 [g/mol] zaś wartość eksperymentalna wynosi 70,78 [g/mol] a błąd procentowy wynosi 7,02 %.
3. Wnioski:
Cel ćwiczenia (wyznaczenie masy molowej substancji) został osiągnięty. Wartość pojemności jonitu wyznaczona przeze jest obarczona błędem 7,02 %. Przedział ufności jest bardzo duży ponieważ wartości masy molowej są bardzo rozbieżne. Rozbieżność wartości może być spowodowane niedokładnościami w czasie pomiarów.
5
Wyszukiwarka
Podobne podstrony:
Wyznaczanie masy cząsteczkowej związków wielkocząsteczkowych, Studia, Politechnika
Wyznaczanie rzędu reakcji metodą graficzną, Studia, Politechnika
34 Wyznaczanie masy cząsteczkowej substancji metodą ebuliom
108. Wyznaczanie modułu Younga metodą ugięcia, studia, studia Politechnika Poznańska - BMiZ - Mechat
22 Wyznaczanie masy cząsteczkowej cieczy metodą V Meyera
Wyznaczanie masy cząsteczkowej białek metodą SDS PAGE
Wyznaczanie masy cząsteczkowej makromolekuł na podstawie pomiarów wiskozymetrycznych
Wyznaczanie masy cząsteczkowej makromolekuł na podstwie pomiarów wiskozymetrycznych, Medycyna 1 rok
Wyznaczanie współczynnika lepkości metodą Stokesa, Studia, Pracownie, I pracownia
Próba tłoczności blach metodą Erichsena, Studia Politechnika Poznańska, Semestr V, Obróbka plastyczn
PIOTREK K WYZNACZANIE OGNISKOWEJ SOCZEWKI METODA BASSELA, studia, Budownctwo, Semestr II, fizyka, Fi
wyznacznie masy czasteczkowej makromolekuł na podstawie pomiarów wiskozymetrycznych cz 1
Wyznaczanie masy cząsteczkowej związków wielkocząsteczkowych
Wyznaczanie SEM metodą kompensacji - CZURYŁOWSKI, Politechnika Lubelska, Studia, Semestr 6, sem VI,
Wyznaczanie prędkości fal akustycznych metodą rury Kundta, Politechnika Lubelska, Studia, Studia, se
Wyznaczanie stałej reakcji szybkości zmydlania estru, Studia, Politechnika
WYZNACZENIE PRĘDKOŚCI DŹWIĘKU METODĄ SKŁADANIA DRGAŃ ELEKTRYCZNYCH 3, budownictwo studia, fizyka
więcej podobnych podstron