REGULAMIN PRACOWNI
1. W pracowni STUDENCI mogą przebywać jedynie w obecności Prowadzącego.
2. Obowiązkiem STUDENTA jest utrzymanie ładu i czystości w miejscu pracy.
3. Podczas wykonywania ćwiczeń należy zachować spokój, powagę i unikać zbędnego gromadzenia się.
4. Ćwiczenia przeprowadzać z zachowaniem wskazanych przez Prowadzącego lub podręcznik środków ostrożności tak, aby nie narazić na niebezpieczeństwo siebie i innych.
5. Wykonywanie ćwiczenia i uruchomienie przyrządu może nastąpić tylko na polecenie Prowadzącego.
6. Pobrane odczynniki, szkło i przyrządy należy po zakończeniu ćwiczeń odnieść na właściwe miejsce w stanie czystym.
7. Każde uszkodzenie sprzętu lub szkła musi być zgłoszone Prowadzącemu.
8. Naczynia z chemikaliami należy zaraz po użyciu zamknąć właściwym korkiem. Nie dopuścić do pomieszania chemikaliów.
9. Nie należy wrzucać do kosza resztek niebezpiecznych substancji lecz zbierać je do przeznaczonych na ten cel pojemników.
10. Nie wrzucać do zlewów stłuczonego szkła i substancji stałych, które mogą spowodować zapchanie przewodów kanalizacyjnych.
11. Żadnych substancji i materiałów nie wolno z pracowni nikomu dawać, ani brać do domu.
12. W razie nieszczęśliwego wypadku należy natychmiast zgłosić się do nauczyciela i podać okoliczności wypadku. Nie wolno samemu podejmować środków zaradczych. We wszystkich sprawach nie objętych regulaminem należy zgłaszać się do Prowadzącego.
13. Zobowiązuje się wszystkich Studentów do ścisłego przestrzegania przepisów BHP dotyczących ćwiczeń laboratoryjnych.
INSTRUKCJA BHP
Prace doświadczalne należy zawsze wykonywać w fartuchu i rękawicach ochronnych.
W pracowni nie wolno spożywać żadnych produktów spożywczych. Na terenie całego budynku obowiązuje bezwzględny zakaz palenia.
Nie zapalaj ognia jeśli pracujesz z substancjami łatwopalnymi (eter, eter naftowy, benzen, aceton, itp.). Pamiętaj, że płytki elektryczne nie zabezpieczają przed zapaleniem się par większości rozpuszczalników organicznych. W przypadku rozlania się łatwopalnych cieczy zetrzyj je natychmiast starannie, a ściereczkę dokładnie spłucz wodą. Pożaru powstałego w skutek zapalenia się rozpuszczalników organicznych nie gas woda lecz kocem pożarniczym lub specjalną gaśnicą.
Wszystkie czynności ze stężonymi kwasami, amoniakiem, bromem i rozpuszczalnikami organicznymi przeprowadzaj pod sprawnie działającym wyciągiem.
Nie wlewaj nigdy wody roztworów kwasów lub zasad. Pamiętaj o zasadzie, że to kwas lub roztwór alkaliczny wlewamy do wody!!!
Nie pipetuj ustami żadnych roztworów. Posługuj się w tym celu pipetami wyposażonymi w gruszki gumowe. Pipetę używaną do pobierania stężonych kwasów lub zasad przepłucz natychmiast wodą. Kroplę stężonego kwasu lub ługu, jaka upadnie przypadkiem, np. na stół laboratoryjny natychmiast, starannie zetrzyj.
Przy oparzeniu skóry kwasem, ługiem- miejsce oparzone płucz dokładnie pod bieżącą wodą i przemyj odpowiednio: 2-3% roztworu wodorowęglanu sodowego w przypadku oparzenia kwasem i 1-2% roztworem kwasu octowego lub cytrynowego w przypadku oparzenia ługiem. Przy oparzeniu oczu- płucz je obficie wodą, wprowadzając strumień wody do zewnętrznych kącików powieki. Natychmiast udaj się do lekarza.
Po dostaniu się kwasu lub zasady do ust - przepłucz je natychmiast dużą ilością wody, a następnie odpowiednio rozcieńczonym roztworem wodorowęglanu sodowego, ewentualnie kwasu octowego czy cytrynowego.
Przy oparzeniu termicznym skóry z objawami I stopnia (zaczerwienienie, obrzęk, ból) - przemyj jej powierzchnię etanolem albo 10% roztworem nadmanganianu potasu. W razie poważnego oparzenia (oparzenie II stopnia, widoczne pęcherze), przemyj otoczenie rany etanolem, przykryj je gazą higroskopijna i udaj się do lekarza.
Zachowaj maksymalna ostrożność przy pracy z rtęcią. Nie rozlewaj (pary rtęci są silnie trujące)! W przypadku stłuczenia termometru rozlaną rtęć należy starannie zebrać do zamkniętego naczynia i zawiadomić pracownika.
Nie przechowuj nigdy roztworów alkalicznych w zetknięciu ze szlifem (biurety, butelki ze szlifem, itp.).
Przy montażu aparatury zaopatrzonej w szlify nie zapomnij o stosowaniu smaru na powierzchni złącza (wystarczy nałożyć smar na 1/3 długości złącza od szerszej strony szlifu).
Dla każdego roztworu używaj oddzielnej pipety szklanej. W przypadku niewielkich ilości cieczy należy używać pipet automatycznych z wymiennymi końcówkami automatycznymi. Końcówki należy zmienić po każdym odpipetowaniu roztworu.
Przy rozcieńczeniu roztworów posługuj się dokładnymi pipetami i kolbami miarowymi.
Na wadze analitycznej odważaj posługując się czystą łyżeczką oraz czystymi i suchymi naczyniami. Przed ważeniem oznacz położenie zerowe. Po ważeniu wagę wyłącz i usuń pędzelkiem ewentualne zanieczyszczenia. Łyżkę do ważenia substancji stałych po użyciu należy umyć i nie stosować jej do ważenia kilku różnych substancji.
Stosując wirowanie pamiętaj o następujących szczegółach:
poziom cieczy w probówkach powinien być co najmniej o 1 cm poniżej brzegu probówki;
w przypadku szklanych probówek konieczna jest podkładka (osłona) gumowa;
tulejki wraz z probówkami z cieczą winny być tarowane naprzeciwlegle, poziom cieczy w probówkach tarowanych winien być zbliżony;
przy ewentualnym stłuczeniu probówki w czasie wirowania należy natychmiast wyłączyć urządzenie i dokładnie oczyścić je z odłamków szkła i rozlanej cieczy.
Oszczędzaj odczynniki i szkło.
Posługuj się wyłącznie dokładnie umytym szkłem laboratoryjnym:
bezpośrednio po użyciu spłucz naczynie bieżącą wodą;
naczynia myj przy użyciu detergentu i z wykorzystaniem czystej szczotki;
spłucz bardzo starannie wodą bieżącą, aż do zupełnego usunięcia detergentu, co najmniej 3-krotnie spłucz szkło woda bieżącą i 1-krotnie destylowaną;
bączek do mieszadła magnetycznego należy wyjąć ze zlewki przed spłukaniem i umyć go osobno;
Pipety bezpośrednio po użyciu przemyj wodą bieżącą i wstaw do wysokiego naczynia wypełnionego roztworem detergentu.
Odpady:
zwykłe śmieci (papier, itp.)wyrzucane są do koszy z workami koloru czarnego;
zużyte końcówki do pipet automatycznych, eppendorfy, żele zawierające bromek etydyny i inne odpady toksyczne wrzuca się do specjalnych, oznakowanych pojemników;
odpady płynne należy magazynować w specjalnie przystosowanych i oznaczonych pojemnikach;
stłuczkę szklaną wyrzuca się do specjalnego pojemnika odpowiednio opisanego;
Przy konieczności wylatania do zlewu stężonego kwasu, zasady lub rozpuszczalników organicznych należy odkręć kran i strumieniem wody rozcieńczaj stężony związek, a następnie dokładnie spłucz zlew.
Wiele odczynników stosowanych w pracowni jest potencjalnymi truciznami. Często więc myj ręce podczas pracy i bezwzględnie po zdjęciu rękawiczek.
Po zakończeniu pracy uporządkuj swoje stanowisko. Wszystkie używane odczynniki i sprzęt laboratoryjny należy odstawić na miejsce.
Ćwiczenie 3
Badanie toksyczności związków chemicznych w stosunku do organizmów wodnych. Test toksyczności ostrej na skorupiakach Artemia salina.
1. Charakterystyka organizmów
Artemia salina (słoniaczek) należy do solowców i jest skorupiakiem ciepłolubnym [29]. Artemie żyją w wodach słonych i słonawych strefy tropikalnej, subtropikalnej i umiarkowanej. W dużych ilościach występują w Jeziorze Słonym w stanie Utah oraz w Zatoce San Francisco w Kaliforni (USA). Inne miejsca masowego występowania artemii to m.in. Shark Bay (Australia) i Chaplin Lake (Kanada). Dorosłe osobniki osiągają do 20 mm. Składają one niezliczone ilości jajeczek, które posiadają grubą osłonkę zbudowaną m.in. z kreatyny. Po wysuszeniu tworzą formę przetrwalnikową tzw. cystę. Cysty Artemia salina są odporne nawet na ekstremalne czynniki zewnętrzne i mogą przetrwać 3-5 lat nie tracąc zdolności do rozwoju. Wysuszone jajeczka bardzo dobrze chłoną wodę i po ponownym uwodnieniu już po 24 h następuje szybki rozwój zarodków tzw. naupliusów czyli inaczej pływików. Naupliusy są wykorzystywane jako organizmy wskaźnikowe w teście toksyczności ostrej.

Rys.1. Dorosłe osobniki Artemia salina, źródło: www.hlasek.com/artemia_salina_6908
2. Metoda badania
2.1. Test wstępny
2.1.1. Podłoża, odczynniki i roztwory
roztwór roboczy badanego związku o stężeniu 1g/dm3,
0.9% r-r NaCl w wodzie,
larwy skorupiaków.
2.1.2. Aparatura i przyrządy
cieplarka
waga analityczna
lupa
podstawowe szkło laboratoryjne: kolby miarowe 50 cm3, pipety
mikropłytki z 24 studzienkami
2.1.3. Zabiegi wstępne
W kolbach miarowych o pojemności 50 cm3 przygotować stężenia badanego preparatu w zakresie 100 ÷ 0,01 mg/L. Stężenia powinny stanowić szereg geometryczny o ilorazie 10. Do rozcieńczania badanego preparatu należy używać 0,9% r-ru NaCl.
Test przeprowadza się w 24 dołkowej płytce testowej.
2.1.4. Wykonanie testu
Do cel w kolumnie 1 (A1, B1, C1, D1) wprowadzić po 1 ml 0,9% r-ru. Kolumna 1 będzie stanowiła próbę kontrolną.
Do cel w kolumnach 2-6 wprowadzić po 1 ml wcześniej przygotowanych roztworów rozpoczynając od najniższego stężenia badanego związku.
Przenieść po 15 organizmów testowych z płytki Petriego do cel w rzędzie A rozpoczynając od celi A1 do A6, za pomocą pipety Pasteura. Przed każdym pobraniem odganizmów z płytki pipetę należy dokładnie przepłukać w zlewce z r-rem NaCl .
Przenieść po 5 organizmów z rzędu A do każdej celi w odpowiedniej kolumnie z substancją badaną.
1 2 3 4 5 6
A transfer larw do cel
B
C
D
Rys. 2. Schemat napełniania dołków testowych.
2.1.5. Odczyt wyników
Odczytu wyników należy dokonać po 24 h inkubacji. Liczbę żywych organizmów w każdej celi zanotować w tabeli 1. Za osobniki martwe należy uznać te, które nie będą wykazywały ruchu w czasie 10 sekund. Na podstawie przeprowadzonych obserwacji ustalić zakres stężeń do testu potwierdzającego.
Tabela 1. Wyniki testu toksyczności ostrej na Artemia salina. Ilość osobników żywych po 24 h inkubacji (test wstępny).
Nazwa próby: |
|||||
Stężenie |
|||||
kontrola |
|
|
|
|
|
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.......% |
.....%
|
.....% |
.....% |
.....% |
.....% |
Efekt toksyczny |
|||||
2.2. Test potwierdzający
W kolbach miarowych o pojemności 50 cm3 przygotować 5 stężeń badanego preparatu w zakresie ustalonym na podstawie testu wstępnego. Stężenia powinny stanowić szereg geometryczny o ilorazie 1,8. Do rozcieńczania badanego preparatu należy używać 0,9% r-ru NaCl.
Sposób napełniania próbek, inkubacji i odczytu wyników przeprowadzić zgodnie z procedurą podaną w punkcie 2.1.
Wyniki obserwacji zanotować w tabeli 2.
Tabela 2. Wyniki testu toksyczności ostrej na Artemia salina. Ilość osobników żywych po 24 h inkubacji (test potwierdzający).
Nazwa próby: |
|||||
Stężenie |
|||||
kontrola |
|
|
|
|
|
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.../5
|
.../5 |
.../5 |
.../5 |
.../5 |
.../5 |
.......% |
.....%
|
.....% |
.....% |
.....% |
.....% |
Efekt toksyczny |
|||||
Wartość LC50 obliczyć metodą logarytmiczno-probitową.
Ćwiczenie 4
Farmaceutyki w środowisku. Ocena wpływu leków na behavior larw wodzienia (Chaoborus sp.)
Wprowadzenie
Wśród mikrozanieczyszczeń środowiska wodnego wzbudzających coraz większe zainteresowanie społeczeństwa i naukowców są farmaceutyki. Farmaceutyki są powszechnymi zanieczyszczeniami dostającymi się do środowiska z wielu rozproszonych źródeł: z urządzeń produkcyjnych, z hodowli ryb, z hodowli zwierzęcej i obiektów związanych z leczeniem ludzi. W konsekwencji, znaczące ilości farmaceutyków docierają do oczyszczalni ścieków, i jeśli nie są właściwie usuwane, są odprowadzane do wód powierzchniowych, gdzie mogą ulegać akumulacji i osiągać stężenia oddziaływujące na organizmy żywe.
Działanie leków w organizmie jest dobrze poznane przed wprowadzeniem preparatu do obrotu handlowego zostało dość dobrze przebadane, jednak działanie pozaustrojowe nie jest do końca znane. Na dzień dzisiejszy wiemy, że obecność pozaustrojowa leków powoduje mutację i powstanie odpornych kultur bakteryjnych., przez co wiele chorób wywołanych infekcją drobnoustrojową nie będzie mogło być leczone za pomoc znanych farmaceutyków. Stanowi to poważne zagrożenie dla zdrowia publicznego. Stężenia farmaceutyków w środowisku osiągają znacznie niższe poziomy, niż te stosowane w celach leczniczych, jednak niebezpieczne może być długotrwałe narażenie organizmów żywych na mieszaninę wielu preparatów.
Badania sugerują, że przy obecnych poziomach farmaceutyków nie można wykluczyć ich efektów biologicznych w środowisku. Konieczne jest zatem intensywne poszukiwanie rozwiązań technologicznych, w tym możliwości jakie oferuje zaawansowane oczyszczanie ścieków (trzeciego stopnia).
Wodzień (Chaoborus) - owad należący do rzędu muchówek i rodziny wodzieniowatych. Postacie dorosłe tych zwierząt - imago swoim wyglądem przypominają komary, jednakże w odróżnieniu od nich samice wodzienia nie kąsają. Wodzienie przechodzą przeobrażenie zupełne. Chaoborus większość życia spędza w postaci larwalnej. Larwy są przezroczyste, trudno zauważalne "gołym okiem" i dlatego zwane są z angielskiego phantom midge larvae. Pomimo tego, że ciało wodzienia jest przezroczyste, po krótkiej obserwacji dostrzec można dobrze widoczne oko złożone, 2 pary przednich i tylnych pęcherzy pławnych, swoim kształtem przypominających ziarna fasoli oraz układ pokarmowy wypełniony pożywieniem. Larwy wodzienia zasiedlają wody stojące - jeziora, stawy, bajora itp., w zależności od rodzaju tego owada.
Celem ćwiczenia jest ocena stanu fizjologicznego larw wodzienia w środowisku zanieczyszczonym farmaceutykami za pomocą częstości skurczów ciała.
Materiały:
- pastylka ibuprofenu 200 mg,
- Tinctura valerianae - nalewka kozłkowa,
- Cardiamid coffein w kroplach,
- pastylka paracetamolu 200 mg,
- 6 zlewek o pojemności 500 ml,
- plastikowe kubki,
- moździeż, minutnik, termometr,
- pipety 5 ml
Wykonanie
A) Przygotowanie roztworów
R-r ibuprofenu i paracetamolu (0.3 mg/ml)
pastylkę ibuprofenu i pastylkę paracetamolu umyć pod bieżącą wodą, aby zmyć otoczkę. Rozgnieść osobno w moździeżu, rozpuścić w 600 ml wody destylowanej; po kilku minutach zlać do zlewki roztwór znad osadu.
R-r kropli walerianowych
odmierzyć 100 kropli nalewki kozłkowej i rozpuścić w 500 ml wody destylowanej
R-r kropli cardiamid-coffein
odmierzyć 80 kropli i rozpuścić w 500 ml wody destylowanej
B) ocena stanu fizjologicznego larw wodzienia za pomocą pomiaru częstości skurczów ciała
Doświadczenie wykonywane jest w 3 - 4 sekcjach. Kazdy z zespołów obserwuje wpływ ibuprofenu, paracetamolu, nalewki kozłkowej i kropli kardiamid-coffein na częstość skurczów ciała u 21 larw muchówki wodzienia (po 7 larw na kazdą badaną substancję). W tym celu należy do plastikowych kubeczków odlać ok. 100 ml wcześniej przygotowanych roztworów. Przed przystąpieniem do pomiarów skurczów ciała należy zmierzyć i zanotować temperaturę roztworów.
Metoda pomiaru:
Za pomocą pipety pobrać z hodowli jedną larwę i umieścić ją w kubeczkuu z czystą wodą (kontrola). Odczekać chwilę, a następnie liczyć skurcze ciała larwy przez 3 minuty (odliczanie należy rozpocząć w momencie jednego ze skurczów). Wynik zanotować. Następnie tego samego osobnika przenieść do kubeczka z badanym roztworem (za pomocą pipety w kropli wody, tak aby nie przenieść dużych ilości czystej wody do badanego r-ru. i po chwili rozpocząć zliczanie skurczów ciała, także przez 3 minuty. Wyni zanotować. Po pomiarze przenieść larwę do osobnej zlewki z czystą wodą, tak aby każda larwa była badana jednokrotnie.
Opracowanie wyników
Dla każdej z przebadanych larw policzyć zmianę częstości skurczów ciała (ilość skurczów ciała w r-rze np. ibuprofenu - ilość skurczów ciała w czystej wodzie = (+/-) zmiana). Wyniki dla wszystkich roztworów zebrać w tabeli, policzyć średnią dla każdego roztworu, a następnie za pomocą arkusza kalkulacyjnego wykonać wykres słupkowy (z naniesionymi odchyleniami standardowymi), na którym należy porównać badane grupy organizmów. Wyciągnąć wnioski.
Ćwiczenie 5
Toksykologia żywności. Substancje antyodżywcze; oznaczanie szczawianów rozpuszczalnych w wybranych używkach
1 Wprowadzenie
W żywności występuje wielu substancji naturalnych mogących działać antyodżwyczo w stosunku do składników mineralnych. Jedna z nich jest kwas szczawiowy, który tworząc nierozpuszczalne sole z metalami dwu- i trójwartościowymi powoduje obniżenie ich wykorzystania z pożywienia.
Kwas szczawiowy to kwas dwukarboksylowy z dwoma atomami węgla w cząsteczce. Jest rozpuszczalny w wodzie, dobrze dysocjuje. Jego sole sodowe i potasowe są również rozpuszczalne w wodzie, natomiast sole wapniowe, magnezowe i sole metali ciężkich są trudno rozpuszczalne w wodzie. Szczawian wapnia jest praktycznie rozpuszczalny tylko w stężonych kwasach. Kwas szczawiony występuje zarówno w świecie roślinnym jak i zwierzęcym głownie w postaci rozpuszczalnych soli potasu i sodu oraz w formie wolnej. Spośród roślin najbogatszych w kwas szczawiowy są: rabarbar, szpinak, szczaw, a także używki: kawa, herbata czy kakao. Sporadyczne spożywanie pożywienia zawierającego szczawiany nie prowadzi do zmniejszenia wapnia w organizmie. Natomiast kwas szczawiowy obecny stale w diecie ludzi lub paszy zwierząt nawet w małych ilościach, wywiera ujemny wpływ na bilans wapnia w ustroju.
W doświadczeniu na dorosłych szczurach otrzymujących pełnowartościowe pożywienie z dodatkiem 0,95% szczawianu wapnia obserwowano zmniejszony przyrost masy ciała w odniesieniu do grupy kontrolnej oraz stwierdzono zmniejszoną retencję wapnia w kościach o prawie 70% oraz występowanie krzywicy. W badaniach z udziałem ludzi żywionych dietą z dodatkiem 120g szpinaku, wykazano spadek absorbancji wapnia z 18,6 do 11,8%.
Antyodżywcze działanie kwasu szczawiowego uwarunkowane jest nie tylko bezwzględną zawartością jonów szczawianowych, ale ponieważ wiązanie jonów metali przebiega stechiometrycznie (np.45mg kwasu szczawiowego wiąże 20mg wapnia), także stosunkiem kwasu szczawiowego do pierwiastków, z którymi tworzy nierozpuszczalne sole (Tab..). Biorąc pod uwagę stosunek kwasu szczawiowego do wapnia produkty spożywcze można podzielić na trzy kategorię:
Produkty, w których zawartość kwasu szczawiowego wielokrotnie przekracza zawartość wapnia: szpinak, szczaw, rabarbar, botwinka, burak, herbata, kawa. Wapń wstępujący w tych produktach jest praktycznie niedostępny, a ponadto nadmiar kwasu może wiązać wapń z innych produktów spożywczych jednocześnie lub jony szczawianowe mogą być wchłaniane do krwi. Wówczas można spodziewać się toksycznego działania kwasu siarkowego.
Produkty takie jak: ziemniaki, owoce jagodowe, w których kwas szczawiowy i wapń występują w ilościach prawie równoważnych, a więc wapń jest praktycznie nierozpuszczalny , lecz spożywanie tych produktów nie ogranicza biodostępności wapnia z innych produktów spożywczych.
Produkty spożywcze, które pomimo występowania w nich kwasu szczawiowego zawierają dużo wapnia i stanowią jego źródło. Należą do nich niektóre rośliny strączkowe: sałata, kapusta, kalafior oraz w mniejszym stopniu inne warzywa i owoce.
Kwas szczawiowy i jego sole mogą być szkodliwe nie tylko ze względu na fakt ich antyodżywczego działania w stosunku do składników pokarmowych ale także w skutek ich toksyczności. Kwas szczawiowy podany omyłkowo w „substancji” może wywoływać objawy hipokalcemii i tężyczki, ma także działanie żrące. Działanie toksyczne, a w skrajnych przypadkach nawet letalne wywiera już 4-5g kwasu szczawiowego lub jego soli. Ostre zatrucie charakteryzuje się nudnościami, wymiotami i biegunką. Występują także ślinotok, szczękościsk, bole w okolicach brzucha i nerek, zmniejszenie ilości moczu. Mocz jest ciemny, zawiera białko, hemoglobinę, wałeczki i kryształki szczawianu wapnia. Wydalany moczu krystaliczny szczawian wapnia może powodować zaczopowanie kanalików nerkowych a następnie bezmocz. Następuje również zwolnienie czynności serca i spadek ciśnienia krwi. Kwas szczawiowy jest także inhibitorem działanie niektórych enzymów. Należy zwrócić uwagę, że kwas szczawiowy pochodzi nie tylko z pożywienia, ale wytwarzany jest także w organizmie jako końcowy produkt metabolizmu glicyny, seryny, hydroksyproliny oraz kwasu askorbinowego i puryny. Normalne stężenie kwasu szczawiowego w surowicy krwi waha się od 0,3 do 0,7mg/100mL. Prawidłowe wydalanie szczawianów w moczu wynosi 20-40mg dziennie.
Ze względu na antyodżywcze działanie , a także stwierdzona toksyczność kwasu szczawiowego dla ludzi, spożywanie nadmiernej ilości produktów bogatych w szczawiany jest niewskazane szczególnie w warunkach nieprawidłowego funkcjonowania wątroby, trzustki, berek i gruczołów wydzielania wewnętrznego.
Ochronę organizmu przed stratami składników mineralnych spowodowanych częstym spożywaniem produktów zawierających kwas szczawiowy można zapewnić przez:
- ograniczenie spożywania produktów , w których stosunek zawartości kwasu szczawiowego do wapnia jest większy od 2,25 lub eliminowanie ich z diety (szczególnie u dzieci i ludzi młodych);
- uzupełnienie diety w wapń poprzez spożycie dodatkowej ilości produktów bogatych w ten pierwiastek (np. kawa z mlekiem, itp.).
Tabela Zawartość kwasu szczawiowego oraz jego stosunek do wapnia w wybranych produktach
Produkt |
Zawartość kwasu szczawiowego Mg/100g |
Kw. szczawiowy/wapnia |
WARZYWA |
||
Rabarbar |
275-1336 |
17,9 |
Szczaw |
27-730 |
12,5 |
Szpinak |
320-1260 |
9,6 |
Botwinka |
300-920 |
5,5 |
Burak ćwikłowy |
121-450 |
11,4 |
Pietruszka |
140-200 |
0,79 |
Sałata |
5-20 |
0,14 |
Cykoria |
15-27 |
0,22 |
Kapusta |
0-125 |
0,24 |
Brukselka |
5-37 |
0,60 |
Kalafior |
0-21 |
0,06 |
Seler liście |
35-65 |
0,55 |
Seler korzeń |
17-60 |
0,73 |
Szparagi |
0-14 |
0,35 |
Cebula |
23-89 |
1,18 |
Ziemniaki |
20-141 |
3,63 |
Buraki |
121-450 |
11,4 |
Marchew |
5-60 |
0,8 |
Fasola |
10-115 |
1,37 |
Groszek zielony |
0-10 |
0,12 |
Owoce |
||
Jabłka |
0-30 |
1,5 |
Gruszki |
0-30 |
1,5 |
Brzoskwinie |
0-30 |
1,5 |
Morele |
5-15 |
0,5 |
Wiśnie |
0-5 |
0,15 |
Pomarańcze |
20-30 |
0,62 |
Mandarynki |
20-30 |
0,62 |
Cytryny |
0 |
0 |
Grejpfrut |
0 |
0 |
Banany |
6 |
0,86 |
Ananas |
6 |
0,31 |
Truskawki |
2-47 |
0,78 |
porzeczki |
2-90 |
1,43 |
Inne |
||
Kawa |
50-150 |
8,33 |
Kakao |
500-900 |
5,6 |
Herbata |
300-2000 |
2,55 |
Czekolada |
900 |
4,37 |
2. Cel ćwiczenia
Celem ćwiczenia jest zapoznanie się z ilościową metodą oznaczania rozpuszczalnego kwasu szczawiowego w wybranych używkach oraz określenie stopnia wiązania wapnia przez kwas szczawiowy. W ramach doświadczenia należy:
Obliczyć ilość rozpuszczalnego kwasu szczawiowego w 100g produktu, przyjmując, że 1mL 0,02N KMnO4 odpowiada 0,9mg(COOH)2.
Podać jaka ilość wapnia jest wiązana przez rozpuszczalny kwas szczawiowy zawarty w naparze przygotowanym z 3g kawy/herbaty, wiedząc, że 90mg kwasu szczawiowego wiąże 40mg wapnia;
Podać ile mleka należy dodać do naparu przygotowanego z 3 g kawy/herbaty aby wapń zawarty w mleku związał rozpuszczony kwas szczawiowy z naparu (w 100g mleka jest 100 mg wapnia).
3. Materiał do badań
Materiał do badań stanowi herbata i kawa różnego gatunku. Herbaty: liściaste, granulowane, zielone, czarne; kawy: sypana, zbożowa, rozpuszczalna.
4. Część doświadczalna
Zasada oznaczenia:
Szczawiany rozpuszczalne wymywane są z produktów woda na gorąco, a szczawiany ogółem roztworem kwasu solnego. Oznaczenie polega na :
[a] wytrąceniu nierozpuszczalnego szczawianu wapnia (osad) buforowym 5% CaCl2 (aceton i niska temperatura przyśpieszają uformowanie osadu);
(COOH)2 + CaCl2 → (COO)2Ca + 2HCl
[b] rozpuszczeniu na gorąco szczawianu wapnia w 10% roztworze kwasu siarkowego;
(COO)2Ca +H2SO4 →(COOH)2 +CaSO4
[c] miareczkowaniu na gorąco 0,02N KMnO4
2KMnO4 +5(COOH)2 +3H2SO4 → 2MnSO4 + K2SO4 + 10CO2 +8H2O
Wykonanie oznaczenia:
Odważyć na wadze technicznej łyżeczkę (3g) kawy lub herbaty, zalać 100mL wrzącej wody destylowanej, mieszać intensywnie, naprzemiennie i odstawić na 5 minut. Przygotowany napar przesączyć. Przenieść 10mL przesączu do probówki wirówkowej o pojemności 100mL. Probówki wstawić (ze względów bezpieczeństwa) do zlewek zawierających 50-100mL zimnej wody. Dodać 5mL 5% chlorku wapnia (CaCl2) i 5mL acetonu. Wstawić do lodówki na 30 minut. Wyjąć probówki ze zlewki, ścianki zewnętrzne probówek osuszyć papierowym ręcznikiem. Probówki wywarzyć parami- ewentualne różnice pomiędzy probówkami zniwelować poprzez dodanie acetonu. Powstały osad szczawianu wapnia odwirować przez 10minut przy obrotach 3000obr/min. Płyn znad osadu wylać. Osad przenieść ilościowo do kolbki stożkowej za pomocą 5mL 10% kwasu siarkowego (H2SO4) (najpierw dodać 4mL H2SO4, a następnie spłukać ścianki pozostałą objętością kwasu) rozpuścić na gorąco w łaźni wodnej (trzymać nad łaźnią wodną przez około 10 minut). Miareczkować natychmiast 0,02N roztworem nadmanganianu potasu KMnO4 do uzyskania barwy różowej utrzymującej się przez około 1 minutę. Po pojawieniu się różowego zabarwienie zwiększyć intensywność mieszania Az do uzyskania trwałego zabarwienia i odstawić. Jeżeli barwa zaniknie przed upływem 1 minuty próbkę należy domiareczkować.
Materiały i odczynniki
Sprzęt laboratoryjny:
- kolby Erlenmayera;
- pipety automatyczne o pojemności z zakresu 10-1000 μL;
- łaźnia wodna
- bagietki;
- statyw do sączenia;
- sączki bibułowe;
- waga techniczna;
- wirówka laboratoryjna + probówki wirówkowe;
Odczynniki:
- 0,02N r-r KMnO4 (nadmanganianu potasu);
- 10% r-r H2SO4 (kwasu siarkowego);
- aceton;
- 5% r-r CaCl2 (chlorku wapnia);
LITERATURA
Brzozowska A.: Toksykologia żywności- Przewodnik do ćwiczeń. SGGW, warszawa, 2004.
Czapski J., Wieland A.: Dodatki do żywności - przyjaciel czy wróg. PWRiL, Poznań, 1992.
Ćwiczenie 6 i 7
Wpływ zanieczyszczenia podłoża na zawartość chlorofilu u roślin wskaźnikowych. Ocena wpływu odcieków ze składowisk na wzrost i syntezę chlorofilu u Lemna minor
1. Wprowadzenie
Analizę barwników chloroplastowych przeprowadza się po wyekstrahowaniu ich z tkanek roślinnych za pomocą rozpuszczalników organicznych. Użycie rozpuszczalników organicznych jest niezbędne ze względu na lipofilne właściwości barwników.
Fotosynteza to złożone reakcje syntezy związków organicznych z prostych substancji nieorganicznych (CO2, H2O), odbywające się z wykorzystaniem energii świetlnej. W procesie tym powstają związki o mniej utlenione, a tym samym bogatsze w energię. Im bardziej zredukowany jest związek (im więcej zawiera atomów H) tym ma wyższą wartość energetyczną. Głównymi związkami powstającymi w wyniku redukcji CO2 są cukry.
Fotosynteza przebiega w chloroplastach w dwóch fazach: świetlnej (w tylakoidach chloroplastów) i ciemnej (w stromie chloroplastu). Istotą fazy świetlnej jest przekształcenie energii świetlnej w energię wiązań chemicznych zawartych w ATP W fazie świetlnej biorą udział dwa fotosystemy (fosforylacji cyklicznej i niecyklicznej) chlorofilu, określane jako PS I i PS II, różniące się głównie właściwościami występujących w nich cząstek chlorofilu i karotenoidów.
Z fosforylacją niecykliczną jest związana fotoliza H2O, która polega na rozpadzie cząsteczki pod wpływem światła na jony wodorowe (H+). i wodorotlenowe (OH-). Jony wodorowe tworzą NADPH2, który łącznie z ATP stanowi siłę asymilacyjną wykorzystywaną w fazie ciemnej, natomiast z jonów wodorotlenowych uwalnia się tlen, będący końcowym produktem fotosyntezy.
Równanie fosforylacji fotosyntetycznej niecyklicznej
światło
NADP + H2O + ADP + Pi NADPH2 + ATP + ½ O2
chlorofil
gdzie: Pi - reszta kwasu fosforowego
Ciemna faza fotosyntezy zwana także cyklem Calvina -Bensona, polega na fotosyntetycznym cyklu redukcji CO2, podczas którego zachodzą 3 etapy przemian:
karboksylacja (czyli przyłączenie cząsteczki CO2),
redukcja (w tej fazie jest zużywana „siła asymilacyjna”: ATP i NADPH + H+)
regeneracja (polega na odtworzeniu związku pięcioweglowego (RuDP) z cząsteczek związku trójwęglowego (PGA).
Produktem końcowym fotosyntezy jest glukoza, która powstaje w wyniku wielu złożonych reakcji.
Niektóre węglowodany, wytworzone w fazie ciemnej są później użytkowane jako źródło energii, inne natomiast - jako surowce do produkcji niezbędnych dla komórki roślinnej związków organicznych, np komórki roślinne wykorzystując pobrane z gleby takie składniki mineralne jak azotany i siarczany mogą przekształcać węglowodany w aminokwasy, elementy budulcowe białek.
Dzięki istnieniu fotosyntezy możliwe jest przekształcanie energii świetlnej w energię chemiczną, wytwarzanie związków organicznych z CO2 i H2O i uwalnianie tlenu.
Produkty fotosyntezy, utrzymujące życie i rozwój roślin samożywnych są warunkiem istnienia organizmów cudzożywnych, gdyż dostarczają im pokarmu, tlenu i energii.
Chlorofil - główny barwnik fotosyntezy, pochłania światło widzialne przede wszystkim w zakresie światła niebieskiego i czerwonego widma, nie pochłania natomiast światła zielonego, które się od niego odbija. Rośliny na ogół wydają się zielone, ponieważ ich liście odbijają większość zielonego światła, które na nie pada.
Istnieje kilka rodzajów chlorofilu. Najważniejszy z nich to chlorofil a, barwnik rozpoczynający reakcje zależne od światła. Dodatkowym barwnikiem, który bierze udział w fotosyntezie, jest chlorofil b. Różni się on od chlorofilu a jedynie grupą funkcyjną pierścienia porfirynowego - grupa metylowa (-CH3) chlorofilu a jest zastąpiona grupą aldehydową (-CHO) w chlorofilu b. Ta różnica przesuwa długość fali światła pochłanianego i odbijanego tak dalece, że chlorofil b ma barwę zielonożółtą, podczas gdy chlorofil a jaskrawozieloną.
Komórki roślinne zawierają także inne dodatkowe barwniki fotosyntetyczne np. karotenoidy o zabarwieniu żółtym i pomarańczowym. Pochłaniają one światło o innej długości fali niż chlorofil, dzięki czemu powiększa się zakres widma światła, które dostarcza energii do fotosyntezy. Chlorofil może być wzbudzony bądź światłem, bądź energią przekazaną z innych barwników, które zostały wzbudzone światłem. Jeśli zatem cząsteczka karotenoidu zostanie wzbudzona, jej energia może być przekazana chlorofilowi.
Charakterystyka organizmów
RZĘSOWATE (Lemnaceae) Wszystkie gatunki z tej rodziny maja łodygę przekształconą w płaską lub lekko wypukłą blaszkę liściową, o kształcie okrągło jajowatych zielonych płytek. Z jednej strony płytka rozgałęzia się, a od spodu odchodzi od niej cienki, nitkowaty półprzezroczysty prosty korzonek (niektóre gatunki ich nie mają). Korzonki spełniają rolę mechaniczną - utrzymując równowagę płytki. Blaszka ma kolor jasnozielony długości 5 [mm] i szerokości 3 [mm]. Na łodyżce znajdują się 1 ÷ 2 kieszonki, w których rozwijają się młode roślinki.
Wykonanie oznaczenia
3.1. Podłoża, odczynniki i roztwory
odcieki ze składowiska odpadów komunalnych,
1.2. hodowla początkowa roślin,
1.3. podłoże do hodowli makrofitów.
3.2. Aparatura i przyrządy
fitotron lub oświetlone stanowisko
podstawowe szkło laboratoryjne: kolby miarowe 100 cm3, kolby Erlenmayera o poj. 200 cm3 lub płytki Petriego, pipety, moździerz
suszarka
waga
3.3. Zabiegi wstępne
W kolbach miarowych o pojemności 100 cm3 wykonać szereg rozcieńczeń badanych odcieków w podłożu do hodowli makrofitów w zakresie 100÷6,25%
Ustalić suchą masę roślin w hodowli początkowej
Wykonanie testu
Na płytki Petriego wprowadzić po 20 cm3 przygotowanych odcieków (każde rozcieńczenie powinno być badane w 3 powtórzeniach), a następnie wprowadzić 3 do 5 roślin do każdego naczynia. Rośliny powinny być podobnego rozmiaru i o tej samej, bądź zbliżonej liczbie płatków. Należy zwrócić uwagę, aby sumaryczna ilość płatków w naczyniu wynosiła 12-16 (np. trzy rośliny czteropłatkowe i 1 trójpłatkowa). Zanotować w tabeli ilość wprowadzonych roślin i sumaryczną ilość płatków w każdym naczyniu. Próby inkubować przy stałym oświetleniu przez okres 7 dni. Kontrolę procesu przeprowadzić w dniu 3 i 5. Po zakończeniu inkubacji oznaczyć zawartość chlorofilu i suchej masy roślin w stosunku do próby kontrolnej.
4.1. Ekstrakcja chlorofilu
Sprzęt:
moździerze porcelanowe, probówki, lejki, sączki, waga, nożyczki, spektrofotometr
Odczynniki:
aceton schłodzony do 40C
benzyna ekstrakcyjna
Z każdej próby zważyć trzy łodygi, zmielić je w moździerzu i ekstrahować chlorofil dwiema 10-mililitrowymi porcjami acetonu schłodzonego do 4ºC. Po przesączeniu roztworu przez karbowane sączki dodać do niego po 5 cm3 wody destylowanej i mierzyć absorbancję roztworu przy dwóch długościach fali - 645 nm i 663 nm.
Zawartość chlorofilu obliczyć na podstawie wzorów:
Ca = (12,7A663 - 2,7A645)/m
Cb= (22,9A645 - 4,7A663)/m
Rozdział barwników metodą Kraussa
Do suchej probówki nalać 2 ml wyciągu barwników. Dodać 4 ml benzyny i silnie wstrząsnąć. Odczekać kilka minut. Jeżeli uzyskany rozdział nie będzie wyraźny należy dodać 3 krople wody destylowanej i ponownie wstrząsnąć. Zanotować barwy poszczególnych warstw. Porównać ekstrakty uzyskane z różnych prób.
Obliczenia
Dla każdego badanego stężenia oraz dla próby kontrolnej obliczyć specyficzną szybkość wzrostu wg. wzoru:
μi-j = 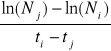
gdzie:
μi-j : specyficzna przeciętna szybkość wzrostu w czasie i do j,
Ni: ilość listków obserwowana w czasie i,
Nj: ilość listków obserwowana w czasie j,
ti: czas rozpoczęcia badań [d],
tj: czas zakończenia badań [d].
Inhibicję szybkości wzrostu (Ir) obliczyć dla każdego stężenia odcieków wg. wzoru:
Ir=![]()
[%]
gdzie:
μC - średnia wartość μ w kontroli,
μT - średnia wartość μ w danym stężeniu.
Wykreślić zależność obserwowanej inhibicji szybkości wzrostu od stężenia odcieków w układzie współrzędnych y=Ir=f(C). Odczytać na wykresie stężenie odcieków powodujące 50% zahamowanie szybkości wzrostu.
Dla próby kontrolnej i wszystkich stężeń odcieków obliczyć czas podwojenia listków
Td = ln2/μ
Porównać czasy podwojenia obliczone dla kontroli i badanych prób.Ćwiczenie 8
Substancje antyodżywcze w żywności. Związki goitrogenne w produktach roślinnych.
Oznaczanie tiocyjanianów w warzywach.
1. Wprowadzenie.
Do goitrogenów czyli substancji wolotwórczych zaliczamy różne związki organiczne oraz jony nieorganiczne, które mogą zaburzać metabolizm jodu w organizmie co skutkuje spadkiem syntezy tyroksyny oraz prowadzi do przerostu tarczycy (wola). Do naturalnych substancji wolotwórczych należą: tioglikozydy, glikozydy cyjanogenne, polifenole oraz hemaglutyniny.
Tioglikozydy, inaczej glukozynolany, to związki charakteryzujące się posiadaniem wiązania S-glikozydowego. Spotyka się je w większych ilościach gównie w roślinach krzyżowych, takich jak: kapusta biała i czerwona, kapusta włoska, sałata, szpinak, jarmuż, rzeżucha, brokuły, kalafior, rzepa, rzodkiewka, cebula, pomidory, pory, pietruszka, seler, chrzan, sałata, orzeszki ziemne i inne a także w niektórych owocach. Substancje te można spotkać we wszystkich częściach roślin, ale w największym stężeniu w nasionach. Do organizmu człowieka trafiają przez bezpośrednie spożywanie warzyw lub dostają się wraz z mlekiem pochodzącym od krów karmionych paszą zawierającą znaczącą ilość roślin krzyżowych.
Pod wpływem tioglikozydazy (myrozynazy) tioglikozydy ulegają hydrolizie i powstają z nich tiocyjaniany ( R - SCN ), izotiocyjaniany ( R - NCS ), związki indolowe, nitryle (R - CN ) oraz tiooksazolidyny. Przeciętną zawartość tiocyjanianów w niektórych warzywach przedstawiono w poniższej tabeli.
Rodzaj warzywa
|
Zawartość SCN-- [mg / 100g] |
Kapusta głowiasta Jarmuż Kapusta włoska Brukselka Kalafior Kalarepa Żółta rzepa Rzepak Sałata, szpinak, cebula, seler, pomidor
|
3 - 6 3 - 25 18 - 31 10 4 - 10 2 - 3 9 2,5 < 1 |
Myrozyna, która się składa z trzech do czterech izoenzymów, występuje w komórkach roślin krzyżowych ale ich oddziaływanie na organizm (ludzki lub zwierzęcy) jest możliwe dopiero po zmiażdżeniu tkanek i uwolnieniu się soku komórkowego. Działa w szerokim zakresie pH (od 3 do 8) i w obecności wody.
Enzymatyczny rozkład tioglikozydów ma miejsce w czasie żucia w jamie ustnej, a także przy rozdrabnianiu warzyw podczas przygotowywania potraw. Jednak dopiero ekstrakcja wodą oraz gotowanie uwalnia większość aktywnych tioglikozydów. Gotowanie w temperaturze powyżej 900Cz zwłaszcza w otwartym naczyniu, powoduje że większość tiocyjanianów (70-90%) ulatnia się a sama myrozynaza ulega denaturyzacji co hamuje jej działanie w organizmie.
Tioglikozydy, które nie uległy przemianom podczas jedzenia czy przygotowywania potraw, trafiają do przewodu pokarmowego, gdzie w dalszych jego odcinkach ulegają hydrolizie pod wpływem tioglikozydazy bakteryjnej. Ich niepożądane działanie można przedstawić na przykładzie kapusty , w dużych ilościach spożywanej w naszej części Europy. Warzywo to zawiera cztery rodzaje glikozydów, w których część niecukrową, aktywną wolotwórczo stanowią: tiocyjaniany (50 mg/kg), izotiocyjaniany (100 mg/kg), tiooksazolidyny (10 mg/kg) oraz antocyjany (polifenole). Ich niepożądane działanie na organizm polega głównie na tym że konkurują z jodem zawartym w wchłanianym powietrzu lub w pożywieniu. Normy zdrowotne zalecają aby dawka pobieranego przez człowieka jodu nie była niższa niż 100 ug I/dobę, gdyż przekroczenie stosunku wagowego Tiocyjaniany / Jod > 500 uważane jest za potencjalnie korzystne dla rozpoczęcia procesu przerostu tarczycy. Stąd w warunkach panujących w środkowej i wschodniej Europie, charakteryzujące się niską zawartością jodu w powietrzu (duże oddalenie od morza) i w pożywieniu negatywne oddziaływanie goitrogenów można częściowo eliminować stosując urozmaiconą dietę. Tam gdzie nie ma takich możliwości (Afryka Środkowa), mamy do czynienia z występowaniem wola endemicznego wśród ludności na skutek codziennego spożywania manioku lub tapioki zawierających nawet do 400mg HCN/kg surowego owocu. Oddziaływanie goitrogenów na organizmy żywe jest bardzo zróżnicowane w zależności od rodzaju i tak:
Tioglikozydy powodują w początkowym okresie spadek aktywności sekrecyjnej tarczycy (wydzielanie przez gruczoł niezbędnych składników) przez zahamowanie syntezy tyroksyny. W konsekwencji następuje obniżenie we krwi poziomów dotyroniny T3 i T4 będących aktywnymi formami hormonu gruczołu tarczycy. W następnym etapie ich malejący poziom w płynach ustrojowych powoduje wzrost aktywności tyreotropowej co powoduje przyrost masy tarczycy.
Tiocyjaniany (SCN--) przenikają przez wszystkie błony komórkowe. W obecności jodu powodują hamowanie jego transportu do tkanek, w tym do gruczołu tarczycy a ponadto przyspieszają wydalanie jodu przez nerki. W samym gruczole tiocyjaniany inaktywują peroksydazę tarczycową
odpowiedzialną za organifikację jodu i sprzęganie jodotyrozyn. W efekcie następuje spadek stężenia jodu w tarczycy, zostaje zablokowane lub utrudnione jodowanie tyrozyny co prowadzi do gromadzenia się mono- i dijodotyrozyny a w rezultacie wzrost masy gruczołu. Oprócz tego tiocyjaniany w różnych tkankach mogą być metabolizowane do cyjanianów i siarczanów.
Izotiocyjaniany (NSC--) to główne toksyczne produkty jakie powstają w wyniku działania myrozynazy na tioglikozydy. Wpływając na aktywność peroksydazy tarczycowej hamują syntezę hormonów tarczycy. W pozostałych tkankach izotiocyjany mogą się przekształcać w tiocyjaniany i działać destrukcyjnie jak wyżej.
Nitryle są najbardziej toksycznymi produktami rozpadu tioglikozydów. Negatywnie wpływają w pierwszym rzędzie na nerki ale w procesie detoksyzacji tych związków zostają przekształcone w tiocyjaniany i w efekcie działają jak wyżej.
Tiooksazolidyny wykazują bardzo silną aktywność goitrogenną przez zaburzenie metabolizmu tarczycy, hamowanie syntezy tyrooksyny oraz jej sekrecję do krwi. Dodatkowa podaż jodu w diecie tylko łagodzi ich wolotwórcze działanie.
Glikozydy cyjanogenne występują w niektórych owocach warzyw (maniok, tapioka). Rośliny te zawierają linamarynę, której część niecukrową stanowi alfa-hydroksy-butylonitryl. W czasie enzymatycznej hydrolizy linamaryny powstaje aceton i kwas cyjanowodorowy. W procesie detoksykacji cyjanków w organiźmie dochodzi do wytworzenia jonów tiocyjanianowych oddziaływujące na organizm jak wyżej. Same cyjanki są bardzo silną trucizną, blokują bowiem oksydazę cytochromową. Powodują także zaburzenia w układzie nerwowym.
Polifenole wchodzą w reakcje z jodem, hamując w ten sposób jodowanie tyrozyny a w efekcie zmniejszając zmniejszając syntezę tyroksyny. To powoduje że są uważane za czynniki wolotwórcze. Naturalne polifenole (kwercetyna) występują najczęściej w połączeniu z cukrami (np. rutyna), głównie w owocach ale także w kapuście czerwonej i orzeszkach ziemnych.
Hemaglutyniny (lektyny) to glikoproteidy występujące między innymi w soi i fasoli. Same w sobie nie wykazują wolotwórczego oddziaływania ale mogą wzmacniać w tym kierunku działanie innych związków poprzez takie mechanizmy jak:
obniżanie możliwości absorpcji jelitowej wchłanianego jodu co ułatwia działanie tiocyjanianów.
obniżenie reabsorpcji tyroksyny wydzielanej z żółcią do światła jelita co skutkuje tym że w efekcie maleje poziom tego hormonu we krwi a to już ma wpływ na działanie tarczycy.
Badania prowadzone na myszach i szczurach wykazały że oprócz swych anty odżywczych właściwości tiocyjaniany, a szczególnie izotiocyjaniany mają także działania korzystne dla zdrowia poprzez obniżania ryzyka zachorowania na nowotwory. Ich pozytywne działanie wyraża się w takich mechanizmach jak:
- inhibicja cytochromu P-450 (hamowanie przekształcania prokancerogenów w biokancerogeny)
- indukcja enzymów II fazy metabolizmu związków obcych w wątrobie i ścianie jelita cieńkiego (szybszy metabolizm i wydalanie kancerogenów)
- przywrócenie apoptozy (zaprogramowanej śmierci komórek rakowych).
Część I Przygotowanie krzywej wzorcowej
Zasada kolorymetrycznego oznaczania tiocyjanianów
Zasada metody polega na wyekstrahowaniu tiocyjanianów z badanej próby kwasem trójchlorooctowym i przeprowadzeniu reakcji z jonami żelazowymi. W środowisku kwaśnym powstaje krwistoczerwone zabarwienie na skutek tworzenia się kompleksów od Fe(SCN)2+ do Fe(SCN)3-- zgodnie z reakcjami:
Fe3+ + SCN-- Fe(SCN)2+
Fe3+ + 6 (SCN)-- Fe(SCN)63—
Przygotowanie krzywej wzorcowej.
Odczynniki:
KSCN, r-r podstawowy A. (16,7 mg KSCN rozpuścić w 100 cm3 5% TCA, w kolbie miarowej)
KSCN, r-r wzorcowy B, (10 cm3 r-ru A rozcieńczyć w kolbie miarowej 5% TCA do 100 cm3). 1 cm3 zawiera 10ug jonów SCN.
Kwas trójchlorooctowy i azotan żelazowy - przygotowane jak wyżej.
Krzywa wzorcowa.
Do kolejnych próbówek odmierzać jak w poniższej tabeli kolejno roztwory:
wzorcowy B, 5% TCA i azotanu żelazowego
R-r B
|
R-r 5% TCA |
R-r Fe(NO3)2 |
Stężenie SCN-- |
Absorbancja |
cm3
|
cm3 |
cm3 |
ug / cm3 |
-- |
0 1 2 3 4 5
|
5 4 3 2 1 0 |
5 5 5 5 5 5 |
0 (ślepa) 2 4 6 8 10 |
0,000
|
Próbówki zamknąć korkami i po dokładnym wymieszaniu odstawić w ciemne miejsce. Po 5 minutach zmierzyć powstałą absorbancję w kolorymetrze SPEKOL przy długości fali 470 nm i użyciu kiuwet o długości 1 cm, wobec próby ślepej. Wykreślić krzywą w układzie współrzędnych.
Część II Badanie obecności tiocjanianów w próbkach warzyw
Celem ćwiczenia jest oznaczenie zawartości tiocyjanianów w wybranych warzywach oraz wykazanie wpływu ogrzewania w środowisku wodnym na zachowanie się tych związków w produkcie w różnych warunkach.
Materiał do ćwiczeń.
Świeżo zakupione warzywa z roślin krzyżowych (kapusta biała, włoska, brykselka, por, kalafior, brokuły).
Odczynniki.
Kwas trójchlorooctowy, 5 % r-r TCA.
Azotan żelazowy r-r (rozpuścić w kolbie miarowej o pojemności 500 cm3 80g Fe(NO3)2 * 9H2O w 250 cm3 2M HNO3, uzupełnić wodą destylowaną do kreski).
Wyposażenie i sprzęt.
Zestaw do rozdrabniania warzyw (deska, nóż)
Waga techniczna
Waga analityczna
Zlewka 100 cm3
Cylinder miarowy 50 cm3
Sitko kuchenne
Statyw z próbówkami
Moździerz porcelanowy, chropowaty100 cm3 z pistelem.
Kolbki stożkowe 250 cm3 z korkiem na szlif
Wytrząsarka laboratoryjna
Zestaw do sączenia + sączki twarde
Wirówka laboratoryjna z próbówkami wirówkowymi 100 cm3
Zestaw do podgrzewania (gazowy lub elektryczny).
Kolorymetr lub spektrofotometr z kuwetami 1 cm.
Przygotowanie materiału.
Wybrać jedno z kupionych warzyw i z części przeznaczonej do spożycia
(np. nać pietruszki, kapusta - liście, cebula - wewnętrzne łupiny) odciąć i odważyć na wadze technicznej około 20 g produktu. Starannie poszatkować nożem na małe skrawki i na wadze analitycznej z dokładnością do 1 mg odważyć 3 osobne porcje po 5 g każda. Jedną z nich przenieść przy pomocy bagietki szklanej do moździerza (próbka surowa), natomiast drugą i trzecią do zlewek na 100 cm3 a następnie dodać do każdej 50 cm3 wody destylowanej.
Zawartość drugiej zlewki kilkakrotnie zamieszać bagietką (próba zimna), natomiast trzeciej na zestawie grzejnym doprowadzić do wrzenia a następnie po zmniejszeniu intensywności grzania - utrzymać w lekkim wrzeniu przez okres 10 minut (próba gotowana).
Stosując sitko kuchenne jako zabezpieczenie odlać wodę ze zlewek i przy pomocy bagietki przenieść odcedzone próbki do drugiego i trzeciego moździerza.
Wykonanie oznaczenia.
Przygotowany jak wyżej materiał (surowy, zimny i gotowany) rozetrzeć dokładnie w moździerzach przy użyciu pisteli. Roztarte próbki przenieść ilościowo do kolb Erlenmajera 250 cm3 ze szlifem, korzystając z pomocy 45 cm3 5 % r-ru TCA. Kolby zamknąć doszlifowanymi korkami a następnie wytrząsać 10 min. w wytrząsarce laboratoryjnej. Zawartość kolb przelać do próbówek wirówkowych i odwirować przy 4000 obr./min. przez 10min. Przed wstawieniem do wirówki próbówki wirówkowe z zawartością muszą zostać zrównoważone na wadze technicznej przy pomocy wkraplanego r-ru 5% TCA. Po odwrowaniu ciecz nad osadową zlewarować na twardy sączek.
Z każdego przesączu (po dokładnym wymieszaniu) pobrać po 2 cm3 do 2 próbówek. Do jednej próbówki dodac 2 cm3 wody destylowanej (I próba ślepa), a do drugiej 2 cm3 azotanu żelazowego. Ponadto przygotować II próbę ślepą (odczynnikową), biorąc do 3 próbówki po 2 cm3 wody i azotanu żelazowego.
Uwaga : z chwilą dodania r-ru azotanu żelazowego próbki trzymać bez dostępu światła.
Zmierzyć absorbancje prób właściwych i ślepych wobec wody destylowanej. Odczytu dokonać po czasie nie dłuższym niż 5 min. od momentu dodania azotanu żelazowego. Stężenie siarkocyjanków w badanej próbce odczytać z krzywej wzorcowej, pomniejszając uzyskaną absorbancję o wartości odpowiednich prób ślepych (ślepej próby i ślepej odczynnikowej) zgodnie ze wzorem:
AC = AP - A1S - A2S
gdzie: AC - absorbancja całkowita próbki
AP - absorbancja pierwotna próbki
A1S - absorbancja próby ślepej
A2S - absorbancja próby ślepej odczynnikowej
Wynik przeliczyć na naważkę i na 100 g produktu.
Opracowanie wyników.
Zestawić uzyskane wyniki i na ich podstawie omówić wpływ różnych czynników na zawartość tiocyjanianów w produktach roślinnych.
Literatura.
1. Zbiorowe pod red. A. Brzozowskiej - „Toksykologia żywności -przewodnik do ćwiczeń”, Wydawnictwo SGGW, Warszawa 2004
Ćwiczenie 9
Związki toksyczne w środowisku. Identyfikacja i oznaczanie związków chromu w ściekach.
1. Wprowadzenie
Chrom należy do grupy pierwiastków rzadkich. Najczęściej jest stosowany do produkcji stopów z żelazem i do pokrywania powierzchni metalowych, ponadto do produkcji pigmentów, farb, preparatów grzybobójczych, jako katalizator, do produkcji cegły ogniotrwałej, zapraw muraraskich. Jest stosowany w przemyśle tekstylnym, garbarskim, do produkcji sacharyny, klejów, żeli, przy oczyszczaniu olejów.
Wszystkie związki chromu są barwne, stąd też jego nazwa pochodząca od greckiego chroma - barwa.
Chrom w związkach może znajdować się na następujących stopniach utlenienia: (-2), 0, (+2), (+3), (+6). Jednakże w naturze, w roztworach wodnych najczęściej chrom występuje na stopniach utlenienia (+3) i (+6) czyli jako chrom trój i sześciowartościowy. W roztworze kwaśnym występują jony: chromawe (Cr+2), chromowe (Cr+3) i dwuchromianowe Cr2O7-2 (chrom +6) a w roztworze zasadowym jony chrominowe CrO2-1 (chrom +3) i dwuchromianowe (chrom +6). Jon dwuchromianowy w połączeniu z stężonym H2SO4 tworzy cząsteczki CrO2 o silnych własnościach utleniających co powszechnie wykorzystuje się w laboratoriach środowiskowych (oznaczanie ChZT, mieszanina chromowa do mycia szkła).
Należy mieć na uwadze że formy chromu są zmienne i zależne od warunków. W dobrze natlenionych wodach powierzchniowych będzie przeważać chrom (+6), natomiast w warunkach anaerobowych pod wpływem siarczków i w obecności związków organicznych ta forma chromu łatwo redukuje się do chromu (+3). Jon chromowy tworzy wiele związków kompleksowych ze związkami organicznymi stąd przy ocenie ogólnej zawartości chromu np. w ściekach czy osadach dennych konieczne jest oznaczanie form chromu nie tylko w próbkach sklarowanych ale i w obecnej w ściekach zawiesinie, która może zawierać nawet 67 - 98% całego chromu ogólnego w jednostce objętości.
Chrom w małych ilościach jest pierwiastkiem istotnym dla życia roślin i zwierząt. Pomimo że chrom jest relatywnie mało toksyczny dla człowieka to w dużych ilościach oddziaływuje szkodliwie. Związki chromu uszkadzają układ oddechowy, przewód pokarmowy, wywołują zmiany skórne. Wykazują działanie rakotwórcze, mutagenne, embriotoksyczne i teratogenne. Chrom wykazuje powinowactwo do wielu enzymów, hamując lub pobudzając katalizowane przez nie reakcje. Chrom trójwartościowy łatwo tworzy trwałe połączenia z DNA, co prowadzi do jego uszkodzenia i w efekcie przyczynia się do rozwoju nowotworów złośliwych. Łącząc się dobrze z białkami chrom (+3) powoduje ich wytrącenie co jest widoczne w szkodliwym działaniu na skórę i błony śluzowe. W oddziaływaniu ciągłym prowadzi to nie tylko do owrzodzenia skóry, przewodu pokarmowego i górnych dróg oddechowych ale także do uszkodzenia nerek.
Jednakże pod względem siły oddziaływania związki chromu (+3) są aż 10-krotnie mniej toksyczne od związków chromu (+6) co znalazło swój wyraz w ustawodawstwie. Jeszcze przed przyjęciem do UE polskie przepisy przewidywały następujące maksymalne zawartości różnych form chromu w wodzie i ściekach [mg Cr / dm3 ] jak podano w tabeli 1:
Tab. 1
Formy chromu |
Klasa czystości wód powierzchniowych I II III |
Ścieki w kanalizacji |
||
Cr +3 |
< 0,5 |
< 0,5 |
< 0,5 |
---------- |
Cr +6 |
< 0,05 |
< 0,05 |
< 0,05 |
---------- |
Cr ogólny |
< 0,05* |
------- |
------- |
< 0,2 |
* - wymagania dla wody do picia
Toksyczne oddziaływanie chromu (+6) na organizmy wodne obserwuje się już wtedy gdy jego stężenie w wodzie przekracza poziom 0,20 mg Cr+6 / dm3 co ilustruje poniższe zestawienie w tabeli 2:
Tab. 2
Organizmy testowe
|
Stężenie w wodzie [ mg Cr+6 / dm3 ] |
Ryby |
15 - 80 |
Mikroorganizmy w biologicznej oczyszczalni ścieków |
2 - 5 |
Glony |
0,7 |
Bakterie |
0,5 |
Mikroorganizmy w samooczyszczaniu rzek |
0,3 |
Pierwotniaki |
0,21 |
Od wejścia Polski do UE egzekwowane są przepisy nakazujące traktować chrom i jego związki jako niebezpieczne dla środowiska co pociąga za sobą konieczność ich wstępnej segregacji i składowania odpadów powstających na ich bazie (ścieki, osady) w odrębnych pojemnikach. Ich zawartość podlega następnie unieszkodliwieniu w wyspecjalizowanych zakładach.
Część I wykonanie krzywej wzorcowej
Chrom (Cr6+) w środowisku kwaśnym daje charakterystyczne fioletowo-czerwone zabarwienie z dwufenylokarbazydem. Intensywność barwy powstałego kompleksu jest wprost proporcjonalna do stężenia jonów Cr6+.
Odczynniki.
K2Cr2O7 r-r podstawowy. 1cm3 = 0.1 mg Cr+6 (0.1415 g dwuchromianu potasowego wysuszonego do stałej wagi w temp. 130oC rozpuścić w 0.5 dm3 H2O destylowanej, starannie wymieszać.
K2Cr2O7 r-r wzorcowy. 1 cm3 = 0.01 mg Cr+6 ( 100 cm3 r-ru podstawowego odmierzyć do kolby miarowej na 1 dm3, uzupełnić do kreski wodą destylowaną. Ten sam roztwór będzie używany jako dawkujący.
DFK. Difenylokarbazyd - świeżo przygotowany. Roztwór 0.25% DFK w acetonie.
H2SO4 - r-r 0.05M
Wykonanie krzywej wzorcowej
Do kolbek miarowych o pojemności 50 cm3 odmierzyć r-r wzorcowy chromu w ilości: 0.00 (próba ślepa), 0.25, 0.50, 1.00, 2.00, 4.00, 6.00, 8.00 cm3.
Do każdej kolbki odmierzyć 1 cm3 r-r DFK i uzupełnić zawartość kolbek do kreski 0.05M H2SO4. Zamknąć kolbki korkami i starannie wymieszać.
Odpowiada to zawartości chromu Cr+6 odpowiednio: 0.00, 0.05, 0.10, 0.20. 0.40, 0.80, 1.20, 1.60 ug Cr+6 / cm3. Zmierzyć intensywność powstałego zabarwienia po upływie 10 min. przy użyciu kiuwet o L=1 cm i długości fali światła 540 nm.
Część II Badanie obecności chromu w ściekach
Ilościowe, kolorymetryczne oznaczanie chromu w ściekach.
Odczynniki.
- 0,04% acetonowy r-r difenylokarbazydu.
0,05M H2SO4
Na2S2O8, stały, (Peroksydisiarczan sodu)
K2Cr2O7 , r-r A, (Z wysuszonego w temp.1300C K2Cr2O7 odważyć 0,2829 g i rozpuścić w wodzie destylowanej, w kolbie miarowej o pojemności 1 dm3.
1cm3 = 0,1 mg Cr+6
K2Cr2O7, r-r B, (r-r świeżo przygotowany). Odmierzyć do kolby miarowej 10 cm3 r-ru A i uzupełnić wodą destylowaną do 1 dm3.
1cm3 = 0,001mg Cr+6.
Wykonanie oznaczenia.
1. Czynności wstępne.
Jeżeli próbka ścieków jest klarowna - przystąpić do wykonania pkt.2
Jeżeli próbka ścieków jest mętna i nie klaruje się - przesączyć lub odwirować a oznaczenie wykonać dla próbki sączonej i niesączonej.
Jeżeli próbka ścieków zawiera klarujące się zawiesiny - oznaczyć chrom w próbce sklarowanej a następnie w dobrze wymieszanej.
2. Oznaczanie chromu.
Do zlewki 150 cm3 pobrać z klarownej próbki ścieków 50 cm3. Wstawić zlewkę na mieszadło magnetyczne i wkraplać 0,05M H2SO4 aż do uzyskania odczynu roztworu poniżej 1,5 pH (kontrolować przy pomocy pehametru). Pałeczką szklaną wsypać około 0,2g Na2S2O8 i po wymieszaniu wstawić na okres 20 min. na łaźnię wodną o temp.800C. Po ochłodzeniu przelać zawartość zlewki do cylindra Nesslera i (w razie potrzeby) uzupełnić wodą destylowaną do poziomu 50 cm3. Dodać do roztworu 2,5 cm3 difenylokarbazydu. Wymieszać i odstawić na 10 min.. Po tym czasie zmierzyć wartość absorbancji przy długości fali 540nm i użyciu kiuwet o długości 1cm wobec próby ślepej (50 cm3 wody destylowanej) równocześnie oznaczanej. W przypadku próbki z zawiesiną przed pomiarem odwirować z szybkością 4000 obr./min.
Z krzywej wzorcowej odczytać zawartość chromu w 50 cm3 próbki.
3. Opracowanie wyników
Ustalić jakie formy chromu występują w badanych ściekach. Podając wyniki oznaczeń ilościowych w mg Cr / dm3 pamiętać o ewentualnym uwzględnieniu zastosowanego rozcieńczenia. Ocenić gdzie występuje najwięcej chromu: w formie rozpuszczonej sklarowanej cieczy, w zawiesinie czy w osadzie. Podać zawartość chromu ogólnego i omówić jaki będzie miała wpływ taka ilość gdy badana próbka:
pochodzi ze ścieków bytowych i płynie na oczyszczalnię biologiczną
pochodzi z wód przemysłowych które są odprowadzane wprost do odbiornika (rzeka lub zbiornik retencyjny).
Literatura.
1.- J. Dojlido - „Chemia wody”, Arkady, Warszawa 1987r
2.- J. Dojlido (red) - „Fizyko-chemiczne badanie wody i ścieków”, Arkady,
Warszawa 1999r.
3.- A. Bajguz, A. Piotrowska - „Ćwiczenia z toksykologii środowiska”,
Wydaw. Uniwersytetu Białostockiego, Białystok, 2005r.
Ćwiczenie 10
Związki toksyczne w środowisku. Identyfikacja i oznaczanie substancji powierzchniowo czynnych w ściekach
Wyszukiwarka
Podobne podstrony:
Obliczenia w ekotoksykologii, OŚ, sem II 1 SOWiG, Ekotoksykologia, Eko Laboratoria
test na inteligencję emocjonalną, OŚ, sem II 1 SOWiG, Negocjacje, testy
techniki sterowania przebiegiem, OŚ, sem II 1 SOWiG, Negocjacje
Akwakompleksy metali, OŚ, sem II 2 SOWiG, Chemia Środowiska, Seminarium ChŚ
Załącznik A4-Oświadczenie Wnioskodawcy, OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska
WNIOSEK C1 , OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska w Polsce, Projekt SFOŚwP
cw zakres KMB, OŚ, sem II 1 SOWiG, Planowanie Przestrzenne
Chemia fizyczna - wykad 5, OŚ, sem II 1 SOWiG, Chemia Fizyczna
Wykaz załączników - B2 kanalizacja, OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska w Po
Ćwiczenie semestr letni 2013 - 2014 2, OŚ, sem II 2 SOWiG, Systemy Finansowania Ochrony Środowiska w
Test kreatywności, OŚ, sem II 1 SOWiG, Negocjacje, testy
informacja, OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska w Polsce, Projekt SFOŚwP
opisy do testów, OŚ, sem II 1 SOWiG, Negocjacje, testy
PwOŚ 18.03.2013, OŚ, sem II 1 SOWiG, Pomiary w Ochronie Środowiska
Chemia fizyczna - Loska, OŚ, sem II 1 SOWiG, Chemia Fizyczna, ChF laboratoria
Formularz Pp2, OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska w Polsce, Projekt SFOŚwP
konflikt i style neg, OŚ, sem II 1 SOWiG, Negocjacje
Formularz Pp1, OŚ, sem II 1 SOWiG, Systemy Finansowania Ochrony Środowiska w Polsce, Projekt SFOŚwP
CHF PYTANIA, OŚ, sem II 1 SOWiG, Chemia Fizyczna
więcej podobnych podstron