skanuj0019 (Kopiowanie)

Badania modelowe doodbytniczych postaci leku prowadzone in vitro nie zawsze dają się porównać z wynikami uzyskanymi in vivo. W badaniach in vitro ważną rolę odgrywać będzie rozpuszczalność substancji leczniczej w wodzie, podczas gdy w badaniach in vivo ważniejszą rolę odgrywa jej forma chemiczna (np. kwas lub sól). Dwie substancje lecznicze, mające taką samą rozpuszczalność w wodzie mogą się wchłaniać z różną szybkością z podłoża tłuszczowego. Natomiast substancje słabo rozpuszczalne w wodzie wchłaniają się z podłoży tłuszczowych niejednokrotnie szybciej niż te, które są dobrze rozpuszczalne w wodzie. Badanie uwalniania i wchłaniania substancji leczniczej z czopków powinno obejmować różne formy chemiczne tego samego związku (wolny kwas, wolna zasada, sól, ester, kompleks).
3.3.2. Uwalnianie substancji leczniczej z maści
Badanie uwalniania substancji leczniczych z podłoży maściowych przeprowadza się głównie 3 metodami:
1. Metodą dyfuzji do agaru — dla substancji działających bakteriobójczo lub bakteriostatycznie, dla barwników i substancji zawierających izotopy promieniotwórcze.
2. Metodą dyfuzji przez błonę (którą może być błona celofanowa, nylonowa, sztuczne błony fosfolipidowe lub błony zwierzęce) do buforu lub
wodnego roztworu chlorku sodowego.
I 3
|
r |
—r—i- ■ i i i J-1—LJ |
1 ! 1 1! ! Ł! ! 1 | ||
|
------1 n- I • |
lilii i • | |||
|
1 1 |
1 ! i J i ii | |||
|
1 1 1 1 -L_l- |
i i. ; i i i* i • 1 ii ii Ł..i. L.L 1 , 1 -L---- | |||
l
36 Zarys biofarmacji
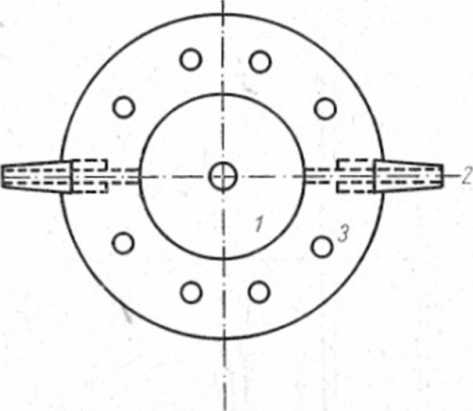
Ryc. 3.7. Schemat przyrządu do badania szybkości uwalniania substancji leczniczej z maści [wg Wardyńskiej]: 1 — komora przepływowa z płynem dializacyjnym, 2 — podłączenie do pompy perystaltyczncj, 3 — zaciski metalowe
3. Przez ekstrakcję substancji leczniczej bezpośrednio z podłoża d<3 płynu ekstrakcyjnego.
Schemat przyrządu do badania uwalniania substancji leczniczej z maści działającego na zasadzie dyfuzji przez błonę półprzepuszczalną przedstawiono na ryc. 3.7.
3.4. Ilościowa interpretacja danych szybkości rozpuszczania
badanie szybkości rozpuszczania za pomocą opisanych przyrządów polega na ilościowym oznaczeniu substancji rozpuszczonej w określonych odstępach czasu. Częstość pobierania próbek jest zależna od szybkości rozpuszczania danej substancji leczniczej.
Całkowitą ilość substancji rozpuszczonej po określonym czasie t oblicza się ze wzoru:
Mt = mt+ £ m, (3.8)
w którym: *
Mt — całkowita ilość substancji rozpuszczona po czasie r,
V — objętość płynu, w którym zanurzona jest tabletka,
v — objętość roztworu badanego pobieranego każdorazowo do analizy,
nu — ilość substancji znaleziona w próbce v,
Sm, — sumaryczna ilość substancji znaleziona w próbkach v uprzednio pobieranych.
Wykres całkowitej ilości substancji rozpuszczonej (wyrażonej w miligramach lub procentach) jako funkcji czasu przedstawiony w skali liniowej (profil rozpuszczania) ilustruje przebieg rozpuszczania w postaci krzywej, z której bezpośrednio można odczytać takie parametry, jak ilość substancji rozpuszczonej po pewnym czasie, np. 20%, 50%, 80%> lub odpowiadające im wartości czasu: t2o%, t5o%, ?8o%.
Dopasowanie danych doświadczalnych do odpowiednich równań przeprowadza się często przez linearyzację tych danych, a ujmując krzywą rozpuszczania jako funkcję czasu otrzymuje się (często dzięki komputeryzacji danych) parametry, które pozwalają porównywać różne formulacje lub przewidywać zachowanie się postaci leku in vivo.
W większości przypadków, jeżeli zachowane są warunki „sink”, mamy do czynienia z reakcją I rzędu, przez co graficzną ilustracją wyników będzie w skali półlogarytmicznej linia prosta zgodnie z równaniem:
ln (d—CV) = -Kt (3.9)
w którym:
C — stężeni: roztworu
V — objętość roztworu,
il — dawka lub deklarowana ilość substancji leczniczej w postaci leku lub jej ilość rozpuszczona po nieskończenie długim czasie.
Uwalnianie substancji leczniczej 37
Wyszukiwarka
Podobne podstrony:
skanuj0014 (Kopiowanie) 3. UWALNIANIE SUBSTANCJI LECZNICZEJ Z POSTACI LEKU Proces wchłaniania poprze
skanuj0031 (Kopiowanie) 4.2.6. Pinocytoza Pinocytoza jest jedynym rodzajem transportu, w którym cząs
skanuj0209 Powyższe funkcje najlepiej wyrażają istotę i zakres zadań oraz działań kierowniczych. Nie
skanuj0065 (Kopiowanie) gicznych okresach półtrwania podawanego leku) i wyrażenie e~’,KT staje się p
skanuj0012 (Kopiowanie) wiązane przez tkanki, podczas gdy inne (sulfonamidy) w ogóle nie wiążą się z
skanuj0157 (11) 168 PHP i MySQL dla każdego Ponieważ porządkowanie leksykograficzne nie zawsze daje
55381 skanuj0050 (36) 53 WSPÓŁCZESNA TURYSTYKA KULTUROWA które pojawiły się na tyle niedawno, iż nie
63135 skanuj0041 pokochasz siebie. automatycznie kochasz też drugiego człowieka. Podobnie jak nie mo
skanuj0001 (140) Reakcja FCR * naśladuje proces replikacji DMA in vitro * &n
DSCF5591 Metody alternatywne w badaniu działania żrącego na skórę Metody in vitro Istnieją cztery me
skanuj0007 (Kopiowanie) zwierzęcia z określonej postaci leku, traktowanej jako system dostarczający
skanuj0067 (Kopiowanie) 9. POZANACZYNIOWE PODAWANIE LEKÓW9.1. Typy postaci leku do podawania pozanac
skanuj0078 (Kopiowanie) 9.3.2. Biofarmaceutyczne aspekty leków doustnych Postacie leku przeznaczone
więcej podobnych podstron