451 [1024x768]

461
ILOŚCIOWY OPIS SZYBKOŚCI REAKCJI CHEMICZNYCH
wszystkie reakcje są dwukierunkowe, dążą do osiągnięcia równowagi termodynamicznej, w której z punktu widzenia kinetycznego szybkości reakcji w obu kierunkach się zrównują. Efektywna szybkość reakcji mierzona w znacznym zaawansowaniu procesu jest wielkością wypadkową z procesu przebiegającego od substratów do produktów i procesu odwrotnego.
Jeżeli wykreślimy doświadczalnie stwierdzoną zależność stężenia substratu lub produktu od czasu, to szybkość reakcji, jako pochodna stężenia względem czasu, może być określona z nachylenia stycznej względem znalezionej krzywej
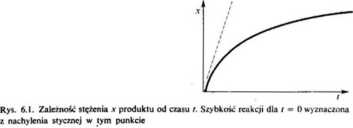
w punkcie dla danego czasu / (rys. 6.1). W przypadku, gdy chcemy określić szybkość początkową reakcji wówczas styczna musi być poprowadzona dla / = 0.
Szybkość reakcji dla / = 0 wynosi
v - kaT (6.18)
gdzie: a — stężenie początkowe substratu, a n — rząd reakcji względem tego substratu. Porównajmy teraz szybkości początkowe reakcji dla dwu różnych stężeń początkowych a, i a2
u, = Ara"; v2 — AraJ
Po zlogarytmowaniu
logt’i = logAr+nloga,; logv2 = logAr+/iloga2 (6.19)
skąd
logv, -logtij = n(loga, -loga2) (6.20)
i ostatecznie
(6.21)
log — log — / «2
Wyszukiwarka
Podobne podstrony:
449 [1024x768] 459 ILOŚCIOWY OPIS SZYBKOŚCI REAKCJI CHEMICZNYCH teczek substratu (lub gdy stężenia d
445 [1024x768] Ilościowy opis szybkości reakcji chemicznychPojęcia
447 [1024x768] ILOŚCIOWY OPIS SZYBKOŚCI REAKCJI CHEMICZNYCH 457 alne stężenie produktu. Weźmy prosts
453 [1024x768] ILOŚCIOWY OPIS SZYBKOŚCI REAKCJI CHEMICZNYCH Po scałkowaniu tego równania kinetyczneg
enzymy14 108 Sekcja C - Ertzyd .imłłłii akcja C - Enzymy gdzie szybkość reakcji w kierunku
CCF20120118�012 grapa 777 1) co to jest równowaga reakcji(czy coś w tym stylu) odpowiedzi: a)kiedy s
AGF00025 Czynnik sferyczny w reakcji SN2 Różnice między szybkościami reakcji są wywołane głównie prz
DSC00063 ku chemicznego; d) wszystkie odpowiedzi są praw;dk> we; e) wszystkie odpowiedzi są niepr
456 [1024x768] 466 KINETYKA CHEMICZNA Z ma wymiar szybkości reakcji; wyraża liczbę cząsteczek reaguj
457 [1024x768] MECHANIZM PRZEMIAN CHEMICZNYO w wyrażeniu na stałą szybkości reakcji gdzie A —tzw. cz
Zdjęcie0527 Szybkość reakcji chemicznej liczb a cząstek danego rodzaju reagupącycn %v jednostce
szybkości reakcji chemicznej. 18. Kinetyka reakcji enzymatycznych. Równanie
skan0237 240 Kinetyka chemiczna Przykład 5.17. Stałe szybkości reakcji w fazie gazowej 1. &nbs
IMAG0373 (4) > Katalizator
więcej podobnych podstron