
s
Ćwiczenie nr 3. Mikrobiologia ogólna – identyfikowanie bakterii na podstawie ich cech
biochemicznych i antygenowych. Oznaczanie wrażliwości bakterii na leki.
Identyfikacja bakterii – ustalenie rodzaju, gatunku, odmiany lub typu w obrębie
wyizolowanego drobnoustroju.
Metody identyfikacji:
•Ocena właściwości biochemicznych
•Metody immunologiczne
•Metody molekularne
Ocena właściwości biochemicznych
Polega na wykorzystaniu różnic w aktywności enzymatycznej między poszczególnymi
gatunkami bakterii. Określona aktywność enzymatyczna jest na ogół cechą stałą. Aktywność ta
jest najczęściej oceniana poprzez wykrywanie końcowych produktów metabolizmu danego
związku. Badania te można wykonywać po uzyskaniu czystej hodowli badanego
drobnoustroju.(posiew redukcyjny)
substrat ------ enzym ------- produkt
Oznacza się właściwości biochemicznych polega na ocenie:
•
właściwości sacharolitycznych
•
właściwości związanych z metabolizmem azotowym
•
właściwości hemolitycznych
•
właściwości lipolitycznych
•
produkcji katalazy
•
występowanie fosfatazy
1. Zestawy do biochemicznej identyfikacji bakterii to „Metody szybkiej identyfikacji
bakterii – test API”
2. Metody immunologiczne – wykrywanie antygenów lub przeciwciał
3. Metody molekularne

Antybiotyki -
Drobnocząsteczkowe substancje, które działają przeciwdrobnoustrojowo,
zabijają lub hamują rozmnażanie komórek drobnoustrojów.
Na początku za antybiotyki uważano substancje pochodzenia naturalnego wykazujące aktywność
przeciwbakteryjną. Obecnie chemioterapeutyki (substancje wytworzone przez człowieka
metodami chemicznymi) uznawane są również za antybiotyki .
Podział ze względu na pochodzenie
- Naturalne
- Półsysnetyczne
- Syntetyczne
- Chemioterapeutyki
Podział ze względu na mechanizm działania
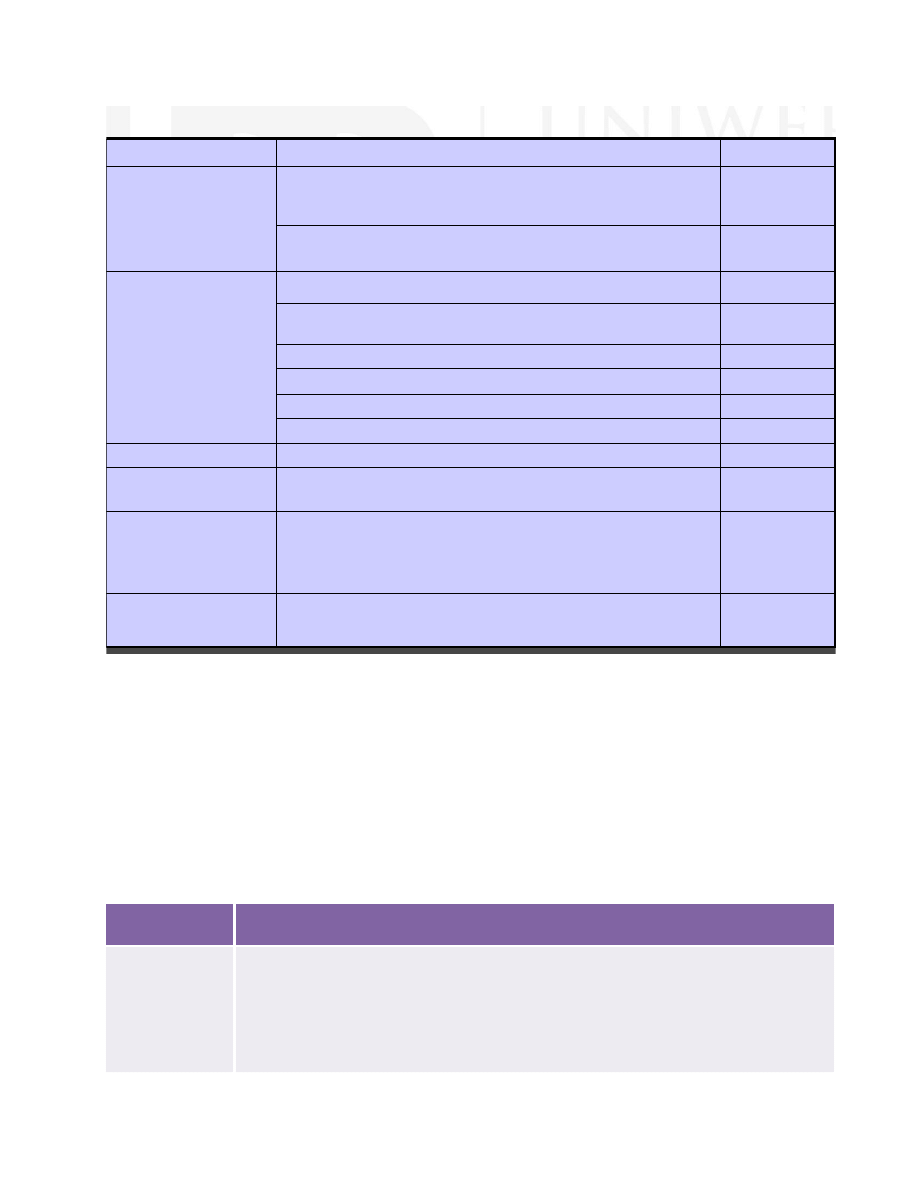
Mechanizm działania antybiotyków
Mechanizm działania
Miejs ce docelowe
antybiotyki
Hamowanie s yntez y
ś ciany komórkowej
P B P („białka wiążące penicylinę”) – mają powinowactwo do
penicyliny i innych antybiotyk ów β-laktamowych (głównie
trans peptydaz y i karboks ypeptydaz y)
Β -laktamy
K ońce dipeptydowe pods tawowej cegiełki peptydoglikanu, łącz ące
s ię z innymi elementami ś ciany komórkowej. H amowanie
polimeryz acji
glikopeptydy
Hamowanie s yntez y
białka
P odjednos tka 30S rybos omu
tetracykliny
P odjednos tka 50S rybos omu
Makrolidy
klindamycyna
P odjednos tka 30S rybos omu
aminoglikoz ydy
P odjednos tka 50S rybos omu
chloramfeikol
P odjednos tka 50S
linezolid
S yntetaz a tR NA-izoleucyny (enz ym wiążący izoleucynę z tR NA
mupirocyna
Hamowanie s yntez y
D NA
G yraz a D NA, T opoizomeraz a IV
chinolony
Hamowanie s yntez y
R NA
D NA-zależ na polimeraz a R NA
ryfampicyna
Nis zczenie błony
zewnętrznej i
cytoplazmatycznej
L ipidy błony cytoplazmatycz nej i z ewnętrznej
P olipeptydy
(polimyks yn A-
E )
daptomycyna
Hamowanie s yntez y
nukleotydów
E nz ymy uczes tnicz ące w s yntezie kwas u foliowego
S ulfonamidy
T rimetoprim
Podział ze względu na zakres działania
- wąskowidmowe – działają na wybraną grupę drobnoustrojów np. tylko na bakterie tlenowe
- szerokowidmowe – obejmują swoim spektrum kilka grup drobnoustrojów tlenowe, beztlenowe,
Gram-dodatnie, Gram-ujemne
Antybiotyki o działaniu bakteriostatycznym
Grupa
antybiotyków
Spektrum działania
makrolidy i
ketolidy
• Działają przede wszystkim na bakterie Gram-dodatnie tlenowe i
beztlenowe
• Duże znaczenie kliniczne ma ich aktywność wobec bakterii
wewnątrzkomórkowych, takich jak Mycoplasma, Chlamydia i
Legionella (bakterie atypowe)
• W mniejszym stopniu na bakterie Gram-ujemne w tym tlenowe i

beztlenowe pałeczki oraz Neisseria i Moraxella
linkozamidy
• Bakterie Gram-dodatnie
• Bakterie beztlenowe
chloramfenikol Bakterie Gram-dodatnie
Bakterie Gram-ujemne
Krętki
Riketsje
Chlamydie
mykoplazmy
Tetracykliny
tigecyklina
Mają szerokie spektrum działania (bakterie tlenowe i beztlenowe):
Bakterie Gram-dodatnie
Bakterie Gram-ujemne
Krętki
Bakterie atypowe
sulfonamidy
kotrimoksazol
Działają na:
Gronkowce
Paciorkowce
Enterobacteriaceae
oksazolidynony
bakterie Gram-dodatnie

Antybiotyki działające bakteiobójczo
Grupa
antybiotyków
Spektrum działania
Β-laktamy
Ziarniaki Gram-dodatnie
Ziarniaki Gram-ujemne
Pałeczki Gram-ujemene (Enterobacteriaceae,
niefermentujące, hemofilne)
Laseczki Gram-dodatnie
Pałeczki Gram-dodatnie
Krętki
Promieniowce
chinolony
Pałeczki Gram-ujemne fermentujące i niefermentujące
Gronkowce (szybko nabywają oporność!)
Paciorkowce
Enterokoki
Haemophilus
Neisseria
Bakterie atypowe
aminoglikozydy
Działają tylko na bakterie tlenowe
:
Pałeczki Gram-ujemne
Ziarniaki Gram-dodatnie
Prątki gruźlicy
glikopeptydy
Działają tylko na bakterie Gram-dodatnie tlenowe i
beztlenowe
polipeptydy
Bacytracyna – działa na bakterie Gram-dodatnie
Gramicydyna – działa wyłącznie na bakterie Gram-
dodatnie
Zakres działania: pałeczki Gram-ujemne fermentujące
i niefermentujące
nitroimidazole
Działają tylko na bakterie beztlenowe
nitrofurany
Bakterie Gram-dodatnie
Bakterie Gram-ujemne
Stosowane w leczeniu zakażeń układu moczowego
•
Terapia empiryczna – oparta jest na domniemaniu najbardziej prawdopodobnego czynnika
etiologicznego zakażenia i jego przypuszczalnej wrażliwości na antybiotyki. Empiryczny dobór
leku musi być oparty na analizie wyników badań klinicznych i lokalnych danych
epidemiologicznych.
•
Terapia celowana jest metodą, w której wyboru antybiotyku dokonuje się po potwierdzeniu w
badaniu mikrobiologicznym aktywności leku in vitro wobec wyizolowanego czynnika
etiologicznego zakażenia (antybiogram).
Terapia celowana = „trafienie w patogen”
•
Leczenie pierwszego rzutu (leczenie początkowe) – polega na zastosowaniu antybiotyku o
udowodnionej skuteczności i bezpieczeństwie.
Ocena aktywności przeciwbakteryjnej
Antybiogram Wynik badania wrażliwości danego drobnoustroju na działanie antybiotyków.
Metody oznaczania lekowrażliowści drobnoustrojów
Jakościowa
•Dyfuzyjno-krążkowa
Ilościowa
•Seryjnych rozcieńczeń
•E-test
Półilościowa
1. Metoda dyfuzyjno-krążkowa
Oparta jest na dyfuzji antybiotyku zawartego w krążku do podłoża. Antybiotyk dyfunduje
promieniście, tworząc gradient stężeń. Największa jego koncentracja występuje przy brzegach
krążka i spada wraz z odległością od krążka. Wielkość strefy zahamowania wzrostu bakterii jest
wprost proporcjonalna do stopnia wrażliwości bakterii na antybiotyk - im większa jest strefa
zahamowania, tym bakteria jest bardziej wrażliwa. W zależności od wielkości strefy, bakterie
określa się, jako: wrażliwe, średnio wrażliwe lub oporne na podstawie przyjętych standardów
(rekomendacje).
Wrażliwy „S” – wrażliwość drobnoustroju na standardowe dawki leku, wysokie
prawdopodobieństwo sukcesu klinicznego
Średnio wrażliwy „I”– szczepy w zakresie MIC pomiędzy wrażliwym a opornym, sukces
terapeutyczny niepewny, może być osiągnięty, gdy lek jest zagęszczany (np. w drogach
moczowych) lub może być stosowany w większej dawce (np. przy niskiej toksyczności)
Oporny „R”– wysokie prawdopodobieństwo niepowodzenia terapeutycznego, niezależnie od
dawki leku i lokalizacji infekcji
2. Metoda seryjnych rozcieńczeń
pozwalają na określenie minimalnego stężenia antybiotyku (MIC – minimum inhibitory
concetration) hamującego wzrost bakterii. Seryjne rozcieńczenia antybiotyku przygotowuje się w
podłożu płynnym lub podłożu agarowym, do których następnie dodaje się odpowiednie inoculum
i inkubuje. Metody pracochłonne, wykorzystywane głównie w badaniach naukowych.
3. E-test

•łączy dyfuzję antybiotyku w agarze i ilościowe określenie stężenia hamującego – MIC.
Wykorzystuje się paski nasycone antybiotykiem w gradiencie stężeń.
MBC (minimal bacteriocidal activity) – najmniejsze stężenie bakteribójcze
MIC (minimal inhibitory concentration) – najmniejsze stężenie hamujące
Mechanizmy oporności
Oporność – stan, w którym antybiotyk nie działa przeciwdrobnoustrojowo (nie zabija ani nie
hamuje namnażania). Taki szczep bakteryjny jest oporny na dany antybiotyk. Leczenie takim
antybiotykiem jest nieskuteczne.
Naturalna (pierwotna) – uwarunkowana genetycznie niewrażliwość pewnych gatunków,
rodzajów lub grup bakterii na dany antybiotyk. Jest to cecha stała bakterii, która była obecna
jeszcze przed odkryciem i zastosowaniem antybiotyków.
Nabyta – pojawienie się nierważliwości na dany antybiotyk bakterii uprzednio wrażliwej.
Pojawia się w wyniku mutacji lub przeniesienia genów oporności z jednej komórki bakteryjnej
do drugiej. Materiał genetyczny zawierający geny oporności może być przenoszony pomiędzy
komórkami drobnoustrojów odległych systematycznie.
Oporność krzyżowa – rozwój oporności na jeden antybiotyk pociąga za sobą oporność na
antybiotyki tej samej grupy
Oporność na antybiotyki - sposoby nabywania oporności
Mutacja – pierwotne zjawisko prowadzące do powstania oporności.
Mutacje spontaniczne - zachodzą samorzutnie, niezależnie od obecności antybiotyku w
środowisku. Są to błędy podczas replikacji DNA.
Mutacje indukowane – pojawiają się po zadziałaniu mutagenów – w warunkach naturalnych
zachodzi niezwykle rzadko.
Selekcja – utrwalenie mutacji. Komórki, które uległy mutacji prowadzącej do powstania
oporności na antybiotyk obecny w środowisku, przeżywają w obecności tego antybiotyku i stają
się początkiem populacji opornej .
Lokalizacja genów oporności
• Chromosomy – oporność chromosomalna
• Plazmidy – oporność plazmidowa
• Transpozony

• Integrony
Sposoby przenoszenia oporności
• Pionowe (wertykalne) – z komórki macierzystej do komórki potomnej
• Poziome (horyzontalne) – przenoszenie z jednej komórki bakteryjnej do innej (również
innych gatunków) genów oporności zlokalizowanych na, na drodze:
•
- koniugacji - wymiana materiału genetycznego pomiędzy komórką męską a
żeńską (tego samego gatunku)
- transdukcji – przenoszenie materiału genetycznego pomiędzy komórkami
bakterii (tego samego gatunku, a nawet szczepu) za pośrednictwem bakteriofagów.
- transformacji – bezpośrednie pobieranie materiału genetycznego ze
środowiska. Materiał genetyczny w pobierany dostaje się do środowiska na skutek śmierci
komórki lub jej rozpadu. W ten sposób mogą być pobierane geny oporności od innych gatunków
drobnoustrojów.
Flora fizjologiczna stanowi rezerwuar genów oporności dla drobnoustrojów patogennych
Życzymy owocnej nauki
Wyszukiwarka
Podobne podstrony:
PFWRE notatki cw, konspekt-1, Historia Unii Europejskiej:
ćw 2 konspekt
gimnastyka (obwód ćw.), konspekty AWF,WF, konspekty, GIMNASTYKA
ćw I konspekt
Cw. Konspekt SSE, Ekonomia UWr WPAIE 2010-2013, Semestr II, Analiza Ekonomiczna
dydaktyka ćw konspekt 2016
Konspekt ćw 1
konspekt ćw. 9, Udostępnione, Dietetyka
Nauka pływania # metoda analityczna, Ćw techniki, koordynacja, konspekty, prezentacje, trnening
Konspekt CPO cw 2
konspekt basen cw. ze współcwicz, fizjoterapia, FIZJOTERAPIA, III SEMESTR, Basen, dla osob starszych
konspekt nr8, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki, Fi
Konspekt zajęć na Pływalni ćw z?ską
ćw II konspekt
Konspekt gim podst ćw ze współpartnerem
konspekt ćw 10
więcej podobnych podstron