1
AGH, Wydział Energetyki i Paliw, kierunek Energetyka
Rok 2014/2015
Inżynieria Materiałowa w Energetyce – ćwiczenia
Zajęcia 3.
Wiązania chemiczne
Literatura:
1. Materials Science and Engineering. An Introduction. W.D. Callister, John Wiley & Sons 2007.
Rozdz. 2. Atomic structure and interatomic bonding.
2. Wstęp do Fizyki Ciała Stałego, C. Kittel, Wydawnictwo Naukowe PWN, Warszawa 1999.
Rozdz. 3. Wiązanie w kryształach i stałe sprężyste.
3. Chemia Ciała Stałego, J. Dereń, J. Haber, R Pampuch, PWN 1975.
Rozdz. 1. Wiązania chemiczne w kryształach.
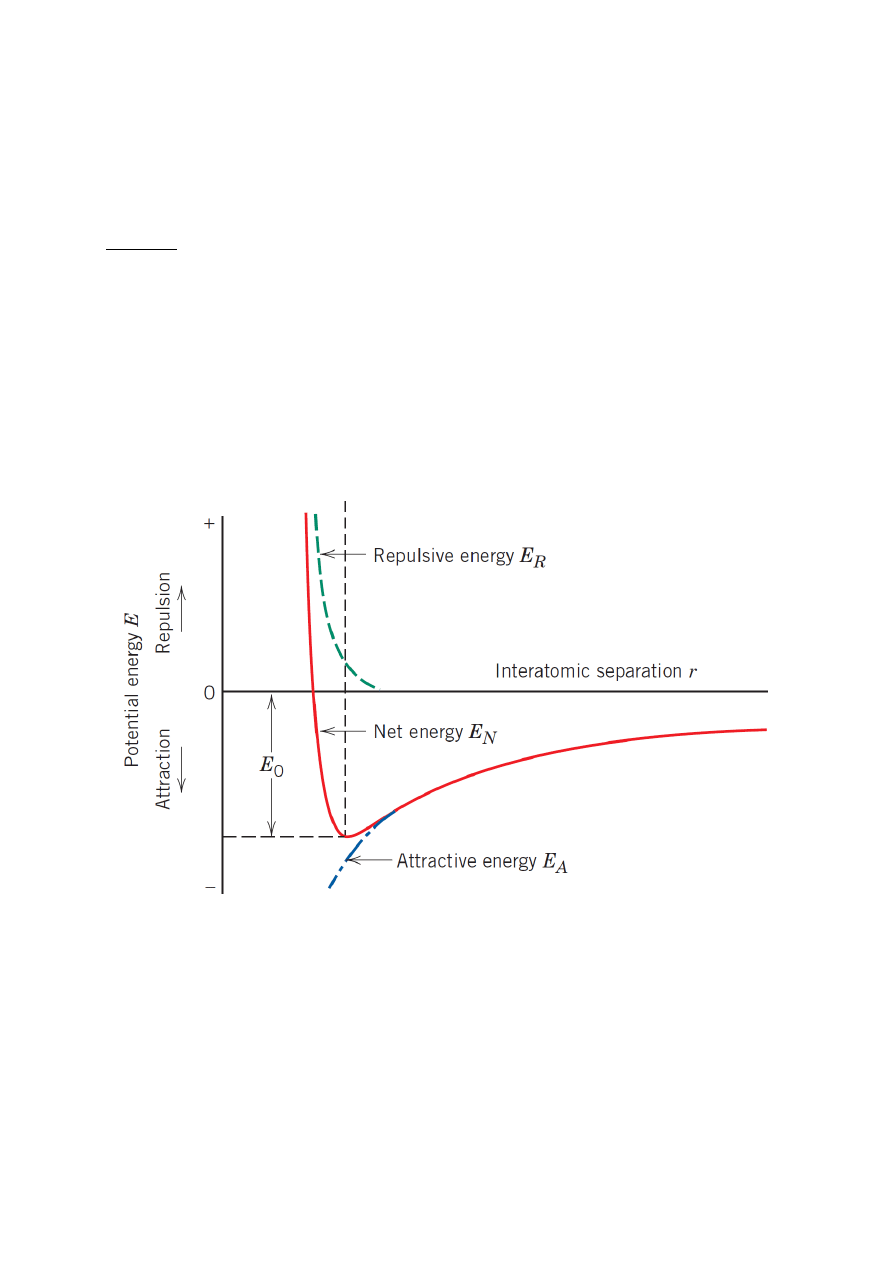
Rys. 1. Energia odziaływań przyciągających (E
A
), odpychających (E
R
) i wypadkowych (E
N
= E
A
+ E
R
) w
funkcji odległości pomiędzy dwoma izolowanymi atomami tworzącymi wiązanie chemiczne.

2
Zadania:
1. Wypadkowa energia oddziaływania pomiędzy dwoma sąsiednimi atomami w funkcji
odległości (przedstawiona na Rys. 1) może być opisana równaniem:
𝐸(𝑟) = −
𝐴
𝑟
+
𝐵
𝑟
𝑛
(1)
Symbole A, B i n oznaczają wartości stałe >0.
a. Na podstawie równania wyznacz energię wiązania i równowagową odległość
międzyatomową.
b. Wyznacz wartość liczbową energii wiązania i równowagowej odległości
międzyjonowej dla oddziaływania pomiędzy jonami Na
+
i Cl
-
, które jest opisane
parametrami: A = 1,436 eV·nm; B = 7,32·10
-6
eVnm
8
; n = 8.
2. Oblicz energię przyciągania elektrostatycznego pomiędzy jonami K
+
i O
2-
znajdującymi się w
odległości 1,5 nm. Porównaj uzyskaną energię oddziaływania elektrostatycznego z energią
oddziaływania grawitacyjnego pomiędzy tymi jonami.
3. Wypadkowa energia pomiędzy sąsiednimi atomami w funkcji odległości (przedstawiona na
Rys. 1) może być opisana równaniem:
𝐸(𝑟) = −
𝐶
𝑟
+ 𝐷 ∙ 𝑒𝑥𝑝 (−
𝑟
𝜌
)
(2)
Symbole C, D i ρ oznaczają wartości stałe >0.
Na podstawie równania wyznacz energię wiązania jako funkcję r
0
opisaną parametrami D i ρ
(stałą C można wyeliminować na podstawie równania wyrażającego warunek zerowania się
pochodnej w punkcie ekstremum funkcji).
Wyszukiwarka
Podobne podstrony:
1F CWICZENIE zadanie wg Adamczewskiego na porownawczą 97id 18959 ppt
Ćwiczenia 9 zadania
Ćwiczenia 7 zadania
ćwiczenia+1+i+2-+zadania+i+odpowiedzi, [ POZOSTAŁE ], [ Logika ]
Cwiczenia 4 zadania
geologia - projekty, ćwiczenia, zadania, notatki, ściągi, geologia - azbest
ĆWICZENIA 4 zadania, MATERIAŁY DYDAKTYCZNE, RACHUNKOWOŚĆ ZARZĄDCZA
cwiczeniadynamika8 zadania
ĆWICZENIA 7 zadania, MATERIAŁY DYDAKTYCZNE, RACHUNKOWOŚĆ ZARZĄDCZA
Cwiczenia, Zadanie 2
cwiczeniadynamika10 zadania
Ćwiczenia 6 zadania
WMech PK cwiczenia zadania
2014 03 30 Metody Wyceny Przedsiębiorstw ćwiczenia zadanieid 28536
3 Cwiczenia zadania2 transformata Z id 606489 (2)
Ćwiczenia 6 zadania
Cwiczenie 6 zadania
Ćwiczenia 4 zadania
więcej podobnych podstron