‹#›
RJC
Addycje Elektrofilowe
Addycje Elektrofilowe
Addycje Elektrofilowe
Addycje Elektrofilowe
Slides 1 to 19
E
E
R
R
R
R
R
R
R
R
X
E
R
R
R
R
X
‹#›
RJC
Addycje Elektrofilowe
Addycje Elektrofilowe
Mogą być rozpatrywane jako reakcje odwrotne do
Mogą być rozpatrywane jako reakcje odwrotne do
eliminacji E1.
eliminacji E1.
R
2
C=CR
2
+
E
X
R
2
C
E
CR
2
X
‹#›
RJC
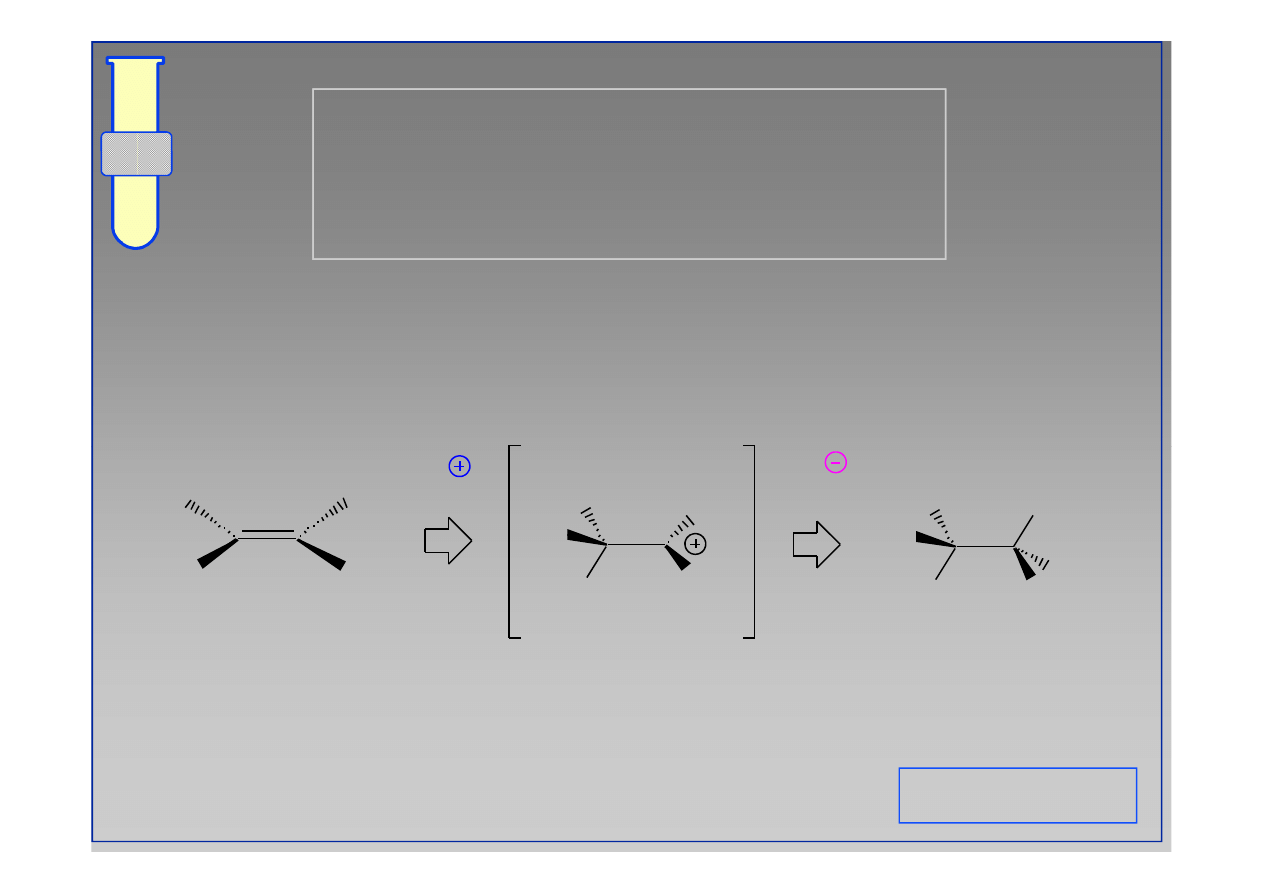
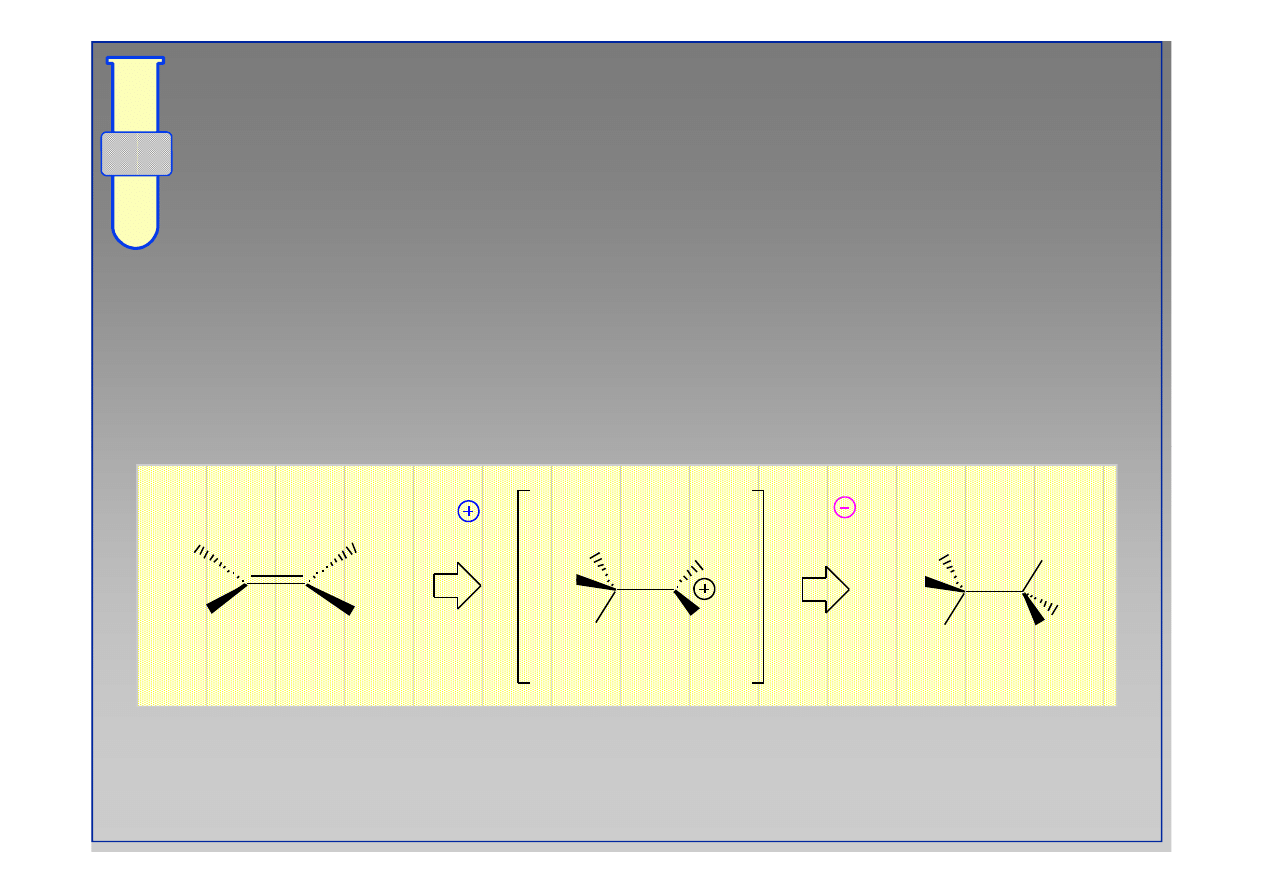
Mechanizm
Mechanizm
Elektrofil (E
Elektrofil (E
+
+
) przyłącza się do wiązania podwójnego, a
) przyłącza się do wiązania podwójnego, a
nukleofil (X
nukleofil (X
--
) neutralizuje utworzony pośrednio
) neutralizuje utworzony pośrednio
karbokation.
karbokation.
E
E
R
R
R
R
R
R
R
R
X
E
R
R
R
R
X
‹#›
RJC
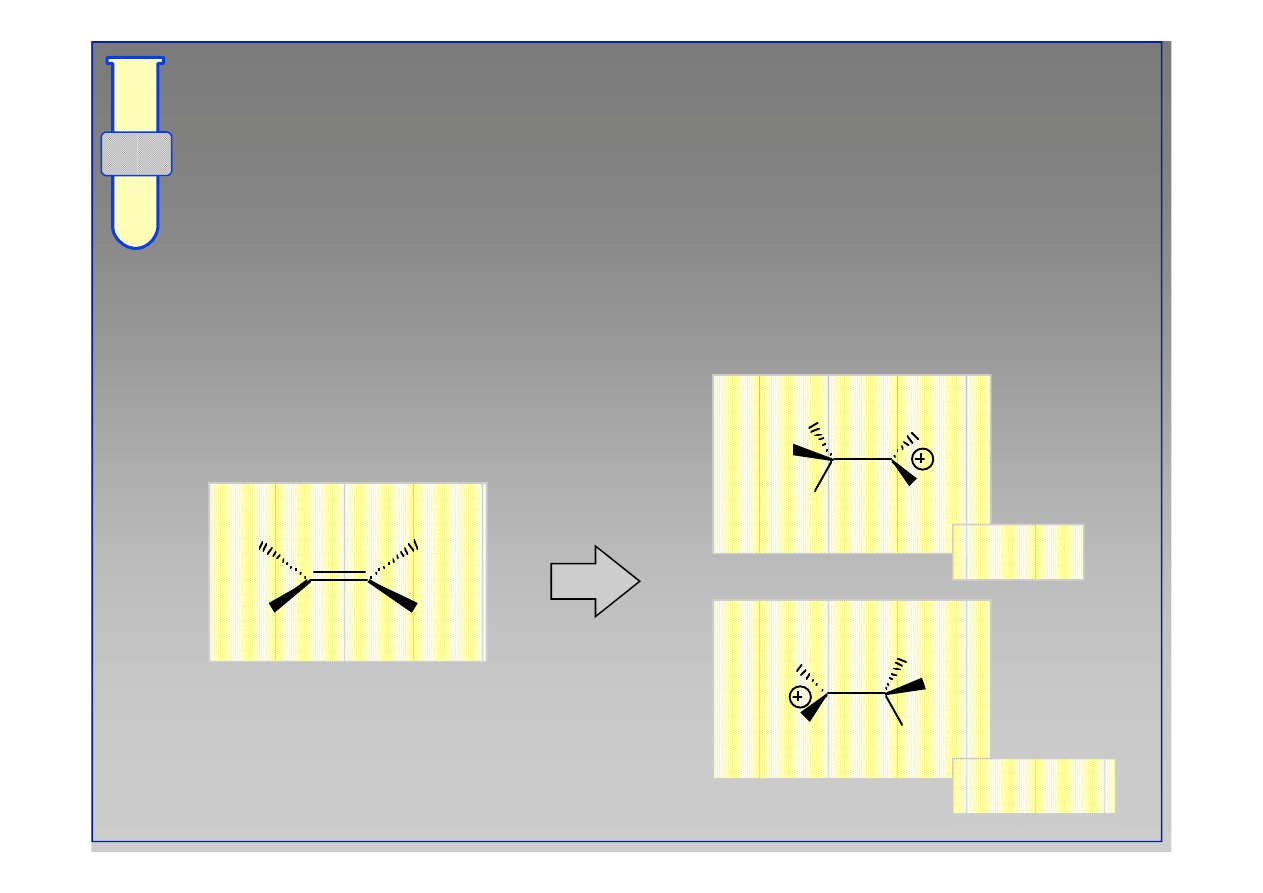
Regioselektywność
Regioselektywność
Jeżeli istnieje możliwość utworzenia dwóch
Jeżeli istnieje możliwość utworzenia dwóch
karbokationów, to preferowany jest ten, który
karbokationów, to preferowany jest ten, który
posiada więcej podstawników wokół centrum
posiada więcej podstawników wokół centrum
kationowego (bardziej podstawiony).
kationowego (bardziej podstawiony).
R
R
H
R
R
H
R
E
H
R
E
R
R
R
H
E
+
główny
poboczny
‹#›
RJC
Reguła Markownikowa
Reguła Markownikowa
Obserwacja eksperymentalna...
Obserwacja eksperymentalna...
„.. w addycji odczynnika HX do alkenu, H
+
przyłącza się do mniej podstawionego atomu
węgla (z większą liczbą atomów H), a fragment
X
–
do bardziej podstawionego..."
X
–
do bardziej podstawionego..."

‹#›
RJC
Inaczej wyrażona reguła Markownikowa...
Inaczej wyrażona reguła Markownikowa...
Interpretacja oparta o teorię mechanizmów ...
Interpretacja oparta o teorię mechanizmów ...
"...Addycja HX do niesymetrycznego wiązania
C=C przebiega poprzez karbokation o wyższej
C=C przebiega poprzez karbokation o wyższej
rzędowości..."
‹#›
RJC
Karbokationy
Karbokationy
Tworzą płaską strukturę (planarną) z atomem
Tworzą płaską strukturę (planarną) z atomem
węgla zhybrydyzowanym sp
węgla zhybrydyzowanym sp
2
2
; są stabilizowane
; są stabilizowane
poprzez efekt hiperkoniugacji oraz efekty
poprzez efekt hiperkoniugacji oraz efekty
indukcyjne.
indukcyjne.
ss
ss sp
sp
2
2
sp
sp
2
2
sp
sp
2
2
ss
ss
C
H
H
H
Struktura płaska, trygonalna
‹#›
RJC
H
H
ii
perkoniugacja
perkoniugacja
Elektrony wiążące ulokowane w pobliskich wiązaniach
Elektrony wiążące ulokowane w pobliskich wiązaniach
C
C--H, pomagają w stabilizacji karbokationu.
H, pomagają w stabilizacji karbokationu.
H
H
δδδδ
+
C
C
H
H
H
H
H
H
C
C
C
C
H
H
H
H
H
H
H
H
H
H
δδδδ
δδδδ
+
‹#›
RJC
Efekty Indukcyjne
Efekty Indukcyjne
Grupy alkilowe R są bardziej elektronodonorowe
Grupy alkilowe R są bardziej elektronodonorowe
niż atomy H i dlatego lepiej stabilizują
niż atomy H i dlatego lepiej stabilizują
karbokation.
karbokation.
δδδδ
+
C
H
H
H
C
H
R
H
δδδδ
+
δδδδ
+
‹#›
RJC
Na przykład ...
Na przykład ...
Ta reakcja przebiega poprzez pośredni karbokation
Ta reakcja przebiega poprzez pośredni karbokation
II
II--rzędowy.
rzędowy.
Br
CH
CH
3
CH = C H
2
CH
3
CH
CH
3
CH C
H
3
CH
3
Br
H
Br
‹#›
RJC
Na przykład ...
Na przykład ...
Ta reakcja przebiega poprzez karbokation
Ta reakcja przebiega poprzez karbokation
III
III--rzędowy.
rzędowy.
Br
C = CHCH
3
CH
3
CH
3
C
C
H
2
CH
3
CH
3
CH
3
Br
H
Br
‹#›
RJC
Elektrofilowa hydratacja ...
Elektrofilowa hydratacja ...
H
H
2
2
SO
SO
4
4
/H
/H
2
2
O
O
Odczynniki elektrofilowe nie są ograniczone do
Odczynniki elektrofilowe nie są ograniczone do
halogenowodorów HX.
halogenowodorów HX.
CH
2
=CH
2
C
H
3
CH
2
C
H
3
CH
2
OH
H
2
SO
4
/H
2
O
H
2
SO
4
/H
2
O
‹#›
RJC
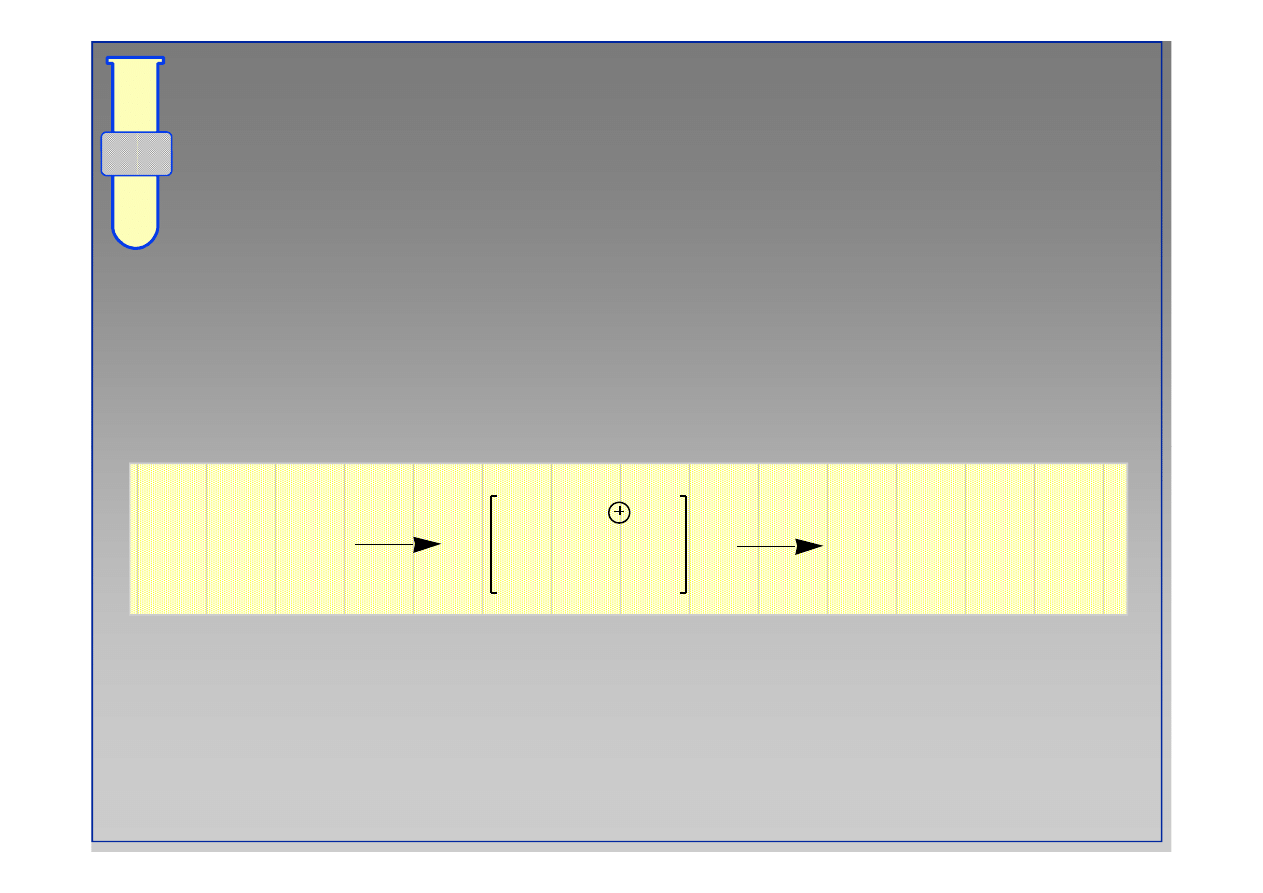
Elektrofil ...
Elektrofil ...
Cl
Cl
2
2
Heterolityczny rozpad cząsteczki Cl
Heterolityczny rozpad cząsteczki Cl
2
2
(ale także
(ale także
innych halogenów) umożliwia tym pierwiastkom
innych halogenów) umożliwia tym pierwiastkom
wchodzenie w reakcję zarówno w roli elektrofila jak
wchodzenie w reakcję zarówno w roli elektrofila jak
neutralizującego karbokation nukleofila.
neutralizującego karbokation nukleofila.
CH
2
=CH
2
Cl
CH
2
CH
2
Cl
CH
2
CH
2
Cl
Cl
2
‹#›
RJC
Elektrofil...
Elektrofil...
Br
Br
2
2
Heterolityczny rozpad cząsteczki Br
Heterolityczny rozpad cząsteczki Br
2
2
(ale także
(ale także
innych halogenów) umożliwia tym pierwiastkom
innych halogenów) umożliwia tym pierwiastkom
wchodzenie w reakcję zarówno w roli elektrofila
wchodzenie w reakcję zarówno w roli elektrofila
jak neutralizującego karbokation nukleofila.
jak neutralizującego karbokation nukleofila.
CH
2
=CH
2
Br
CH
2
CH
2
Br
CH
2
CH
2
Br
Br
2
‹#›
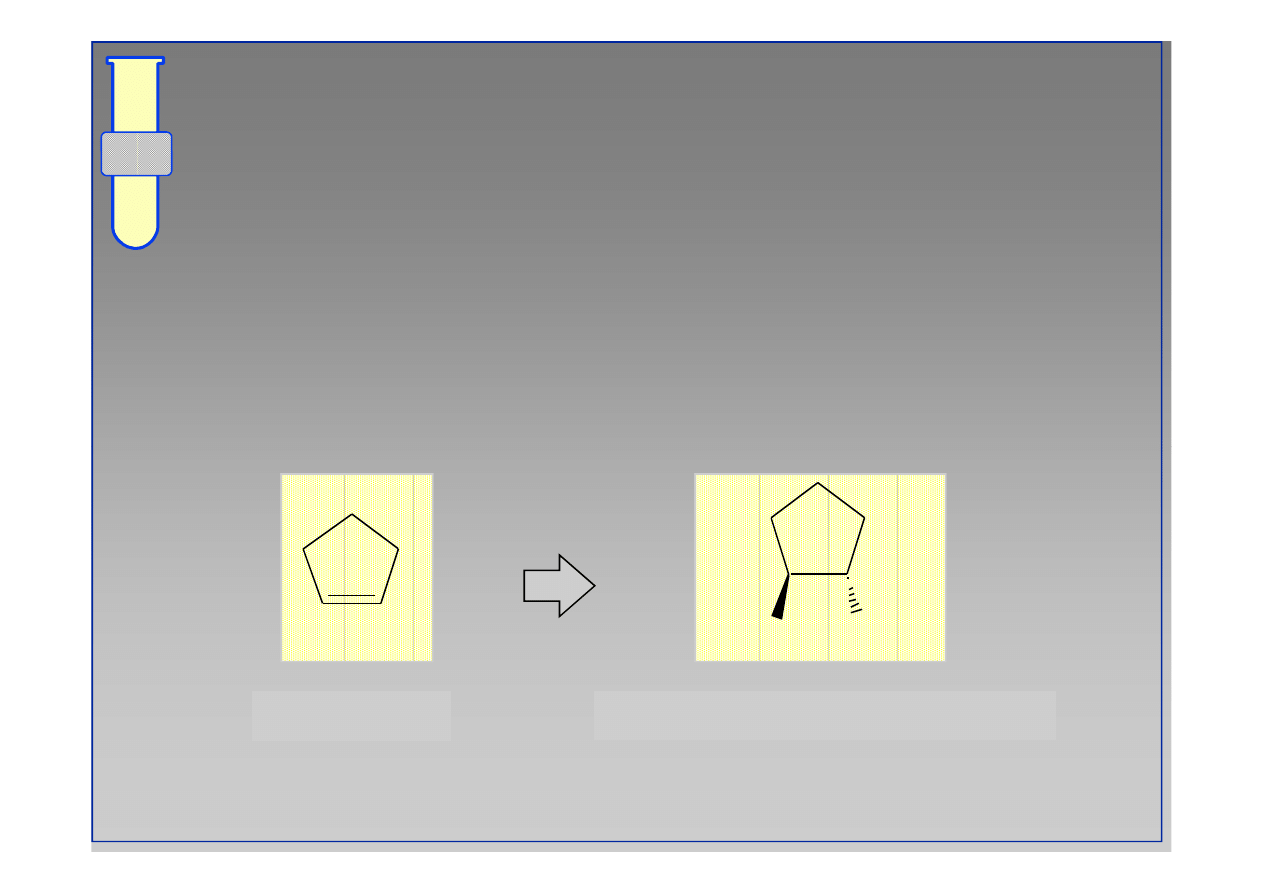
RJC
Cykloalkeny
Cykloalkeny
Addycja Br
Addycja Br
2
2
do cyclopentenu prowadzi do
do cyclopentenu prowadzi do
powstawania
powstawania trans
trans--1,2
1,2--dibromocyclopentanu jako
dibromocyclopentanu jako
jedynego produktu.
jedynego produktu.
Br
2
trans-1,2-dibromocyklopentan
cyklopenten
Br
Br
‹#›
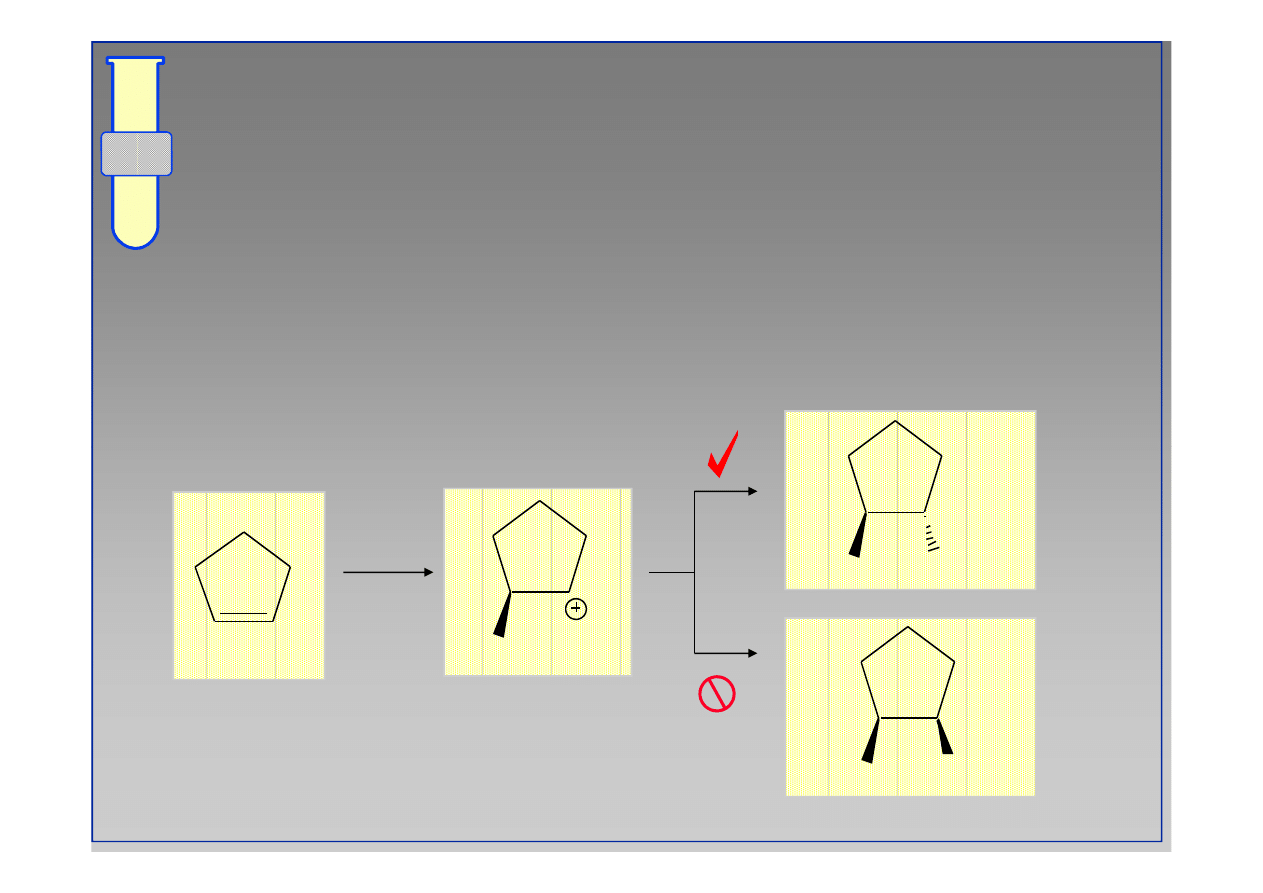
RJC
Możliwy Mechanizm
Możliwy Mechanizm
Jedna strona karbokationu jest bardziej osłonięta,
Jedna strona karbokationu jest bardziej osłonięta,
co wymusza stereoselektywną addycję nukleofila.
co wymusza stereoselektywną addycję nukleofila.
Br
2
Br
Br
Br
Br
Br
‹#›
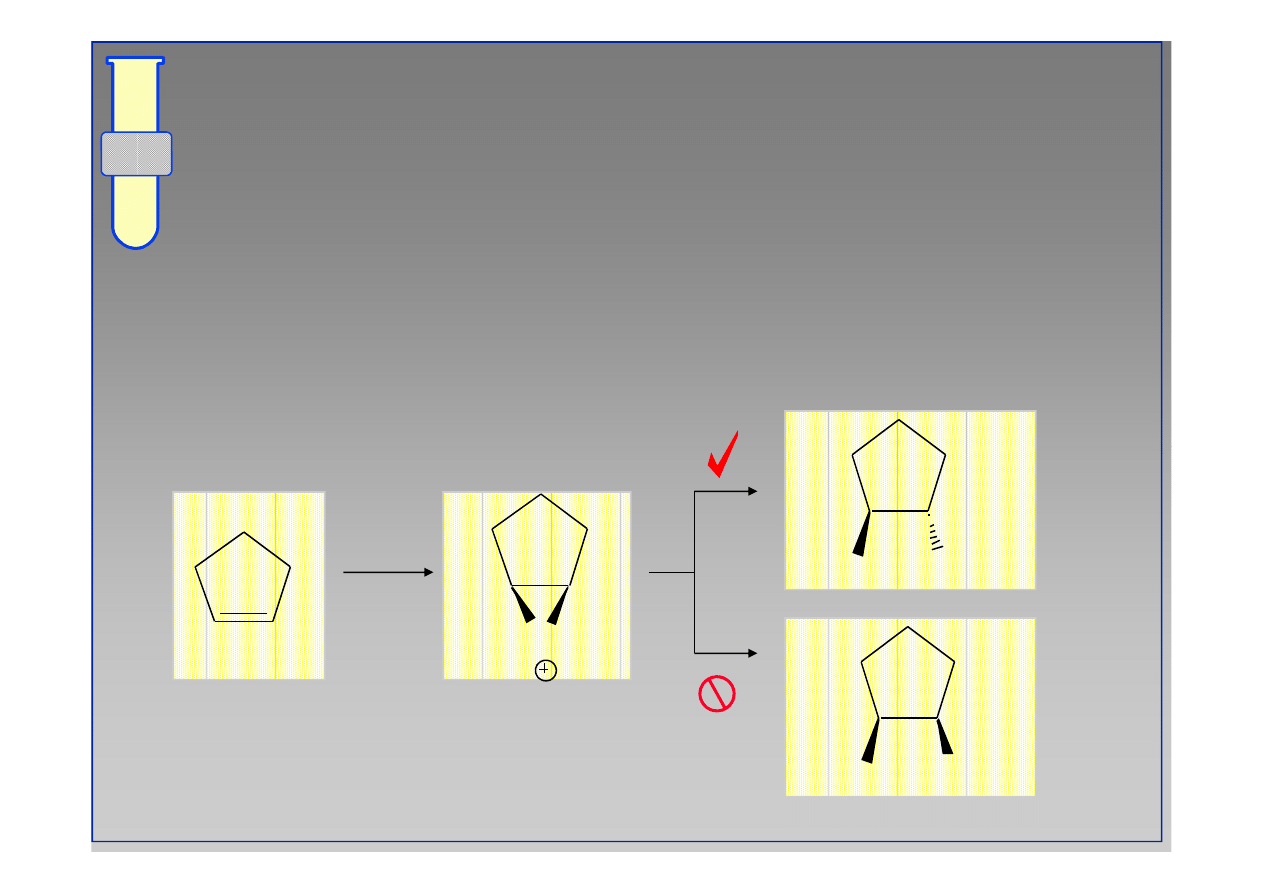
RJC
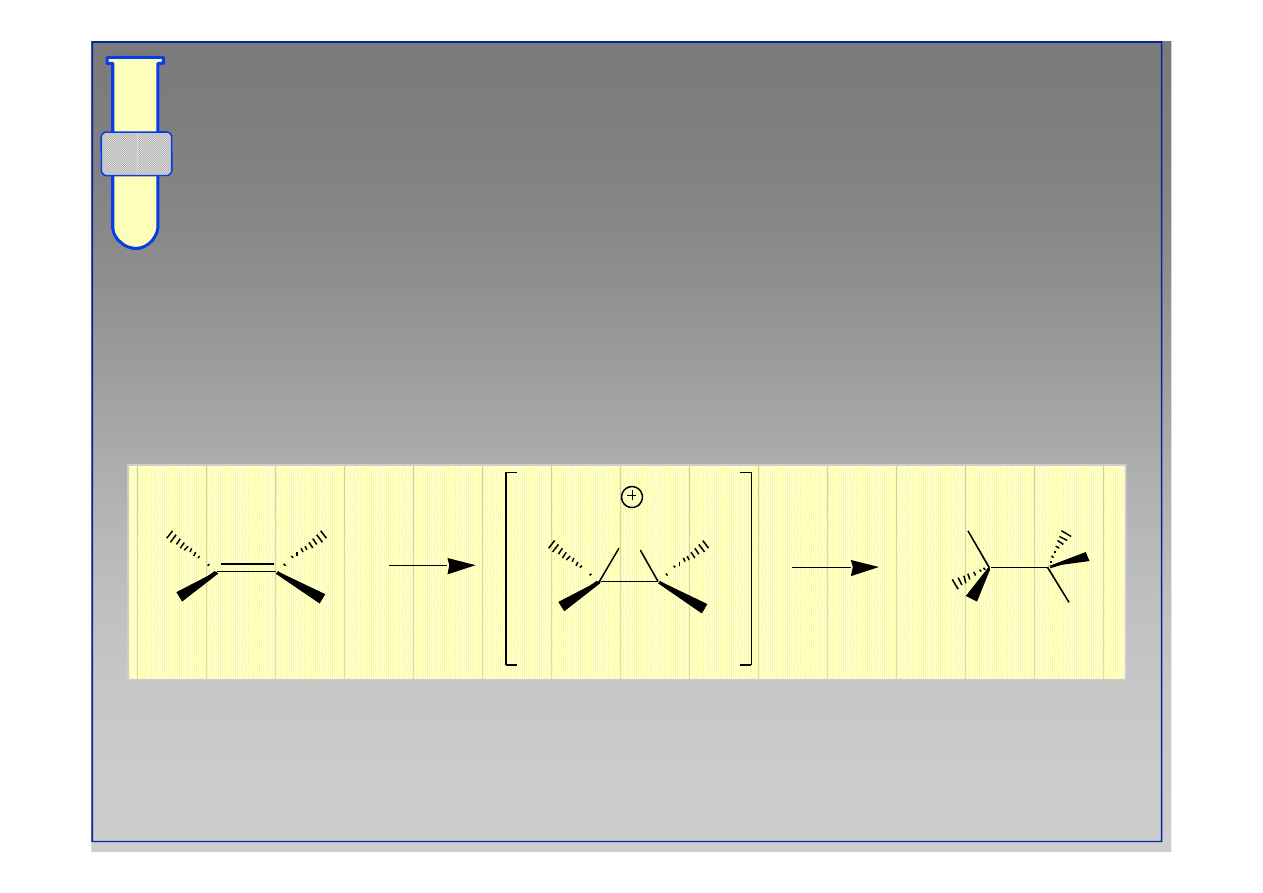
Lepszy, Alternatywny Mechanizm
Lepszy, Alternatywny Mechanizm
W cyklicznym kationie bromoniowym, atom Br
W cyklicznym kationie bromoniowym, atom Br
całkowicie osłania jedną stronę cząsteczki
całkowicie osłania jedną stronę cząsteczki
(związku przejściowego).
(związku przejściowego).
Br
2
Br
Br
Br
Br
Br
‹#›
RJC
Halohydryny
Halohydryny
Neutralizacja pośredniego kationu haloniowego
Neutralizacja pośredniego kationu haloniowego
cząsteczką wody prowadzi do powstania
cząsteczką wody prowadzi do powstania
halohydryny.
halohydryny.
Br
OH
R
R
R
H
R
R
H
R
Br
2
R
R
H
R
Br
H
2
O

‹#›
RJC
Podsumowanie
Podsumowanie
Elektrofilowa addycja do alkenów
Regioselektywność
Reguła Markownikowa
Karbokationy
Karbokationy
Hiperkoniugacja
Efekt indukcyjny
Cykloalkeny
Halohydryny
Wyszukiwarka
Podobne podstrony:
Sprawozdanie 10, Semestr 1, Elektronika, Sprawozdania i instrukcje, sprawozdanie rejestry scalone
10 ROZTWORY ELEKTROLITW 09
10 Nagrzewanie elektronowe 1
10 PRZEWODNICTWO ELEKTRYCZNE TKANEK
E 10, sgsp, Elektroenergetyka, ELEKTROE
AUT E-ka 10, Inżynieria Elektryczna, Automatyka napędu
[10]opracowanie, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki,
10-oświetlenie elektryczne, Instrukcje BHP, XXXV - INSTR. ENERGETYCZNE
ETP wyklad 10 dalmierze elektromagnetyczne dokladnosc pomiaru dalmierzami wplyw warunkow meteorologi
10 opracowanie, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki,
10 W EM, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki, Laborki
10 BARCHNICKI, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki, L
[10]konspekt, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki, la
Wykład 10 Pierwiastki -d i -f elektronowe CHC13005w, chemia, chemia ogólna ; nieorganiczna ; metale
10-LAB, Elektrotechnika AGH, Semestr II letni 2012-2013, Fizyka II - Laboratorium, laborki, laborki
10 Prom elektromagn
Addycje elektrofilowe
mechanizm reakcji addycji elektrofilowej ppt
więcej podobnych podstron