
Farmakologia – nauka o działaniu
leków na zdrowe i chore organizmy
Farmakokine
Farmakokine
tyka
tyka
Matematyczna ocena ilościowa procesów kinetycznych,
Matematyczna ocena ilościowa procesów kinetycznych,
jakim lek podlega w organizmie
jakim lek podlega w organizmie
Farmakodyna
Farmakodyna
mika
mika
Badanie wpływu leku na organizm i poszczególne narządy
Badanie wpływu leku na organizm i poszczególne narządy
oraz mechanizm jego działania
oraz mechanizm jego działania

• Zjawisko eksplozji leków (nowe leki moczopędne,
sulfonamidy, hipotensyjne, leki psychotropowe,
cytostatyczne, adrenergiczne)
• Zjawisko patologii polekowych – katastrofa z
talidomidem, leki adrenergiczne w areozolu, brak
badań klinicznych leków
• Farmakologia kliniczna – 1969 rok WHO – nowa
gałąź medycyny
Farmakologia kliniczna – nowa dziedzina
Farmakologia kliniczna – nowa dziedzina
medycyny
medycyny
Farmakologia kliniczna – nowa dziedzina
Farmakologia kliniczna – nowa dziedzina
medycyny
medycyny

•
5 -20% hospitalizacji rocznie - pacjenci z
powikłaniami polekowymi
•
Niepożądane działania leków i szkodliwych
interakcji występują średnio u 27%
hospitalizowanych osób
•
Zejście śmiertelne spowodowane niewłaściwym
stosowaniem leków – 1/200 chorych
•
Wysokość kosztów leczenia skutków niepożądanego
działania leków – 3mln dolarów rocznie (USA)
Skutki patologii polekowych

Farmakologia kliniczna
Farmakologia kliniczna
Dyscyplina
Dyscyplina
obejmująca wszystko co wiąże się z działaniem
obejmująca wszystko co wiąże się z działaniem
leku u ludzi,
leku u ludzi,
tj. kontrolę skuteczności, mechanizm działania, działania
tj. kontrolę skuteczności, mechanizm działania, działania
niepożądane i toksyczne
niepożądane i toksyczne
1. Prace badawcze
1. Prace badawcze
2. Nauczanie
2. Nauczanie
3. Działanie orzecznicze i konsultacyjne
3. Działanie orzecznicze i konsultacyjne
4. Planowanie i koordynacja badań
4. Planowanie i koordynacja badań
5. Informacja o leku
5. Informacja o leku
Zadania farmakologii
Zadania farmakologii
klinicznej
klinicznej

• Badania farmakokinetyczne procesów składających się
na losy leków w organizmie ludzkim
• Poznanie mechanizmu działania leków u człowieka,
zależności : dawka-siła i czas działania leku
• Określenie szkodliwych, niepożądanych działań
substancji leczniczej, zapobieganie
• Badania kliniczne leków
• Poznanie czynników zmieniających losy leków w
organizmie – proces chorobowy, genotyp, wiek, czynniki
środowiskowe, interakcje.
Farmakologia kliniczna – praca badawcza
Farmakologia kliniczna – praca badawcza

•
Poprawienie opieki nad pacjentem przez
Poprawienie opieki nad pacjentem przez
zalecanie stosowania bezpiecznych i
zalecanie stosowania bezpiecznych i
skutecznych leków –
skutecznych leków –
indywidualizacja
indywidualizacja
farmakoterapii (uwzględnienie odmienności
farmakoterapii (uwzględnienie odmienności
osobniczych)
osobniczych)
•
Zwiększenie wiedzy o lekach
Zwiększenie wiedzy o lekach
•
Świadczenie usług – farmakokinetyka,
Świadczenie usług – farmakokinetyka,
farmakodynamika, informacja o leku,
farmakodynamika, informacja o leku,
rejestracja działań niepożądanych
rejestracja działań niepożądanych
Farmakologia kliniczna
Farmakologia kliniczna

Dziedziny Farmakologii Klinicznej
Dziedziny Farmakologii Klinicznej
•
Farmakogenetyka
Farmakogenetyka
•
Chronofarmakologia (biorytmy w
Chronofarmakologia (biorytmy w
działaniu leków)
działaniu leków)
•
Poszukiwanie i badanie nowych leków
Poszukiwanie i badanie nowych leków
•
Farmakoekonomika
Farmakoekonomika
•
Farmakologia społeczna
Farmakologia społeczna

Farmakogenetyka
Badanie wpływu czynników
Badanie wpływu czynników
dziedzicznych
dziedzicznych
na działanie leków w organizmie.
na działanie leków w organizmie.
(Vogel 1957, Meyer 2001)
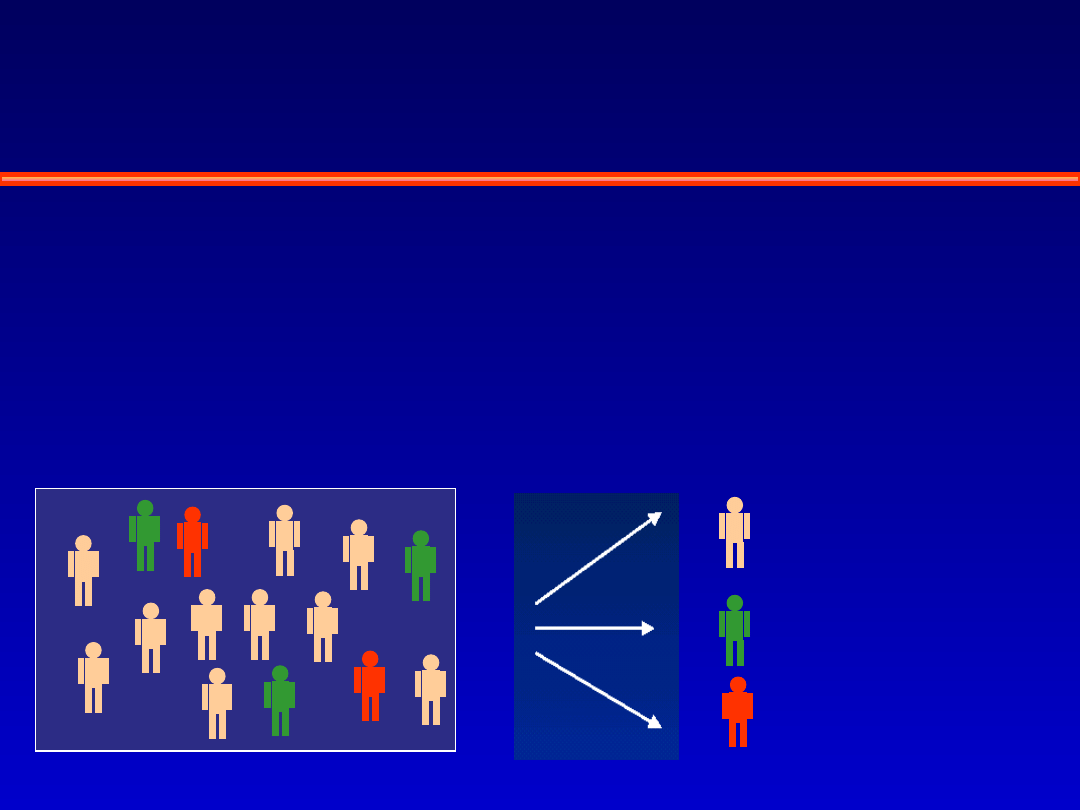
Odmienne reakcje chorych na leki
Odmienne reakcje chorych na leki
•
Reakcja na sukcynylocholinę
Reakcja na sukcynylocholinę
(pseudocholinoesteraza)
(pseudocholinoesteraza)
•
Odmienne działanie izoniazydu
Odmienne działanie izoniazydu
DOBRA
DOBRA
ODPOWIEDŹ
ODPOWIEDŹ
BRAK
BRAK
ODPOWIEDZI
ODPOWIEDZI
TOKSYCZNOŚĆ
TOKSYCZNOŚĆ

Chronofarmakologia – (biorytmy
w działaniu leków)
Rytmy dobowe – największe znaczenie u ludzi
Wykazano to w odniesieniu do:
• Temperatura ciała
• Częstość skurczów serca
• Ciśnienie tętnicze krwi
• Czynność płuc i nerek
• Stężenie neuroprzekaźników, hormonów, enzymów, elektrolitów,
glukozy
• Zmiany chorobowe
(np. zawał serca 8-12 godz. rano)

Działanie leków a rytm
dobowy
•
Leki znieczulające miejscowo i przeciwbólowe: rano
lub w nocy – słabsze działanie, dłuższe działanie
wczesnym popołudniem (wydzielanie endogennych
endorfin)
•
Glikokortykosteroidy – zmniejszenie działań
niepożądanych dostosowując ich podawanie do rytmu
dnia (kortyzol) – stężenia maks. rano 6-9godz. (rano i w
południe)
•
Leki przeciwastmatyczne – napady dychawicy
oskrzelowej w nocy - wieczorem większe dawki
•
Leki przeciwhistaminowe (anty-H2) – podawać tylko
jeden raz wieczorem (choroba wrzodowa)

Racjonalizacja
farmakoterapii
• Indywidualizacja terapii
– terapia
kontrolowana pomiarem stężenia leku we
krwi
• Oznaczanie genotypu / fenotypu pacjenta
• Przeciwdziałanie objawom niepożądanym
Fazy badania leku
Fazy badania leku
Badania przedkliniczne – skrining farmakologiczny,
Badania przedkliniczne – skrining farmakologiczny,
badania u zwierząt
badania u zwierząt
Badania kliniczne –
Badania kliniczne –
u ludzi
u ludzi
Faza 1 – ogólna ocena działania leku u
Faza 1 – ogólna ocena działania leku u
zdrowych ochotników
zdrowych ochotników
Faza 2 – ogólna ocena działania leku
Faza 2 – ogólna ocena działania leku
u
u
chorych
chorych
Faza 3 – badania porównawcze
Faza 3 – badania porównawcze
Faza 4 – badania po wprowadzeniu leku do
Faza 4 – badania po wprowadzeniu leku do
sprzedaży
sprzedaży

Badania przedkliniczne
Badania przedkliniczne
Badania wstępne i szczegółowe
Badania wstępne i szczegółowe
podanie jednorazowe i wielokrotne,
podanie jednorazowe i wielokrotne,
dawka,
dawka,
toksyczność, mechanizm działania,
toksyczność, mechanizm działania,
farmakokinetyka, czas trwania od 1-5 lat
farmakokinetyka, czas trwania od 1-5 lat
(średnio 2,6 lat)
(średnio 2,6 lat)

Toksyczność ostra
Toksyczność ostra
LD50, maksymalna dawka. Zazwyczaj co
LD50, maksymalna dawka. Zazwyczaj co
najmniej 2 gatunki,
najmniej 2 gatunki,
dwie drogi podania, pojedyncza dawka leku.
dwie drogi podania, pojedyncza dawka leku.
Toksyczność podostra
Toksyczność podostra
Zazwyczaj trzy dawki leku, 2 gatunki. Czas
Zazwyczaj trzy dawki leku, 2 gatunki. Czas
trwania do 6 miesięcy (zwykle przed
trwania do 6 miesięcy (zwykle przed
rozpoczęciem badań klinicznych). Czas badania
rozpoczęciem badań klinicznych). Czas badania
zależy od przewidywanego czasu klinicznego
zależy od przewidywanego czasu klinicznego
podawania leku.
podawania leku.
Toksyczność przewlekła
Toksyczność przewlekła
1 do 2 lat. Wymagana, gdy przewiduje się
1 do 2 lat. Wymagana, gdy przewiduje się
długotrwałe
długotrwałe
stosowanie leków. Zazwyczaj prowadzone
stosowanie leków. Zazwyczaj prowadzone
równolegle do badań klinicznych.
równolegle do badań klinicznych.
Wpływ na płodność, działanie teratogenne
Wpływ na płodność, działanie teratogenne
Działanie rakotwórcze
Działanie rakotwórcze
Dwa lata, dwa gatunki. Wymagane, gdy
Dwa lata, dwa gatunki. Wymagane, gdy
przewiduje się długotrwałe stosowanie leków.
przewiduje się długotrwałe stosowanie leków.
Działanie mutagenne
Działanie mutagenne
Wpływ na stabilność genetyczną: test
Wpływ na stabilność genetyczną: test
Amesa lub hodowle
Amesa lub hodowle
komórkowe
komórkowe
Badania przedkliniczne
Badania przedkliniczne
Wpływ na układ immunologiczny i ośrodkowy układ nerwowy
Wpływ na układ immunologiczny i ośrodkowy układ nerwowy

Badania kliniczne – etyczne aspekty badań
klinicznych nowych leków
Główny cel -właściwa ocena stosunku
ryzyka do korzyści
Deklaracje międzynarodowe
Kodeks Norymberski – 1947r.
Deklaracja Helsińska I – 1964r.
Deklaracja Helsińska II (z Tokio) – 1975r.
Wytyczne Rady Międzynarodowych
Organizacji Medycznych 1981r. (WHO do
spraw Badań Klinicznych)

Badania kliniczne
Powołanie Komisji Bioetycznych
– ocena etyczna
badań
nowych
leków u ludzi
Polska –
Centralna Komisja Nadzoru nad
Dokonywaniem Badań na
Ludziach
(Komisja Etyki badań Naukowych)
Komisje terenowe - Komisja Bioetyczna

Badania kliniczne
1992r. - Zasady prawidłowego prowadzenia badań
klinicznych
produktów medycznych w krajach Wspólnoty
Europejskiej
(„Good Clinical Practice for Trials on Medicinal Products
in the European
Community”- GCP)
zasady GCP w Polsce – I - IV fazy badań klinicznych
produktów medycznych, badania biodostępności,
biorównoważności leków
2003r. – Rozporządzenie Ministra Zdrowia w Sprawie
Określenia Szczegółowych Wymagań Dobrej Praktyki
Klinicznej

Badania kliniczne
Faza I – wstępne badania kliniczne – ustalenie reakcji całego
organizmu na lek, działania niepożądane
•Określenie tolerancji osoby badanej na stopniowo zwiększane pojedyncze
lub wielokrotne dawki dobowe nowej substancji
•Badanie dostępności biologicznej i właściwości farmakokinetycznych
•Obserwacja działań niepożądanych
• 10-15 zdrowych osób, wiek 21-55 lat
Badania lekarskie oraz rutynowe badania laboratoryjne
(przed i po zakończeniu badania)
Wymagana świadoma zgoda badanego i Komisji Bioetycznej

Faza II
–
wstępne kontrolowane badania kliniczne
Randomizowanie
pacjenci dobierani po względem wieku, płci,
stadium zaawansowania choroby
•Ustalenie skutecznych dawek leczniczych, wskazań,
rejestracja działań niepożądanych, wstępne badania
farmakokinetyczne 3 ośrodki (10-30 osób)
(łącznie 100-150 pacjentów)
•Badania z grupą kontrolną – placebo lub lek standardowy
•Badania równoległe, cross-over
•Badania podwójnie ślepe, potrójnie ślepe
•Wymagana świadoma zgoda badanego i Komisji Bioetycznej
Badania kliniczne

Faza III – rozszerzone kontrolowane badania kliniczne
•Określenie związku pomiędzy bezpieczeństwem a skutecznością
podczas krótkotrwałego i przewlekłego stosowania preparatu
•Porównanie działania badanego leku z działaniem terapeutycznym
leku zarejestrowanego lub placebo
•Wiele ośrodków (do 2000 pacjentów)
•Ocena jakości życia pacjentów
•Statystyczna ocena leku
•Wymagana świadoma zgoda badanego i Komisji Bioetycznej
Badania kliniczne

Faza IV – przedłużone badania kliniczne (po rejestracji leku)
•Powtórna ocena wskazań do stosowania leku (również nowych wskazań)
•Ocena przedawkowania i innych działań niepożądanych, postępowanie
•Interakcje leków
•Ocena leku u ludzi w wieku podeszłym, dzieci, kobiet w ciąży,
w chorych z niewydolnością nerek lub wątroby
Badania kliniczne
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
Wyszukiwarka
Podobne podstrony:
Lekarski farmakologia kliniczna,definicja1
Lekarski farmakologia kliniczna,definicja1
Lekarski farmakologia kliniczna,definicja1
osteoporoza, medycyna zabrze SUM lekarski, FARMAKOLOGIA - PRZYDATNE MATERIAŁY, FARMAKOLOGIA KLINICZ
Leczenie ostrej niewydolności nerek, medycyna zabrze SUM lekarski, FARMAKOLOGIA - PRZYDATNE MATERIA
FARMAKOLOGIA KLINICZNA WYDZIAŁ LEKARSKI Katowice, MEDYCYNA - ŚUM Katowice, V ROK, Farmakologia klini
Leczenie wybranych schorzeń przewodu pokarmowego, medycyna zabrze SUM lekarski, FARMAKOLOGIA - PRZY
inne, medycyna zabrze SUM lekarski, FARMAKOLOGIA - PRZYDATNE MATERIAŁY, FARMAKOLOGIA KLINICZNA
pierwotniaki, Lekarski, FARMAKOLOGIA, 1. semestr, 1sem
farma kliniczna- pytania, Medycyna, Pobr materiały, V rok UMB-2015-09-30, V rok UMB, Farmakologia Kl
Seminarium 1 - Farmakoterapia bolu, 5 ROK, FARMAKOLOGIA KLINICZNA
okulistyka, Lekarski, FARMAKOLOGIA, 3. semestr, 3sem
lipidy, Lekarski, FARMAKOLOGIA, 2. semestr, 2sem
wrzody, Lekarski, FARMAKOLOGIA, 1. semestr, 1sem
farma.test 1, 6 rok, Farmakologia kliniczna, giełda
wyniki gr. C, 5 ROK, FARMAKOLOGIA KLINICZNA
farmakologia kliniczna 2010, MEDYCYNA - ŚUM Katowice, V ROK, Farmakologia kliniczna
więcej podobnych podstron