1
RJC
Substytucja nukleofilowa S
Substytucja nukleofilowa S
N
N
2
2
Substytucja nukleofilowa S
Substytucja nukleofilowa S
N
N
2
2
Slides 1 to 28
Y
R
1
R
2
R
3
Nu
Y
R
1
R
2
R
3
Nu
Y
R
1
R
2
R
3
Nu
2
RJC
Substytucja nukleofilowa
Substytucja nukleofilowa
Nukleofil (Nu) zastępuje grupę
Nukleofil (Nu) zastępuje grupę
opuszczającą (Y) w cząsteczce
opuszczającą (Y) w cząsteczce
substratu.
substratu.
Nu
+
CH
3
Y
Nu
CH
3
+
Y
3
RJC
S
S
N
N
1 versus S
1 versus S
N
N
2
2
Istnieją dwa mechanizmy służące
Istnieją dwa mechanizmy służące
wyjaśnieniu przebiegu tych dwóch
wyjaśnieniu przebiegu tych dwóch
różnych reakcji;
różnych reakcji;
S
N
1
S
N
1
S
N
2
S
N
2
SUBSTYTUCJA
NUKLEOFILO
WA
1
go
rzędu
Nucleophilic
Substitution
2
go
rzędu
4
RJC
substrat
Zależy tylko od stężenia substratu,
Zależy tylko od stężenia substratu,
ponieważ określa on stan przejściowy
ponieważ określa on stan przejściowy
określający szybkość reakcj.
określający szybkość reakcj.
Nu
+
CH
3
Y
Nu
CH
3
+
Y
S
S
N
N
1 : Szbkość reakcji
1 : Szbkość reakcji
5
RJC
Substrat &
nukleofil
S
S
N
N
2 : Szybkość reakcji
2 : Szybkość reakcji
Zarówno nukleofil jak i substrat
Zarówno nukleofil jak i substrat
[Nu]
[Nu]
&
&
[substrate]
[substrate]
są włączone w stan
są włączone w stan
przejściowy, który określa szybkość
przejściowy, który określa szybkość
rakcji.
rakcji.
Nu
+
CH
3
Y
Nu
CH
3
+
Y
6
RJC
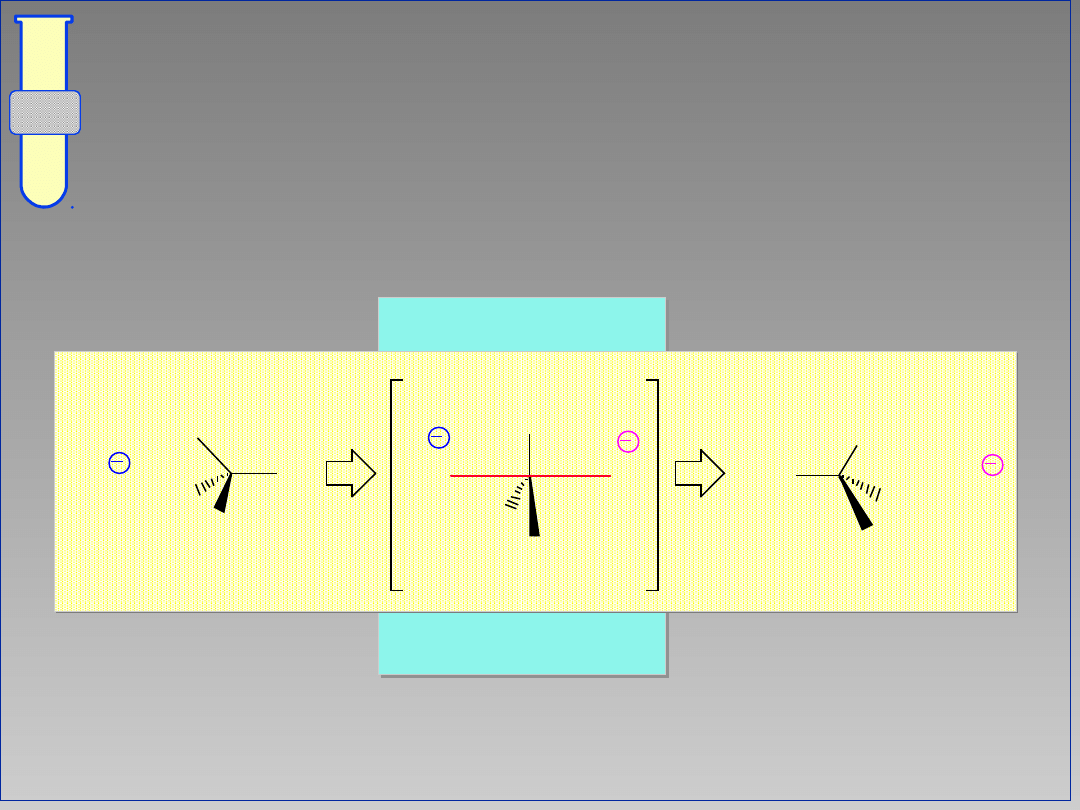
Mechanizm S
Mechanizm S
N
N
2
2
Reakcja przebiega w jednym etapie.
Reakcja przebiega w jednym etapie.
Nu + CH
3
Y
Nu
....
CH
3
....
Y
NuCH
3
+ Y
Energia
Przebieg reakcji
7
RJC
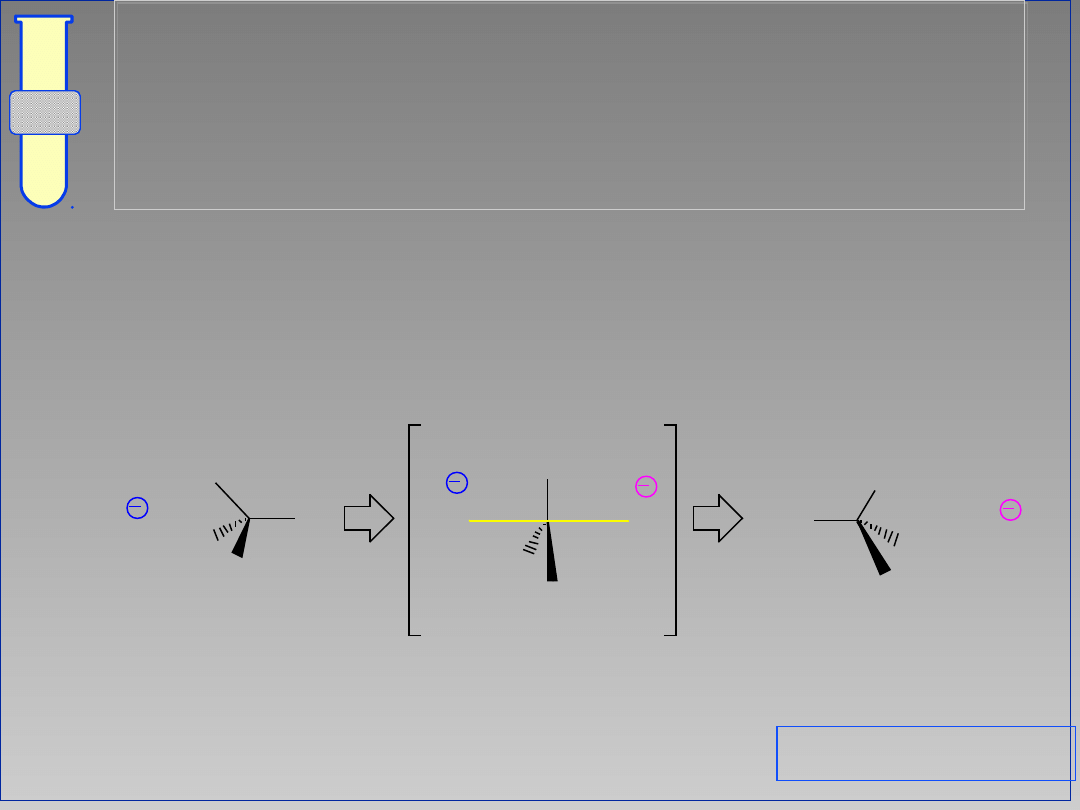
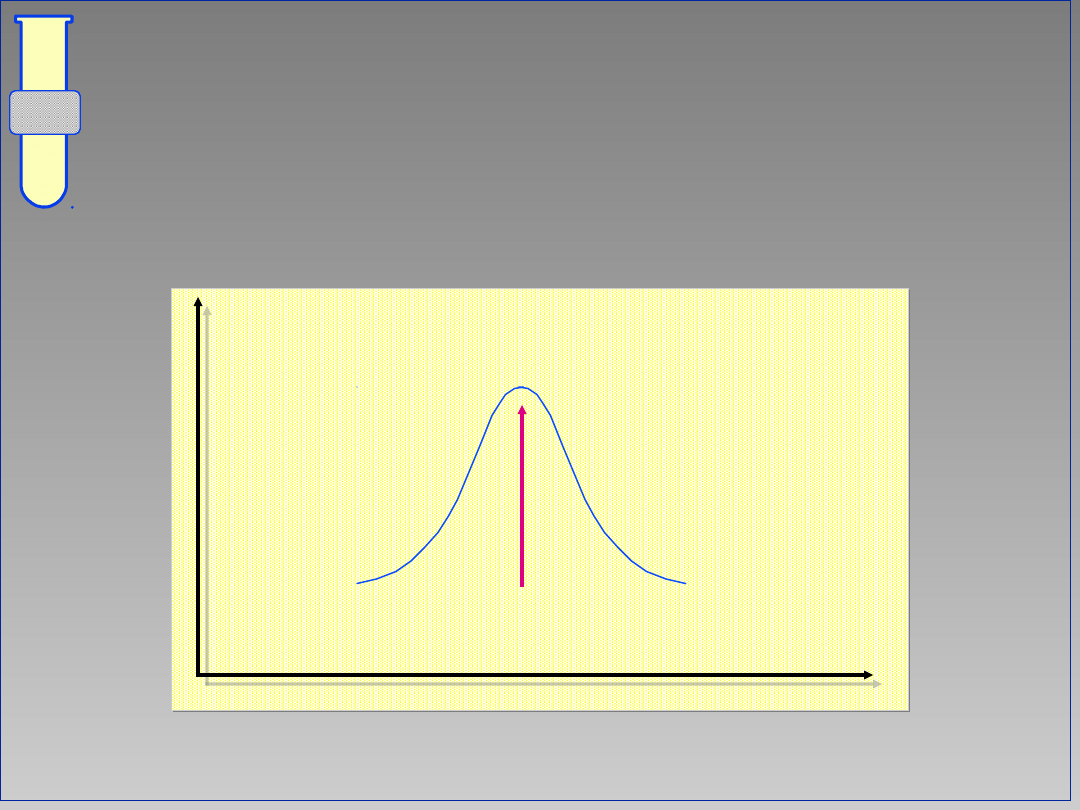
inwersja
inwersja
S
S
N
N
2 : Mechanizm &
2 : Mechanizm &
Stereochemia
Stereochemia
Y
R
1
R
2
R
3
Nu
Y
R
1
R
2
R
3
Nu
Y
R
1
R
2
R
3
Nu
8
RJC
S
S
N
N
2 : Profil energetyczny reakcji
2 : Profil energetyczny reakcji
Szybkość reakcji jest określona przez
Szybkość reakcji jest określona przez
G
G
‡
‡
Nu + CH
3
Y
Nu
....
CH
3
....
Y
NuCH
3
+ Y
Energia
Postęp reakcji
G
‡
9
RJC
Czynniki określające
Czynniki określające
G
G
‡
‡
Substrat
Nukleofil
Grupa opuszczająca
Rozpuszczalnik
10
RJC
Struktura substratu
Struktura substratu
Sterycznie zatłoczony substrat jest
Sterycznie zatłoczony substrat jest
mniej podatny na atak nukleofila.
mniej podatny na atak nukleofila.
Zmniejszająca się reaktywność S
N
2
Zmniejszająca się reaktywność S
N
2
CH
3
Br
CH
3
CH
2
Br
(CH
3
)
2
CH
Br
(CH
3
)
3
CCH
2
Br
(CH
3
)
3
C
Br
11
RJC
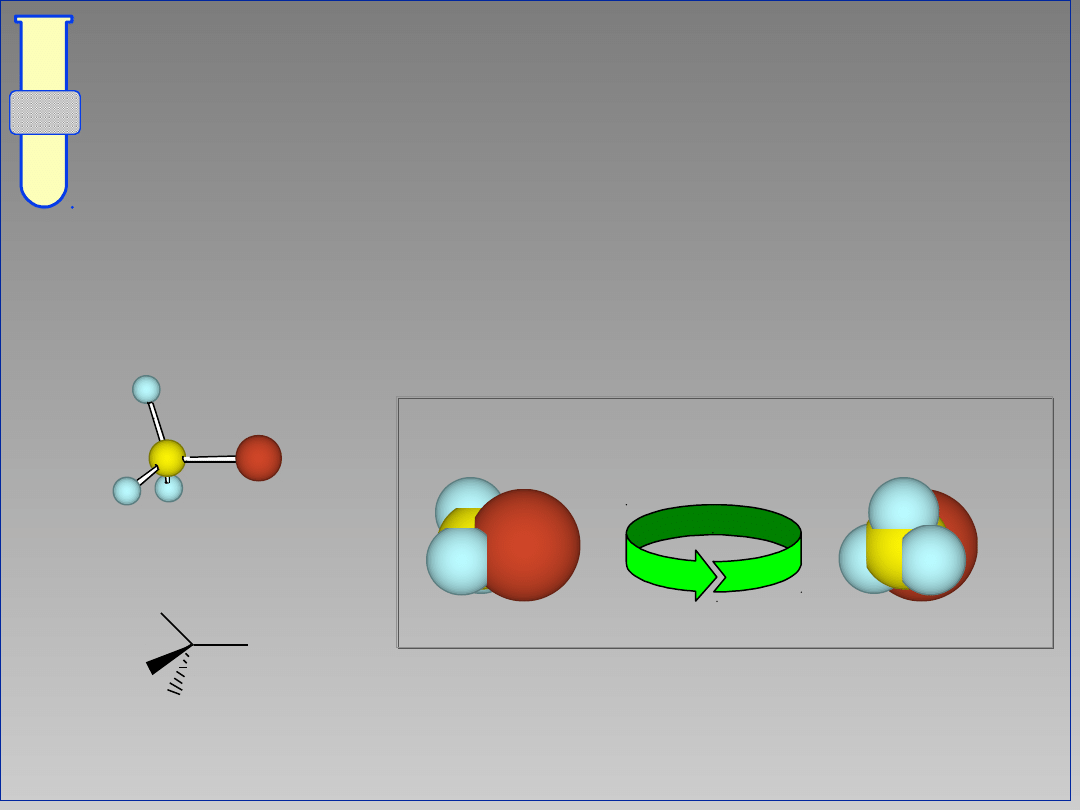
Na przykład ... bromometan
Na przykład ... bromometan
Reakcja S
Reakcja S
N
N
2 zachodzi bardzo szybko.
2 zachodzi bardzo szybko.
90°
Br
H
H
H
12
RJC
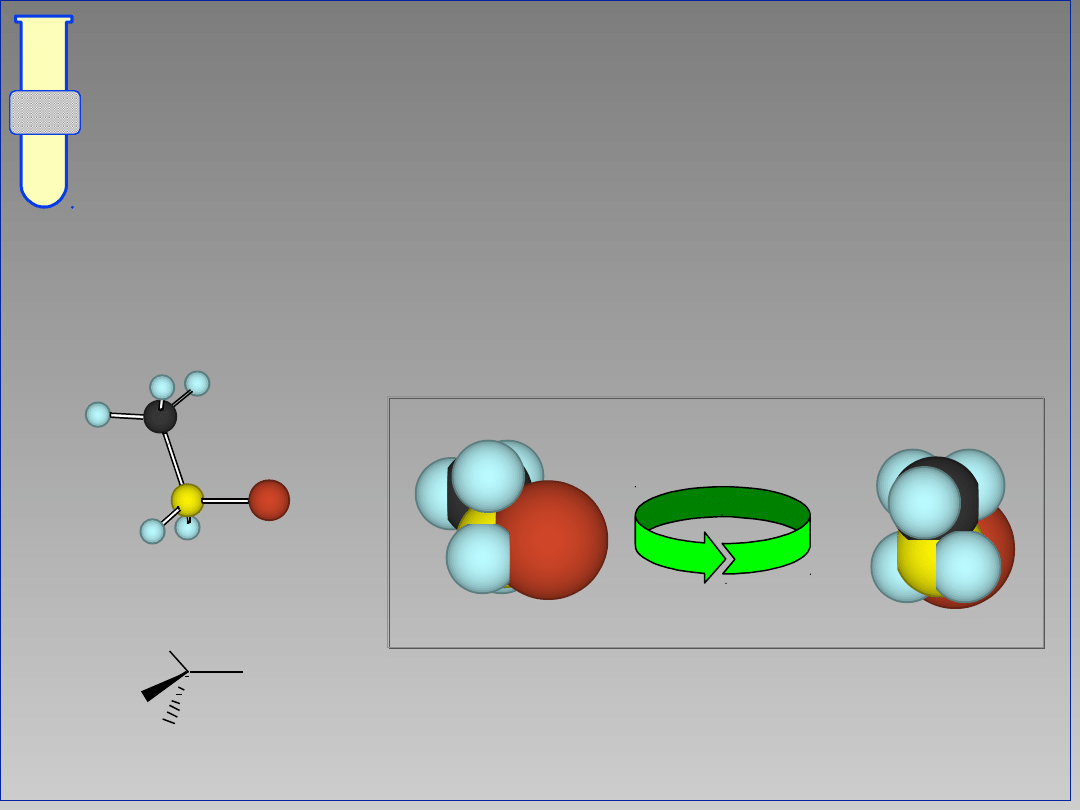
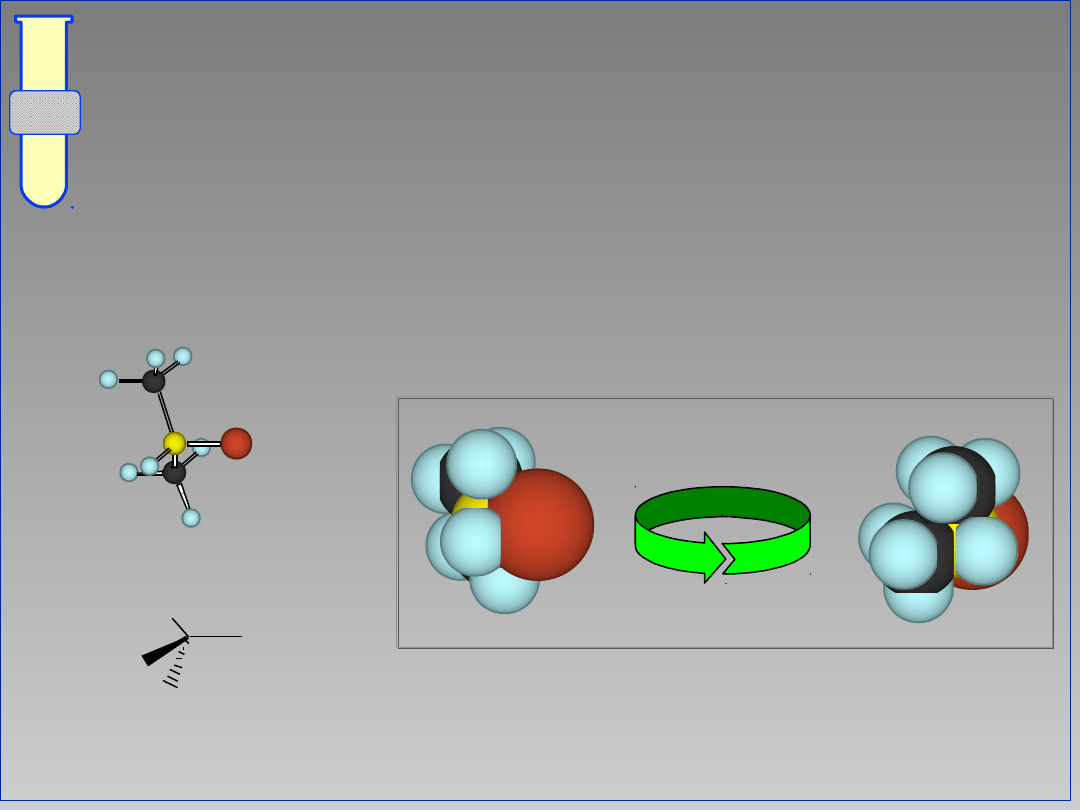
Na przykład ... bromoetan
Na przykład ... bromoetan
Reakcja S
Reakcja S
N
N
2 zachodzi szybko.
2 zachodzi szybko.
90°
Br
CH
3
H
H
13
RJC
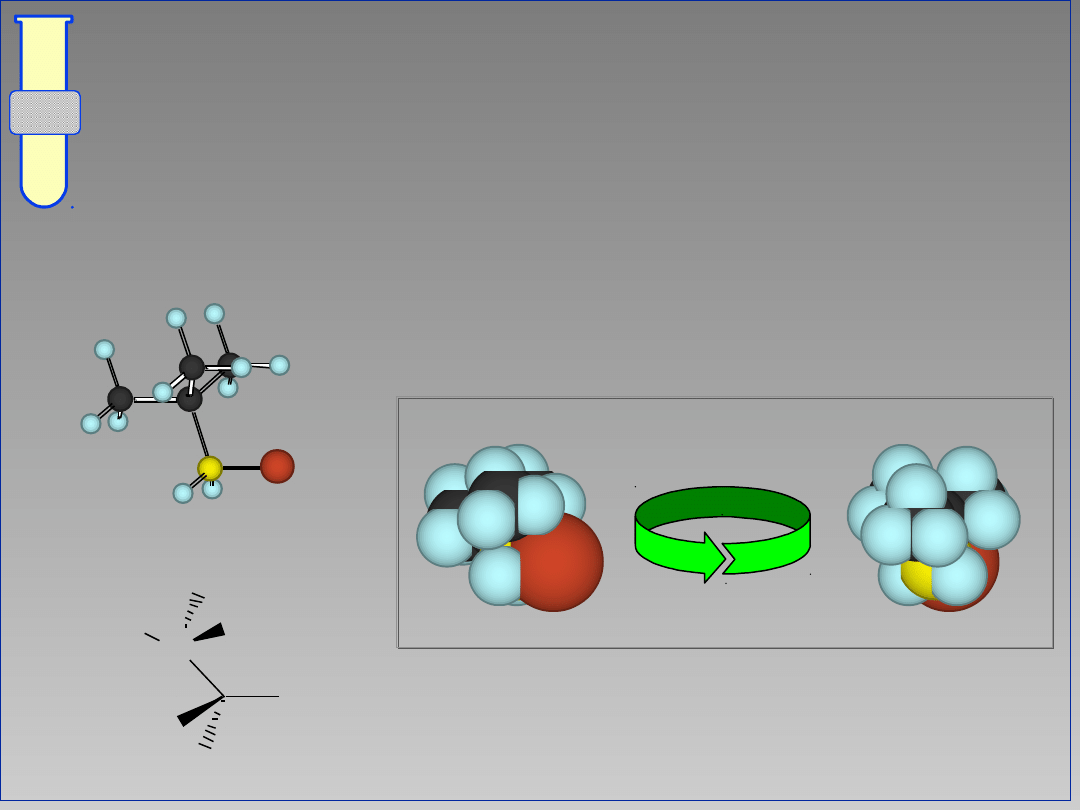
Na przykład ... 2-bromopropan
Na przykład ... 2-bromopropan
Reakcja S
Reakcja S
N
N
2 zachodzi.
2 zachodzi.
90°
Br
CH
3
H
CH
3
14
RJC
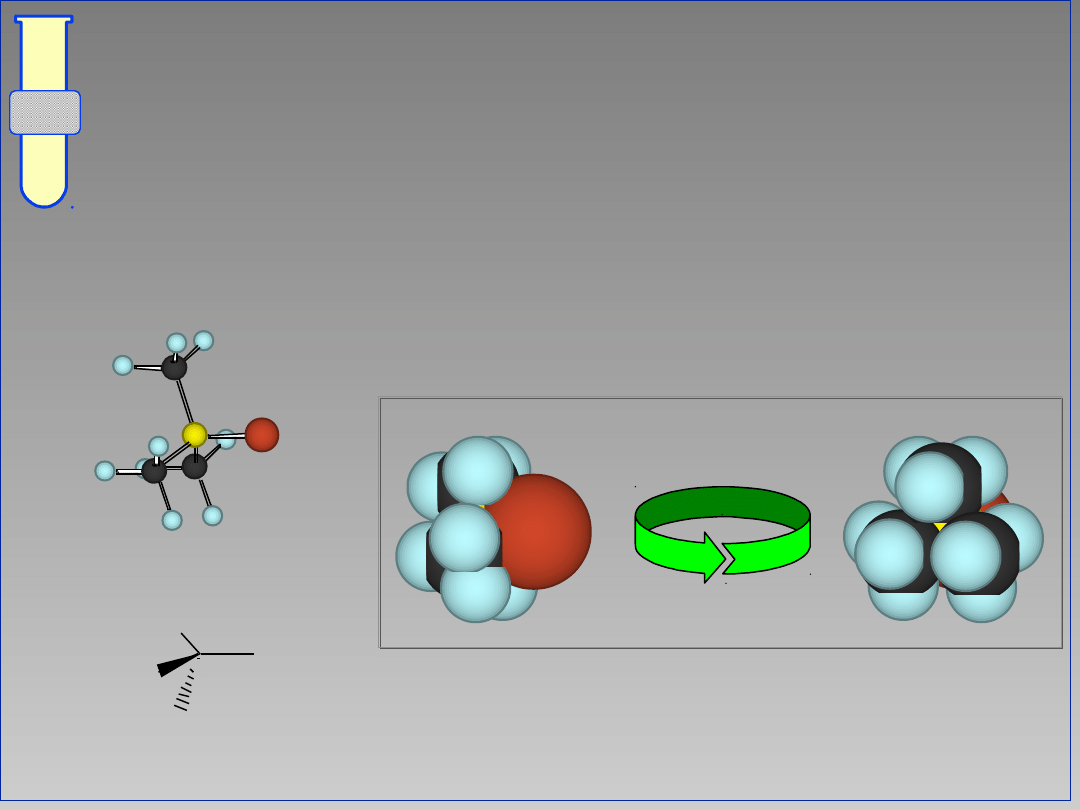
Na przykład ...2,2-dimethyl-1-
Na przykład ...2,2-dimethyl-1-
bromopropane
bromopropane
Reakcja S
Reakcja S
N
N
2 zachodzi bardzo wolno.
2 zachodzi bardzo wolno.
90°
Br
C
H
H
CH
3
CH
3
CH
3
15
RJC
Na przykład ... 2-bromo-2-
Na przykład ... 2-bromo-2-
metylopropan
metylopropan
Reakcja S
Reakcja S
N
N
2 wcale nie zachodzi.
2 wcale nie zachodzi.
90°
Br
CH
3
CH
3
CH
3
16
RJC
Względne szybkości reakcji
Względne szybkości reakcji
bromometan
3,000,000
bromoetan
100,000
2-bromopropan
25,000
2,2-dimetylo-1-bromopropan
1
2-bromo-2-metylpropan
0
17
RJC
Nukleofil
Nukleofil
Istnieją nukleofile o zróżnicowanej
Istnieją nukleofile o zróżnicowanej
aktywności.
aktywności.
I
-
HO
-
NH
3
anion
jodkowy
anion
jodkowy
anion
hydroksylo
wy
anion
hydroksylo
wy
amoniak
amoniak
Malejąca nukleofilowość
Malejąca nukleofilowość
18
RJC
I
-
HO
-
NH
3
anion
jodkowy
anion
jodkowy
anion
hydroksylowy
anion
hydroksylowy
amoniak
amoniak
Malejąca zasadowość
Malejąca zasadowość
Nukleofilowość
Nukleofilowość
W przybliżeniu, szereg nukleofilowości
W przybliżeniu, szereg nukleofilowości
pokrywa się z szeregiem zasadowości.
pokrywa się z szeregiem zasadowości.
••
••
••
••
•
•
•
•
••
••
••
••
••
••
•
•
•
•
•
•
•
•
19
RJC
Popularne nukleofile
Popularne nukleofile
HS
-
125
HO
-
16
CN
-
125
Cl
-
1.0
I
-
100
NH
3
0.7
CH
3
O
-
25
H
2
O
0.001
Wz. reaktyw.
Nu
Nu
Wz. reak.
20
RJC
Grupa opuszczająca
Grupa opuszczająca
Grupa Y jest dobrą grupą odchodzącą,
Grupa Y jest dobrą grupą odchodzącą,
jeżeli jednocześnie jest słąbym
jeżeli jednocześnie jest słąbym
nukleofilem (słąbą zasadą ?).
nukleofilem (słąbą zasadą ?).
Nu
+ CH
3
Y
Nu
CH
3
+
Y
21
RJC
Najważniejsze grupy odchodzące
Najważniejsze grupy odchodzące
TsO
-
60
F
-
0.001
I
-
30
HO
-
0
Br
-
10
H
2
N
-
0
Cl
-
0.2
RO
-
0
Wz. Reak.
Y
Y
Wz. Reak.
22
RJC
Anion tosylanowy jest dobrą grupą
Anion tosylanowy jest dobrą grupą
odchodzącą
odchodzącą
Stabilizacja rezonansowa poprawia
Stabilizacja rezonansowa poprawia
zdolność grupy odchodzącej.
zdolność grupy odchodzącej.
Nu
-
+ R
OTs
Nu
R +
TsO
-

23
RJC
Wpływ rozpuszczalnika
Wpływ rozpuszczalnika
Nukleofile są to cząsteczki
Nukleofile są to cząsteczki
‘wzbogacone’ w elektrony i dlatego
‘wzbogacone’ w elektrony i dlatego
polarne rozpuszczalniki są potrzebne
polarne rozpuszczalniki są potrzebne
jako właściwe środowisko dla reakcji
jako właściwe środowisko dla reakcji
S
S
N
N
2.
2.
“...Podobne rozpuszcza
podobne...”
“...Podobne rozpuszcza
podobne...”
“Polarne rozpuszczają polarne ...”
“Polarne rozpuszczają polarne ...”
“Nie-polarne rozpuszczają nie-
polarne...”
“Nie-polarne rozpuszczają nie-
polarne...”
24
RJC
Solwatacja
Solwatacja
Rozpuszczalniki hydroksylowe solwatują
Rozpuszczalniki hydroksylowe solwatują
cząsteczkę nukleofila (Nu) i dlatego
cząsteczkę nukleofila (Nu) i dlatego
zmniejszają jej reaktywność.
zmniejszają jej reaktywność.
Nu
-
••
•
•
•
••
••
•
•
• •• •
25
RJC
Najlepszymi rozpuszczalnikami dla
Najlepszymi rozpuszczalnikami dla
reakcji S
reakcji S
N
N
2 są polarne rozpuszczalniki
2 są polarne rozpuszczalniki
aprotyczne;
aprotyczne;
Acetonitryl .... CH
3
CN
DMSO .......... (CH
3
)
2
SO
HMPA ....... [(CH
3
)
2
N]
3
PO
Polarne rozpuszczalniki
Polarne rozpuszczalniki
aprotyczne
aprotyczne

26
RJC
Na przykład ...
Na przykład ...
W HMPTA (czas reakcji 1 hr)
W HMPTA (czas reakcji 1 hr)
W CH
W CH
3
3
OH (czas reakcji 22.8 lat!)
OH (czas reakcji 22.8 lat!)
Na
N
3
+ CH
3
CH
3
CH
3
CH
2
Br
Na
Br
+ CH
3
CH
3
CH
3
CH
2
N
3

27
RJC
Podsumowanie
Podsumowanie
Substytucja nukleofilowa S
N
2
Inwersja konfiguracji
Diagram energetyczny reakcji S
N
2
Nukleofile, grupa opuszczająca,
zawada steryczna
Nukleofil i nukleofilowość
Anion tosylanowy
Rozpuszczalnik i solwatacja
Polarne rozpuszczalniki
aprotyczne
Substytucja nukleofilowa S
N
2
Inwersja konfiguracji
Diagram energetyczny reakcji S
N
2
Nukleofile, grupa opuszczająca,
zawada steryczna
Nukleofil i nukleofilowość
Anion tosylanowy
Rozpuszczalnik i solwatacja
Polarne rozpuszczalniki
aprotyczne
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
Wyszukiwarka
Podobne podstrony:
Substytucja Nukleofilowa SN (1)
3 Halogenoalkany Substytucja nukleofilowa
Substytucje Nukleofilowe w Pochodnych Karbonylowych
Zadania z reakcji substytucji nukleofilowej i eliminacji w halogenkach alkilowych
Halogenki alkilowe – substytucja nukleofilowa – grupa opuszczająca – kwasy i zasady
substytucja nukleofilowa, ochrona środowiska UJ, IV semestr, chemia ograniczna, sprawozdania
Halogenoalkany Substytucja nukleofilowa2
Substytucje Nukleofilowe w Pochodnych Karbonylowych
Mię¶niaki macicy w ci±ży[2]
aldehydy i ketony addycja nukleofilowa
cykliczne nukleotydy
Koniec z kacem stworzono substytut alkoholu
Nukleotydy
Kosmos ?śń Andersena
Kogel SN P 90 1 110
Kulas S Koncepcja zakresu wyposazania sieci rozdzielczych SN w reklozery
Gibbs Siła sugestii [SN]
de Waal I natura, i kultura [SN]
WYROK SN Z DNIA 2 PAŹDZIERNIKA 2006 R., Studia, Ochrona własności intelektualnej
więcej podobnych podstron