
1
T E R P E N O I D Y
A. Kołodziejczyk
(
izoprenoidy
)
Gdańsk 2012
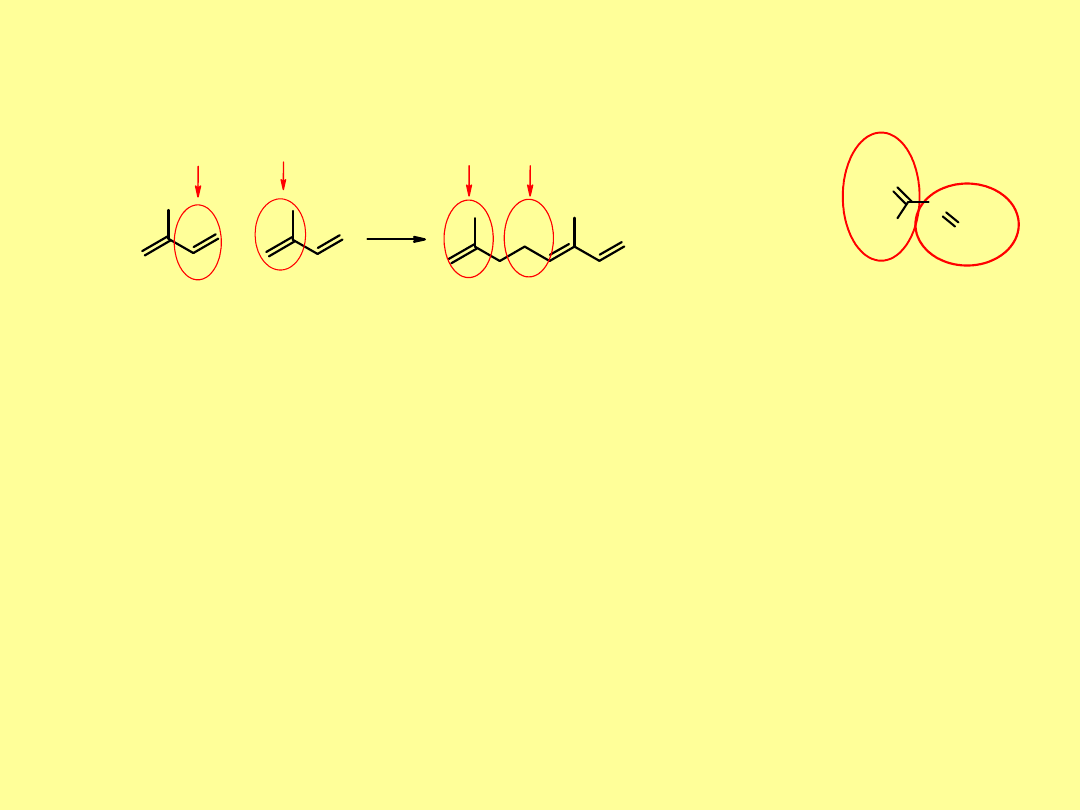
2
Terpenami
nazywane są naturalne węglowodory, pochodzenia
głównie roślinnego, o ogólnym wzorze (C
5
H
8
)
n
. Formalnie są one
oligomerami
izoprenu
, w których reszty izoprenowe połączone
są ze sobą w sposób
ogon-głowa
.
+
ogon
głowa
izopren
ogon głowa
ocymen
CH
C
H
2
C
H
3
CH
2
głowaogon
W zależności od stopnia polimeryzacji n w (C
5
H
8
)
n
terpeny dzielą
się na: -
monoterpeny
(terpeny), n = 2;
C
10
H
16
-
seskwiterpeny
, n = 3; C
15
H
24
;
-
diterpeny
, n = 4; C
20
H
32
;
-
sesterterpeny
, n = 5; C
25
H
40
;
-
triterpeny
, n = 6; C
30
H
48
;
-
tetraterpeny
, n = 8; C
40
H
64
;
-
politerpeny
, n > 8;
izopren
Terpeny
zawierające
dodatkowe grupy funkcyjne, np. -OH, -CHO,
=CO, -COOH, -O-O- i inne nazywane są
terpenoidami
.

3
Izoprenoidami
nazywane są oligomery
izoprenu
połączone
inaczej niż
ogon-głowa
(niezgodnie z
regułą Ruzički
), należą do
nich karotenoidy, steroidy, irydoidy czy kauczuk.
Terpenoidy są bardzo rozpowszechnione w przyrodzie. Ich
fragmenty wchodzą w skład tak ważnych, biologicznie czynnych
związków jak tokoferole, ubichinowy, antybiotyki, alkaloidy czy
chlorofile. Do początku XXI w. opisano 40 000 związków
zaliczanych do terpenoidów . Wchodzą w skład
olejków
eterycznych
wydzielanych
do atmosfery. Drzewa i krzewy iglaste wydzielają około miliarda ton
terpenoidów rocznie. Znaczne ilości terpenoidów wytwarzają
organizmy morskie.
Biosynteza terpenów
Biosubstratem terpenów,
podobnie jak
sterydów jest
pirofosforan 3-
izopentylu
.
CH
3
O
O
O
O
CH
2
=CCH
2
CH
2
-O-P-O-P-O
-
-
-
Szkiel
et
izopre
nu
Monoterpeny (C
5
H
8
)
2
są dominująca frakcją naturalnie
emitowanych do atmosfery związków organicznych. Ich głównym
źródłem są drzewa i krzewy iglaste. Wielkość emisji zależy od
temperatury i rodzaju roślin. W lasach iglastych sumaryczne
stężenie wydzielanych pięciu głównych monoterpenoidów:
-
pinenu
,
-pinenu
,
karenów
i
limonenu
waha się w zależności od
pogody i pory roku od 5 do 1500 g/m
3
. Lasy iglaste produkują
rocznie średnio 5 ton lotnych związków/km
2
.

4
W obszarach niezabudowanych terpenoidy stanowią największe
„zanieczyszczenie” powietrza, główne źródło tworzącego się ozonu i
smogu fotochemicznego. Smoky Mauntains – Zadymione Góry w
USA – zawdzięczają swoją nazwę
smogowi
, który tworzy się z
terpenów wydzielanych przez rosnące tam drzewa w
nasłonecznione ciepłe dni. Powstaje on z terpenów, powietrza i
wilgoci pod wpływem światła i podwyższonej termperatury; z daleka
widoczny jest jako zadymienie.
Olejki eteryczne
(OE)
Znanych jest grubo ponad 1000 roślin wydzielających, lotne (tw.
150 ÷ 300
o
), zwykle przyjemnie pachnące kompozycje zapachowe.
Substancje te nazywane olejkami eterycznymi wydzielane są
zwykle przez określone części roślin, takie jak kwiaty, owoce, liście,
łodygi, drewno, korę lub korzenie. Oprócz terpenów i
terpenoidów w ich skład wchodzą także estry (
octan linalilu
),
alkohole (
benzylowy
,
fenyloetylowy
), aldehydy (
cynamowy
,
benzoesowy
), ketony (
iron
), fenole (
tymol
), etery (
anetol
,
eugenol
), węglowodory, a także związki pozbawione zapachu.
Niektóre z nich mają nieprzyjemny zapach, jak np. czosnkowy czy
gorczyczny.
OE swoje nazwy zawdzięczają zwykle roślinie, z której pochodzą, np.
olejki:
anyżowy,
cedrowy,
cynamonowy, cytrynowy,
eukaliptusowy,
goździkowy, jałowcowy,
jaśminowy,
kamforowy, kminkowy,
koprowy,
lawendowy, miętowy,
pomarańczowy,
różany,
rumiankowy, świerkowy,
tymiankowy, waniliowy
i wiele
innych

5
Olejki eteryczne wydobywa się różnymi sposobami, najczęściej
przez destylację z parą wodną, a także poprzez ekstrakcje
rozpuszczalnikami czy tłuszczami, a ostatnio za pomocą ekstrakcji w
stanie nadkrytycznym. Ze 100 kg kwiatu lawendy otrzymuje się do 2
kg olejku lawendowego. Z 1 t płatków różanych wydobywa się 200-
500 g olejku różanego.
Skład olejku
zmienia się w zależności od
pory roku, pory dnia, pogody, stopnia rozwoju (dojrzałości), a także
czasu jaki minął od pozyskania surowca.
Kompozycja zapachowa owocu brzoskwini
Zawartość składników aromatu
owoców brzoskwini [%]
Główne składniki
przed
zerwaniem
5 godz. po
zerwaniu
oktanian etylu
43
11
octan (Z)-heks-3-enylu
10
0
octan etylu
6
0
lakton kwasu-4-hydroksydekanowego
2,5
39
lakton kwasu-4-hydroksynonanowego
0
10
Pomimo tak istotnych różnic nasz nos zawsze identyfikuje te
kompozycje jako aromat owocu brzoskwini. Skład olejku może
zależeć również od części rośliny z jakiej został wyodrębniony, np.
głównym składnikiem olejku z liści
drzewa cynamonowego
jest
eugenol
, podczas gdy w jego korze dominuje
aldehyd
cynamonowy
.
6
Ponad połowa przemysłowo wydobywanych OE jest
wykorzystywana w przemyśle spożywczym, jako dodatki
aromatyzujące i przyprawy. Znaczącym odbiorcą OE jest przemysł
kosmetyczny. Coraz więcej OE stosowana jest w terapii, w tym
aromatoterapii
.
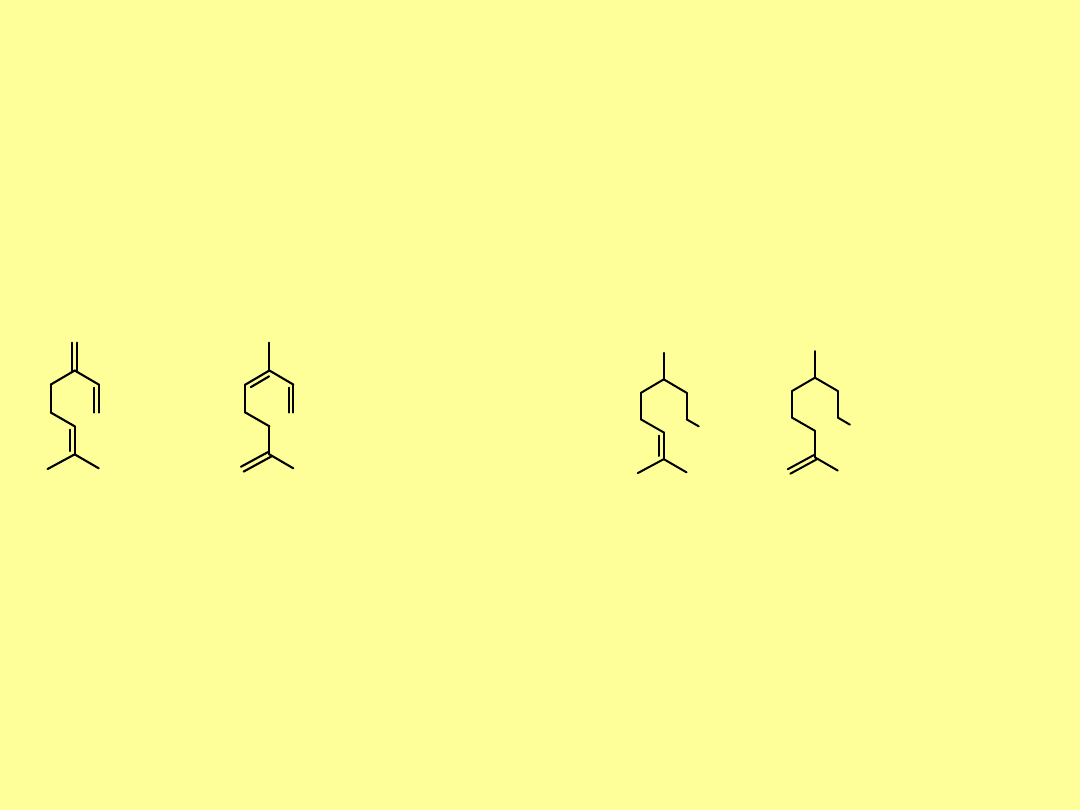
Monoterpeny niecykliczne
Monoterpeny niecykliczne zawierają 3 podwójne wiązania. Ich
przykładem jest, znajdujący się w igłach świerku
mircen
. Jego
izomer –
ocymen
występuje
m.in.w bazylii i w lawendzie. Czerwone glony wytwarzają duże ilości
chloromircenu
.
Monoterpenoidy niecykliczne
Najbardziej znane pośród nich nich to izomery
cytronelolu
,
składniki olejku różanego
i pelargoniowego. Oba izomery mają silny zapach różany. Izomer
(3R)(+) występuje w wydzielinie gruczołów aligatora. Cytronnelole
i ich estry wykorzystywane są w przemyśle kosmetycznym;
zapach
estrów w znacznym stopniu zależy od reszty acylowej.
OH
OH
cytronelol
cytronelol
*
*
ocymen
mircen
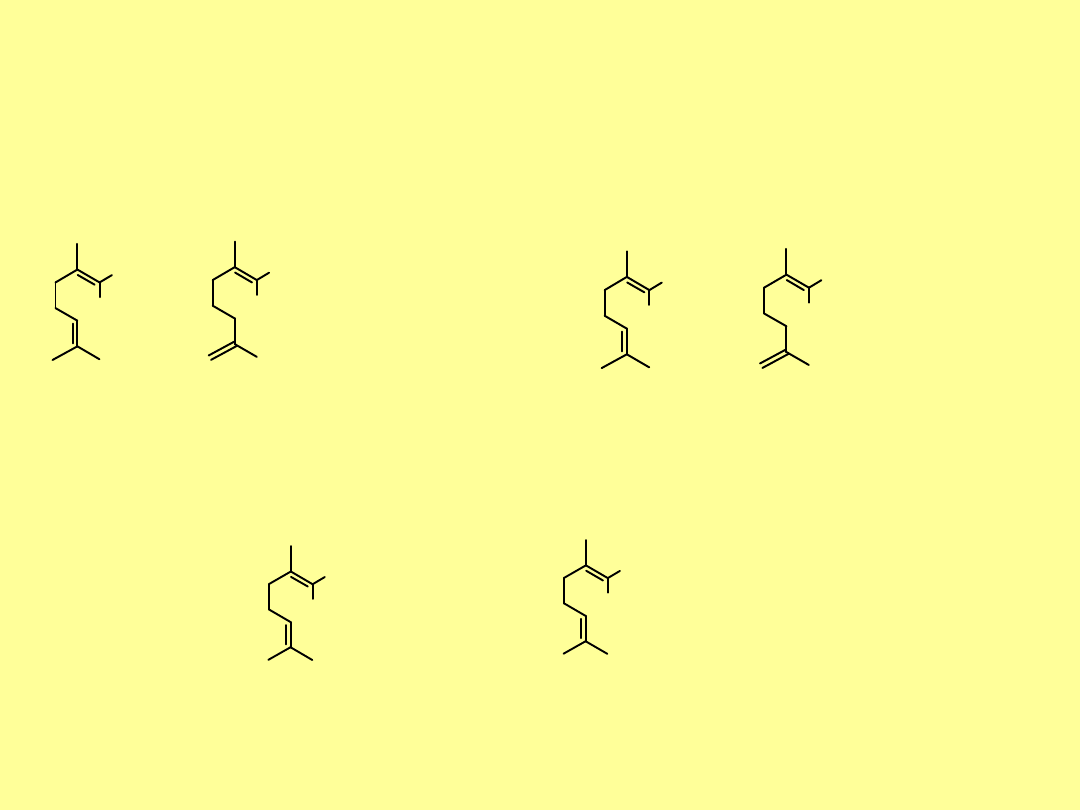
7
Geraniole i nerole, należą do szeroko rozpowszechnionych
terpenoidowych alkoholi. Występują zarówno jako wolne
alkohole, jak i ich estry.
Geraniol
jest głównym składnikiem olejku
różanego, pelargoniowego i cytrynowego. Jest dobrze poznany
ponieważ z CaCl
2
tworzy krystaliczna pochodną. Stereoizomerem
geranilu
jest
nerol
.
Pirofosforan geranylu
pełni kluczową rolę w
biosyntezie steroidów i terpenoidów. Oba te alkohole są
stosowane w przemyśle kosmetycznym i żywnościowym.
H
CH
2
OH
H
CH
2
OH
H
CH
2
OH
CH
2
OH
H
geraniol
nerol
Cytrale, taką nazwą noszą aldehydy powstałe w wyniku utlenienie
nerolu
–
neral
(
cytral b
) lub
geraniolu
–
geranial
(
cytral a
).
Cytrale w postaci mieszany izomerów występuje w wielu OE. W
olejku lemongrasowym stanowią 80% jego składu (40-50%
neralu
i
30-35%
geranialu
). Olejek lemongrasowy służy do perfumowania
mydeł.
neral
(
cytral b
)
geranial
(
cytral a
)
W niektórych olejkach cytrale stanowią ponad 90% ich składu;
znajdują się też
w olejku cytrynowym. Terpenoidy niecykliczne pod wpływem
kwasów łatwo
izomeryzują
do terpenoidów cyklicznych.
H
CHO
H
CHO
8
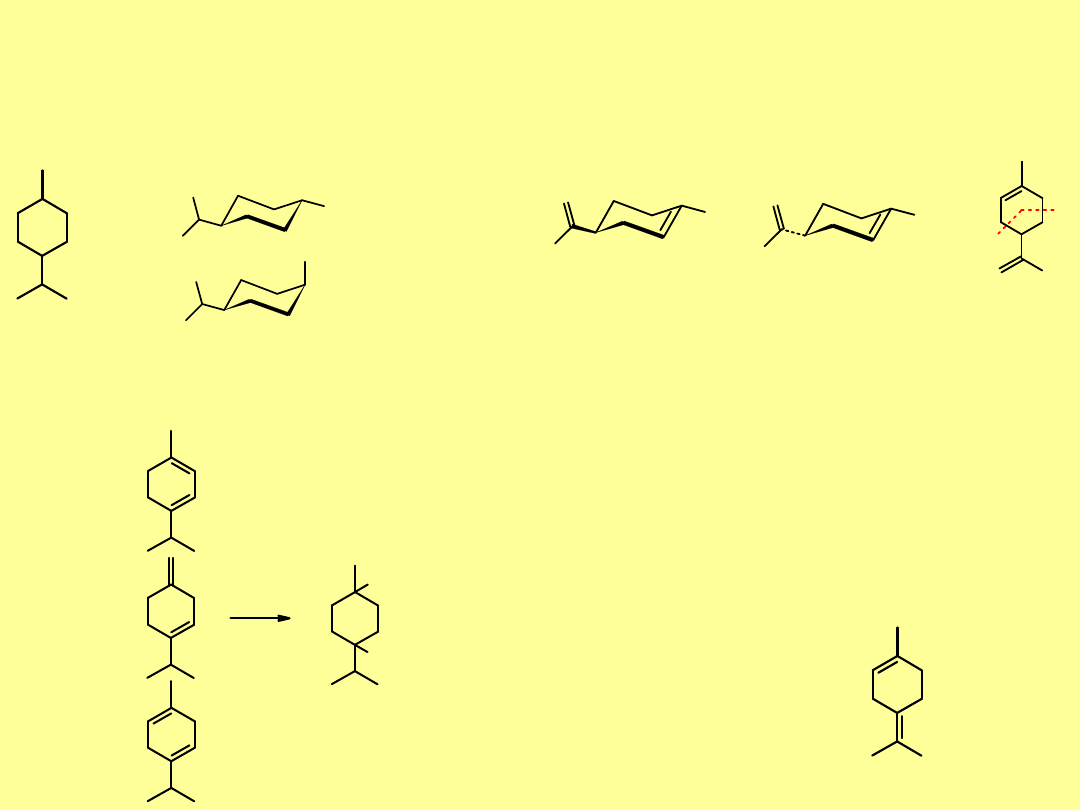
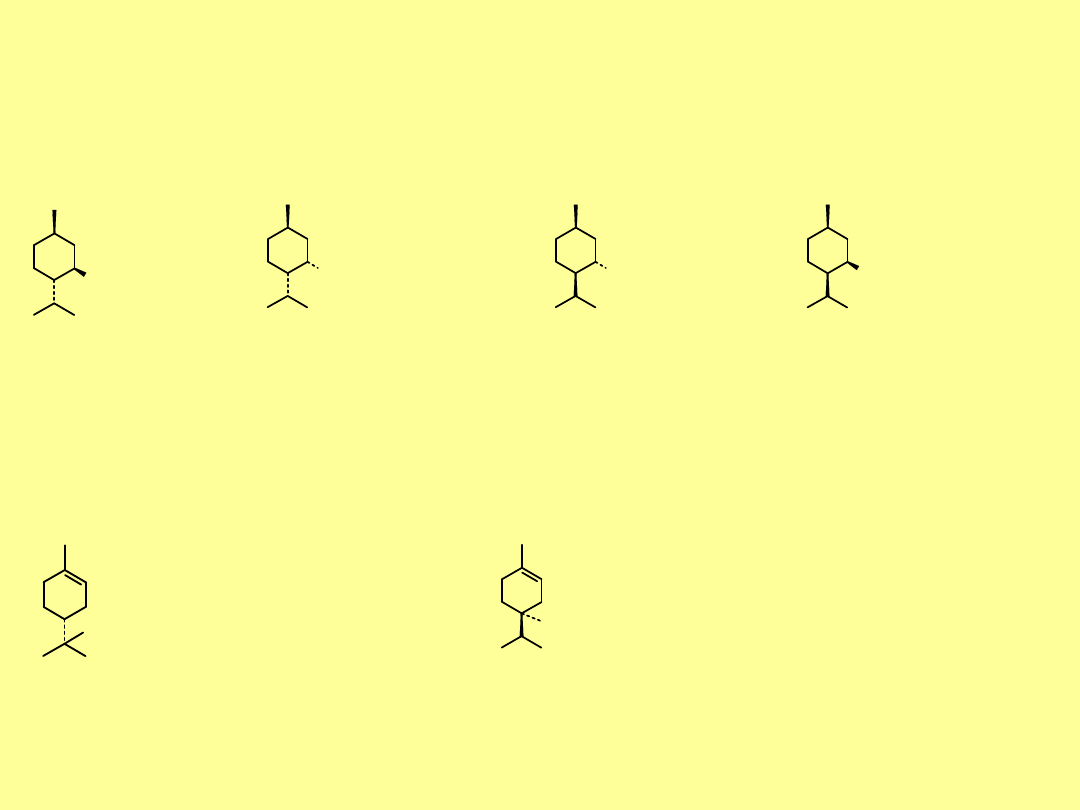
Monoterpeny monocykliczne
Węglowodór macierzysty monoterpenów monocyklicznych –
mentan
(
1-metylo-4-izopropylocykloheksan
) – jest rzadko spotykany w naturze;
występuje
on zarówno w formie trans, jak i cis. Ma zapach kminku.
menta
n
trans-mentan
cis-mentan
Typowym przedstawicielem terpenów monocyklicznych jest
limonen
. Oba jego izomery chiralne występują w naturze.
Limonen
racemiczny
nosi nazwę
dipentenu
. W cząsteczce
limonenu
widoczne są fragmenty
izoprenu
.
(-)-(S)-limonen
(+)-(R)-limonen
Terpineny są achiralnymi izomerami
limonenu
.
Wspólną ich cechą jest to, że w wyniku
przyłączenia do nich 2 moli HCl powstaje
racemiczny
1,4-dichloromentan
.
-terpinen
-terpinen
-terpinen
Cl
Cl
1,4-dichloromentan
Terpineny występują jako mieszanina
izomerów, najczęściej i , np. w
olejku kolendrowym i majerankowym.
Inny izomer położenia
C=C –
terpinolen
jest
składnikiem olejku z
pasternaku.
terpinolen
HCl
9
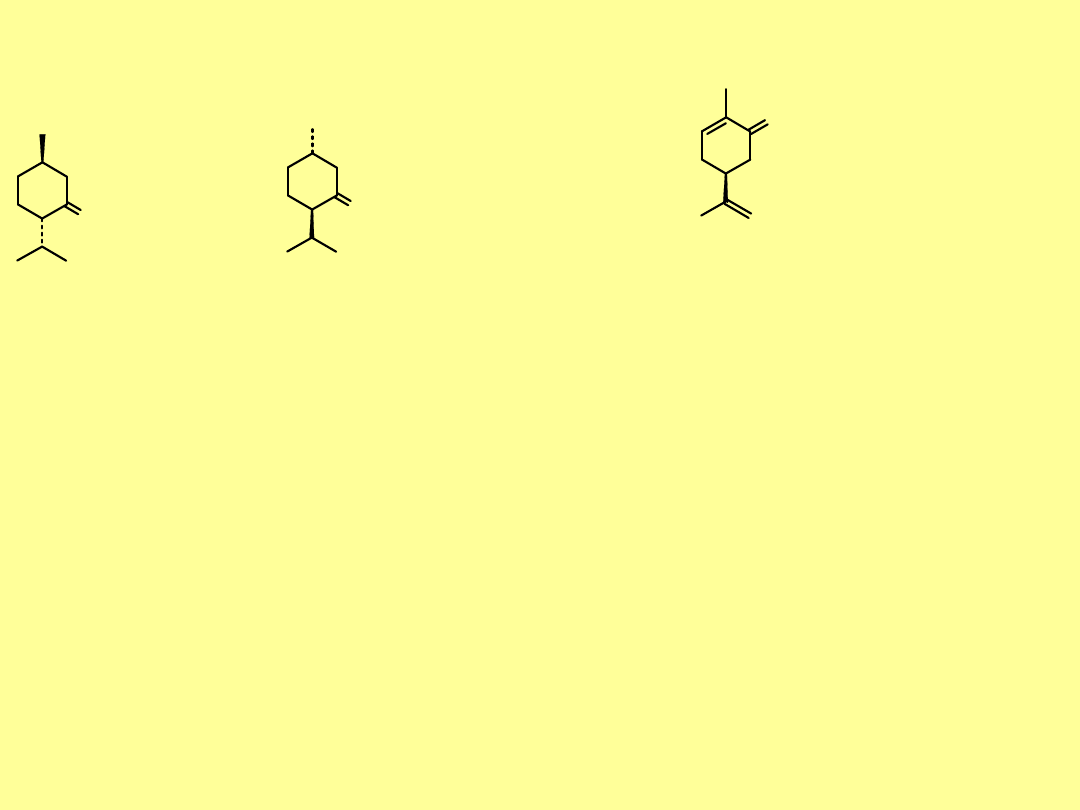
Monoterpenoidy monocykliczne
Najpospolitszym przedstawicielem tej grypy związków jest
mentol
,
(1R,3R,4S)-1-me-tylo-4-izopropylocyklohesan-3-ol
). Mentol jest
nietypowym terpenoidem, ponieważ nie zawiera podwójnego
wiązania. Znane są jego 3 stereoizomery. W olejku mięty polnej
znajduje się 85%
mentolu
i 3%
neomentolu
.
(-)-mentol
OH
S
S
R
(+)-neomentol
OH
S
R
R
(+)-izomentol
OH
R
R
R
(+)-neoizomentol
Mentol
ma właściwości fizjologiczne wykorzystywane w terapii.
Działa np. przeciwwymiotnie, znieczula błonę śluzową żołądka,
ułatwia trawienie, drażni zakończenia nerwów zimna.
OH
1 2
3
4
8
7
R
S
R
Typowymi monocyklicznymi alkoholami terpenowymi są
terpineole, zwane są również
mentenolami
. Formalnie powstają z
terpinenów przez przyłączenie 1 mola wody.
OH
(R)-(-)--terpineol
-Terpineol
występuje w postaci obu stereoizomerów. Największe
znaczenie ma
(R)-(-)--terpineol
z uwagi na przyjemny zapach bzu; jest głównym
składnikiem olejku sosnowego.
Terpinen-4-ol
występuje w olejkach
majerankowym, cyprysowym
i muszkatołowym.
OH
terpinen-4-ol

10
Aromatyczne analogi alkoholi terpenowych
Tymol
i inne cymenole różniące się położeniem grupy
hydroksylowej można uważać za odwodornione mentole.
Tymol
występuje w tymianku. Z uwagi na większą hydrofobowość jego
aktywność przeciwbakteryjna jest 25 silniejsza niż
fenolu
.
OH
tymol
(
p-cymen-3-
ol
)
OH
karwakrol
(
p-
cymen-2-ol
)
Eugenol
(
allilogwajakol
lub
eter metylowy 4-allilopirokatechiny
),
aromatyczny składnik olejku goździkowego, należy do tej samej
grupy związków.
CH
2
CH=CH
2
OH
OMe
eugen
ol
Anetol
,
eter metylowy p-allilofenolu
, aromatyczny analog
terpenoidów występuje
w wielu olejkach eterycznych; Znajduje się w olejku anyżowy i
koprowym. Jest toksyczny, ale mniej niż
tymol
. Stanowi główny
składnik atraktantu owada – szkodnika uszkadzającego korzenie
kukurydzy. Olejek anyżowy, naturalny, a także syntetyczny
anetol
stosowane są do wyrobu nalewek (anyżówka), aromatów,
kosmetyków, a także w fotografii barwnej.
CH
2
CH=CH
2
OMe
anetol
11
Menton
(
5-metylo-2-izopropylocykloheksanon
) jest
przedstawicielem ketonów terpenowych. Występuje obok
mentolu
i
limonenu
w olejkach miętowych. Znane
są wszystkie jego stereoizomery.
(-)-menton
W olejku z Mentha arvensis znajduje się 35%
(-)mentonu
, a w
olejku z Micromeria biflora 55% jego izomeru
(+)
.
(-)-Izomenton
występuje w olejku geraniowym. Popularnym przedstawicielem
ketonów terpenowych jest
karwon
.
(+)-Karwon
ma zapach
kminku i jest głównym składnikiem olejku kminkowego oraz
koperkowego.
(-)-izomenton
(R)-2-metyl-5-izopropenylocykloheks-2-en-1-on
O
R
1
2
5
O
S
R
1
2
5
O
R
S
1
2
5
(+)-karwon

12
Jonony czyli trimetylocykloheksenylobut-3-en-2-ony
Ich konstytucja przypomina terpenoidy, jednak nie spełniają
reguły
Ruzički
,
tzn. reszty
izoprenu
nie są połączone w sposób
ogon-głowa
.
CH=CHCCH
3
O
CH=CHCCH
3
O
Różnią się
położeniem
podwójnego
wiązania
-jonon
-jonon
Powstają w wyniku degradacyjnego
utlenienia
karotenów. Zwykle
występują w małym stężeniu, np. w owocach, warzywach, także w
herbacie i tytoniu. Są głównymi składnikami olejku z kwiatów
fiołków.
Zapach czystych jononów przypomina woń drzewa cedrowego, a ich
roztwory alkoholowe mają zapach fiołków.
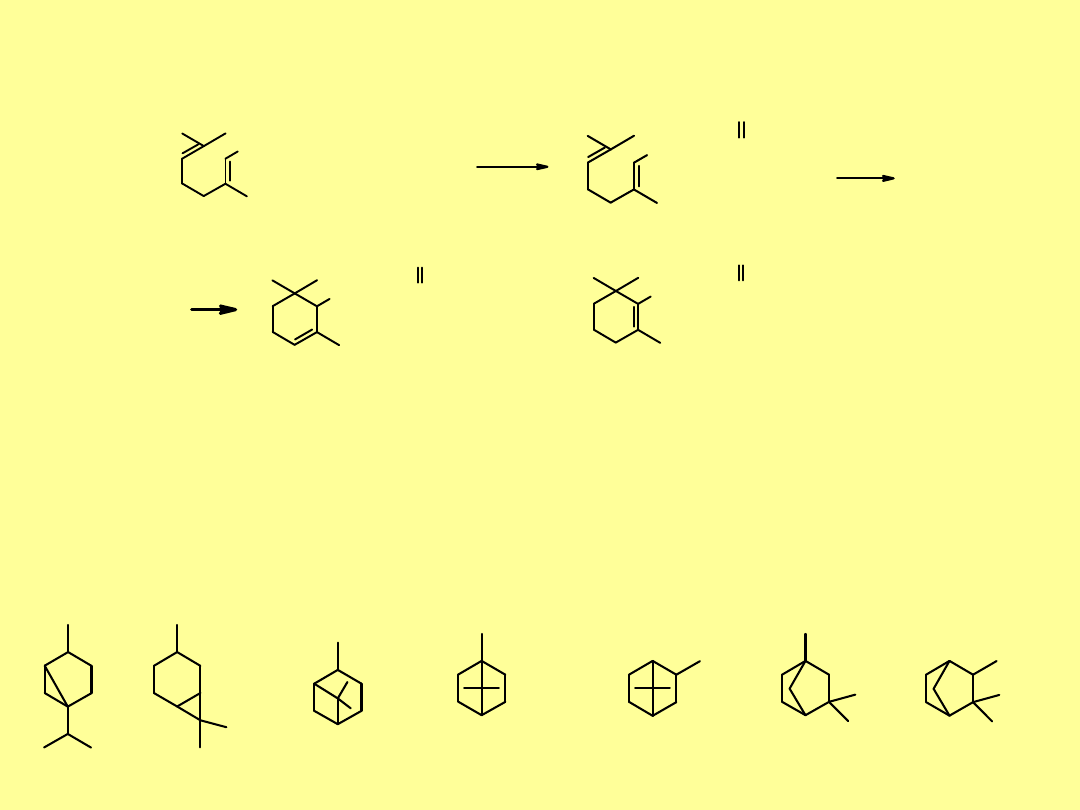
13
Jonony są produkowane na skalę przemysłową z uwagi na
zapotrzebowanie w przemyśle perfumeryjnym. Surowcem jest
cytral
, który poddaje się kondensacji z
acetonem
, po czym produkt
kondensacji cyklizuje do jononów pod wpływem H
2
SO
4
.
CHO + CH
3
COCH
3
cytral aceton
HO
-
- HOH
O
CH=CHCCH
3
H
2
SO
4
CH=CHCCH
3
O
CH=CHCCH
3
O
+
-jonon -jonon
Ugrupowania jononowe
stanowią fragment karotenów.
Bicykliczne monoterpeny i monoterpenoidy
Dzielą się na siedem grup, ze względu na duże zróżnicowanie
szkieletów.
Nazwy tych grup wywodzą się od nazw węglowodorów o
odpowiednim szkielecie.
tujan
karan
pinan boran
(
kamfan
)
izobornylanfenchanizokamfan
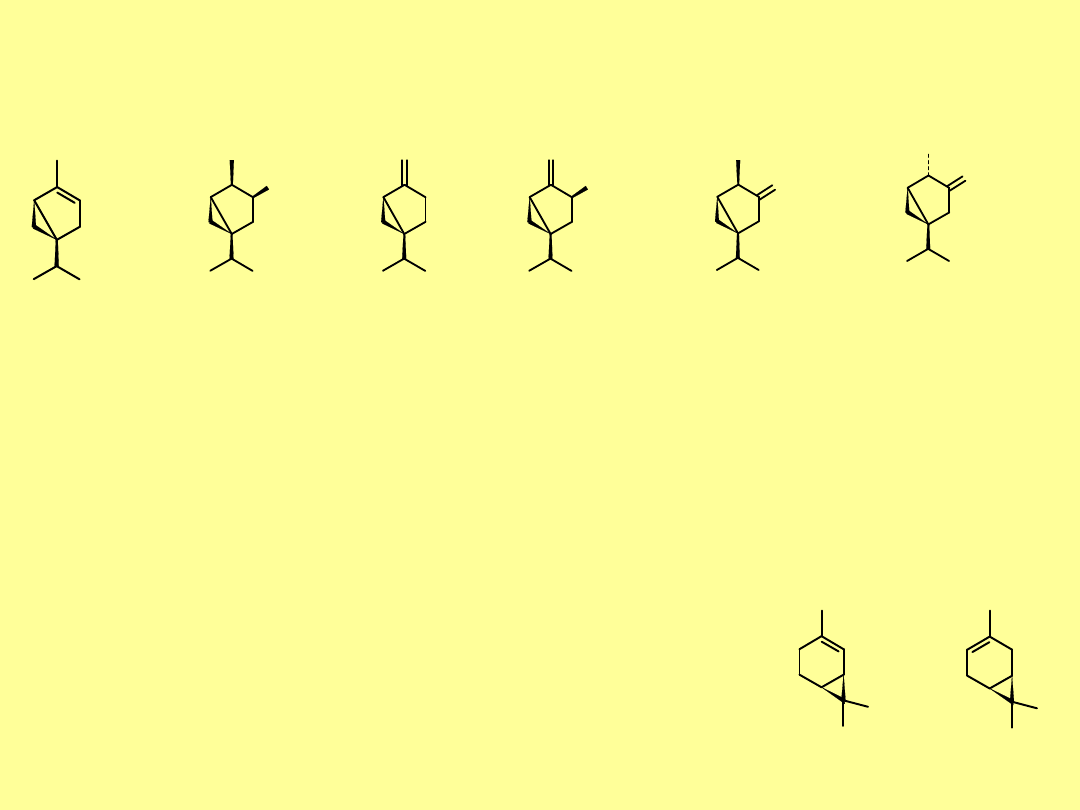
14
Grupa tujanu. Popularne tujeny,
(+)
i
(-)--tujeny
są składnikami
m.in. olejków cyprysowego, eukaliptusowego i z jałowca rosnącego
w Rosji. W olejku piołunowym występuje
(-)-tujol
, wolny i jego
estry. Znane są
sabinen
i
sabinol
; spotykane
są także pochodne ketonowe.
(-)--tujen
OH
(-)-tujol
sabinen
OH
sabinol
O
(-)--tujon
O
(+)--tujon izotujon
1
3
5
R
R
-Tujon
jest
neurotoksyną
, która w małych dawkach pobudza korę
mózgową i wywołuje niepokój. Większe dawki powodują drżenie
mięśni, drgawki i drażliwość. Nalewki piołunowe (absynt) wywołują
nie tylko upojenie alkoholowe, ale i dodatkowe pobudzenia. Również
wina typu wermut zawierają wyciąg z piołunu. Wyciągi piołunowe są
stosowane do zwalczania pasożytów skóry (świerzbu, wszawicy).
Preparat przeciw wszawicy zawiera zarówno
-tujon
(z piołunu), jak
i
-tujon
z wrotycza.
Grupa karanu.
Karan
nie występuje w naturze;
popularne
są natomiast kareny:
kar-2-en
(dawniej
2
-
karen
) i
kar-3-en
(
3
-karen
). Występują w olejku
sosnowym i w olejkach z roślin tropikalnych.
Produkty utlenienia karenów są stosowane do
wyrobu perfum.
(+)-kar-2-en
(+)-kar-3-en
15
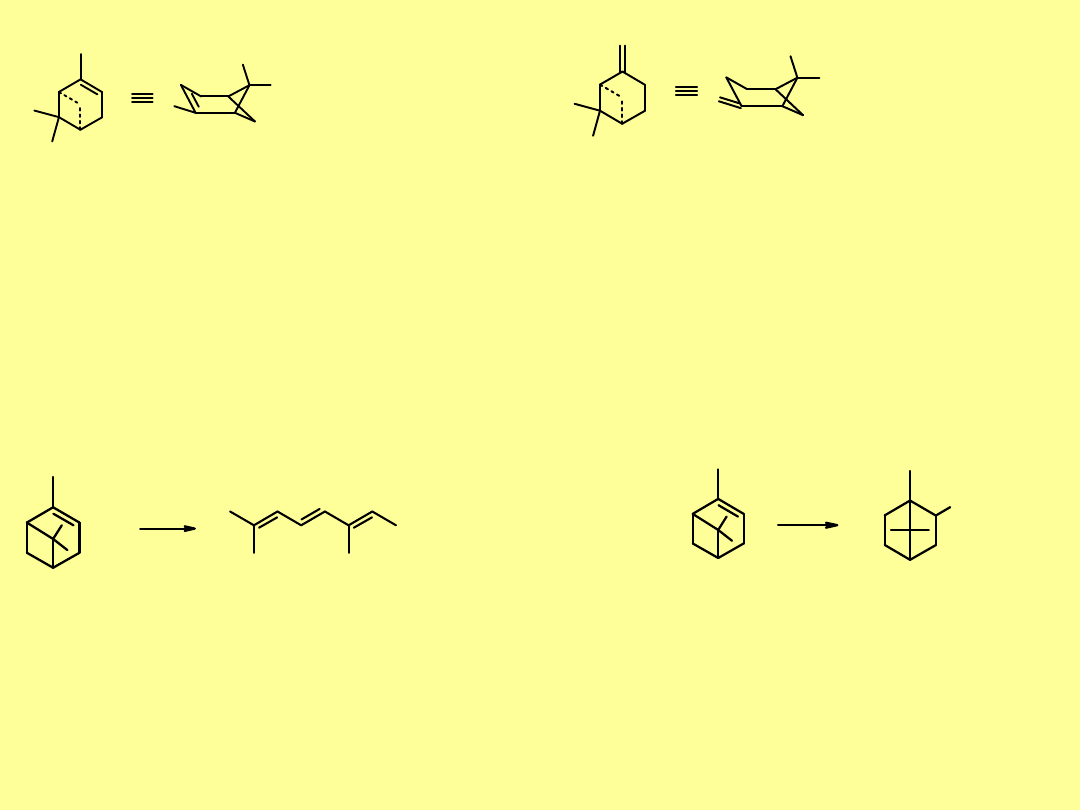
Grupa pinanu. Najczęściej spotykanymi przedstawicielami tej
grupy to pineny, i .
(+)--pinen
(+)--pinen
(+)-(1R,5R)-2,6,6-trimetylo-
bicyklo[3.1.1]hept-2-en
(+)-(1R,5R)-6,6-trimetylo-2-
metylenobicyklo[3.1.1]hept-2-en
Wszystkie stereoizomery
pinenu
występują w naturze, przede
wszystkim w igłach, szyszkach i drewnie wielu drzew iglastych. Są
głównymi składnikami
terpentyny
– lotnej części żywicy.
1
3
1
3
W temp. około 250
o
C oba izomery
pinenu
izomeryzują do
dipentenu
.
Pinen
w reakcji z chlorowodorem tworzy krystaliczny
chlorek bornylu
, zwany
sztuczną kamforą
; reakcji towarzyszy
przegrupowanie.
pinen
dipenten
Cl
HCl
pinen chlorek bornylu
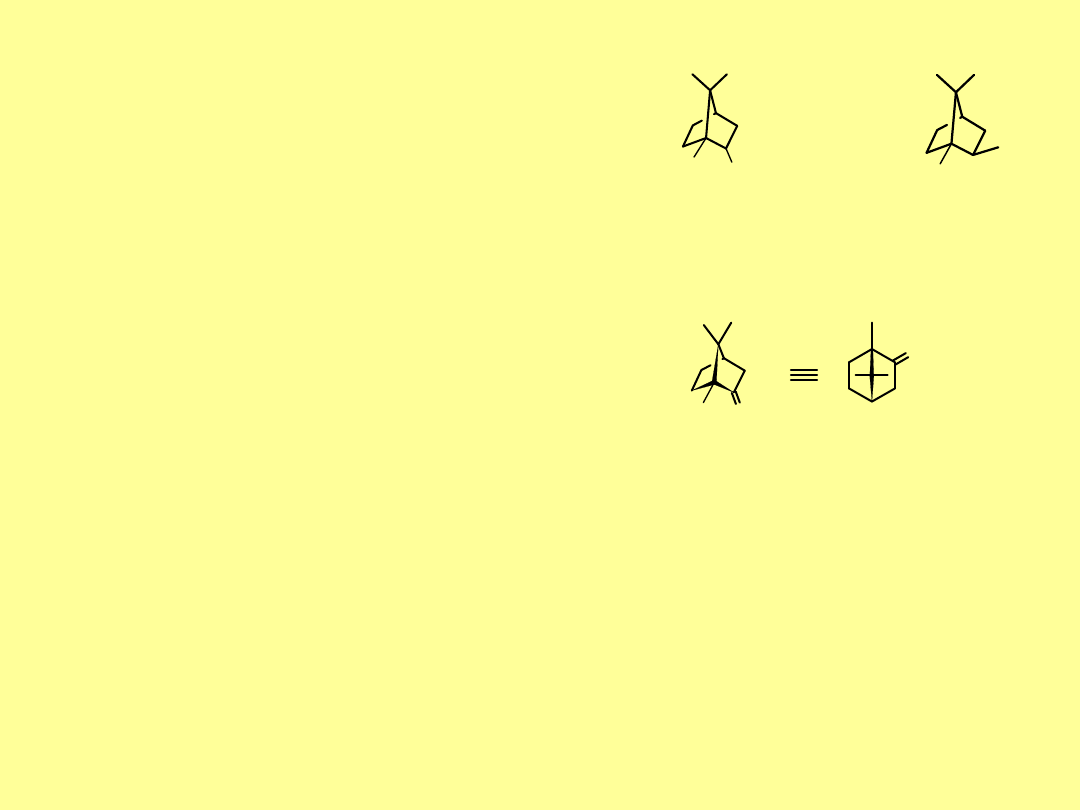
16
Grupa bornanu (kamfanu). Najbardziej znanymi terpenoidami
tej grupy to
kamfora
,
borneol
i
izoborneol
.
Borneole spotyka się w postaci 4
stereoizome-rów i 2 racematów.
Borneol
, zwany
kamforą borneo
, ma
zapach kamfory; występuje w ponad
100 roślinach jako wolny alkohol lub
jego estry.
(-)-borneol
(endo)
(+)-izoborneol
(egzo)
Borneole służą jako dodatki zapachowe do soli kąpielowych, mydeł i
preparatów aromatyzujących.
OH
OH
Kamfora
była znana już w starożytności,
do Europy sprowadzili ją Arabowie.
kamfora
Występuje w postaci 2 stereoizomerów:
(1R,4R)-
i
(1S,4S)-
oraz
racematu. Najczęściej spotykana jest prawoskrętna, zwana
naturalną
,
pospolitą
lub
japońską
. Pozyskuje się ją na drodze
destylacji z parą wodną
rozdrobnionego drewna drzewa
kamforowego (cynamonowiec kamforowy lub kamforowiec lekarski –
Cinnamonum camphora).
O
1 2
4
O
1
2
4
Kamfora
ma charakterystyczny, silny zapach, drażni skórę i działa
miejscowo znieczulająco. Jest hydrofobowa, łatwo sublimuje, z uwagi
na zwarty kształt cząsteczki. Stąd powiedzenie:
zniknął jak
kamfora
. Ze względu na dużą wartość stałej krioskopowej była
stosowana jako rozpuszczalnik do wyznaczania MM
metodą Rasta
.
Służyła za standard porównawczy do określania
konfiguracji
względnej
terpenów.
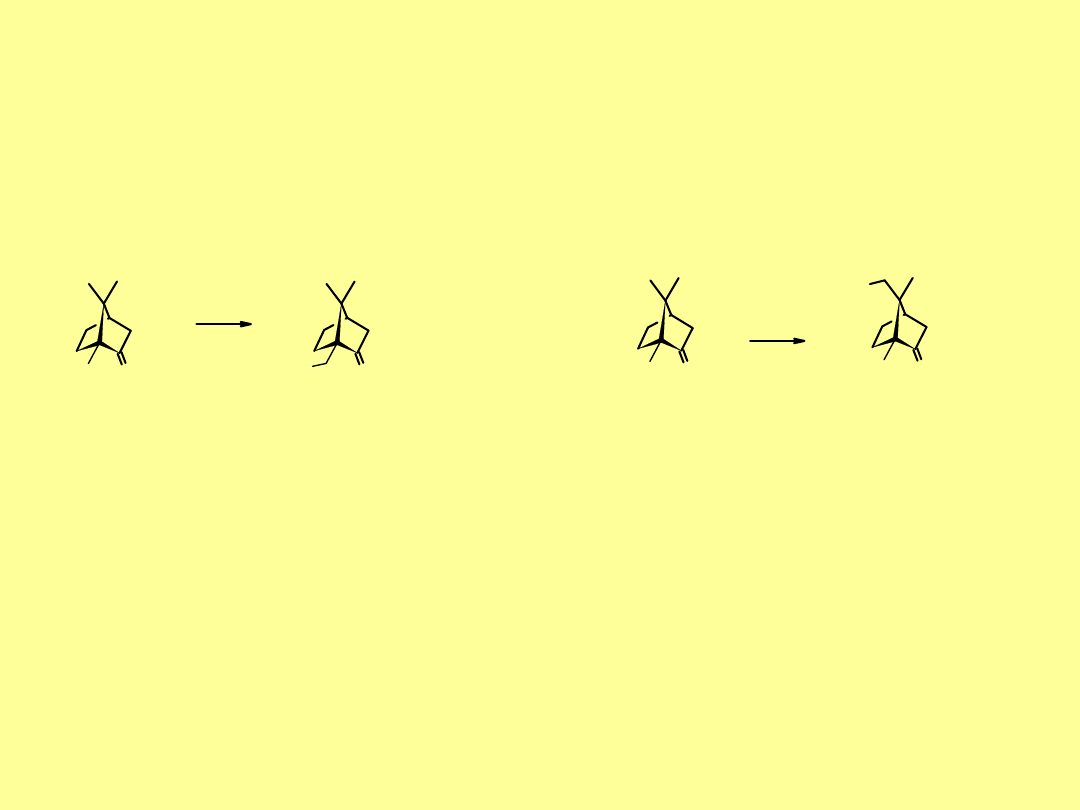
17
Kamfora
była podawana jako lek nasercowy. Obecnie jej roztwór w
oleju (olejek kamforowy) lub w alkoholu (spirytus kamforowy)
stosowany jest do
zewnętrznego odkażania
,
drażnienia
(reakcja
immunologiczna) czy
zapobieganie odleżynom
.
Jest składnikiem preparatów „na katar” – udrażniających drogi
oddechowe i „na reumatyzm” – zmniejszającym bóle reumatyczne.
W Ac
2
O pod wpływem stężonego H
2
SO
4
ulega sulfonowaniu –
powstaje
kwas (+)-kamforo-10-sulfonowy
.
kamfora
Sulfonowanie
kamfory
w samym, stężonym H
2
SO
4
prowadzi do
kwasu (+)-kamforo-9-sulfonowego
. Kwasy kamforosulfonowe
służą do rozdzielania racemicznych amin na
enancjomery
, w tym
aminokwasów.
kwas (+)-kamforo-9-sulfonowy
kwas (+)-kamforo-10-sulfonowy
O
1 2
4
10
O
HO
3
S
H
2
SO
4
Ac
2
O
1 2
4
10
O
1 2
4
9
O
HO
3
S
H
2
SO
4
1 2
4
9
W połowie XX w.
kamfora
miała duże znaczenie jako plastyfikator.
Po zmieszaniu
kamfory
(do 25%) z
kolodium
(
nitrocelulozą
o
małej zawartości N) otrzymano
celuloid
– pierwsze tworzywo
„sztuczne”. Do tego celu stosowano głównie uzyskiwaną z
pinenu
kamforę
syntetyczną.
Celuloid
jest przeźroczysty i z tego powodu
został nazwany szkłem organicznym. Był stosowany do wytwarzania
zabawek, szyb organicznych i taśm filmowych (taśmy celuloidowe).
W latach 60. XX w. produkcja
celuloidu
została wstrzymana, ze
względu na jego
wyjątkową łatwopalność
.
18
Seskwiterpeny i seskwiterpenoidy
Jest to bardzo zróżnicowana grupa
trimerów
izoprenu
o wzorze
C
15
H
24
, spotykana powszechnie w roślinach, grzybach, u zwierząt,
rzadziej w bakteriach. Są to gęste, hydrofobowe oleje o tw. >250
o
C.
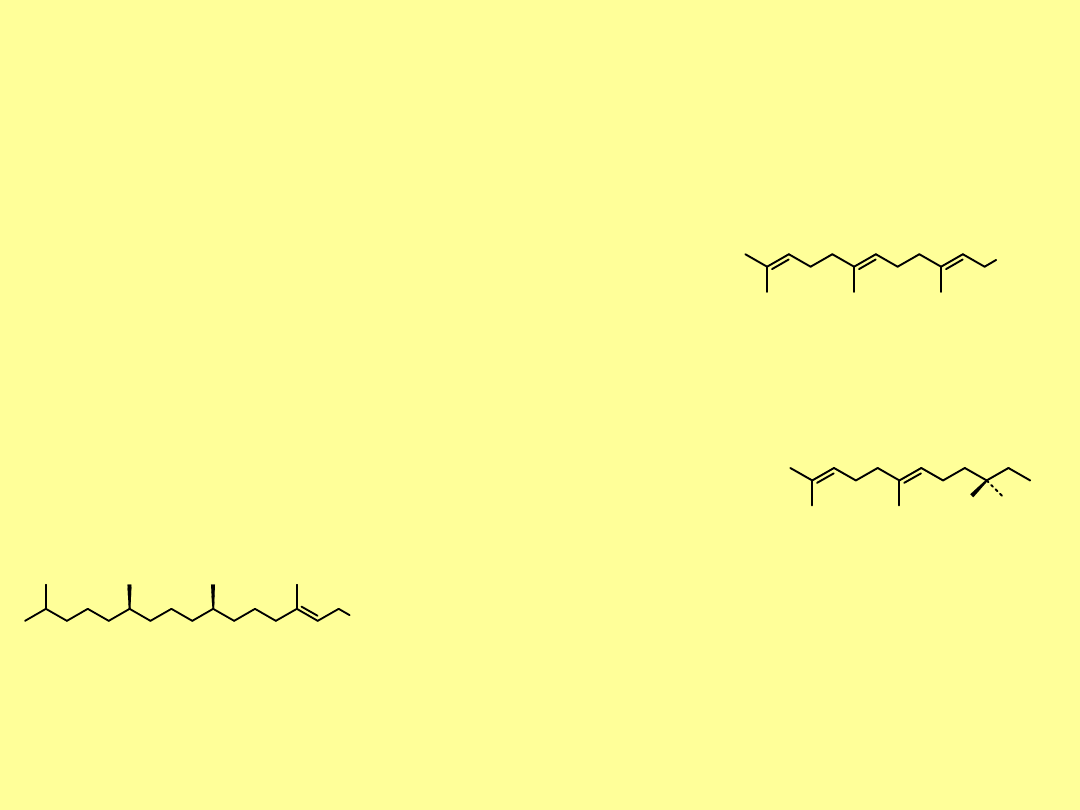
Seskwiterpenoidy niecykliczne
Farnezol
– nienasycony alkohol,
składnik olejku konwaliowego, lipowego,
akacjowego i innych; wydzielany jest
przez niektóre owady jako feromon.
OH
farnezol
Difosforan farnezylu
jest produktem pośrednim w biosyntezie
wszystkich seskwiterpenów i wyższych terpenoidów. Służy do
perfumowania mydeł.
Nerolidol
jest składnikiem
olejku neroli
(
bergamontowego
),
otrzymywanego z kwiatów gorzkiej pomarańczy.
O
H
nerolidol
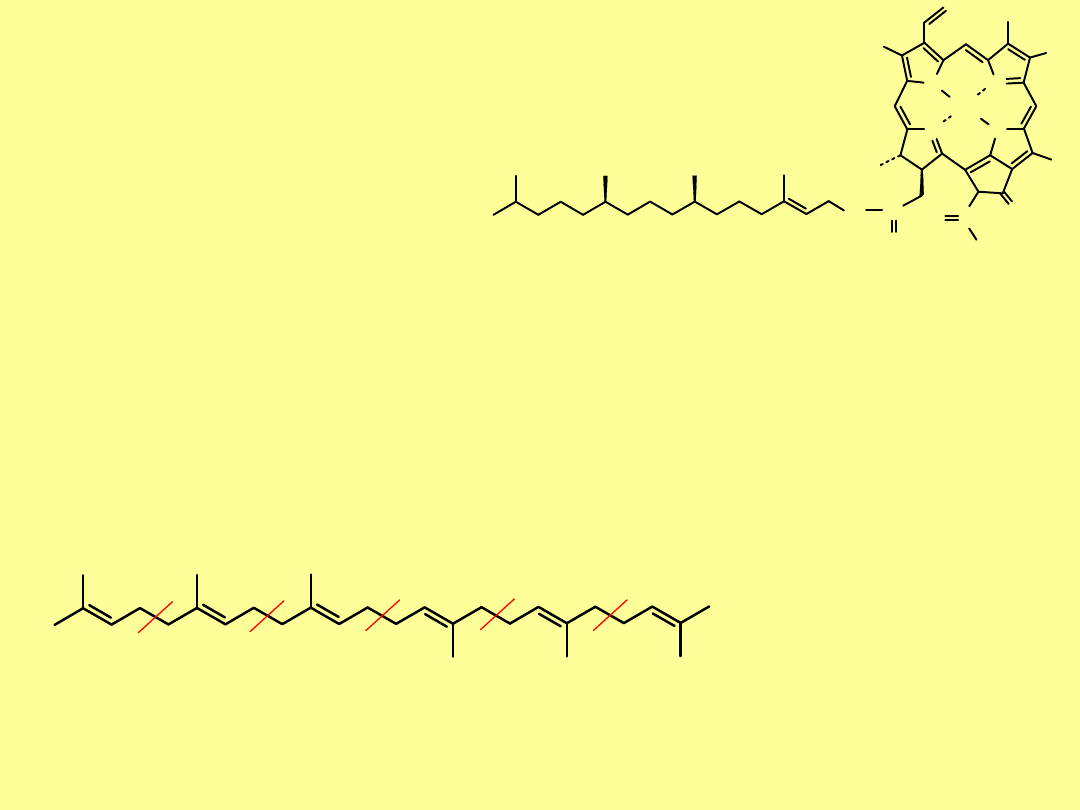
Fitol stanowi fragment wielu
biologicznie
czynnych substancji, np.
chlorofilu
,
witamin
E
i
K
. Jest gęstym, lepkim olejem.
OH
fitol
19
Reszta fitolowa w
chlorofilu
, to najbardziej
hydrofobowa część tej substancji; nadaje mu
postać wosku.
Fitol
jest wykorzystywany jako
surowiec do produkcji witaminy K.
N
N
N
N
Et
O
OMe
O
O
O
C
C
Mg
chlorofil
Triterpeny i triterpenoidy
Opisano ponad 4 000 tego typu związków. Ich prekursorem jest
skwalen
. Wiele tych związków ma szkielet
cyklopentanoperhydrofenantrenu, podobnie jak steroidy, które
też powstają ze
skwalenu
. Często triterpenoidy stanowią
aglikon
glikozydów, np. saponin. Są składnikami roślinnych i zwierzęcych
wosków.
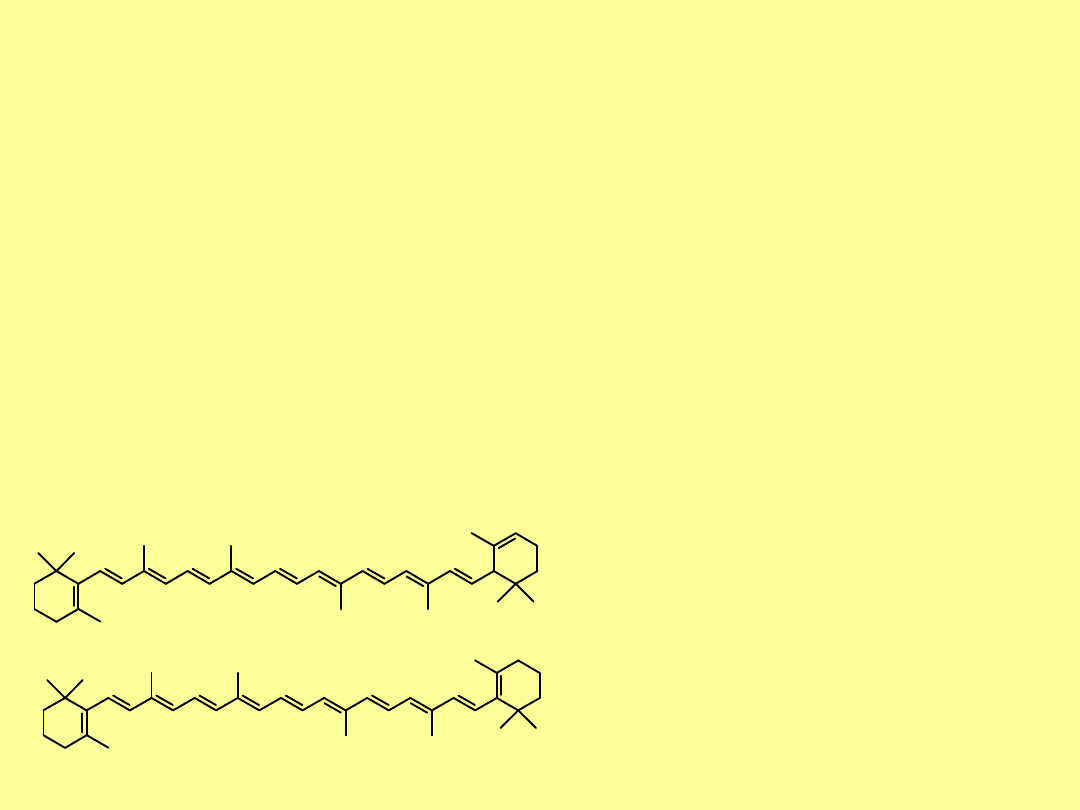
Skwalen
ma zbliżoną budowę do triterpenów – jednak nie
wszystkie fragmenty
izoprenu
są połączone w sposób ogon-głowa;
podobnie jest w triterpenach i karotenach.
Występuje powszechnie w naturze, w największym stężeniu w
wątrobie niektórych zwierząt morskich. Po raz pierwszy wydobyto go
z wątroby rekina. Oliwa zawiera
go 0,1-0,7%, a olej rzepakowy 0,03%; jest też składnikiem tłuszczu
ludzkiego.
głowa
ogon
głowa
głowa
głowa
głowa
głowa
ogon
ogon
ogon
ogon
ogon
20
Tetraterpeny i tetraterpenoidy
Najważniejszymi ich przedstawicielami są karoteny i karotenole.
Wywodzą się z jononów; ich wzór sumaryczny = C
40
H
56
. W
zależności od liczby i rodzaju pierścieni jononowych wyróżnia się
-
,
-
i
-karoteny
. Najbardziej rozpowszechniony jest
-karoten
,
barwnik roślinny, nadający żółte zabarwienie, np. marchewce.
Zawiera dwa pierścienie
-jononu
połączone łańcuchem, który jest
tetramerem
izoprenu
, często w skrócie zapisuje się go (,),
-
karoten
to (,), zawiera po jednym pierścieniu
-
i
-jononu
, a
-
karoten
ma tylko jeden pierścień
-jononu
– ().
Likopen
, podobnie jak i inne karoteny, ulega w wątrobie
przekształceniu w witaminę A. Ma bardzo silne działanie
przeciwnowotworowe.
Kapsantyna
, czerwony barwnik owoców
papryki, jest w niektórych krajach dopuszczona do barwienia
żywności i kosmetyków. Karoteny i karoteiny, np. ksantofile
(utlenione karoteny) biorą czynny udział w fotosyntezie, są w stanie
absorbować kwanty energii świetlnej.
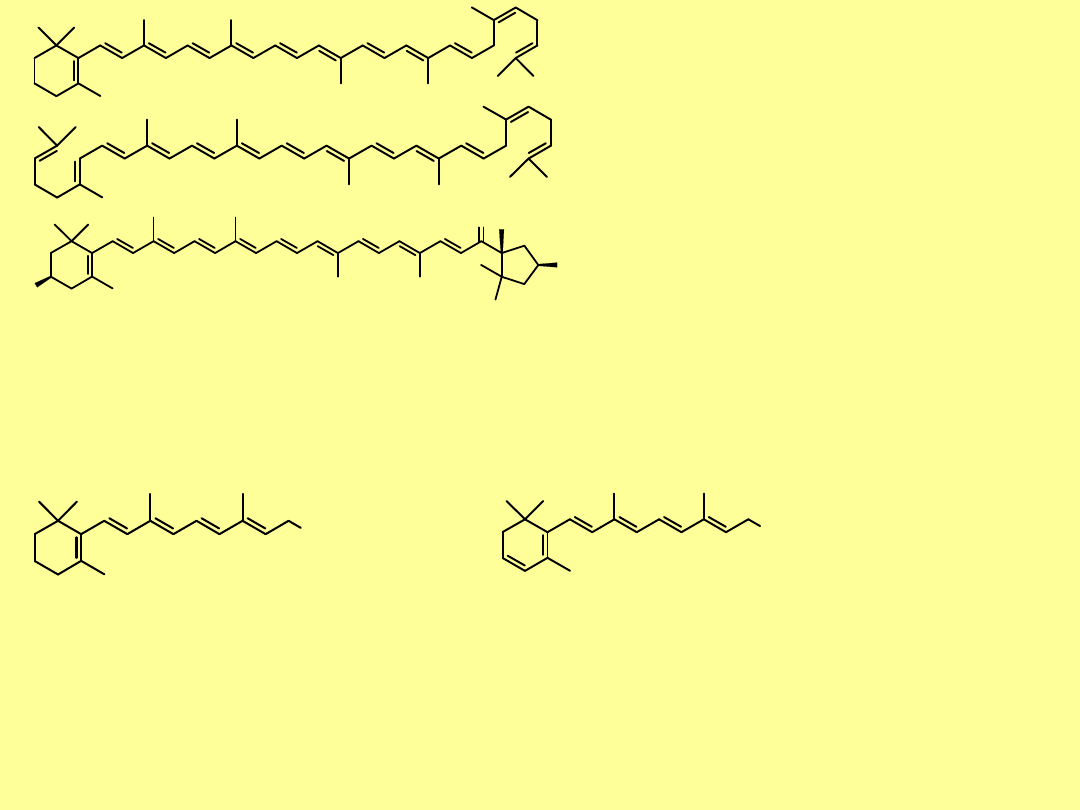
-karoten
, (,), ciemnoczerwony
-karoten
, (,), czerwonobrązowy
21
-karoten
, (), fioletowy
likopen
,
,-karoten
; czerwony
barwnik
pomidorów
O
O
H
OH
kapsantyna
, czerwony
barwnik
owoców papryki
Witamina A jest to grupa związków zawierających
pierścień
-
jononu
i
łańcuch oligoizoprenowy
. Za witaminę A
1
, zwaną
również
retinolem
lub
akseroftolem
uważa się polienowy alkohol –
3,7-dimetylo-9-(2,6,6-trimetylo-cykloheksen-1-ylo)nona-
2,4,6,8-(all trans)tetraen-1-ol
.
OH
witamina A
1
,
retinol
witaminą A
2
,
3-dehydroretinoletinol
OH
Warto zauważyć, że z mola
-karotenu
powstają 2 mole witaminy A,
zaś z
-
i
-karotenu
tylko po jednym, dlaczego? Karoteny są
prowitaminami
witaminy A. Dzienne zapotrzebowanie na
witaminę A wynosi 15 g
retinolu
lub 30 g najbardziej aktywnej
prowitaminy
, jaką jest
-karoten
. Witamina A
2
wykazuje 3-50%
aktywności
retinolu
.

22
Karoteny często są słabo wchłaniane z przewodu pokarmowego; ich
przyswajanie ułatwia gotowanie i rozdrabnianie warzyw. Witamina
A jest niezbędna do adaptacji wzroku przy niedostatecznym dostępie
światła. Łączy się ona z białkiem zwanym
opsyną
i tworzy się
rodopsyna
, barwnik siatkówki. Witamina A jest magazynowana
w wątrobie i uwalniana do krwi w miarę potrzeby; jej zapas w
wątrobie wystarcza na kilka miesięcy. Dostarczana jest z mięsem,
mlekiem, jajami, a także jako
prowitamina
.
Do
awitaminozy
dochodzi u osób źle odżywianych. Brak witaminy
A powoduje kurzą ślepotę, a u dzieci dodatkowo zmniejszenie
odporności na zakażenia oraz ułatwia łuszczenie i rogowacenie
naskórka. W mleku kobiecym jest go 2x więcej niż w mleku krowim.
Przetwarzanie mleka obniża w nim zawartość witaminy A, wobec
czego mleko konsumpcyjne jest często w nią wzbogacane. Nadmiar
witaminy A (kilkadziesiąt mg dziennie) jest bardzo szkodliwy.
Powoduję nadmierną pobudliwość, utratę łaknienia, suchość skóry,
uszkodzenie wątroby i krwiomocz. Nadmiar karotenów nie jest
szkodliwy.
23
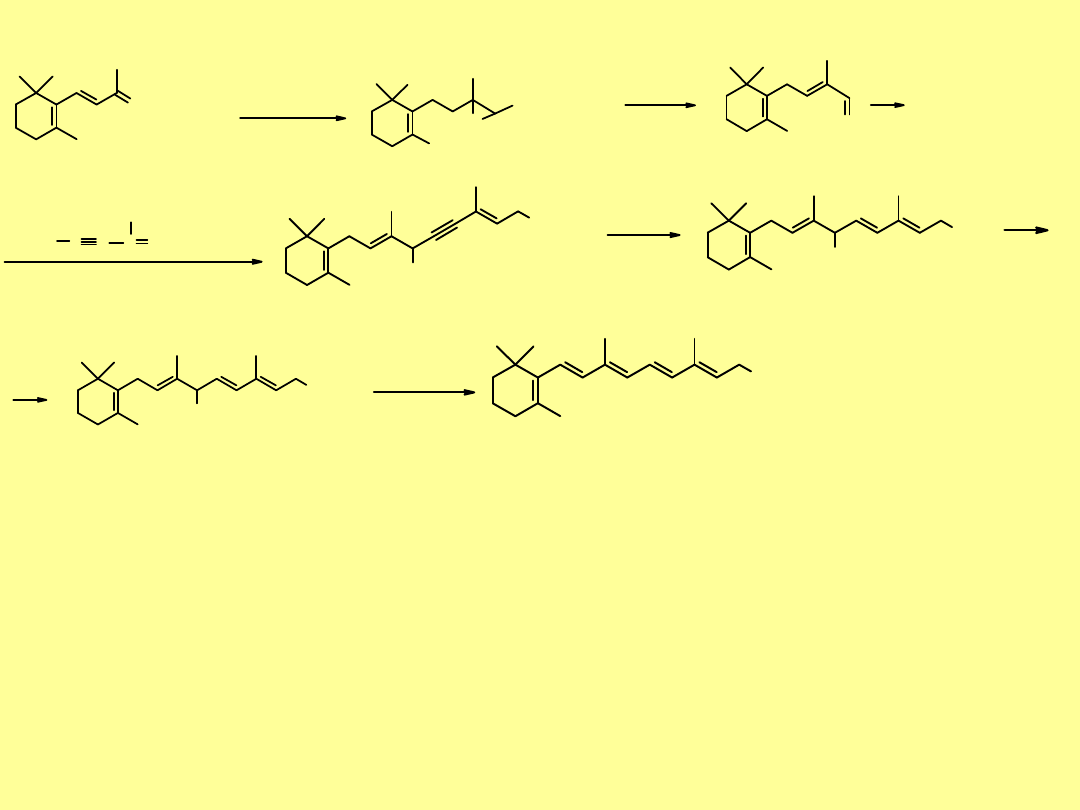
Surowcem do otrzymywania witaminy A jest
-jonon
O
-jonon
O
COOEt
ClCH
2
COOEt
O
H
+
/HOH
, - CO
2
OH
OH
BrMg
CHCH
2
OMgBr
C C C
OH
OH
H
2
katalizator
Lindlara
OAc
OH
Ac
2
O
retinol
OH
1.
- HOH
2.
H+/HOH
24
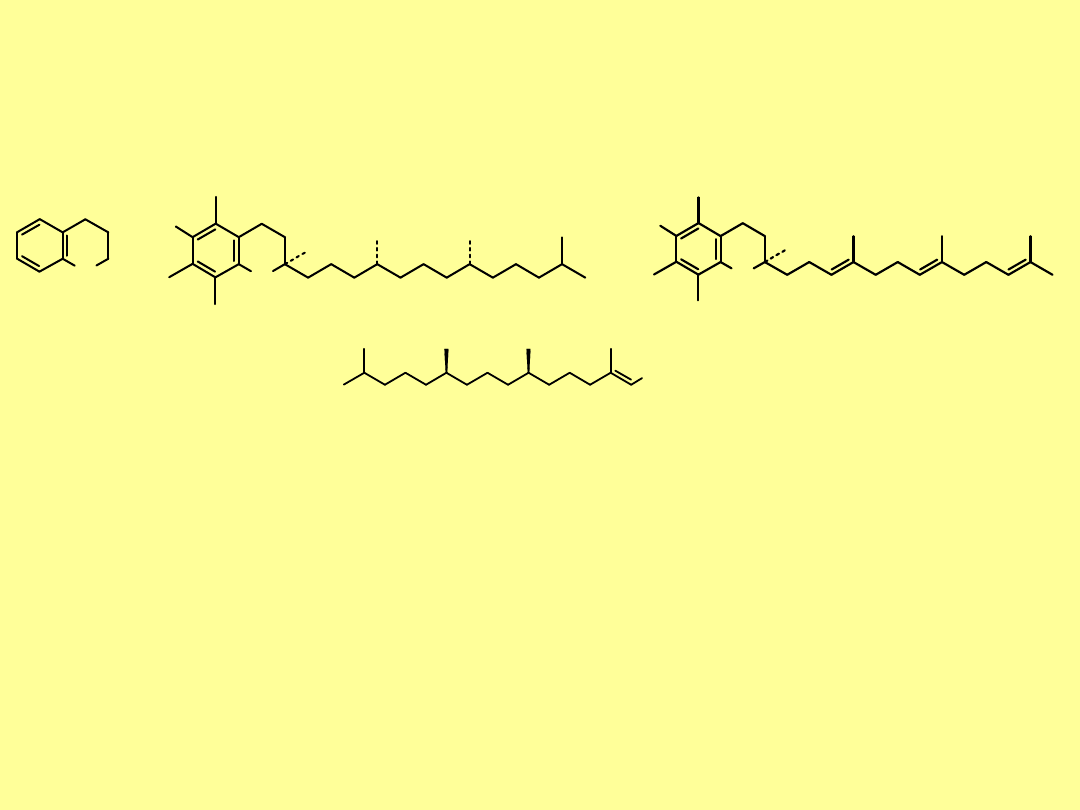
Witamina E zwana inaczej
tokoferolem
nie jest jednym,
zdefiniowanym związkiem. Wyizolowano 8 substancji o
właściwościach witaminy E. Aktywność witaminy E, wpływającej
na prawidłowy rozwój narządów płciowych i funkcję rozrodczą
wykazują pochodne
chromanu
zawierające funkcję fenolową, grupy
metylowe i nasycony lub nienasycony łańcuch o szkielecie
triizoprenu
(
fitolu
).
O
chroman
OH
tokoferol
-tokotrienol
O
O
H
1 2
3
4
5
6
1'
2'
4'
12'
7 8
8'
O
O
H
1
3
4
5
6
1'
2'
4'
12'
78
8'
fitol
Zwierzęta doświadczalne karmione wyłącznie mlekiem stają się
bezpłodne. W 1936 r. z kiełków pszenicy wyizolowano substancję,
której brak w pożywieniu szczurów powodował bezpłodność samic i
samców. Nazwano ją
tokoferolem
od greckich słów tocos –
potomstwo i pherei – rodzić. Witamina E oprócz stymulowania
funkcji rozrodczych jest antyutleniaczem zarówno in vivo, jak i in
vitro substancji podatnych na utlenienie, np. witaminy A czy
kwasów polienowych. Służy jako dodatek stabilizujący tłuszcze
spożywcze. Dzienne zapotrzebowanie na w. E wynosi 10-30 mg
tokoferolu
. Jego analogi są mniej aktywne, w tym syntetyczny
DL
-
tokoferol
. Witamina E pełni wiele funkcji leczniczych; jej nadmiar
jest szkodliwy.
25
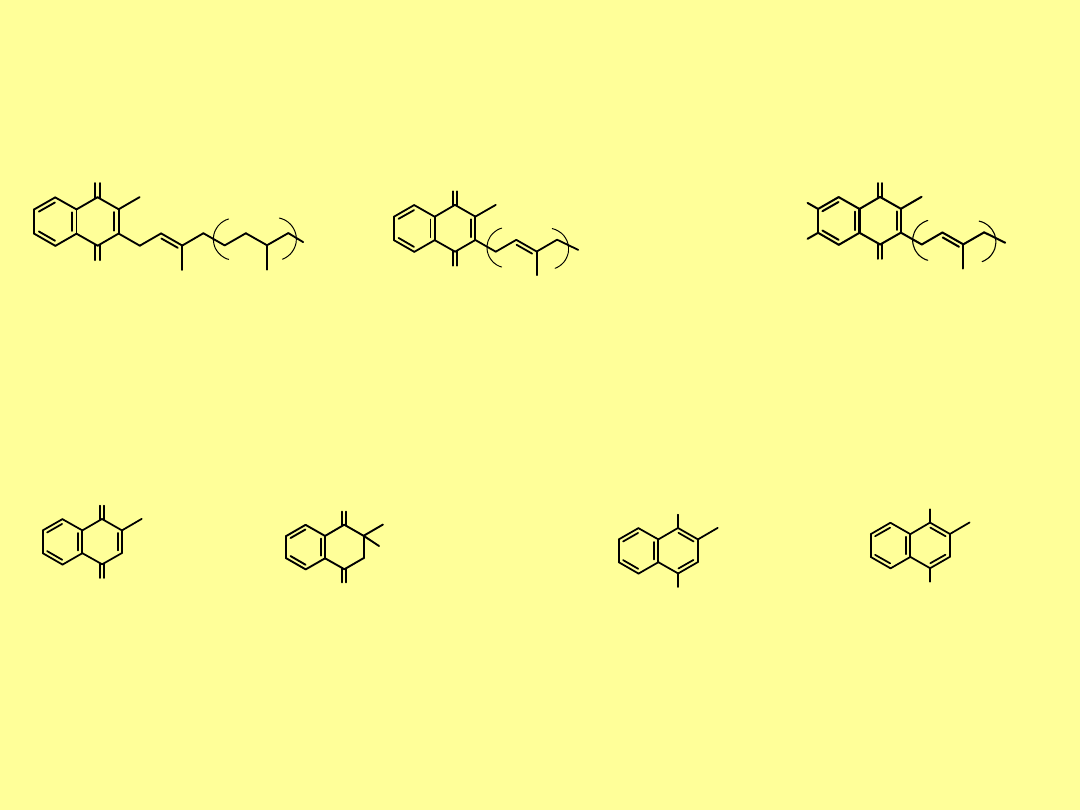
Witamina K zwana również
czynnikiem koagulacyjnym
ma
właściwości przeciwkrwotoczne
. Takie działanie wykazuje kilka
związków, są to pochodne
1,4-naftochinonu
. Witaminą K
1
nazywany jest
filochinon
, czyli
2-metylo-3-(3
’
,7
’
,11
’
,15
’
-
tetrametyloheksadec-2
’
-enylonaftaleno-1,4-dion
H
O
O
n
witamina K
1
Inne witaminy K różnią się budową łańcucha alifatycznego i
podstawnikami
w pierścieniu aromatycznym. Syntetyczne witaminy K mają
znacznie mniej skomplikowana budowę. Ich nazwy ponumerowano
od K
3
-K
7
.
H
O
O
n
witamina K
1
(
menachinon
, MK-n)
H
O
O
CH
3
O
CH
3
O
n
ubichinon
,
(
koenzym Q
)
O
O
witamina K
3
,
menadion
O
O
SO
3
Na
sól sodowa kwasu me-
nadionosulfonowego
OH
OH
witamina K
4
OH
NH
2
witamina K
5
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
Wyszukiwarka
Podobne podstrony:
11 3id 12114 ppt
11 DEPRESJAid 12399 ppt
11 Farmakokinetykaid 12413 ppt
11 listopadaid 12481 ppt
01 Rozp UE w sprawie kosmetyków 11 09id 2656 ppt
11 Linuxid 12466 ppt
11 ODCZULANIEid 12533 ppt
wyk 11 Andropauza i menopauza ppt
11 NOWOTWORYid 12216 ppt
11 2 1 Zanieczyszczeniaid 12341 ppt
11 regeneratorid 12598 ppt
11 06 11 20id 12326 ppt
11 wykładid 12671 ppt
11 Posagid 12560 ppt
10 Czw II 2010 11 28id 10540 ppt
11) Metody (wyklad 11)id 12718 ppt
11 polimeryid 12236 ppt
więcej podobnych podstron