
1
STATYKA I
STATYKA I
KINETYKA
KINETYKA
CHEMICZNA
CHEMICZNA

2
Aspekt statyczny
czyli zapis przemiany chemicznej
w postaci równania z uwzględnieniem zależności
molowych wynikających z podstawowych praw
chemii, czyli prawa stałości składu i zachowania
masy.
Interpretacja
kinetyczna
dotyczy
zagadnień
związanych z przebiegiem reakcji, czyli jej
szybkością,
stanem
równowagi
reakcji
i
możliwością wpływania na przesunięcie równowagi
reakcji.
Przemiany chemiczne rozpatruje się w
dwóch aspektach:
statycznym i kinetycznym

3
STATYKA CHEMICZNA
STATYKA CHEMICZNA
1. REAKCJE ODWRACALNE - STAN RÓWNOWAGI
CHEMICZNEJ
2. STAŁA RÓWNOWAGI CHEMICZNEJ
3. REGUŁA PRZEKORY
____________________________________
STATYKA
CHEMICZNA
zajmuje
się
układami o składnikach zdolnych do
reagowania ze sobą, w których reakcja
chemiczna
zakończyła
się
wskutek
osiągnięcia STANU RÓWNOWAGI.
REAKCJE ODWRACALNE
4
Reakcje odwracalne
Reakcje odwracalne
Reakcje
chemiczne
Reakcje
Reakcje
odwracalne
odwracalne
Reakcje
nieodwracalne
REAKCJA ODWRACALNA –
może przebiegać zarówno ze
strony lewej na prawą jak i w
kierunku przeciwnym – osiąga
stan równowagi, np.
A + B C + D
C + D A +B
A + B C + D – reakcja
odwracalna
np.
2H
2(g)
+ O
2(g)
2H
2
O
(g)
2H
2
O
(g)
2H
2(g)
+ O
2(g)
2H
2(g)
+ O
2(g)
2H
2
O
(g)
(Biegną do wyczerpania
substratów),
np. reakcja
Ag
+
+ Cl
-
=
AgCl
jest reakcją
nieodwracalną – nie
osiąga stanu równowagi
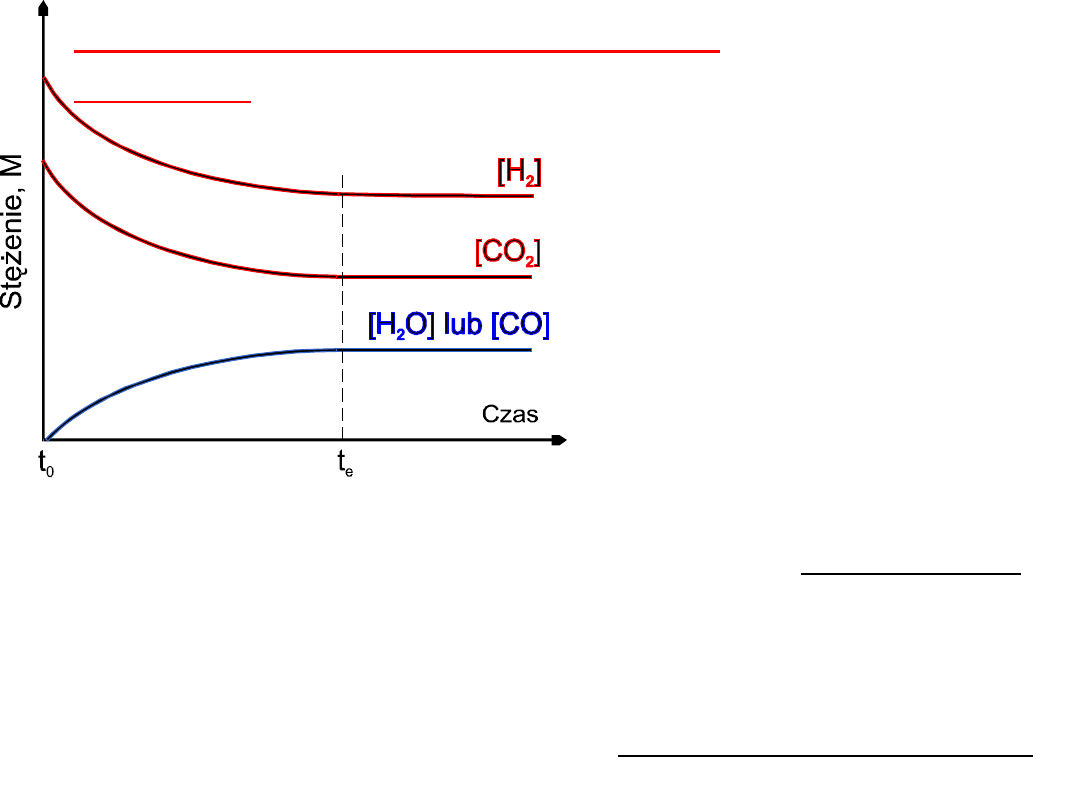
Osiąganie stanu równowagi
reakcji:
H
2(g)
+ CO
2(g)
H
2
O
(g)
+ CO
(g)
W momencie t
e
stężenia [H
2
], [CO
2
],
[H
2
O] i [CO] są stałe.
Stężenia substratów
maleją, a produktów
rosną w trakcie
przebiegu reakcji
Dla
reakcji
odwracalnych
,
przekształcenie
substratów w produkty często jest niezupełne,
bez względu na czas reakcji.
Osiągnięty zostaje stan, w którym stężenia nie
zmieniają się z upływem czasu. Stan ten, który
trwa tak długo, jak długo warunki zewnętrzne
nie ulegają zmianie.
Stan równowagi chemicznej.
Stan równowagi chemicznej.

6
Cechy reakcji odwracalnych:
Cechy reakcji odwracalnych:
1. W danych warunkach ciśnienia i temperatury
stężenia produktów i nieprzereagowanych
substratów są stałe –
RÓWNOWAGA
CHEMICZNA
4. Szybkości reakcji w stanie równowagi w obu
kierunkach są jednakowe: V
1
= V
2
2. Równowaga chemiczna jest równowagą
DYNAMICZNĄ
– po zmianie warunków
fizycznych zostanie wznowiony bieg reakcji
w jednym z kierunków
3. Każdej reakcji odwracalnej odpowiada jej
własny ściśle określony stan równowagi,
który charakteryzuje się odpowiednią
zależnością między stężeniami reagentów -
stała równowagi.
7
Stała równowagi
Stała równowagi
chemicznej
chemicznej
Warunek równowagi:
v
1
= v
2
K
C
- stała równowagi chemicznej wyrażona
stężeniem
k
1
i k
2
są stałe, więc K
C
jest również wartością
stałą
Matematycznym wyrazem stanu równowagi chemicznej
jest
STAŁA RÓWNOWAGI CHEMICZNEJ
STAŁA RÓWNOWAGI CHEMICZNEJ
:
:
D, E, F, L –
reagenty
d, e, f, l – ilość
moli
v – szybkość
reakcji
k – stała szybkości
reakcji
C – stężenie
v
1
dD + eE
fF + lL
v
2
Reakcja odwracalna:
l
L
f
F
2
2
e
E
d
D
1
1
)
C
(
)
C
(
k
v
)
C
(
)
C
(
k
v
l
L
f
F
2
e
E
d
D
1
)
C
(
)
C
(
k
)
C
(
)
C
(
k
e
E
d
D
l
L
f
F
C
2
1
)
C
(
)
(C
)
C
(
)
(C
K
k
k

Przeprowadźmy serię trzech doświadczeń
zrealizowanych w tej samej temperaturze, ale
różniących się początkowymi stężeniami substratów
tej reakcji:
Rozważmy tę zależność na przykładzie równowagi
pomiędzy PCl
3(g)
, Cl
2(g)
i PCl
5(g)
.
PCl
5(g)
jest termicznie nietrwały i ulega rozkładowi na
PCl
3
i Cl
2
:
PCl
5(g)
PCl
3(g) +
Cl
2
(g)
PCl
5(g)
PCl
3(g) +
Cl
2
(g)
PCl
5(g)
PCl
3(g) +
Cl
2
(g)
Stała równowagi chemicznej
Stała równowagi chemicznej
WARTOŚĆ STAŁEJ RÓWNOWAGI WYZNACZA
SIĘ DOŚWIADCZALNIE.
Po zmieszaniu PCl
3
i Cl
2
reagują, tworząc PCl
5
:
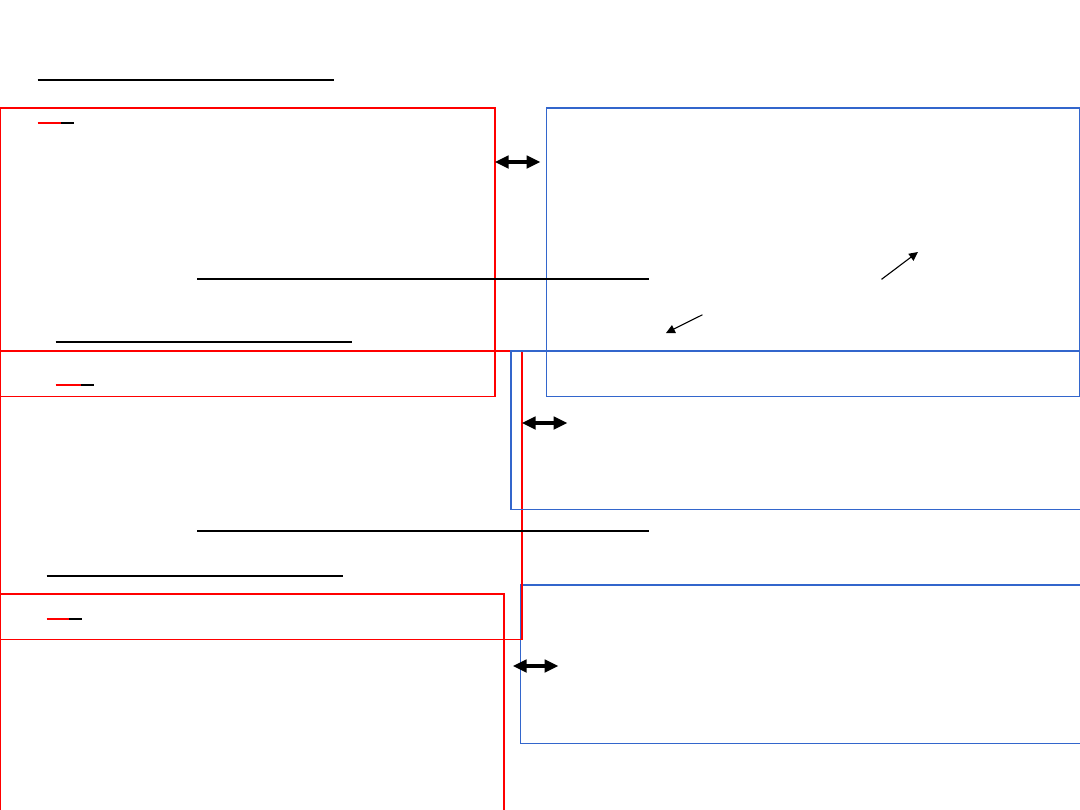
Doświadczenie
c
:
[PCl
5
] początkowe = 1
mol/dm
3
[Cl
2
] początkowe = 3
mol/dm
3
[PCl
3
] początkowe = 2
mol/dm
3
[PCl
5
] końcowe =2,82 mol/dm
3
[Cl
2
] końcowe = 1,175 mol/dm
3
[PCl
3
] końcowe = 0,175 mol/dm
3
[PCl
5
] początkowe = 0
mol/dm
3
[Cl
2
] początkowe = 1
mol/dm
3
[PCl
3
] początkowe = 1
mol/dm
3
[PCl
5
] końcowe = 0,764 mol/dm
3
[Cl
2
] końcowe = 0,236 mol/dm
3
[PCl
3
] końcowe = 0,236 mol/dm
3
Doświadczenie
b
:
T=546 K
PCl
5(g)
PCl
3(g) +
Cl
2
(g)
Doświadczenie
a
:
[PCl
5
]początkowe = 1
mol/dm
3
[Cl
2
] początkowe = 0
mol/dm
3
[PCl
3
] początkowe = 0
mol/dm
3
[PCl
5
]końcowe=0,764
mol/dm
3
[Cl
2
] końcowe = 0,236
mol/dm
3
[PCl
3
]końcowe =0,236
mol/dm
3
Stężenia w
równowadze

10
7
,
13
175
,
0
175
,
1
82
,
2
236
,
0
236
,
0
764
,
0
]
Cl
[
]
[PCl
]
[PCl
2
3
5
W każdym przypadku otrzymujemy taką samą
wartość liczbową wynoszącą 13,7
wynoszącą 13,7
:
Obliczamy dla doświadczeń: a); b); c) dla stanu
równowagi ułamek:
]
Cl
[
]
[PCl
]
[PCl
2
3
5
stężeni
a
Stała równowagi chemicznej
Stała równowagi chemicznej
Ogólnie można napisać, że dla reakcji:
dD + eE fF + lL
Stała w równowagi wyniesie:
C
i
- stężenie reagentów w mol/dm
3
e
E
d
D
l
L
f
F
C
C
C
C
C
K
)
(
)
(
)
(
)
(
PCl
5(g)
PCl
3(g) +
Cl
2
(g)
a i b
c
Stała równowagi
Stała równowagi
chemicznej
chemicznej
Dla reakcji przebiegającej w fazie gazowej stężenia
molowe można zastąpić ciśnieniami cząstkowymi:
K
p
- stała równowagi wyrażona
ciśnieniem:
p
i
- ciśnienie cząstkowe reagentów
Stałą równowagi można też wyrazić za pomocą stężenia
określonego w ułamkach molowych (X):
Ułamek
molowy:
i
i
i
i
n
n
X
Ponieważ: p
i
= X
i
·P
oraz p
i
= C
i
·RT,
n
X
C
n
C
p
n
X
p
)
RT
P
(
K
K
(RT)
K
K
P
K
K
i
i
i
i
(substr.)
n
(prod.)
n
Δn
gdzie:
P - ciśnienie całkowite
Zależności
pomiędzy K
C
,
K
p
i K
X
e
E
d
D
l
L
f
F
X
)
(X
)
(X
)
(X
)
(X
K
e
E
d
D
l
L
f
F
p
)
p
(
)
p
(
)
p
(
)
p
(
K
12
PRAWO DZIAŁANIA MAS
PRAWO DZIAŁANIA MAS
Wartości stałych równowagi zmieniają się od bardzo dużych
do bardzo małych wartości. Im większa wartość tym reakcja
jest przesunięta bardziej w prawo.
np. K = 9,39 10
9
dla reakcji syntezy siarkowodoru
K = 2,38 10
-3
dla reakcji syntezy amoniaku
„Gdy w roztworze doskonałym panuje
stan równowagi chemicznej w określonej
temperaturze, to iloraz iloczynu stężeń
(ciśnień) produktów reakcji do iloczynu
stężeń
(ciśnień)
substratów
reakcji
podniesionych odpowiednio do potęg,
których
wykładniki
odpowiadają
współczynnikom
stechiometrycznym
równania reakcji, ma wartość stałą”.
Stała równowagi chemicznej
określana jest w chemii pod nazwą:
prawo działania mas
.
e
E
d
D
l
L
f
F
C
C
C
C
C
K
)
(
)
(
)
(
)
(

13
Jeśli równowagę układu reakcyjnego zostanie
zakłócona, to reakcje chemiczne zostają wznowione i
zostanie osiągnięty nowy stan równowagi.
PRZESUNIĘCIA STANU
PRZESUNIĘCIA STANU
RÓWNOWAGI CHEMICZNEJ
RÓWNOWAGI CHEMICZNEJ
„Jeżeli na układ znajdujący się w stanie
równowagi działa jakiś czynnik zewnętrzny,
to powoduje on naruszenie stanu równowagi
w taki sposób, który częściowo osłabia
działanie tego czynnika”.
Kierunek takich przesunięć określa zasada (reguła)
LE CHATELIERA- reguła przekory.
Równowaga chemiczna jest równowagą
DYNAMICZNĄ
– po zmianie warunków
fizycznych zostanie wznowiony bieg reakcji w
jednym z kierunków
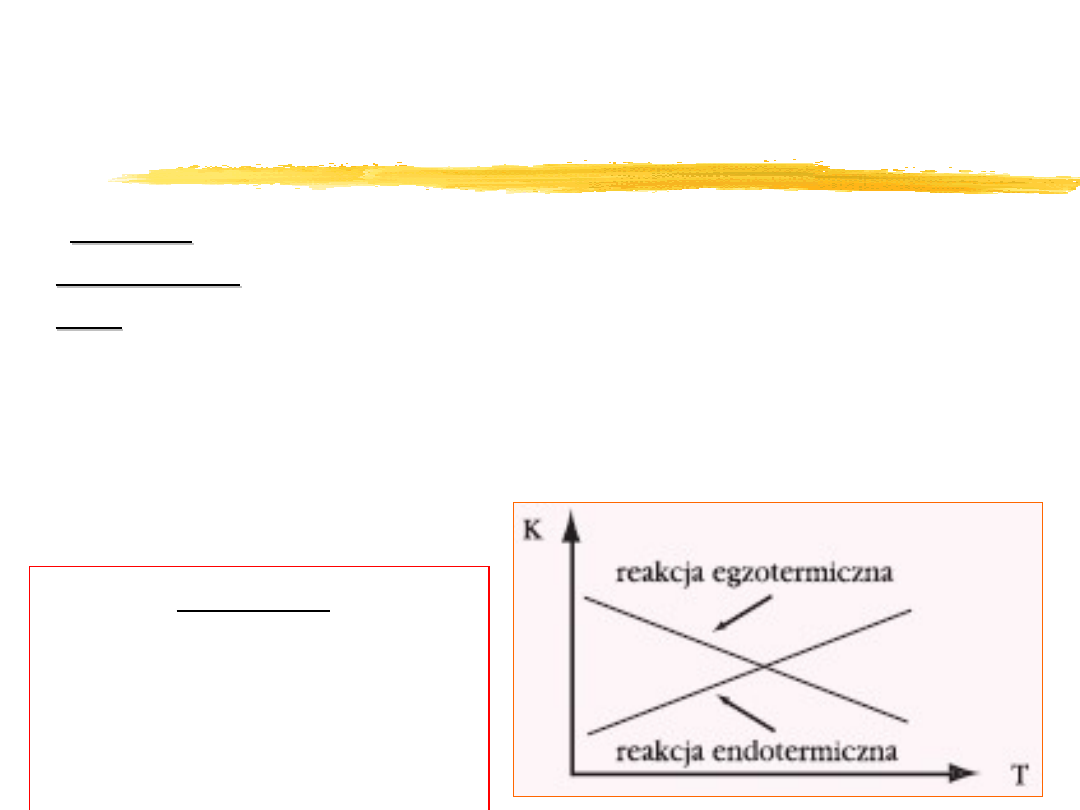
Reguła przekory
Reguła przekory
/Reguła Le Chateliera i Brauna/
/Reguła Le Chateliera i Brauna/
H < 0 - reakcja egzotermiczna
3H
2
+ N
2
2NH
3
równowaga
T=const.
H > 0 - reakcja endotermiczna
A. Podwyższamy temperaturę wznawia bieg
reakcja rozkładu NH
3
(endotermiczna)
wpływ
wpływ
temperat
temperat
ury
ury
B. Obniżamy temperaturę wznawia bieg reakcja
syntezy NH
3
(egzotermiczna)
Ogólnie:
podwyższenie temp.
podwyższenie temp.
sprzyja reakcjom
sprzyja reakcjom
endotermicznym, a
endotermicznym, a
obniżenie –
obniżenie –
egzotermicznym
egzotermicznym
.
14

1
5
Reguła przekory
Reguła przekory
/Reguła Le Chateliera i Brauna/
/Reguła Le Chateliera i Brauna/
wpływ
wpływ
ciśnienia
ciśnienia
v maleje
3H
2
+ N
2
2NH
3
równowaga
p=const.
V rośnie
A. Zwiększamy ciśnienie układ reaguje zmniejszeniem
objętości – liczby cząsteczek (równowaga przesuwa
się w prawo) tworzenie NH
3
B. Zmniejszamy ciśnienie układ reaguje
zwiększeniem objętości – liczby cząsteczek
(równowaga przesuwa się w lewo) rozpad NH
3
Z 4 moli substratów powstaje 2 mole produktów. Reakcji
przebiegającej z lewa na prawo, towarzyszy zmniejszenie
ilości moli.
Wzrost ciśnienia w układzie, w którym zachodzi
reakcja
syntezy
amoniaku,
spowoduje
przesunięcie
równowagi
w
kierunku
kompensacji
ciśnienia,
czyli
w
kierunku
zmniejszenia ilości moli (tzn. w kierunku
syntezy)
16
CIŚNIENIE
CIŚNIENIE
(reakcje w fazie
gazowej)
(1) V
prod.
= V
sub.
np.
H
2
+ J
2
= 2HJ
(2) V
prod.
< V
sub.
np.
N
2
+ 3H
2
=
2NH
3
przesunięcie równowagi
• wzrost ciśnienia
:
nie wpływa
:
nie wpływa
• obniżenie ciśnienia
• obniżenie ciśnienia
• wzrost ciśnienia
przesunięcie
równowagi
:
:
(3) V
prod.
> V
sub.
np. N
2
O
4
=
2NO
2
przesunięcie
równowagi
:
:
• wzrost ciśnienia
• obniżenie ciśnienia

17
C. Wpływ zmian stężenia na stan równowagi
[A][B]
[C][D]
K
D
C
B
A
1. Wprowadzenie substratów do roztworu
Następuje zwiększenie wartości mianownika, ponieważ
stała K w danej temperaturze nie ulega zmianie
musi zwiększyć się wartość licznika.
Wniosek: Przy zwiększeniu stężenia substratów w
roztworze następuje przesunięcie równowagi w
kierunku powstawania produktów ( w prawo).
2. Wprowadzenie produktów do roztworu ( lub
usuwanie substratów)
Następuje zwiększenie wartości licznika, ponieważ
stała K nie ulega zmianie
musi nastąpić zwiększenie
wartości mianownika.
Wniosek: przy zwiększeniu stężenia produktów w
roztworze następuje przesunięcie równowagi w
kierunku substratów( w lewo).

KINETYKA CHEMICZNA
KINETYKA CHEMICZNA
zajmuje się badaniem szybkości reakcji
szybkości reakcji
oraz mechanizmami reakcji, a więc obejmuje
zagadnienia szybkości dochodzenia układu
do stanu równowagi.
Reakcja:
Ag
+
+ Cl
-
AgCl
; przebiega bardzo szybko
do wyczerpania jednego z
substratów
Reakcja:
H
2
+ 0,5O
2
H
2
O
; w temp. otoczenia
przebiega wolno
Większość reakcji przebiega
z szybkością, którą można mierzyć
19
SZYBKOŚĆ REAKCJI CHEMICZNEJ
SZYBKOŚĆ REAKCJI CHEMICZNEJ
Jakie czynniki decydują o szybkości reakcji chemicznej?
1.
Stężenie substratów
2.
Temperatura
3.Obecność katalizatora (katalizatory dodatnie i
ujemne)
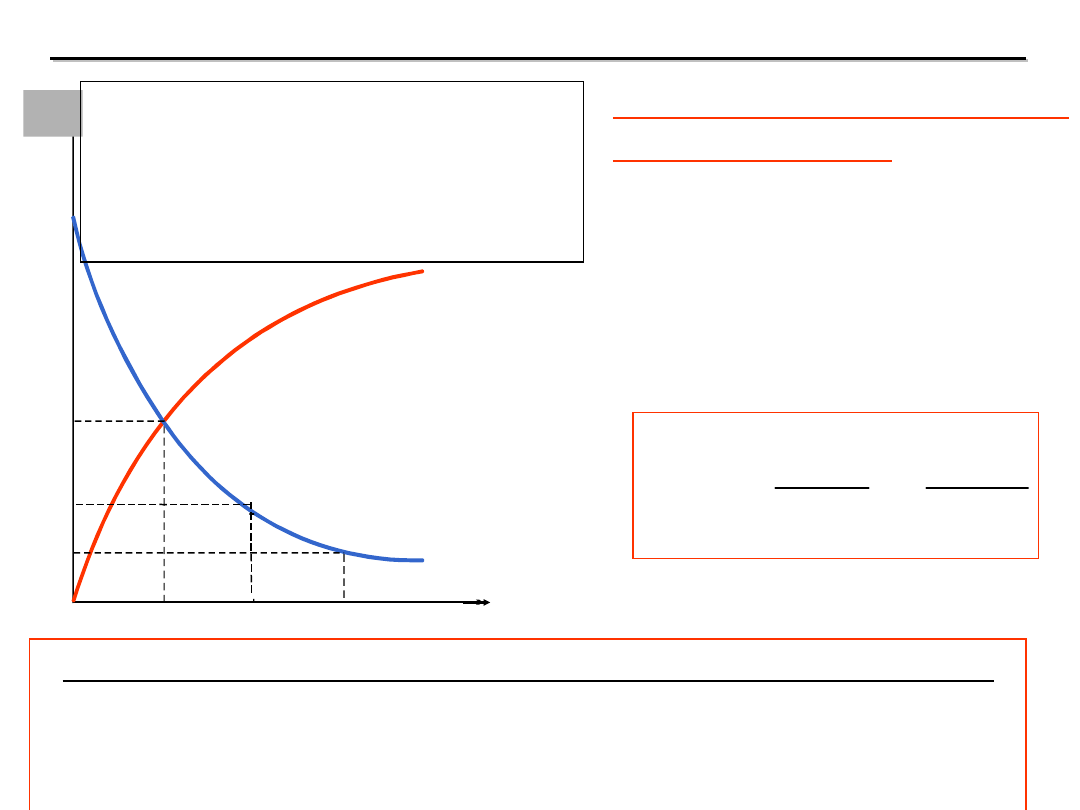
C
s
C
s
,C
x
Zmiana
stężenia
substratów (C
S
) i stężeń
produktów (C
X
) w czasie (t)
przebiegu reakcji.
C
X
t
t
2t
3t
C
s
C
s
/
2
C
s
/
4
C
s
/
8
SZYBKOŚĆ REAKCJI
CHEMICZNEJ
(V) jest
to
ubytek
stężenia
substratów reakcji lub
przyrost
stężenia
produktów reakcji w
nieskończenie
małym
odstępie czasu:
dt
dC
dt
dC
V
x
s

20
Jeżeli reakcja ma postać:
aA + bB + ............. = IL + mM + .................
to szybkość reakcji wyniesie:
gdzie: C
A
, C
B
-
stężenia substratów
a,b -
współczynniki
stechiometryczne
k -
STAŁA SZYBKOŚCI
REAKCJI
Równanie opisujące zależność szybkości reakcji
od stężenia reagentów nazywamy:
RÓWNANIEM KINETYCZNYM REAKCJI
k – szybkość reakcji gdy stężenia substratów
równe są jedności: gdy C
A
= C
B
= ... = 1, to
k =
VStała szybkości reakcji k
nie zależy od
stężenia reagentów.
.....
C
C
k
V
b
B
a
A
)
(
)
(
Równanie kinetyczne
reakcji

21
Równanie kinetyczne
reakcji
Sumę wykładników potęgowych w równaniu
kinetycznym na szybkość reakcji nazywamy
rzędem reakcji
:
a + b + ... = n
rząd reakcji
Rząd niekatalizowanych reakcji wynosi na ogół:
n = 0 – 3; a katalizowanych n = 1 – 2.
Zależność szybkości reakcji od stężenia
substratów jest zatem funkcją potęgową:
n
s
)
(C
k
V
C
S
- stężenie substratów
.....
C
C
k
V
b
B
a
A
)
(
)
(

22
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
REAKCJI CHEMICZNYCH
REAKCJI CHEMICZNYCH
CZĄSTECZKOWOŚĆ
reakcji
jest
liczbą
cząsteczek uczestniczących jednocześnie w
tworzeniu
cząsteczki
produktu
–
limituje
szybkość reakcji chemicznej.
Wyróżniamy reakcje: jednocząsteczkowe,
dwucząsteczkowe, trójcząsteczkowe, itd.
A
PRODUKTY
np.:
Br
2
2 Br
A
C
k
V
REAKCJE JEDNOCZĄSTECZKOWE
W reakcji bierze udział jedna cząsteczka substratu:
Szybkość reakcji jednocząsteczkowych:

23
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
REAKCJI CHEMICZNYCH
REAKCJI CHEMICZNYCH
2
A
B
A
)
(C
k
V
C
C
k
V
W
równaniach
tych,
stężenie
substratu
występuje
w
drugiej
potędze.
Szybkość reakcji dwucząsteczkowych:
REAKCJE DWUCZĄSTECZKOWE
W utworzeniu produktu biorą udział dwie
cząsteczki substratu:
A + B
PRODUKTY
2A
PRODUKTY
np.:
H
2
+ Cl
2
2 HCl
2 HI
H
2
+ I
2

24
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
REAKCJI CHEMICZNYCH
REAKCJI CHEMICZNYCH
REAKCJE TRÓJCZĄSTECZKOWE
Reagują ze sobą trzy cząsteczki substratu:
np.: H
2
SO
3
+ I
2
+ H
2
O
H
2
SO
4
+ 2 HI
2 NO + O
2
2 NO
2
A + B + C
PRODUKTY
3A
PRODUKTY
2A + B
PRODUKTY
3
A
B
2
A
C
B
A
)
C
(
k
V
C
)
C
(
k
V
C
C
C
k
V
Szybkość reakcji trójcząsteczkowych:
Suma wykładników
potęgowych wynosi
trzy

25
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
CZĄSTECZKOWOŚĆ I RZĘDOWOŚĆ
REAKCJI CHEMICZNYCH
REAKCJI CHEMICZNYCH
Teoretycznie
: szybkość reakcji jednocząsteczkowej
jest proporcjonalna do pierwszej potęgi stężenia
substratów;
dwucząsteczkowej
–
do drugiej potęgi;
trójcząsteczkowej
–
do trzeciej potęgi.
RZĘDOWOŚĆ REAKCJI:
RZĘDOWOŚĆ REAKCJI:
Suma wykładników potęgowych w równaniu na
szybkość reakcji, do której należy podnieść stężenia
substratów by doświadczalnie wyznaczona szybkość
reakcji była zgodna z wyliczoną z równania
kinetycznego.
Praktycznie
:
Rzeczywista cząsteczkowość – RZĘDOWOŚĆ
RZĘDOWOŚĆ
REAKCJI
REAKCJI
– nie zawsze jest zgodna z pozorną
(teoretyczną) cząsteczkowością.
Nie zawsze: a + b + ... + k = n
rzędowość.
k
k
b
B
a
A
)
C
(
.....
)
C
(
)
C
(
k
V
REAKCJE PIERWSZEGO RZĘDU
REAKCJE PIERWSZEGO RZĘDU
:
Reakcje, dla których doświadczalnie wyznaczona
szybkość reakcji jest proporcjonalna do pierwszej
potęgi stężenia substratu.
s
C
k
V
1;
n
REAKCJE
DRUGIEGO
REAKCJE
DRUGIEGO
RZĘDU:
RZĘDU:
2
s
C
k
V
2;
n
)
(
3
s
)
(C
k
V
3;
n
Dla reakcji
n-tego
rzędu
:
Występują również reakcje rzędu zerowego.
Wówczas szybkość reakcji nie zależy od stężenia
substratu:
k
V
n
s
C
k
V
)
(
REAKCJE
TRZECIEGO
REAKCJE
TRZECIEGO
RZĘDU:
RZĘDU:

27
Wpływ temperatury na
szybkość reakcji
chemicznych
SZYBKOŚĆ
REAKCJI
CHEMICZNYCH
SZYBKOŚĆ
REAKCJI
CHEMICZNYCH
ROŚNIE ZE WZROSTEM TEMPERATURY,
ROŚNIE ZE WZROSTEM TEMPERATURY,
co wiąże się ze wzrostem stałych szybkości
stałych szybkości
reakcji
reakcji
(k).
np.
chcąc
przeprowadzić
reakcję
syntezy wody z wydajnością 15% należy
go prowadzić:
w temp. 20C
-
54 miliardy lat;
w temp. 500C
-
50 minut;
w
temp.
700C
-
przebiega
wybuchowo.
28
Empiryczna reguła van’t
Hoffa:
Jeżeli = 3, a temperatura wzrośnie o 100
o
to
szybkość reakcji wzrośnie 3
10
razy.
Współczynnik temperaturowy szybkości reakcji
jest to liczba wskazująca ile razy wzrasta
szybkość reakcji po podwyższeniu temperatury o
10 stopni.
Podwyższenie temperatury o 10 stopni powoduje
zwiększenie szybkości reakcji 2-4 razy.
Współczynnik
temperaturowy
szybkości
Współczynnik
temperaturowy
szybkości
reakcji:
reakcji:
T
10
T
k
k
gdzie: k
T+10
- stała
szybkości reakcji w
temp. T+10
k
T
- stała szybkości
reakcji w temp. T
29
Współczynnik temperaturowy szybkości reakcji
zależy od temperatury, przy czym zbliża się do
jedności
gdy
temperatura
dąży
do
nieskończoności:
gdy
T
to
1
Empiryczna reguła van’t
Hoffa:
Można obliczać K w różnych
temperaturach.
10
1
T
2
T
k
k
2
1
lg
T
T
T
k
k
lg
1
1
2
2
1
k
1
, k
2
– stałe szybkości reakcji w temp. T
1
i
T
2
.
Ilościowo zależność ta wygląda następująco:

30
Teoria zderzeń aktywnych –
równanie Arrheniusa
Wg
kinetycznej
teorii
materii
reakcje
chemiczne zachodzą w wyniku zderzeń
cząsteczek substratów (np. dwóch).
Nie wszystkie zderzenia są jednak efektywne,
tzn. prowadzą do powstania produktów reakcji.
Przyjmuje się, że efektywne są tylko te
zderzenia, w których biorą udział cząsteczki
obdarzone energią wyższą od początkowej,
równą lub większą od wartości E zwaną:
ENERGIĄ AKTYWACJI
ENERGIĄ AKTYWACJI
ENERGIA AKTYWACJI
ENERGIA AKTYWACJI przedstawia zatem
najmniejszą energię jaką muszą mieć cząsteczki
substratów, aby mogły wejść w daną reakcję:
E > E
E > E
śr.
śr.
31
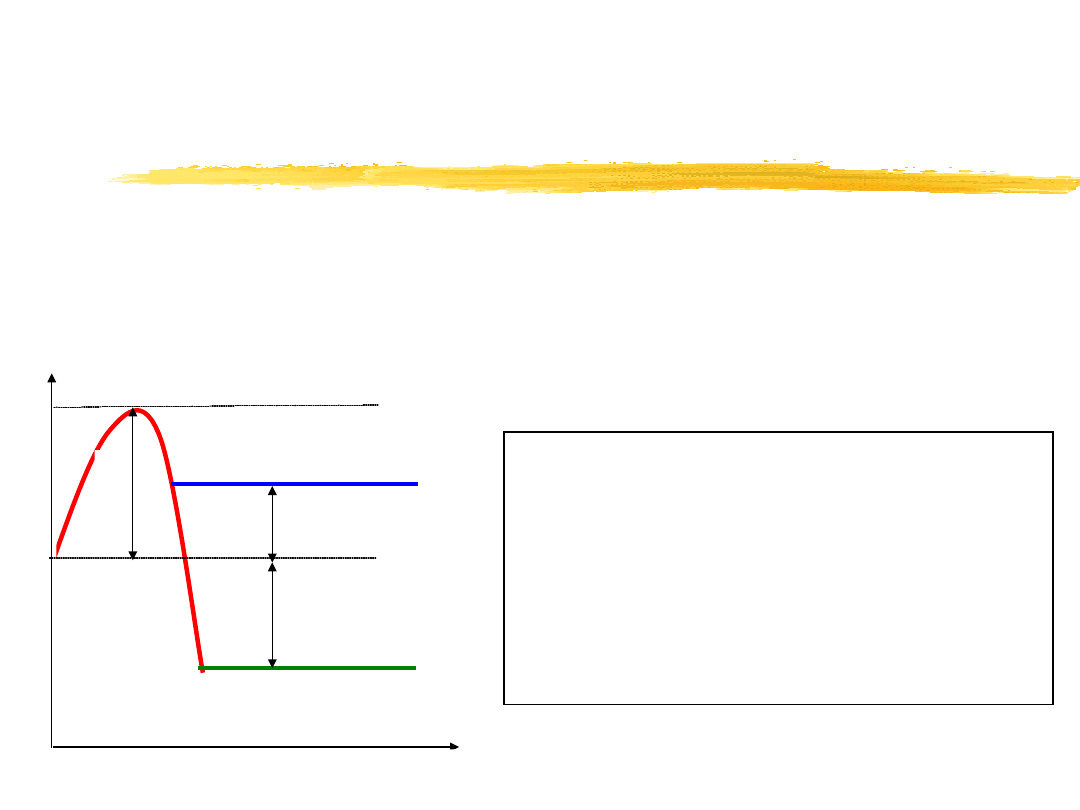
Teoria zderzeń aktywnych
– równanie Arrheniusa
Cząsteczka substratu o przeciętnej energii musi zatem przed
wejściem w reakcję uzyskać pewien nadmiar energii, na skutek
zderzeń z innymi cząsteczkami. Przejście cząsteczki ze stanu
energii zbliżonej do początkowej do stanu energii aktywacji dla
reakcji endotermicznej i egzotermicznej przedstawia rysunek:
H
1
H
2
E
s
E
Energi
a
E
p
E
p
Współrzędna
reakcji
E – energia aktywacji
E
s
– energia substratów
E
p
– energia produktów
H
1
– ciepło reakcji
endotermicznej
H
2
– ciepło reakcji
egzotermicznej

32
Teoria zderzeń aktywnych
– równanie Arrheniusa
Teoria zderzeń aktywnych pozwala śledzić
zmiany
szybkości
reakcji
w
funkcji
temperatury.
RT
E
lnZ
k
ln
e
Z
k
o
RT
E
o
Jest to tzw. równanie ARRHENIUSA
równanie ARRHENIUSA
Z
o
–
ogólna
liczba
zderzeń,
E – energia aktywacji,
R – stała gazowa,
T – temperatura
k
-
stała
szybkości
reakcji
Wg PRAWA PODZIAŁU ENERGII MAXWELLA-
PRAWA PODZIAŁU ENERGII MAXWELLA-
BOLTZMANA
BOLTZMANA
liczba zderzeń aktywnych cząsteczek
(Z = k) wynosi:
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
Wyszukiwarka
Podobne podstrony:
10 wykad Statyka kinetyka chemiczna[F 2006]
Statyka Kinetyka
Statyka Kinetyka
kinetyka i statyka zadania do spr teoria
energetyka kinetyka statyka
Kinetyka Chemiczna
06 Kinetyka reakcji enzymatycznych
Łancuchy kinetyczne
4 Badanie kinetyki reakcji zmy Nieznany (2)
kinetyka, studia, ochrona środowiska UJ, chemia ogólna i nieorganiczna, wyrównawcze
04 Kinetyka reakcji chemicznych i kataliza
więcej podobnych podstron