
WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA
CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH
MATERIAŁÓW OPAKOWANIOWYCH
ENZYMOLOGIA
Kierunek:
Technologia Żywności
i Żywienie Człowieka
semestr I
Wykład 7
Przegląd najważniejszych enzymów

Zakres materiału ENZYMOLOGIA
1. Biochemia, Autor: Jeremy Berg, Lubert Stryer, John L. Tymoczko,
PWN Warszawa (2005)
Rozdziały:
8. Enzymy:: podstawowe pojęcia i kinetyka
9. Strategie katalityczne
10. Strategie regulacyjne:: enzymy i hemoglobina
2. Ćwiczenia z enzymologii i technik biochemicznych. Bartoszewska, Niziołek,
Paszowski, Wydawnictwo SGGW
3. Handbook of Food Enzymology – ed. John R. Whitaker et al., CRC Press; (2002)
4. Enzymes in Food Technology -‐ ROBERT J. WHITEHURST, BARRY A.
LAW, Editors Sheffield Academic Press CRC Press (2002)
3. Food chemistry -‐ Hans-‐Dieter Belitz, Werner Grosch, Peter
Schieberle, Springer (2004)

Enzymy dzieli się na 6 grup (mechanizm reakcji…):
EC 1 oksydoreduktazy: katalizują reakcje utleniania i redukcji,
EC 2 transferazy: przenoszą grupy funkcyjne,
EC 3 hydrolazy: katalizują hydrolizę różnych wiązań,
EC 4 liazy: rozcinają różne wiązania na drodze innej niż hydroliza czy utlenianie,
EC 5 izomerazy: katalizują zmiany izomeracyjne cząsteczek,
EC 6 ligazy: łączą cząsteczki wiązaniami kowalencyjnymi.
Nazewnictwo/klasyfikacja enzymów EC
• EC1
oksydoreduktazy
-‐ AH
2
+ B → A + BH
2
;
• EC2
transferazy
-‐ AB + C → A + BC;
• EC3
hydrolazy
-‐ AB + H
2
O → A + B;
• EC4
liazy
-‐ AB → A + B;
• EC5
izomerazy
-‐ AB → BA;
• EC6
ligazy
-‐ A + B → AB;
E.C. 1.1.1.1 (E.C. – kod enzymu)
Pierwsza liczba -‐ klasa enzymu lub grupa
Druga liczba – grupa utleniona w donorze
Trzecia liczba – akceptor
Czwarta liczba – nazwa systematyczna (wskazuje działanie)
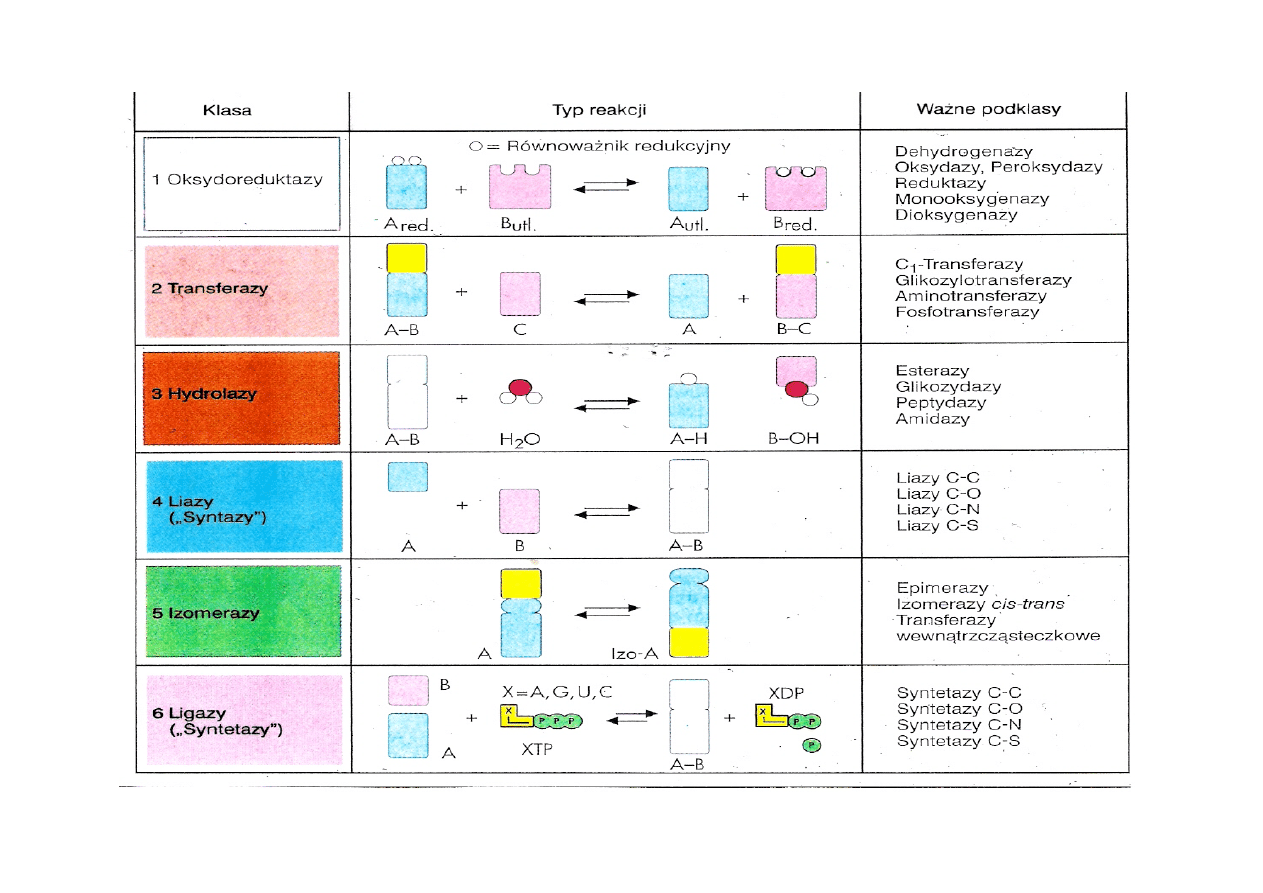

Nazewnictwo/klasyfikacja enzymów EC
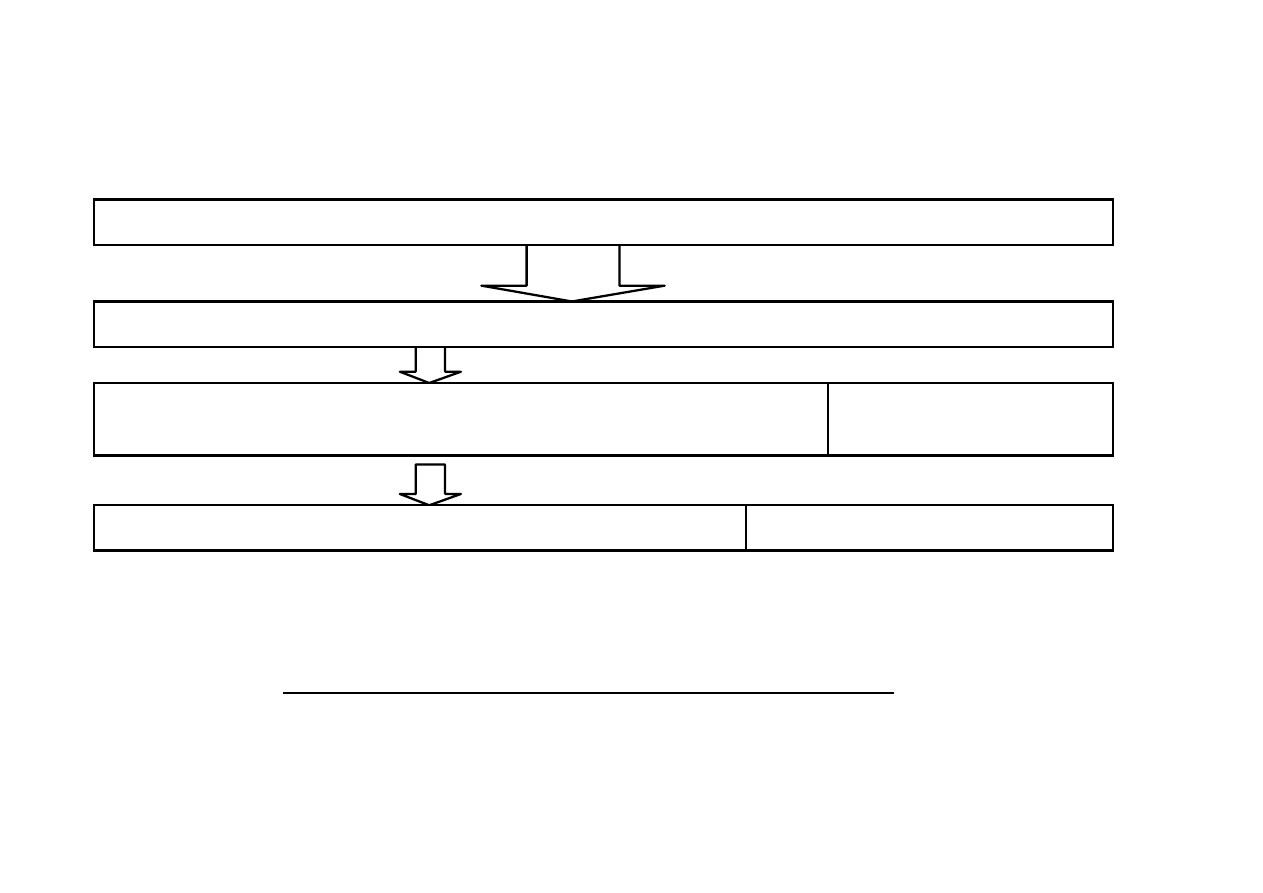
Ok. 4-5%
Oko!o 4100 enzymów sklasyfikowanych
Ponad 80% to enzymy hydrolityczne
20% inne klasy g!ównie
oksydoreduktazy
70% to proteinazy i amylazy
30% inne hydrolazy
Oko!o 100 – 130 enzymów znalaz!o zastosowanie w technologii "ywno#ci
Najważniejsze enzymy w technologii żywności
Jedynie ligazy nie znalazły do tej pory bezpośredniego zastosowania przemysłowego, lecz
są przydatne w inżynierii genetycznej.
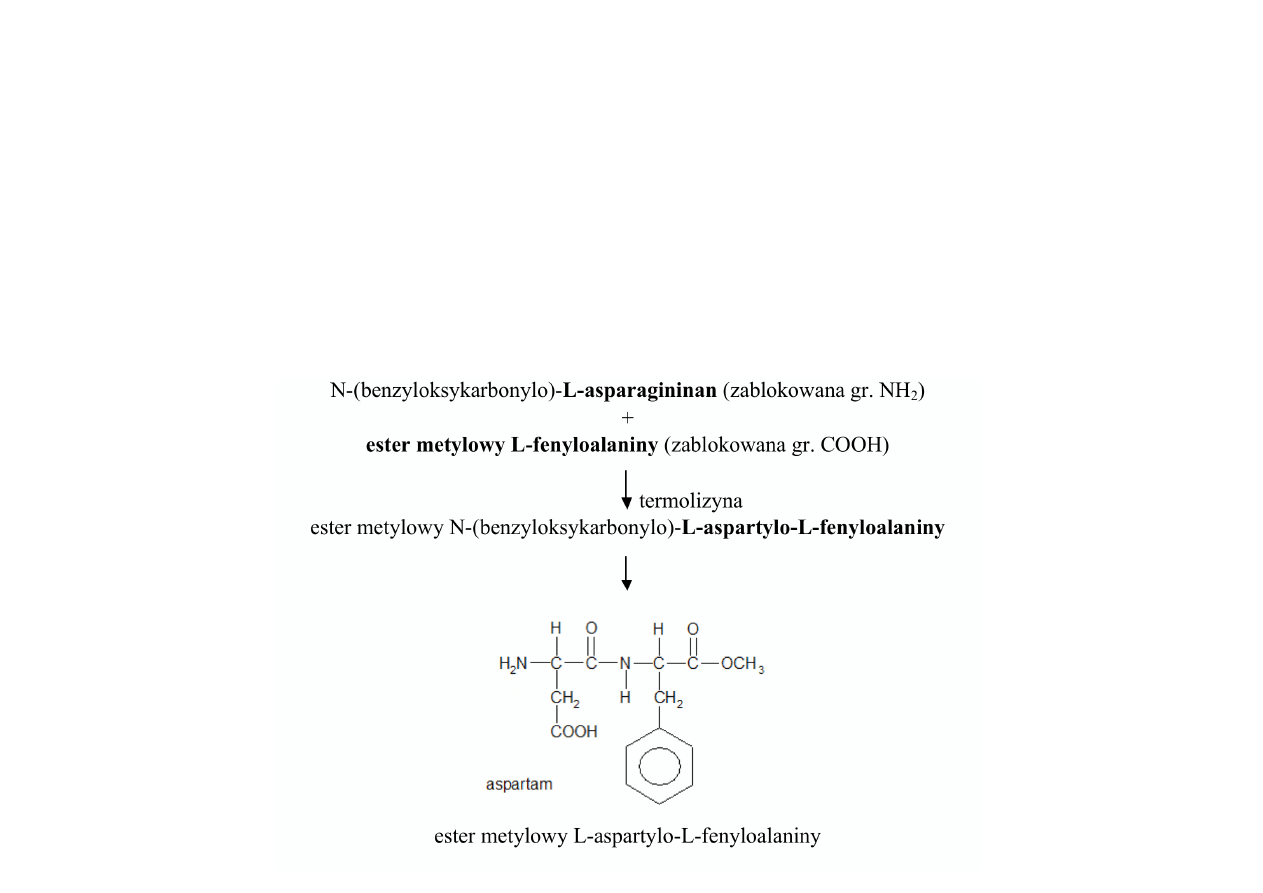
TERMOLIZYNA -‐ hydrolza
termostabilna metaloendoproteina (endoproteinaza) (Zn, Ca) z Bacillus
thermoproteoly1cus,
-‐ preferuje hydrolizę wiązań peptydowych Aa/Leu, Aa,Phe,
-‐ katalizuje też syntezę wiązań peptydowych na drodze kondensacji hydrolitycznej,
w większości przypadków reakcje katalizowane przez enzym są ODWRACALNE
(synteza wiązań peptydowych).
Aspartam – zmetylowany dipeptyd
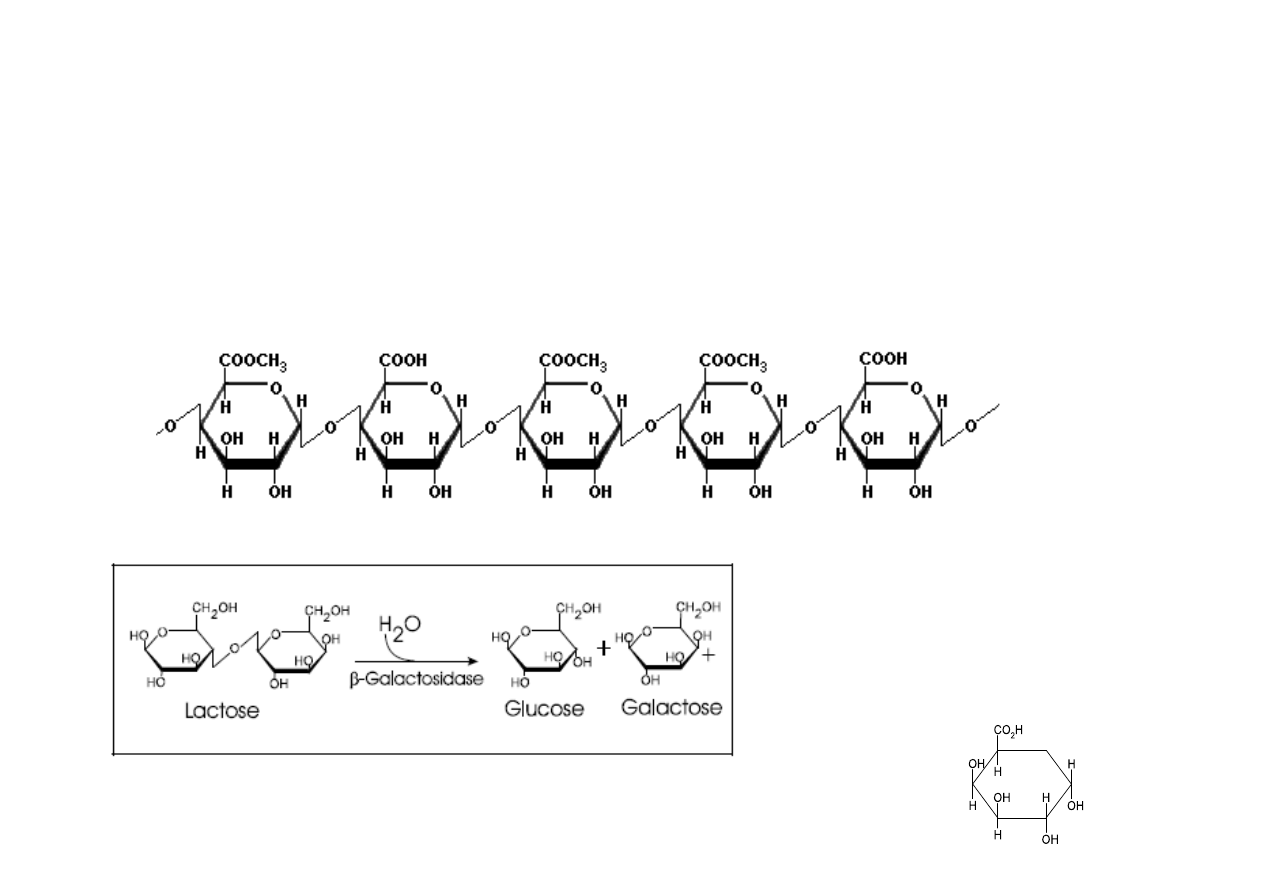
PEKTYNAZY – hydrolazy
hydrolizują wiązania glikozydowi w pektynach,
ułatwiają uwalnianie soków z miazgi, klarowanie soków (usuwanie zmętnień
pektynowych),
pektyny są heteropolisacharydami, składają się głównie z połączonych ze sobą
wiązaniami α–1,4– glikozydowymi jednostek kwasu D–galakturonowego, w
znacznej części zestryfikowanych gr. metylowymi,
!
kwas galakturonowy – powstaje na skutek utleniania α–D–galaktozy,
posiada grupę aldehydową przy C1 i karboksylową przy C6.
β–D–galaktozydaza – hydrolaza
(usuwanie laktozy z mleka
)
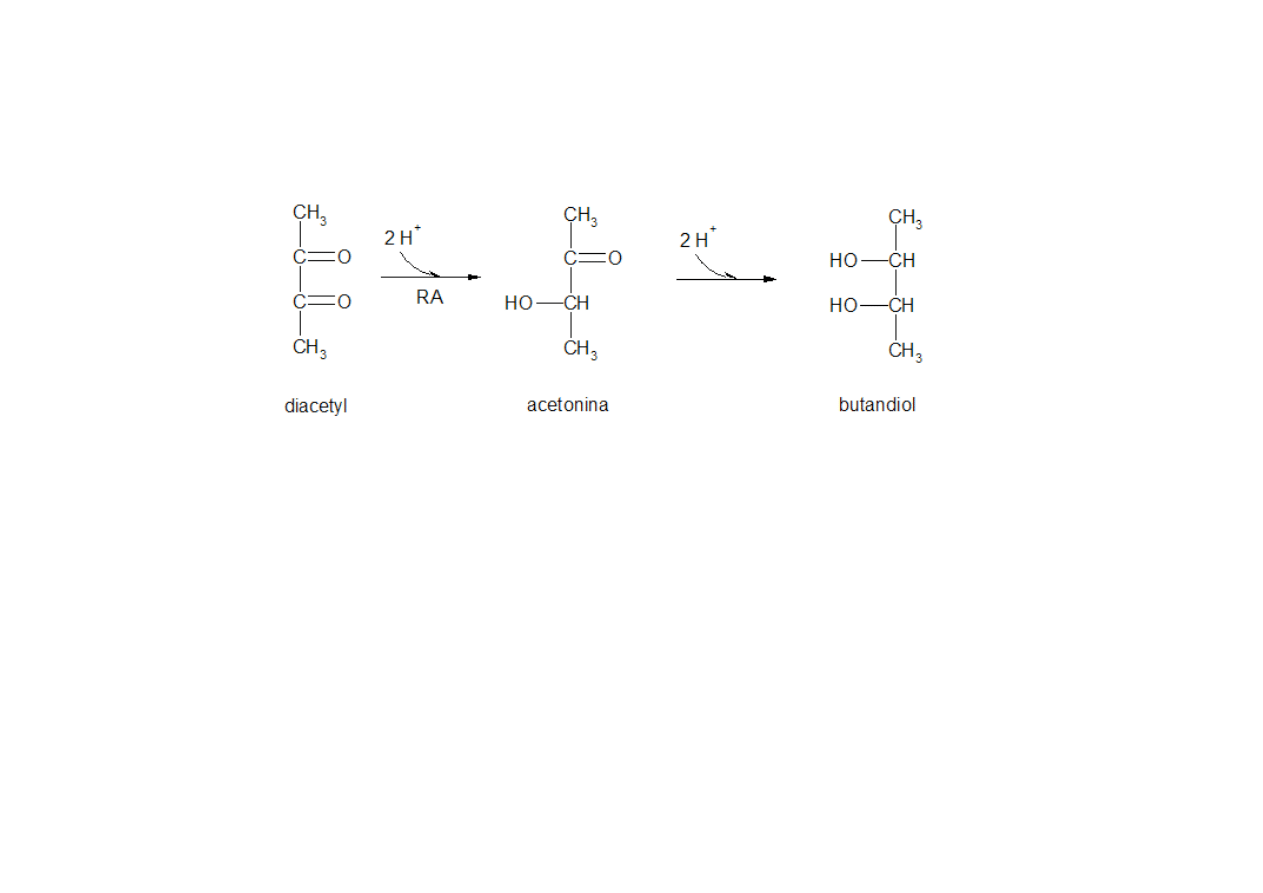
Reduktaza diacetylowa (RA) – oksydoreduktaza
Diacetyl + NADH + H
+
↔ NAD + Acetoina
!
Diacetyl (produkcja piwa)
-‐ diketon o nazwie systematycznej 2,3-‐butandion, zapachu maślanym, znajduje się
w piwie jako produkt uboczny fermentacji przez drożdże, przy odpowiednim
stężeniu wykazuje korzystne właściwości – pozwala dłużej odczuwać w ustach
smak piwa,
-‐ w stężeniu większym niż 0,2 mg/l nadaje piwu niekorzystny „maślany posmak”,
powstaje w wyniku przetwarzania cukrów przez drożdże, czasami bakterie w
procesie fermentacji,
-‐ w czasie leżakowania piwa te same drożdże redukują diacetyl do obojętnych
smakowo produktów (acetoina, butandiol).
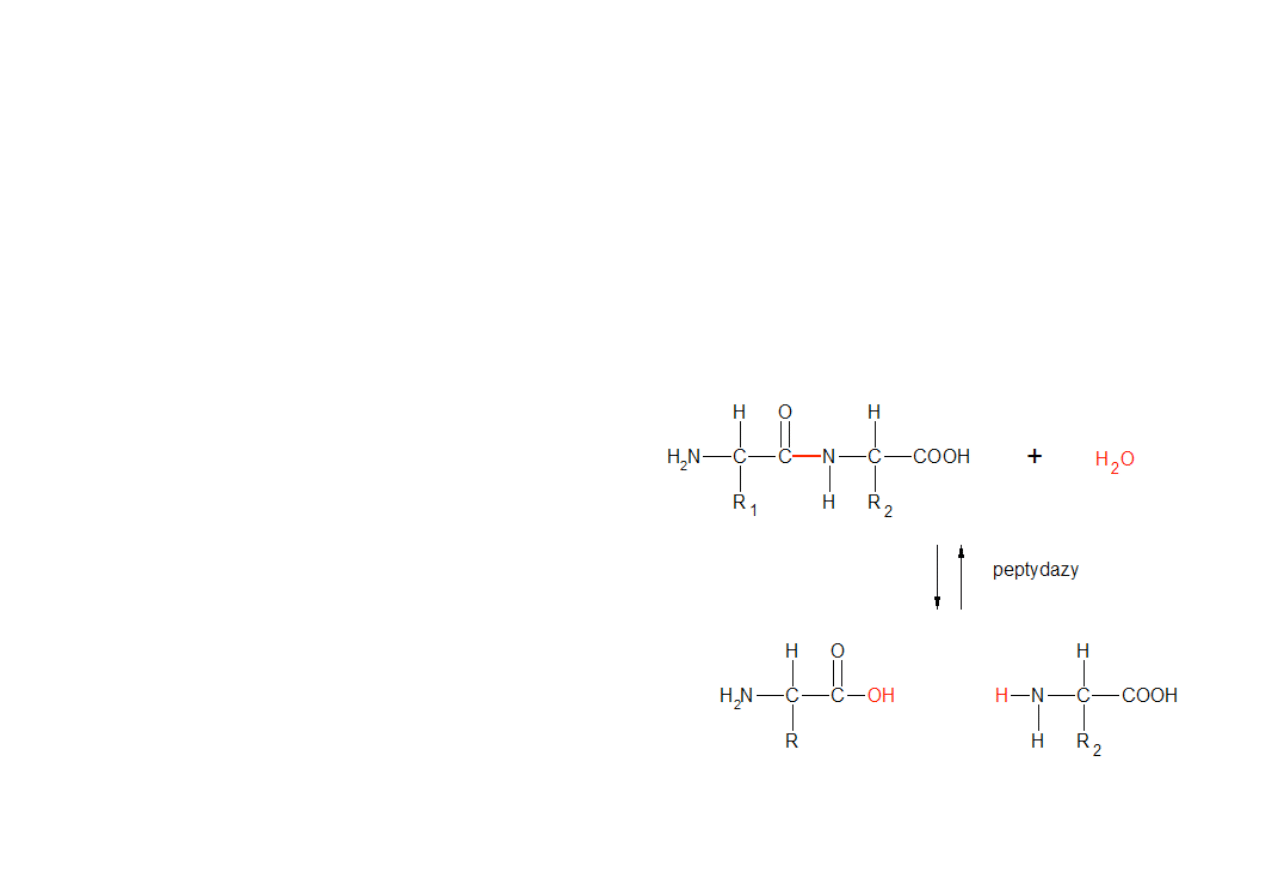
!
PEPTYDAZY (enzymy proteolityczne, proteazy
)
-‐ katalizują hydrolizę wiązań peptydowych w białkach i peptydach (podstawowe
zadanie),
-‐ należą do klasy 3 – hydrolaz,
-‐ niektóre z nich katalizują ponadto hydrolizę wiązań estrowych i amidowych oraz
reakcję transpeptydacji i transamidacji,
-‐ w odpowiednich warunkach niektóre peptydazy mogą ponadto syntetyzować
wiązanie peptydowe.
Peptydazy – niska specyficzność
substratowa, jednakże charakteryzują
się wybiórczością w stosunku do
położenia rozkładanego wiązania w
łańcuchu
polipeptydowym
oraz
swoistością w stosunku do hydrolizy
wiązań
pomiędzy
określonymi
aminokwasami.

PEPTYDAZY -‐ klasyfikacja
Egzopeptydazy -‐ EC 3.4.11-‐19 (odcinają 1 lub 2 aminokwasy od końca N lub C)
aminopeptydazy EC 3.4.11: odcinające pojedyncze aminokwasy od końca
aminowego,
karboksypeptydazy EC 3.4.16-‐18: odcinające pojedyncze aminokwasy od końca
karboksylowego,
dipeptydazy EC 3.4.14: hydrolizują wiązania peptydowe w dwupetydach,
dwupeptydylo-‐peptydazy lub tripeptydylo-‐peptydazy: odszczepiają jednostki
dwupetydowe lub tripeptydowe od końca N (EC 3.4.14) lub
końca C (EC
3.4.15),
omega peptydazy EC 3.4.19: odcinające różnie podstawione reszty
aminokwasowe.
Egzopeptydazy ważne dla przemysłu spożywczego:
Aminopeptydazy i karboksypeptydazy
Lactococcus lac1s
Aspergillus sp.
Rhizopus oryzae
Zastosowanie: usuwanie gorzkiego smaku z hydrolizatów białkowych, także przy
produkcji sera.

PEPTYDAZY -‐ klasyfikacja
Endopeptydazy (proteinazy) – EC 3.4.21-‐24, EC 3.4.99 (hydrolizują wiązania
wewnątrz łańcucha polipeptydowego)
Na podstawie budowy centrum, wrażliwości na inhibitory oraz mechanizm katalizy
wyróżniono:
serynowe EC 3.4.21
seryna oraz histydyna w centrum aktywnym,
są hamowane przez DFP (diizopropylofluorofosforan)
cysteinowe EC 3.4.22
cysteina i histydyna w centrum aktywnym, wrażliwość na czynniki utleniające,
hamowane przez PCMB (p-‐Chloromercuribenzoic Acid) – reakcja z grupami -‐SH
aspartylowe EC 3.4.23
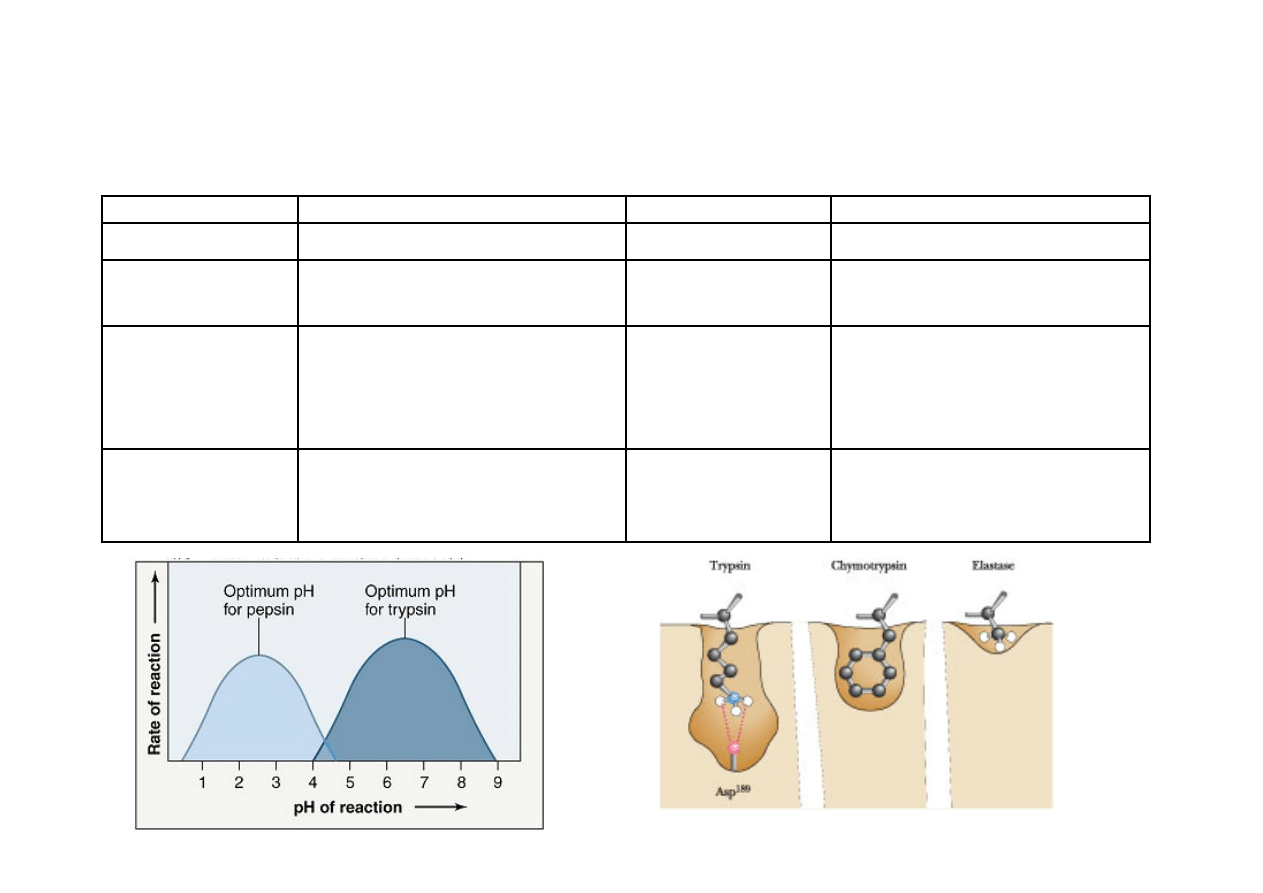
dwie reszty asparaginianu w centrum aktywnym, aktywność przy niskim pH 1.5-‐5
metaloproteinazy EC 3.4.24
inhibicja przez EDTA
Enzym
EC numer
Preferencyjna hydroliza
x
Serynowe proteazy
chymotrypsyna
trypsyna
subtylizyna
3.4.21
3.4.21.1
3.4.21.4
3.4.21.12
Tyr-, Trp-, Phe-, Leu-
Arg-, Lys-,
G!ównie hydrofobowe
Cysteinowe proteazy
Katepsyna B*
Papaina*
Ficyna*
Bromalina*
3.4.22
3.4.22.1
3.4.22.2
3.4.22.3
3.4.22.32-33
Arg-Arg-, Lys-, Phe-X-
Arg-, Lys-, hydrofobowe-X-
Phe-, Tyr-
Lys-, Arg-, Phe-, Tyr-
Aspartylowe proteazy
Pepsyna
Chymozyna#
3.4.23
3.4.23.1
3.4.23.4
Phe-, Tyr-, Leu-, Asp-, Glu-
Phe1
05
-Met
106
w "-kazeinie
Metaloproteazy
Termolizyna
Neutralne proteinazy
3.4.24
3.4.24.27
3.4.24.28
Ile-, Leu-, Val-, Phe-,
Leu-, Phe-, i inne
Endopeptydazy o znaczeniu przemysłowym
* szeroka specyficzność w stosunku do aminokwasów hydrolizowanego wiązania peptydowego
# specyficzność podobna do pepsyny
x preferencyjna hydroliza
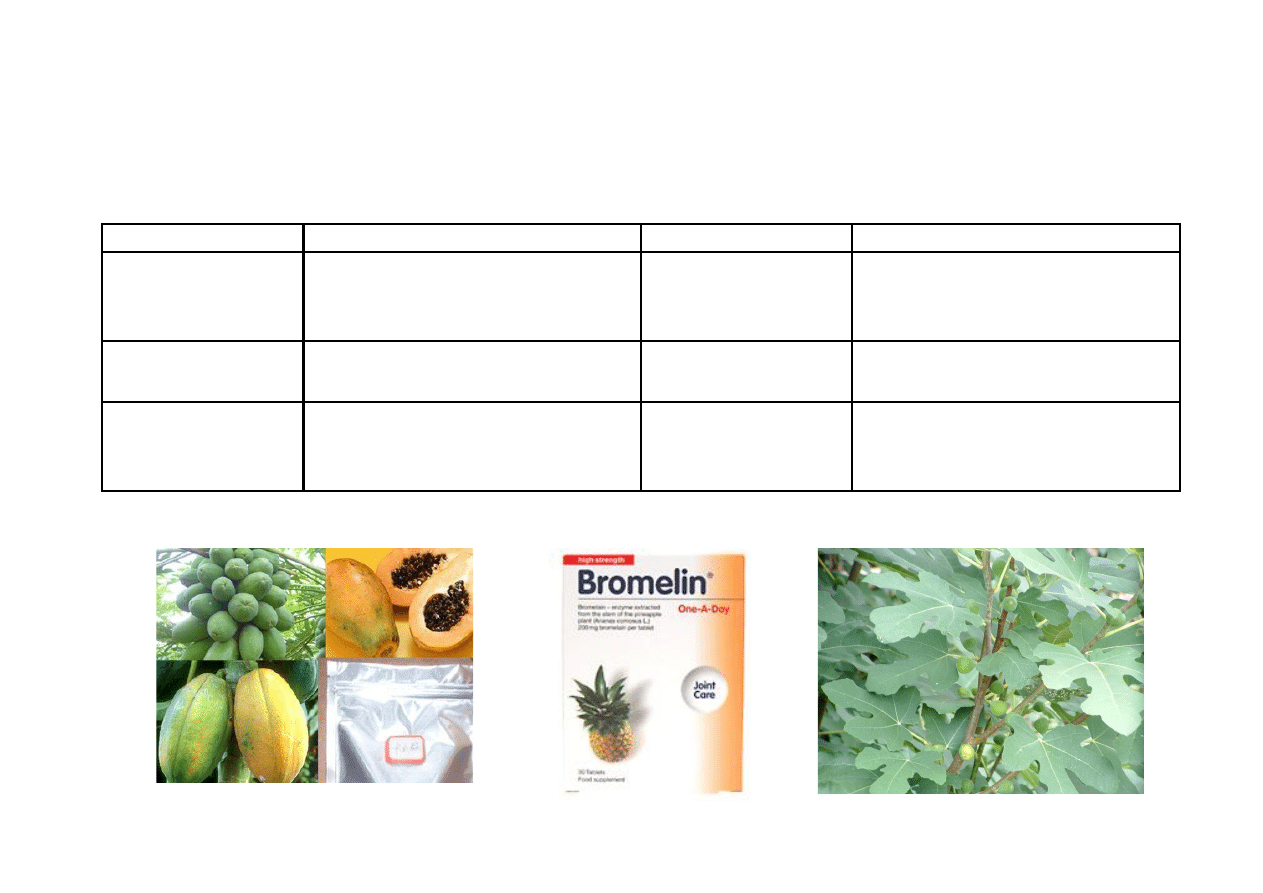
Otrzymywanie i zastosowanie peptydaz roślinnych
Papaina, bromelina, ficyna -‐ wewnątrzkomórkowe proteazy cysteinowe, opymum
pH 5-‐7
Enzym
!ród"o
Skala produkcji
G"ówne zastosowanie
Papaina
Sok z niedojrza!ych owoców
papai
(Carica papaya)
> 10 t/rok
Kruszenie mi"sa, browarnictwo
– usuwanie zm"tnienia piwa
Bromelina
Sok (lateks) z pnia ananasa
< 1 t/rok
Browarnictwo,
kruszenie mi"sa
Ficyna
Sok z niektórych odmian drzew
figowych
g!. Ficus glabrata
< 1 t/rok
Modyfikacja sk!adników
#ywno$ci

Komercyjne otrzymywanie papiny
Zebranie mleczka kauczukowego z niedojrzałych owoców papai
-‐ (nacięcie rano, z 1 drzewa 1 l rocznie, mleczko przypomina wyglądem mleko
krowie, po kilku minutach po wypływie z naciętego owocu ścina się i tworzy żel)
Sch!odzenie
Mieszanie mechaniczne " #el w p!yn
Wst$pna filtracja i odwirowanie
Ultrafiltracja
Klarowny i przezroczysty przes%cz zag$szcza si$ w pró#ni
oraz suszy w suszarni rozpy!owej
Mielenie na proszek i pakowanie
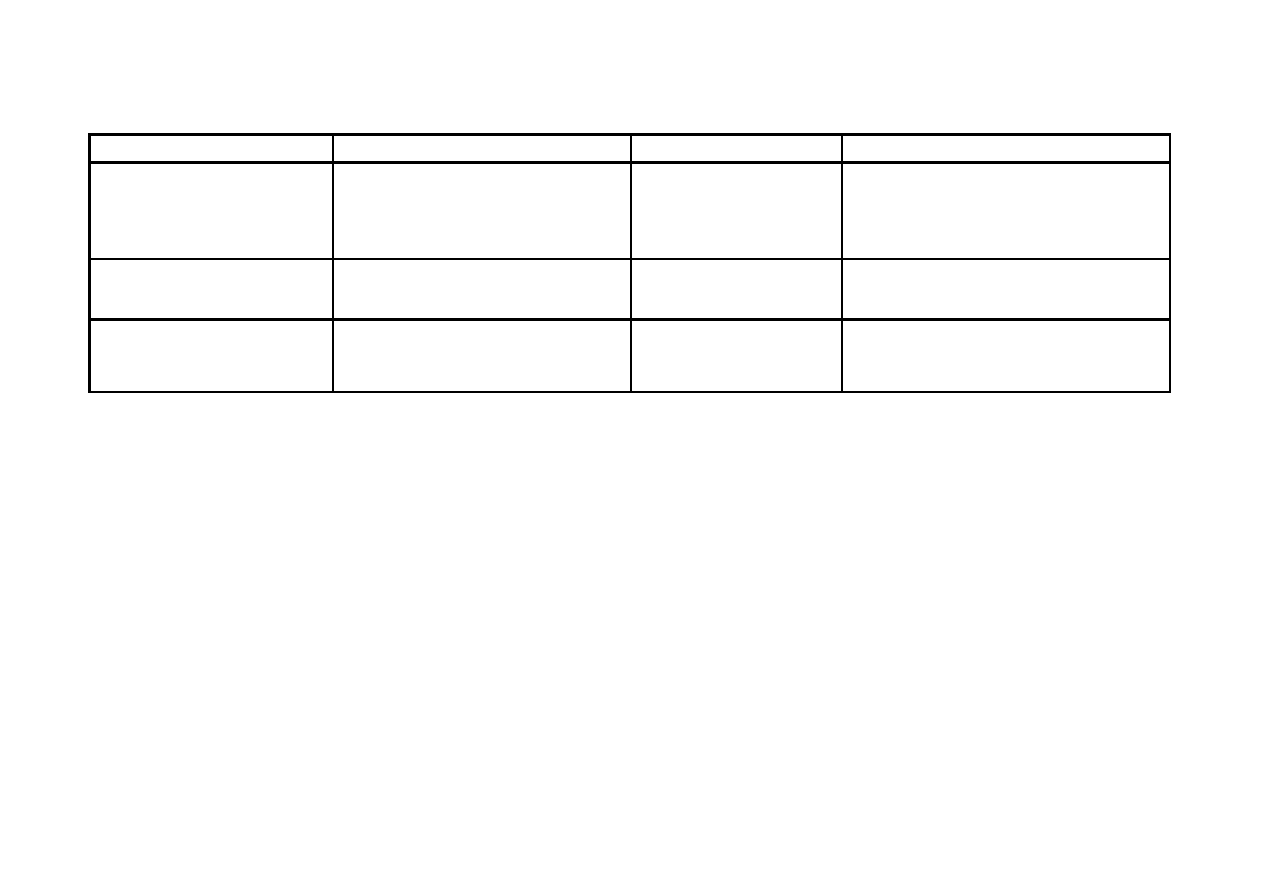
Otrzymywanie i zastosowanie peptydaz zwierzęcych
Zewnątrzkomórkowe enzymy trawienne:
Enzym
!ród"o
Skala produkcji
G"ówne zastosowanie
Chymozyna
!o"#dek m"odych cielaków
> 1 t/rok
Serowarstwo
Pepsyna
!o"#dek $wini
< 1 t/rok
Modyfikacja sk"adników
%ywno$ci, serowarstwo
Trypsyna
Trzustka $wini lub byd"a
< 1 t/rok
Modyfikacja sk"adników
%ywno$ci,
hydrolizaty bia"kowe,
odw"asianie skór
Chymotrypsyna
Trzustka $wini
< 1 t/rok
Modyfikacja sk"adników
%ywno$ci,
odw"asianie skór

Rozdrobnienie i mielenie surowca (wy!ció"ko #o"$dka !wini)
Autoliza !luzówki #o"$dka w obecno!ci HCl
Usuni%cie t"uszczu heksanem
Wysolenie sol$ lub izopropanolem
Rozpuszczenie w wodzie
Filtrowanie, suszenie sublimacyjne (45-55
o
C) w pró#ni
(odparowanie heksanu i izopropanolu)
Mielenie na proszek i pakowanie
Komercyjne otrzymywanie pepsyny przemysłowej
Enzym
!ród"o
Skala produkcji
G"ówne zastosowanie
Neutralne peptydazy
Bacillus subtilis
> 100 t/rok
Hydrolizaty bia!kowe, dodatek
do proszków do prania,
browarnictwo
Kwa"ne peptydazy g!.
koagulaty bia!ek mleka
Rhizmucor miehei
> 10 t/rok
Serowarstwo
Kwa"ne peptydazy
Aspergillus niger,
Aspergillus oryzae
> 1 t/rok
Piekarnictwo,
wytrawianie skór
Otrzymywanie peptydaz z mikroorganizmów
Neutralne proteinazy Bacillus sub1lis; proteinazy serynowe, metaloproteinazy.
Podpuszczka – handlowa nazwa zalecana dla preparatów z żołądków przeżuwaczy
zawierająca głównie chymozyną i w niewielkim stopniu pepsynę (Międzynarodowa
Federacja Mleczarska).
Peptydazy pochodzenia mikrobiologicznego zdolne do koagulacji białek mleka zaleca się
nazywać koagulantami białek mleka.
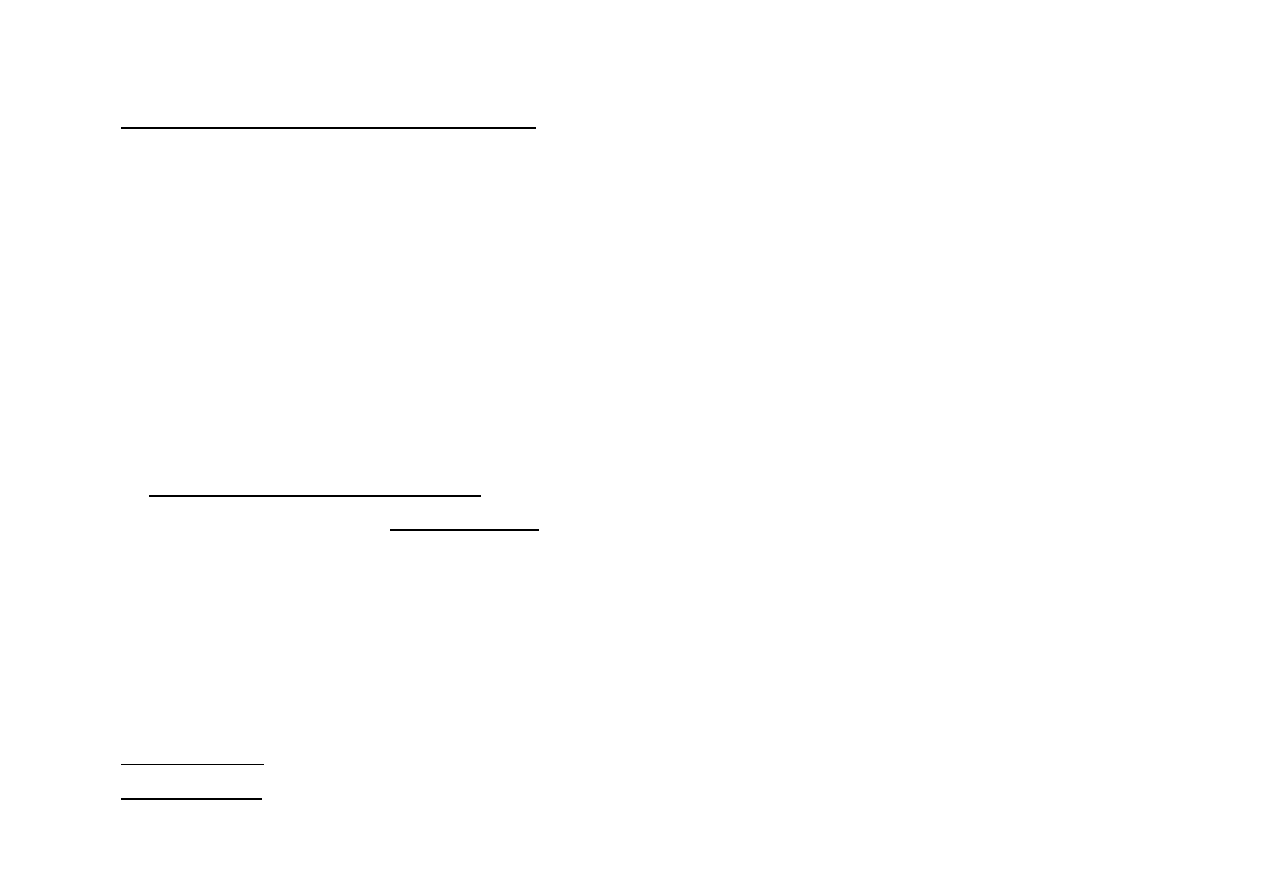
Hydrolizaty bialkowe
Produkcja hydrolizatów białkowych odbywa się w wyniku enzymatycznej lub kwasowej/
zasadowej hydrolizy białek)
Enzymatyczne modyfikacja składu i właściwości białek -‐ hydrolizaty białkowe
Enzymatyczna hydroliza białek nie powoduje rozkładu aminokwasów, jest bardziej
specyficzna od hydrolizy kwasowej i alkalicznej białek.
W wyniku częściowej proteolizy
Zmieniają się reologiczne, fizyczne, chemiczne właściwości białek,
Powstają charakterystyczne cechy smakowe i zapachowe produktów.
np. hydrofobowe aminokwasy schowane wewnątrz cząsteczki białka zostają odsłonięte,
najczęściej powstaje gorzki smak, zwiększa się rozpuszczalność, obniża napięcie
powierzchniowe, zwiększa się zdolność do emulgowania tłuszczów (tworzenia emulsji) i
tworzenia piany, wzrasta strawność i przyswajalność produktu.
Gdy jednak zbyt długo prowadzi się hydrolizę to właściwości emulgujące i tworzenia piany
mogą spadać.
Hydrolizaty białek na skalę przemysłową otrzymuje się z:
białek mleka (kazeiny, albuminy, białka serwatkowe),
białek mięsa, soi, glutenu pszenicy, fibrynogenu lub kolagenu.

Hydrolizaty białkowe – zastosowanie
Jako koncentraty spożywcze i przyprawowe, np. zupy instant, sosy sojowe,
przyprawy do pieczenia mięsa, buliony mięsne w proszku,
Dodatki do żywności wytwarzające i stabilizujące pianę, emulgujące tłuszcze,
modyfikujące smak, poprawiające teksturę i ułatwiające krojenie, np. do parówek,
Do otrzymywania żywności przeznaczenia specjalnego:
-‐ odżywki dla niemowląt,
-‐ preparaty odchudzające,
-‐ odżywki białkowe dla sportowców,
-‐ odżywki o obniżonej alergenności dla dzieci „atopowych” oraz z zaburzeniami
-‐ wchłaniania i trawienia o podłożu immunologicznym, niealergizującym,
Wzbogacanie produktów w białko, np. chleba i żywności specjalnej.
Laktoalbumina zawarta w białku serwatkowym mleka krowy oraz albumina jaja
zostały uznane za białka o najwyższej wartości odżywczej przez FAO/WHO (nie
tylko zawartość egzogennych aminokwasów, ale i proporcje aminokwasów
egzogennych do endogennych) => ale RYZYKO REAKCJI ALERGICZNYCH!!!

PROCES PLASTEINOWANIA
Proces plasteinowania, jako przykład polepszania jakości białek
Enzymatyczna reakcja resyntezy wiązań peptydowych (w konkretnych warunkach),
Enzymatyczne
przeprowadzanie
hydrolizatów
białkowych
w
peptydy
wielkocząsteczkowe, nierozpuszczalne w 10% TCA o konsystencji żelu nazwanego
„plasteiną”.
Proces dwuetapowy:
ETAP 1: polega na częściowej hydrolizie wiązań peptydowych białek przy użyciu
proteinaz, takich jak pepsyna, papaina, α-‐chymotrypsyna.
ETAP 2: otrzymany uprzednio hydrolizat białkowy (mieszanina peptydów), po
zatężeniu, poddaje się reakcji plasteinowania katalizowanej przez enzymy, takie
same bądź inne niż stosowane w procesie hydrolizy, lecz przy pH innym niż w
procesie hydrolizy w wyniku, czego otrzymuje się plasteinę charakteryzującą się, w
porównaniu z białkiem wyjściowym, lepszym składem jakościowym oraz obniżoną
zawartością substancji antyżywieniowych.
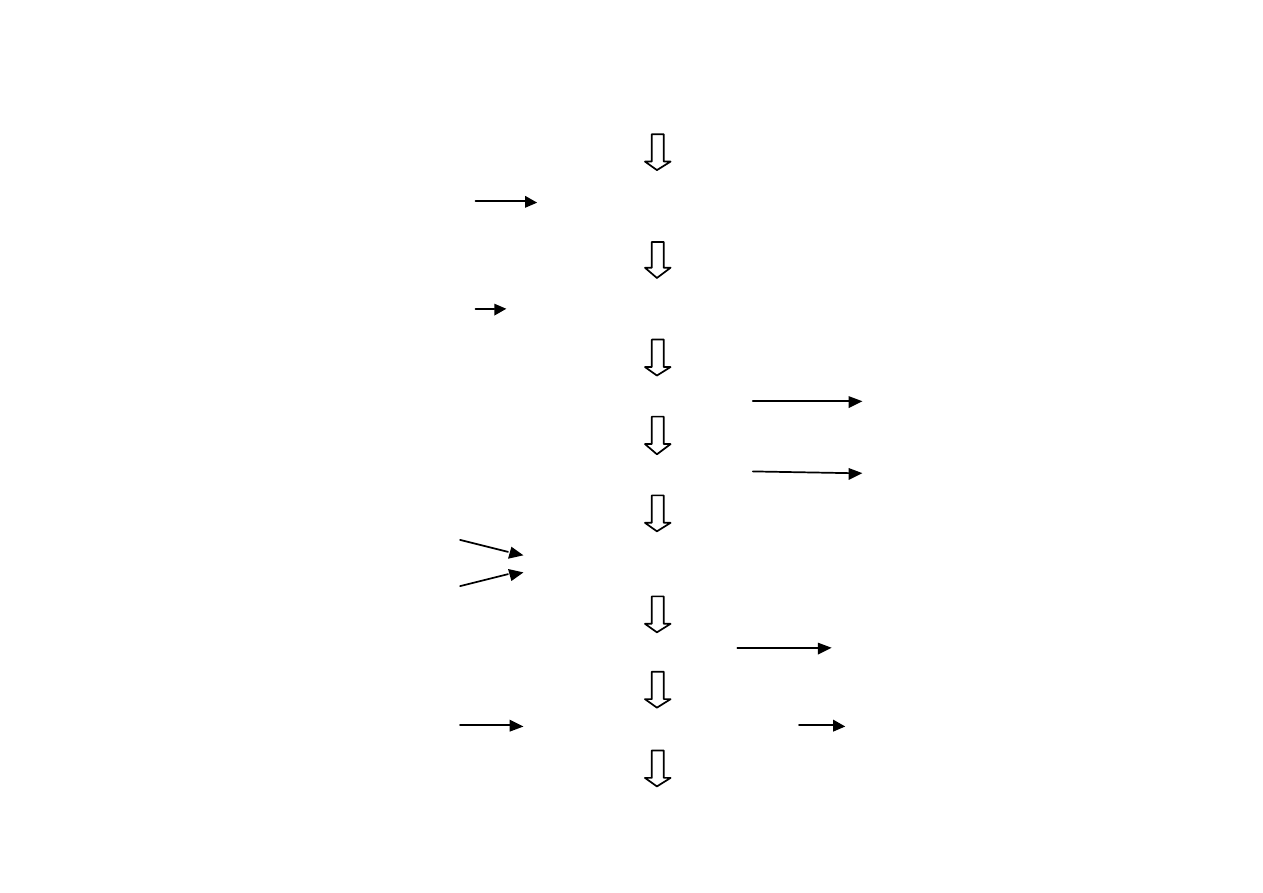
Schemat technologiczny otrzymywania plastein
Plasteiny o po!"danym sk#adzie
aminokwasowym
Hydroliza wi"za$ estrowych
Zag%szczenie
Cz%&ciowa hydroliza
do peptydów
Odszczepienie niepo!"danych
aminokwasów
Roztwór bia!ek
Endopeptydaza,
np. pepsyna
Egzopeptydaza
Rozdzielenie
Niepo!"dane
aminokwasy
Woda
Reakcja plasteinowa w 50 %
roztworze substratów
Estry etylowe po!"danych
aminokwasów
Rozpuszczalnik
organiczny
Rozdzielenie
Frakcja zwi"zków
ma#ocz"steczkowych
Alkohol etylowy
NaOH

KIERUNKI WYKORZYSTYWANIA REAKCJI PLASTEINOWANIA
-‐ wbudowywanie aminokwasów egzogennych w białka, np. gluten (białko
zapasowe zbóż) w lizynę, zeinę w lizynę, tryptofan,
-‐ usuwanie niepożądanych aminokwasów w przypadku szczególnych diet, np. w
fenyloketonurii konieczne jest wyeliminowanie z produktów fenyloalaniny (do
produkcji hydrolizatów wykorzystywane są rybny koncentrat białkowy i białko
sojowe),
-‐ usuwanie gorzkiego smaku hydrolizatów białkowych – usunięcie aminokwasów
hydrofobowych lub ich ukrycie wewnątrz długich łańcuchów plastein,
-‐ usuwanie właściwości alergennych białek – usunięcie części epitopów (z końca N
lub C) ,
-‐ rozbicie epitopów lub ich ukrycie wewnątrz łańcuchów plastein => konieczność
poznania sekwencji aminokwasowych uczulających.

ZASTOSOWANIE PEPTYDAZ
PIEKARNICTWO
-‐ rozluźnienie zbyt mocnego białka glutenowego mąki, co prowadzi do skrócenia
czasu wyrabiania ciasta,
-‐ polepsza jego pulchność i konsystencję (peptydazy grzybowe i bakteryjne),
BROWARNICTWO
-‐ podczas przerobu zbożowych surowców niesłodowanych w celu zapewnienia
odpowiednich właściwości organoleptycznych (zapachu, pienistości, klarowności)
=> stabilizacja piwa (szczególne znaczenie przy schładzaniu piwa),
-‐ przy słodowaniu jęczmienia i w początkowej fazie zacierania słodu => odpowiedni
stopień rozkładu substancji białkowych,
PRZEMYSŁ MIĘSNY
-‐ przyspieszenie procesu dojrzewania mięsa, głównie wołowego, poprzez częściowy
rozkład ... białka włókna mięśniowego uzyskuje się poprawę konsystencji
(delikatność, kruchość), poprawę wartości odżywczej i cech organoleptycznych
=> 2-‐3 x skrócony czas dojrzewania => zwiększona strawność,
-‐ oddzielenie resztek mięsa od kości – zwiększenie odzysku białka,
-‐ zmiękczanie, odwłasianie skór,
-‐ zwiększenie wydajności ekstrakcji tłuszczu,

ZASTOSOWANIE PEPTYDAZ
PRZEMYSŁ RYBNY
-‐ dojrzewanie solonych, marynowanych śledzi (pleśnie Aspergillus),
MLECZARSTWO
-‐ koagulacja białek mleka w produkcji sera,
-‐ produkcja hydrolizatów kazeiny,
-‐ produkcja mleka sojowego, mleka w proszku,
-‐ w procesie dojrzewania sera – proces złożony, proteoliza niezbędna do uzyskania
prawidłowej struktury, głębokiego smaku,
-‐ dostarczenia aminokwasów niezbędnych do wytworzenia charakterystycznego
smaku i zapachu.

Reakcje katalizowane przez transglutaminazę
-‐ sieciowanie łańcuchów polipeptydowych.
Transglutaminaza
-‐ występuje w krwi ssaków, uczestniczy w wytwarzaniu skrzepów;
-‐ produkowana także przez drobnoustroje;
-‐ jako acylotransferaza, katalizuje reakcje łączenia reszty acylowej glutaminy
wbudowywanej w białko lub w peptyd z pierwszorzędową grupą aminową
aminokwasu wolnego lub wbudowanego w białko lub peptyd (lizyna).
O O
|| ||
bia!ko
1
-(CH
2
)
2
-C-NH
2
+ H
2
N-(CH
2
)
4
-bia!ko
2
! bia!ko
1
-(CH
2
)
2
-C-N-(CH
2
)
4
-bia!ko
2
+ NH
3
|
H
O O
|| ||
bia!ko-(CH
2
)
2
-C-NH
2
+ H
2
NR ! bia!ko-(CH
2
)
2
-C-N-R + NH
3
wolny |
aminokwas H
Jedynym producentem enzymatycznych preparatów amylolitycznych, pektynolitycznych i
proteolitycznych w Polsce są Zakłady Przemysłu Ococowo-‐Warzywnego PEKTOWIN w Jaśle.
Enzymy proteolityczne otrzymywane głównie w wyniku biosyntezy bakterii Bacillus sub1lis,
szczepu Aspergillus niger.
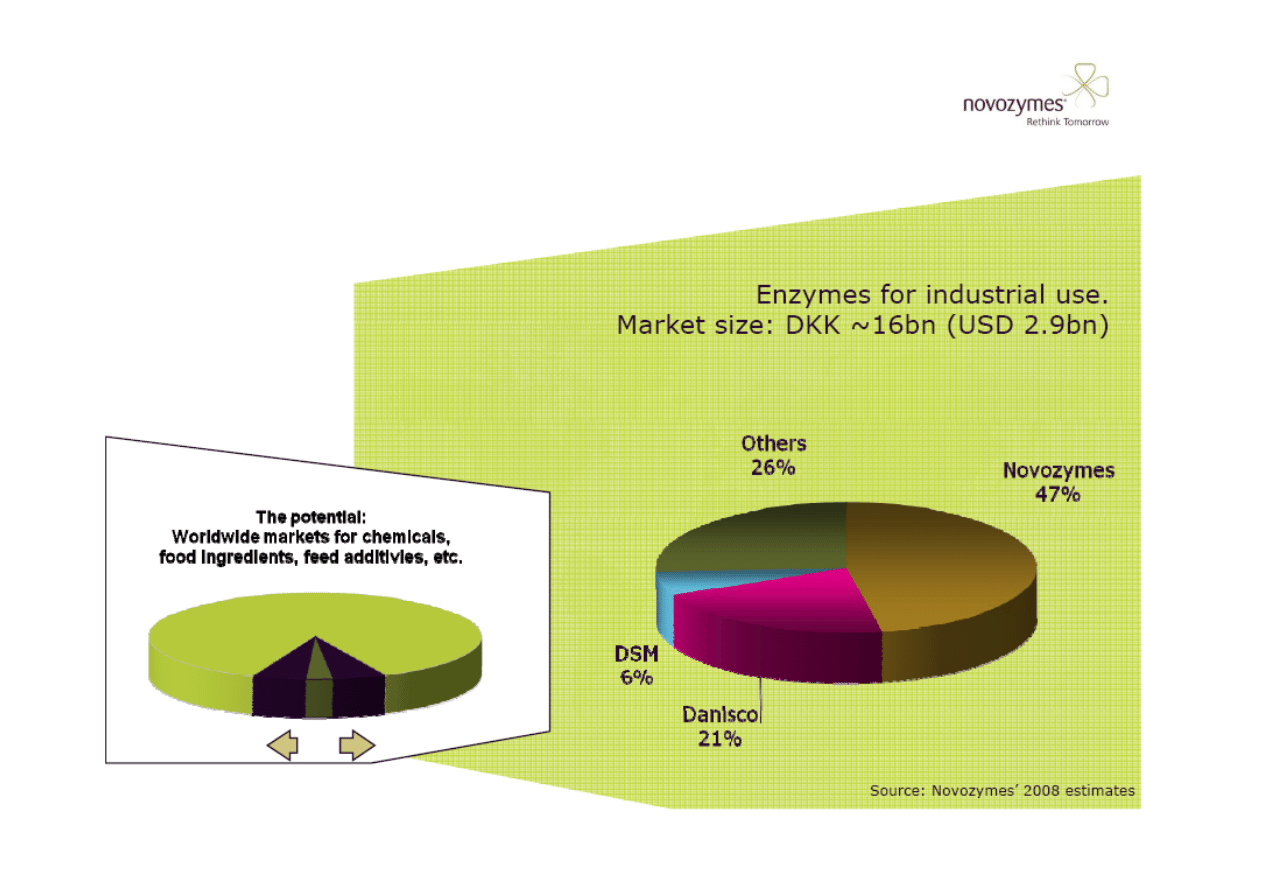
Novozymes niekwesmonowany lider produkcji enzymów

Historia firmy Novozymes

Znaczenie innowacji w rozwoju firm
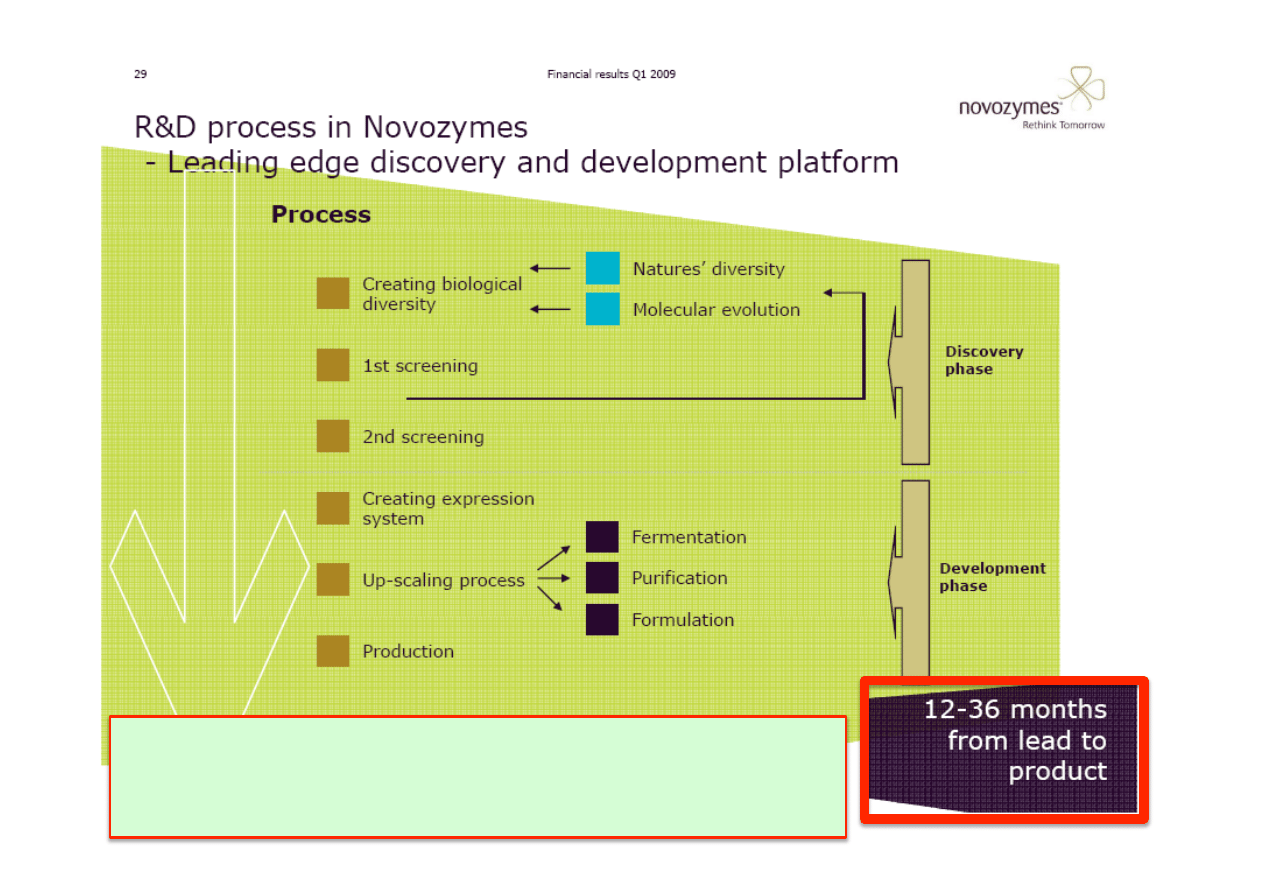
Każda nowo projektowana linia biotechnologiczna
poprzedzona jest fazą badawczą i wdrożeniową
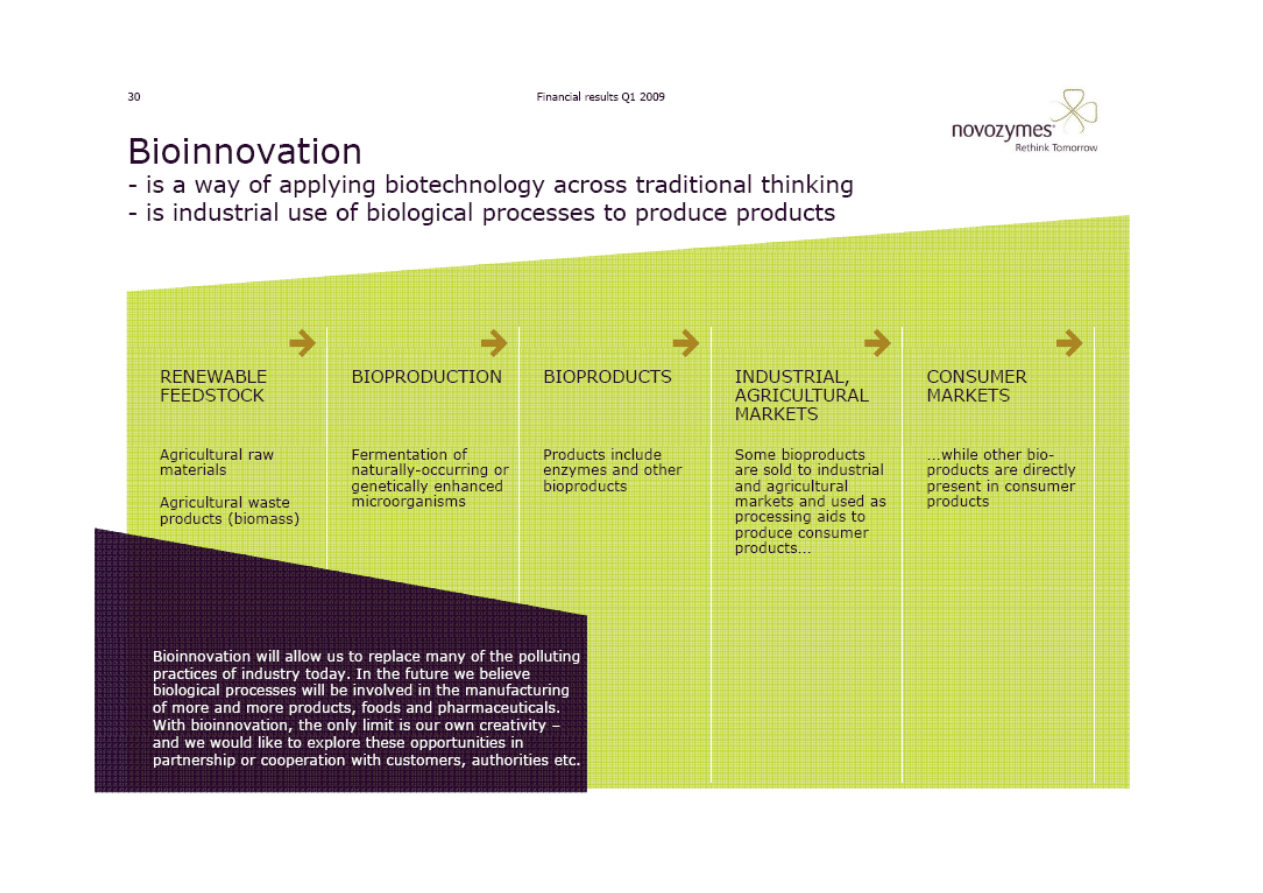
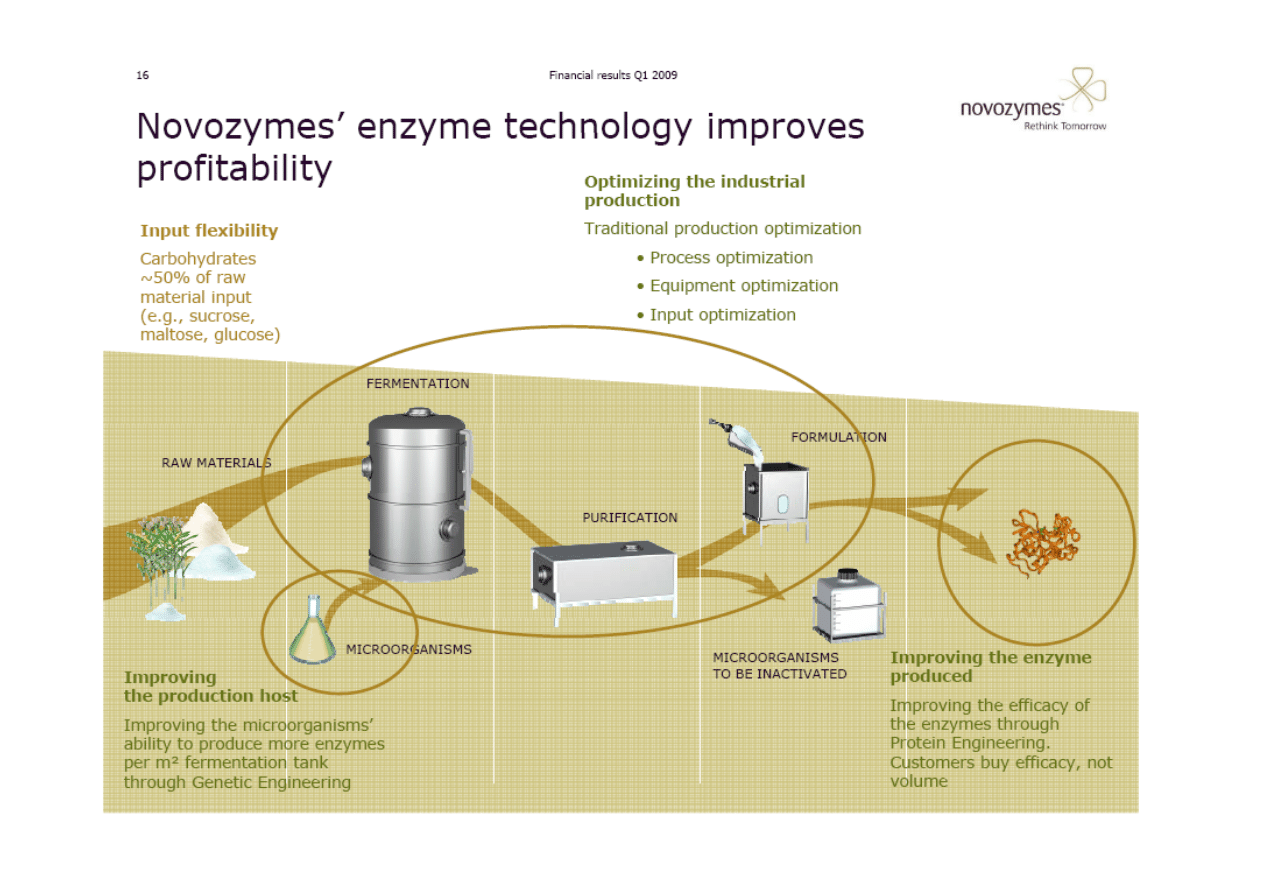

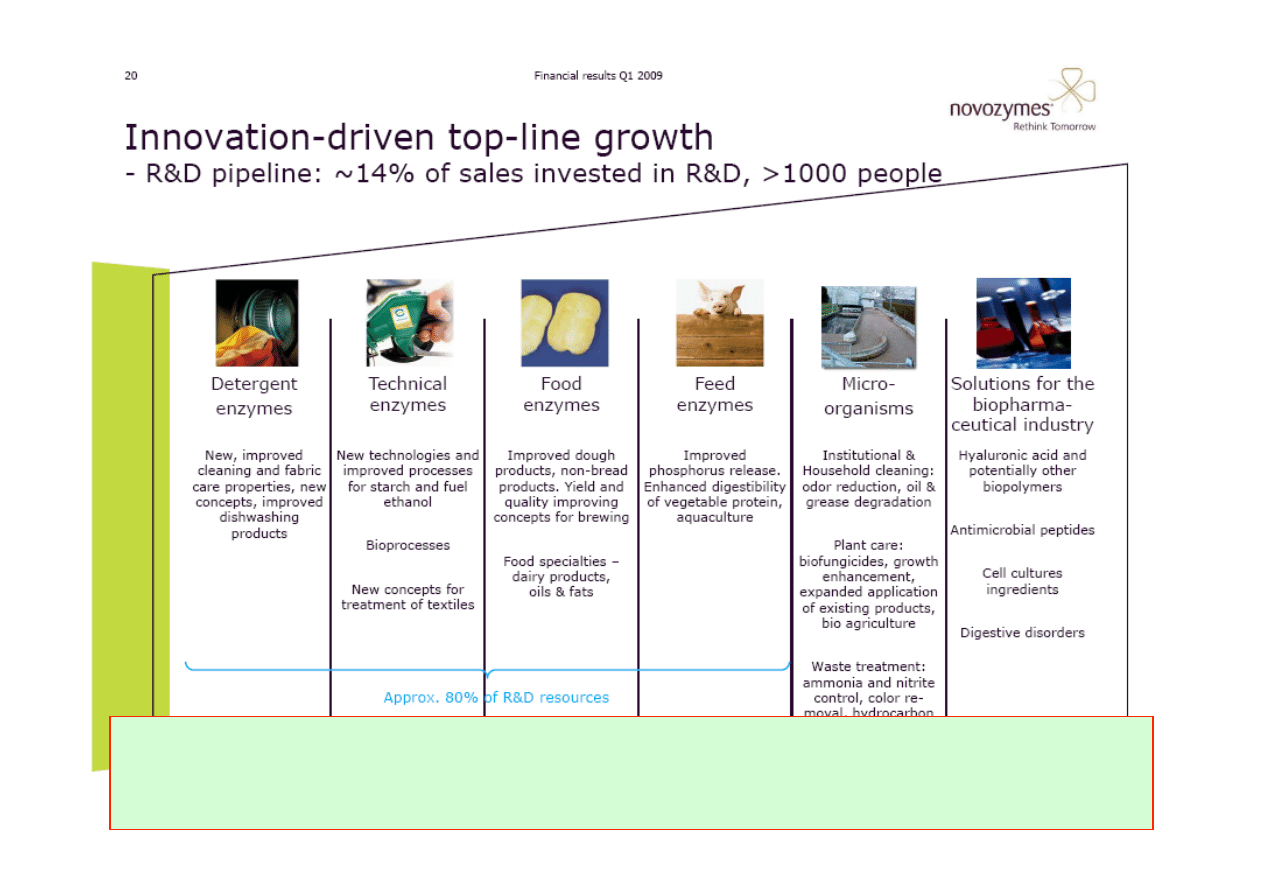
Dla dynamicznego rozwoju firmy biotechnologicznej należy zwiększać swoją zdolność
innowacyjną poprzez posiadanie własnego ośrodka badawczo-‐wdrożeniowego (od 10-‐30%
zysku ze sprzedaży powinno być inwestowane w takie badania).
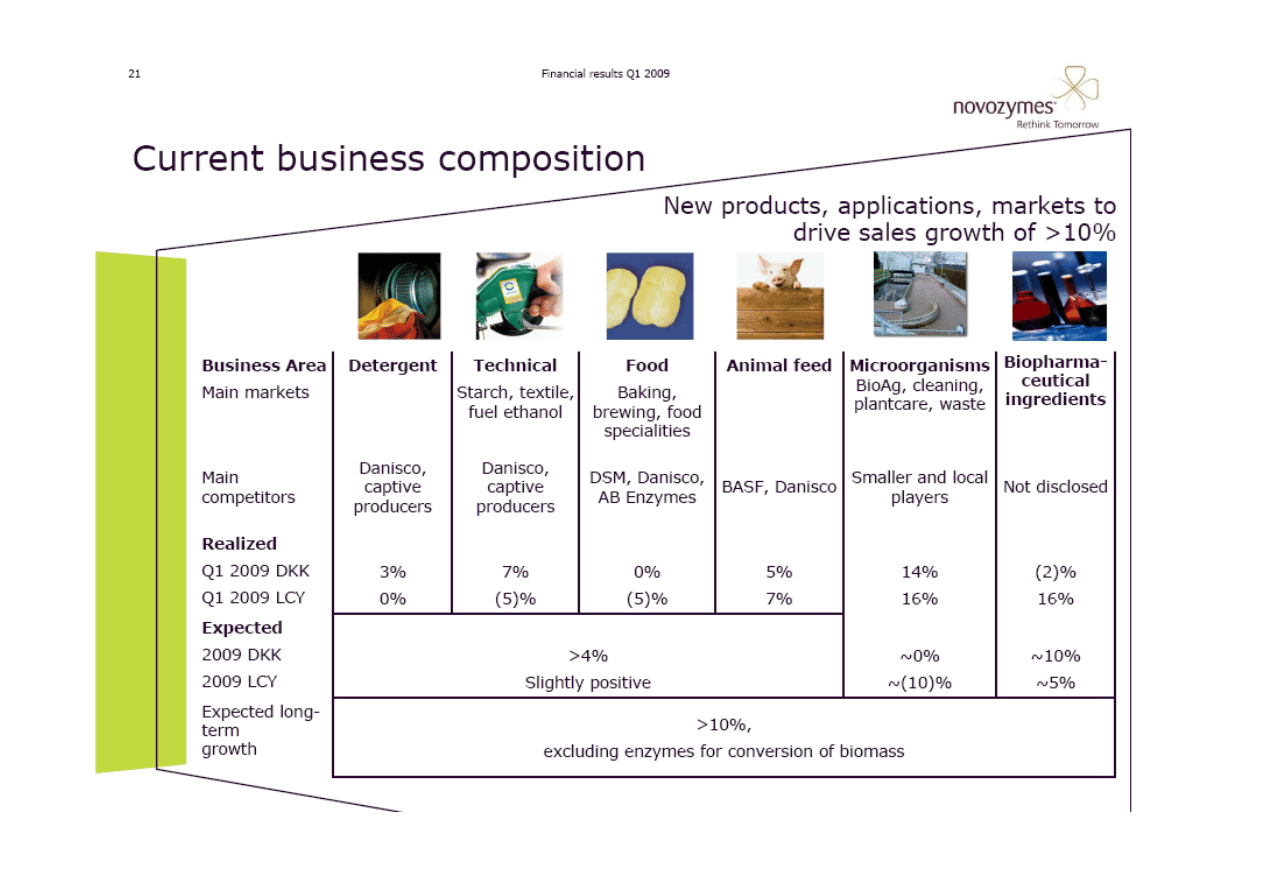
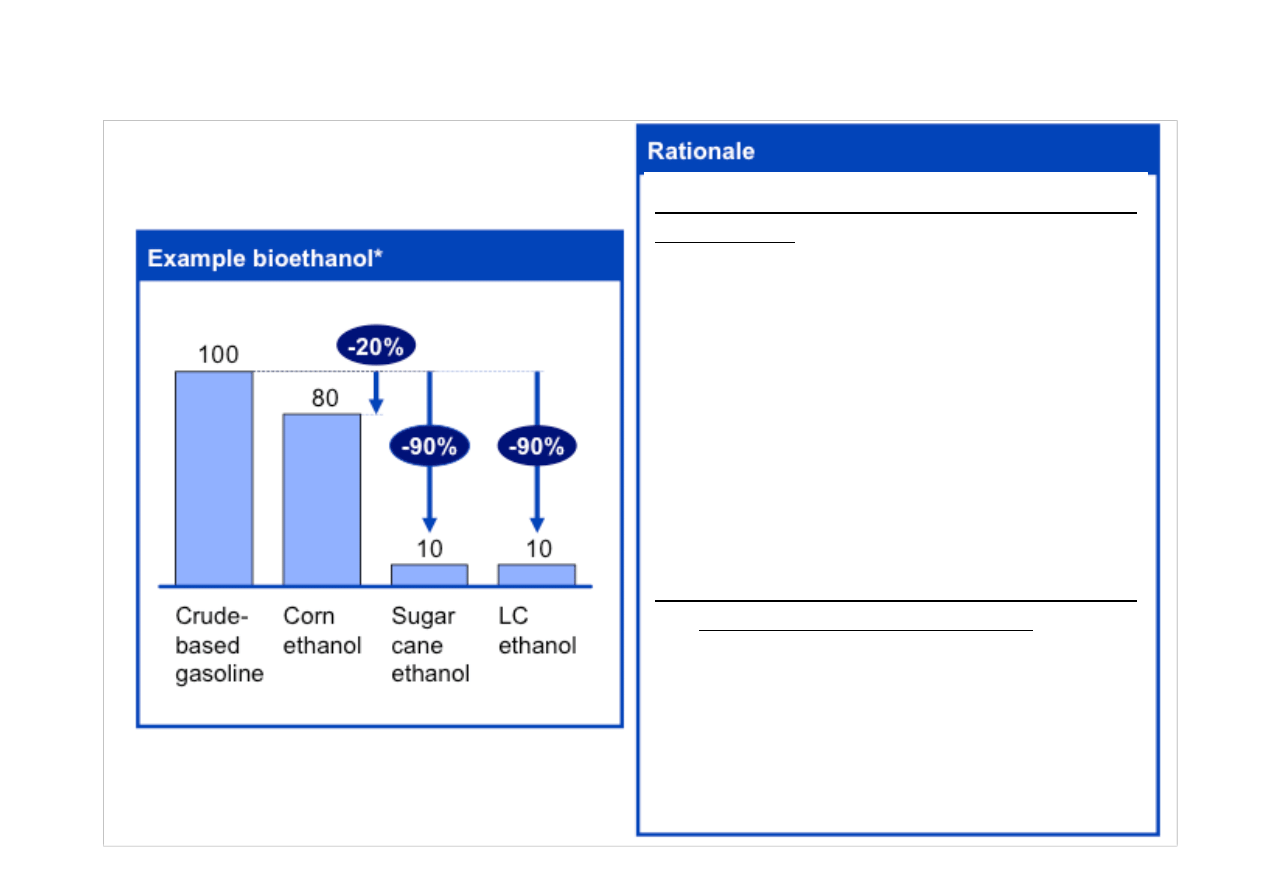
Mniejszy wpływ na środowisko produktów bio-‐
spowodowało gwałtowny wzrost biotechnologii
przemysłowej
-‐ Redukcja emisji gazów cieplarnianych w
porównaniu do emisji dwutlenku surowców
kopalnych
-‐ Mniejsze zużycie energii podczas produkcji
(np. poprzez zastosowanie enzymów)
-‐ Mniejszy wpływ na środowisko
(''zielonych''rozpuszczalników, zmniejszenie
zużycia wody, degradacji produktów
ubocznych, itp.)
-‐ Surowce odnawialne
Prawdziwe korzyści wymagają oceny dla
każdego związku, w zależności od
-‐ Typ surowca (np. trzciny cukrowej vs
kukurydziane)
-‐ Pochodzenie surowca (np. produkcji na
gruntach rolnych vs wylesianie)
-‐
Techniki
rolniczej
(np.,
nawożenie,
nawadnianie, stosowanie pestycydów)
Bio-‐produkty na bazie chemicznej są korzystne dla emisji dwutlenku węgla i innych
kryteriów środowiskowych

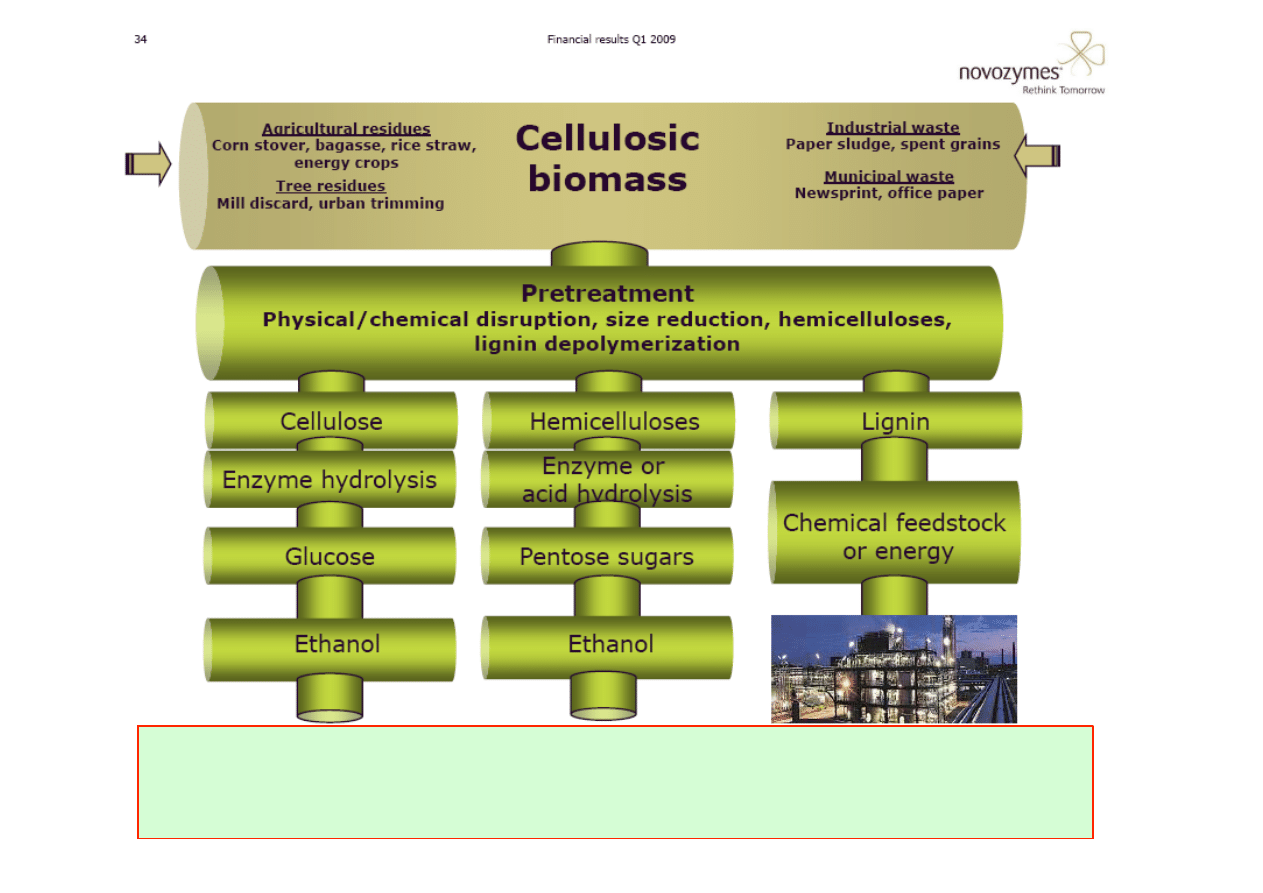
Projektowana linia biotechnologiczna powinna opierać się o określone standardy
bezpieczeństwa (farmacja vs. produkcja bioetanolu) oraz zakąłdać możliwe pełne
wykorzystanie surowców i odpadów produkcyjnych (surowce wtórne/pośrednie).
Wyszukiwarka
Podobne podstrony:
Enzymologia wykłady ściąga
EnzymologiaTZ wyklad 4
Wyklad 1 z enzymologii, Studia, Przetwórstwo mięsa - Semestr 1, Enzymologia, Wykłady
Enzymologia wykład, V sem
Enzymologia wyklad 30 11
WYKŁAD 7, Studia Biologia, Enzymologia, wykłady
EnzymologiaTZ wyklad 3
EnzymologiaTZ wyklad 7
enzymologia w8, studia, bio, 3rok, 6sem, enzymologia, enzymologia wykłady
WYKŁAD 3, Studia Biologia, Enzymologia, wykłady
wyklad w11, studia, bio, 3rok, 6sem, enzymologia, enzymologia wykłady
WYKŁAD 6, Studia Biologia, Enzymologia, wykłady
enzymologia w10, studia, bio, 3rok, 6sem, enzymologia, enzymologia wykłady
wykłady z enzymologii, Studia Biologia, Enzymologia, wykłady
enzymologia w7, studia, bio, 3rok, 6sem, enzymologia, enzymologia wykłady
Enzymologia wykłady ściąga
EnzymologiaTZ wyklad 4
więcej podobnych podstron