
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
1/9
Wykład 5.
TEORIA PASMOWA CIAŁA STAŁEGO
METALE, PÓŁPRZEWODNIKI i DIELEKTRYKI
1) Rozpatrzmy strukturę elektronową typowego metalu, to
jest sodu.
Jest to metal którego atomy posiadają tylko 1 elektron
walencyjny
→
→
→
→
znajduje się on na orbitalu 3s.
2) Teraz rozpatrzmy sieć przestrzenną zbudowaną z dwóch
atomów. Następuje nakładanie się zewnętrznych orbitali 3s,
a w wyniku powstają dwa orbitale cząsteczkowe:
-
orbital wiążący o energii niższej,
-
orbital antywiążący o energii wyższej.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
2/9
3) Dla 3 atomów pojawiają się 3 orbitale cząsteczkowe, tj.
wiążący, niewiążący i antywiążący.
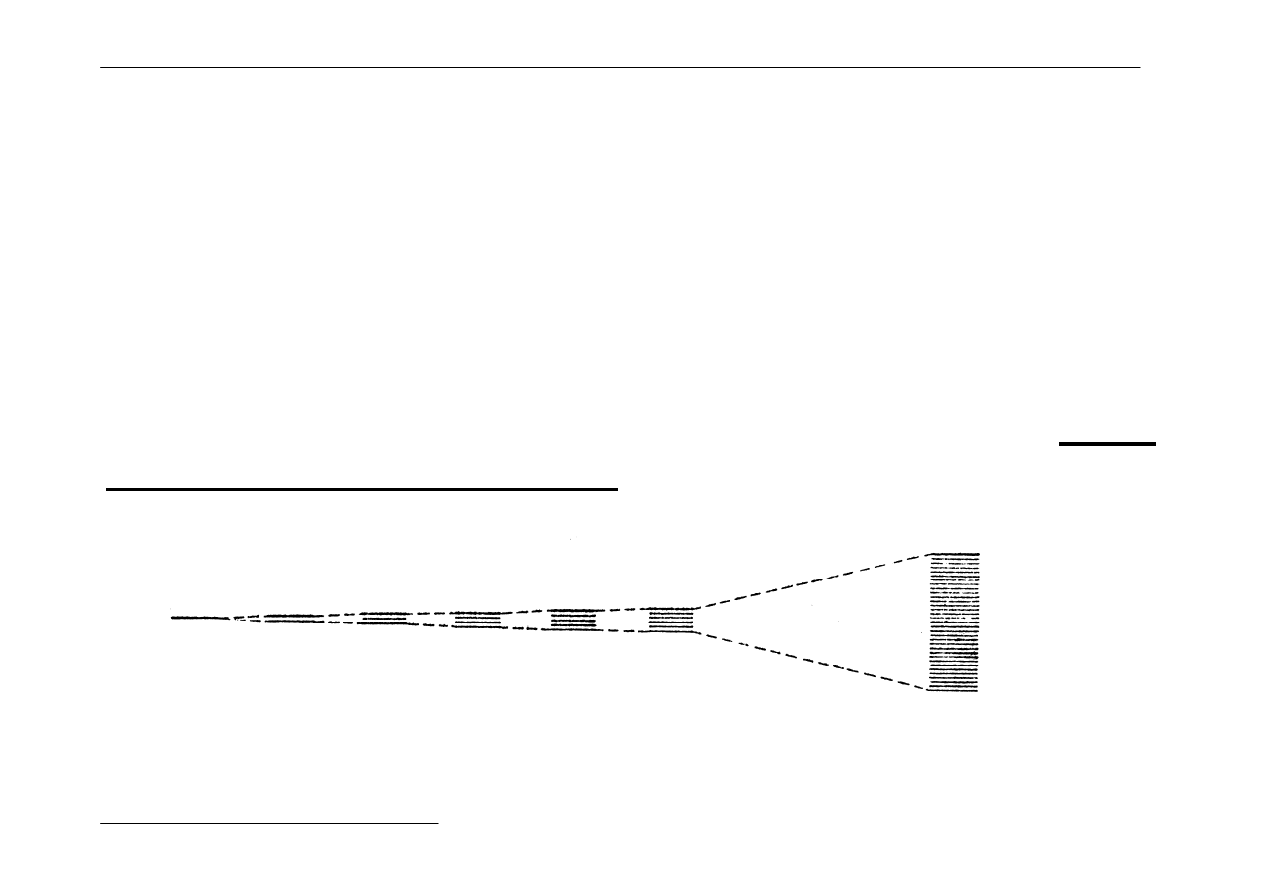
4) Teraz rozpatrzmy sieć przestrzenną złożoną z N - atomów
→
→
→
→
opisuje je N orbitali cząsteczkowych.
Każdemu z tych orbitali odpowiada inny poziom energetyczny.
W rzeczywistości poziomy te są tak blisko, że tworzą ciągłe
pasmo stanów energetycznych
odległości tych poziomów są rzędu 10
-22
eV tj. 10
-41
J

Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
3/9
Takie pasmo energetyczne jest tylko w połowie zapełnione
elektronami.
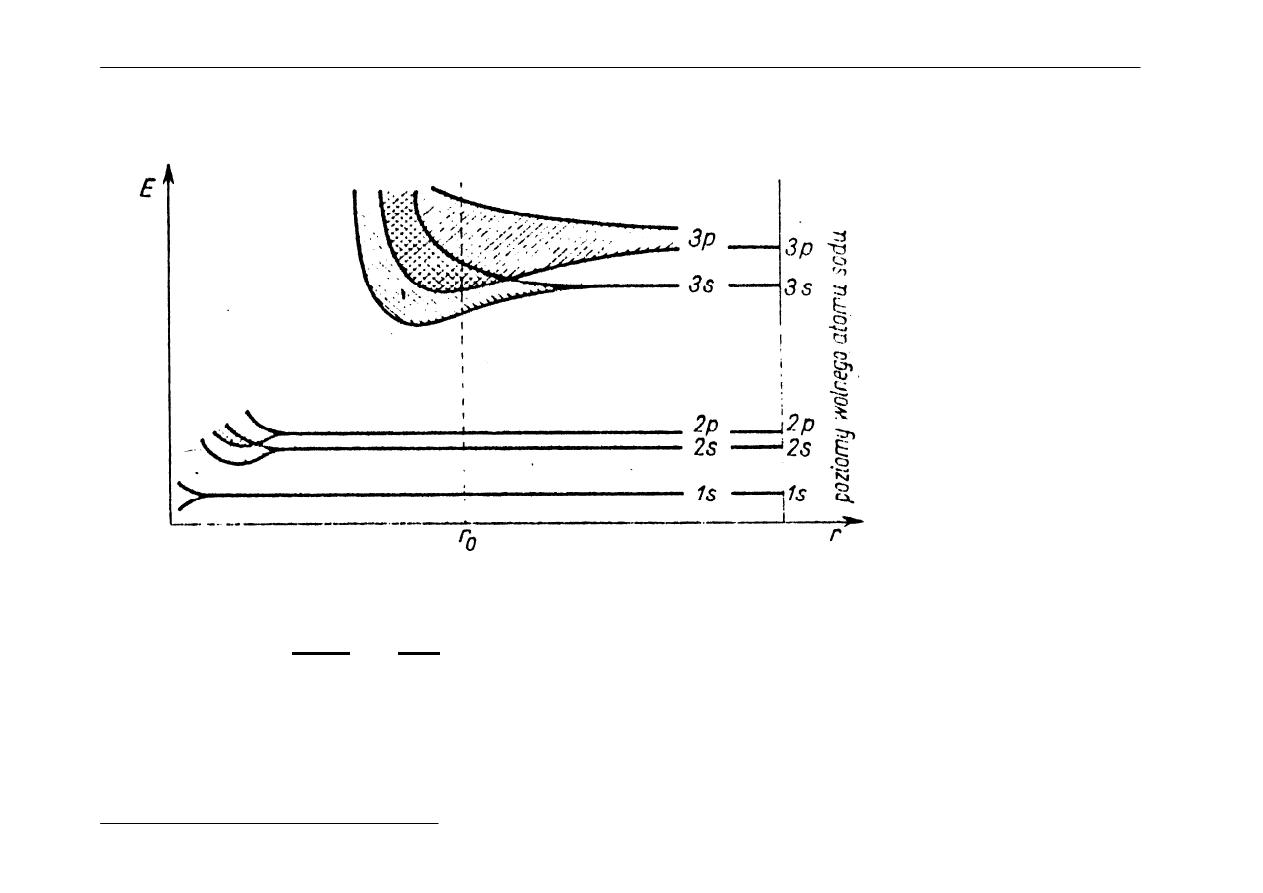
5) Co się dzieje z orbitalami 3p?
W miarę zbliżania się atomów sodu do odległości r
o
(odległość 2 węzłów) rozszczepieniu ulega
też zdegenerowany poziom energetyczny 3p.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
4/9
6) Pasma 3s i 3p tworzą jedno wspólne pasmo. Tak więc
łączna liczba zdelokalizowanych orbitali wynosi 4 N dla
N - atomów. Mogą one pomieścić 8 N - elektronów.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
5/9
7) Tak więc powstało szerokie pasmo tylko częściowo
wypełnione elektronami
→
→
→
→
jest to charakterystyczne dla
metali.
8) W temp. 0 K zajęte są tylko poziomy najniżej położone
- poziomy Fermiego.
9) W miarę podwyższania temperatury elektrony przechodzą
na coraz wyższe poziomy.
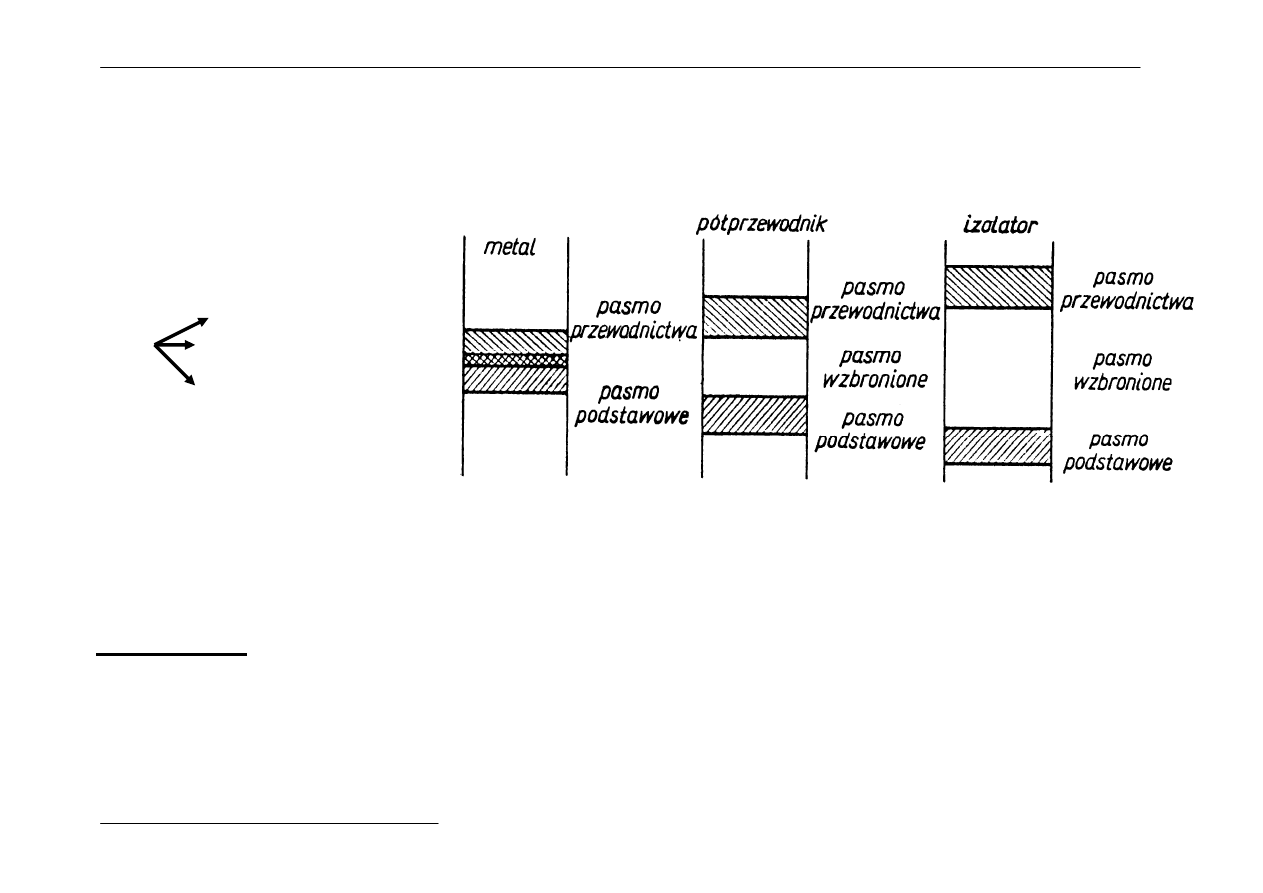
10) Takie rozszczepienie poziomów energetycznych zachodzi
nie tylko w metalach. Ale w kryształach nie wykazujących
właściwości metalicznych, pasma energetyczne nie zachodzą
na siebie.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
6/9
Wyróżniamy tutaj :
Izolatory
- diament, kwarc (SiO
2
), tlenek magnezu (MgO) Pasmo
wzbronione 5 - 10 eV
→
→
→
→
przewodnictwo elektryczne w bardzo
wysokiej temperaturze lub pod wpływem bardzo wysokiego
napięcia elektrycznego.
podstawowe
pasma przewodnictwa
wzbronione
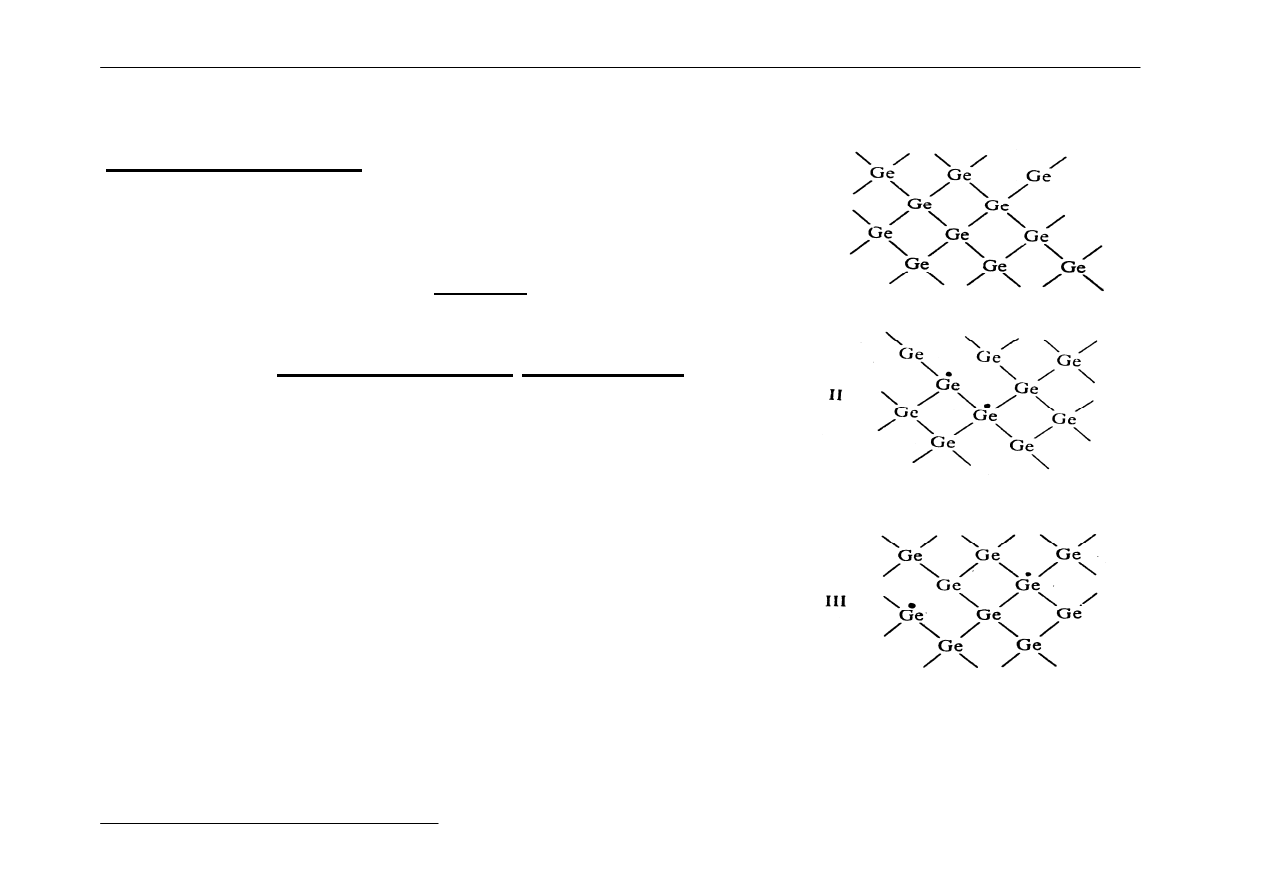
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
7/9
Półprzewodniki
- np. german (sieć typu diamentu)
- Pasmo wzbronione 1 - 2 eV
I
- Przemieszczanie się dziury
elektronowej i swobodnego
elektronu – przewodnictwo samoistne.
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
8/9
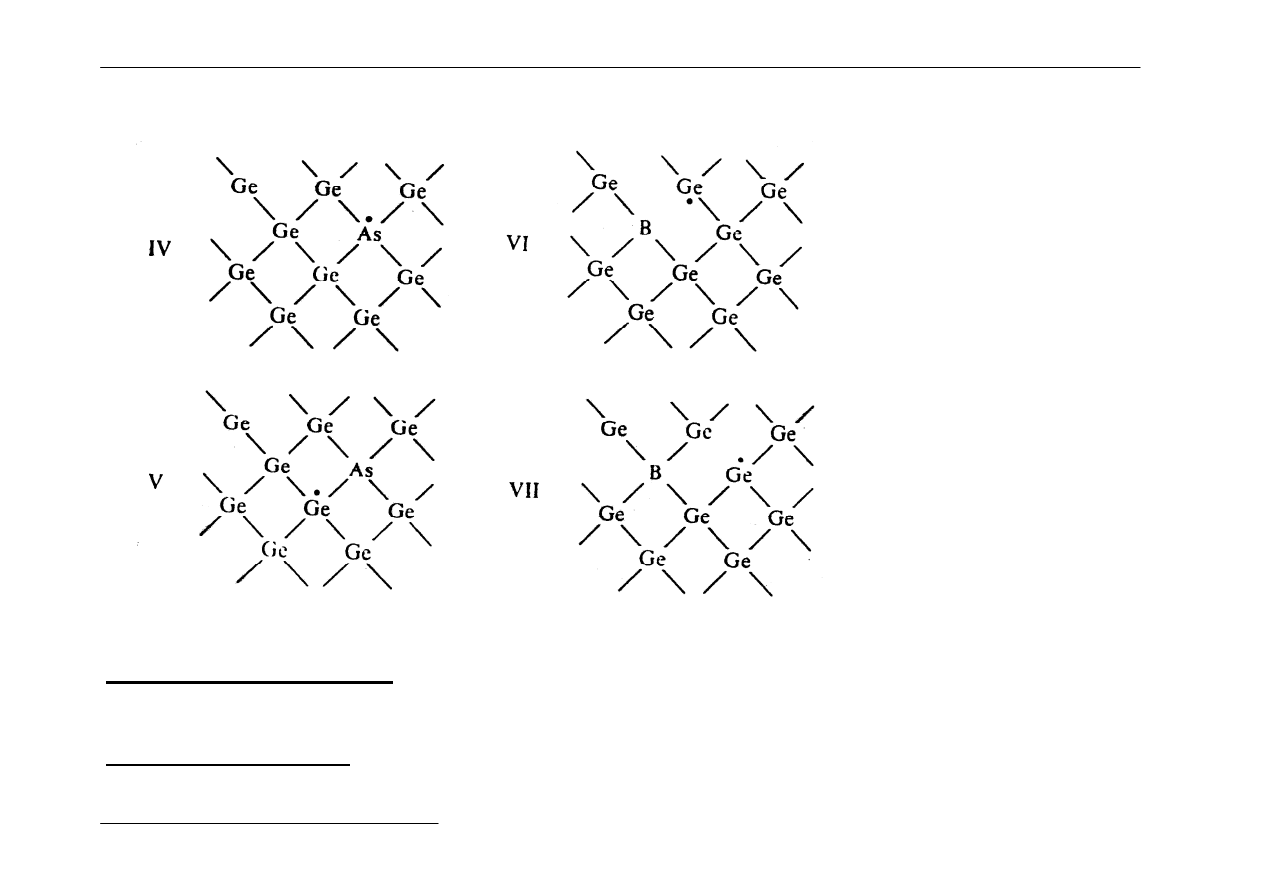
Przewodnictwo typu n
Przewodnictwo typu p
Domieszka arsenu
→
→
→
→
nadmiar jednego elektronu
→
→
→
→
centrum
donorowe
→
→
→
→
przewodnictwo typu n
Domieszka boru
→
→
→
→
niedobór jednego elektronu dziura elektronowa
→
→
→
→
centrum akceptorowe
→
→
→
→
przewodnictwo typu p
Władysław Walkowiak Podstawy Chemii Nieorganicznej - kurs WPC2002w
Wykład 5. Teoria Pasmowa Ciała Stałego
9/9
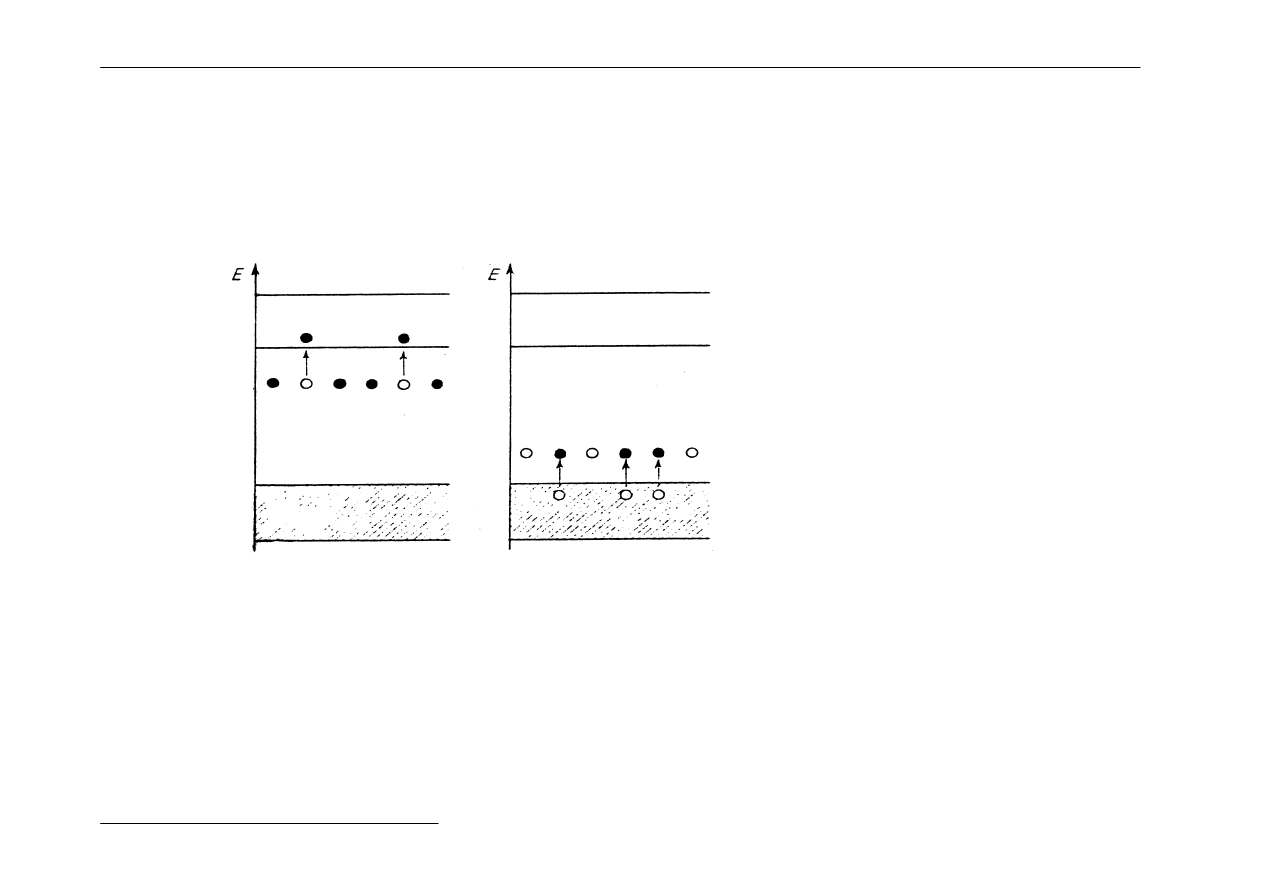
Półprzewodnik Półprzewodnik
typu n typu p
Koniec rozdziału V
pasmo
przewodnictwa
Centrum
akceptorowe
pasmo
podstawowe
Centrum
donorowe
Wyszukiwarka
Podobne podstrony:
Leszek wyklad9 teoria pasmowa ciala stalego
Wykład 5. Teoria pasmowa ciała stałego
5 Teoria pasmowa ciala stalego Nieznany (2)
TEORIA PASMOWA CIAŁA STAŁEGO, Fizyka
5 Teoria pasmowa ciała stałego
5 Teoria pasmowa ciala stalego Nieznany (2)
WYK 5 Teoria pasmowa ciala stalego
MODEL PASMOWY CIAŁA STAŁEGO
F-6 Model pasmowy ciała stałego
F 6 Model pasmowy ciała stałego
Wykład 4c Chemia ciała stałego
Wyklad 1 Fizyka ciala stalego podstawy
wykład 8 budowa ciała stałego
TEORIA fizyka rok 1, Studia, Mibm, semestr II, Fizyka Ciała Stałego, Fizyka
Fizyka ciała stałego, STUDIA, SEMESTR I, Mechanika, Mechanika Wyklady, Mechanika net
4. Budowa ciala stałego, pwr biotechnologia(I stopień), II semestr, Chemia nieorganiczna, Wykłady Ap
więcej podobnych podstron