Wstęp teoretyczny
Katalizatory metaliczne wykorzystywane są w ochronie środowiska w celu usunięcia tlenków węgla, węglowodorów i tlenków azotu z gazów wydechowych silników spalinowych. Wielkością charakteryzującą katalizatory metaliczne jest stopień dyspersji, czyli ułamek jaki stanowią atomy metalu znajdujące się na powierzchni wśród wszystkich atomów obecnych w próbce. Sama dyspersja natomiast jest definiowana jako stan rozdrobnienia substancji rozproszonej na powierzchni ciała stałego. Jest ona związana z wielkością cząsteczek oraz ich powierzchnią właściwą. Posiadamy wiele metod służących do pomiaru dyspersji:
chemisorpcja
elekromikroskopia
rentgenowskie
magnetyczne
Chemisorpcja jest techniką służącą do badań gazów takich jak wodór, tlen, tlenek węgla. Może ona być realizowana w formie statycznej lub dynamicznej. Do statycznych metod chemisorpcyjnych należą wulometria i grawimetria. Aparatura do pomiaru badań wulometrycznych składa się z: pomp, miernika ciśnienia, urządzenia dozującego gaz, naczynka do umieszczania badanej próbki oraz pieca stosowanego do wstępnej obróbki. Ilość chemisorbowanego gazu można wyznaczyć na podstawie ekstrapolacji liniowego odcinka izotermy do ciśnienia zerowego. Dzięki temu można wyznaczyć objętość potrzebną do pokrycia monowarstwy, a następnie można obliczyć powierzchnię właściwą metalu.
Aparatura stosowana do pomiarów grawimetrycznych jest podobna jak w przypadku wulometrycznych. Ilość zaadsorbowanego gazu jest tutaj mierzona bezpośrednio na podstawie przyrostu masy próbki. Poprzez ciągłą rejestrację masy zaadsorbowanego gazu można w sposób łatwiejszy rozróżnić adsorpcję odwracalną od nieodwracalnej. Jest to proces powolniejszy od pomiarów wulometrycznych.
Metody dynamiczne polegają na wprowadzeniu adsorbatu do gazu nośnego i oznaczeniu ilość adsorbatu zatrzymanego przez badany adsorbent lub katalizator. Nie wymagane są tutaj warunki próżniowe. Gazy tworzące mieszaninę powinny różnić się pod względem przewodnictwa cieplnego. Technika dynamiczna dzieli się na ciągłą i impulsową. Metoda ciągła jest wtedy kiedy przez próbkę adsorbentu przepuszcza się gaz nośny o określonym stężeniu, aż do momentu kiedy katalizator zacznie adsorbować wodór, czyli tak długo jak detektor wskaże ustalenie składu fazy gazowej. Metoda impulsowa polega na dostarczeniu za pomocą zaworu wielodrożnego adsorbatu do gazu nośnego w określonych odstępstwach czasu. Wymiatanie adsorbatu z pętli dozującej prowadzi się tyle razy aż detektor zarejestruje trzy kolejne piki o tej samej powierzchni.
Najczęściej stosowane adsorbaty to:
wodór (H2),
tlen (O2),
tlenek węgla (CO),
azot (N2)
etylen (C2H4),
acetylen (C2H2),
dwutlenek węgla (CO2).
Adsorpcję gazów na powierzchni metali prowadzi się w temperaturze od -200 do
300 °C i przy ciśnieniu 0,013 - 1,33 Kpa.
Cel ćwiczenia
Celem ćwiczenia było zapoznanie się z techniką statycznej, objętościowej (wolumetrycznej) chemisorpcji tlenku węgla w celu oznaczania wielkości powierzchni selektywnej oraz rozmiaru nanocząstek katalizatora
Wykonanie ćwiczenia
Wykonano pomiary adsorpcji tlenku węgla dla katalizatora palladowego 5% osadzonego na tlenku glinu. Odważono 0,7241 g katalizatora. Przeniesiono próbkę do u-rurki. Następnie u-ruka została zamontowana w stacji analizy. Po wprowadzeniu danych do oprogramowania aparatu, rozpoczęto pomiar.
Opracowanie wyników
Tab nr 1 Podstawowe widomości dotyczące próbek
mkat. [g] |
Vmol [cm3/mol] |
၍Pd [g/mol] |
ၷPd [m2/at.] |
ၲPd [g/cm3] |
Próbka 5 % Pd/Al2O3 |
||||
1,0582 |
22,40 ×103 |
106,4 |
7,87×10-20 |
12,02 |
Próbka 5 % Pd/TiO2 |
||||
0,9999 |
22,40 ×103 |
106,4 |
7,87×10-20 |
12,02 |
Próbka 5 % Pd/SiO2 |
||||
0,9928 |
22,40 ×103 |
106,4 |
7,87×10-20 |
12,02 |
Rys nr 1 Wykres izotermy sorpcji dla próbki 5 % Pd/Al2O3 (000-024)
Rys nr. 2 Wykres izotermy sorpcji dla próbki 5 % Pd/TiO2 (000-036)
Rys nr 3 Wykres izotermy sorpcji dla próbki 5 % Pd/SiO2 (000-011)
Tab nr. 2. Wielkości odczytane na podstawie wykresów
Całkowita objętość chemisorbowanego gazu [cm3/g] |
Objętość odwracalnie chemisorbowanego gazu [cm3/g] |
Objętość nieodwracalnie chemisorbowanego gazu [cm3/g] |
Próbka 5 % Pd/Al2O3 |
||
2,45 |
0,356 |
2,094 |
Próbka 5 % Pd/TiO2 |
||
1,434 |
0,969 |
0,466 |
Próbka 5 % Pd/SiO2 |
||
0,587 |
0,142 |
0,445 |
Tab. nr 3 Wyniki z pomiarów dla różnych próbek
|
Próbka 5 % Pd/TiO2 |
Próbka 5 % Pd/SiO2 |
Próbka 5 % Pd/Al2O3 |
Powierzchnia selektywna |
0,940 |
0,985 |
4,427 |
Powierzchnia właściwa |
18,81 |
19,69 |
88,54 |
Dyspersja [%] |
4,22 |
4,43 |
19,89 |
Rozmiar krystalitów [nm] |
26,53 |
25,34 |
5,64 |
Wykonane obliczenia:
Powierzchnia selektywna katalizatora obliczona ze wzoru
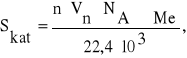
n - liczba powierzchniowych atomów Me przypadająca na 1 cząsteczkę adsorbatu
Vn - objętość nieodwracalnie zachemisorbowanego adsorbatu (cm3/gkat)
ώMe - aktywna powierzchnia atomu Me (nm2/atom lub Å2/atom)
Na - liczba Avogadro (6.022·1023 cząsteczek/mol)
Przykład obliczenia dla próbki 5 % Pd/Al2O3
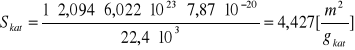
Powierzchnia właściwa metalu obliczona ze wzoru
![]()
Przykład obliczenia dla próbki 5 % Pd/Al2O3
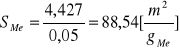
Dyspersja obliczona ze wzoru
![]()
Przykład obliczenia dla próbki 5 % Pd/Al2O3
![]()
Wielkości krystalitów metalu obliczona ze wzoru
![]()
Przykład obliczenia dla próbki 5 % Pd/Al2O3
![]()
Wnioski
Celem przeprowadzonego ćwiczenia było zapoznanie z techniką statycznej, objętościowej (wolumetrycznej) chemisorpcji tlenku węgla w celu oznaczania wielkości powierzchni selektywnej oraz rozmiaru nanocząstek katalizatora na różnych podłożach.
Podczas doświadczenia uzyskałyśmy następujące wyniki:
|
Próbka 5 % Pd/TiO2 |
Próbka 5 % Pd/SiO2 |
Próbka 5 % Pd/Al2O3 |
Powierzchnia selektywna |
0,940 |
0,985 |
4,427 |
Powierzchnia właściwa |
18,81 |
19,69 |
88,54 |
Dyspersja [%] |
4,22 |
4,43 |
19,89 |
Rozmiar krystalitów [nm] |
26,53 |
25,34 |
5,64 |
Wyniki uzyskane z naszych obliczeń są wykonane poprawnie, ponieważ pokrywają się z wynikami zwróconymi przez aparat.
Katalizator 5 % Pd/Al2O3 wykazuje znacznie mniejsze rozdrobnienie krystalitów ( ok. pięciekrotnie większe niż w przypadku pozostałych dwóch podłóż). Skutkiem tego powierzchnia selektywna, właściwa oraz dyspersja jest znacznie większa w porównaniu do katalizatorów palladowych osadzonych na tlenku tytanu i tlenku krzemu, co wiąże się z lepszą wydajnością i własnościami katalicznymi Pd/Al2O3 .
Wyszukiwarka
Podobne podstrony:
spr chemisorpcja, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych, chemisorpcja
spis cwiczen, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych
z czym to się je, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych, tranzystory
Zasady zaliczenia, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych
spr UV-Vis, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych, Vis
SEM-EDS IS, studia, nano, 3rok, 6sem, metody badań nanomateriałów funkcjonalnych, SEM
spr szampon, studia, nano, 3rok, 6sem, materiały i nanomateriały kosmetyczne, lab
spr krem z mocznikiem, studia, nano, 3rok, 6sem, materiały i nanomateriały kosmetyczne, lab
spr pomadka, studia, nano, 3rok, 6sem, materiały i nanomateriały kosmetyczne, lab
spr rurki, studia, nano, 3rok, 6sem, polimery w medycynie
czesc I, studia, nano, 3rok, 6sem, projektowanie wyrobów z materiałów polimerowych
projekt - elastomery o optymalnym usieciowaniu, studia, nano, 3rok, 6sem, projektowanie wyrobów z ma
spr enkapsulacja, studia, nano, 3rok, 6sem, polimery w medycynie
spr rurki, studia, nano, 3rok, 6sem, polimery w medycynie
sprawozdanko moje - 7, studia, bio, 3rok, 6sem, biotechnologia, lab
metody dezintegracji komórek, studia, bio, 3rok, 6sem, biotechnologia, wyklad
met.bad.ped.program, Studia, Semestry, semestr IV, Metody badań pedagogicznych
Zadanie do modułu 3, Studia, Semestry, semestr IV, Metody badań pedagogicznych, Zadania
spr6, studia, bio, 3rok, 6sem, biotechnologia, lab
więcej podobnych podstron