17912
|
Czas |
planowane czynności nauczyciela |
przewidywane czynności uczniów |
uwagi |
|
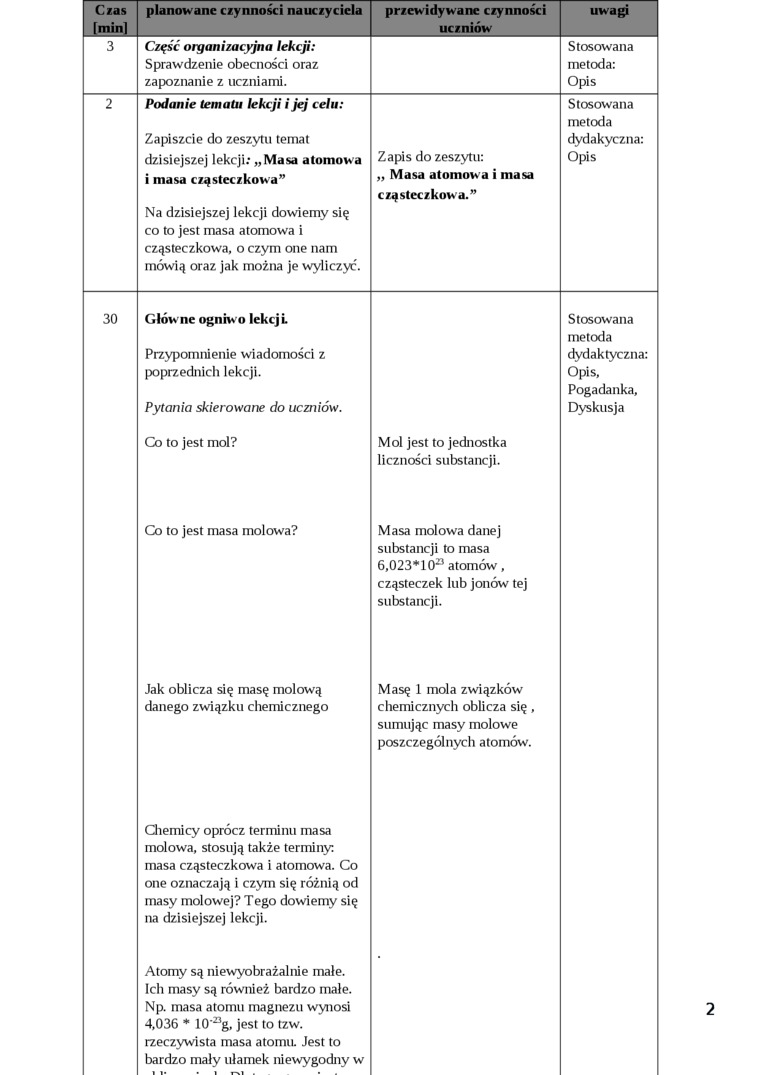
3 |
Część organizacyjna lekcji: Sprawdzenie obecności oraz zapoznanie z uczniami. |
Stosowana metoda: Opis | |
|
2 |
Podanie tematu lekcji i jej celu: Zapiszcie do zeszytu temat dzisiejszej lekcji; „Masa atomowa i masa cząsteczkowa” Na dzisiejszej lekcji dowiemy się co to jest masa atomowa i cząsteczkowa, o czym one nam mówią oraz jak można je wyliczy:. |
Zapis do zeszytu: „ Masa atomow a i masa cząsteczkowa.” |
Stosowana metoda dydakyczna: Opis |
|
30 |
Główne ogniw o lekcji Przypomnienie wiadomości z poprzednich lekcji. Pytania skierowane do uczniów. Co to jest mol? |
Mol jest to jednostka liczności substancji. |
Stosowana metoda dydaktyczna: Opis, Pogadanka, Dyskusja |
|
Co to jest masa molowa? |
Masa molowa danej substancji to masa 6,023*1021 atomów, cząsteczek lub jonów tej substancji. | ||
|
Jak oblicza się masę molową danego związku chemicznego |
Masę 1 mola związków chemicznych oblicza się, sumując masy molowe poszczególnych atomów. | ||
|
Chemicy oprócz terminu masa molowa, stosują także terminy: masa cząsteczkowa i atomowa. Co one oznaczają i czym się różnią od masy molowej? Tego dowiemy się na dzisiejszej lekcji. | |||
|
Atomy są niewyobrażalnie małe. Ich masy są również bardzo małe. Np. masa atomu magnezu wynosi 4,036 * 10 ag, jest to tzw. rzeczywista masa atomu. Jest to bardzo mały ułamek niewygodny w |
Wyszukiwarka
Podobne podstrony:
Lp. Czynności nauczyciela Czynności uczniów Czas Uwagi CZĘŚĆ WSTĘPNA / faza wprowadzająca
Lp. Czynności nauczyciela Czynności uczniów Czas Uwagi CZĘŚĆ WSTĘPNA / faza wprowadzająca
Lp. Czynności nauczyciela Czynności uczniów Czas Uwagi CZĘŚĆ WSTĘPNA / faza wprowadzająca
PLAN LEKCJI: L.p. Czynności nauczyciela i uczniów Czas trwania 1. Czynności wstępne:
PLANOWANY PRZEBIEG ZAJĘĆ lp Czynności nauczyciela (N- nauczyciel), czynności uczniów (UU-
Przewidywane wypowiedzi i czynności nauczyciela Przewidywane czynności i odpowiedzi uczniów 1. Konk
Przewidywane wypowiedzi i czynności nauczyciela Przewidywane czynności i odpowiedzi uczniów a)
IMG?28 Panują nniłt Babi N redaktora przez cały czas czynności, albowiem z uwagi na sytuację pozosta
Czynności nauczyciela związane z przygotowaniem uczniów do rozwiązywania zadań tekstowych. 88.
Tok lekcji Ogniwo lekcji Czynności nauczyciela Czynności ucznia Uwagi I. Faza
Druga jednostka lekcyjna. Ogniwo lekcji Czynności nauczyciela Czynności ucznia Uwagi I.
CZYNNOŚCI NAUCZYCIELA CZYNNOŚCI UCZNIÓW 1. Rozpoczęcie. - Powitanie i sprawdzenie obecności -
Przebieg zajęć: Faza wstępna Czynności nauczyciela Czynności uczniów Materiały i
Przebieg zajęć Czynności uczniówCzynności nauczyciela - czynności organizacyjno
Bieg na orientację 2 Konspekt lekcji CZYNNOŚCI UCZNIÓW CZYNNOŚCI NAUCZYCIELA docelowe zadania Cz
więcej podobnych podstron