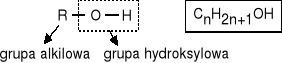ALKOHOLE MONOHYDROKSYLOWE |
|
||
szereg homologiczny:
|
|||
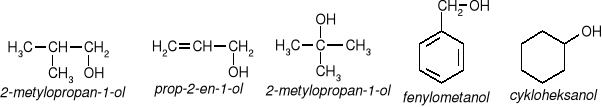
przykłady:
|
|||
właściwości fizyczne etanolu:
|
|||
właściwości fizyczne alkoholi:
|
|
||
właściwości chemiczne: 1) tworzenie alkoholanów w reakcji z aktywnymi metalami (litowcami lub berylowcami)
|
|||
sól ulega w wodzie hydrolizie zasadowej
|
|||
2) podstawienie grupy hydroksylowej atomem fluorowca w reakcji z kwasami fluorowcowodorowymi.
|
|||
3) reakcja eliminacji wody prowadząca do alkenów.
|
|||
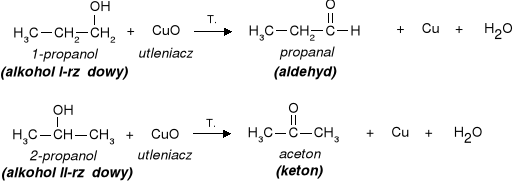
4) reakcja utleniania alkoholi pierwszorzędowych do aldehydów i drugorzędowych do ketonów.
Alkohole III-rzędowe są odporne na utlenianie. |
|||
5) reakcja estryfikacji z kasami karboksylowymi i nieorganicznymi.
|
|||
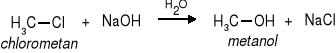
Otrzymywanie: a) hydroliza fluorowcopochodnych alkilowych.
|
|||
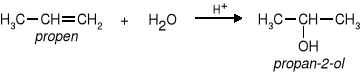
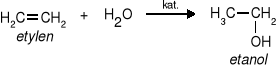
b) addycja wody do alkenów.
|
|||
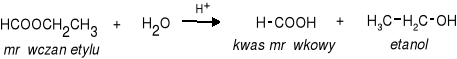
c) hydroliza estrów
|
|||
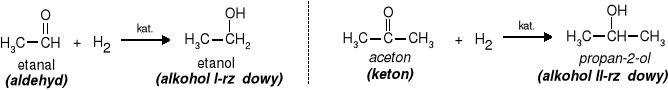
d) redukcja aldehydów do alkoholi I-rzędowych i ketonów do alkoholi II-rzędowych
|
|||
Metody specyficzne: |
|||
ETANOL - alkohol etylowy |
METANOL - alkohol metylowy; spirytus drzewny; karbinol |
||
|
|
||
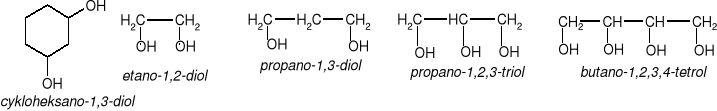
ALKOHOLE WIELOWODOROTLENOWE - POLIHYDROKSYLOWE |
|
Alkohole mające dwie lub więcej grupy wodorotlenowe -OH przyłączone do różnych atomów węgla. |
|
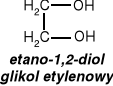
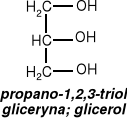
Przykłady:
|
|
|
|
|
|
właściwości fizyczne gliceryny i glikolu:
|
|
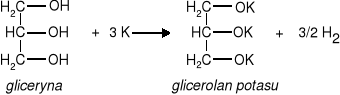
właściwości chemiczne:
|
|
|
|
|
|
|
|
Otrzymywanie:
I) glikolu etylenowego |
|
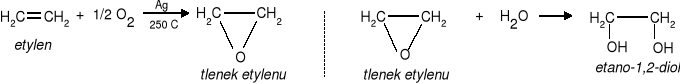
b) utlenianie etylenu w obecności katalizatora i hydroliza powstałego produktu w środowisku kwaśnym.
|
c) reakcja alkenów z roztworem nadmanganianem potasu
|
II) gliceryny
b) produkt uboczny przy wyrobie mydła
d) przez fermentację alkoholową cukru w obecności Na2SO4 |
Zastosowanie: a) glikolu etylenowego
b) gliceryny
|
Pochodne: nitrogliceryna (nazwa zwyczajowa) - triazotan (V) gliceryny (ester kwasu azotowego i gliceryny) |
|
|
|
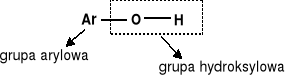
FENOLE - hydroksylowe pochodne węglowodorów aromatycznych, w których grupa hydroksylowa związana jest z atomem węgla pierścienia aromatycznego |
|||
wzór ogólny: |
|
||
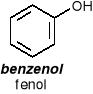
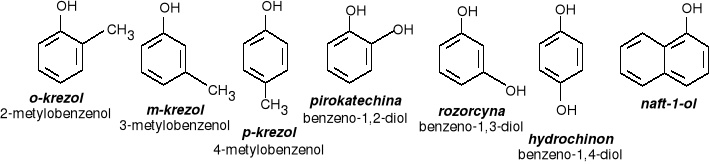
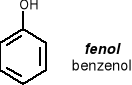
przykłady:
|
|||
|
właściwości fizyczne fenolu:
|
||
właściwości chemiczne fenolu: |
|||
|
|
||
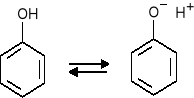
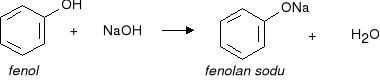
reakcje charakterystyczne:
|
|||
Fenolany jako sole słabych kwasów i mocnych zasad ulegają w wodzie hydrolizie zasadowej:
|
|||
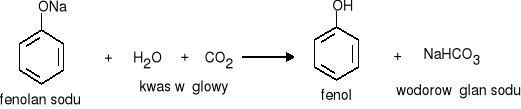
Fenol może być wyparty ze swej soli przez mocniejszy od niego kwas na przykład kwas węglowy.
|
|||
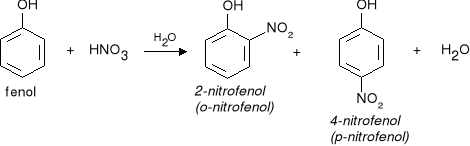
2) rekcje tworzenia barwnych związków kompleksowych z solami żelaza (III) - kolor fioletowy, granatowy lub czerwonobrunatny
|
|||
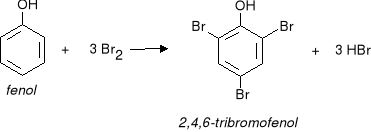
b) chlorowanie lub bromowanie fenolu
|
|||
3) reakcja ze stężonym kwasem bromowodorowym w obecności stężonego kwasu siarkowego nie zachodzi
|
|||
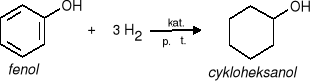
4) Reakcja uwodornienia
|
|||
5) reakcje estryfikacji z kwasami karboksylowymi.
|
|||
Zastosowanie:
|
|||
Otrzymywanie:
destylacja smoły węglowej |
|||
Porównanie ALKOHOLI i FENOLI
|
Na |
NaOH aq |
Cu(OH)2 aq |
HCl aq |
Estryfikacja |
Akolhole jednowodorotlenowe |
+ |
- |
- |
+ |
Zachodzi łatwo |
Alkohole wielowodorotlenowe |
+ |
- |
+ |
+ |
Zachodzi łatwo |
Fenole |
+ |
+ |
+ |
- |
Zachodzi bardzo trudno |
ALKOHOLE I FENOLE - 3 / 7
3
Wyszukiwarka
Podobne podstrony:
Alkohole monohydroksylowe id 58 Nieznany (2)
alkohole monohydroksylowe
alkohole monohydroksylowe
Alkohole i fenole 3 id 58102 Nieznany
instrukcja węglowodory, alkohole i fenole
test alkohole i fenole chem, chemia gimnazjum
Alkohole, tiole, fenole i etery wiadomosci ogolne id 58092
alkohole i fenole 2 id 58101 Nieznany (2)
Alkohole i fenole - test, Napisz brakujące nazwy następujących związków:
Alkohole i fenole - test, Napisz brakujące nazwy następujących związków:
alkohole i fenole, Chemia- liceum
Alkohole i Fenole
Alkohole i fenole
alkohole i fenole 2 id 58114 Nieznany (2)
Alkohole, fenole, aldehydy, ketony, cukry
więcej podobnych podstron