
AKTYWNOŚĆ
ENZYMATYCZNA
ĆWICZENIE 3
50
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
3. ENZYMY – AKTYWNOŚĆ I CZYNNIKI WPŁYWAJĄCE NA NIĄ
3.1. Podstawy teoretyczne
3.2. Wykonanie ćwiczenia
A. Wykrywanie aktywności pepsyny
Wykonanie ćwiczenia:
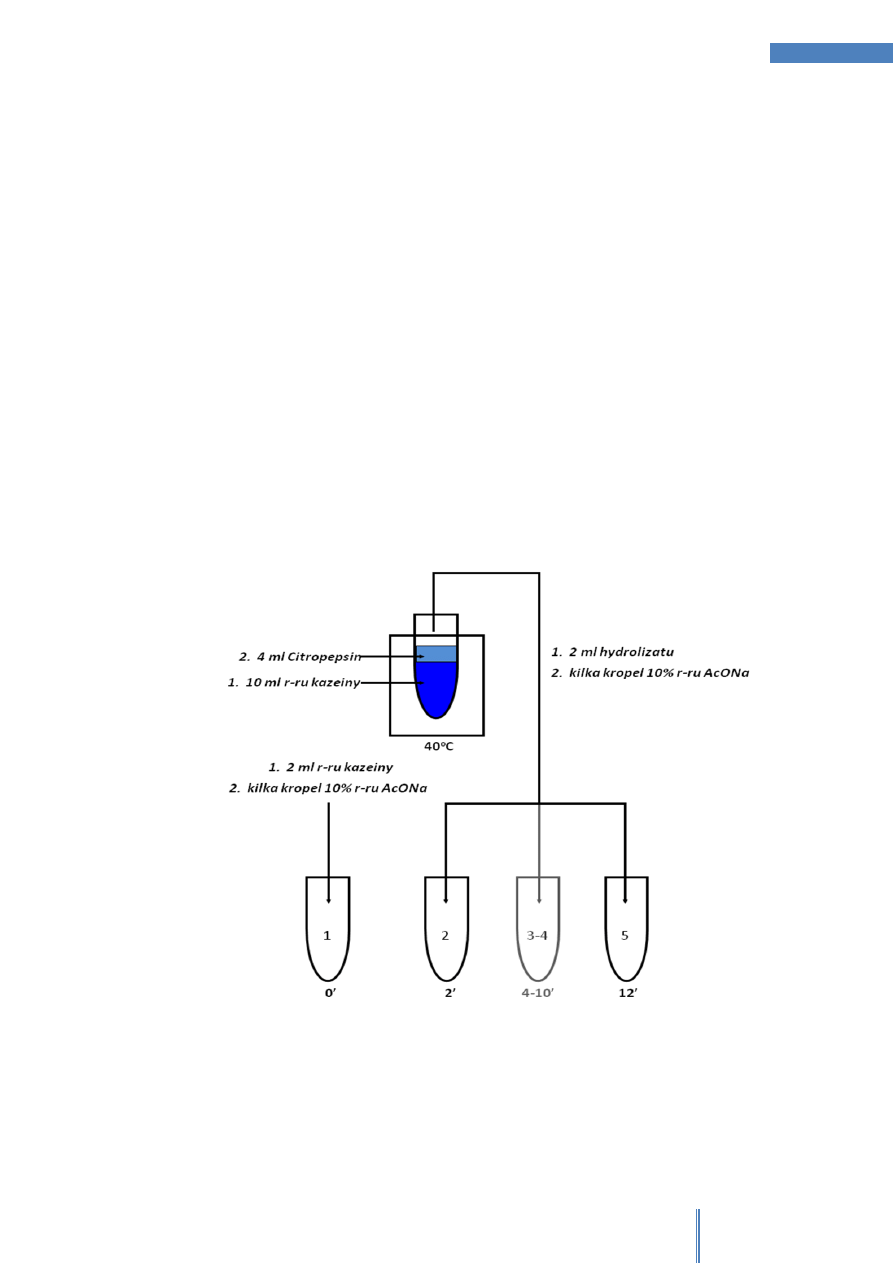
Przygotować szereg kilku probówek (minimum 4; maxymalnie 6).
Do jednej z nich odmierzyć 2 ml kwaśnego roztworu kazeiny (w lodówce) i dodać
kilka kropel 10% roztworu AcONa (próba odniesienia).
Do kolejnej probówki odmierzyć: 10 ml kwaśnego roztworu kazeiny i 4 ml preparatu
Citropepsin; wstawić probówkę do łaźni wodnej o temperaturze 40°C.
Po dwóch minutach pobrać pipetą 2 ml hydrolizatu z probówki i natychmiast
dodawać kroplami 10% roztwór AcONa. Kolejną (ostatnią) próbę wykonać po 12
minutach lub
opcjonalnie jeszcze maxymalnie 2 razy pomiędzy pierwszą i ostatnią
.
Zapisać obserwacje w tabeli 1.
Rysunek 1
Przygotowanie sprawozdania (część pierwsza):
Wypełnić tabelę 1 z obserwacjami.
Napisać do jakiej klasy enzymów należy pepsyna i jaki proces katalizuje.

51
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
SPRAWOZDANE (część pierwsza)
Obserwacje:
Tabela 1
Nr probówki
1
2
3
4
5
0’
2’
……..’
……..’
12’
Wnioski:

52
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
B. Wykrywanie aktywności inwertazy
Przed przystąpieniem do ćwiczenia B należy przygotować:
Roztwór inwertazy z drożdży: Drożdże świeże (0.5g) rozetrzeć w moździerzu
z piaskiem, dodać 200ml wody destylowanej, następnie przesączyć przez lejek.
Supernatant, zawierający inwertazę, stanowi materiał do ćwiczeń. Można również
wykorzystać roztwór inwertazy przygotowany przez grupę studentów wykonującą
ćwiczenie 4.
Wykonanie ćwiczenia:
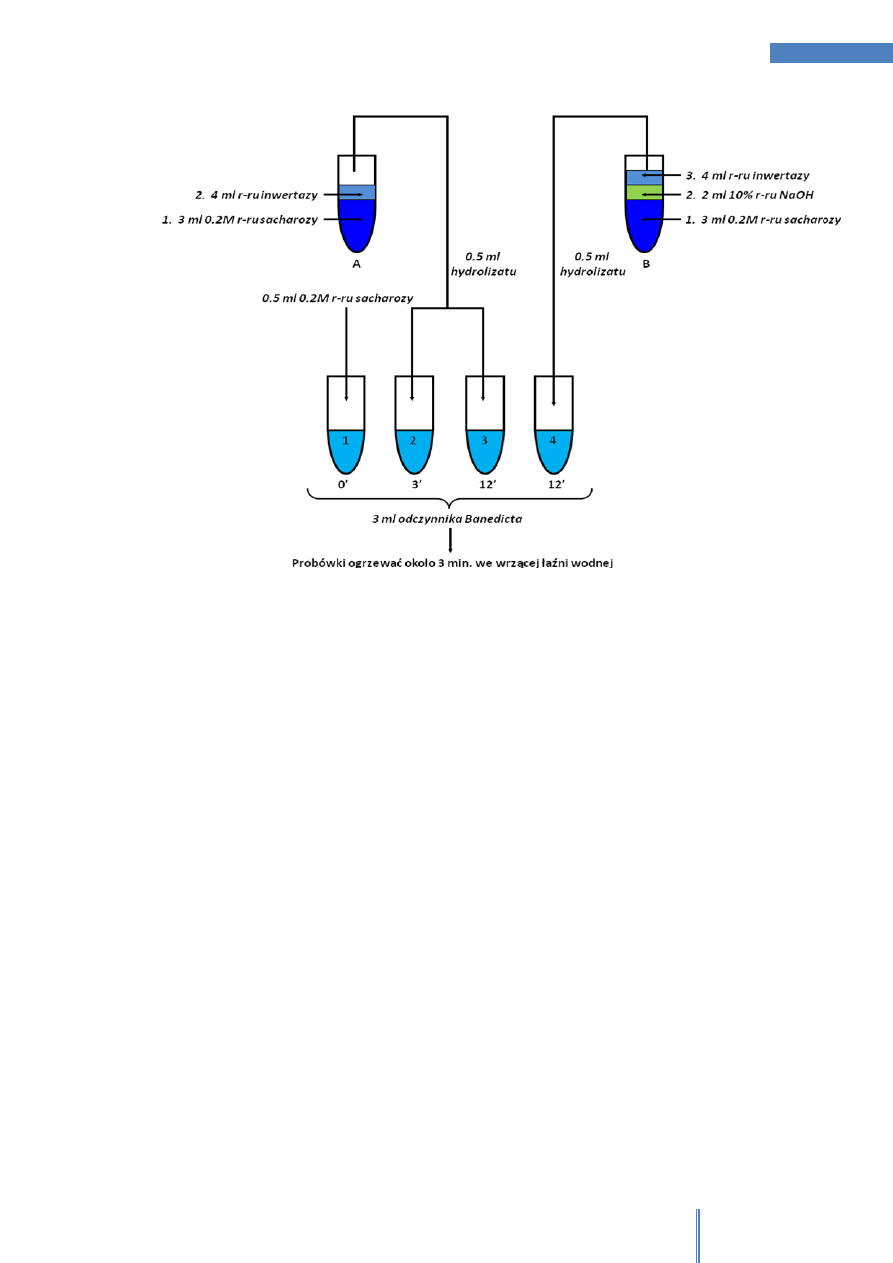
Przygotować szereg 6 probówek.
W dwóch probówkach (A, B) umieścić po 3 ml 0.2 M roztworu sacharozy. Do
probówki B dodać 2 ml 10% roztworu NaOH.
Do czterech kolejnych (1-4) wlać po 3 ml odczynnika Benedicta.
Do pierwszej (1) z nich wlać 0.5 ml 0.2M roztworu sacharozy (próba odniesienia).
Do probówek A i B dodać 4 ml roztworu inwertazy z drożdży.
Po 3 minutach pobrać z probówki A 0.5 ml hydrolizatu i wprowadzić do probówki nr
2. Kolejną porcję hydrolizatu pobrać po 12 minutach i wprowadzić do probówki nr 3.
Po 12 minutach pobrać 0.5 ml hydrolizatu z probówki B i wprowadzić do probówki
nr 4.
Probówki 1-4 ogrzewać 3 minuty we wrzącej łaźni wodnej. Zanotować obserwacje
w tabeli 2.
53
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
Rysunek 2
Przygotowanie sprawozdania (część druga):
Wypełnić tabelę 2 z obserwacjami
Do jakiej klasy enzymów należy inwertaza?? Napisz równania zachodzących reakcji.
Jeśli reakcja jest ‘typowym’ procesem redoks napisz jej bilans jonowo-elektronowy.
W równaniu reakcji zaznaczyć, który produkt był obserwowany podczas
przeprowadzania eksperymentu.
Jaki wpływ na aktywność enzymu ma zmiana pH środowiska?

54
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
SPRAWOZDANIE (część druga)
Obserwacje:
Tabela 3
Nr probówki
1
2
3
4
0’
3’
12’
12’
Wnioski:

55
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
C. Wykrywanie aktywności ureazy
Przed przystąpieniem do ćwiczenia należy rozetrzeć kilka ziaren soi w moździerzu.
Wykonanie ćwiczenia:
Ziarna soi umieścić w 4 probówkach zgodnie z informacjami zawartymi w Tabeli 3.
Jedną probówkę ogrzewać przez kilka minut nad płaszczem grzejnym następnie
probówkę należy ostudzić. Do wszystkich probówek należy dodać jednocześnie po 5 ml
r-ru mocznika i dodać kilka (3-5) kropli fenoloftaleiny. Obserwuj zmianę intensywności
zabarwienia w czasie. Obserwacje zapisać w Tabeli 3.
Przygotowanie sprawozdania (część trzecia):
Zapisać obserwacje w tabeli 3.
Napisać do jakiej klasy enzymów należy ureaza oraz zapisać równanie katalizowanej
reakcji. Obecność jakich cząsteczek lub jonów jest odpowiedzialna za pojawienie się
zabarwienia roztworu w trakcie przeprowadzania doświadczenia.
Jak na przebieg reakcji enzymatycznej wpłynęło rozdrobnienie ziaren i ich prażenie.
Uzasadnij zmiany obserwowane zmiany.

56
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
SPRAWOZDANIE (część trzecia)
Tabela 3
próba ziarna
temp.
barwa (intensywność)
30s
20 min
50min
A
całe
-
B
roztarte -
C
roztarte prażone
Wnioski:

57
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
D.
Wykrywanie oksydaz, peroksydaz i katalaz
Przed przystąpieniem do ćwiczenia C należy przygotować:
Wyciąg ziemniaczany: umytą i obraną połówkę ziemniaka utrzeć na tarce. Miazgę
umieścić w zlewce z 150 ml wody i łagodnie zamieszać. Roztwór należy przesączyć.
Supernatant stanowi materiał do ćwiczeń. Uwaga!!! Czynności opisane należy wykonać
sprawnie, a do doświadczenia należy stosować świeży roztwór (nie posiadający
ciemnego, brązowego zabarwienia)
Wyciąg z korzenia chrzanu: wysuszony i starty korzeń chrzanu (lub chrzan dostępny w
sklepie) umieścić w kolbie stożkowej ze szlifem zadać kilkoma ml wody, dokładnie
wytrząsnąć przez kilka minut. Roztwór przesączyć lub zdekantować. Supernatant
stanowi materiał do ćwiczeń.
Wykonanie ćwiczenia:
Należy przygotować zestaw probówek zawierający substancje wymienione
w Tabeli 4. Obserwować zmiany w probówkach w czasie. Należy zwrócić szczególną
uwagę na zmianę zabarwienia w czasie i wydzielające się gazowe produkty. Następnie
zapisać obserwacje w Tabeli 4.
Przygotowanie sprawozdania (część czwarta):
Wypełnienie tabeli 4.
Do jakich klas lub klasy enzymów należą okzydaza/peroksydaza/katalaza.
Napisz równania katalizowanych reakcji. Jakie produkty były obserwowane
w próbach przeprowadzonych z użyciem fenolu i pirokatechiny (z dodatkiem i
bez dodatku H
2
O
2
)?
W jaki sposób na szybkość katalizowanej reakcji wpływa budowa substratu
(fenol lub pirokatechina)? Odpowiedź uzasadnij.
Jaki wpływ na przebieg reakcji enzymatycznej ma dodatek Na
2
S?
Wypełnić tabelę 5.
58
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
SPRAWOZDANIE (część czwarta)
Obserwacje:
Tabela 4
5ml
10 kropel
kilka
kropel
10
kropel
uwagi
obserwacje
próba
wyciąg z
fenol
Na
2
S
H
2
O
2
A
ziemniaka
fenol
-
-
B
ziemniaka pirokatechina
-
-
C
ziemniaka
fenol
-
+
H
2
O
2
dodać
natychmiast po
dodaniu fenolu
D
ziemniaka pirokatechina
-
+
E
chrzanu
fenol
-
+
obserwuj barwę
przed dodaniem
H
2
O
2
F
chrzanu
pirokatechina
-
+
G
ziemniaka
-
-
+
H
ziemniaka
-
+
+

59
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
Wnioski:

60
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
Wnioski:
Tabela 5
próba
skład mieszaniny reakcyjnej
obecny enzym
oksydaza/peroksydaza/katalaza
A
wyciąg z ziemniaka + fenol
B
wyciąg z ziemniaka + pirokatechina
C
wyciąg z ziemniaka + fenol + H
2
O
2
D
wyciąg z ziemniaka + pirokatechina +H
2
O
2
E
wyciąg z chrzanu + fenol + H
2
O
2
F
wyciąg z chrzanu + pirokatechina + H
2
O
2
G
wyciąg z ziemniaka + H
2
O
2
H
wyciąg z ziemniaka + Na
2
S + H
2
O
2
----------
Enzymy obecne w wyciągu z ziemniaka:
Enzymy obecne w wyciągu z chranu:

61
Ćwiczenie 3
Pracownia z BIOCHEMII dla studentów III roku na Wydziale Chemii UŁ
Wyszukiwarka
Podobne podstrony:
Instrukcja biologia Aktywnosc enzymatyczna
Instrukcja biologia, Aktywnosc enzymatyczna
Aktywność enzymatyczna mikroflory gleby
IG.6 - Oznaczanie aktywności enzymatycznej metaloproteinaz komórkowych, Genetyka, Inżynieria genetyc
(), biologia, sprawozdanie aktywność enzymatyczna
12. Inhibitory aktywności enzymatycznej, Lekarski WLK SUM, lekarski, biochemia, enzymy
aktywność enzymatyczna bakterii
Aktywnośc enzymatyczna mikroplanktonu
spr 2 Aktywność enzymatyczna, biologia
instrukcja biologia aktywnosc enzymatyczna wersja1
,biologia L, aktywność enzymatyczna
Instrukcja biologia Aktywnosc enzymatyczna
Wzrost i aktywnosc enzymatyczna drozdzy w mleku
Aktywność enzymatyczna gleb pożarzysk wielkoobszarowych w zróżnicowanych warunkach siedliskowych i p
METODY AKTYWNE W NAUCZANIU I WYCHOWANIU, Materiały z ćwiczeń
08.Aktywność fizyczna, Zdrowie publiczne, W. Leśnikowska - Ścigalska - ĆWICZENIA I sem, cz. I
więcej podobnych podstron