
Zaburzenia krzepnięcia

Wykrzepianie
wewnątrznaczyniowe:
rozpoznanie
• obecność schorzenia
predysponującego,
• objawy kliniczne,
• krwawienie,
• upośledzenie funkcji poszczególnych
narządów,
• wyniki badań laboratoryjnych.
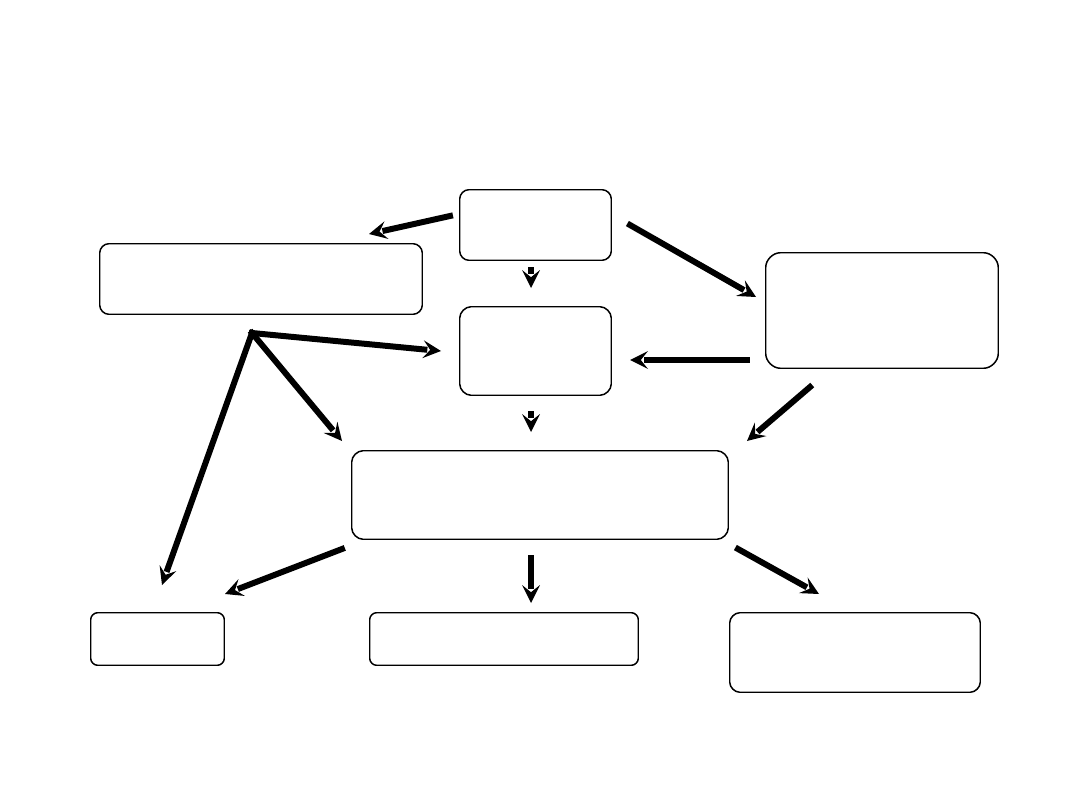
Patogeneza sepsy
Bakterie
Neutrofile
(elastaza)
Uszkodzenie śródbłonka
(IL-6)
Wstrząs
Reakcja ostrej fazy
Trombocytopenia
DIC
Monocyty,
Makrofagi
(TNF, IL-1, IL-6)
C3a, C4a,
Aktywacja przez kontakt

Patogeneza sepsy
Infekcja
(bakterie, wirusy, grzyby etc.)
Substancje wyzwalające
(endotoksyny, egzotoksyny etc.)
Pierwotne mediatory
(TNF, IL - 1, C5 a etc.)
Aktywacja kaskad humoralnych i komórkowych
Wtórne mediatory
(cytokiny, składowe dopełniacza, prostanoidy, PAF, wolne rodniki tlenowe)
Wstrząs
MODS

Analogi heparyny
Syntetyczne związki o właściwościach
heparynopodobnych
• SSHA: półsyntetyczny analog heparyny,
wybiórczo hamuje czynnik Xa bez wpływu
na krzepnięcie ogólne,
• SP - 54: wykazuje aktywność
antytrombinową bez udziału AT III oraz
uczynnia CH - II
(II kofaktor heparyny).
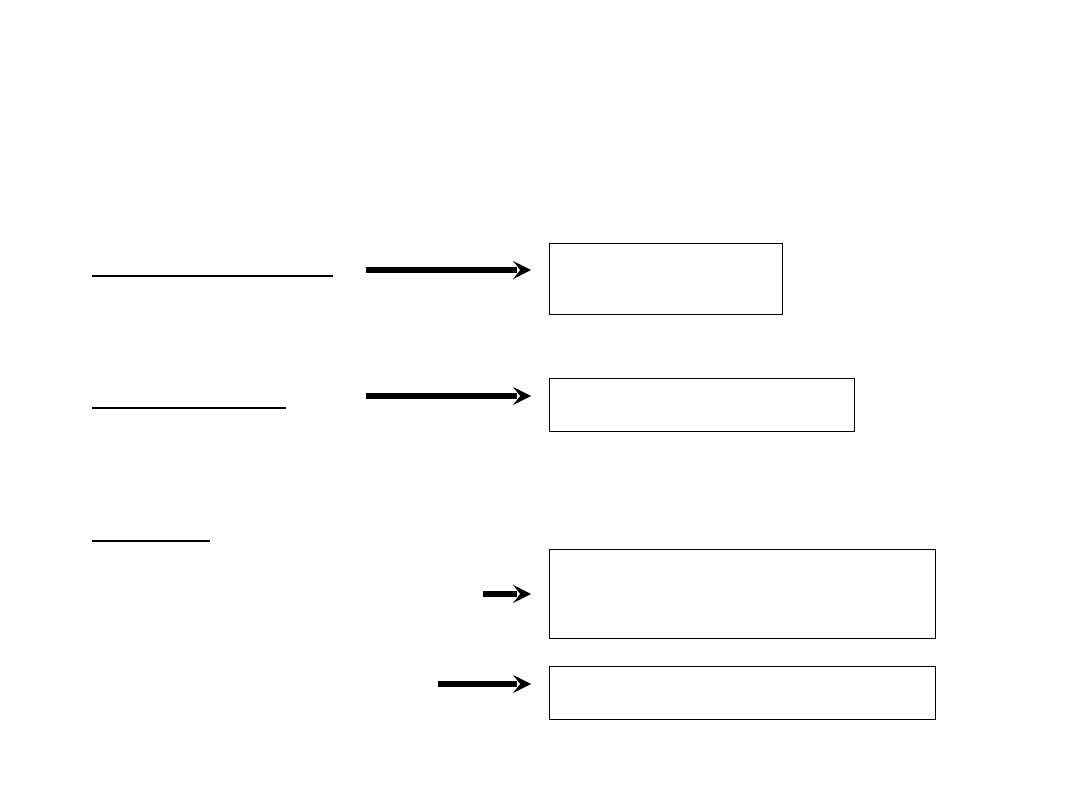
DIC
PRZEWLEKŁY
PODOSTRY
OSTRY
• koagulopatia ze
zużycia
• zespół odwłóknienia
FDP
Małopłytkowość
Wydłużenie APTT i TT
Wydłużenie PT
Wydłużenie czasu krzepnięcia
Spadek poziomu fibrynogenu
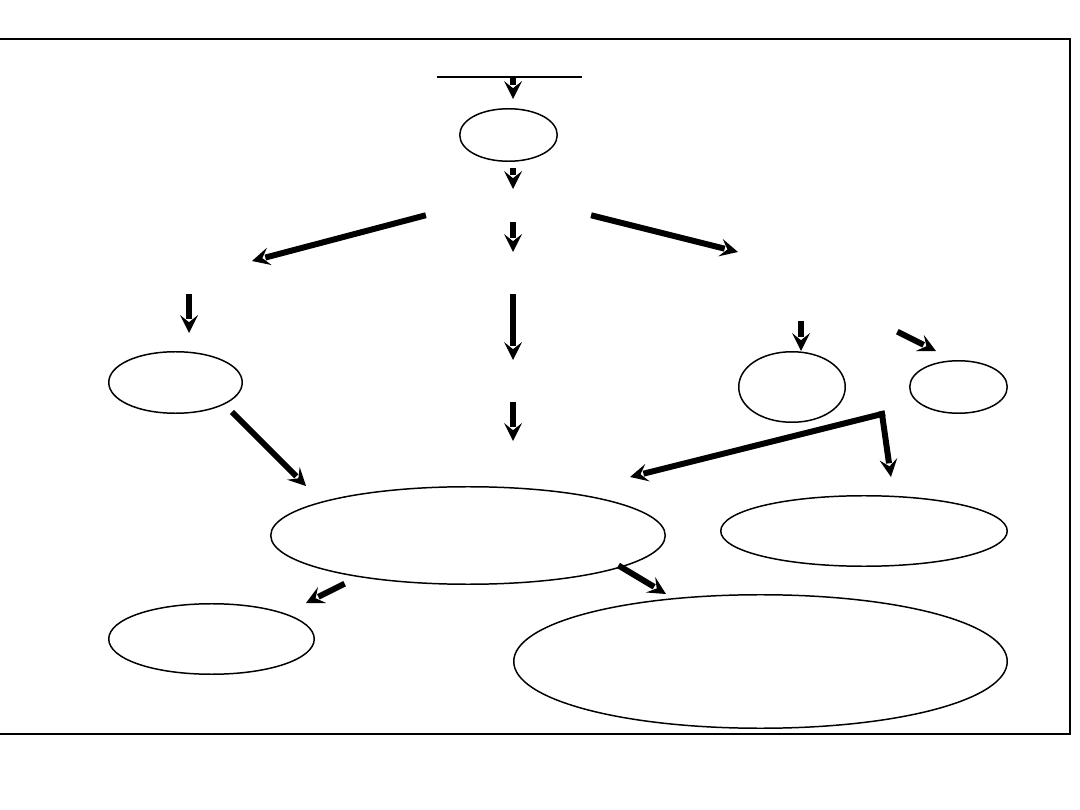
Bakterie
LPS
Aktywacja:
Dopełniacz
Układ krzepnięcia
Monocyty,
makrofagi
C3a, C5a
Kininy, fibrynoliza
IL-1,6...
TNF
DIC
Uruchomienie i aktywacja
Reakcje ostrej fazy
PMN
Wolne rodniki
Mediatory stanu zapalnego
(prostaglandyny, leukotrieny, PAF
elastaza, MPO)
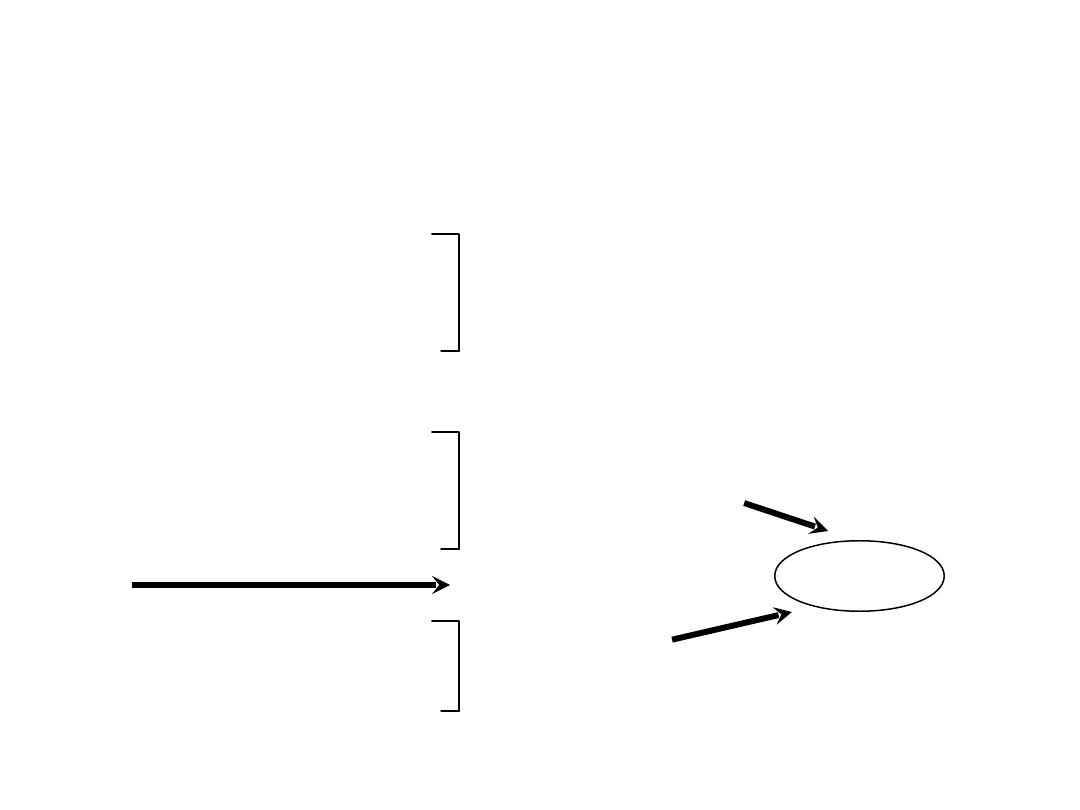
Aktywatory: LPS, TNF, IL-
1
PAF
PA-1
tromboplastyna
spadek trombomoduliny
GMP-140
ELAM
ICAM
VCAM
NO
PGI2
endotelina
Działanie prokoagulacyjne
Wzrost liczby monocytów i neutrofili,
zwiększenie adhezji
Zmiany napięcia naczyniowego
Wysięk
IL-1, IL-6, IL-8

Nietrombogenne właściwości
śródbłonka zapewniają:
•
Kofaktory krążących inhibitorów (siarczan
heparanu, siarczan dermatanu,
trombomodulina),
•
Prostacyklina,
•
EDRF (czynnik relaksacji mięśniówki gładkiej
naczyń),
•
Aktywator plazminogenu,
•
Ujemny ładunek elektryczny błon
komórkowych śródbłonka.
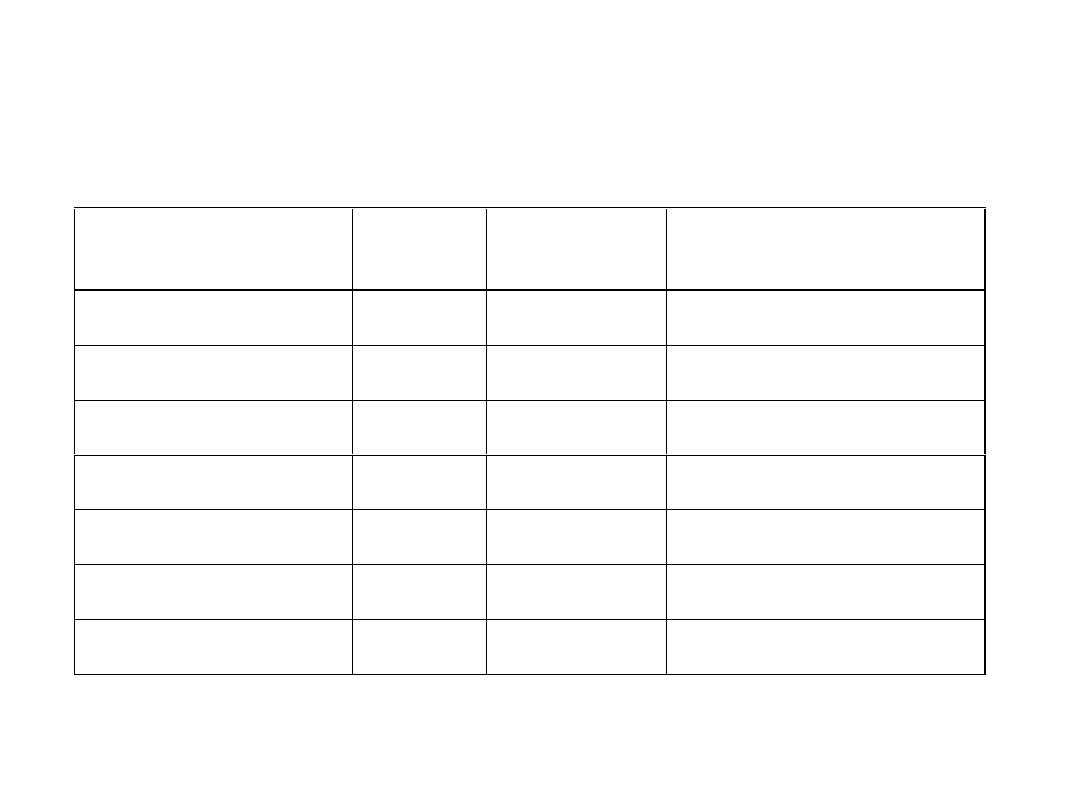
Inhibitory proteaz
serynowych
Inhibitor
Stężenie
we krwi
(mol/l)
Masa
cząsteczkowa (D)
Funkcja
Antytrombina III
2
61000
Inaktywacja Xa, trombiny, IXa,
Xia, XIIa, elastazy
II kofaktor heparyny
1
66000
Inaktywacja trombiny
Inhibitor białka C
10
-5
57000
Inaktywacja białka C
Inhibitor aktywatora
plazminogenu PAI-1 i PAI-2
10
-4
50000
Inaktywacja aktywatorów
plazminogenu
1 - antytrypsyna
15
Inaktywacja elastazy neutrofilów
Antyplazmina
1
70000
Inaktywacja plazminy
Inhibitor C1
2
104000
Inaktywacja C1s i kalikreiny
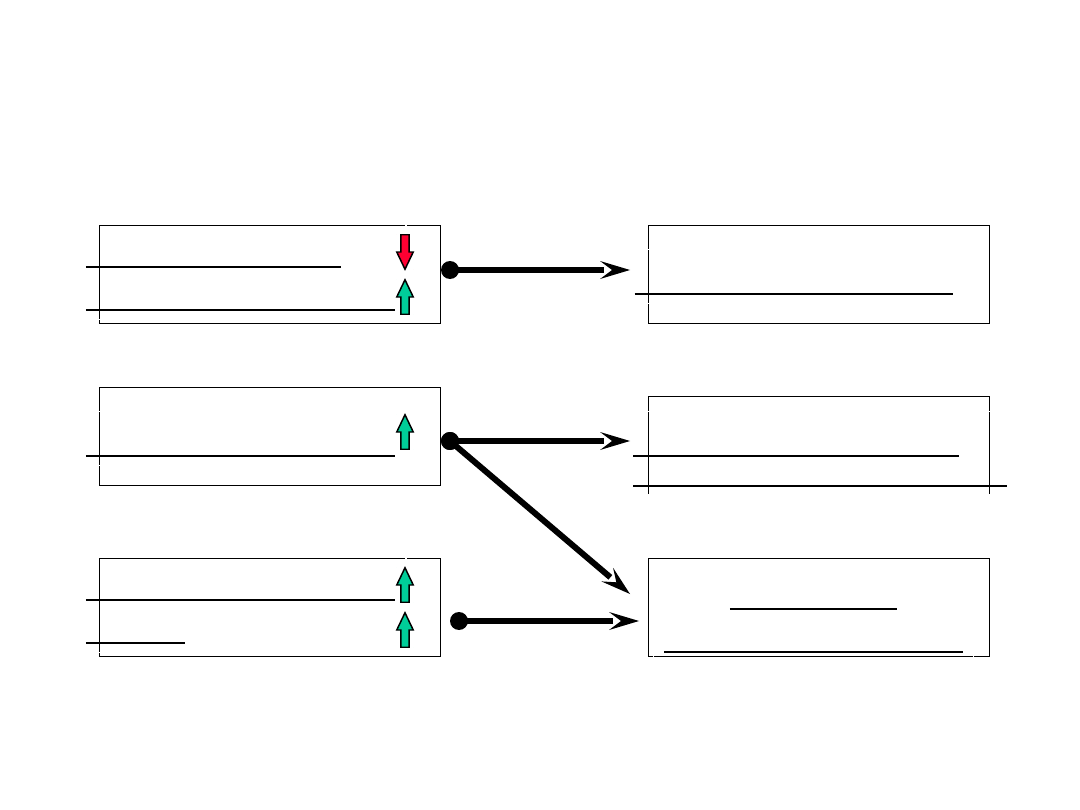
Interpretacja badań
Liczba płytek
Czas krwawienia
Czas krwawienia
Czas krwawienia
APTT
Trombocytopenia
Dysfunkcja płytek
(aspiryna, dekstran, heparyna)
Choroba
von Willebranda
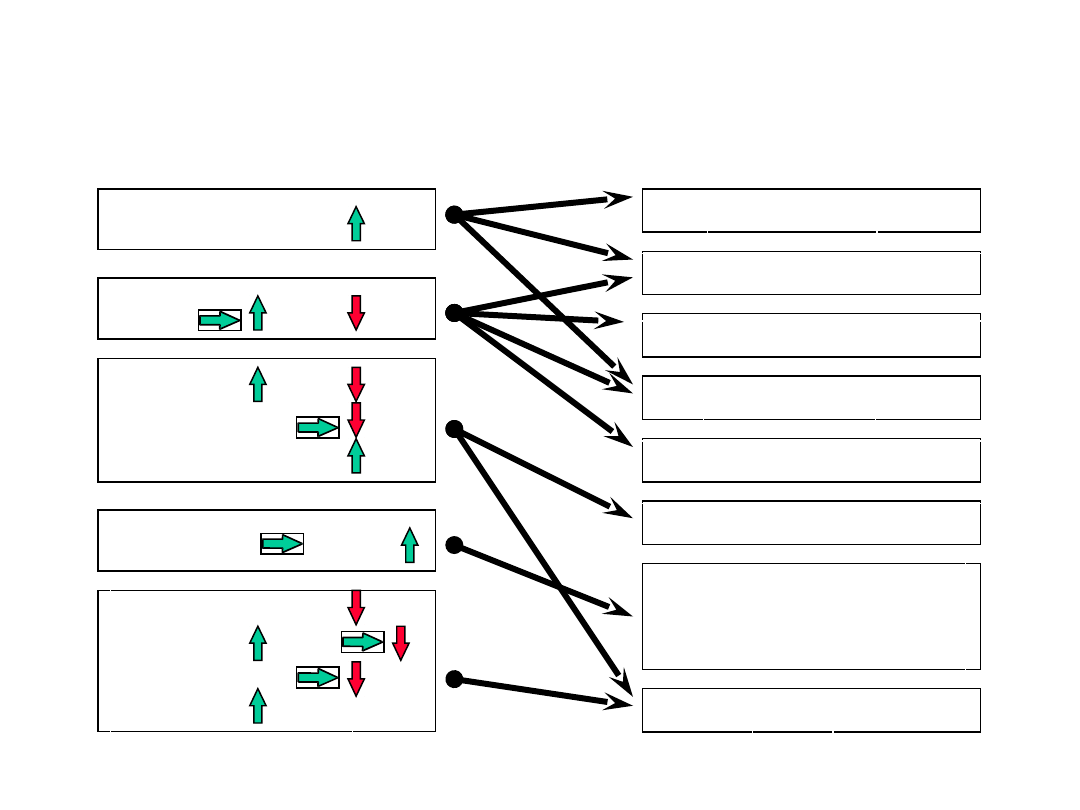
Interpretacja badań c.d.
APTT
APTT
PT
APTT
PT
Fibrynogen
FDP
Fibrynogen FDP
TPK
APTT
PT
Fibrynogen
FDP
Hemofilia
Inne zaburzenia krzepnięcia
Niedobór wit.K / Zab. wchłaniania
Heparyna
Doustne antykoagulanty
Niewydolność wątroby
DIC
Aktywacja fibrynolizy,
niedobór
alfa2-antyplazminy
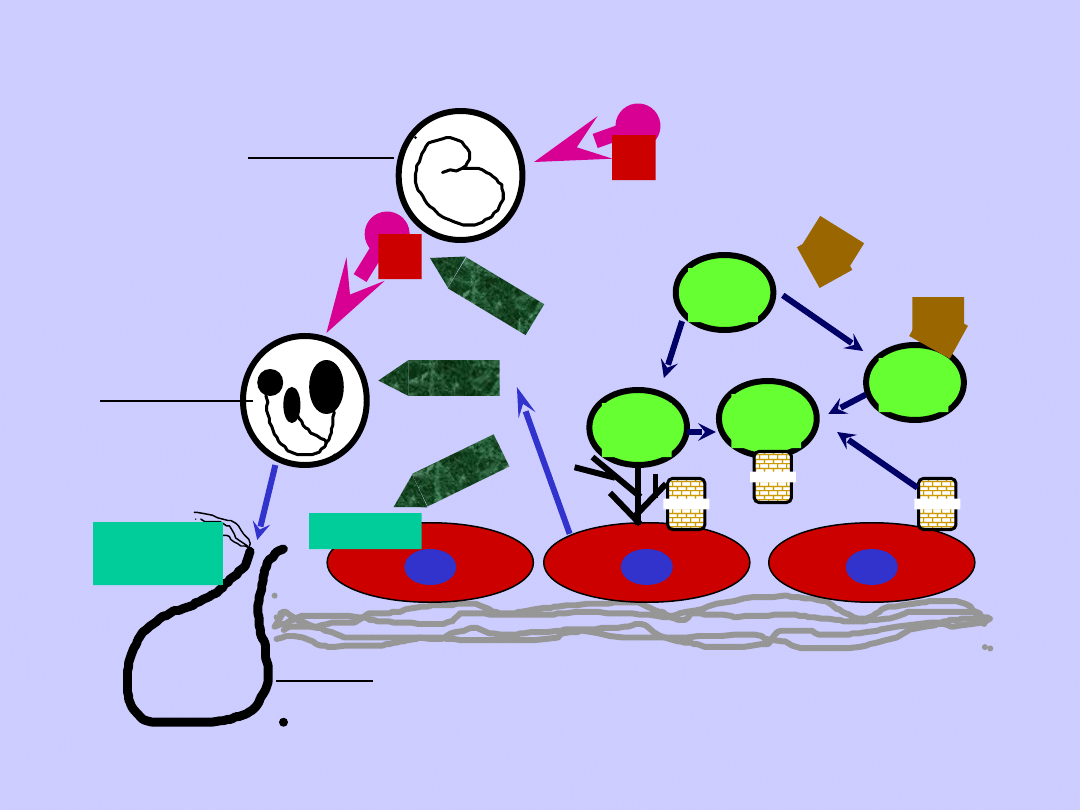
AT
AT
AT
AT
Trombina
Trombina
Trombina
Hep
Hep
Uszkodzenie
śródbłonka
Adhezja
E
E
PGI2
PG
I2
PG
I2
Endotoksyna
Endotoksyna
Cytokiny
Monocyty
Neutrofile
Proteazy,
O
2
, H
2
O
2
GAG
Komórki śródbłonka
ARDS
Wysięk
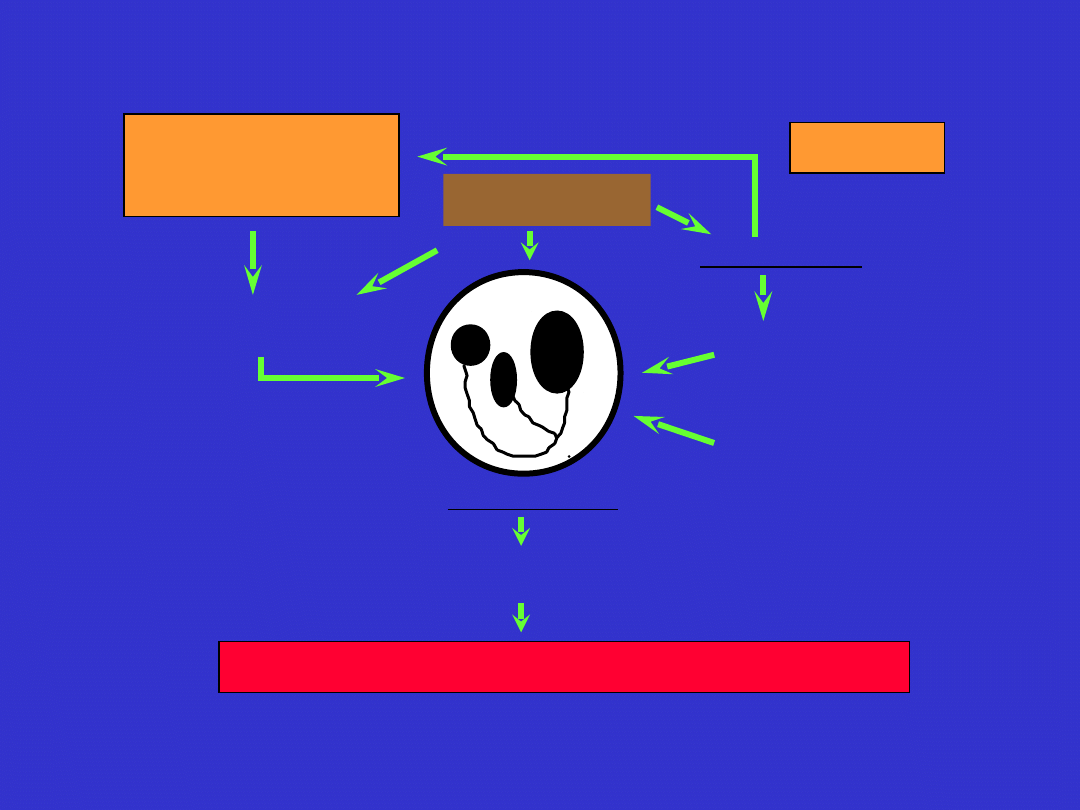
Neutrofile
Elastaza
i inne mediatory
Uszkodzenie płuca, niewydolność oddechowa
Rozsiane
wykrzepianie
wewnątrznaczyniowe
Infekcja
Endotoksyna
Monocyty
Cytokiny
C5a
XIIa, kalikreina
Cytokiny, cz. tkankowy
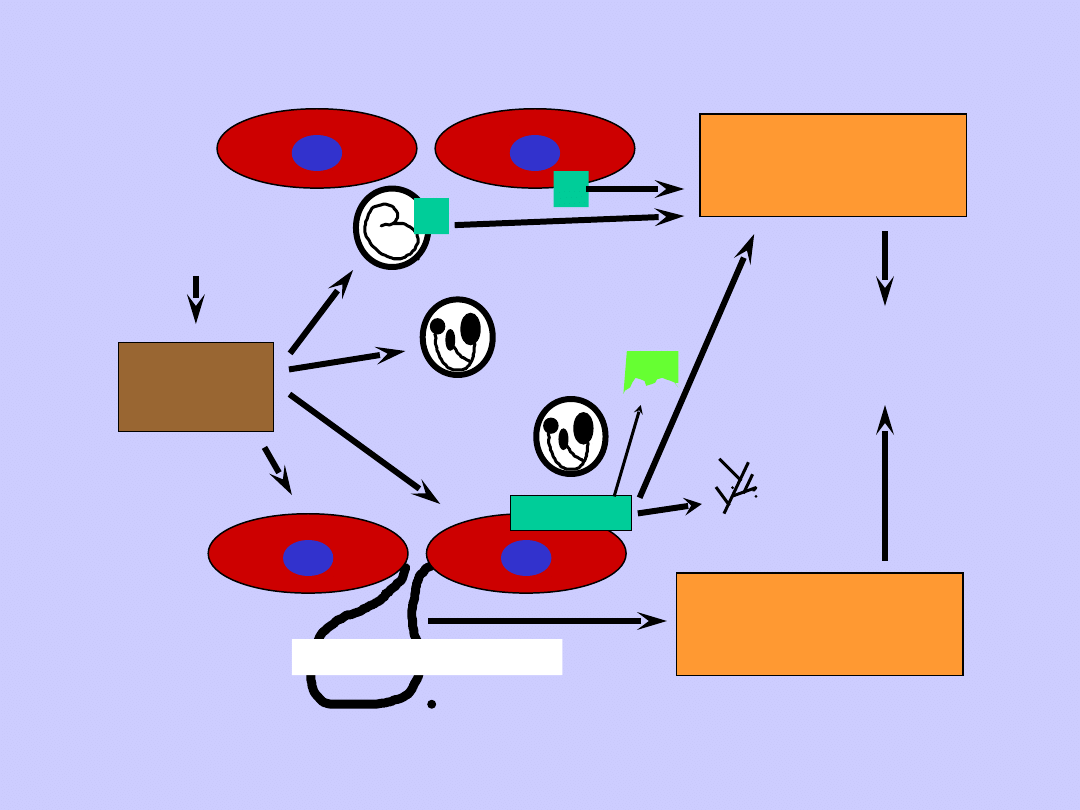
Rozsiane
wykrzepianie
wewnątrznaczyniowe
MODS
ARDS
Niewydolność wątroby
Cytokiny
(TNF, IL-1)
Sepsa,
uszkodzenie tkanek
TF
TF
TM
ELAM-1
GAG
Elastaza
Wolne rodniki
Uszkodzenie śródbłonka
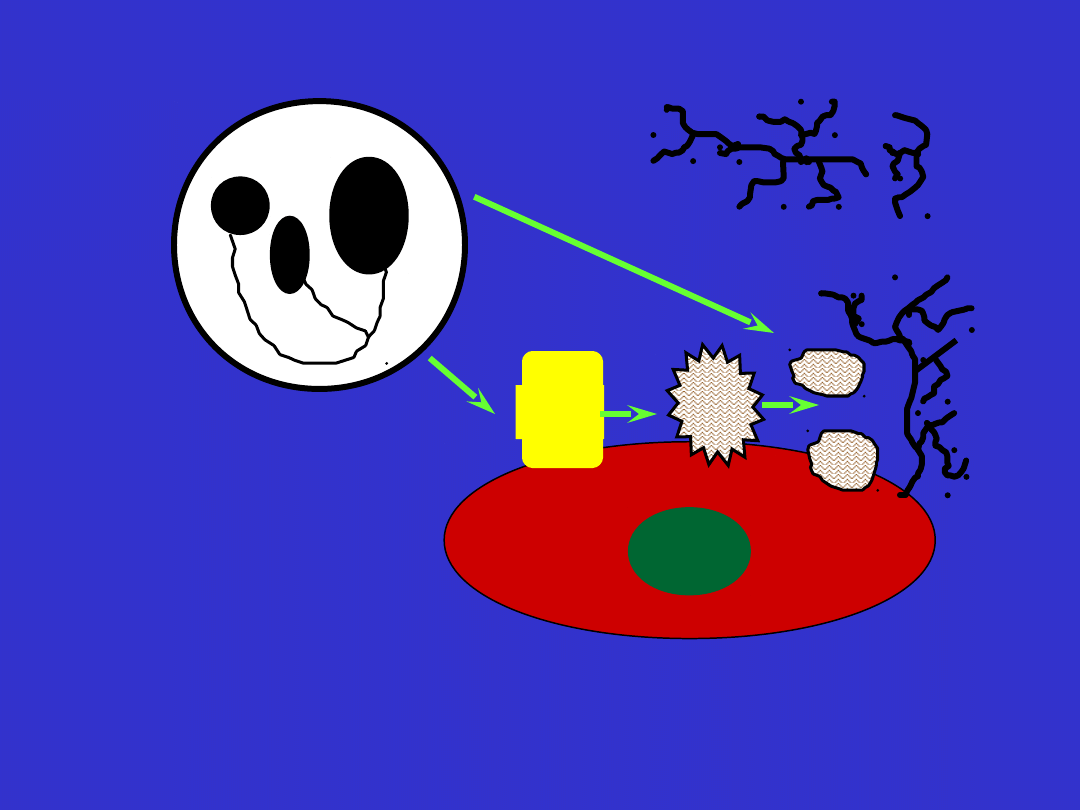
TM
TM
T
T
GAG
Neutrofil
Komórka śródbłonka
Elastaza
Katepsyna G
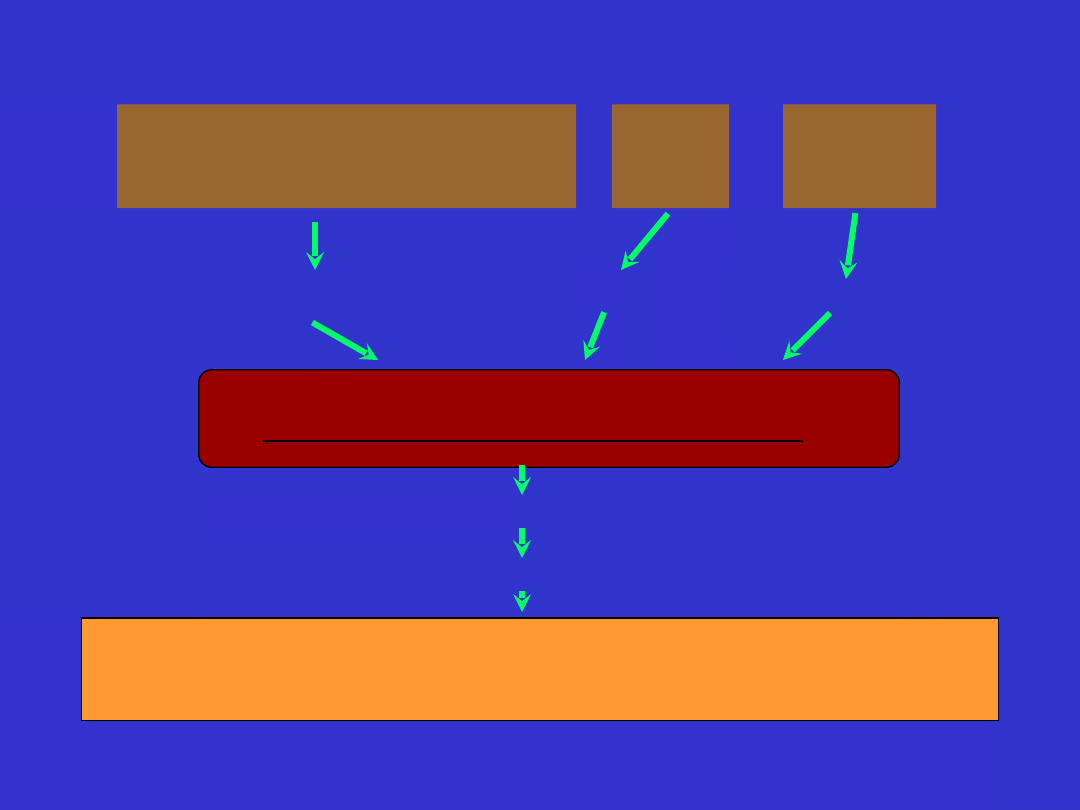
Rozsiane wykrzepianie wewnątrznaczyniowe
Czynnik tkankowy (TF)
Powikłania Piorunujące
Uraz
położnicze zap. wątroby
mnogi
Guzy
lite
Sepsa
Uszkodzenie tkanek
Komórki guza
Leukocyty
Aktywacja toru zewnątrzpochodnego
Mikrozatory

Fizjologiczne inhibitory
układu krzepnięcia
• Antytrombina III + siarczan heparanu,
• II kofaktor heparyny + siarczan
dermatanu,
• Białko C + trombina + trombomodulina.

Heparyna jest kofaktorem
AT III
• swoje działanie antykoagulacyjne heparyna
wywiera za pośrednictwem antytrombiny
III,
• w przypadku niedoboru AT III,
podana heparyna nie hamuje wystarczająco
krzepnięcia,
• jej skuteczność zarówno profilaktyczna,
jak i lecznicza jest niedostateczna.
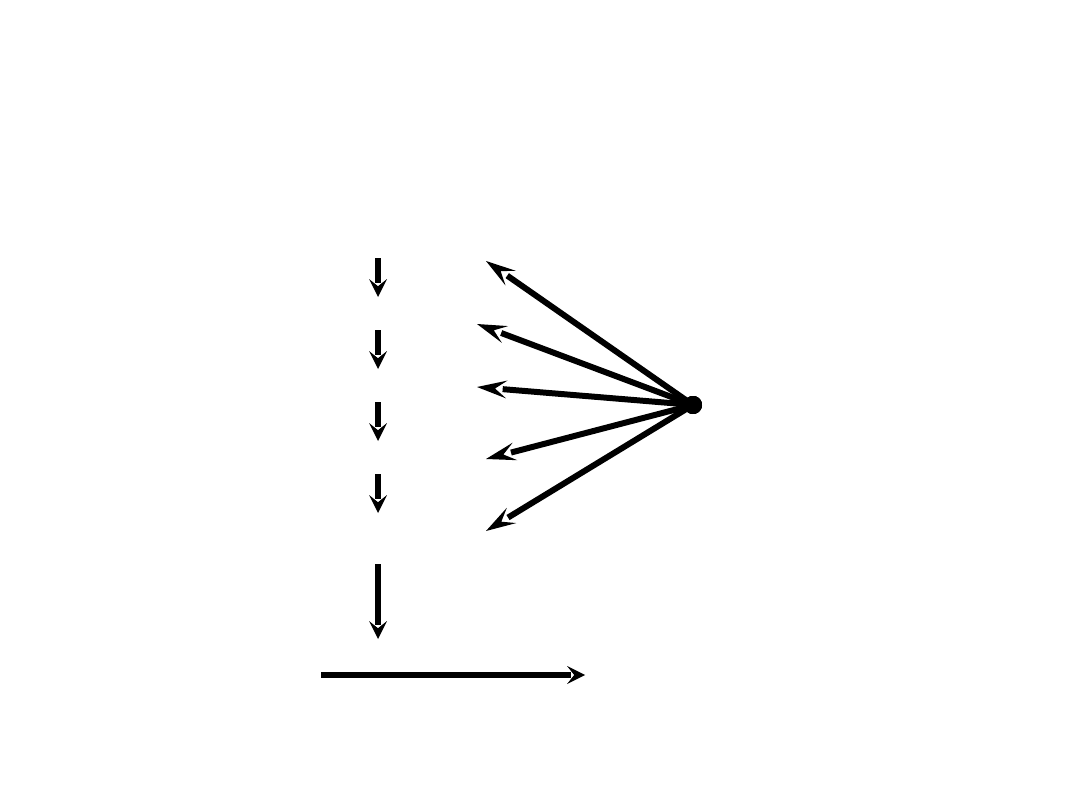
Działanie kompleksu AT III -
heparyna
Fibrynogen
Skrzep
XII a
XI a
VIII c - IX a
V a - X a
II a
Kompleks
AT III - heparyna
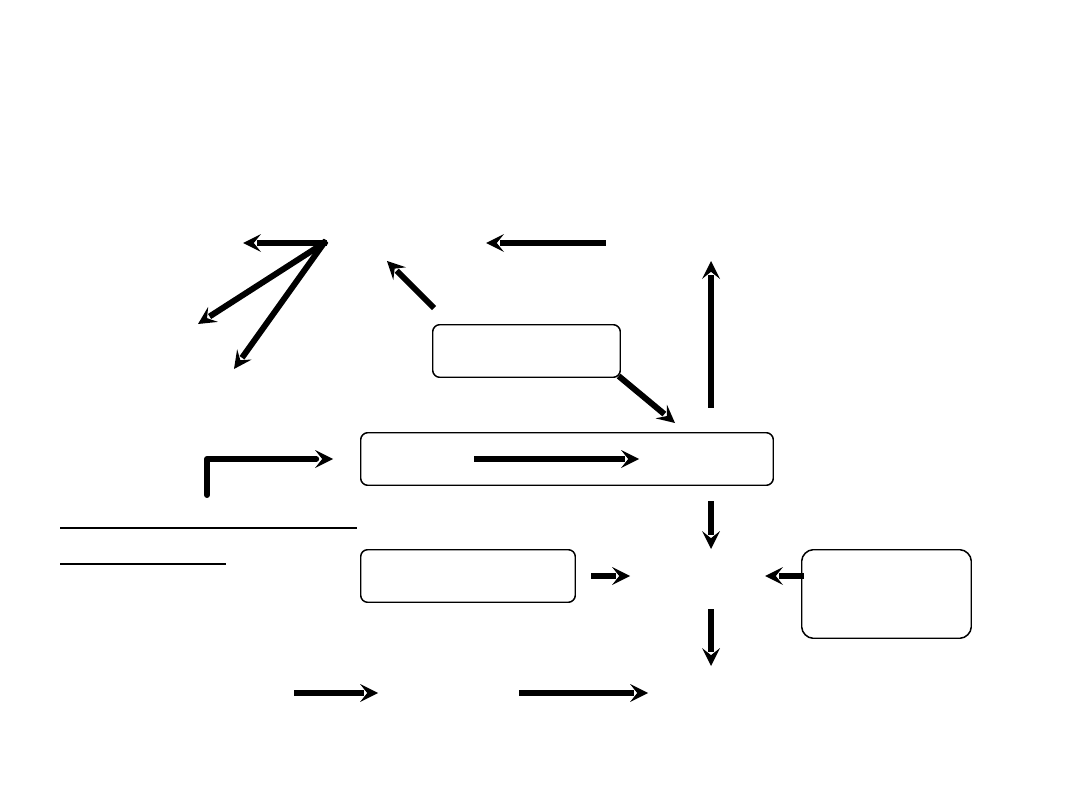
Aktywacja krzepnięcia przez
kontakt
Kalikreina
Prekalikreina
F XII
F XII a
Antytrombina III Trombina Heparyna
kofaktor II
Plazminogen
Plazmina
Skrzep
Dopełniacz
Kininy
Fibrynoliza
C1 - inhibitor
Fibrynoliza
Droga kontaktu /
aktywacja

Leczenie zespołu
wykrzepiania
śródnaczyniowego
1. Rozsądne, ale agresywne leczenie
przyczynowe,
2.Intensywna terapia wspomagająca,
3.Lecznicze uzupełnianie inhibitorów
krzepnięcia.
4.Leczenie przeciwzakrzepowe.

Lecznicze uzupełnianie
inhibitorów krzepnięcia
• C1 - inhibitor - blokowanie wewnętrzpochodnego toru
krzepnięcia. Jest to najsilniejszy inhibitor cz.XIIa
,kalikreiny, podjednostek dopełniacza C1r i C1s,
• Inhibitory trombiny : AT III , Białko C , Białko S,
• TFPI - specyficzny inhibitor czynnika tkankowego
(blokowanie zewnętrzpochodnego toru krzepnięcia),
• anty - TF - mononuklealne przeciwciała anty - TF.

Leczenie
przeciwzakrzepowe.
• Heparyna niefrakcjonowana,
• Heparyna
drobnocząsteczkowa,
• Analogi heparyny.

Testy w DIC
Testy przesiewowe:
• PT - czas protrombinowy,
• TT - czas trombinowy,
• APTT - czas częściowej
aktywowanej tromboplastyny,
• Liczba płytek.

Testy w DIC c.d.
Testy potwierdzające:
• D - dimery,
• monomery fibryny,
• AT III,
• fibrynogen,
• czas reptilazowy.

Główne funkcje
śródbłonka
w warunkach
fizjologicznych
• Sekrecja (renina, endotelina,
tlenek azotu, prostacyklina),
• Katabolizm (prostaglandyny
PGE
2
, aktywne aminy).

Śródbłonek odgrywa
ważną rolę w:
• hemostazie,
• regulacji napięcia
naczyniowego,
• fibrynolizie.

Pod wpływem cytokin
komórki śródbłonka:
• tracą zdolność wytwarzania
trombomoduliny,
• zaczynają wytwarzać czynnik
tkankowy: inhibitor
aktywatora plazminogenu (PAI
- 1).

Powierzchnię śródbłonka
pokrywa glikokaliks:
• glikozaminoglikany (80%
stanowi siarczan heparanu),
• glikolipidy.

Śródbłonek naczyń
syntetyzuje:
• siarczan heparanu,
• siarczan dermatanu,
• siarczan
chondroityny,
• kolagen,
• elastynę,
• fibronektynę,
• witronektynę,
• składową C
3
dopełniacza,
• czynnik von
Willebranda,
• czynniki mitogenne:
PDGF, FGF, EDGF,
• EDRF, NO,
• prostacyklina,
• t - PA, u - PA,
• PAI, białko C i S

AT III: jednołańcuchowa
glikoproteina, zbudowana z 424
aminokwasów
o m.c. 58000 - 61000 D
Synteza
Wątroba, komórki śródbłonka,
megakariocyty
Miejsce magazynowania
w ustroju
Przestrzeń pozakomórkowa: 50%,
Plazma: 40%,
Komórki śródbłonka naczyń: 10%
Biologiczny okres półtrwania 65 godzin, w DIC: 3 - 4 godz.
Stężenie w osoczu
30 mg/100 ml
Aktywność
80 - 120% (100% = 100 IU / dl)
Minimalna skuteczna
aktywność
70%

Rak stercza
• pierwotna fibrynoliza czy
pierwotne DIC?
• DIC z wtórną fibrynolizą +
pierwotna aktywacja układu
fibrynolitycznego,
• przewaga procesu fibrynolizy nad
wykrzepianiem.

Przyczyny DIC w
nowotworach
• nowotworzenie naczyń, które mają
wadliwą wyściółkę śródbłonkową,
mogącą aktywować układ krzepnięcia,
• guzy lite mogą uwalniać do krążenia
martwicze tkanki i enzymy komórkowe,
które aktywują układ krzepnięcia (TF),
• nieenzymatyczna aktywacja cz. X przez
reszty kwasu sjalowego mucyny w
gruczolakorakach śluzowych.

Przyczyny spadku
aktywności AT III w
posocznicy
• zwiększone zużycie,
• dramatycznie skrócony okres
półtrwania
z 48 do 3 godzin, pomimo nasilonej
produkcji w wątrobie,
• inaktywacja AT III przez elastazę
uwalnianą z aktywowanych neutrofili.

Endotoksyna bakteryjna
ma zdolność:
• bezpośredniego aktywowania cz. XII,
• wywoływania reakcji uwalniania
substancji z płytek krwi,
• uszkadzania śródbłonka,
• uwalniania substancji
prokoagulacyjnych
z granulocytów.

Dekstrany: 10 ml / kg
• obniżają zdolność agregacyjną płytek,
• hamują polimeryzację włóknika,
czyniąc go bardziej podatnym na
działanie plazminy,
• pod wpływem dekstranów dochodzi
do zwiększonego uwalniania tPA
przez śródbłonek naczyniowy.

• New therapeutic implications of antithrombin III replacement in
disseminated intravascular coagulation and multiple organ failure
K. Okajima et al., Intensivmed. 1996
• posocznica Gram-dodatnia
DIC
ARDS
MOF
AT-III:
działanie przeciwkrzepliwe
dodatkowe działanie przeciwzapalne
• AT-III wzmaga uwalnianie prostacykliny z komórek śródbłonka na
drodze interakcji z GAG-ami obecnymi na powierzchni komórki
– PGI
2
hamuje wydzielanie cytokin, wolnych rodników tlenowych
z pobudzonych neutrofilów oraz TNF-u z pobudzonych
monocytów
– PGI
2
hamuje aktywację leukocytów
• Heparyna niweczy to działanie
Działanie przeciwzapalne
AT III

Attenuation of Endotoxin-induced Pulmonary Vascular Injury by
Antithrombin -III
M. Uchiba et al.; 1996
Heparin - like Glycosaminoglycan is a Receptor for Antithrombin-III-
dependent but not for Thrombin-dependent Prostacyclin Production
in Human Endothelial Cells
S. Horie et al.; Thromb. research 1990
Antithrombin Replacement in DIC and MOF
K. Okajima et al. ??
- cytokiny lub pobudzone leukocyty w patofizjologii DIC and MOF
- szczególną uwagę zwrócono na mechanizm działania AT-III in DIC
and MOF, gdzie ważną rolę odgrywają mediatory stanu zapalnego z
pobudzonych leukocytów.
Działanie przeciwzapalne
AT III

Heparin -like Glycosaminoglycan is a Receptor for Antithrombin
-III dependent but not for Thrombin-dependent Prostacyclin
Production in Human Endothelial Cells
S. Horie et al.; Thromb. research 1990
• Badano wpływ trombiny i ATIII na wytwarzanie prostacycliny;
próbowano też ustalić, które receptory odpowiadają za
uwalnianie PGI
2
• Uwalnianie prostacycliny z HUVEC jest indukowane przez AT-III
(HUVEC: cultured human umbilical vein endothelial cells)
• Mechanizm: AT-III wiąże się z GAG-ami
• Wytwarzanie prostacycliny indukowane przez AT-III jest
niezależne od jej wytwarzania indukowanego przez trombinę
Działanie przeciwzapalne
AT III

Experimental Endotoxemia in Humans: Analysis of Cytokine Release and
Coagulation, Fibrinolytic and Complement Pathways
S.J.H. van Deventer, Blood 1990
• Endotoksemia u sześciu zdrowych ochotników: celem pracy było zbadanie
uwalniania cytokin i następstw klinicznych i hematologicznych tego zjawiska
– stężenie TNF osiągnęło maksymalny poziom po 60 min.
– stężenie IL-6 osiągnęło maksymalny poziom po 20 to 150 min.
– Temperatura ciała i tętno wzrosły w tym samym czasie
– Spadek ciśnienia tętniczego krwi po 120 min.
– Aktywacja układu krzepnięcia po 120 min. (F 1+2; TAT)
– Aktywacja komórek śródbłonka (t-PA, vWF)
– Aktywność fibrynolityczna
• Zebrane dane sugerują, że do leukopenii wywoływanej przez
endotoksyny i do aktywacji komórek śródbłonka dochodzi za
pośrednictwem TNF
Działanie przeciwzapalne
AT III

Niedobór AT-III
• The Clinical Significance of Inhereted Antithrombin Deficiency
U. Abildgaard et al., Biom. Prog. 1990
– Tło genetyczne
– Kiedy należy podejrzewać niedobór AT-III
– Kiedy rozpoznaje się niedobór AT-III
– Środki zapobiegawcze
»
przewlekłe leczenie doustnymi lekami przeciwkrzepliwymi
»
ciąża: s.c. heparyna 15.000 -35.000 IU / dobę
»
operacja, uraz: 2.000 IU / dobę przez 2-4 dni

Niedobór AT-III
• Acquired Antithrombin III Deficiency and Risk of
Thromboembolism
G. Finazzi et al., Biom. Prog. 1990
– Zespół nerczycowy
– Doustne środki antykoncepcyjne
– Leczenie L-Asparaginazą
– Choroby wątroby
– DIC,
– Rozległy zabieg operacyjny,
– Ciężki uraz,
– Choroby nowotworowe,
– Posocznica

DIC
• High Dose of Intravenous Antithrombin III Without Heparin in the
Treatment of Disseminated Intravascular Coagulation and Organe
Failure in Four Children
S. Fuse et al., 1996
• Doniesienie: 4 dzieci z DIC and MOF
– Zespół Reye’a
– Operacja na otwartym sercu
– Niewydolność krążenia (2x)
• AT-III podawano w dawce 120-150 U/kg/d. przez 2-3 dni (bez heparyny)
(była to dawka AT-III 3-6 razy wyższa niż stosowana zazwyczaj)
• Wszyscy opisywani pacjenci wyzdrowieli szybko i bez powikłań w
ciągu 14 dni

• Antithrombin Concentrates in Heparin-Resistant Cardiopulmonary
Bypass Patients
M.S. Irani , 1996
• 12 pacjentów poddawanych zabiegom na otwartym sercu (CPB wymaga
stosowania leków przeciwkrzepliwych)
• Skuteczność antykoagulacji monitorowano określając czas ACT (>
400s)
• Oporność na heparynę: gdy po bolusie 300U/kg ACT był < 400s
• Heparin podawana przed AT-III:
306-1070 U/kg
• AT-III (Bayer)
:
1080 - 3408 U
• ACT przed AT-III:
250 - 395 s po:
427 - > 1500 s.
• stosowanie AT III, gdy heparyna nie zapewnia wystarczającej
antykoagulacji, jest prawdopodobnie bezpieczniejsze niż
podawanie nadmiernych dawek heparyny lub
Chirurgia serca

Chirurgia serca
• Fibrinolysis, Antithrombin III and Protein C in Neonates During Cardiac
Operations
Petäjä et al. , 1996
• Badano stan układu krzepnięcia i fibrynolizy (parametry laboratoryjne)
u 10 noworodków (4-14 dni) po operacjach na otwartym sercu (CPB)
• Haemostazę podczas operacji kontrolowano podając FFP,
krioprecypitat, koncentrat płytkowy ,IX czynnik krzepnięcia and
aprotinin
• U 9 patients aktywność AT-III spadła poniżej wartości prawidłowej,
• U trojga doszło do zakrzepicy żył centralnych, jeden noworodek zmarł

Chirurgia serca
• Heparin and Antithrombin III Levels During Cardiopulmonary Bypass
K. Hashimoto et al., 1995
• Podczas CPB poziom AT-III spada
• badanie kontrolowane, prospektywne, randomizowane
• 14 pacjentów pediatrycznych: 6 otrzymywało 1000 IU heparyny (bolus); 200
IU/kg
8 otrzymywało 1000 IU heparyny (bolus); 200 IU/kg + 1000
IU AT-III (75 IU/kg)
• Aktywność AT-III : pozostała na stałym poziomie, który był wyższy
niż w grupie kontrolnej
• ACT: najbardziej wydłużony w grupie otrzymującej AT-III
• Fibrynopeptid A: poziom pozostał prawie stały (niski) w grupie
otrzymującej AT-III

Ch. W. Francis et al.
J. of Bone and Joint Surgery 1989, 1990
• Do zakrzepicy żylnej dochodzi: 45-70% po plastyce stawu biodrowego
41- 84% po plastyce stawu kolanowego
- W 1 to 3% dochodzi do śmiertelnej zatorowości płucnej
• Aktywność AT- III spada po zabiegu operacyjnym
( w przypadku zaburzeń wrodzonych do 50% normy)
po wymianie stawu biodrowego < po operacji brzusznej
• Dwa prospektywne randomizowane badania potwierdzają bezpieczeństwo i
skuteczność kombinacji AT- III heparyny w niskich dawkach (w porównaniu z
dekstranem 40) :
03 pacjentów po plastyce stawu biodrowego
83 pacjentów po plastyce stawu kolanowego
• Wszyscy pacjenci, u których aktywność AT III była mniejsza niż 65%, mieli
zakrzepicę
Zakrzepica żylna po plastyce stawu biodrowego i
kolanowego : działanie profilaktyczne antytrombiny III i
heparyny

Zakrzepica żylna po plastyce stawu biodrowego i
kolanowego : działanie profilaktyczne antytrombiny III i
heparyny
Ch. W. Francis et al.
Grupa AT-III / Heparyna
STAW BIODROWY
• 1500 IU AT-III 2 godziny przed
zabiegiem
• 1000 IU/day przez 5 dni po
zabiegu
• 5000 IU Heparin s.c. co 12
godzin
2 godziny przed zabiegiem, a
potem do 5 dnia po operacji
STAW KOLANOWY
• 3000 IU AT-III 2 godziny przed
zabiegiem
• 2000 IU/day przez 5 dni po
zabiegu
Grupa AT-III / Heparyna
STAW BIODROWY
• 1500 IU AT-III 2 godziny przed
zabiegiem
• 1000 IU/day przez 5 dni po
zabiegu
• 5000 IU Heparin s.c. co 12
godzin
2 godziny przed zabiegiem, a
potem do 5 dnia po operacji
STAW KOLANOWY
• 3000 IU AT-III 2 godziny przed
zabiegiem
• 2000 IU/day przez 5 dni po
zabiegu
Grupa otrzymująca dextran 40
• 10 ml/kg
początek 2 godziny przed
zabiegiem, czas wlewu 12
godzin
• 7 ml/kg BW / dobę przez 5,5 dni
50% przypadków zakrzepicy
żylnej w grupie otrzymującej
dekstran, po operacjach na
stawie kolanowym, przy
dawkach takich jak do operacji
na stawie biodrowym
27% przypadków u pacjentów
otrzymujących podwójną dawkę
Grupa otrzymująca dextran 40
• 10 ml/kg
początek 2 godziny przed
zabiegiem, czas wlewu 12
godzin
• 7 ml/kg BW / dobę przez 5,5 dni
50% przypadków zakrzepicy
żylnej w grupie otrzymującej
dekstran, po operacjach na
stawie kolanowym, przy
dawkach takich jak do operacji
na stawie biodrowym
27% przypadków u pacjentów
otrzymujących podwójną dawkę
Zakrzepica żylna po plastyce stawu biodrowego i
kolanowego : działanie profilaktyczne antytrombiny III i
heparyny
Ch. W. Francis et al.
AT-III
DEXTRAN
STAW BIODROWY (83 pacjentów):
Pacjenci, u których wykonywano wenografię 41
42
Zakrzepica żylna
2 (4,9%)
12 (28,6%)
Proteza cementowa (56 pacjentów)
- Zakrzepica 2 (7,4%)
12 (40%)
Proteza inna niż cementowa (26 pacjentów)
- Zakrzepica 0
0
STAW KOLANOWY
Pacjenci, u których wykonywano wenografię 39
38
Zakrzepica żylna 14 (36%
)
31 (82%)
Aktywność AT-III
> 100 %
> 70%
Wszyscy pacjenci, u których aktywność AT III była mniejsza niż 65%,
mieli zakrzepicę

Sepsa
Inflammatory Mediators and Their Influence on Haemostasis
A. Salgado et al., Haemostasis 1994
Mechanizm ogólnoustrojowej odpowiedzi zapalnej jest
skomplikowany
-
aktywacja różnych rodzajów komórek (monocyty/makrofagi,
neutrofile, komórki śródbłonka)
-
uwalnianie mediatorów procesu zapalnego (np. cytokin )
Antithrombin - III Stimulates Prostacyclin Production by
Cultured Aortic
Endothelial Cells
T. Yamauchi, 1989
Wyniki sugerują, że ATIII może stymulować wytwarzanie PGI
2
na
drodze wiązania się z cząsteczkami na powierzchni śródbłonka, które
mają budowę podobną do heparyny.

• Antithrombin-III: A Causal Therapeutic Regime in Children Suffering
from Consumption Coagulopathy due to Septicaemia
U. Novak-Göttl, 1992
• opisuje leczenie nabytego niedoboru AT-III i DIC u dzieci tylko
preparatem Kybernin P
2 grupy:
noworodki+sepsa (n 21)
noworodki i dzieci (n 18)
dawkowanie:
200 U AT-III/kg/dobę
80 U /kg/dobę ciągły wlew
w obu gr.
+ heparyna 50 IE /kg/dobę
Aktywność ATIII:18 - 63,5 - 85,5 - 75 %
38 - 92 - 98 - 113 %
śmiertelność:
10 /21 3/18
zgon/sepsa: 1/10 1/3
• zalecenia: 100 IU AT-III/kg/d. u dzieci: obowiązkowo należy
określać aktywność AT-III kilkukrotnie w ciągu dnia;
SEPSA

• AT-III Replacement DIC and MOF
K. Okajima et. al
• AT-III + Heparyna może być bardziej skuteczna u pacjentów z
DIC z powodu powikłań położniczych
• Stosowanie samej AT-III może być bardziej skuteczne niż jej
połączenie z heparyną w leczeniu DIC u pacjentów, u których
występują zaburzenia krzepnięcia i uszkodzenie narządów
poprzez aktywację leukocytów
SEPSA
SEPSA
• Meningococcemia and Purpura Fulminans in Adults: Acute deficiencies
of protein C and S and early Treatment with Antithrombin III
Concentrates
Fourrier et al., 1989
• Badanie 5 pacjentów z piorunującą plamicą (purpura fulminans)
• Stwierdzono spadek poziomu AT-III, białka C i białka S
• AT-III: natychmiast 60 IU /kg/ 3h - “loading dose”; 60 IU /kg/24h przez
2 dni
+LMWH (20mg/24h)
• po 24h aktywność AT-III całkowicie wróciła do normy, poziom białka C
pozostał niski u 4 pacjentów
Dzięki uzupełnieniu AT III doszło do niezwykle szybkiej poprawy objawów
ciężkiej infekcji z niewydolnością wielonarządową, łącznie z centralnym
układem nerwowym, układem krążenia i nerkami).
• AT-III kompensuje ostry spadek aktywności białka C

• Substitution of AT-III in Shock and DIC: A Randomized Study
B. Blauhut et al., 1985
• Badanie randomizowane u 51 pacjentów we wstrząsie z DIC
• Kryteria włączenia: AT-III< 70%
3 grupy:
Heparyna
AT-III AT-III & Heparyna
dawki:
3000 IU,
aktywność 100%, = grupa 2 +1000
IU,100 IU/h
250IU/h gdy aktywność< 80%
• Aktywność w grupie 1 pozostała bez zmian
• 12 z 51 pacjentów zginęło, bez wyraźnego związku z DIC
• czas trwania DIC najkrótszy w grupie AT-III (42h)
• jednoczesne stosowanie heparyny nie wykazało dodatkowych
korzyści
SEPSA

Proszę się obudzić!
Teraz będzie coś ważnego...

Dziękuję za uwagę

A teraz...
Ten pan z drugiego rzędu
powie,
co było na poprzednim
przeźroczu...
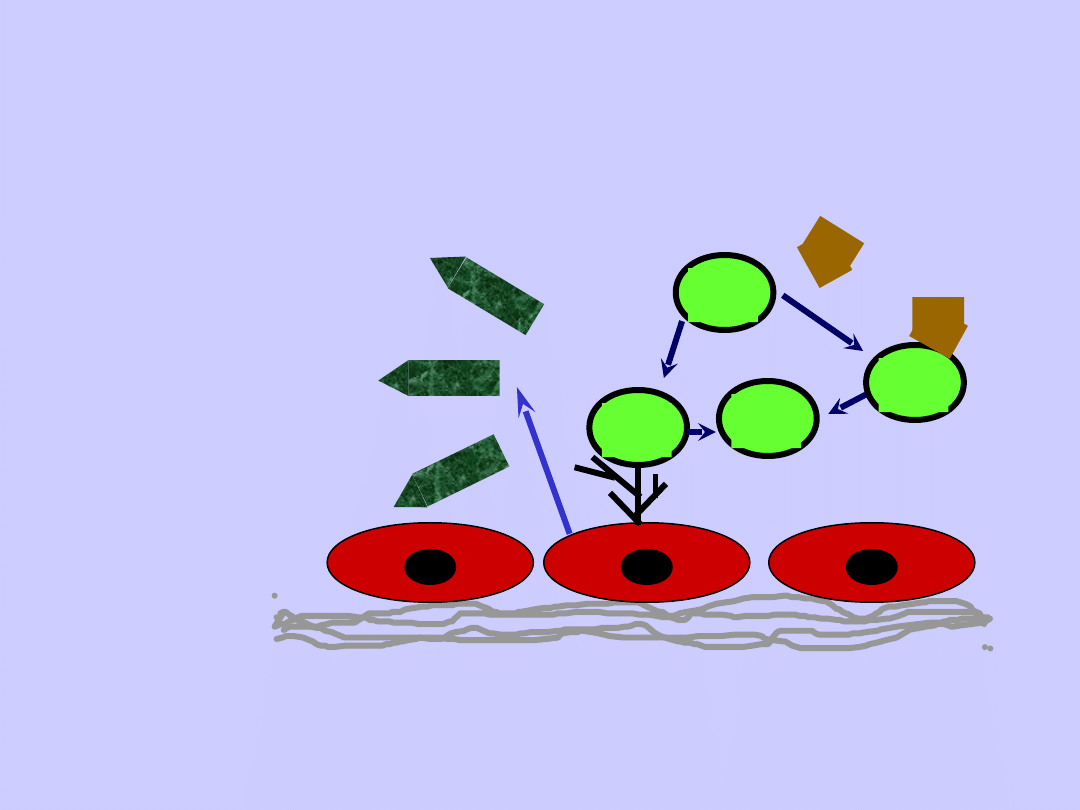
AT
AT
AT
AT
Hep
Hep
PGI2
PG
I2
PG
I2
GAG
Komórki śródbłonka
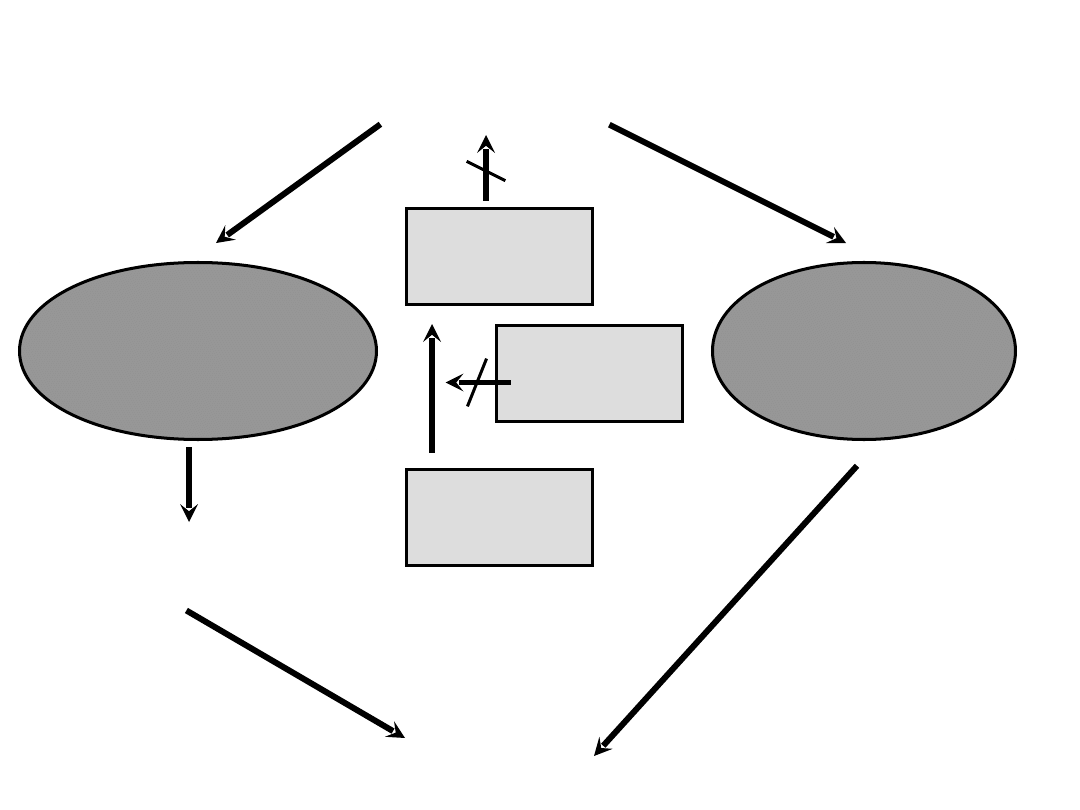
Cytokiny
PGI2
Hep
AT III
MOF
Aktywacja toru
Uszkodzenie
zewnątrzpochodnego
śródbłonka
DIC

Antytrombina III:
nie tylko
inhibitor układu krzepnięcia
Małgorzata Złotorowicz
Centrum Medyczne
Kształcenia Podyplomowego
Warszawa
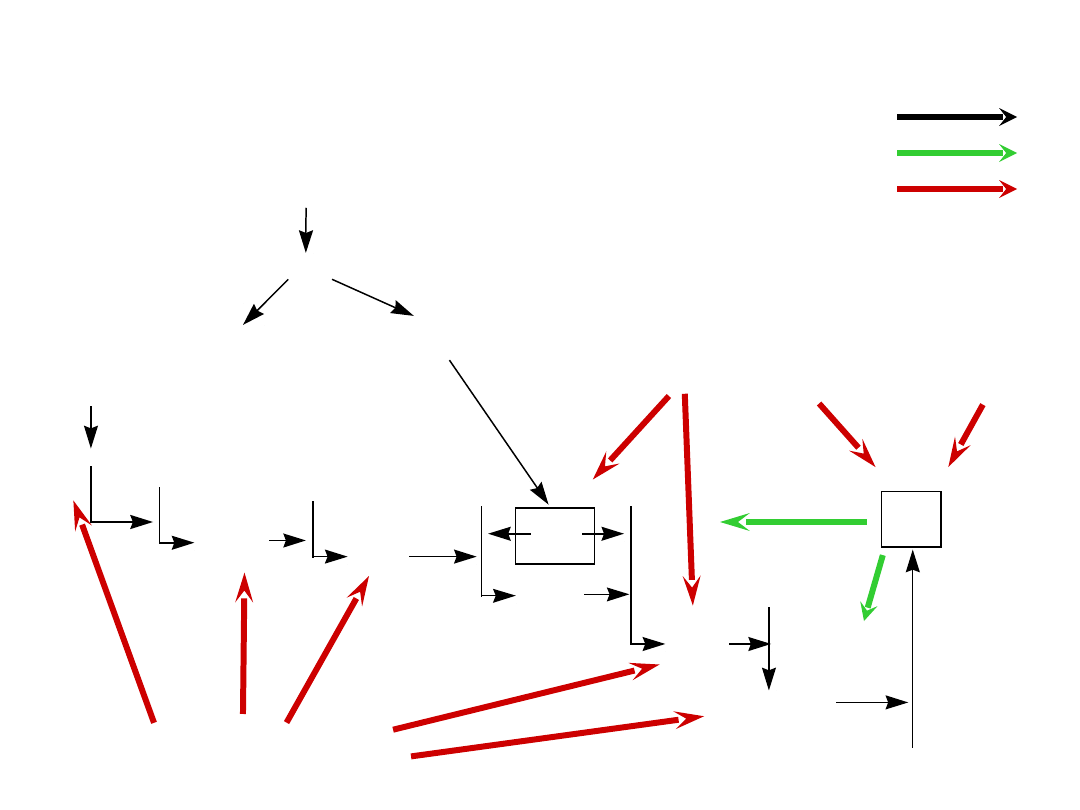
USZKODZENIE KOMÓREK
BC
BS
BCa
TM
cz. Va
Ca
2+
PROKALIKREINA
KALIKREINA
cz. XII
cz. XIIa
cz. XI
cz. XIa
Ca
2+
HMK
TF
cz. VIII
cz. IX
cz. X
PROTROMBINA
cz. IXa
cz. Xa
TROMBINA
KOLAGEN
CZYNNIK TKANKOWY
TF
INHIBITOR
BIAŁKA C
TFPI
ANTYTROMBINA III
INHIBITOR
TRYPSYNY
URAZ, SEPSA, WSTRZĄS
inhibitor
inaktywator
reakcja
KASKADA KRZEPNIĘCIA
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
Wyszukiwarka
Podobne podstrony:
Leki hematologia, Leki stosowane w zaburzeniach krzepni˙cia i wytwarzania kom˙rek krwi
4 Ćwiczenia Patofizjologia zaburzeń krzepnięcia krwi1
Problemy związane z diagonstyką zaburzeń krzepnięcia (dla le
Ostre zaburzenia krzepnięcia
PATOMECHANIZMY ZABURZEŃ KRZEPNIĘCIA KRWI
Zaburzenia krzepnięcia
ZABURZENIA KRZEPNIĘCIA I WYTWARZANIA KOMREK KRWI, Studia, farmakologia
zaburzenia krzepnięcia atest 2009 2
Zaburzenia krzepni cia krwi23
LEKI STOSOWANE W ZABURZENIACH KRZEPNIÄCIA KRWI, farmakologia
Zaburzenia krzepnięcia
Zaburzenia krzepnięcia 3
4 Ćwiczenia Patofizjologia zaburzeń krzepnięcia krwi2
Zaburzenia nerwicowe wyklad
Zaburzenia funkcji zwieraczy
Seminarium3 Inne zaburzenia genetyczne
więcej podobnych podstron