
1
Andrzej Wojtowicz
pokój 331
konsultacje wtorek 12.00 –
14.00
www.fizyka.umk.pl/~andywojt

2
LITERATURA i materiały pomocnicze
H.E. Enge, M.R. Wehr, J.A. Richards,
Wstęp do fizyki atomowej,
PWN, Warszawa 1983
H. Haken, H.C. Wolf,
Atomy i kwanty, PWN, Warszawa 2002
Richard P. Feynman,
Feynmana wykłady z fizyki. T. III
D. Halliday, R. Resnick, J. Walker
Podstawy fizyki, t. 5, rozdz. 39, 40, 41
Andrzej Wojtowicz:
www.fizyka.umk.pl/~andywojt

3
PODSTAWY MECHANIKI
KWANTOWEJ
Richard P. Feynman,
Feynmana wykłady z fizyki
T. I rozdz. 37 i 38
T. III rozdz. 3 i 7

4
PLAN WYKŁADU
Atomowa struktura materii
Elektryczność, a atomowa struktura
materii
Korpuskularny charakter
promieniowania elektromagnetycznego
Falowy charakter cząstek
materialnych
Proste modele atomu
Atom wodoru w mechanice kwantowej
Atom wodoru i jony wodoropodobne;
atomy wieloelektronowe; układ
okresowy; widma atomów metali
alkalicznych
Momenty magnetyczne i poprawki
energetyczne do struktury energetycznej
atomu wodoru

5
PLAN WYKŁADU
Struktura subtelna w atomie
wodoru; oddziaływanie spin – orbita,
struktura nadsubtelna
Funkcje falowe elektronu w atomie
wodoru z uwzględnieniem spinu,
składanie momentów pędu
Zasada Pauliego; atom helu
Rozszczepienie subtelne,
oddziaływanie spin-orbita, sprzężenie
L – S
Sprzężenie j – j, reguły wyboru,
zjawisko Zeemana. Promieniowanie X
a energetyczna struktura atomów
Cząsteczki; wiązania chemiczne

6
Atomowa struktura materii
Elektryczność, a atomowa struktura
materii

7
Atomowa struktura materii
Demokryt i Szkoła Epikurejska (atomy)
atomos (niepodzielny)
Arystoteles i Stoicy (ciągłość przestrzeni
i materii, cztery elementy: gorąco, zimno,
suchość i wilgoć)
Rozwój alchemii i chemii (2 połowa XVIII
wieku)

8
Atomowa struktura materii; wkład
chemików:
Joseph Priestley:
podgrzewając HgO, tlenek rtęci, otrzymał
tlen,
odkrył także amoniak, tlenek węgla,
chlorowodór, kwas siarkowy, tlenek siarki,
tlenek azotu, wodę sodową
Antoine Lavoisier; pierwiastki chemiczne
„ostatnie stadium osiągalne przez
analizę”,
zachowanie materii (tlen i wodór, woda)
DALTON PLAYHOUSE
http://web.visionlearning.com/dalton_playhouse/ad
_loader.html

9
1799, J.L. Proust, prawo stałych
stosunków:
„stosunek ciężarów
pierwiastków w określonym związku
chemicznym jest wielkością stałą,
niezależną od warunków w jakich ten
związek otrzymano”
John Dalton, prawo stosunków
wielokrotnych:
„jeśli dwa pierwiastki chemiczne A i B
łączą się ze sobą na dwa lub więcej
sposobów tworząc związki C i D, to
przy utrzymywanej stałej masie
pierwiastka A, masy pierwiastka B w
różnych związkach pozostają do siebie
w stosunku prostych liczb
całkowitych”

10
Gay-Lussac:
„jeśli gaz A łączy się z gazem B
tworząc gaz C, bez zmiany
temperatury i ciśnienia, wówczas
stosunki objętości gazów A, B i C
pozostają do siebie w stosunku
prostych liczb całkowitych”
2 objętości wodoru + 1 objętość tlenu
= 2 objętości pary wodnej
1 objętość azotu + 3 objętości wodoru
= dwie objętości amoniaku

11
Avogadro, 1811
(problem małych cząsteczek,
kontrowersja pomiędzy Daltonem i
Gay-Lussac’iem)
Avogadro postulował istnienie atomów
i cząsteczek, stanowiących
najmniejszą ilość danego ciała,
występującą w przyrodzie,
zaproponował także prawo Avogadry:
„w tej samej temperaturze i pod tym
samym ciśnieniem jednakowe
objętości wszystkich gazów zawierają
tę samą liczbę cząsteczek”
Azot, tlen, wodór składają się z
dwuatomowych cząsteczek.
Cząsteczka wody musi się składać z
dwóch atomów wodoru i jednego tlenu

12
Wczesne argumenty fizyczne:
Ruchy Browna, kinetyczna teoria
gazów, prawa elektrolizy Faradaya
NOWOCZESNA FIZYKA ATOMOWA
Dzięki rozwojowi nowych technik nie
ma już dyskusji o istnieniu atomów.
Poznajemy subtelne szczegóły budowy
atomów i dziwne nieintuicyjne prawa
rządzące ich zachowaniem
(mechanika kwantowa).

13
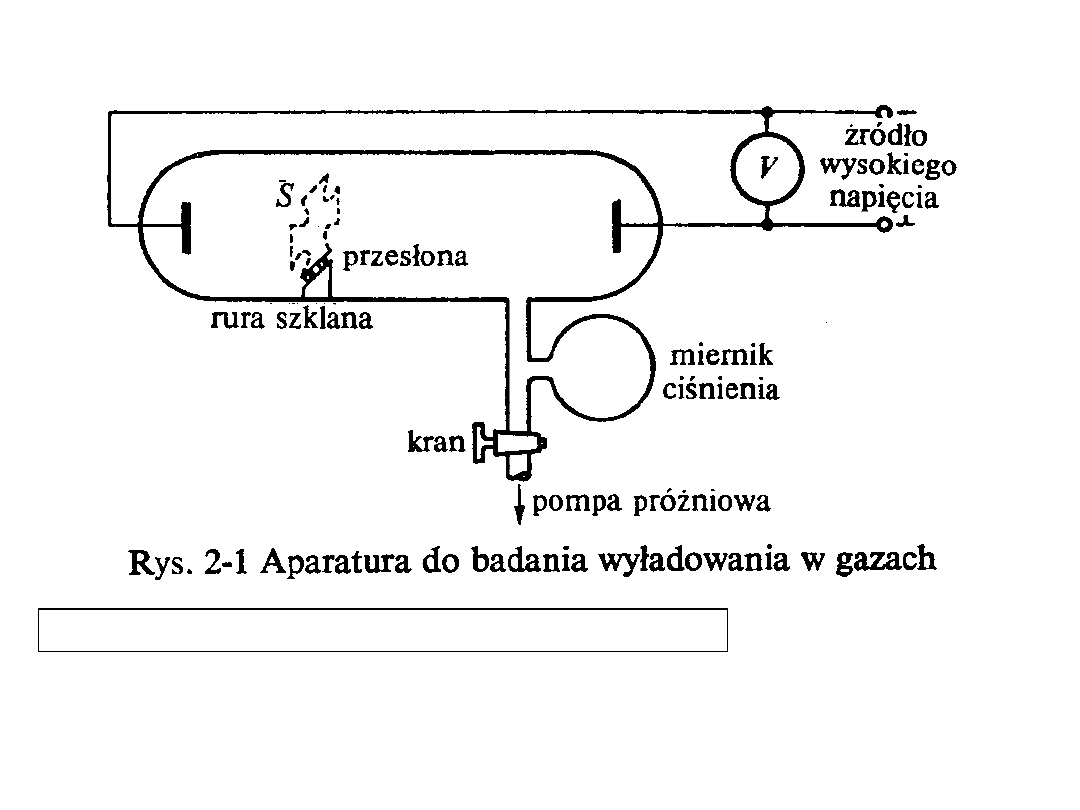
RURA WYŁADOWCZA
(jedno z ważniejszych osiągnięć
technicznych XX wieku)
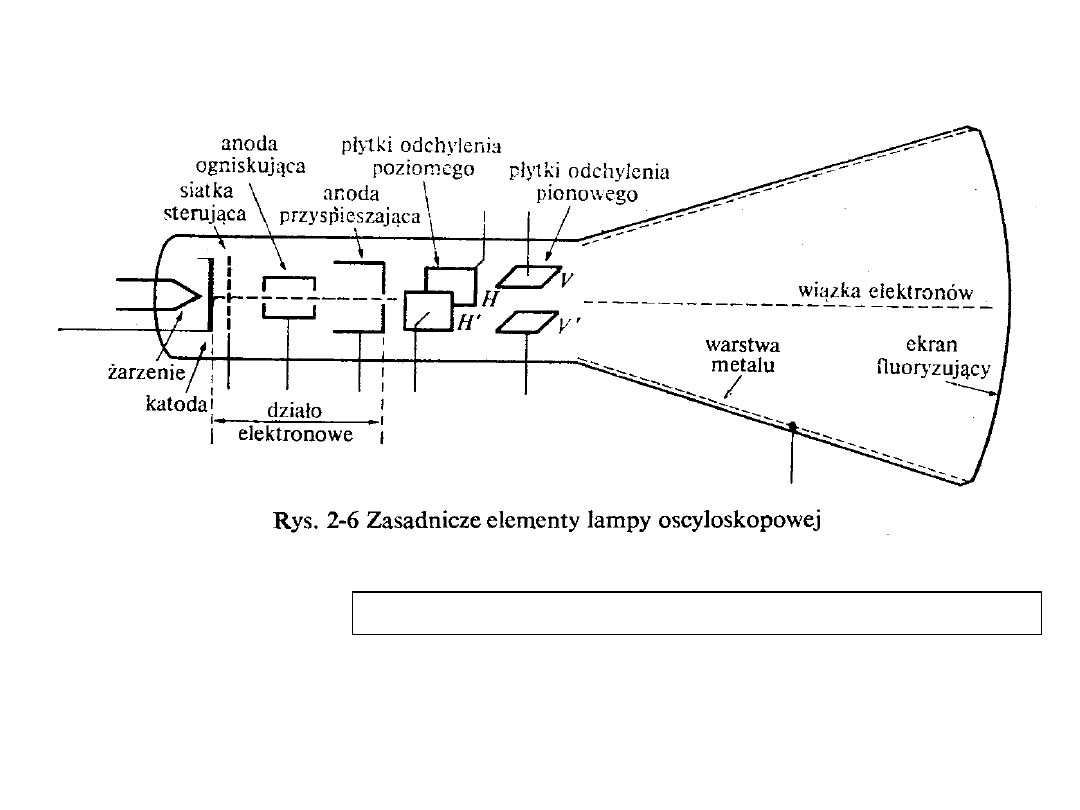
lampy oscyloskopowe
lampy elektronowe (termoemisja)
kineskopy TV
monitory, itd.
świetlówki, “neony”
spektrografy masowe
lampy rtg
fotokomórki i fotopowielacze
(efekt fotoelektryczny)
http://tubedevices.com/alek/pwl/pwl.htm
14
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983
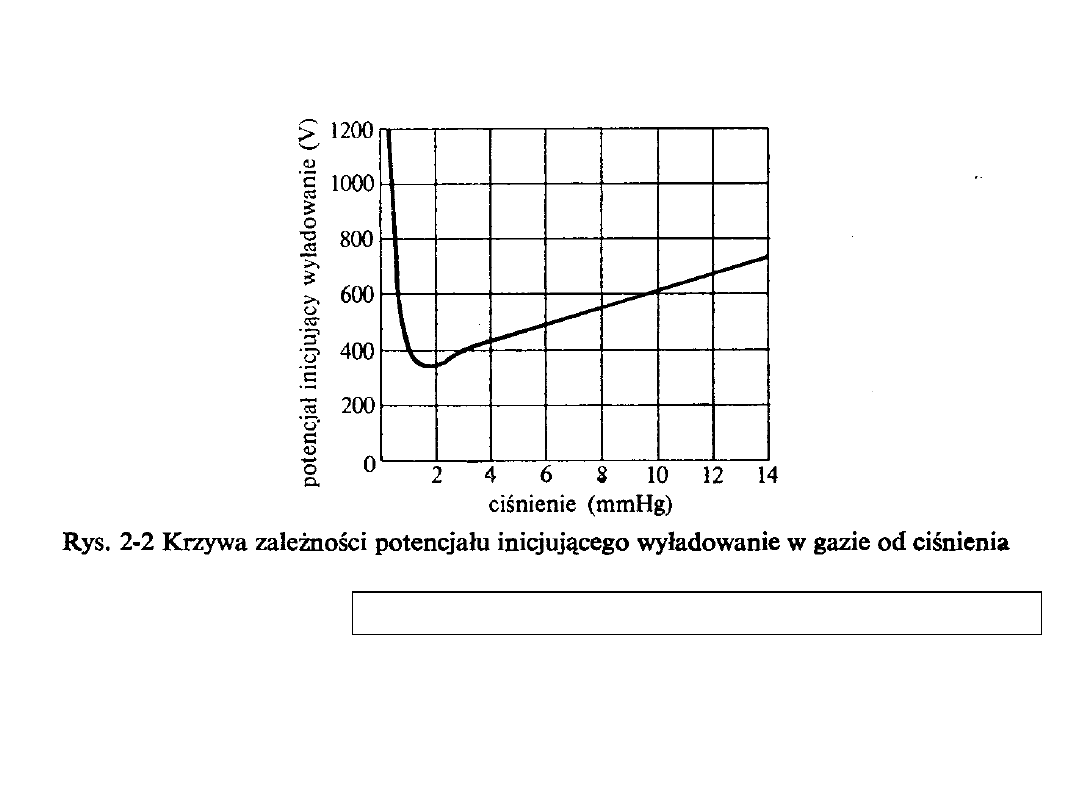
15
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983
16
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983
17
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983

18
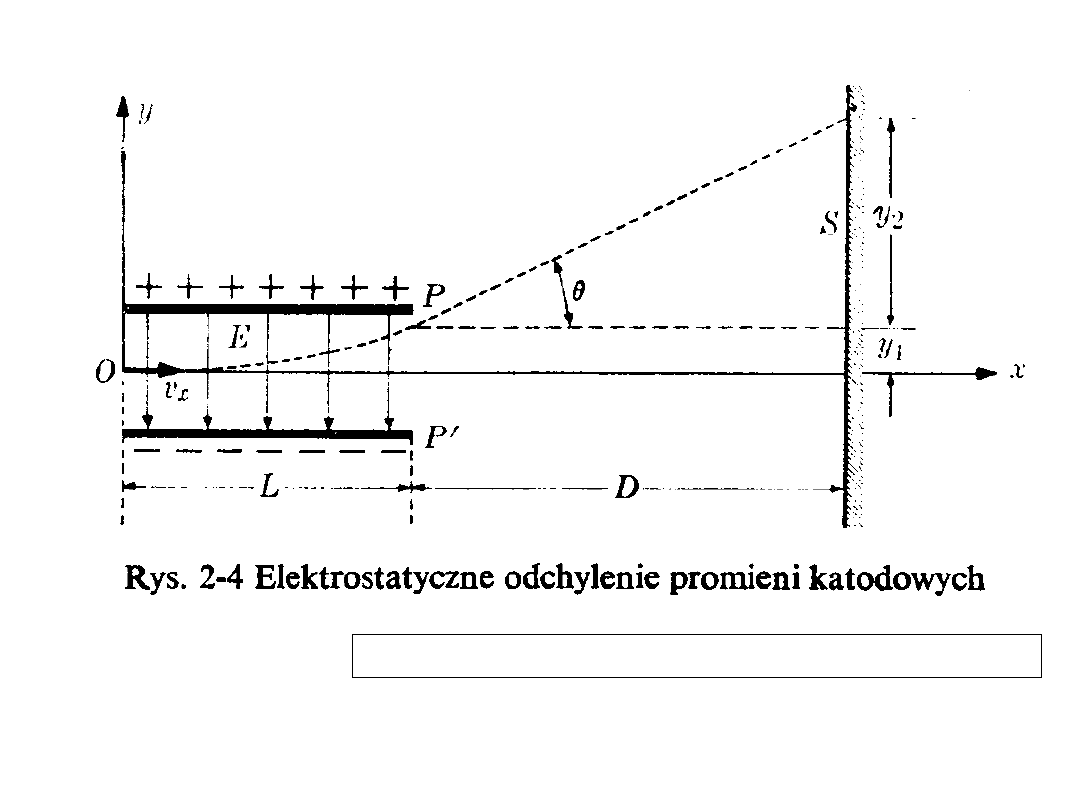
RUCH CZĄSTEK
NAŁADOWANYCH
W POLACH ELEKTRYCZNYM I
MAGNETYCZNYM
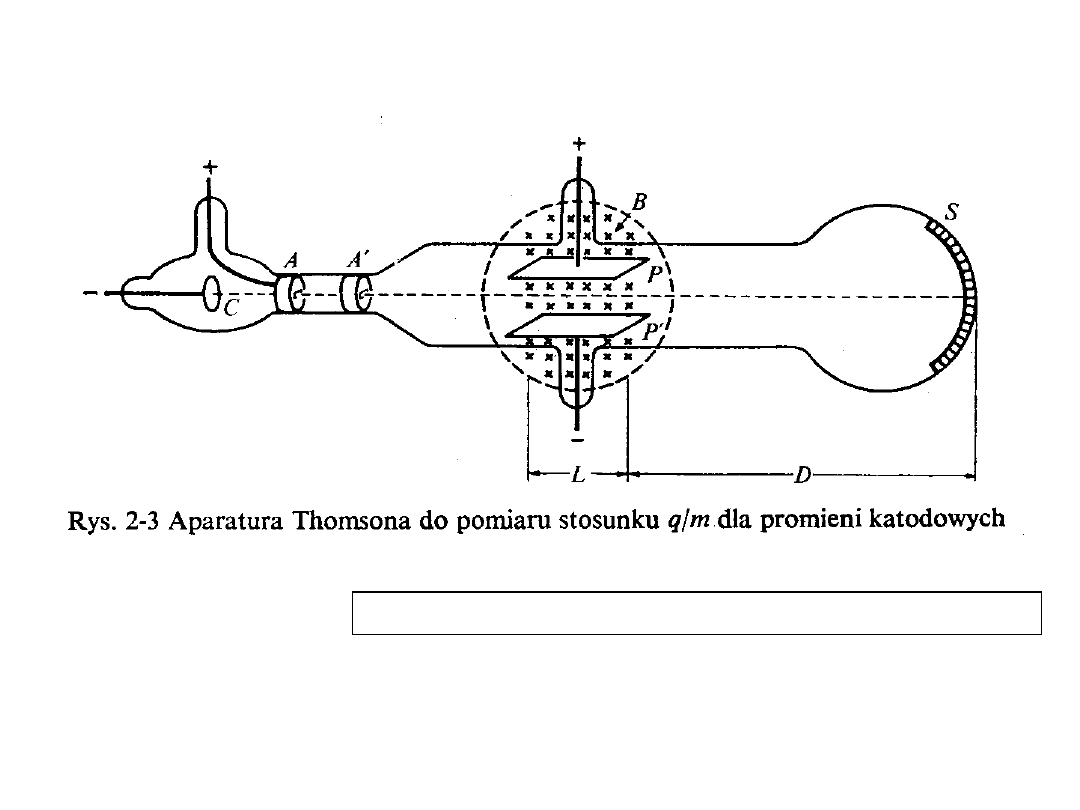
ELEKTRONY i
SPEKTROSKOPIA MAS
Enge, Wehr i Richards, str. 40-
47, 51-57
Haken, Wolf, str. 48-55
19
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983

20
2
2
2
2
1
2
1
2
y
2
2
2
1
1
2
1
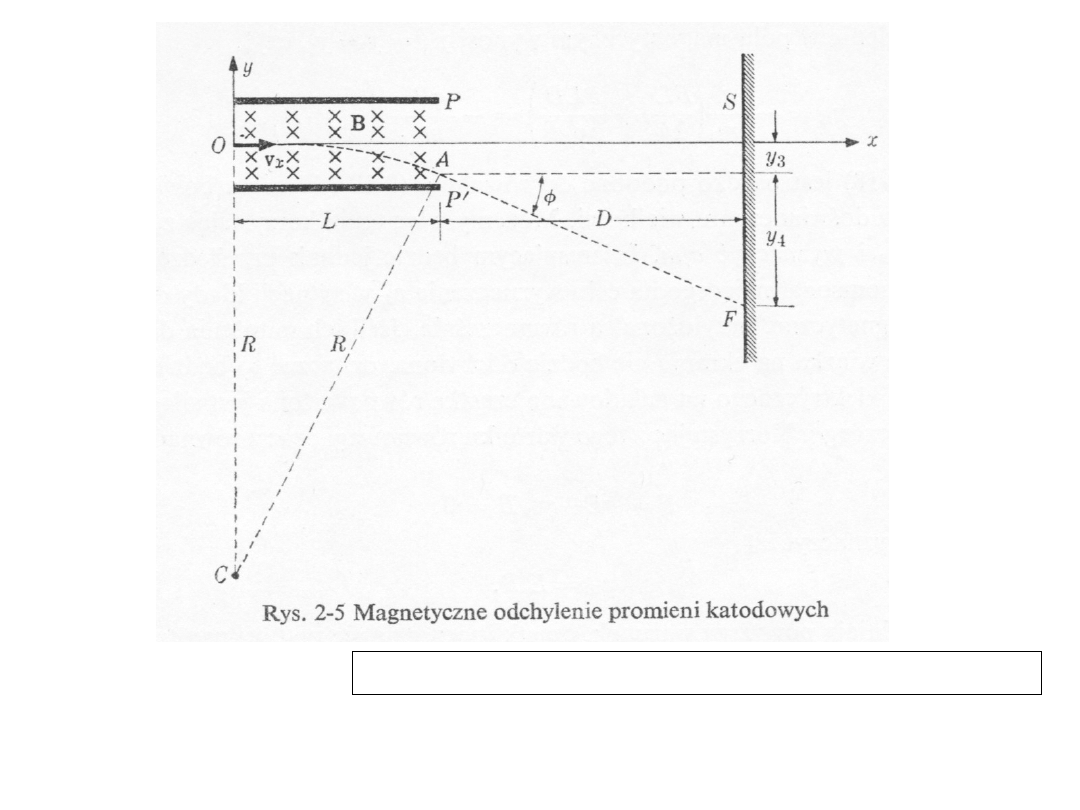
E
mv
qELD
mv
2
qEL
y
y
v
D
v
L
m
qE
t
at
t
v
y
v
L
m
2
qE
2
at
y
y
y
y
D
2
L
mv
qEL
y
2
E
21
Copyright © 1972 by Addison-Wesley Publishing Company, Inc, Introduction to Atomic
Physics by Harald A. Enge.
© Copyright for the Polish edition by Państwowe Wydawnictwo Naukowe, Warszawa
1983
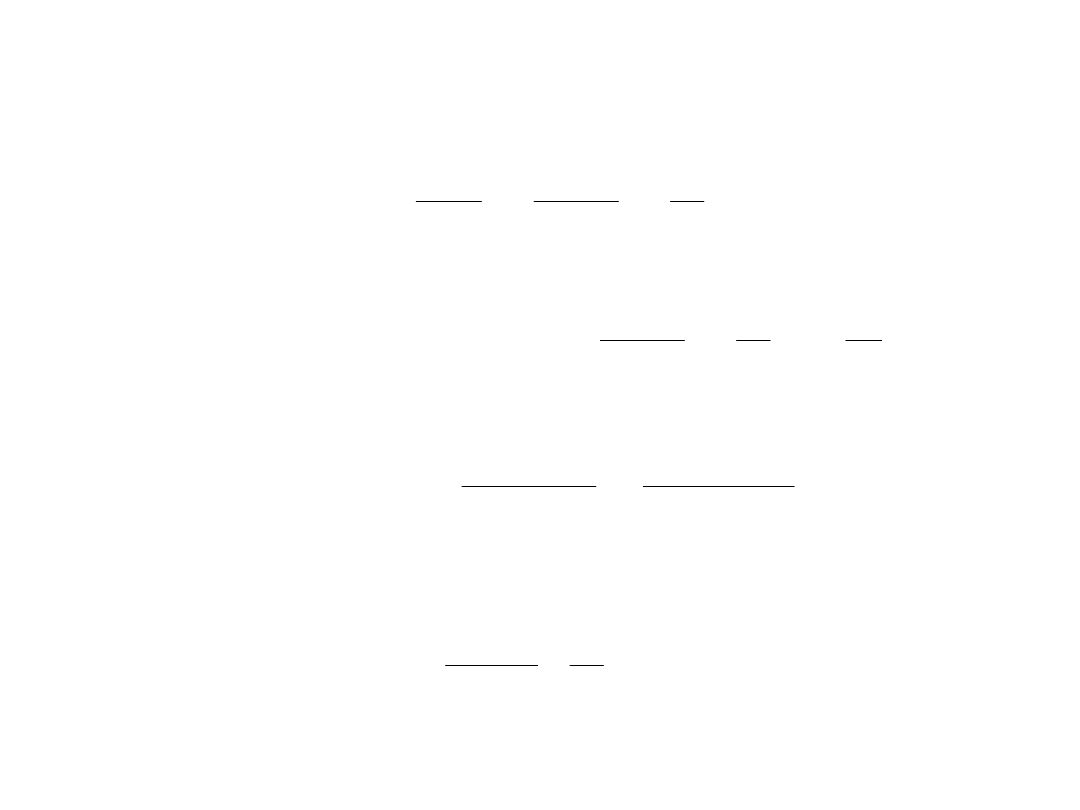
22
2
2
2
4
3
2
1
2
y
4
2
2
1
3
4
3
B
mv
qvBLD
mv
2
qvBL
y
y
v
D
v
L
m
qvB
t
at
t
v
y
v
L
m
2
qvB
2
at
y
y
y
y
D
2
L
mv
qBL
y
B

23
D
2
L
mv
qEL
y
2
E
D
2
L
mv
qBL
y
B
B
E
y
y
y
filtr energetyczny filtr
pędowy
Pole magnetyczne (albo
elektryczne) dobieramy tak, by y
= 0;
B
E
v
Wartość q/m dla promieni katodowych jest
dobrze określona (ostra wyraźna plamka)
Mamy wówczas:
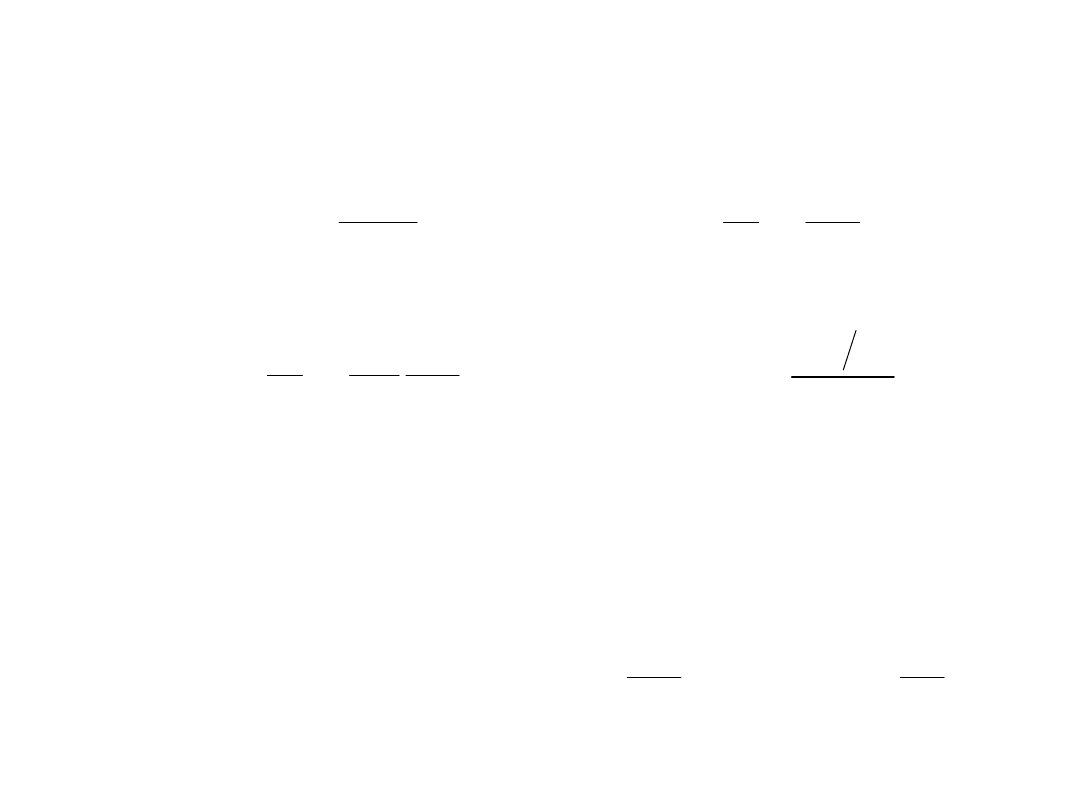
24
Znając napięcie przyspieszające U
mamy:
2
mv
qU
2
co daje:
U
2
v
m
q
2
i dalej:
U
2
1
B
E
m
q
2
2
kg
C
10
76
.
1
m
q
11
e
e
U
B
m
q
2
E
2
2
wykreślając w funkcji U przy
stałym B (napięcie odchylające
dobieramy tak, by pole E równoważyło
pole B dla danego v)
z nachylenia prostej
otrzymamy:
czyli:
2
E
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
Wyszukiwarka
Podobne podstrony:
Wyklad 7 Fiz At Mol 2011
Wyklad 6 Fiz At Mol 2011
Wyklad 9 Fiz At Mol 2011 (1)
Wyklad 10 Fiz At Mol 2011
Wyklad 7a Fiz At Mol 2011
Wyklad 14 Fiz At Mol 2011
Wyklad 12 Fiz At Mol 2011 (1)
Wyklad 13 Fiz At Mol 2011
Wyklad 11 Fiz At Mol 2011
Wyklad 10 Fiz At Mol 2011
WYKLAD z fizyki atomowej i mol w6 2011, Wyklad 6
WYKLAD z fizyki atomowej i mol w14 2011, Wyklad 15
wyklad z kardiologii 30 11 2011
Fizyka wykład dajzeta 20 02 2011
Mikroekonomia wykłady I zjazd, Finanse i Rachunkowość 2011-16, notatki, mikroekonomia
Prawo karne wykład nr 3 z dn ) 10 2011
FM wyklad 12 20 01 2011
Test z biol.mol 2011, UG, MOLEKUŁY, biologia molekularna
Wykład 1 - Wprowadzenie - 01.03.2011 r, studia
więcej podobnych podstron