
Wykład XI
Leki psychotropowe
A. Czernikiewicz

Prometazyna
• 1947
– Antyhistaminowe właściwości
prometazyny odkryte przez
Charpentiera
• „koktajl lityczny” używany w anestezjologii
(prometazyna + petydyna)
• „duża relaksacja pacjentów”
• Przypuszczenie o „antystresowym” działaniu
prometazyny
2

Fenotiazyny
• 1950
– Charpentier syntetyzuje fenotiazyny
• W teście wspinania się u gryzoni Couvoisier
wykazuje, iż chloropromazyna blokuje odruch
unikania, w odróżnieniu od innych środków
antyhistaminowych
• W czasie wojny koreańskiej Laborit wykazuje u
żołnierzy „zobojętniający” efekt chloropromazyny
– Wykazano „trankwilizację” pacjentów
maniakalnych i schizofrenicznych, oraz efekt
antyemetyczny
3

Chloropromazyna
• 1952
–
CPZ powoduje katatonię
u szczurów
• Czy lek powodujący
katatonię może być
lekiem na schizofrenię?
–
W badaniach klinicznych
trankwilizacja
pacjentów, bez
nadmiernej sedacji
–
Dramatyczne
wyzdrowienia u
niektórych
schizofreników w USA i
Francji jako odpowiedź
na kurację CPZ
• 1955-1960
–
Dowody na
antypsychotyczne
działanie CPZ w Europie
• 1953
–
Rezerpina pierwszym
lekiem neuroleptycznym
stosowanym w USA
–
Lehmann (Montreal)
kontynuuje badania
europejskie nad CPZ
–
Thorazine wprowadzona
przez SB w USA, Joel
Elkes (Birmingham)
kontynuuje badania nad
CPZ
4

Badania nad mechanizmem
działania fenotiazyn
• 1950
– Użycie pierwszego
spektrofluorometru w
USA przez Bowmana
• Rezerpina powoduje
deplecję amin
biogennych w mózgu
– LSD zaburza
gospodarkę serotoniny
w mózgu, co prowadzi
Brodie’go i Shawa do
hipotezy o
nadaktywności
serotoninowej w
schizofrenii
• Być może CPZ blokuje
ten proces
• Bradley i Elkes
wykazują, iż CPZ
blokuje
nadaktywność RAS
u szczurów
– Nie jest to związane
z efektem
uspokajającym
• Leki
antycholinergiczne
blokuje EPS po CPZ
5

Od fenotiazyn do butyrofenonów
• 1956
– Prochloroporomazyna jest
mniej uspokajająca,
bardziej
antypsychotyczna, ale i z
większym ryzykiem EPS
– Wykazano wpływ CPZ na
występowanie akatyzji
– Termin „neuroleptyk”
użyty po raz pierwszy
przez Delaya i Denikera
• Lata 50-e
– Nadużywanie amfetaminy
w Japonii i duża liczba
psychoz paranoidalnych
– Janssen wprowadza
pochodną petydyny –
haloperidol
• Podobnie jak CPZ
haloperidol znosi objawy
psychozy po amfetaminie,
ale i powoduje objawy
katatonii
• 1958
– Haloperidol wprowadzony
do leczenia schizofrenii,
szczególnie do terapii
pacjentów pobudzonych,
ale większe ryzyko EPS
6

Dalsze badania
• 1964
– Pierwsze badanie CPZ
metodą „podwójnie ślepej
próby” nadzorowane przez
NIMH
– Czy CPZ to „chemiczny
kaftan bezpieczeństwa”
czy leczenie specyficzne
• 1965
– Haloperidol
zarejestrowany w USA
• 1968
– Pierwsze neuroleptyki
depot (prolixin)
• Lata 50-e
– Dopaminowa hipoteza
schizofrenii
– Działanie neuroleptyków
związane z blokowaniem
receptroa D2
– Farde (Szwecja) wykazuje ,
iż efekt antypsychotyczny
neuroleptyków wiąże się z
powinowactwem do
receptorów D2
• 1958
– Wander Labs (Szwajcaria)
produkuje klozapinę
• Klozapina wykazuje efekt
jako agonista
presynaptyczny DA
7

W kierunku neuroleptyków
atypowych
• Hippius dowodzi, iż
klozapina jest skuteczna w
lekoopornej schizofrenii
• 1975
– Objawy agranulocytozy
po klozapinie u
pacjentów w Finlandii
• 1984
– Dowody na skuteczność
klozapiny w TD
– Kane i Meltzer
udowadniają
skuteczność klozapiny w
terapii lekoopornej
schizofrenii
• 1989 – powrót klozapiny
• 1994
– Janssen wprowadza
risperidon
– Risperidon blokuje
receptory 5HT2A i D2
– Rozwój koncepcji
neuroleptyków
atypowych
• Mniejsze ryzyko EPS i
TD, większa skuteczność
przy terapii objawów
negatywnych
8

Neuroleptyki atypowe
• 1958
– Odkrycie sulpirydu w
badaniach nad
benzamidami
• Brak EPS i TD,
umiarkowane działanie
antypsychotyczne i
anksjolityczne
• Selektywny antagonista
D2
• 1978
– Amisulpiryd – selektywny
antagonista D2/D3
– Remoxipiride – aplasyczna
anemia
– Sertindol – wydłużenie QT
• Lata 90-e
– Badania nad
„bezpieczną
klozapiną”
– Rozwój koncepcji
SDA
• 1996
– Wprowadzenie
olanzapiny
9

10

Co to są leki
antypsychotyczne?
• Leki antypsychotyczne (przez wiele lat nazywane
neuroleptykami – ta nazwa funkcjonuje jeszcze
obecnie i jest synonimem leków antypsychotycznych)
wprowadzono w latach 50-ch naszego stulecia.
• Powodują one ustępowanie objawów psychozy,
przyjmowane dłużej pozwalają na stabilizację stanu
psychicznego chorego, przyjmowane odpowiednio
długo w dużej mierze zabezpieczają chorego przed
nawrotem psychozy.
• Ich działanie redukuje przede wszystkim objawy
wytwórcze psychozy, w nieco mniejszym stopniu
wpływają one na pozostałe objawy.
11

Historia terapii schizofrenii
• Do 1930 r. – przetrzymywanie w szpitalach
70% przewlekłych przebiegów i hospitalizacji
• 1929 r. – Sakel wprowadza insulinoterapię >
ostatni ośrodek Lublin ’90
• 1936 r, Moniz wprowadza leukotomię
prefrotalną – w następnych 15 latach ok. 50
000 lobotomii Moniz ginie zabity przez
pacjenta
• 1952 r. largactil pierwszym neuroleptykiem – u
70% chorych uzyskuje się długie remisje
• ’80 – klozapina pierwszym neuroleptykiem
atypowym
12

Kiedy należy spodziewać się
pierwszych efektów działania leków
antypsychotycznych?
• Trwa do różnie długo, ale zwykle
jeśli po 4-6 tygodniach u pacjenta
nie występuje wyraźna poprawa
lekarz zmienia lek na inny.
• Przy stosowaniu klozapiny (klozapol,
leponex) wyraźny efekt następuje
zwykle nieco później – nawet po 2-3
miesiącach.
13

Które z leków antypsychotycznych
wybiera się do terapii pierwszego
epizodu psychozy?
• Dawniej były to wyłącznie typowe
(klasyczne) leki antypsychotyczne, obecnie
wybiera się częściej leki atypowe (II
generacji), ze względu na większe
bezpieczeństwo ich stosowania i większy
komfort leczenia dla samego pacjenta.
• Nie dotyczy do klozapiny (leponex,
klozapol), który to lek włącza się dopiero po
dwu nieudanych kuracjach innymi lekami –
jest to zalecenie dla lekarzy w większości
krajów świata, w tym i w Polsce.
14

Jaki lek wybiera się do terapii nawrotu
psychozy?
•
Jeśli chory dobrze funkcjonował na poprzednim leku, i
przestał go przyjmować ponieważ czuł się już wyleczony,
najczęściej wraca się do poprzedniego leku, w ostatniej przed
przerwaniem kuracji dawce.
• Jeśli chory przerwał przyjmowanie leku z powodu objawów
ubocznych, szczególnie z powodu znacznego nasilenia
objawów pozapiramidowych, to można włączyć poprzedni lek
w niższej, ale jeszcze skutecznej dawce, lub przywrócić jego
poprzednią dawkę i dołączyć do niej lek korygujący, lub
można spróbować zmiany leku z typowego, na atypowy.
• Jeśli chory nie przestrzegał zaleceń związanych z
przyjmowaniem leku doustnego, można go wymienić na ten
sam lek w postaci o przedłużonym działaniu (depot).
• Jeśli pogorszenie wystąpiło pomimo dobrej tolerancji leku,
i przy jego właściwym dawkowaniu, lekarz zmieni pacjentowi
lek na inny, dający większą szansę powrotu do zdrowia. W
wielu przypadkach będzie to lek antypsychotyczny atypowy,
często klozapina (klozapol, leponex).
15

Jak długo należy przyjmować leki
antypsychotyczne?
• Jeśli był to pierwszy epizod choroby, to
wtedy okres przyjmowania leków w czasie
remisji powinien wynosić od roku do dwu lat.
• Jeśli był to drugi lub trzeci epizod choroby,
to okres przyjmowania leków po każdym z
nich powinien wynosić trzy do pięciu lat.
• Jeśli był to epizod czwarty, piąty, lub
dalszy, okres przyjmowania leków powinien
wynosić minimum 5 lat po każdym z nich.
16

17
Czynnik etiologiczne
Czynnik etiologiczne
schizofrenii
schizofrenii
Hipoteza dopaminowa
Hipoteza dopaminowa
–
Nadaktywność dopaminowa
Nadaktywność dopaminowa
-->
-->
schizo
schizo
f
f
renia
renia
•
Wysokie poziomy DA
Wysokie poziomy DA
•
Więcej receptorów DA
Więcej receptorów DA
•
Większa czułość receptorów
Większa czułość receptorów
DA
DA

18
Dowody na słuszność
Dowody na słuszność
hipotezy dopaminowej
hipotezy dopaminowej
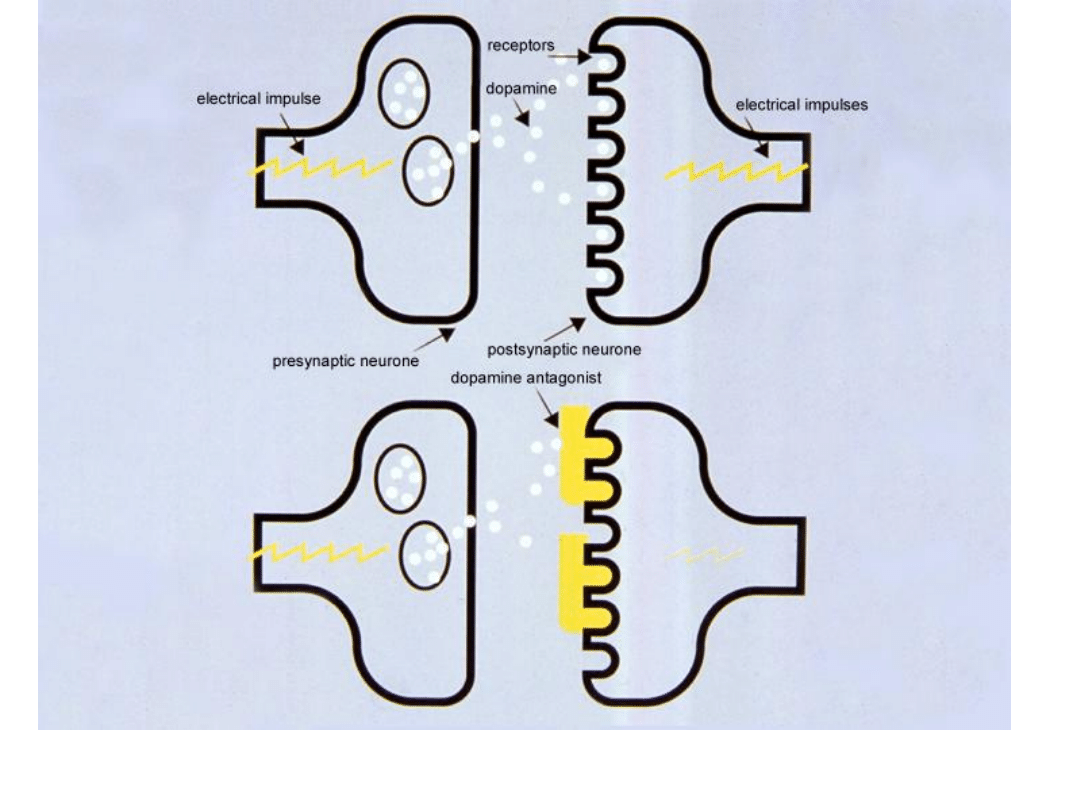
Leczenie
Leczenie
–
Neuroleptyki blokują receptory DA
Neuroleptyki blokują receptory DA
•
Redukcja objawów schizofrenii
Redukcja objawów schizofrenii
–
Amfetamina powoduje wzrost DA
Amfetamina powoduje wzrost DA
•
Nasilenie objawów psychotycznych
Nasilenie objawów psychotycznych
•
Psychozy eksperymentalne
Psychozy eksperymentalne
•
Psychozy po fenmetrazynie
Psychozy po fenmetrazynie
–
L-Dopa
L-Dopa
powoduje wzrost DA
powoduje wzrost DA
•
Objawy psychotyczne
Objawy psychotyczne

19
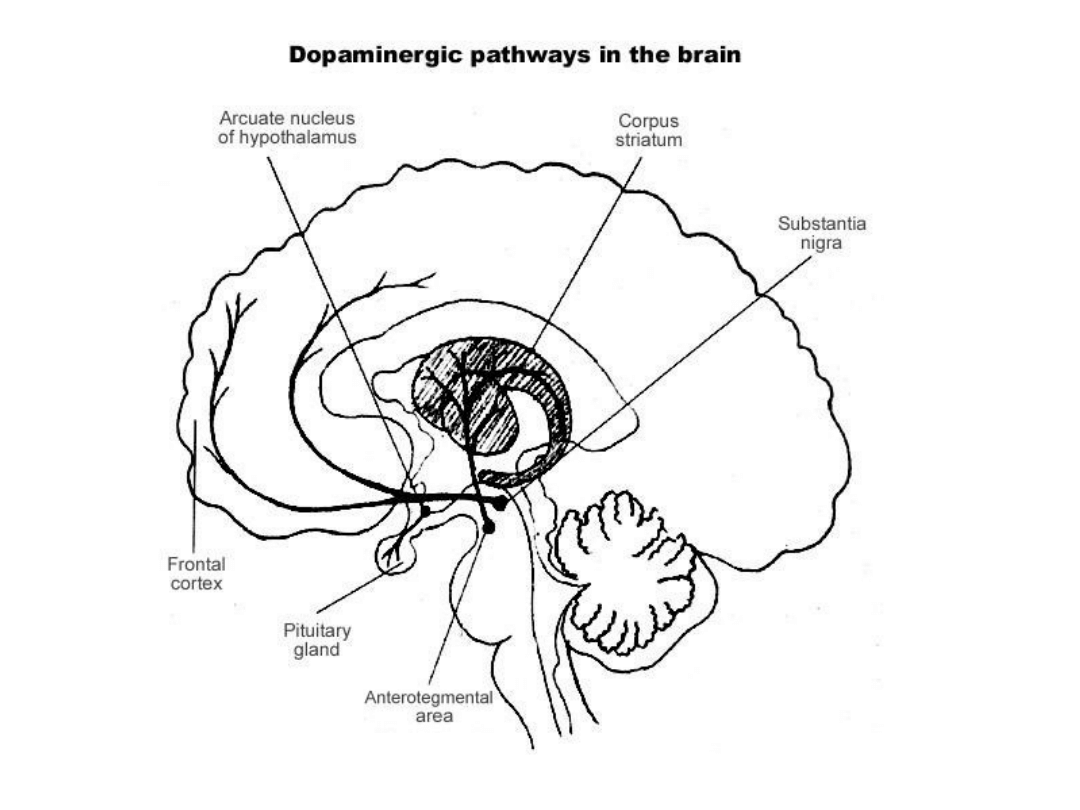
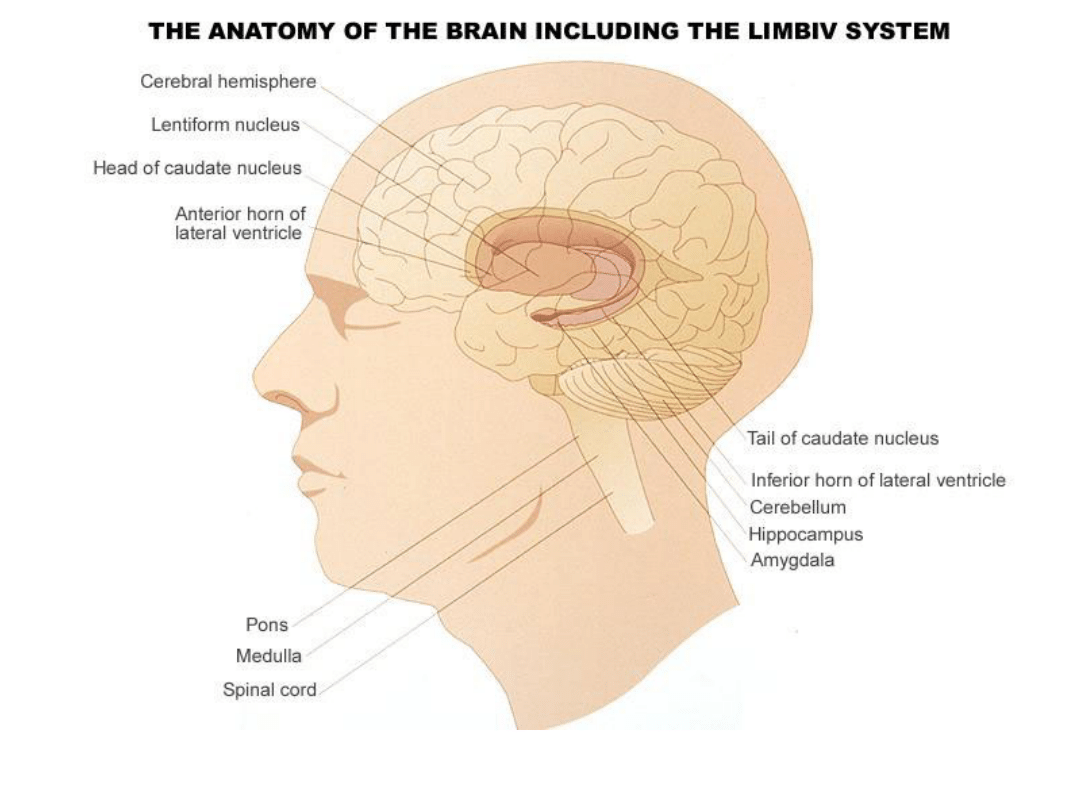
W jaki sposób DA
W jaki sposób DA
„produkuje” objawy
„produkuje” objawy
?
?
Układ limbiczny - emocje
Układ limbiczny - emocje
Płat czołowe – teoria
Płat czołowe – teoria
hypofrontality
hypofrontality
Płaty skroniowe – omamy
Płaty skroniowe – omamy
słuchowe
słuchowe
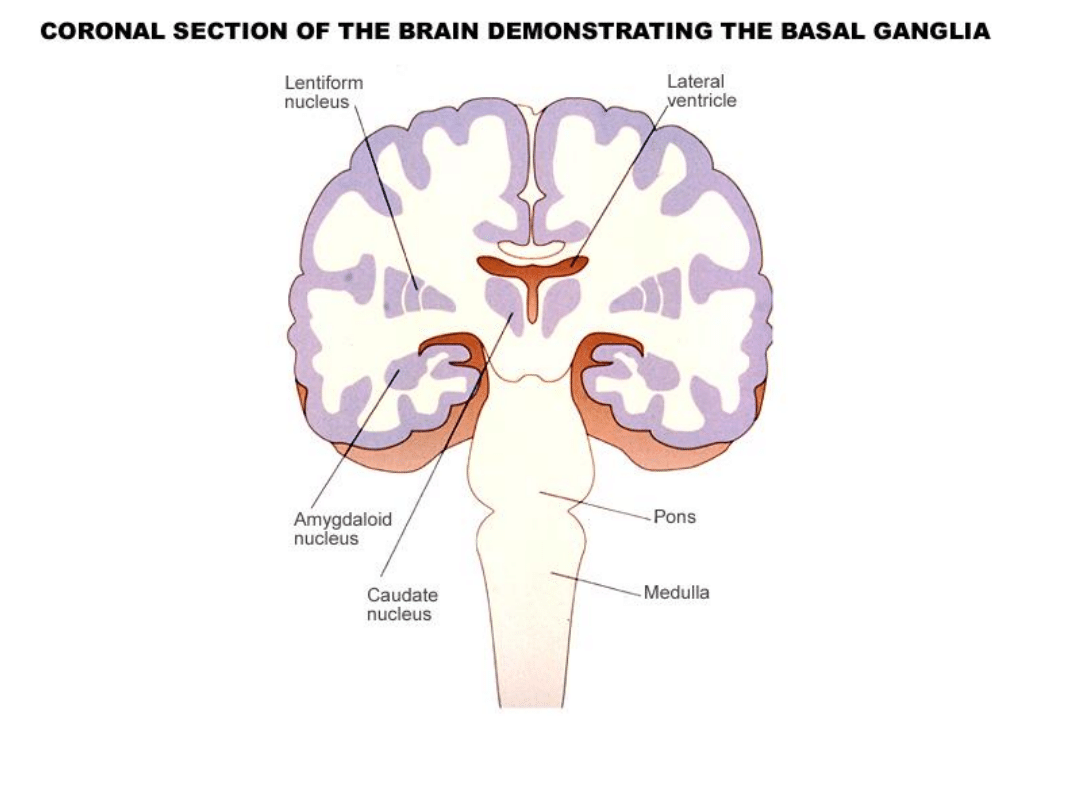
Zwoje podstawy – zaburzenia
Zwoje podstawy – zaburzenia
ruchowe
ruchowe
20
Kliniczne korelaty
aktywności dopaminowej
DOPAMINA
kontrola
układu
krążenia
EPS
funkcje
poznawcze
i wykonawcze
patogeneza
depresji?

21
22
23
24
25
Wiązanie z receptorami in vitro
Ki(nM)
D1
D1
D2
D2
D3
D3
5HT
5HT
2-A
2-A
M1
M1
alfa
alfa
-
-
2A
2A
haloperido
haloperido
l
l
275
275
2.2
2.2
5.6
5.6
302
302
3467
3467
1047
1047
klozapina
klozapina
537
537
177
177
239
239
6.3
6.3
34
34
61
61
olanzapina
olanzapina
117
117
63
63
50
50
2.5
2.5
55
55
21.8
21.8
risperidon
risperidon
616
616
4.8
4.8
14
14
0.46
0.46
>
>
5000
5000
amisulpiry
amisulpiry
d
d
>1000
>1000
0
0
20
20
2.9
2.9
2200
2200
>
>
10000
10000
125
125
26

27
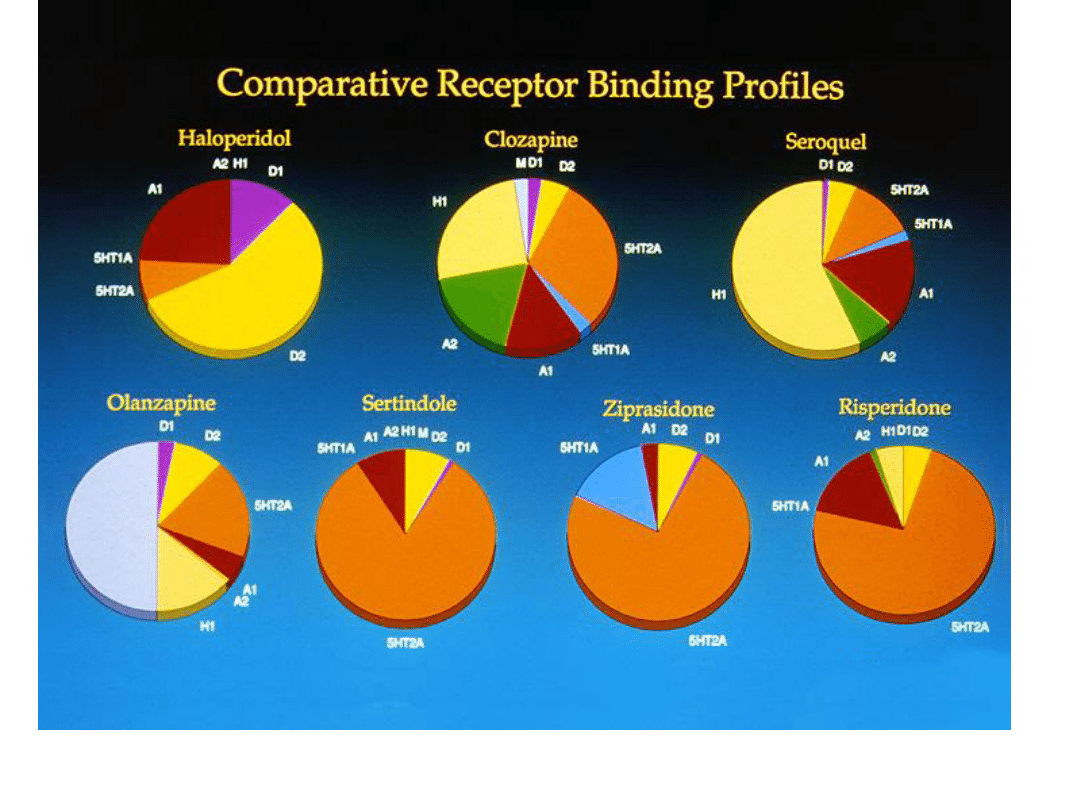
Mechanizm receptorowego działania
typowych leków antypsychotycznych
D2
a1
H1
M1

28
Mechanizm receptorowego działania
haloperidolu
D2
a1

Jak dzielą się leki
antypsychotyczne?
• Zasadniczy podział tych leków jest
bardzo prosty – dzielą się one na
dwie grupy:
– leki typowe (klasyczne) – I generacji
– leki atypowe (nowsze)- II generacji
29

30
Leki antypsychotyczne
typowe (klasyczne)
Leki antypsychotyczne
atypowe (Nowsze)
Wpływają głównie na
redukcję objawów
wytwórczych
Wpływają w większym
stopniu, niż leki typowe, na
redukcję objawów
ubytkowych i objawów
dezorganizacji
Ich skuteczność jest
związana głównie z ich
wpływem na receptory
dopaminowe
Ich szeroki profil działania
(a więc wpływ na
ustępowanie różnych typów
objawów) wiąże się z tym, że
wpływają one również na
inne neuroprzekaźniki, np.
serotoninę
Powodują typowe objawy
uboczne – tzw. objawy
pozapiramidowe
Powodują objawy
pozapiramidowe o
niewielkim nasileniu, lub
nie powodują ich w ogóle
Są dostępne w postaci depot
Nie były dostępne w postaci
depot
Obecnie: RISPOLEPT
CONSTA

31
silniejsze leki
antypsychotyczne
słabsze leki
antypsychotyczne
Haloperidol
Fenactil
Mirenil
Tisercin
Trilafon
Pernazinum
Stelazine
Thioridazin

Kiedy stosuje się typowe
leki antypsychotyczne?
• Do chwili wprowadzenia pierwszych leków
atypowych (lata 70-e) leki typowe
stosowano w każdym przypadku psychozy.
• Obecnie, ze względu na wprowadzenie
wielu leków atypowych, które przewyższają
leki typowe w zakresie korzystnego wpływu
na objawy dezorganizacji i ubytkowe, oraz
ze względu na mniejsze ryzyko objawów
ubocznych, szczególnie tzw. objawów
pozapiramidowych częstość ich stosowania
znacznie się zmniejszyła, ale nadal należą
do głównego nurtu terapii psychoz.
32

Kiedy stosuje się typowe
leki antypsychotyczne?
• · Kiedy chory poprzednio dobrze reagował na te
leki, a więc były one nie tylko skuteczne i bezpieczne,
ale również były akceptowane przez chorego
• · Kiedy chory nie współpracuje w przebiegu
terapii, przerywa ją – wtedy wskazane może być
zastosowanie leków o przedłużonym działaniu, tzw.
leków typu depot – jest to tylko możliwe przy użyciu
leków typowych
• · Kiedy na psychozę chorował ktoś z rodziny
chorego i dobrze reagował na leki antypsychotyczne
typowe, a słabo reagował, lub reagował objawami
ubocznymi na leki atypowe.
33

Co to są neuroleptyki (leki
antypsychotyczne) typu depot (po polsku –
o przedłużonym działaniu) ?
• Jest to grupa kilku neuroleptyków typowych, dla których udało
się stworzyć takie ich preparaty, które po wstrzyknięciu
domięśniowym powoli uwalniają się w organizmie. Dzięki temu
chory ma w swoim organizmie stałe stężenie tego leku, tak
jakby codziennie przyjmował pewną dawkę leku doustnie.
• Zastrzyki wykonuje się co 2-4 tygodnie, ponieważ taki jest okres
utrzymywania się leku w stałym stężeniu. W ten sposób pacjent
nie musi codziennie pamiętać o przyjmowaniu jakiejś ilości
tabletek, a konieczność wykonania kolejnego zastrzyku pozwala
lekarzowi, choremu, i jego rodzinie nadzorować proces terapii.
• Liczba objawów ubocznych po neuroleptykach depot nie jest
większa, niż przy ich doustnym stosowaniu. Stosowanie
neuroleptyków typu depot co najmniej dwukrotnie redukuje
ryzyko nawrotu psychozy, w porównaniu ze stosowaniem
typowych leków antypsychotycznych w formie doustnej.
34

Dostępne w Polsce
neuroleptyki depot
• Clopixol
• Fluanxol
• Decaldol (Haloperidol)
• Trilafon
• RISPOLEPT CONSTA
35

Jakie są typowe objawy uboczne powstające
w przebiegu terapii lekami
antypsychotycznymi typowymi?
• U znacznej liczby osób przyjmujących te leki
dochodzi do rozwoju tzw. zespołów
pozapiramidowych (często używa się skrótu z
języka angielskiego – EPS).
• Pojawiają się one zwykle, albo w fazie
podnoszenia dawek, albo w wyniku przewlekłego
przyjmowania tych leków.
36
37

38
zespół pozapiramidowy
jego objawy
Zespół Parkinsona
Drżenie (zwykle rąk, głowy),
sztywność mięśniowa, powolne
poruszanie się
Dystonia
Nagłe skurcze mięśni, np.
wyginanie szyi, gwałtowne
zwracanie oczu do góry, a
nawet skurcze utrudniające
przełykanie
Akatyzja
Niemożność usiedzenia czy
ustania w miejscu, tzw.
„niespokojne nogi”
Późne dyskinezy
Dziwne, rytmiczne
niekontrolowane ruchy,
najczęściej w obrębie twarzy,
ciągłe ruchy warg (tzw. zespół
królika), rytmiczne ruchy
językiem

Jakie są inne objawy uboczne w
trakcie terapii typowymi lekami
antypsychotycznymi?
• Przy stosowaniu słabszych leków typowych można
się również liczyć, szczególnie na jej początku, z
gwałtownymi spadkami ciśnienia krwi, a więc
zawrotami głowy, czy nawet zasłabnięciami.
Występują one szczególnie przy wstawaniu, dlatego
też chory powinien na początku takiego leczenia
mieć mierzone ciśnienie zarówno w pozycji leżącej
jak i siedzącej, i być pouczony, iż przy wstawaniu z
łóżka należy robić to powoli i poświęcić długą chwilę
(ok. minuty) na posiedzenie z nogami spuszczonymi z
łóżka.
• Kolejnym objawem ubocznym, który może być
uciążliwy, szczególnie na początku terapii jest
nadmierna senność w ciągu dnia.
39

Mechanizm receptorowego działania
atypowych leków antypsychotycznych
40
5HT1a
5HT2A
5HT2C
5HT3
5HT6
5HT7
D4
D3
D2
D1
a1
a2
H1
M1

Co to są atypowe leki
antypsychotyczne?
• Są to, jak już wcześniej było podane, leki powodujące
zwykle minimalne tylko objawy pozapiramidowe. Z
drugiej strony, wpływają one w znaczący sposób na
objawy ubytkowe i objawy dezorganizacji związane z
psychozą.
• Zostały wprowadzone w latach 70-ch i są coraz
częściej stosowane w terapii psychoz, szczególnie w
okresie leczenia chorego już po jego pobycie w
szpitalu.
• Obecnie w Polsce stosuje się z tych leków: klozapinę
(leponex, klozapol), sulpiryd (sulpiryd), risperidon
(rispolept), olanzapinę (zyprexa, zolafren),
amisulpiryd (solian), kwatiepinę (seroquel),
ziprasidon
41

42
lek
cechy typowe
objawy niepożądane
klozapina
Skuteczny w 25-50%
przypadków w terapii
psychoz lekoopornych
na typowe leki
antypsychotyczne
Poważne powikłanie u
co setnej osoby
przyjmującej ten lek:
uszkodzenie szpiku
kostnego – dlatego
konieczność kontroli
krwi w wyznaczonych
terminach; początkowo
duża senność
amisulpryd
Działanie
antydepresyjne obok
antypsychotycznego,
silny wpływ na objawy
ubytkowe
U części kobiet
przyjmujących ten lek
mogą się pojawić
zaburzenia
miesiączkowania
miesiączki
risperidon
W porównaniu z innymi
lekami powoduje
niewielkie tylko
zaburzenia poznawcze
Pomimo, że jest lekiem
nietypowym mogą po
nim występować objawy
pozapiramidowe
olanzapina
Zrównoważony wpływ
na objawy wytwórcze i
ubytkowe, zwykle
stosuje się lek tylko raz
dziennie, wieczorem
Senność i wzrost wagi w
początkowym okresie
terapii
43
Porównanie objawów ubocznych ze
strony OUN w grupie atypowych
leków antypsychotycznych
klozapin
klozapin
a
a
risperido
risperido
n
n
olanzapina
olanzapina
kwatiepina
kwatiepina
amisulpiry
amisulpiry
d
d
EPS
EPS
0
0
0-+
0-+
0-(+)
0-(+)
0-+
0-+
0-+
0-+
Napady
Napady
drgawkow
drgawkow
e
e
+++
+++
0
0
0
0
0
0
0
0
ZZN
ZZN
(+)
(+)
(+)
(+)
?
?
?
?
?
?

44
Porównanie innych objawów
ubocznych w grupie atypowych
leków antypsychotycznych
klozapina
klozapina
risperido
risperido
n
n
olanzapina
olanzapina
kwatiepina
kwatiepina
amisulpiryd
amisulpiryd
hipotonia
hipotonia
+ -
+ - +++
+++
+
+
+
+
+
+
0
0
sedacja
sedacja
+++
+++
(+)
(+)
+
+
+
+
(+)
(+)
QT-prolong.
QT-prolong.
0 - +
0 - +
0 - +
0 - +
0
0
0 - +
0 - +
0
0
obj. anty-
obj. anty-
cholinergiczn
cholinergiczn
e
e
+++
+++
0
0
+
+
0 - +
0 - +
0
0
agranulocytoz
agranulocytoz
a
a
+++
+++
0
0
0
0
0
0
0
0
wzrost PL
wzrost PL
0
0
0 -
0 - ++
++
+
+
0 -
0 - ++
++
+++
+++
wzrost wagi
wzrost wagi
+++
+++
+
+
+ ddi
+ ddi
+
+
(+)
(+)
blokada nosa
blokada nosa
0 - +
0 - +
0 - +
0 - +
0 -
0 - ++
++
0
0
0
0

45
Na ile dany lek spełnia kryteria
atypowego neuroleptyku?
SDA?
SDA?
tak
tak
Mniejszy EPS niż haloperidol?
Mniejszy EPS niż haloperidol?
tak
tak
Czy u pacjentów nigdy nie występuje
Czy u pacjentów nigdy nie występuje
EPS?
EPS?
tak
tak
Czy pacjenci nigdy nie mają TD?
Czy pacjenci nigdy nie mają TD?
tak
tak
Niższa prolaktynemia niż po
Niższa prolaktynemia niż po
haloperidolu?
haloperidolu?
tak
tak
Czy nigdy nie dochodzi do wzrostu
Czy nigdy nie dochodzi do wzrostu
prolaktyny?
prolaktyny?
tak
tak
Mniej objawów negatywnych niż po
Mniej objawów negatywnych niż po
haloperidolu?
haloperidolu?
tak
tak
Skuteczny dla objawów lekoopornych
Skuteczny dla objawów lekoopornych
na konwencjonalne leki AP?
na konwencjonalne leki AP?
tak
tak

Główne cechy risperidonu
• Pożyteczny do terapii
pobudzenia u
dementywnych
pacjentów
• Jedyny atypowy
neuroleptyk
powodujący wzrost
poziomu prolaktyny
• Tylko przy niskich
dawkach niskie ryzyko
EPS
• Niższy wzrost wagi niż
przy innych lekach AP
• Mniej może dać więcej
• Niskie dawki powodują
obniżenie kosztów
terapii
• Przy opanowywaniu
agresji należy raczej
augmentować BDA,
lub klasycznymi LAP ,
niż podnosić dawki
• Możliwość podawania
jednej dawki dziennie
46

Główne cechy olanzapiny
• Zaliczana do leków AP,
również przy zaburzeniu
bipolarnym
• Udokumentowana
efektywność w
augmentacji SSRI przy
terapii niepsychotycznej,
lekoopornej depresji
• Pomimo działania na
receptor muskarynowy
brak dowodów na
negatywny wpływ na
funkcje poznawcze
• Znaczący wzrost wagi w
czasie terapii
• Więcej daje więcej
• Po stabilizacji pacjenta
można obniżyć dawkę
• Przy wyższych dawkach i
częściowej skuteczności –
augmentacja przy użyciu
BDA, lub klasycznych LAP
• Kobiety wymagają zwykle
mniejszych dawek niż
mężczyźni
• Zawsze stosować tylko
jedną dawkę na dobę
47

Główne cechy klozapiny
• Najbardziej efektywna,
ale jednocześnie
najbardziej
niebezpieczna
• Redukuje pobudzenie i
agresywność
• Zmniejsza objawy TD
• Stopniowa, ciągła
poprawa w czasie
wielu lat stosowania
• Nie jest uznawana za
lek pierwszego wyboru
przy pierwszym
epizodzie
• Może powodować
aganulocytozę (0.5-
2%)
• Dawkowanie powyżej
550 mg wymaga
zwykle podawania
leku
przeciw/drgawkowego
• Może powodować
znaczący wzrost wagi
• Ślinotok, szczególnie
w nocy może być
uciążliwy
48

Jakie inne poza stosowaniem leków formy
terapii stosuje się w leczeniu psychoz?
•
Psychoedukacja
dla chorych i ich rodzin na temat
przyczyn psychoz, ich objawów, i sposobów ich leczenia.
• Terapia systemowa chorych i ich rodzin, opierająca się na
leczeniu całej rodziny chorego – choroba jednego członka
rodziny odbija się istotnie na funkcjonowaniu całej rodziny
(systemu rodzinnego).
• Trening i pomoc w codziennych czynnościach życiowych
chorych, takich jak robienie zakupów, planowanie wydawania
pieniędzy, wychodzenie do kina, itd.. Choroba, i częsta izolacja
chorych powoduje czasami, iż „zapominają” oni jak wykonuje się
tego typu czynności.
• Uczestnictwo w grupach wsparcia osób (grupy
samopomocy) z psychozami i innymi zaburzeniami
psychicznymi. Często takie grupy wsparcia składają się nie tylko
z chorych, ale i członków ich rodzin, czy ich bliskich przyjaciół.
49

Kiedy konieczna jest
hospitalizacja?
•
Chory na tyle nie kontroluje swoich zachowań,
że zachodzi wyraźna obawa, iż zachowania te mogą
być zagrażające dla niego, lub jego otoczenia
(zagrożenie życia, poważne zagrożenie zdrowia)
• Chory, pomimo pogorszenia, zaprzecza mu, nie
bierze zaleconych leków, co stwarza poważną
obawę, że jego stan będzie się pogarszał
• Chory z powodu pogorszenia przestał
zaspakajać swoje podstawowe potrzeby życiowe,
np. : śpi pod gołym niebem, nie je, nie pije płynów
• U chorego współistnieje z psychozą poważna
choroba fizyczna, albo wystąpiły u niego takie
objawy uboczne działania leków, że nie będzie
można sobie poradzić z nimi bez pobytu chorego w
szpitalu.
50

Co można zaproponować choremu, jeśli nie
wymaga hospitalizacji, a jednocześnie wyniki
leczenia w domu nie są zadawalające?
• Jest to kilka tzw. pośrednich form terapii, takich jak:
• Pobyt na oddziale dziennym – np. od godziny 8 do
14, przez pięć dni w tygodniu, połączony zwykle z
intensywną terapią zajęciową;
• Terapia w oddziale leczenia domowego – gdzie w
domu chorego pojawia się co pewien czas lekarz,
psycholog, lub pielęgniarka, a rodzina pacjenta
spełnia na co dzień rolę terapeutycznego opiekuna
chorego;
• Pobyt w hostelu – domu, czy mieszkaniu dla
pacjentów, zwykle młodych, w którym uczą się oni
współpracy, oraz niezależności życiowej – terapeuci
pojawiają się w hostelu, tylko po to, aby monitorować
terapię
51

52
Schizofrenia - faza ostra
Jest to faza w której pacjent wykazuje wyraźne
objawy psychotyczne.
Cele terapii to „zapobieganie przejawom
zagrażającym pacjentowi i jego otoczeniu,
uzyskanie kontroli nad zachowaniem, redukcja
objawów, a w efekcie szybki powrót do
normalnego poziomu funkcjonowania...”
Niebezpieczeństwa: 10% osób ze schizofrenią
ginie śmiercią samobójczą, u
60% leczonych
w tej fazie rozwijają się objawy
pozapiramidowe.
wg APA (1997)

53
Schizofrenia - faza
stabilizacji
Jest to faza obejmująca pierwszych 6
miesięcy (lub więcej) od początku
epizodu psychotycznego, w czasie której
dochodzi do stopniowej redukcji
objawów ostrych.
Cele terapii to „wczesne zapobieganie
nawrotowi psychozy, readaptacja
pacjenta w jego środowisku, dalsza
redukcja objawów, utrwalanie remisji...”
Niebezpieczeństwa:
„mechanizm drzwi
obrotowych”
wg APA (1997)

54
Schizofrenia - faza remisji
Jest to faza w której objawy
psychotyczne są minimalne lub
nieobecne.
Cele terapii to „poprawa
funkcjonowania i minimalizacja ryzyka
nawrotu psychozy i jego
konsekwencji...”.
Niebezpieczeństwa: u
40-60% leczonych
w okresie roku występuje nawrót
psychozy
.
wg APA (1997)
55
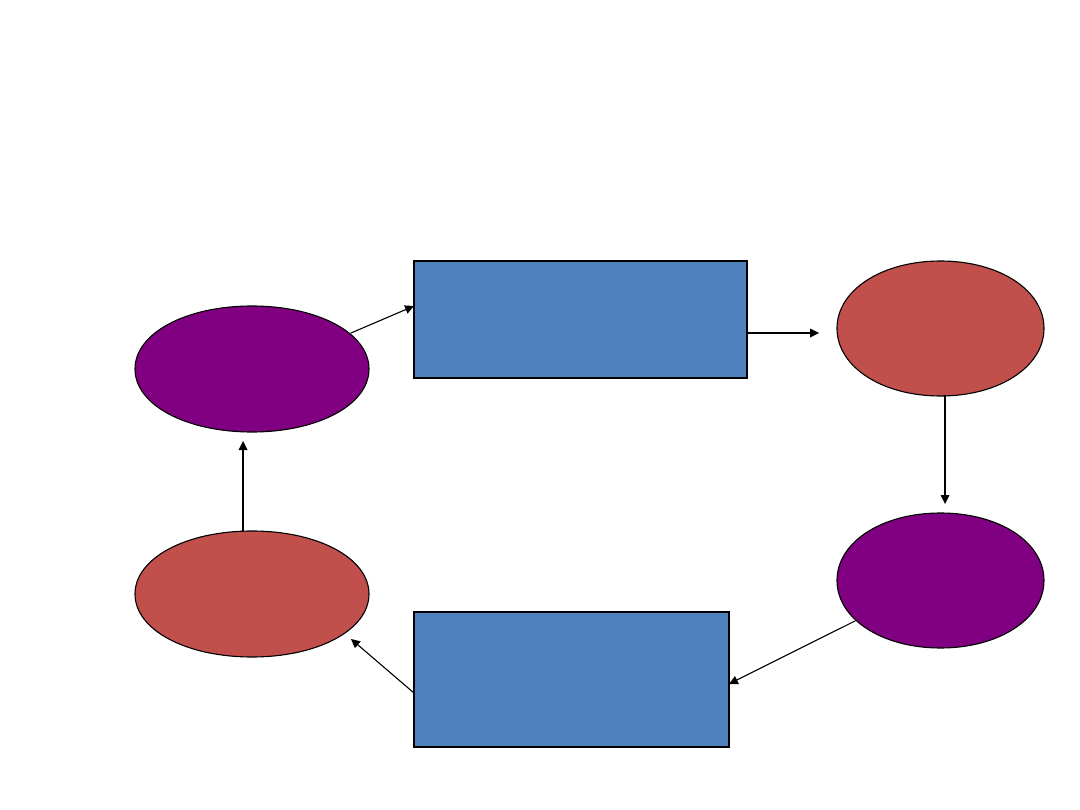
„Błędne koło” nawrotów schizofrenii.
Pierwotne ON
Wtórne ON
nawrót
Brak współpracy
nawrót
Brak współpracy

56
Dlaczego chorzy na schizofrenię
mają nawroty psychozy?
ambiwalencja lekarzy co do terapii
ambiwalencja lekarzy co do terapii
podtrzymującej po pierwszym epizodzie
podtrzymującej po pierwszym epizodzie
psychozy
psychozy
brak wglądu u chorych
brak wglądu u chorych
ambiwalencja rodzin co do leczenia w ogóle
ambiwalencja rodzin co do leczenia w ogóle
niechęć otoczenia do leków
niechęć otoczenia do leków
psychotropowych
psychotropowych
wg Angermayera i wsp. 1993
wg Kane 1996

57
Kane
„one out of every three
„one out of every three
compliant patients become
compliant patients become
noncompliant within twelve months”
noncompliant within twelve months”
wątpliwości chorych czy powinni brać
leki, jeśli czują się dobrze
objawy uboczne leków
„nierealne” dążenia do całkowitego
wyzdrowienia
traktowanie przyjmowania leków jako
przymusu „to przypomina mi, że
jestem chory”
brak zgody wśród profesjonalistów na
temat zasad terapii podtrzymującej

Co należy wiedzieć o
lekach
przeciwdepresyjnych?
Andrzej Czernikiewicz
Andrzej Czernikiewicz

59
Idealny LPD
Idealny LPD
Skuteczny we wszystkich klinicznych
typach depresji
Skuteczny w terapii depresji na podłożu
organicznym
Efektywny we wszystkich grupach
wiekowych
O szybkim początku działania
Bez objawów ubocznych
Skuteczny u większości chorych
Ułatwiający współpracę

60
Wybór leku przeciwdepresyjnego jest
Wybór leku przeciwdepresyjnego jest
empiryczny i zwykle opiera się na:
empiryczny i zwykle opiera się na:
Poprzedniej odpowiedzi chorego na LPD
Stanie klinicznym chorego
(psychicznym i somatycznym)
Spodziewanym profilu objawów
ubocznych LPD
Ryzyku interakcji z innymi lekami
Cenie leku

61
•Safety
•Therapeutic index
•Drug-drug interactions:
•Pharmacodynamics
•Pharmacokinetics
Tolerability
•Efficacy
•Overall
•Unique spectrum of activity
•Rate of response
•Maintenance and prophylaxis
•Payment
•Simplicity
•Ease of administration
STEPS
STEPS

Jaki powinien być lek antydepresyjny
• B
ezpieczny
• O
niskim profilu objawów ubocznych
• S
kuteczny
• K
oszty raczej niskie
• I
inne
62

63
LPD - skuteczność
LPD - skuteczność
LPD są skuteczne u 65-75%
pacjentów z depresją
Właściwą ocenę skuteczności LPD
można dokonać po 4-6 tygodniach
podawania leku we właściwej dawce

Podział leków przeciwdepresyjnych ze względu na przyjęty
mechanizm działania
Preskorn-1999
• Nieselektywni
antagoniści
wychwytu zwrotnego
i receptorów NA i 5-
HT (MRNrAs):
amitryptylina,
imipramina,
amoksapina,
klomipramina,
doksepina,
trimipramina
• Selektywni
antagoniści
wychwytu
zwrotnego NA
(NSRISs):
desimipramina,
maprotylina,
nortryptylina,
protryptylina
64
65
TLPD
TLPD
Stahl - 2000
Stahl - 2000
TLPD
TLPD
SRI
SRI
NRI
NRI
M-ACh

TLPD
zalety i wady
• Skuteczne
• Znane od lat
• Nieliczne interakcje
z lekami AP
• Tanie
• Kardiotoksyczne
• Liczne
przeciwwskazania
• Ryzyko zatrucia
• Objawy uboczne –
działanie na
receptor
muskarynowy
• Możliwość złej
współpracy
66

67
Dawkowanie
Dawkowanie
TLPD
Amitriptylina
75
75-300
Imipramina
75
75-300
Nortriptylina
10-50
50-200
Klomipramin
a
75
75-300
Klasa
Nazwa
początkow
a
Okno
tera-
peutyczn
e

Podział leków przeciwdepresyjnych ze względu na przyjęty
mechanizm działania
Preskorn-1999
• Selektywne inhibitory wychwytu
zwrotnego serotoniny (SSRIs; SI-5-
HT):
Citalopram, Escitalopram
Sertralina
Paroksetyna
Fluwoksamina
Fluoksetyna
68

69
SSRI’s - wspólne cechy
SSRI’s - wspólne cechy
Szeroki indeks
terapeutyczny
minimalny efekt
cholinolityczny i
antyhistaminowy
minimalny wpływ
na układ krążenia
nie obniżają
progu
drgawkowego
Niewielkie ryzyko
zmiany fazy
dobra tolerancja
dobra współpraca
małe ryzyko
teratogenności
możliwy
negatywny wpływ
na funkcje
psychoseksualne

70
SSRI - OBJAWY UBOCZNE
SSRI - OBJAWY UBOCZNE
DYSFUNKCJE SEKSUALNE:
WSZYSTKIE SSRI Z WYJĄTKIEM
FLUWOKSAMINY
HIPONATREMIA: WSZYSTKIE SSRI
ZNACZĄCE INTERAKCJE NA
POZIOMIE CYP450
71
T1/2 SSRI (h)
T1/2 SSRI (h)
Osoby
młodsze
Osoby
starsze
Citalopram
33
59
Fluoksetyna
48
43
Norfluoksetyna
254
185
Fluwoksamina
19
25
Paroksetyna
17
30
Sertralina
27
37
72
Selektywnośc inhibitorów 5HT / NA
in vitro
citalopram
sertalina
paroksetyna
fluvoksamina
fluoksetyna
venlafaksyna
klomipramina
amitryptylina
imipramina
nortryptylina
dezipramina
reboksetyna
maprotylina
Bech 1999
5HT
NA

73
Substraty izoenzymów
Substraty izoenzymów
CYP-450
CYP-450
2C19
Fenytoina
Warfaryna
3A4
BDZ
TLPD
CCB
Leki antyarytmiczne
1A2
TLPD
Kofeina
Teofilina
Paracetamol
Beta-blokery
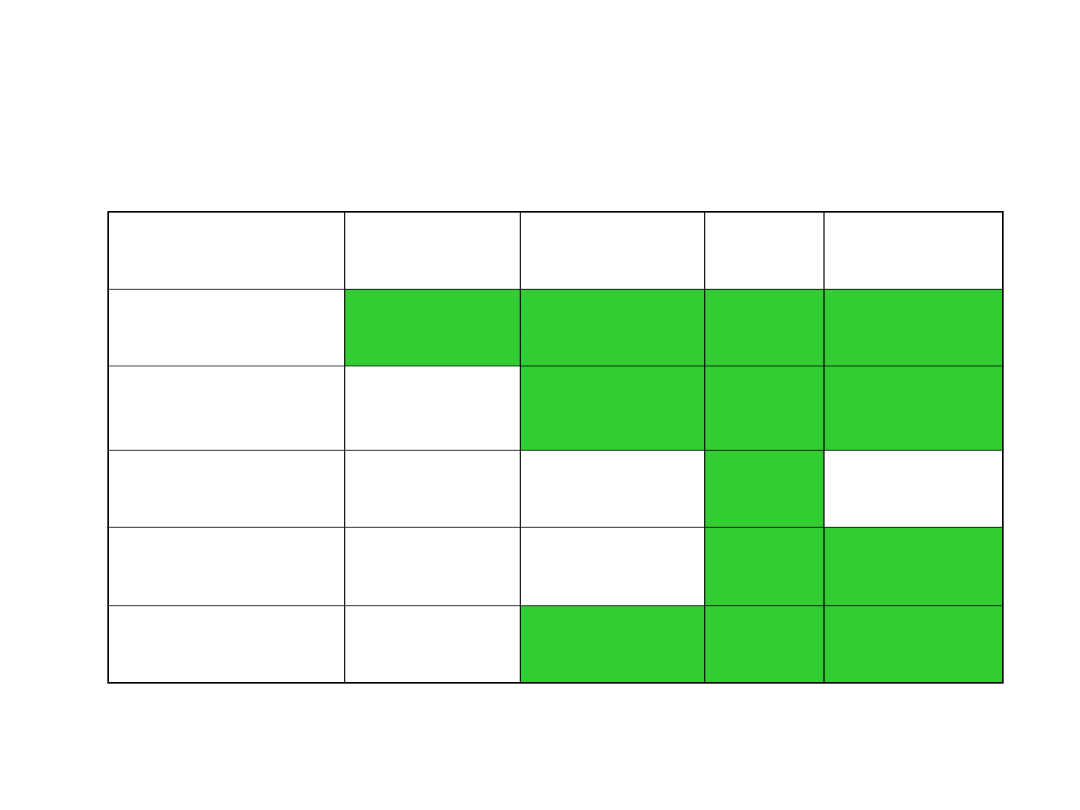
Objawy uboczne po SSRI występujące u >10% leczonych Harvey & Preskorn
-1996
11-15%
16-20%
21-
25%
26-30%
citalopram
fluoksetyna
Nudności,
niepokój
fluwoksamina
zaparcia
senność
nudności
paroksetyna
zmęczenie Senność,
nudności
sertalina
nudności
74
FLUOKSETYNA
Stahl - 2000
75
SSRI
SSRI
SRI
SRI
NRI
NRI
5-HT2c
5-HT2c
CYP 2D6
CYP 2D6
CYP 3A3,4
CYP 3A3,4
CITALOPRAM
Stahl - 2000
76
SRI
SRI
CITALOPRAM

Praktyczna wskazówka
• Jeśli nie brać pod
uwagę bezpośredniej
ceny leku,
lekami
przeciwdepresyjnymi
pierwszego wyboru
w terapii depresji
niepsychotycznej są
SSRI
, ze względu na
bezpieczeństwo ich
stosowania i profil
objawów ubocznych
Bazire-1999
77
78
Dawkowanie
Dawkowanie
SSRI
Fluoksetyna
20
20-40
Sertralina
50
100-150
Paroxetina
20
20
Fluvoxamin
a
50
50-300
Citalopram
10
20-60

79
Dlaczego LPD w leczeniu
Dlaczego LPD w leczeniu
zaburzeń lękowych?
zaburzeń lękowych?
W przebiegu depresji występuje lęk i
vice versa
LPD mają działanie p/lękowe
BDA uzależniają - LPD nie
Współczesne LPD mają niewiele
objawów ubocznych
W patogenezie większości zaburzeń
lękowych, szczególnie w leczeniu
napadów paniki i OCD , ważny jest
deficyt serotoniny

80
Zastosowanie LPD w terapii zaburzeń nie-depresyjnych
Zastosowanie LPD w terapii zaburzeń nie-depresyjnych
Zaburzenie
Terapia 1. wyboru
Terapia 2. wyboru
Napady paniki
SSRI, wenlafaksyna TLPD
GAD
SSRI
RIMA, TLPD
Fobia socjalna
RIMA
SSRI
OCD
SSRI, klomipramina SSRI, klomipramina
bulimia
SSRI
PTSD
SSRI

81
Inhibitory monoaminooxydazy
Inhibitory monoaminooxydazy
(IMAO)
(IMAO)
Nieselektywne:
phenelzyna,
trancylpromina
Selektywne:
selegilina (jumex)
Selektywne,
odwracalne
inhibitory MAO A
(RIMA): moklobemid
(aurorix, mocloxil)
82
Mechanizm działania IMAO
Mechanizm działania IMAO
MAO-A
5-HT
NA
MAO-B
DA
depresja
Choroba Parkinsona
RIMA
selegilina

83
RIMA
RIMA
ZALETY WADY
ZALETY WADY
Skuteczne przy
terapii depresji
atypowej
Mała liczba
interakcji
Bezpieczne w terapii
osób w wieku
podeszłym
Brak dysfunkcji
seksualnych
Lek z wyboru w
terapii fobii socjalnej
Dawkowanie – 300-
600 mg/p.d./BID
Mniej skuteczne w
terapii depresji
typowej

84
Inne LPD
Inne LPD
Inhibitory wychwytu zwrotnego NA i
serotoniny: wenlafaksyna
Inhibitory wychwytu zwrotnego
katecholamin: bupropion
Alfa-2 antagoniści (NASSA): mirtazapina
Antagoniści receptorów 5-HT-2A i inhibitory
wychwytu zwrotnego serotoniny: trazodon,
nefazodon
Agoniści wychwytu zwrotnego serotoniny:
tianeptyna

WENLAFAKSYNA
• SNRI
• Wysoka skuteczność antydepresyjna
• Forma ER
• Dawkowanie – 75-225 mg p.d.
85

86
TIANEPTYNA
TIANEPTYNA
ZALETY WADY
ZALETY WADY
Znaczący efekt
przeciwlękowy
Brak
niebezpiecznych
interakcji
Dobrze tolerowana
przez osoby w wieku
podeszłym
Skuteczna w terapii
depresji alkoholowej
Dawkowanie – 2-3 x
12.5 mg
Mniejsza
efektywność
przeciwdepresyjna w
porównaniu z TLPD i
SSRI
87
Karmienie piersią, a leki
psychotropowe
grupa
Niskie
ryzyko
Średnie
ryzyko
Wysokie
ryzyko
Leki
antypsychotyczne
Flupentixol
Haloperidol
Fenotiazyny
sulpiryd
Klozapina
Risperidon
Leki antydepresyjne
Tianeptyna
Mianseryna
Moklobemid
TLPD
SSRI *
Mirtazapina
Doxepina
Maprotylina
Wenlafaxyn
a
Leki anksjolityczne
BDA LD
Beta-bokery
BDA
Klometiazol
Buspiron
88
Ciąża a leki
psychotropowe
grupa
Niskie
ryzyko
Średnie
ryzyko
Wysokie
ryzyko
Leki antypsychotyczne
Sulpiryd
Tioxanteny
Klozapina
Olanazapina
Fenotiazyny
Butyrofenony
Risperidon
Leki antydepresyjne
Mianseryna
Mirtazapina
Moklobemid
SSRI
TLPD*
Amitryptylina
Nortryptylina
Leki anksjolityczne
Beta-blokery
Klometiazol
Buspiron
BDA
Strategia terapii depresji
niepsychotycznej
TMAP-1999
89
Etap 1.
MONOTERAPIA
SSRI, BUP, NEF, VLF
MONOTERAPIA
SSRI, BUP, NEF, VLF
AUGMENTACJA
AUGMENTACJA
Etap 2.
MONOTERAPIA
SSRI, BUP, NEF, TCA, VLF
MONOTERAPIA
SSRI, BUP, NEF, TCA, VLF
Strategia terapii depresji niepsychotycznej
TMAP-1999
90
Etap 3.
MONOTERAPIA
SSRI, BUP, NEF, VLF, TCA,
RIMA, MAOI
LEK Z GRUPY NIESTOSOWANEJ
W ETAPACH 1. i 2.
MONOTERAPIA
SSRI, BUP, NEF, VLF, TCA,
RIMA, MAOI
LEK Z GRUPY NIESTOSOWANEJ
W ETAPACH 1. i 2.
Etap 4.
AUGMENTACJA LITEM
LEKU Z ETAPU 3.
AUGMENTACJA LITEM
LEKU Z ETAPU 3.

91
#1
#1
JB, 36-letnia kobieta została
przyprowadzona przez swoją
siostrę do gabinetu
psychiatry na dwa tygodnie
przed wyznaczoną wizytą.
Leczona od 9 lat z powodu
depresji. W czasie wizyty:
znacznie obniżony nastrój, z
anhedonią. Spowolniała, ze
znacznymi zaburzeniami
koncentracji myślenia w
czasie rozmowy. Dodatkowo
skargi na zaburzenia
zasypiania i wczesne
budzenie. Skargi na brak
łaknienia, szybkie
chudnięcie. Wyraźne objawy
odwodnienia. Potwierdza
myśli rezygnacyjne, ale
„raczej chce umrzeć w czasie
snu”, niż planuje
samobójstwo.
Do tej pory rozpoznawano u
niej „depresję powrotną”.
Kilka razy hospitalizowana z
tego powodu. Ostatni raz
leczona przed rokiem – 3-
miesięczny pobyt. Od czasu
tej hospitalizacji przyjmowała
amitryptylinę 200 mg na noc,
i czuła się dobrze jeszcze na
miesiąc przed wizytą. W
wyniku tej wizyty została
przyjęta do szpitala, gdzie po
nawodnieniu
zaproponowoano ELD.
Pacjentka i jej rodzina nie
wyrazili zgody na zabiegi
elektryczne. Nadal leczona
amitryptyliną.

92
# 1
# 1
Uzyskano od chorej
informację, że przy
jednej z poprzednich
hospitalizacji po
dołączeniu litu nie
było wyraźnej
poprawy,
zdecydowano się
dołączyć do
amitryptyliny
fluvoxaminę w dawce
50 mg na noc.
5 dni później
pacjentka zaczęła się
skarżyć, że czuje się
bardzo źle, że
wysychają jej śluzówki
i niewyraźnie widzi.
Wystąpiło kilka
epizodów
zasłabnięcia, pojawiła
się tachykardia. Nie
było objawów
odwodnienia.

93
#1 - uwagi
#1 - uwagi
Ocena stężenia TLPD
jest bardzo istotna dla
analizy braku
współpracy i
obserwacji
metabolizmu tych
leków.
Większość SSRI ma
wpływ inhibicyjny na
cytochromy
wątrobowe
SSRI blokują
metabolizm TLPD,
powodują objawy
toksyczne.

94
#2
#2
TR, 45-letni
mężczyzna został
przyjęty to szpitala
psychiatrycznego z
powodu silnego lęku i
agitacji. Badanie
wykazało gorsze
samopoczucie rano,
wczesne budzenie się,
spadek wagi i
anhedonię. Przyznał
się do planów
samobójczych.
Jednocześnie nie
wykazywał cech
psychotycznej
depresji.
Leczony
psychiatrycznie
ambulatoryjnie od
czasu śmierci swojej
matki. Od 1,5 roku
leczony fluoxetyną.
Jest osobą samotną i
mieszka w wynajętej
kawalerce. Pracował
przez wiele lat jako
stolarz meblowy, ale z
powodu depresji od
roku jest na rencie.

95
#2
#2
Pali ok. 30 papierosów
dziennie, nie
nadużywa alkoholu.
Cierpi na ból w
okolice lewego biodra,
po wypadku
motocyklowym przed
15 laty. Od 10 tygodni
przyjmuje dziennie:
20 mg fluoxetyny, 20
mg temazepamu na
noc i 75 mg
indometacyny na noc.
Rutynowe badania
krwi – bez odchyleń
od normy.
W szpitalu
otrzymał
paroxetynę (20>40
mg) pd., ale po 8
tygodniach terapii
jego stan nie
poprawił się.

96
#2-uwagi
#2-uwagi
Pacjenci, którzy nie
reagują na lek z jednej
grupy, powinni być
leczeni LPD z innej
grupy.
Augmentacja przy
użyciu litu lub
buspironu jest
bezpieczną i
sprawdzoną metodą
poprawy efektów
terapii PD.
Tylko u 5% chorych z
depresją oporną na
terapię uzyskuje się
poprawę w ciągu 3 lat
stałej terapii PD.

Standardy terapii zaburzenia afektywnego
dwubiegunowego
Andrzej Czernikiewicz
Spektrum afektywne
98
cyklotymia
BP II
BP I
SA
BP NOS
RMDD
Depresja psychotyczna
Depresja atypowa
SMDE
dystymia
99
Mania
Hypomania
Euthymia
„mała”
depresja
„duża”
depresja
Faza terapii ostrego epizodu
Faza leczenia profilaktycznego
Fazy terapii zaburzenia afektywnego
dwubiegunowego
Frank E, et al. Biol Psychiatry. 2000;48(6):593-
604.

100
Jaki powinien być „lek normotymiczny”?
Jaki powinien być „lek normotymiczny”?
[Schatzberg-2001]
[Schatzberg-2001]
Efekt antymaniakalny
Efekt antymaniakalny
Efekt antydepresyjny
Efekt antydepresyjny
Możliwość zapobiegania epizodom: maniakalnym,
Możliwość zapobiegania epizodom: maniakalnym,
depresyjnym
depresyjnym
Niewielkie ryzyko „szybkiej zmiany fazy”
Niewielkie ryzyko „szybkiej zmiany fazy”
Terapia objawów rezydualnych
Terapia objawów rezydualnych
Brak ryzyka precypitacji epizodu manii
Brak ryzyka precypitacji epizodu manii
Brak ryzyka precypitacji depresji
Brak ryzyka precypitacji depresji
Łatwość stosowania
Łatwość stosowania
„
„
przyjazne” monitorowanie
przyjazne” monitorowanie
Niewielkie objawy uboczne
Niewielkie objawy uboczne
Poprawa współpracy
Poprawa współpracy
Zalety farmakoekonomiczne
Zalety farmakoekonomiczne
101
Ryzyko samobójstwa po przerwaniu kuracji
Ryzyko samobójstwa po przerwaniu kuracji
litem
litem
[Mueller i Oerlinghausen i in.-1992]
[Mueller i Oerlinghausen i in.-1992]
Kuracja
litem
Przerwanie
kuracji
litem
risk ratio
p<
Zachowania
suicydialne
9,3%
85,7%
9,3
p<0,01
Samobójstw
a
1,8%
35,7%
19,3
p<0,01

102
Objawy uboczne po lekach o
Objawy uboczne po lekach o
możliwym działaniu
możliwym działaniu
normotymicznym
normotymicznym
[Schatzberg-2001; Taylor i
[Schatzberg-2001; Taylor i
Patton-2002]
Patton-2002]
LIT
LIT
wagi, drżenia, objawy ze strony układu
wagi, drżenia, objawy ze strony układu
pokarmowego,
pokarmowego,
funkcji tarczycy, dysfunkcje
funkcji tarczycy, dysfunkcje
poznawcze
poznawcze
WALPROINIANY
WALPROINIANY
wagi, zaburzenia
wagi, zaburzenia
wątrobowe
wątrobowe
KARBAMAZEPINA
KARBAMAZEPINA
WBC, RBC; zmiany
WBC, RBC; zmiany
skórne, nudności
skórne, nudności
KLOZAPINA
KLOZAPINA
wagi, AIHG, sedacja,
wagi, AIHG, sedacja,
agranulocytoza, ślinotok
agranulocytoza, ślinotok
OLANZAPINA
OLANZAPINA
wagi, AIHG, sedacja
wagi, AIHG, sedacja
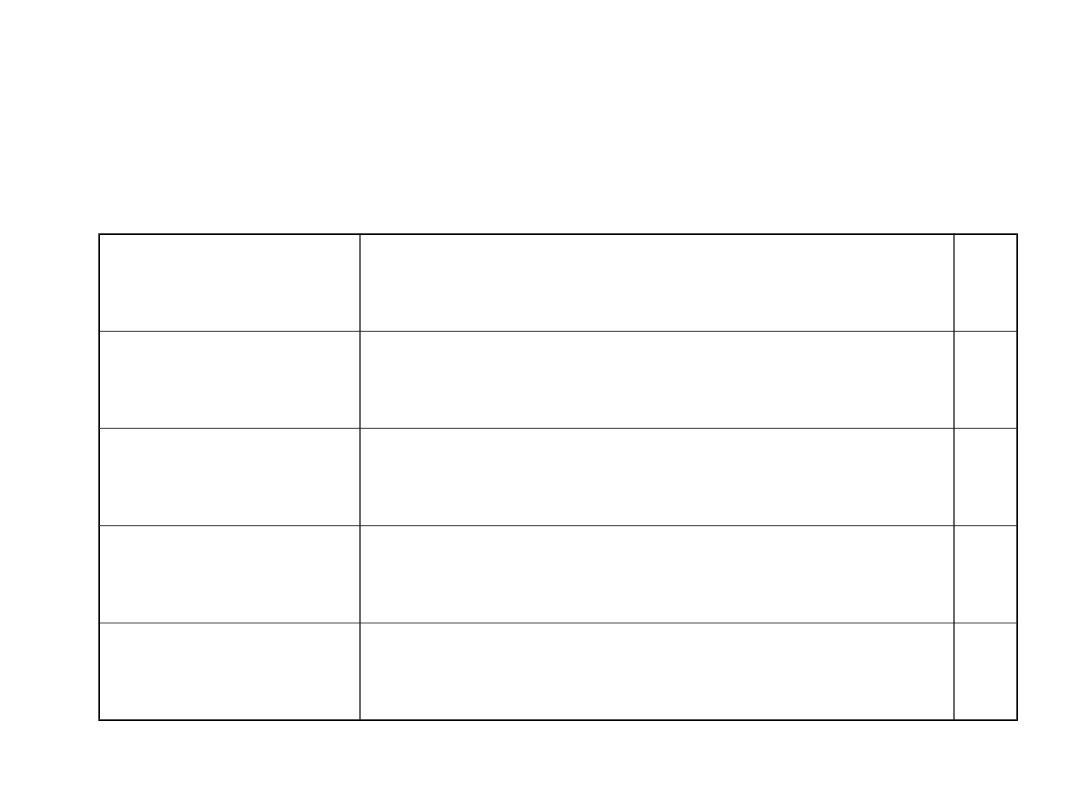
Strategia początku terapii pierwszego epizodu manii
Obraz kliniczny
Preferowana strategia
Mania z psychozą Normotymik (MS)+ lek antypsychotyczny
(AP)
Mania z dysforią
lub epizod
mieszany
MS
Mania euforyczna MS
MS + BDZ
Hipomania
MS
103
104
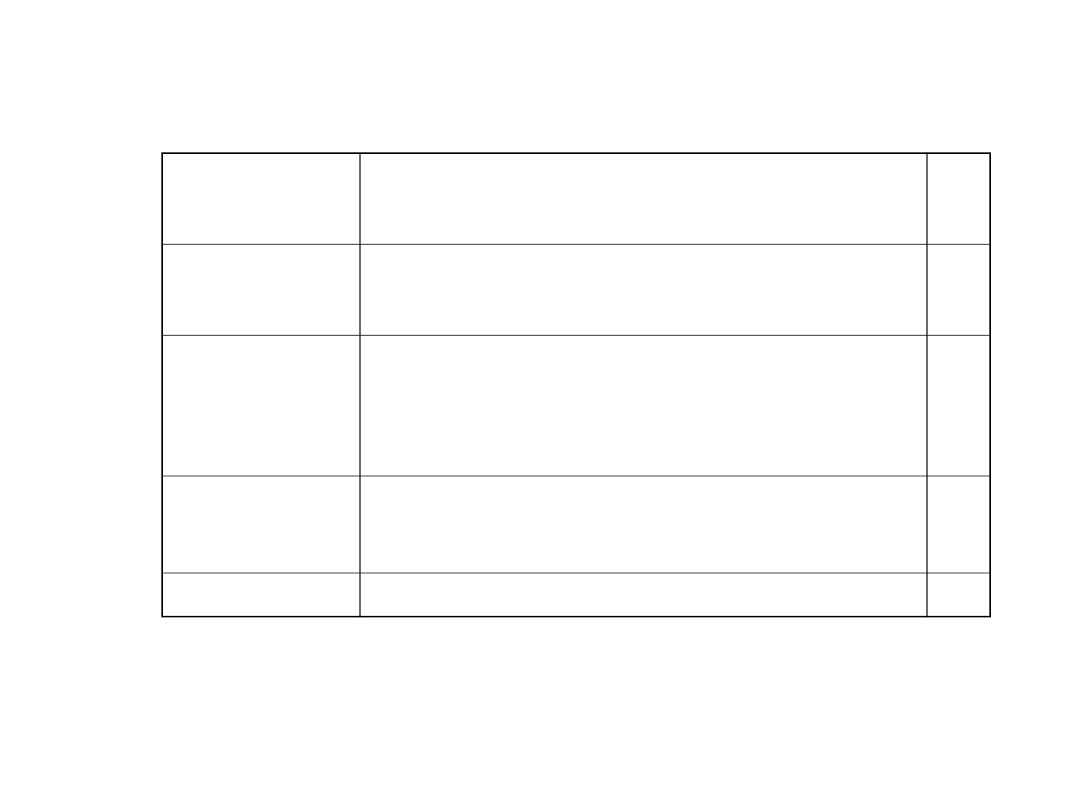
Strategia wyboru AP
Strategia wyboru AP
Obraz
kliniczny
Preferowana strategia
Mania z
psychozą
OLA, HPCAP, RIS
Mania z
dysforią
lub epizod
mieszany
OLA, RIS
Mania
euforyczna
OLA, RIS
Hipomania
---
Strategia terapii manii u
pacjentów z częstą zmianą
faz
105
VAL + CBZ lub Lit
+ atypowy AP
VAL + Lit + CBZ
CLO
LMG, GBP, ELD, T4
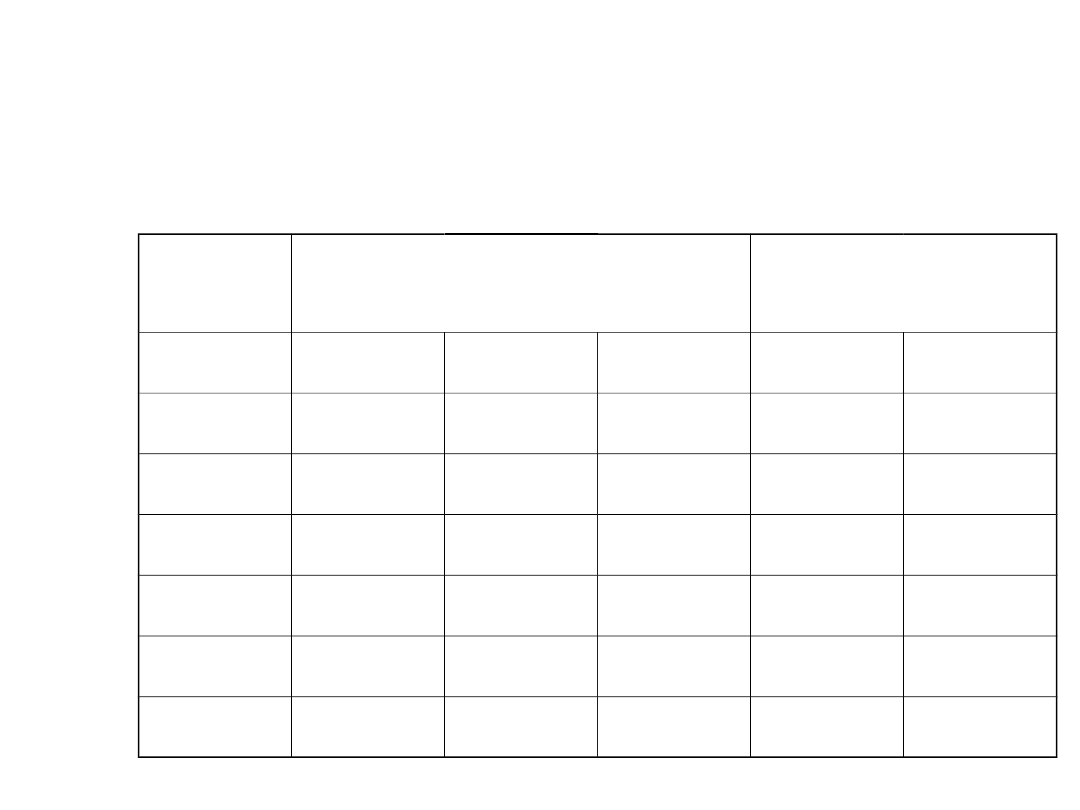
Właściwe dawki i stężenia
Terapia manii
dawki
Leczenie
Pod-
trzymujące
dawki
Lek
Początkowa
Niska
docelowa
Wysoka
docelowa
Niska
Wysoka
CBZ (mg)
400+-100
600+-200
1400+-400
CBZ (g/mL)
6,1+-2,6
12,6+-4,2
5,7+-1,5
10,8+-2,2
VAL (mg)
750+-375
750+-375
2750+-1000
VAL (g/mL)
58,9+-14,9
120+-16,6
56,6+-12
109+-17
Lit (mg)
900+-300
900+-300
2100+-600
Lit(mEq/L)
0,7+-0,1
1,2+-0,1
0,6+-0,1
1,1+-0,1
106

Preferowane normotymiki przy pierwszym
epizodzie depresji w przebiegu ChAD
• Wyłącznie
normotymik:
– Lit
– VAL
– LAM
• Normotymik + AD:
– Lit
– VAL
107

VAL > Lit, CBZ
• Insomnia
• Pobudzenie psychomotoryczne
• Agresja
• Współistniejące: PD, PTSD, ZUA, narkomania
• Choroba serca
• Stan po udarze mózgu
• Pacjenci w podeszłym wieku z objawami
otępienia
108

Lit > VAL, CBZ CBZ > Lit, VAL
• Znaczące spowolnienie
psychomotoryczne
• Niewydolność wątroby
• Drugi lub trzeci
trymestr ciąży
• Dzieci
• Dziewczęta w okresie
adolescencji
• Niewydolność nerek
• Obawa przed
wzrostem wagi
109

110
APA Bipolar 2002 Practice Guideline
(c.d.)
Leczenie biologiczne (farmakologiczne)
Ciężka mania lub stany mieszane: lit lub walproinian
+ lek antypsychotyczny
Preferowanie stosowania leków antypsychotycznych
drugiej generacji
ze względu na mniejsze ryzyko
objawów ubocznych
Pacjenci bez objawów ciężkiej manii, lub stanu
mieszanego:
monoterapia – lit, walproinian
, lub lek
antypsychotyczny drugiej generacji, np.
olanzapina
Terapia podtrzymująca
Terapia podtrzymująca
:
:
walproinian
walproinian
,
,
lit
lit
,
,
lub inne leki przy których osiągnięto obecną remisję:
lub inne leki przy których osiągnięto obecną remisję:
np.
np.
olanzapin
olanzapin
a
a
APA. Am J Psychiatry. 2002;159(4 suppl):1-50.

111
Co obok leków w terapii ChAD?
Co obok leków w terapii ChAD?
[Montgomery i Cassano-2000]
[Montgomery i Cassano-2000]
Wspólna z pacjentem i jego bliskimi
Wspólna z pacjentem i jego bliskimi
decyzja terapeutyczna
decyzja terapeutyczna
Psychoedukacja
Psychoedukacja
Zapewnienie wsparcia rodziny
Zapewnienie wsparcia rodziny
Rozpoznawanie zwiastunów nawrotu
Rozpoznawanie zwiastunów nawrotu
Wiara w możliwość leczenia
Wiara w możliwość leczenia
Nauka życia z chorobą
Nauka życia z chorobą
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
- Slide 99
- Slide 100
- Slide 101
- Slide 102
- Slide 103
- Slide 104
- Slide 105
- Slide 106
- Slide 107
- Slide 108
- Slide 109
- Slide 110
- Slide 111
Wyszukiwarka
Podobne podstrony:
Ppt0000012
Ppt0000040
Ppt0000007
Ppt0000000
Ppt0000001
Ppt0000024
Ppt0000005
Ppt0000000 2
Ppt0000019 ketony
Ppt0000001
Ppt0000003
Ppt0000005
więcej podobnych podstron