
RAK PIERSI
III Katedra i Klinika Chirurgii Ogólnej CM UJ w
Krakowie
Kierownik
Prof. dr hab. med. Roman M. Herman
RAK PIERSI
Epidemiologia i
Patofizjologia
Leczenie
Screening
Rozpoznanie
Epidemiologia i Patofizjologia
Zapadalność i umieralność
Czynniki ryzyka
Wpływy genetyczne i hormonalne
Klasyfikacja raka piersi
Stopień zaawansowania
Czynniki prognostyczne
EPIDEMIOLOGIA I PATOFIZJOLOGIA
ZAPADALNOŚĆ I UMIERALNOŚĆ
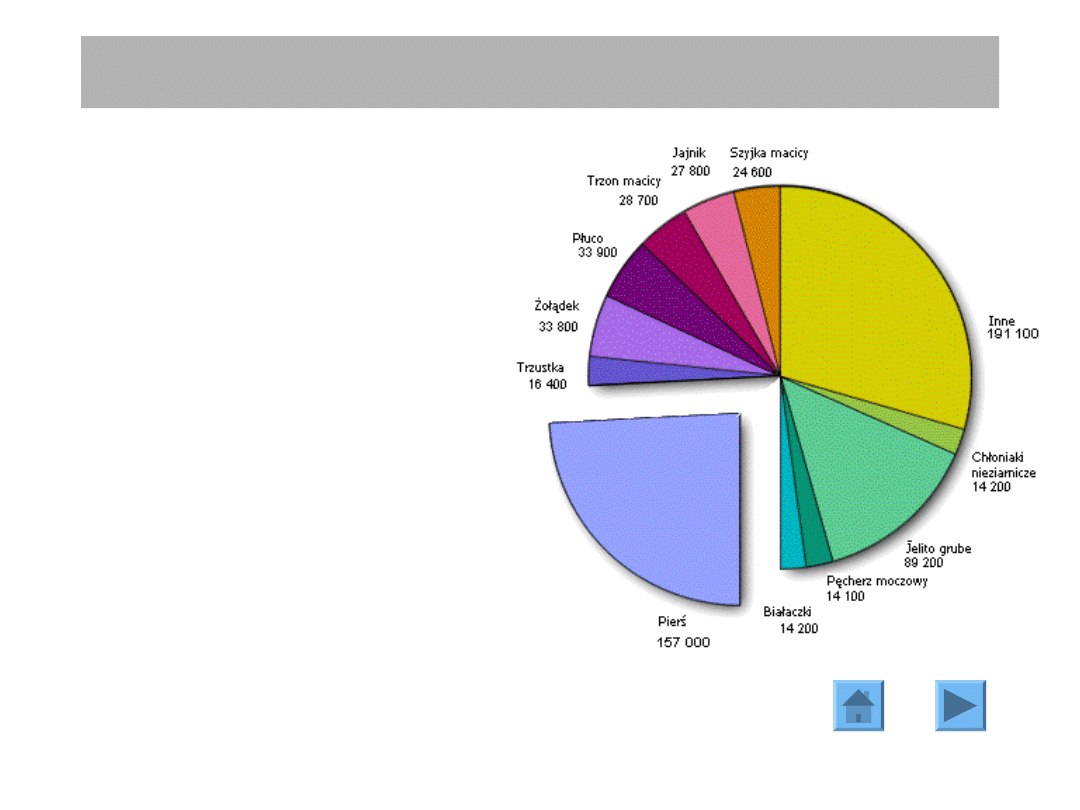
Rak piersi jest najczęstszym
nowotworem złośliwym u kobiet z
ponad 570000 nowych przypadków
rocznie na świecie.
W krajach Wspólnoty Europejskiej rak
piersi odpowiada za 24% zgonów z
powodu chorób nowotworowych.
W ciągu ostatnich 40 lat współczynnik
zapadalności na raka piersi stale
wzrasta, nie jest jednak jasne czy
spowodowane jest to większą i
wcześniejszą wykrywalnością poprzez
samobadanie i mammografię czy
związane z czynnikami
środowiskowymi.
Skala problemu

EPIDEMIOLOGIA I PATOFIZJOLOGIA
ZAPADALNOŚĆ I UMIERALNOŚĆ
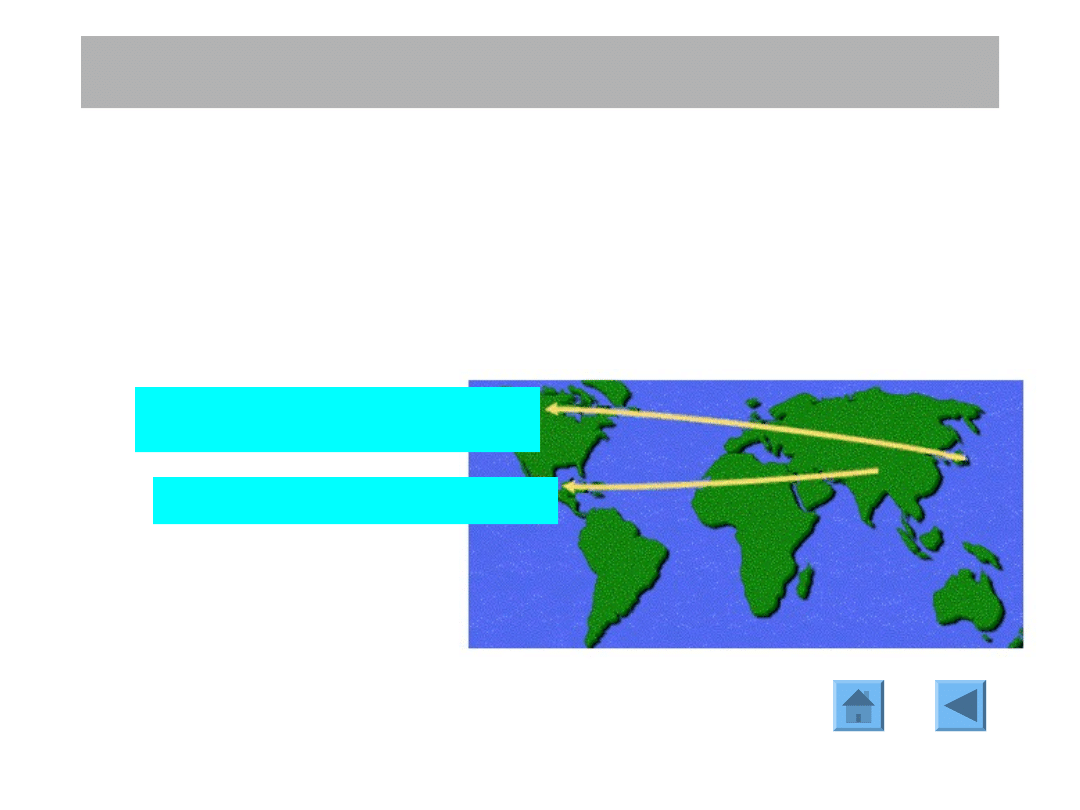
Współczynnik zapadalności na
raka piersi jest niższy w
niektórych częściach Chin i
Japonii, pośredni w Afryce
Południowej, na Karaibach i we
Wschodniej Europie, a wyższy w
Europie Zachodniej i w Ameryce
Północnej.
Zmienność zapadalności na
świecie
EPIDEMIOLOGIA I PATOFIZJOLOGIA
ZAPADALNOŚĆ I UMIERALNOŚĆ
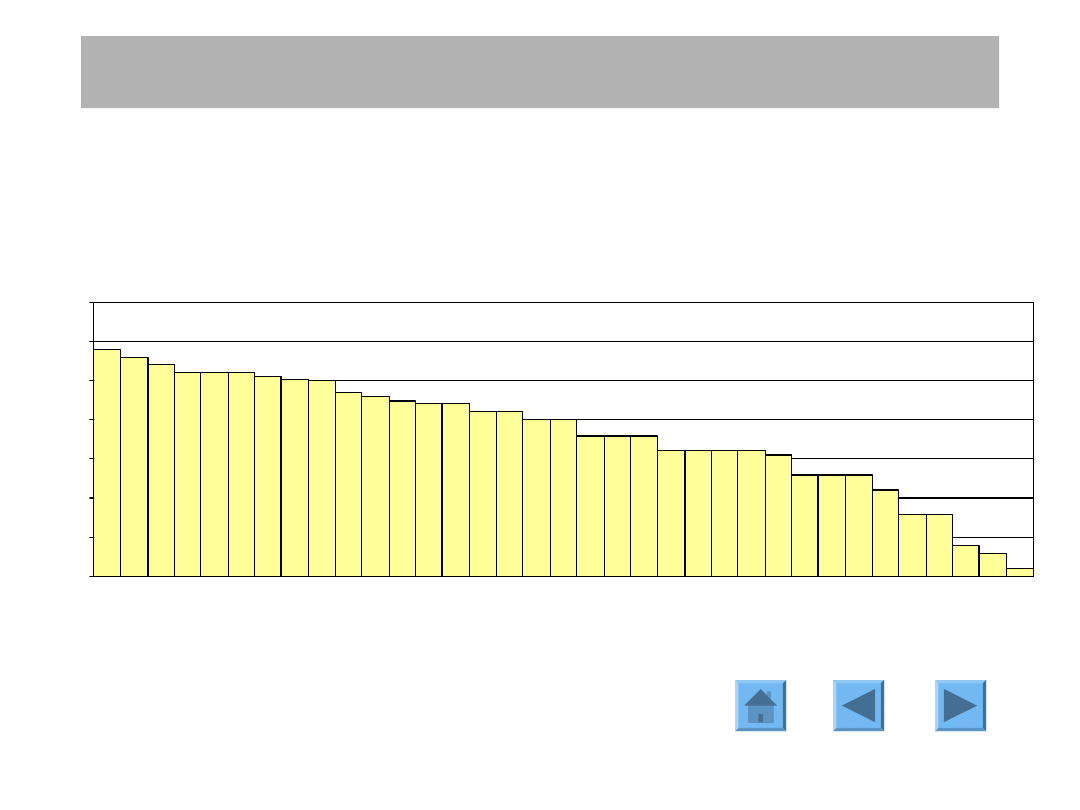
Istnieje uderzająca różnica pomiędzy umieralnością z powodu
raka piersi w różnych krajach świata. Generalnie wskaźnik
umieralności jest wyższy w krajach Europy Zachodniej i Ameryki
Północnej niż w krajach azjatyckich.
Umieralność
0
5
10
15
20
25
30
35
A
ng
lia
i
W
al
ia
D
an
ia
Ir
la
nd
ia
B
el
gi
a
N
.Z
el
an
di
a
H
ol
an
di
a
U
ru
gw
aj
S
zw
aj
ca
ria
K
an
ad
a
N
ie
m
cy
(
d.
R
F
N
)
Iz
ra
el
U
S
A
A
us
tr
ia
W
ęg
ry
W
ło
ch
y
A
us
tr
al
ia
C
ze
ch
os
ło
w
ac
ja
F
ra
nc
ja
N
or
w
eg
ia
F
in
la
nd
ia
N
ie
m
cy
(
d.
N
R
D
)
P
or
tu
ga
lia
H
is
zp
an
ia
K
ub
a
G
re
cj
a
P
ol
sk
a
ZS
R
R
C
hi
le
K
uw
ej
t
H
on
g
K
on
g
M
ek
sy
k
Ja
po
ni
a
C
hi
ny
K
or
ea
P
łd
T
aj
la
nd
ia
U
m
ie
ra
ln
o
ś
ć
n
a
1
0
0
t
y
s
.
k
o
b
ie
t
n
a
r
o
k

EPIDEMIOLOGIA I PATOFIZJOLOGIA
ZAPADALNOŚĆ I UMIERALNOŚĆ
Najwyższy wskaźnik umieralności z powodu raka
piersi mają Anglia i Walia, a najniższy Japonia i
Tajlandia.
Wskaźnik ten w wielu krajach pozostaje
niezmienny lub wzrasta. Od połowy lat 70-tych
do połowy lat 80-tych w wielu krajach o
największym wskaźniku umieralność nie
zmieniła się.
Odwrotnie zaś, w krajach o niskiej umieralności
wskaźnik ten zwiększył się co spowodowało
zacieranie się różnic.
Różnice w umieralności w krajach świata
EPIDEMIOLOGIA I PATOFIZJOLOGIA
ZAPADALNOŚĆ I UMIERALNOŚĆ
Badania nad rakiem piersi w populacjach emigrantów przyniosły wgląd w
etiologię raka piersi.
Zazwyczaj w ciągu 2 pokoleń rak piersi występuje tak samo często w
populacjach imigrantów co w populacji przyjmującej.
Wskazuje to na większe znaczenie czynników środowiskowych niż
genetycznych w etiologii tej choroby.
Badania nad migracjami
Japonki mieszkające w USA i na Hawajach mają
wyższy wskaźnik umieralności niż Japonki
mieszkające w Japonii.
Chinki które żyją w Singapurze, Hong Kongu i USA
mają wyższą umieralność niż Chinki z Szanghaju.
EPIDEMIOLOGIA I PATOFIZJOLOGIA
CZYNNIKI RYZYKA
Przyczyna(y) raka piersi jest
nieznana, jest jednak
prawdopodobne, że udział
mają czynniki genetyczne,
wrodzone czynniki
metaboliczne i wpływy
środowiskowe.
Zidentyfikowano wiele
czynników które są związane
z wyższą niż średnia
zapadalnością na raka piersi.
Zostały one podzielone na
„stałe”
(których nie można
zmniejszyć) i
„niestałe”
(na
które można mieć wpływ).
Czynniki ryzyka raka piersi
Leczenie estrogenami
i doustna antykoncepc
ja
Późna pierwsza ciąża i
bezdzietność.
Pochodzenie z kraju
Europy Zachodniej i
Ameryki Północnej
EPIDEMIOLOGIA I PATOFIZJOLOGIA
WPŁYWY GENETYCZNE I HORMONALNE
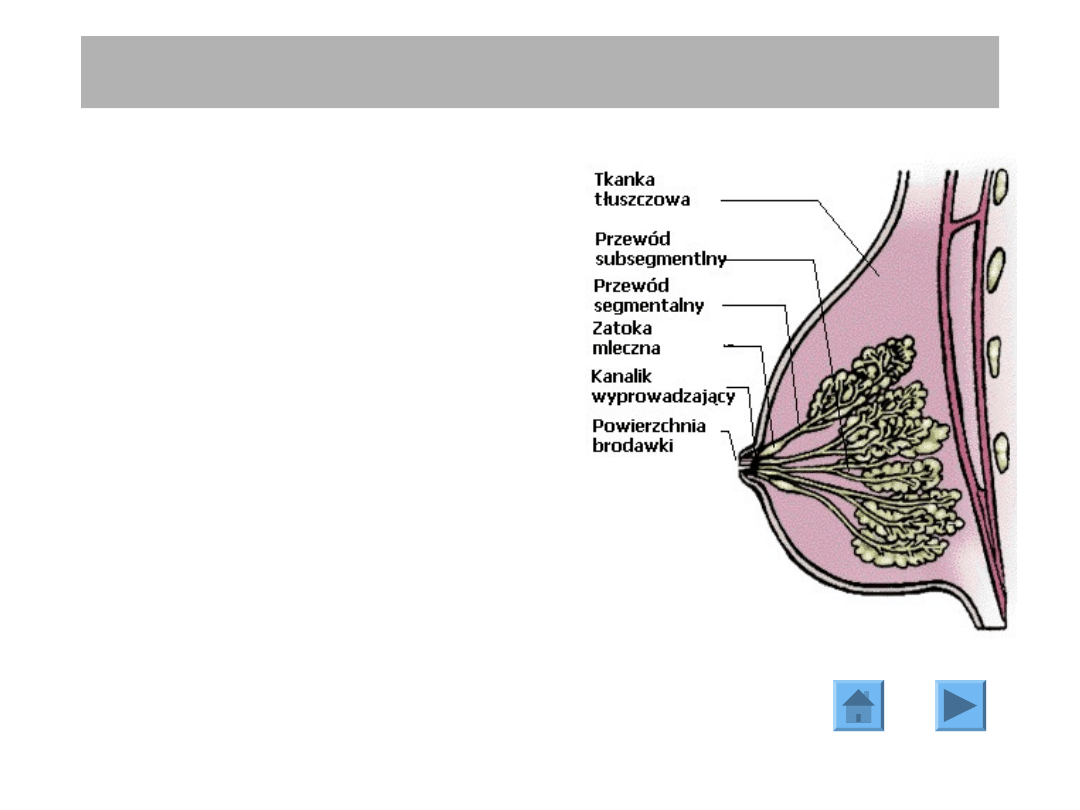
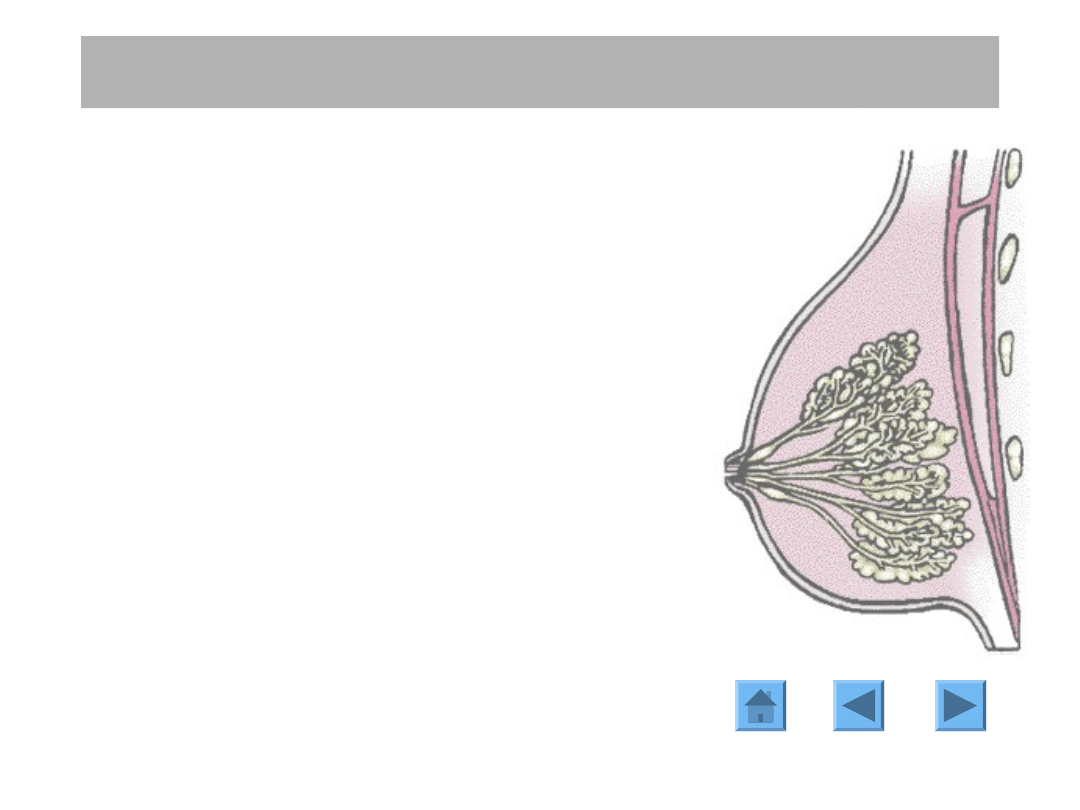
Pierś dojrzałej kobiety zbudowana jest z
elementów nabłonkowych i podścieliska.
Tkanki nabłonkowe tworzą rozgałęziające
się przewody budujące czynnościowe i
morfologiczne jednostki czyli zraziki, które
łączą się pod brodawką.
Podścielisko tworzą tkanka tłuszczowa i
włóknista, które stanowią większość
objętości gruczołu w okresie
nielaktacyjnym.
Ponad 95% złośliwych nowotworów piersi
rozwija się z tkanek nabłonkowych.
Anatomia gruczołu
EPIDEMIOLOGIA I PATOFIZJOLOGIA
WPŁYWY GENETYCZNE I HORMONALNE
Jako drugorzędowy organ płciowy, pierś odpowiada
na hormonalne środowisko ciała. I normalne i
złośliwe komórki są wrażliwe na działanie steroidów
płciowych, szczególnie estrogenów, progesteronu i
androgenów.
To działanie mediowane jest przez receptory , takie
jak receptor estrogenowy ( ER), progesteronowy ( PR
). Estrogeny głównie zdają się pobudzać normalny
wzrost przewodów, podczas gdy progesteron jest
odpowiedzialny rozwój pęcherzyków zrazikowych.
Pewna część raków piersi wykazuje ekspresję ER i
PR. Takie guzy są zazwyczaj lepiej zróżnicowane i
pacjenci z tymi guzami mają lepsze rokowanie.
Ilość ER i PR jest czynnikiem pozwalającym
przewidywać odpowiedź na leczenie hormonalne.
Wpływy hormonalne
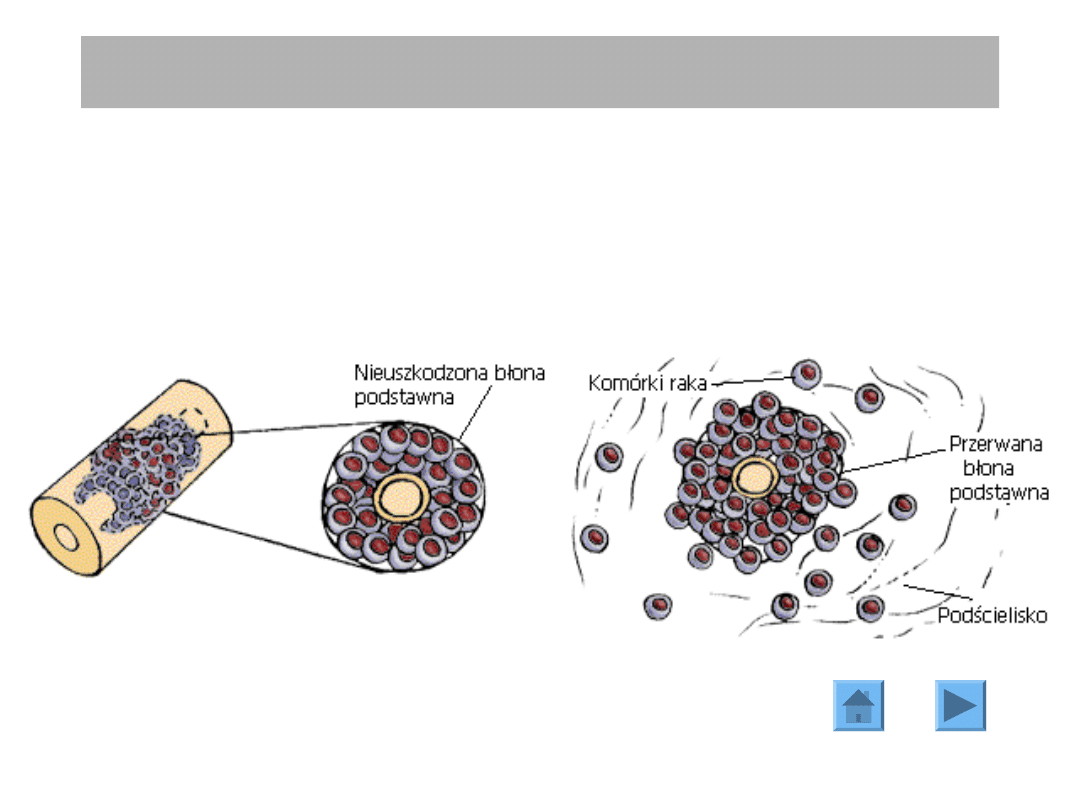
EPIDEMIOLOGIA I PATOFIZJOLOGIA
KLASYFIKACJA RAKA PIERSI
Rak piersi klinicznie i patologicznie jest bardzo niejednorodną chorobą,
obejmującą grupę zmian o różnym obrazie mikroskopowym i różnej biologii.
Przebieg choroby może różnić się znacznie u różnych pacjentek w zależności od
stopnia złośliwości i indywidualnej odpowiedzi na chorobę.
Wyróżnia się dwie główne grupy raków piersi:
Ogólny podział raka
piersi
Rak nienaciekający (in situ)
Rak naciekający
EPIDEMIOLOGIA I PATOFIZJOLOGIA
KLASYFIKACJA RAKA PIERSI
Rozróżnia się dwa główne typy raka piesi in situ:
rak przewodowy in situ
(CDIS - carcinoma ductale in situ) i
rak zrazikowy in situ
(CLIS - carcinoma
lobulare in situ).
Rak nienaciekający (in
situ)
DCIS
LCIS
Występowanie
częsty
rzadki
Objawy
przypadkowe stwierdzenie, zmiana w mammografii, zmiana na
przypadkowe
brodawce, guzek wyczuwalny palpacyjnie, choroba Pageta
stwierdzenie
Lokalizacja
przewody
zraziki
Postacie
comedo
non-comedo mixtum
(czopiasty)
cribriforme
micropapillare
papillare
solidum
solidum
Mikrozwapnienia
obecne
lub brak
zazwyczaj brak
Ryzyko naciekania
wysokie
niskie
Leczenie
chirurgiczne i napromienianie
obserwacja lub
chirurgiczne

EPIDEMIOLOGIA I PATOFIZJOLOGIA
KLASYFIKACJA RAKA PIERSI
Jest to niejednorodna grupa raków piersi o różnych cechach histologicznych.
Raki naciekające (inwazyjne)
Rak przewodowy naciekający „bez cech
Rak zrazikowy naciekający
specyficznych”
Częstość
częsty (ok. 75% raków naciekających)
raczej rzadki (5-10% raków naciekających)
Wykrycie
przypadkowe wykrycie, zmiana w mammo- zgrubienie skóry lub palpacyjnie
badalny guz
grafii, choroba Pageta, badalny guz
Wygląd
lity guz
lity guz, czasempolicykliczny
makroskopowy
Wygląd
różny stopień zróżnicowania
(skala
małe komórki z owalnymi jądrami
mikroskopowy
Blooma - Richardsona)
Pozostałe podtypy raka przewodowego naciekającego (raki przewodowe
naciekające „o cechach specyficznych”) są bardzo rzadkie:
ca tubullare
ok. 2%,
ca medullare
ok. 7%,
ca mucinosum
ok. 2%,
ca papillare
1-
2%
Raki te zazwyczaj lepiej rokują niż rak przewodowy naciekający „bez cech
specyficznych”.
EPIDEMIOLOGIA I PATOFIZJOLOGIA
KLASYFIKACJA RAKA PIERSI
Niektóre typy raka piersi wymagają
szczególniejszej uwagi. Są one często
klasyfikowane oddzielnie od ogólnego
podziału na raki in situ i inwazyjne.
Są to:
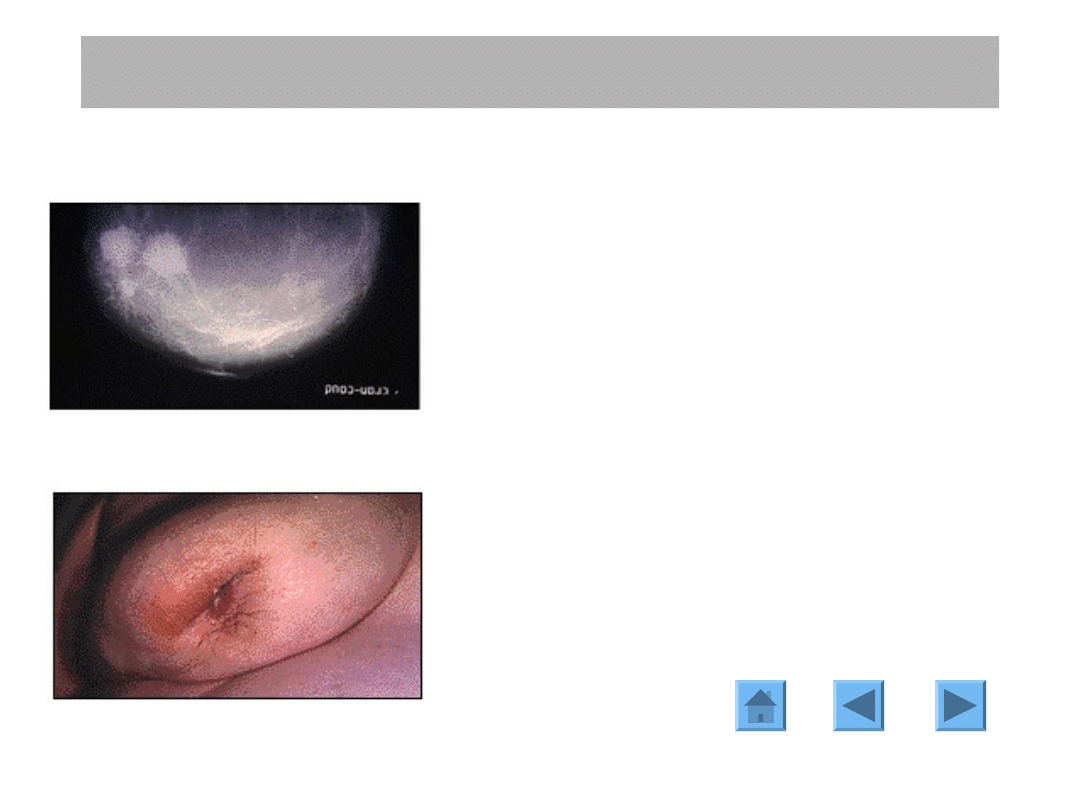
rak zapalny sutka
choroba Pageta
brodawki sutkowej
Raki rzadko spotykane

EPIDEMIOLOGIA I PATOFIZJOLOGIA
KLASYFIKACJA RAKA PIERSI
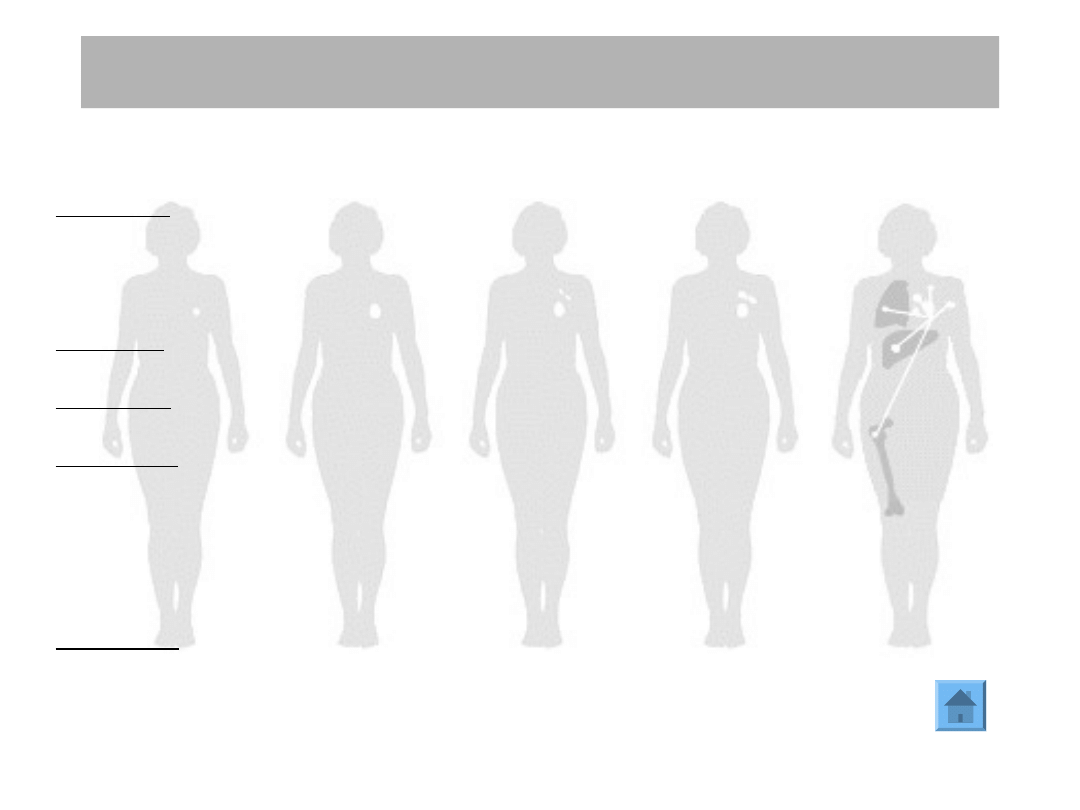
Rak piersi może przerzutować do niemal wszystkich tkanek i narządów
ustroju. Przerzuty mogą być stwierdzone w chwili rozpoznania choroby jak i
mogą się rozwinąć po leczeniu systemowym.
Najczęstszymi miejscami rozwoju przerzutów jako wznowy po leczeniu są:
okoliczne
węzły chłonne i ściana klatki piersiowej
(20-40%),
kości
(20-60%),
wątroba
(5-15%),
płuca i opłucna
(15-25%),
centralny system nerwowy
(5-
10%).
W badaniach pośmiertnych przerzuty najczęściej rozpoznaje się w
kościach
(60-90%),
płucach i opłucnej
(50-75%),
wątrobie
(50-75%),
centralnym
systemie nerwowym
(30-75%). Zajęte mogą też być narządy
układu
pokarmowego
inne niż wątroba (trzustka, jelita, żołądek) w 30-40%,
układu
wewnątrzwydzielniczego
(jajniki, tarczyca, nadnercza, przysadka) w 40-60%,
układu krążenia
(osierdzie, mięsień sercowy) w 25-40%.
Przerzutowanie raka
piersi

EPIDEMIOLOGIA I PATOFIZJOLOGIA
STOPIEŃ ZAAWANSOWANIA
Aktualnie
przyjęte
jest
określanie
stopnia
zaawansowania raka piersi według systemu TNM
zaakceptowanego przez International Union Against
Cancer (IUCC) i American Joint Committee on
Cancer (AJCC).
W systemie tym cecha T określa guz, N stan
okolicznych węzłów chłonnych a M obecność
przerzutów.
Kliniczne
określenie
stopnia
zaawansowania (z ang. „staging”) oparte jest na
wszystkich dostępnych
przed podjęciem leczenia
informacjach pochodzących z badania fizykalnego,
badań obrazowych i badania histopatologicznego (w
tym przypadku stosuje się przedrostek p).
Jeżeli istnieją wątpliwości co do kategorii do jakiej
włączyć daną pacjentkę, to klasyfikuje się ją do
grupy o mniejszym zaawansowaniu (kategorii
niższej).
Klasyfikacja TNM
T - tumor
N - nodi
lymphatici
M -
metastases
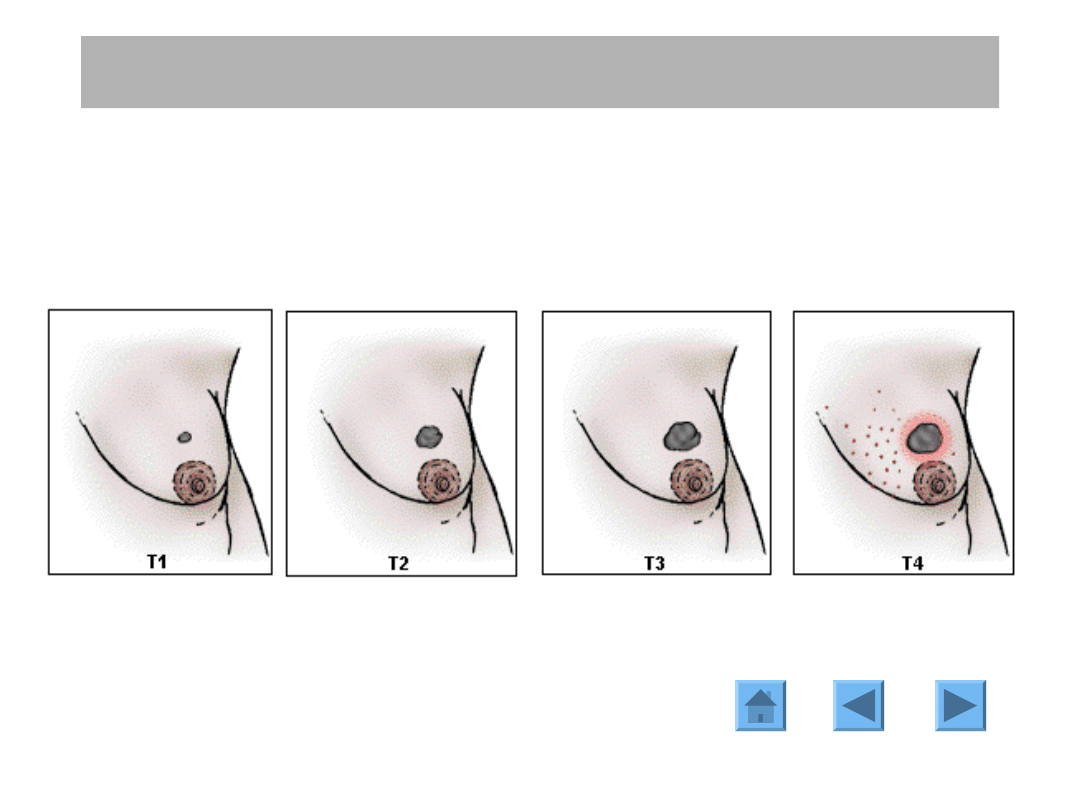
EPIDEMIOLOGIA I PATOFIZJOLOGIA
STOPIEŃ ZAAWANSOWANIA
Tx guz pierwotny nie może być określony
T0 nie stwierdza się obecności guza pierwotnego
Tis rak in situ
Cecha T (guz pierwotny)
guz <2cm w na
jwiększym wym
iarze
guz >2cm i
<5cm w
największym
wymiarze
guz >5cm w
największym
wymiarze
Bardziej zaawans
owane miejscowo
postacie
EPIDEMIOLOGIA I PATOFIZJOLOGIA
STOPIEŃ ZAAWANSOWANIA
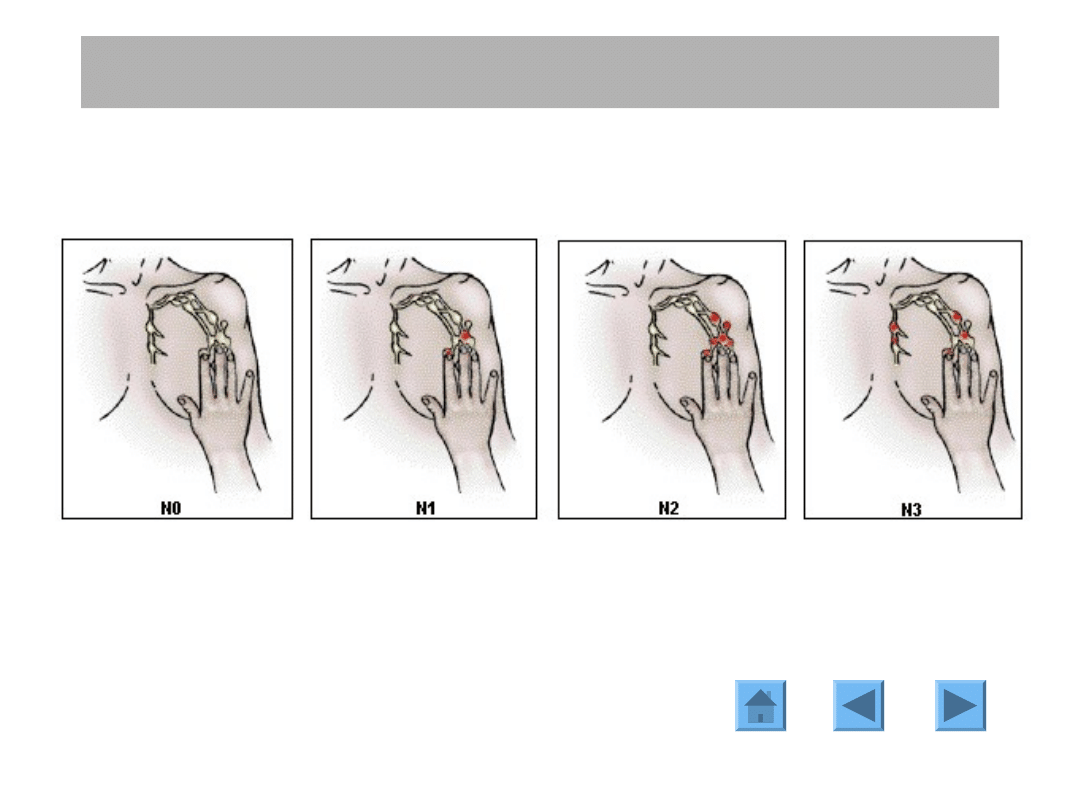
Cecha N (węzły chłonne)
Węzły chłonne
pachowe
niebadalne
ruchome węzły
chłonne
węzłów
chłonnych
węzłach
chłonnych
wzdłuż tętnicy
piersiowej
wewnętrznej
EPIDEMIOLOGIA I PATOFIZJOLOGIA
STOPIEŃ ZAAWANSOWANIA
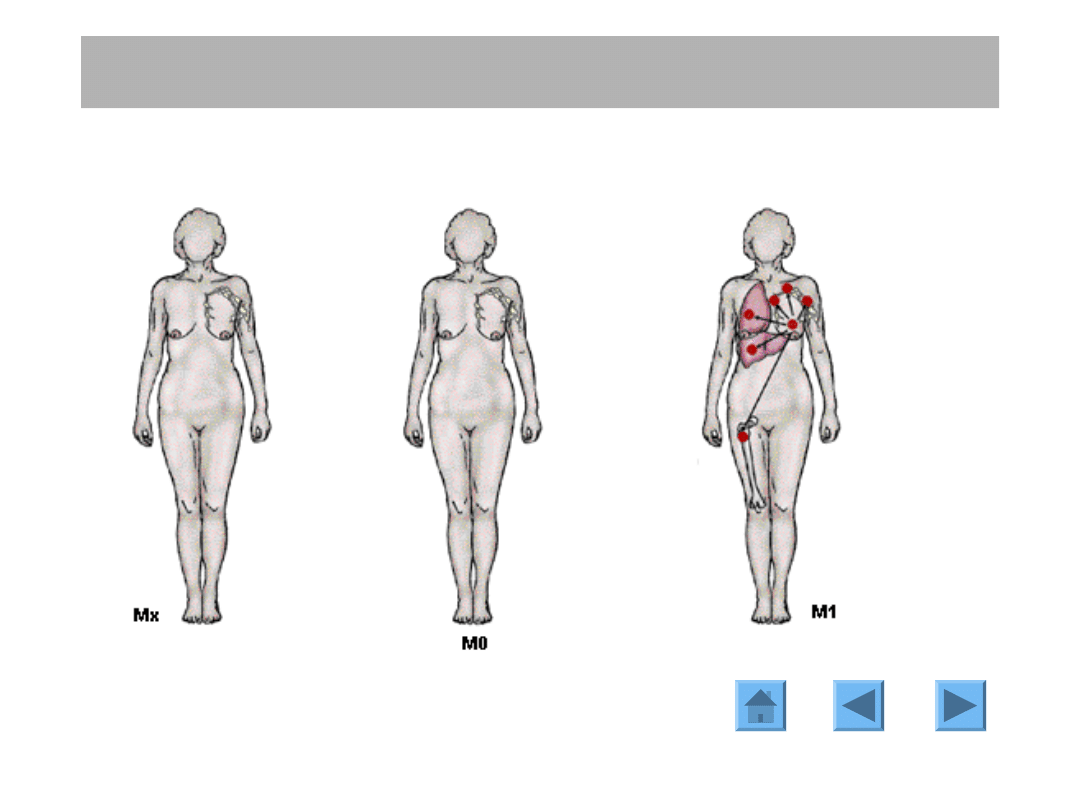
Cecha M (przerzuty)
Obecność przerzutów
nie może być
określona
Brak przerzutów
odległych
Obecne przerzuty
odległe (w tym
również w węzłach
nadobojczykowych)

0
I
IIA
IIB
IIIA
IIIB
IV
Tis
T1
T0
T1
T2
T2
T3
T0
T1
T2
T3
T3
T4
każde T
każde T
N0
N0
N1
N1
N0
N1
N0
N2
N2
N2
N1
N2
każde N
N3
każde N
M0
M0
M0
M0
M0
M0
M0
M0
M0
M0
M0
M0
M0
M0
M1
EPIDEMIOLOGIA I PATOFIZJOLOGIA
STOPIEŃ ZAAWANSOWANIA
Nieoficjalną i nieprecyzyjną
ale powszechnie stosowaną
skalą
jest skala
stadiów
klinicznych
oparta
na
systemie TNM.
Stopnie zaawansowania
Stopnie
zaawansowania
EPIDEMIOLOGIA I PATOFIZJOLOGIA
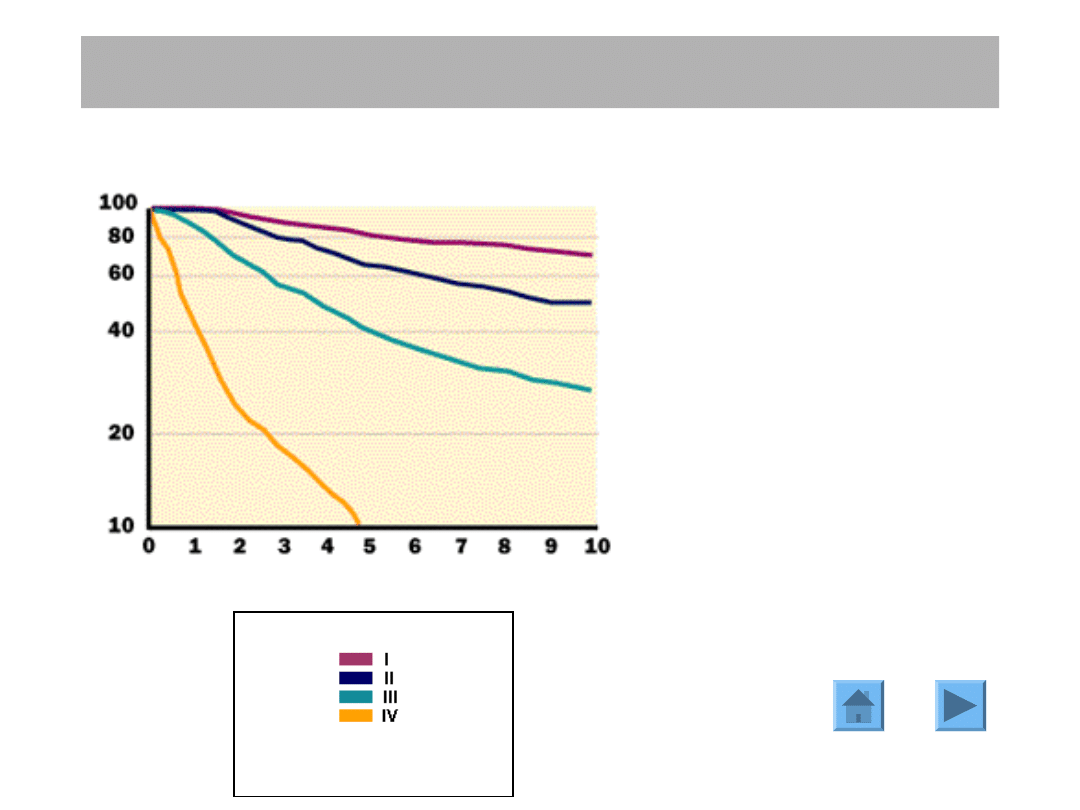
CZYNNIKI PROGNOSTYCZNE
Kliniczny
stopień
zaawansowania jest jednym z
najważniejszych
czynników
rokowniczych. Szansa pacjentki
na przeżycie ponad 5 do 10 lat
bezpośrednio
zależą
od
zaawansowania
w
chwili
rozpoznania.
Kliniczny stopień zaawansowania
rozpoznaniu
se
te
k
p
rz
e
ży
ć
(%
)
EPIDEMIOLOGIA I PATOFIZJOLOGIA
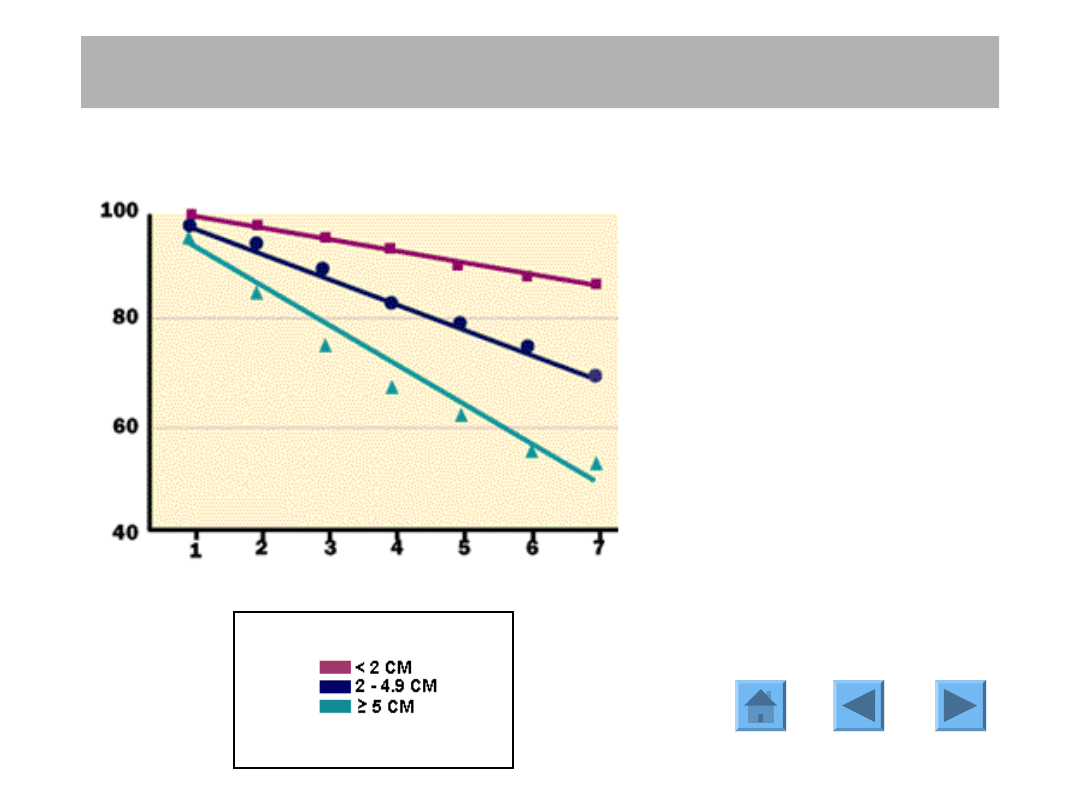
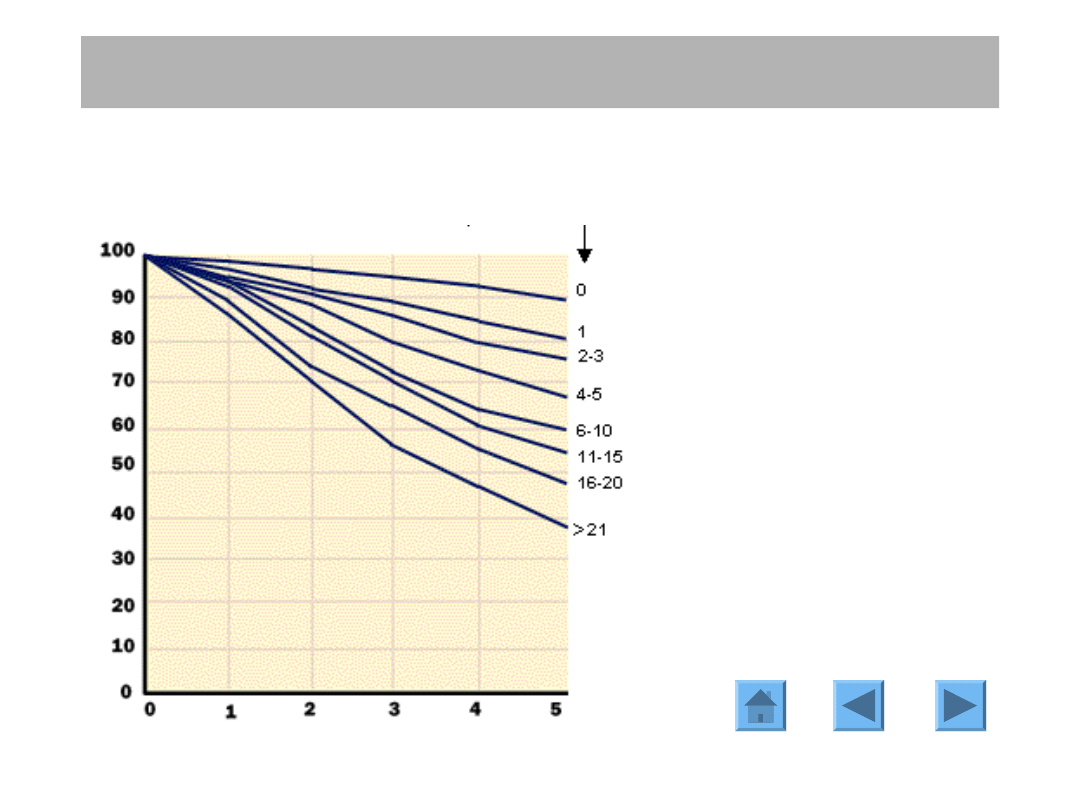
CZYNNIKI PROGNOSTYCZNE
Wielkość guza określana w
badaniu
histopatologicznym
bezpośrednio
koreluje
z
przeżyciem
i
jest
silnym
czynnikiem ryzyka wystąpienia
nawrotu choroby.
Wielkość guza
O
d
se
te
k
p
rz
e
ży
ć
(%
)
Lata po
rozpoznaniu
Wielkość guza
EPIDEMIOLOGIA I PATOFIZJOLOGIA
CZYNNIKI PROGNOSTYCZNE
Obecność
lub
brak
przerzutów
w
węzłach
chłonnych pachowych jest
najsilniejszym
czynnikiem
rokowniczym przeżycia w
raku piersi.
Zajęcie węzłów chłonnych
sugeruje bowiem obecność
mikroprzerzutów w innych
narządach.
Obecność przerzutów w węzłach chłonnych
pachowych
Lata po
rozpoznaniu
O
d
se
te
k
p
rz
e
ży
ć
(%
)
Liczba zajętych
węzłów
EPIDEMIOLOGIA I PATOFIZJOLOGIA
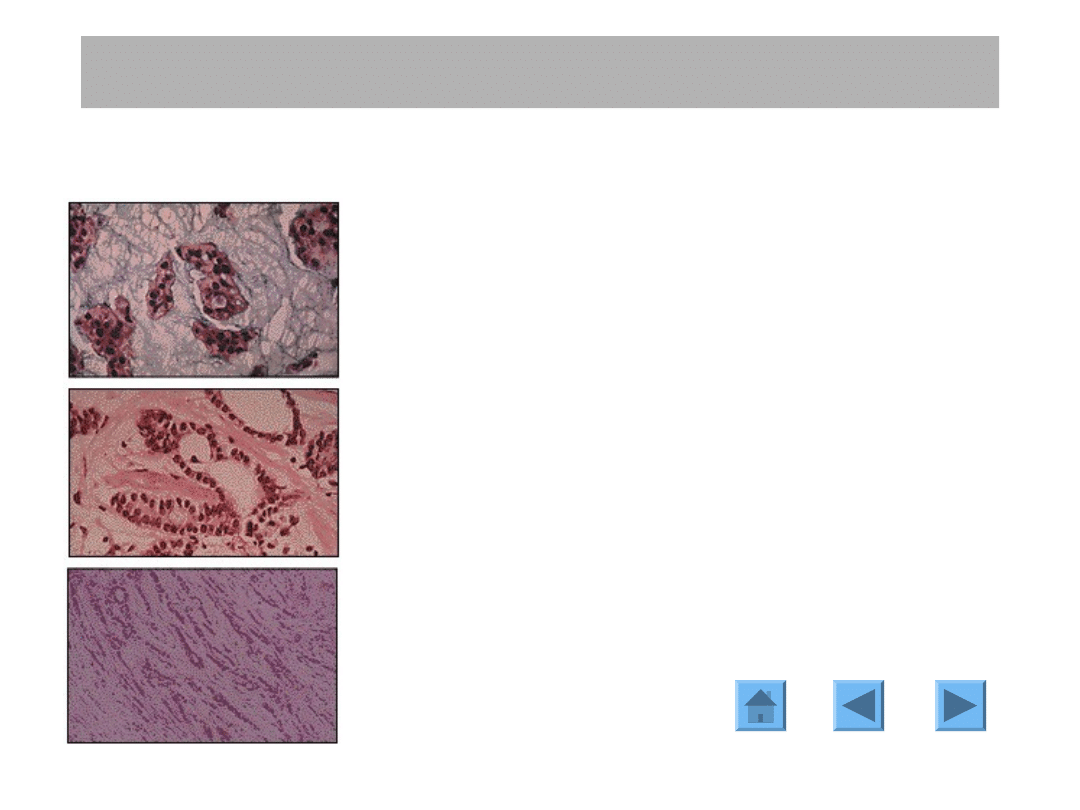
CZYNNIKI PROGNOSTYCZNE
Typ
histologiczny
jest
dobrym
czynnikiem
rokowniczym przeżycia odległego. Niektóre typy
raka naciekającego (np. ca mucinosum,
ca medullare, ca tubulare, ca papillare, ca
lobulare) wiążą się z lepszym rokowaniem niż rak
przewodowy
naciekający
„bez
cech
specyficznych”.
Histologiczny stopień złośliwości jest również
ważnym czynnikiem rokowniczym.
Mniej korzystne
rokowanie
związane
jest
ze
słabym
zróżnicowaniem komórek (
stopień III
wg Blooma
Richardsona) a
lepsze
w guzach o zróżnicowanych
komórkach (
stopień I
).
Histologiczny typ i stopień złośliwości
EPIDEMIOLOGIA I PATOFIZJOLOGIA
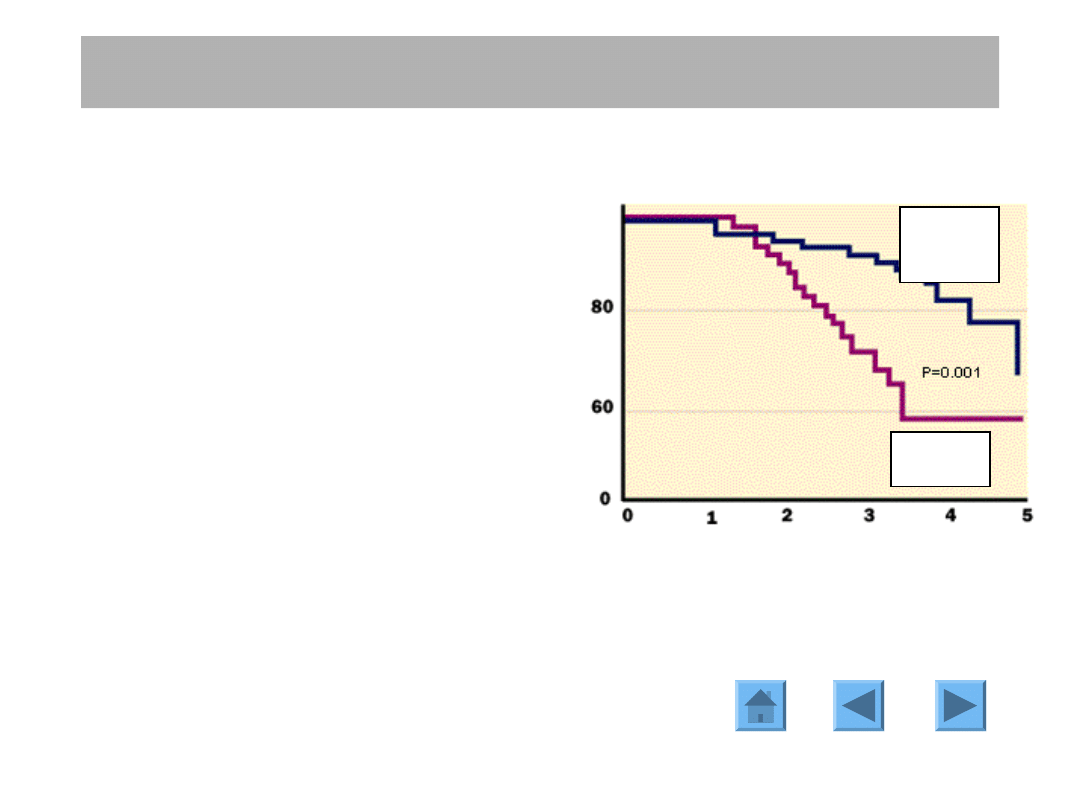
CZYNNIKI PROGNOSTYCZNE
Obecność
receptora estrogenowego
(RE)
jest
ważnym
czynnikiem
rokowniczym i pozwala przewidywać
odpowiedź na leczenie hormonalne.
Pacjentki z RE dodatnim mają dłuższy
okres przeżycia bezobjawowego niż z
RE ujemnym: różnica w przeżyciach
wynosi ok. 10% po 5 latach.
Obecność
receptora dla nabłonkowego
czynnika wzrostu ( z ang. EGFR)
w
błonie komórek raka piersi odwrotnie
koreluje z obecnością RE i jest związana
ze
skróceniem
czasu
przeżycia
bezobjawowego
oraz
zmniejsza
całkowite
przeżycia.
Pacjentki
z
dodatnimi EGFR słabo odpowiadają na
leczenie hormonalne.
Receptory hormonalne i dla czynnika wzrostu
RE
dodatni
e
RE
ujemne
O
d
se
te
k
p
rz
e
ży
ć
(%
)
Lata po
rozpoznaniu
Receptory dla EGF są obecnie badane pod kątem
możliwości leczniczych (przeciwciała monoklonalne).
EPIDEMIOLOGIA I PATOFIZJOLOGIA
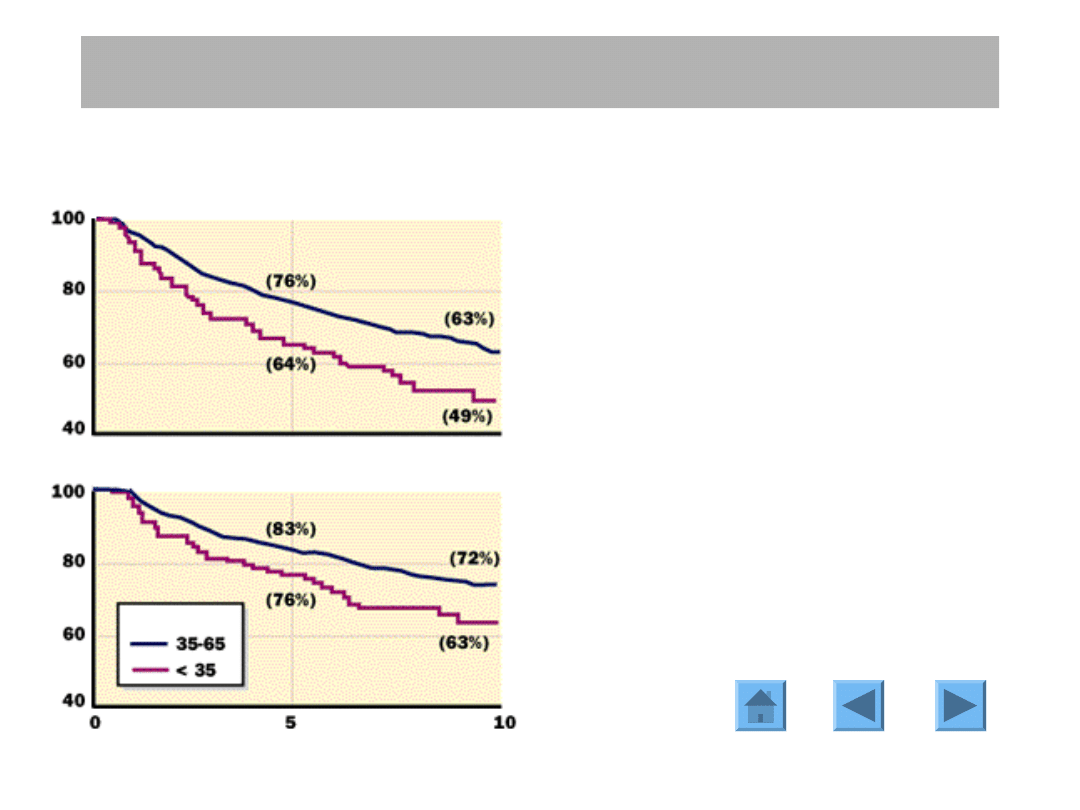
CZYNNIKI PROGNOSTYCZNE
Wiek
Lata po
rozpoznaniu
Wznowa
miejscowa
Rozsiew
Wiek
(lata)
Pacjentki młode (poniżej 35 r.ż.) mają
raczej gorsze rokowanie zarówno jeśli
chodzi o wznowę miejscową jak i
rozsiew choroby niż pacjentki starsze
mające raka w tym samym stopniu
zaawansowania.
Może to sugerować że biologia raka u
pacjentek młodszych jest różna od tej
u starszych. Identyfikacja genów
BRCA1 i BRCA2 w części przypadków
rodzinnego raka piersi może pozwolić
na wyjaśnienie różnic w biologii
nowotworu w zależności od wieku.

Leczenie
Leczenie chirurgiczne
Chemioterapia
Radioterapia
Hormonoterapia
Immunoterapia

LECZENIE
LECZENIE CHIRURGICZNE
Rola leczenia chirurgicznego
Leczenie oszczędzające
Mastektomia prosta
Radykalna mastektomia
Rekonstrukcja piersi
LECZENIE
LECZENIE CHIRURGICZNE
Rola leczenia chirurgicznego
Stadium 0 - Ca ductale in situ: tumorektomia lub leczenie oszczędzające (odchodzi się
od limfadenektomii pachowej w tym przypadku) lub mastektomia prosta
Ca lobulare in situ: leczenie oszczędzające (zazwyczaj bez
limfadenektomii pachowej)
Stadium I - leczenie oszczędzające lub zmodyfikowana radykalna mastektomia
Stadium II - leczenie oszczędzające lub zmodyfikowana radykalna mastektomia
Stadium III - IIIA: zmodyfikowana radykalna mastektomia lub standardowa radykalna
mastektomia lub leczenie oszczędzające po chemioterapii
neoadjuwantowej
IIIB: biopsja diagnostyczna. Jeżeli skuteczna była chemioterapia
neoadjuwantowa to standardowa radykalna mastektomia lub
zmodyfikowana radykalna mastektomia
Stadium VI - biopsja diagnostyczna

LECZENIE
LECZENIE CHIRURGICZNE
Leczenie to polega na wycięciu guza z odpowiednio dużym marginesem
zdrowych tkanek (zabieg nazywany tumorektomią, lumpektomią) i układu
chłonnego pachy (limfadenektomia pachowa).
Stanowi ono alternatywę dla amputacji piersi (względy psychologiczne i
kosmetyczne)
Leczenie operacyjne
musi być uzupełnione pooperacyjnym
napromienianiem
.
Efekty takiego leczenia (przy zachowaniu przeciwwskazań) nie różnią się od
efektów zmodyfikowanej radykalnej mastektomii.
Leczenie oszczędzające (BCT-breast conserving
therapy)

LECZENIE
LECZENIE CHIRURGICZNE
Wskazaniami do BCT są:
- Rak przewodowy in situ
- Rak przewodowy naciekający nie przekraczający 3
cm średnicy, bez badalnych węzłów chłonnych lub
pojedynczy podejrzany węzeł
Leczenie oszczędzające: wskazania
LECZENIE
LECZENIE CHIRURGICZNE
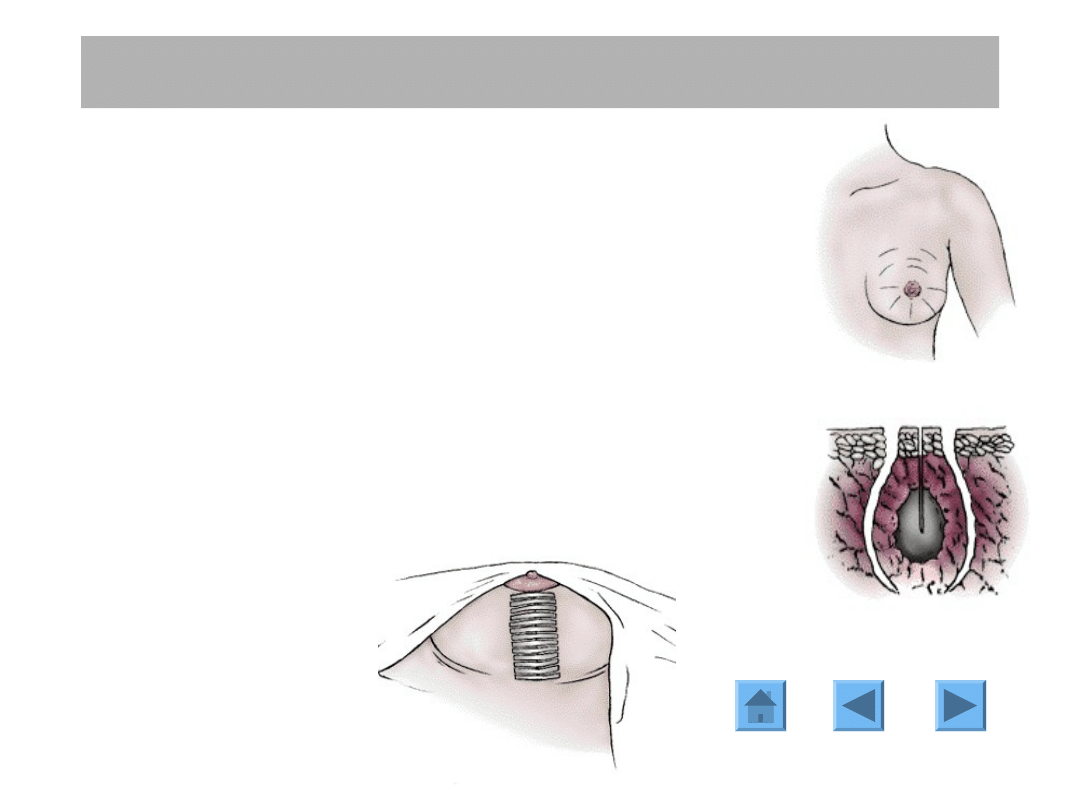
1. Słabo ograniczone guzy
2. Wzrost wieloogniskowy
3. Ciąża
4. Przebyte napromienianie piersi
5. Guzy położone centralnie z zajęciem
brodawki
6. Przewidywany efekt kosmetyczny
będzie niesatysfakcjonujący
7. Brak współpracy ze strony pacjentki
8. Choroby płuc, serca, kolagenozy,
choroby psychiczne.
Leczenie oszczędzające: przeciwwskazania
Guz wieloogniskowy
Guz położony centralnie z
naciekiem brodawki
LECZENIE
LECZENIE CHIRURGICZNE
U pacjentek z dużymi guzami można
zastosować
przedoperacyjną
chemioterapię dla zmniejszenia masy
guza.
Badanie Mediolańskie (The Milan Study)
wykazało że zastosowanie stosunkowo
krótkiej chemioterapii neoadjuwantowej
powoduje
zmniejszenie
stopnia
zaawansowania
(„down
-
staging”)
dużego, ale operacyjnego, pierwotnego
guza piersi do średnicy mniejszej niż 3 cm
u większości pacjentek.
Daje to możliwość zastosowania leczenia
oszczędzającego.
Leczenie oszczędzające po chemioterapii
neoadjuwantowej
LECZENIE
LECZENIE CHIRURGICZNE
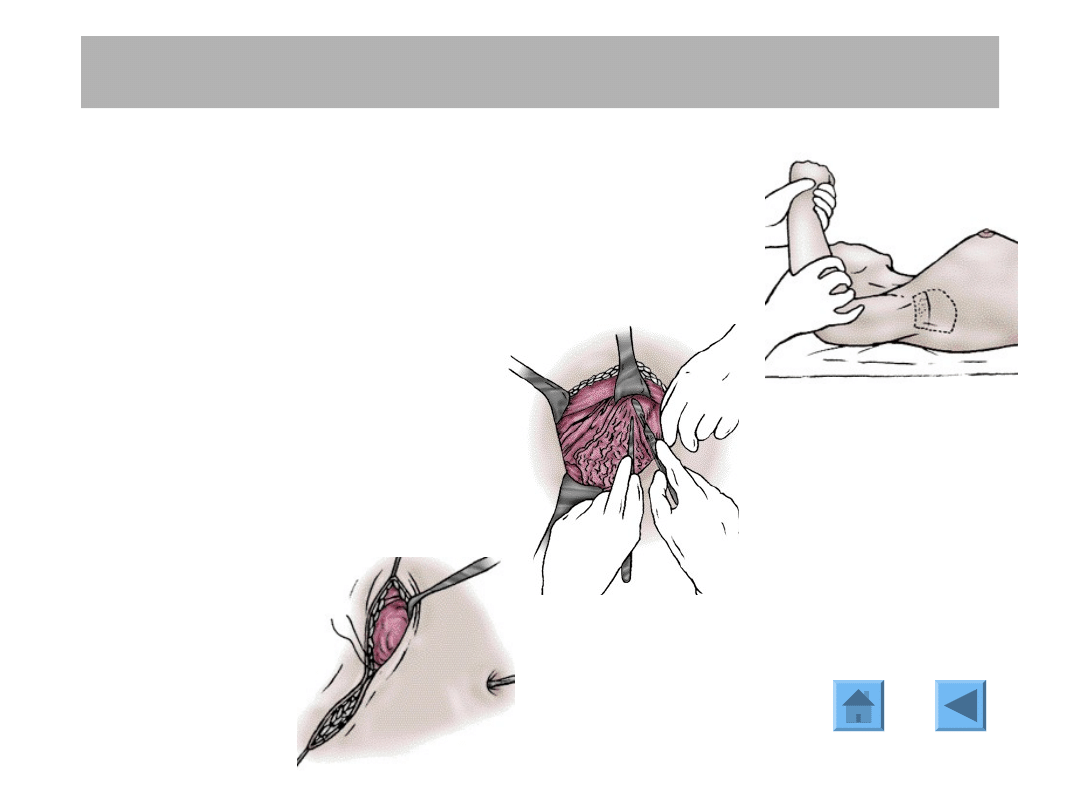
Cięcie skórne wykonuje się bezpośrednio nad guzem
wzdłuż linii napięcia skóry lub wokół areoli.
Cięcie powinno obejmować bliznę po uprzedniej biopsji.
Leczenie oszczędzające: technika
Wycięcie guza do powięzi z marginesem zdrowych tkanek i
oznaczenie brzegów w sposób zrozumiały dla patologa.
Niektórzy chirurdzy pozostawiają w brzegach loży tzw. „klipsy”
- metalowe znaczniki dla ułatwienia radioterapii.
Zamknięcie rany
1
2
3
LECZENIE
LECZENIE CHIRURGICZNE
Limfadenektomia pachowa. W przypadku guzów
położonych w górno-bocznym kwadrancie możliwe
jest wykonanie operacji z jednego cięcia i wycięcie
wraz z guzem.
Leczenie oszczędzające: technika
Wycięcie zawartości dołu pachowego.
Zamknięcie
rany.
1
2
3

LECZENIE
LECZENIE CHIRURGICZNE
Mastektomia prosta: wskazania
Mastektomia prosta (mastectomia simplex) to zabieg polegający na
wycięciu całego gruczołu piersiowego.
Wskazaniami do niego są:
- Mięsaki piersi
- Rak przewodowy in situ (o niekorzystnych cechach
rokowniczych - Van Nuys Prognostic Index równy 8-9)
- Profilaktyka raka piersi u kobiet z grupy wysokiego
ryzyka (np. w raku zrazikowym in situ około 15-20%
pacjentek rozwinie raka naciekającego w tej samej
piersi a dalsze 10-15% w drugiej piersi)
LECZENIE
LECZENIE CHIRURGICZNE
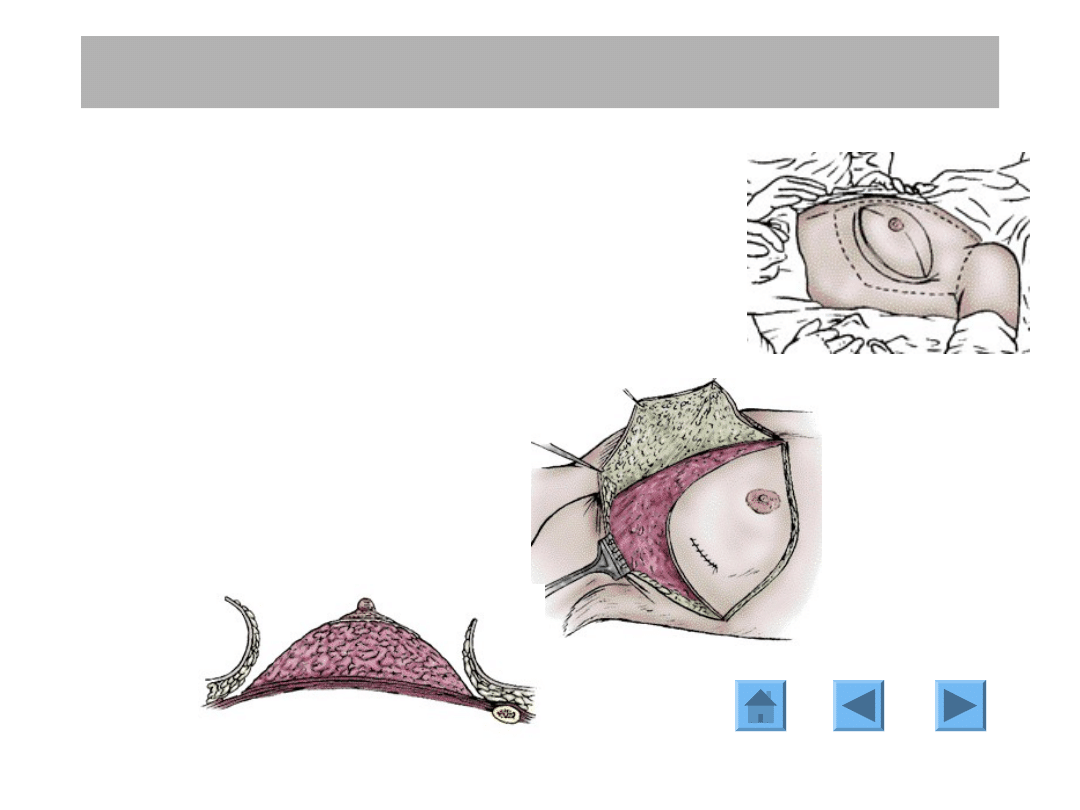
Mastektomia prosta: technika
Cięcie okalające i bbrodawkę i areolę oraz bliznę po
biopsji lub tumorektomii.
Odpreparowanie płatów skórnych.
1
2
LECZENIE
LECZENIE CHIRURGICZNE
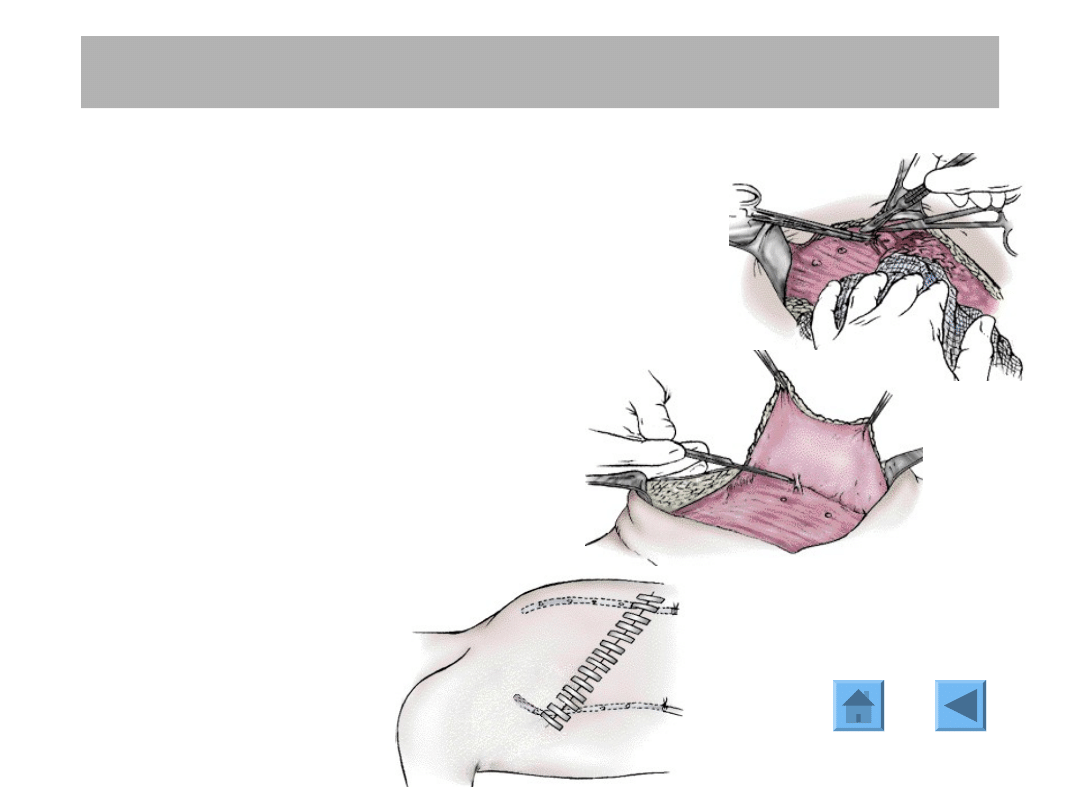
Mastektomia prosta: technika
Odjęcie gruczołu z powięzią mięśnia
piersiowego większego.
Drenaż i zamknięcie rany
3
4
LECZENIE
LECZENIE CHIRURGICZNE
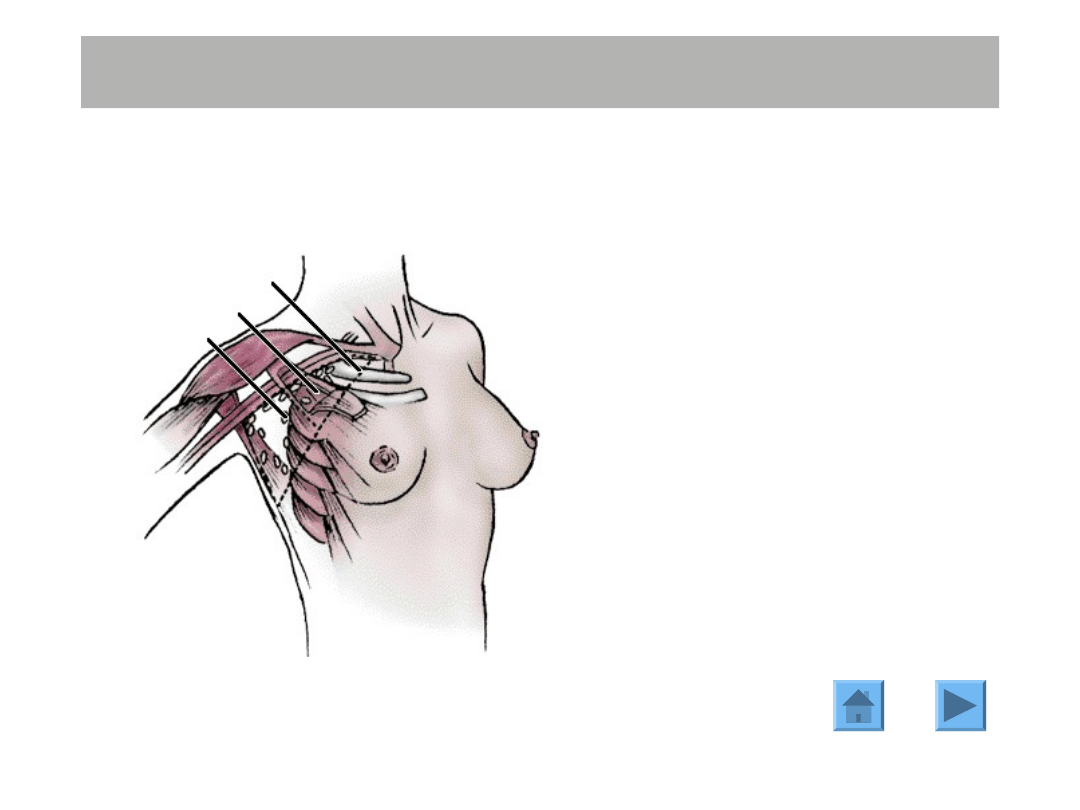
Operacja
ta
polega
na
usunięciu
gruczołu
piersiowego wraz z układem
chłonnym pachy.
Koncepcja
tego
zabiegu
wywodzi się z teorii Halsteda
mówiącej o tym że rak szerzy
się najpierw do okolicznych
węzłów chłonnych a dopiero
potem do innych narządów
Zmodyfikowana radykalna mastektomia
(operacja Patey’a)
Grupy węzłów chłonnych
pachowych
Poziom III
Poziom II
Poziom I
LECZENIE
LECZENIE CHIRURGICZNE
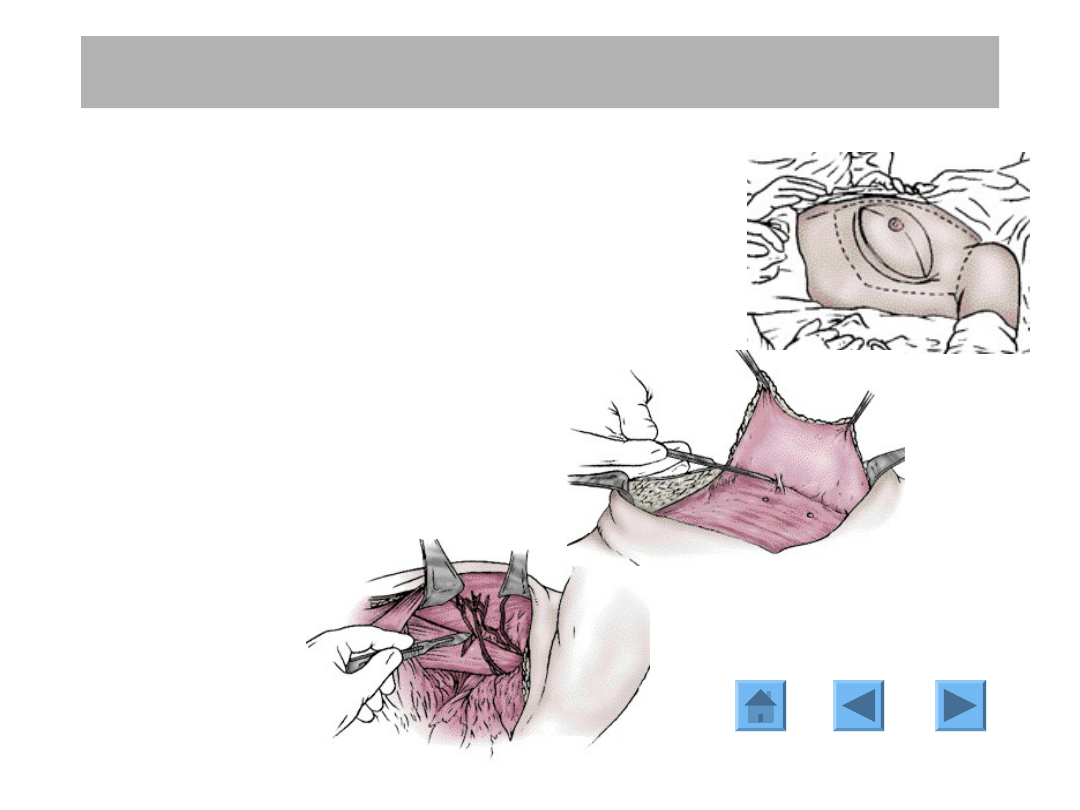
Operacja Patey’a: technika
Cięcie okalające brodawkę i areolę oraz bliznę po
biopsji lub tumorektomii.
Odpreparowanie gruczołu.
1
2
3
Dostęp do dołu
pachowego
(klasycznie poprzez
przecięcie mięśnia
piersiowego
mniejszego,
obecnie nie
przecina się go
tylko odsuwa).
LECZENIE
LECZENIE CHIRURGICZNE
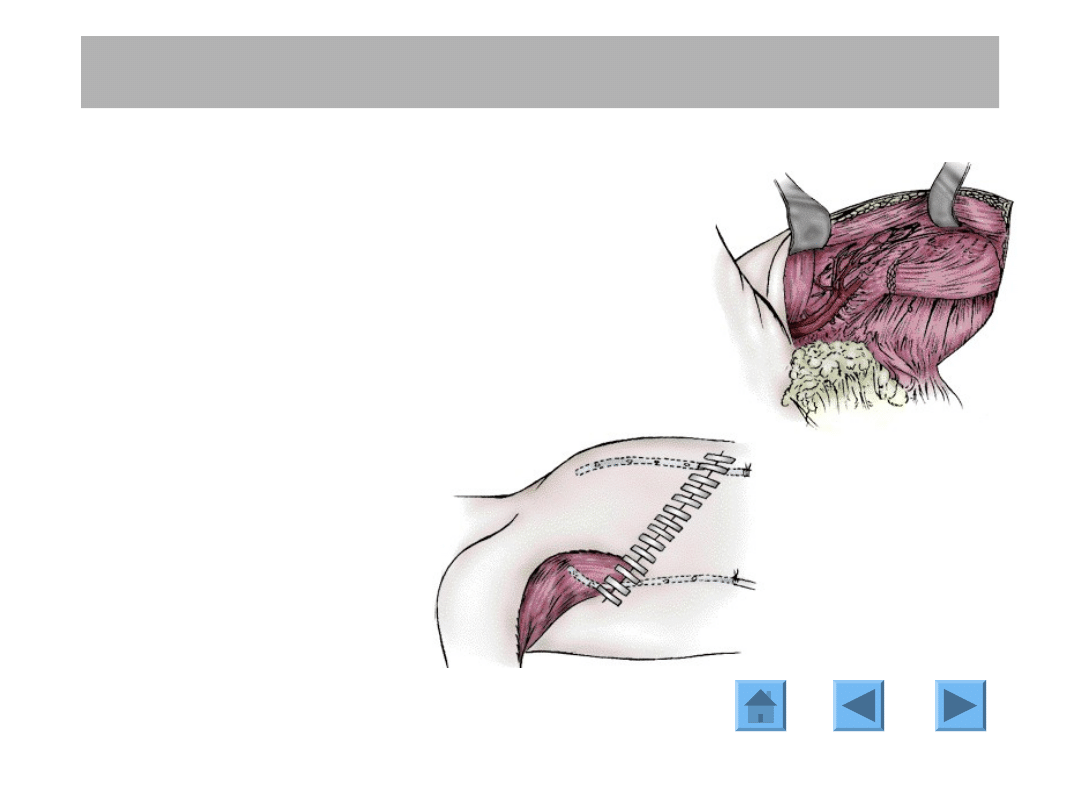
Operacja Patey’a: technika
Wycięcie zawartości dołu pachowego
en bloc z gruczołem piersiowym.
Drenaż i zamknięcie rany.
4
5

LECZENIE
LECZENIE CHIRURGICZNE
Operacja Halsteda (standardowa radykalna
mastektomia)
Operacja sposobem Halsteda polega na wycięciu w jednym bloku
gruczołu piersiowego,
mięśni piersiowych
i układu chłonnego pachy.
Następstwem jej jest dość znaczne upośledzenie ruchów kończyny
górnej oraz deformacja klatki piersiowej.
Z tego powodu, a także ze względu na coraz liczniejsze doniesienia o
braku przewagi w wynikach leczenia tym sposobem w porównaniu do
operacji Patey`a coraz bardziej zawężają się wskazania do jej
wykonywania (obecnie są to naciekanie przez guz mięśnia
piersiowego, duży guz po chemioterapii indukcyjnej).
LECZENIE
LECZENIE CHIRURGICZNE
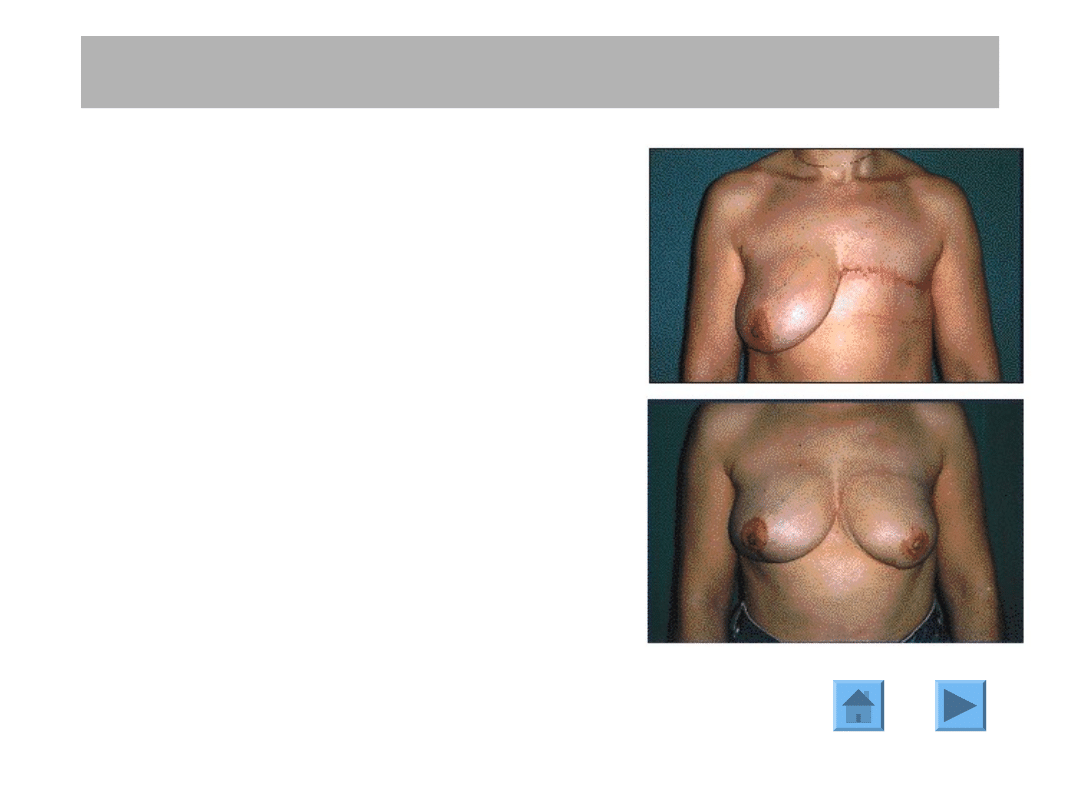
Rekonstrukcja piersi.
Dla wielu kobiet groźba utraty kobiecości
jest
bardziej
psychologicznie
traumatyzującą niż strach przed śmiercią z
powodu raka piersi. Jedno z badań
wykazało że jedna na cztery kobiety po
mastektomii ma myśli samobójcze.
W
czasie
ostatnich
dwóch
dekad
rekonstrukcja piersi stała się integralną
częścią leczenia raka piersi.
Dokonane w ostatnich latach postępy w
zakresie
ekspanderów
tkankowych,
materiałów stosowanych do wyrobu protez,
postępy mikrochirurgii naczyniowej oraz
nowe miejsca pobierania przeszczepów
autologicznych znacznie polepszyły wyniki
operacji odtwórczych.
LECZENIE
LECZENIE CHIRURGICZNE
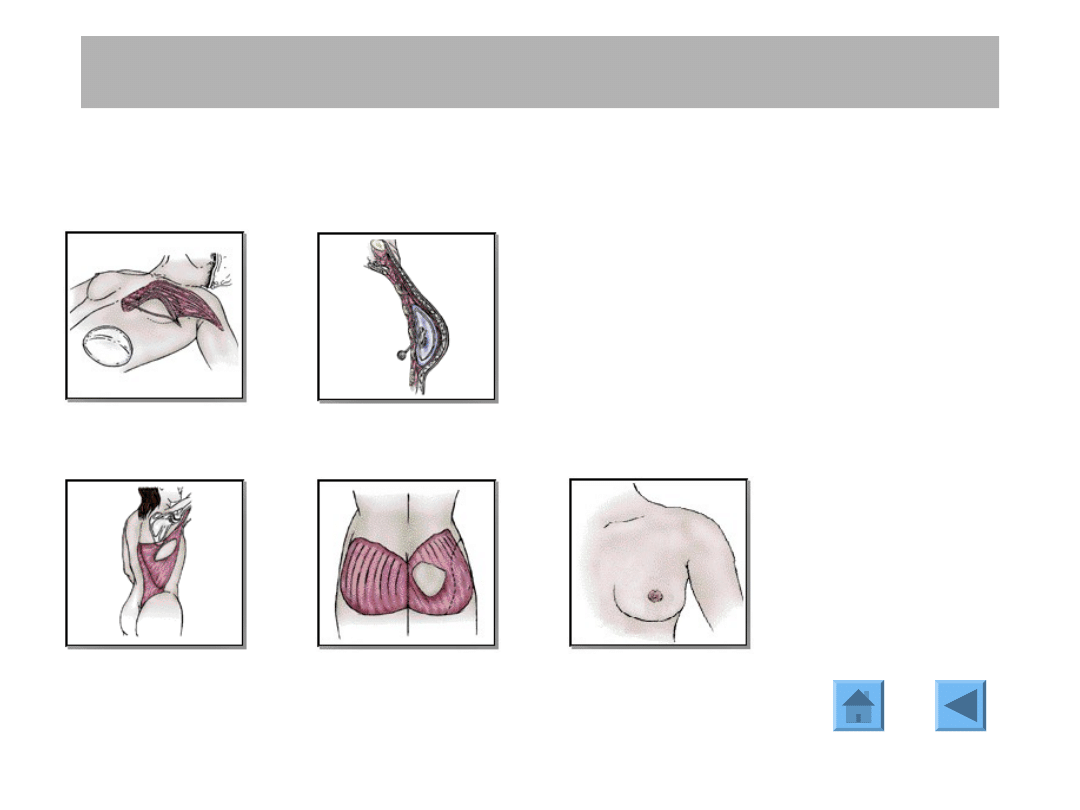
Rekonstrukcja piersi.
Rekonstrukcja piersi może być
- wczesna
(jednoczasowo z mastektomią)
preferowana obecnie powszechnie z
powodu korzyści psychologicznych,
braku wpływu na biologię raka i na
leczenie uzupełniające, braku
konieczności przeprowadzania drugiej
operacji a także ze względów
ekonomicznych
- odroczona
LECZENIE
LECZENIE CHIRURGICZNE
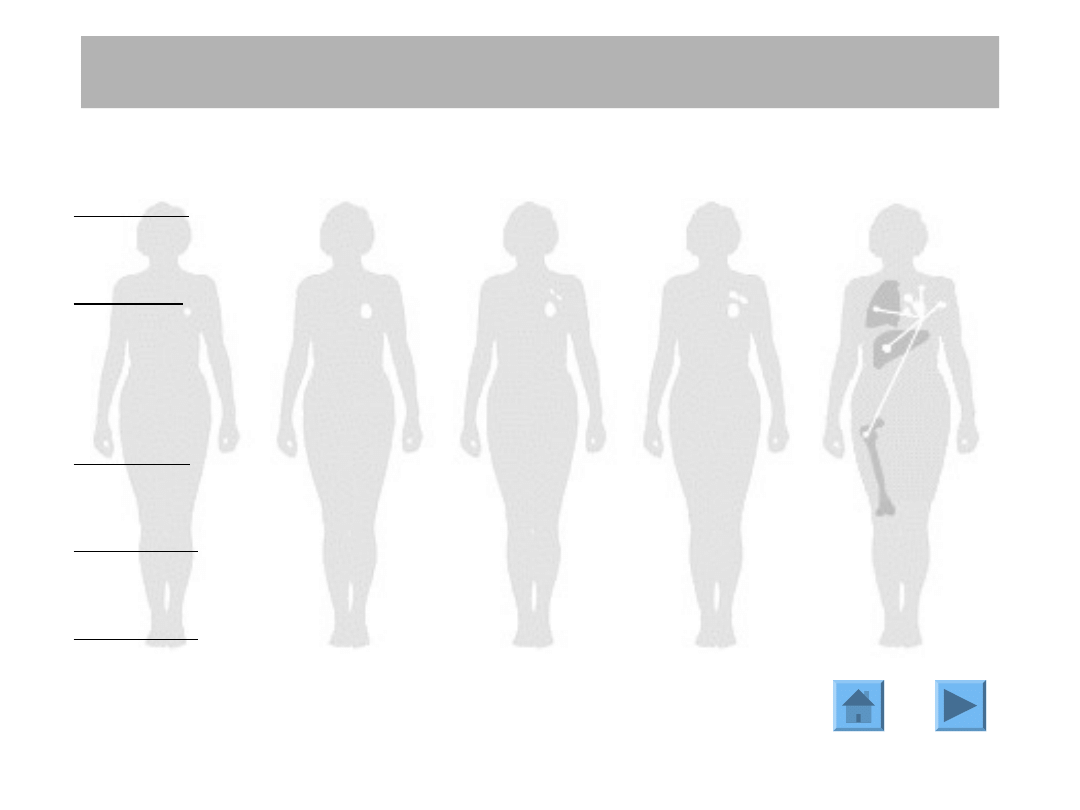
Techniki rekonstrukcji piersi.
Istnieje kilka technik rekonstrukcji
piersi.
Każda z nich ma swoje wady i zalety
i ma zastosowanie u różnych
pacjentek.
Proteza
Ekspander
Płat
uszypułowany
Wolny płat
autologiczny
Rekonstrukcja
brodawki
LECZENIE
CHEMIOTERAPIA
Rola chemioterapii w raku piersi
Stadium 0 - chemioterapia nie jest wskazana
Stadium I - leczenie chemiczne jest wskazane w razie istnienia niekorzystnych
czynników rokowniczych (najważniejszy: zajęcie węzłów chłonnych pachowych);
sądzi się że u kobiet w wieku przedmenopauzalnym, z rakiem o III stopniu
złośliwości i bez zajęcia węzłów też należy podać chemioterapię
Stadium II - chemioterapia adjuwantowa lub neoadjuwantowa
Stadium III - chemioterapia adjuwantowa lub neoadjuwantowa
Stadium VI - chemioterapia paliatywna (u ok. 10-20% może wystąpić całkowita
remisja)
LECZENIE
CHEMIOTERAPIA
Powszechnie akceptowana jest dzisiaj teoria że mikroprzerzuty
narządowe mogą powstawać jeszcze przed klinicznym
ujawnieniem się guza. Są one niewykrywalne żadnymi
metodami i oczywiście leczenie lokoregionalne nie może ich
zniszczyć.
Właśnie w celu wyleczenia
mikroprzerzutów
stosuje się
leczenie systemowe.
Generalnie mikroprzerzuty odpowiadają na leczenie w ten sam
sposób jak przerzuty wykrywalne. Odpowiedzi w przypadku
jawnych przerzutów są zazwyczaj częściowe lub niepełne.
Stopień odpowiedzi na leczenie zależy od
masy guza
,
nabytej
lub
wewnątrzpochodnej oporności na leki
,
kinetyki wzrostu
.
W mikroprzerzutach prawdopodobnie więcej komórek dzieli
się i przez to są bardziej wrażliwe na efekt cytotoksyczny
leków. Z powodu niestabilności genetycznej w komórkach
guza wciąż zachodzą mutacje które mogą powodować
oporność na leczenie i stąd przerzuty małe (lub
mikroprzerzuty) są bardziej wrażliwe niż duże.
Chemioterapia adjuwantowa

LECZENIE
CHEMIOTERAPIA
Wskazania do chemioterapii adjuwantowej nie są jasno sprecyzowane.
Wyodrębniono grupy chorych które przypuszczalnie odniosą korzyść z jej
zastosowania:
Pacjentki przed menopauzą z zajętymi węzłami chłonnymi
-leczenie chemiczne nie budzi kontrowersji
Pacjentki po menopauzie z zajętymi węzłami
- w ich przypadku
przy obecnych receptorach estrogenowych podstawowym leczeniem
uzupełniającym jest hormonoterapia, jednak w przypadku niekorzystnych
czynników rokowniczych warto rozważyć również leczenie chemiczne
Pacjentki z niezajętymi węzłami chłonnymi
- tu zastosowanie
jest kontrowersyjne. Ze względu na toksyczność chemioterapii podejście
do każdej pacjentki powinno być zindywidualizowane, należy rozważyć
czynniki prognostyczne.
Chemioterapia adjuwantowa: wskazania

LECZENIE
CHEMIOTERAPIA
W przeciwieństwie do konwencjonalnej chemioterapii, chemioterapię
neoadjuwantową podaje się
przed
leczeniem operacyjnym. Jest to metoda
stosunkowo nowa i jej wartość wymaga jeszcze potwierdzenia, jednak
dotychczasowe efekty są obiecujące.
Leczenie adjuwantowe znacznie polepsza wyniki leczenia w stadiach
wczesnych nowotworu. Kluczowym problemem jest jednak to że leczenie
mikroprzerzutów prowadzone jest „na ślepo” bez możliwości monitorowania
efektów. W terapii neoadjuwantowej „markerem” odpowiedzi nowotworu na
leczenie jest guz pierwotny. W zależności od jego zachowania można
zwiększać dawki leków lub stosować inne, skuteczniejsze schematy leczenia.
Chemioterapia neoadjuwantowa

LECZENIE
CHEMIOTERAPIA
Zalety:
- możliwość dobrania optymalnego schematu leczenia
- zmiejszenie ryzyka rozwinięcia lekooporności (zgodnie z hipotezą Goldie -
Coldmana prawdopodobieństwo powstania klonów opornych zwiększa się wraz z
masą guza z powodu coraz większej liczby dzielących się i ulegających
mutacjom komórek)
- zmniejszenie niekorzystnego wpływu operacji na wzreost nowotworu (badania
doświadczalne wykazały że zabieg operacyjny i gojenie rany powodują wzrost
poziomu czynników wzrostu, które działając na mikroprzerzuty mogą promować
ich wzrost. Powstała hipoteza że leczenie ich przed operacją może wyeliminować
ten wpływ)
Wady:
- niemożność określenia po operacji najważniejszych czynników prognostycznych
(stanu węzłów chłonnych, złośliwości histologicznej i dokładnej wielkości guza)
Chemioterapia neoadjuwantowa
Leki alkilujące
Cyklofosfamid
Chlorambucil
Mitomycyna C
Antracykliny
Doxorubicyna
Epirubicyna
Mitoksantron
Antymetabolity
5-Fluorouracyl
Metotreksat
Leki antytubulinowe
Docetaksel
Paklitaksel
Winorelbina
Winkrystyna
Winblastyna
Windesyna
LECZENIE
CHEMIOTERAPIA
Leki stosowane w leczeniu raka
piersi
Najczęstsze efekty uboczne:
- nudności, wymioty
- zapalenia i owrzodzenia śluzówek
przewodu pokarmowego
- mielosupresja i wynikające stąd
neutropenia, anemia, małopłytkowość
- wyłysienie
- infekcje
- utrata masy ciała
- neuropatie (pochodne Vinca rosea)
- kardiotoksyczność (antracykliny)
- krwotoczne zapalenie pęcherza
moczowego (Cyklofosfamid)

LECZENIE
CHEMIOTERAPIA
Leczenie I rzutu
CMF (Cyklofosfamid, Metotreksat, 5-Fluorouracyl)
FAC (5-Fluorouracyl, Adriamycyna (Doxorubicyna), Cyklofosfamid)
FEC (5-Fluorouracyl, Epirubicyna, Cyklofosfamid)
Leczenie II rzutu
Taksany (Docetaksel, Paklitaksel)
Navelbina (Winorelbina)
Najczęściej stosowane schematy:
LECZENIE
RADIOTERAPIA
Rola radioterapii w raku piersi
Stadium 0 - inegralna część leczenia oszczędzającego
Stadium I - część leczenia oszczędzającego lub jako leczenie uzupełniające po
radykalnej mastektomii
Stadium II - część leczenia oszczędzającego lub jako leczenie uzupełniające
po radykalnej mastektomii
Stadium III - leczenie uzupełniające po radykalnej mastektomii
Stadium VI - radioterapia paliatywna (najczęściej napromienia się przerzuty
do kości i centralnego układu nerwowego)

LECZENIE
RADIOTERAPIA
-
CDIS
(przy VNPI 5-7 pkt wycięcie guza z napromienianiem)
-
Leczenie oszczędzające
-
Obecność przerzutów w więcej niż 3 węzłach
chłonnych pachowych lub wielkość guza wynosząca
ponad 5 cm lub G3 według Blooma Richardsona
-
Nieradykalność zabiegu
-
Nawrót lokoregionalny
-
Uzupełniająco po chemioterapii neoadjuwantowej i
operacji guza pierwotnie nieoperacyjnego
Wskazania do napromieniania.
Cel
radioterapii:
Zmniejszenie częstości wystąpienia wznowy
miejscowej oraz przedłużenie przeżyć
odległych.
LECZENIE
RADIOTERAPIA
Leczenie to w raku piersi polega na
napromienieniu z kilku pól całego
gruczołu (w przypadku leczenia
oszczędzającego) lub ściany klatki
piersiowej i blizny (w przypadku operacji
radykalnych) oraz pól zawierających
okoliczne węzły chłonne.
Narządami krytycznymi (najbardziej
narażonymi na wystąpienie powikłań),
których napromieniania należy uniknąć
napromieniając pierś są płuca i serce.
Jednym z najważniejszych etapów tego
leczenia jest zaplanowanie
napromieniania.
Planowanie napromieniania
Tomografia
komputerowa
Określenie obszaru
naprom.
Ustalenie pól
napromieniania
Symulacja 3D
Stworzenie bloków
Potwierdzenie rozkładu
dawki

LECZENIE
RADIOTERAPIA
- Powikłania miejscowe (owrzodzenia, zapalenie skóry)
- Uszkodzenie splotu ramiennego
- Obrzęk kończyny górnej (częściej bywa powikłaniem po operacji radykalnej)
- Choroba niedokrwienna serca i popromienne zapalenie i zwłóknienie płuca -
powikłania te zostały w znacznej mierze wyeliminowane dzięki zastosowaniu
nowoczesnych technik napromieniania (pola styczne, omijanie płuc i serca)
- Złamania żeber
- Wtórny nowotwór (rak drugiej piersi, mięsak tkanek miękkich lub kości, rak
płuca, białaczka) - powikłanie raczej rzadkie
Efekty uboczne radioterapii
LECZENIE
HORMONOTERAPIA
Rola hormonoterapii w raku piersi
Stadium 0 - nie stosuje się
Stadium I, II, III, IV - wskazana jest u kobiet z dodatnimi receptorami
estrogenowymi
Profilaktyka - u kobiet z grup wysokiego ryzyka (zastosowanie w fazie
badań)

LECZENIE
HORMONOTERAPIA
Leczenie hormonalne polega na długotrwałym (5 lat) podawaniu
antagonistów
receptorów estrogenowych
(Tamoksifen, Raloksifen) lub
blokerów aromatazy
(enzymu biorącego udział w syntezie hormonów płciowych) (Femara,
Arimidex) lub
agonistów LHRH
(w fazie badań, raczej u kobiet przed
menopauzą „kastracja farmakologiczna”) (Goserelina, Buserelina, Leuprolid).
Lekiem z wyboru jest
Tamoksifen.
Wskazania
:
- Rak naciekający piersi
, z odpowiednim statusem receptorowym
(
dodatnie receptory estrogenowe
; dodatkowo obecność receptorów
progesteronowych polepsza odpowiedź na leczenie i rokowanie)

LECZENIE
HORMONOTERAPIA
Efekty uboczne są
rzadkie
.
Najczęstsze to:
- objawy braku estrogenów (podobne do menopauzalnych)
- zaburzenia miesiączkowania, krwawienia z dróg rodnych
- zwiększone ryzyko raka endometrium
- zakrzepowe zapalenie żył głębokich, zator tętnicy płucnej (zwłaszcza u
kobiet po 50 rż)
- upośledzenie czynności wątroby
Efekty uboczne

LECZENIE
IMMUNOTERAPIA
Leczenie immunologiczne nowotworów wciąż jeszcze znajduje się w fazie
badań, jakkolwiek w przypadku czerniaka złośliwego lub raka
jasnokomórkowego nerki badania te są już daleko posunięte.
W raku piersi próby leczenia takiego podejmowane są w chorobie w stadium
rozsiewu.
Rola immunoterapii w raku piersi

LECZENIE
IMMUNOTERAPIA
Zidentyfikowano kilka antygenów które spotyka się często (choć nie zawsze
w komórkach raka piersi). Są to:
- Antygen karcinoembrionalny (CEA)
- Polimorficzna mucyna nabłonkowa (PEM)
- p53
- c-erb B2 (her-2)
- c-myc
Antygeny związane z guzem
(Tumour-Associated Antigens, TAAs)
LECZENIE
IMMUNOTERAPIA
Celem dla przeciwciał mogą
być antygeny zlokalizowane na
powierzchni komórki takie jak
PEM
lub
c-erb B2 (her-2)
.
Wprowadzono już do leczenia
preparat
HERCEPTYNA
będący
monoklonalnymi
przeciwciałami
przeciwko
antygenom c-erb B2.
Immunoterapia z użyciem
przeciwciał
Antygen
Przeciwciał
o
KOMÓRKA
RAKA

SCREENINIG
BADANIA PRZESIEWOWE
1. Waga problemu. Rak piersi u kobiet jest chorobą częstą (24% zgonów z powodu
nowotworów wśród kobiet w UE). Rokowanie jest związane ze stopniem
zaawansowania choroby a więc wczesne wykrycie polepsza wyniki leczenia.
2. Nieskomplikowane metody diagnostyczne.
3. Mała uciążliwość metod diagnostycznych dla pacjentki.
4. Potwierdzona w wielu badaniach międzynarodowych skuteczność
skriningu.
5. Względy ekonomiczne. Tańsze jest prowadzenie badań przesiewowych i leczenie
we wczesnych stadiach niż leczenie raków zaawansowanych.
Sens prowadzenia skriningu.

SCREENINIG
BADANIA PRZESIEWOWE
Samobadanie piersi.
Badanie piersi przez
lekarza.
Mammografia.
Ulrasonografia
Badania genetyczne.
Rodzaje badań przesiewowych.

SCREENINIG
BADANIA PRZESIEWOWE
Stwierdzono, że około 80% pacjentek leczonych z powodu raka piersi zgłosiło
się do lekarzy z powodu stwierdzenia u siebie podejrzanej zmiany w piersi.
Kobiety powinny rozpocząć regularne samobadanie piersi około 20 roku życia.
Badanie to powinno być wykonywane raz w miesiącu. W przypadku kobiet
miesiączkujących najlepiej wykonywać je około tydzień od zakończenia
miesiączki (ze względu na luźniejszą konsystencję gruczołów). Kobiety w wieku
pomenopauzalnym powinny wyznaczyć sobie jeden określony, stały dzień
miesiąca kiedy będą dokonywać samobadania.
Samobadanie piersi.

SCREENINIG
BADANIA PRZESIEWOWE
Jako badanie przesiewowe powinno być wykonywane
co około 3 lata u kobiet przed 40 rż
co około 1 rok u kobiet po 40 rż
Badanie przez lekarza.

SCREENINIG
BADANIA PRZESIEWOWE
Pierwsza mammografia (u kobiet bez podejrzanych zmian palpacyjnych)
powinna być wykonana ok. 40 - 45 roku życia.
Po 50 roku życia zaleca się regularne wykonywanie mammografii w dwóch
projekcjach co około 18 miesięcy.
Mammografia.

SCREENINIG
BADANIA PRZESIEWOWE
Ultrasonografia jest raczej metodą diagnostyczną pozwalającą różnicować
zmiany lite i torbielowate.
Jako badanie przesiewowe, alternatywne dla mammografii, może być
stosowana u kobiet w ciąży lub w trakcie laktacji, u kobiet młodych oraz u
kobiet o bardzo spoistej konsystencji piersi.
Ultrasonografia.

SCREENINIG
BADANIA PRZESIEWOWE
U kobiet z obciążającym wywiadem rodzinnym (rak piersi u krewnej pierwszego
stopnia, zwłaszcza w młodym wieku) powinno się przeprowadzić diagnostykę w
kierunku ewentualnych mutacji genów
BRCA1, BRCA2, Rb-1, p53
.
Testy genetyczne.
Rozpoznanie
Badanie kliniczne
Mammografia
Ultrasonografia
Biopsja aspiracyjna cienkoigłowa
Biopsja
Nowe techniki

ROZPOZNANIE
BADANIE KLINICZNE
Zbierając wywiad u chorej ze zmianą w piersi należy zwrócić szczególną
uwagę na:
- dynamikę zmian w piersiach, związek z cyklem miesiączkowym,
bolesność, obecność i charakter wycieku z brodawki
- obecność czynników ryzyka raka piersi
- wywiad rodzinny
Wywiad.
ROZPOZNANIE
BADANIE KLINICZNE
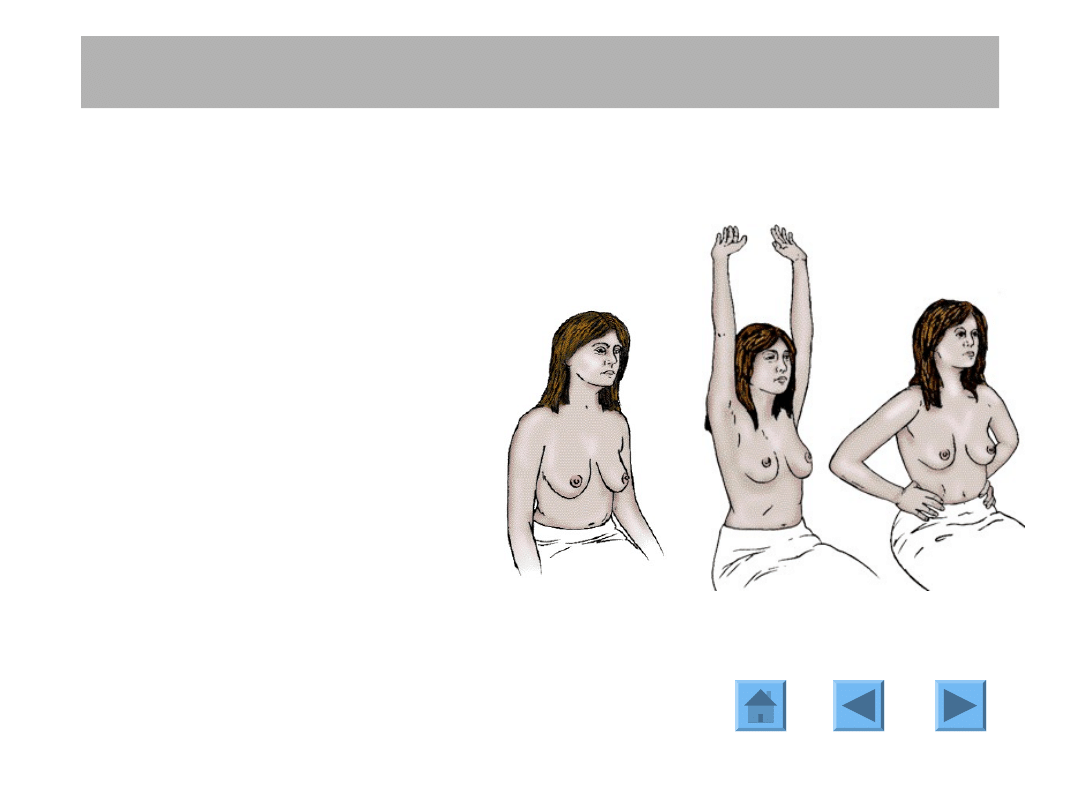
W trakcie oglądania piersi
należy zwrócić uwagę na:
- symetrię piersi
- wygląd skóry piersi
(obecność ewentualnego
zaciągania skóry, objawu
„skórki pomarańczy”, nacieku
zapalnego, owrzodzeń)
- wygląd brodawki i otoczki
Badanie fizykalne - oglądanie.
ROZPOZNANIE
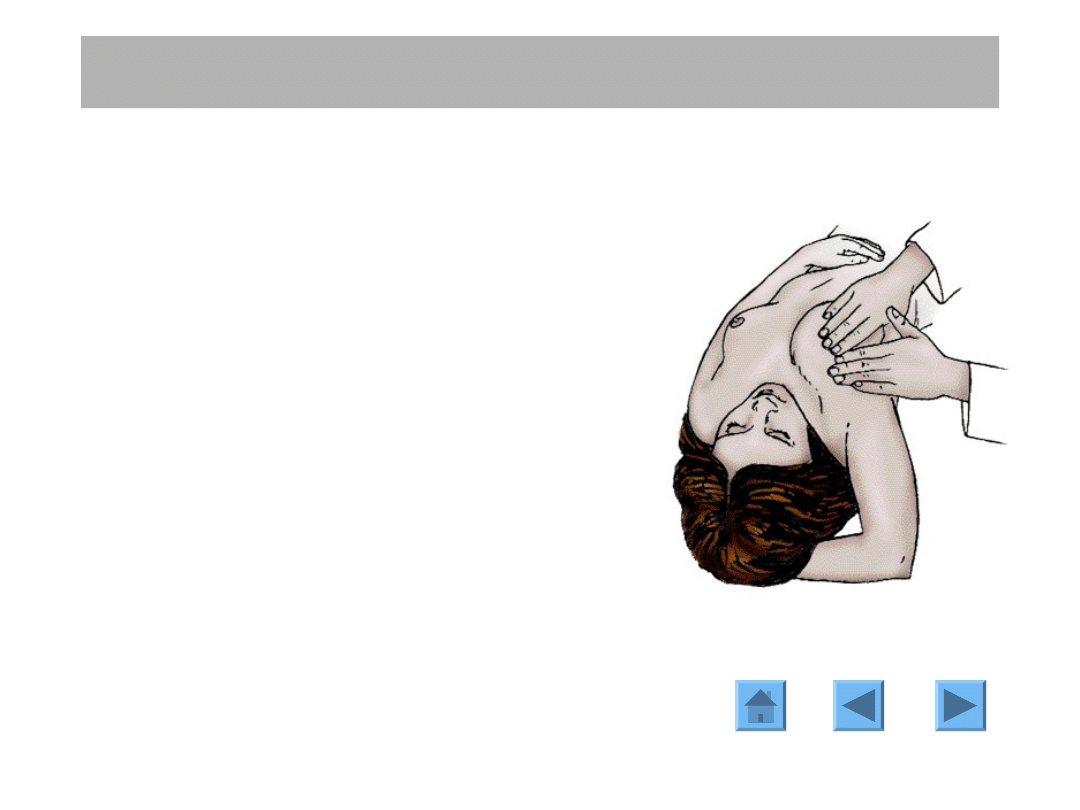
BADANIE KLINICZNE
Badanie fizykalne - palpacja.
W razie stwierdzenia badaniem palpacyjnym
guzka należy ocenić jego:
- położenie
(kwadrant)
- wielkość
(w centymetrach)
- bolesność
- konsystencję
(twardy-miękki)
- stosunek do otaczających tkanek
(dobrze lub nieostro odgraniczony, ruchomość
w stosunku do podłoża, stan skóry nad guzem)
ROZPOZNANIE
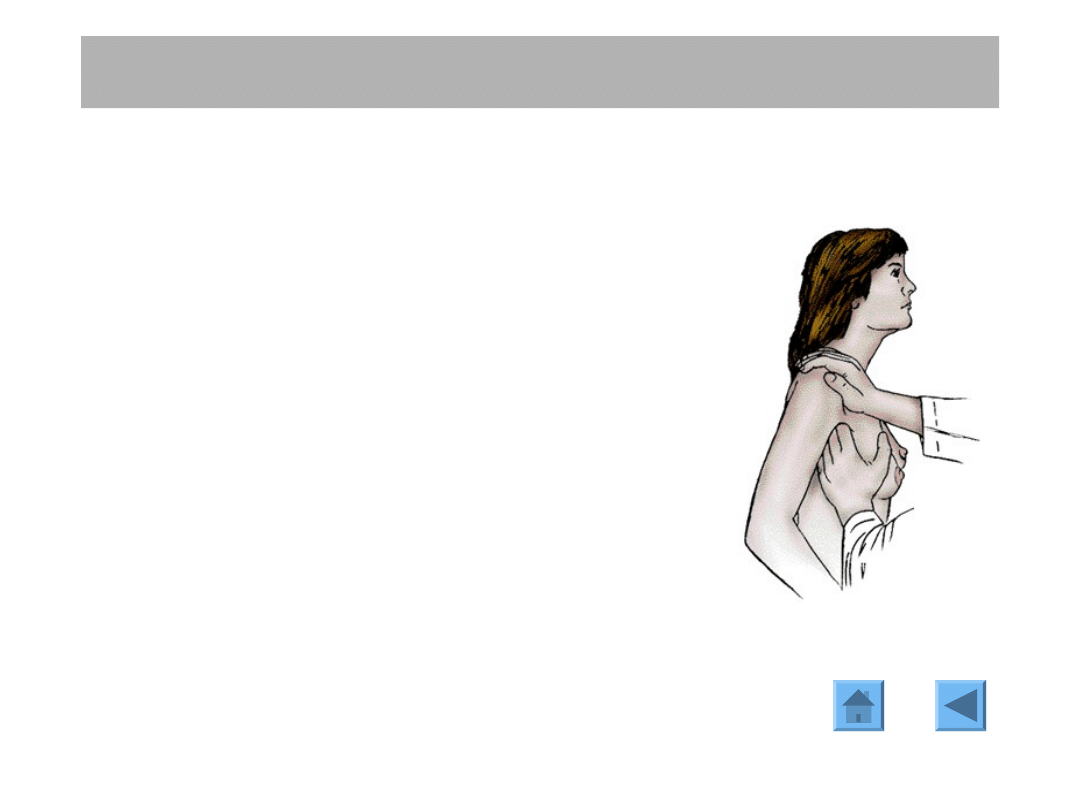
BADANIE KLINICZNE
Nieodzowną częścią badania fizykalnego
piersi jest ocena palpacyjna stanu węzłów
chłonnych
- pachowych
- podobojczykowych
- nadobojczykowych
i ocena ich wielkości, konsystencji,
ruchomości względem podłoża i skóry i
ewentualnego tworzenia pakietów.
Badanie fizykalne - badanie węzłów chłonnych.

ROZPOZNANIE
MAMMOGRAFIA
Oprócz zastosowania mammogafii jako metody skriningowej, badanie to
służy też jako metoda diagnostyki wyczuwalnych zmian palpacyjnych w
piersiach.
Badanie to powinno być wykonane przed biopsją aspiracyjną guzka (w
bliźnie po nakłuciu zmiany mogą powstać zwapnienia) i pozwala
- wzmóc podejrzenie charakteru złośliwego zmiany lub
- wykazać niezłośliwy charakter guzka i uniknąć diagnostyki inwazyjnej
(rzadko).
Jeżeli zmiana w badaniu klinicznym wydaje się podejrzana, ujemny
wynik mammografii nie zwalnia od dalszej diagnostyki!
Rola mammografii

ROZPOZNANIE
MAMMOGRAFIA
Badanie mammograficzne jest
zdjęciem RTG piersi, każdej w dwóch
projekcjach:
- CC (craniocaudal view)
- MLO (mediolateral oblique view)
Wiąże się ono z narażeniem pacjentki
na promieniowanie jonizujące, ale
dawka promieniowania jest mała
(średnio ok. 40 mrad w głębi piersi
dla każdej projekcji).
Technika

ROZPOZNANIE
MAMMOGRAFIA
Lekarz oceniający zdjęcia mammograficzne musi zwrócić uwagę na:
symetrię obu piersi
obecność i wygląd mikrozwapnień
morfologię guza
brzegi guza
położenie i wymiary guza
Ocena badania
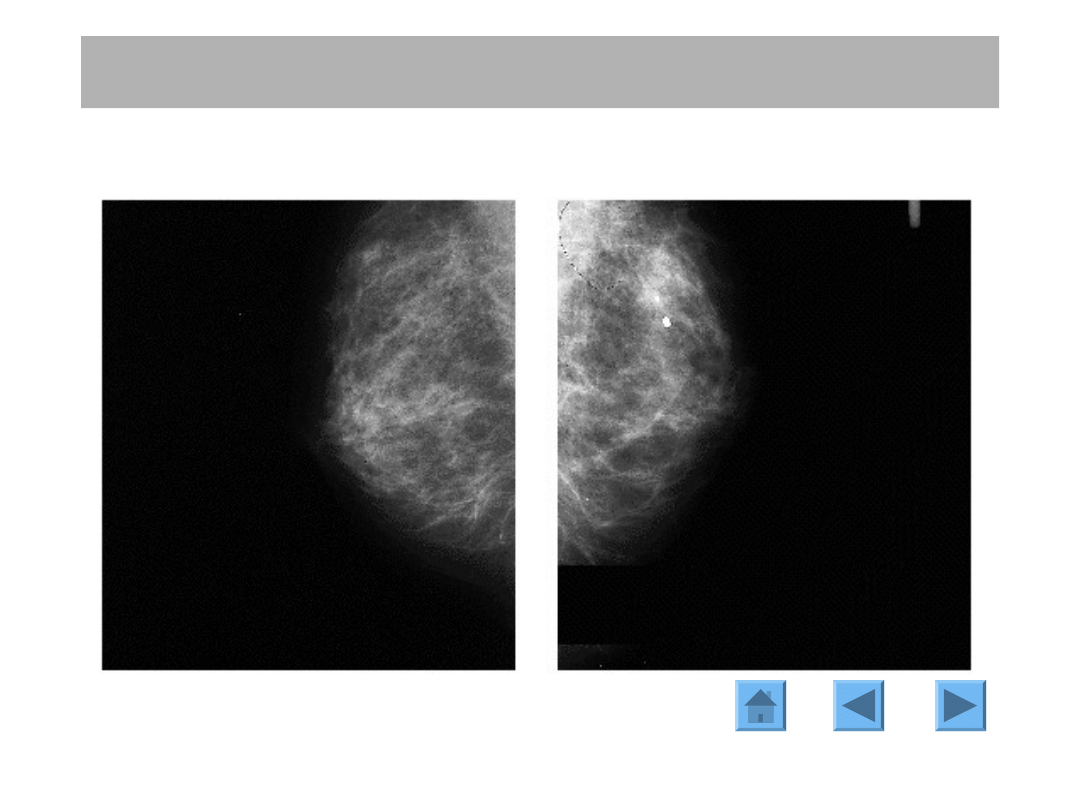
ROZPOZNANIE
MAMMOGRAFIA
Asymetria
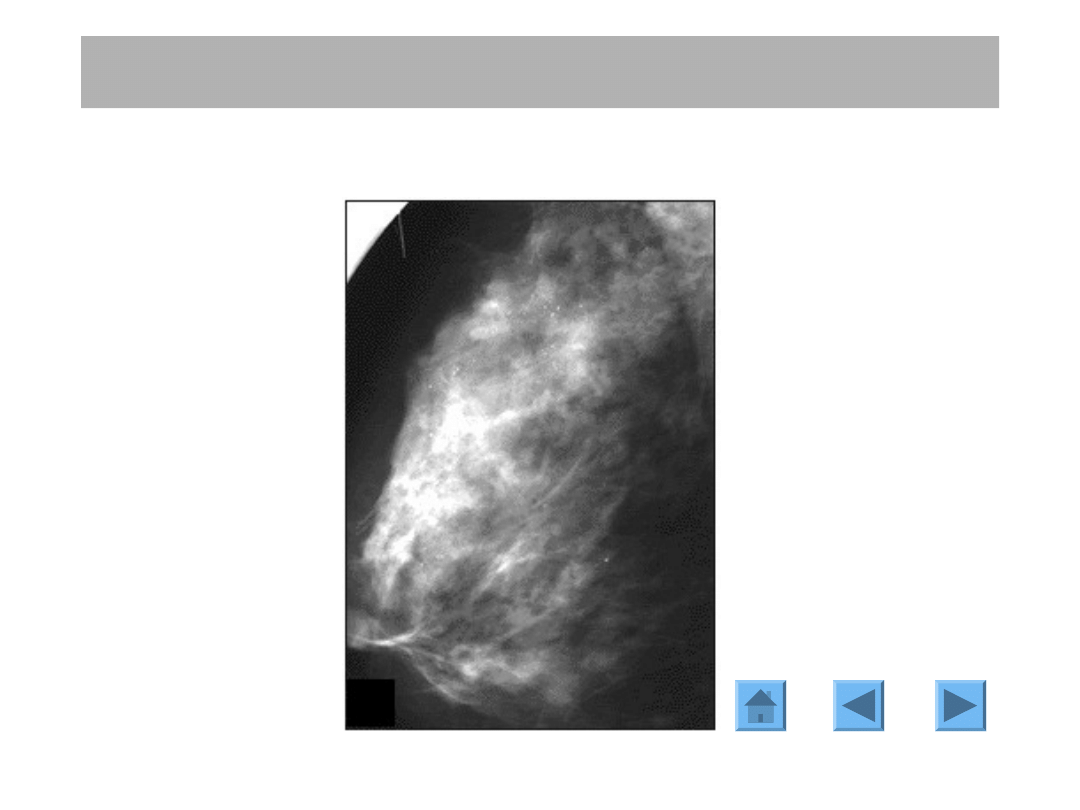
ROZPOZNANIE
MAMMOGRAFIA
Mikrozwapnienia
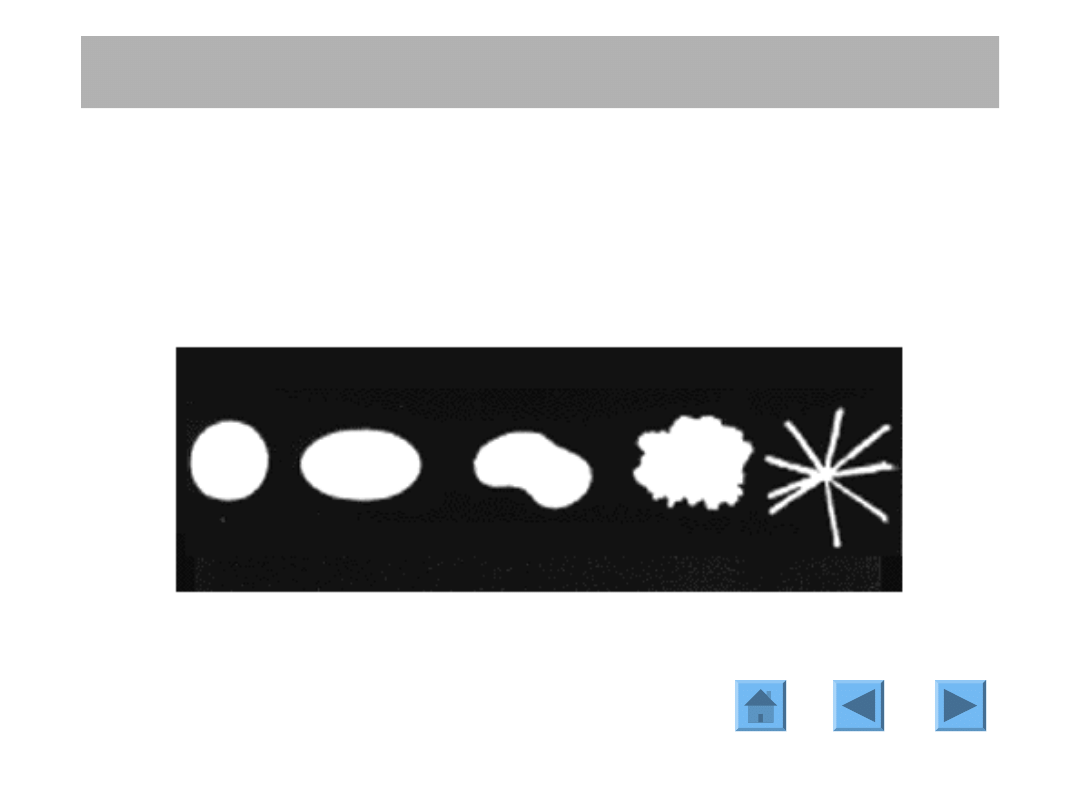
ROZPOZNANIE
MAMMOGRAFIA
Morfologia masy guza
Obszar podejrzany może mieć w mammografii różny wygląd.
Ogólnie, im bardziej jest on nieregularny tym większe jest
prawdopodobieństwo raka.

ROZPOZNANIE
MAMMOGRAFIA
Wygląd brzegów masy
Bardzo ważna jest ocena granic podejrzanego obszaru.
Zmiany łagodne są zazwyczaj dobrze, ostro odgraniczone od otaczającego miąższu.
Większość natomiast raków piersi ma nieostre obrysy, klasycznie z wypustkami.
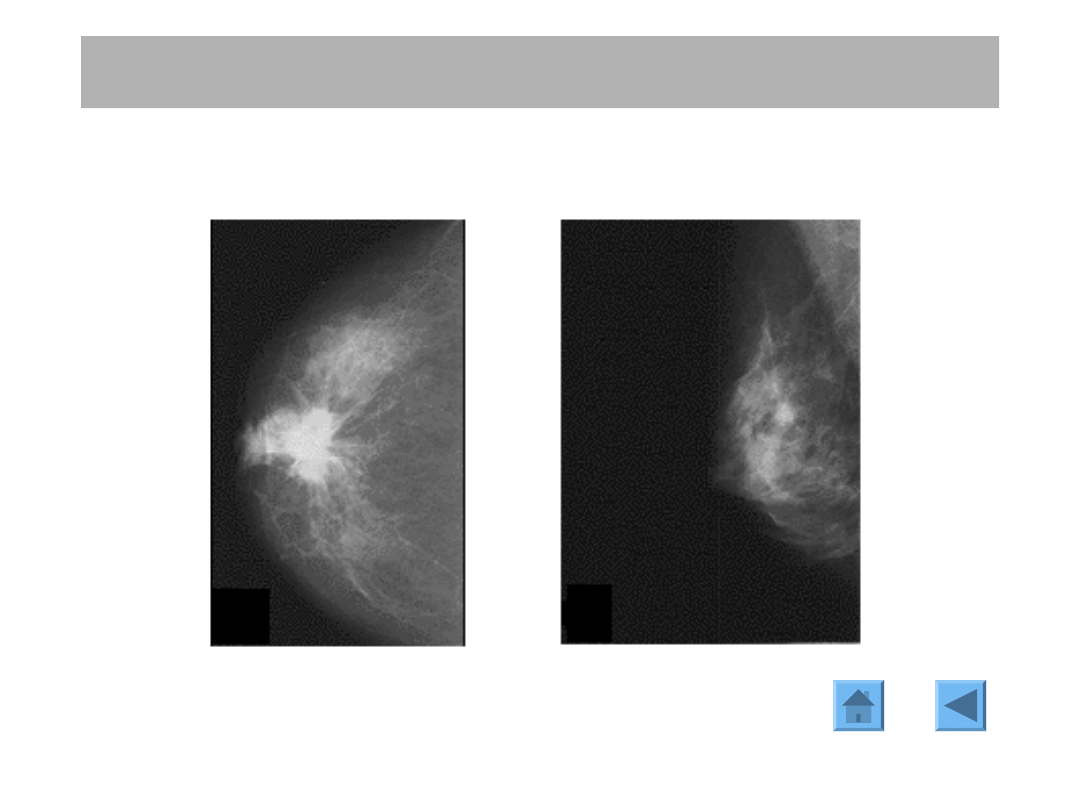
ROZPOZNANIE
MAMMOGRAFIA
Wielkość i położenie masy

ROZPOZNANIE
ULTRASONOGRAFIA
Jest ono badaniem uzupełniającym badanie mammograficzne i w przypadku
stwierdzenia zmian w mammografii powinno być wykonane.
Pozwala przede wszystkim różnicować zmiany lite od zmian torbielowatych,
nie daje odpowiedzi na pytanie czy zmiana jest złośliwa czy łagodna.
Wskazania do wykonania USG:
- wykrycie zmian podejrzanych mammograficznie
- guzek u kobiety poniżej 30 roku życia (w tym wieku mammografia jest
raczej niewskazana)
- okres ciąży i laktacji
- zmiany bolesne w piersiach (mammografia ze względu na konieczność
ściśnięcia piersi może być niewykonalna)
- kobiety o spoistych piersiach (radiologicznie „gęstych”)
Rola badania USG

ROZPOZNANIE
ULTRASONOGRAFIA
Lekarz wykonujący USG piersi powinien ocenić
położenie, rozmiar i granice zmiany
echogeniczność wnętrza zmiany
obecność lub brak cienia akustycznego za zmianą
Ocena USG
ROZPOZNANIE
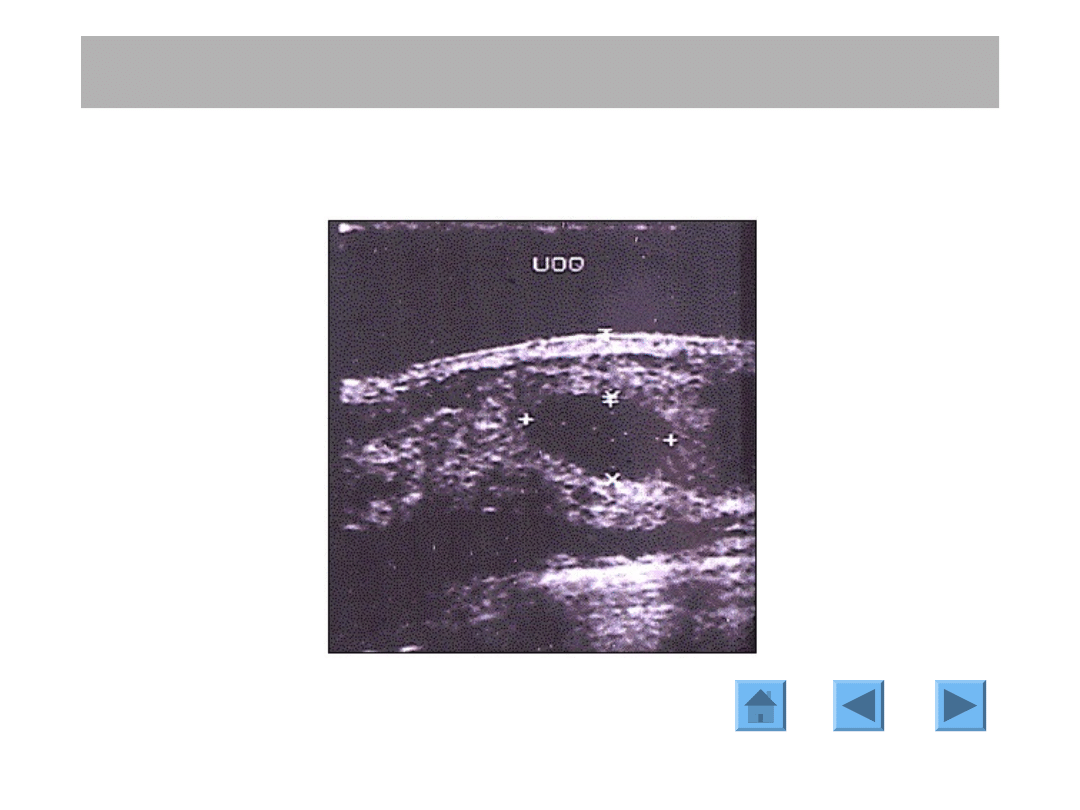
ULTRASONOGRAFIA
Obraz USG torbieli piersi
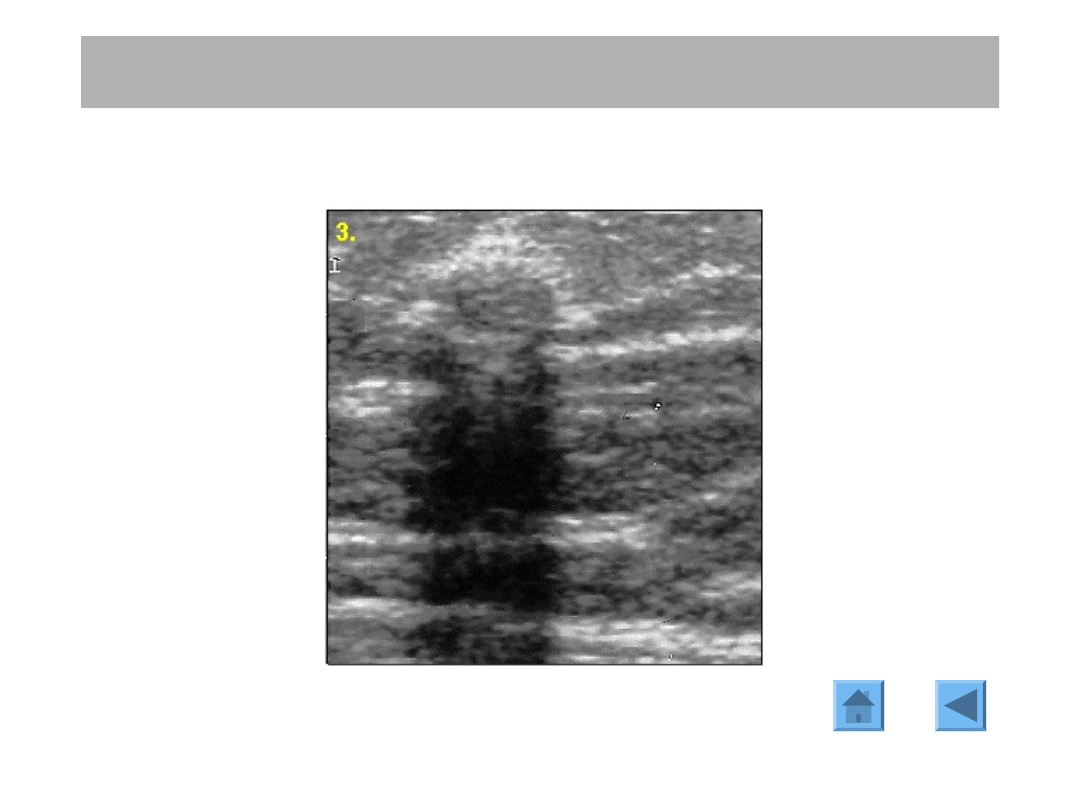
ROZPOZNANIE
ULTRASONOGRAFIA
Obraz USG zmiany podejrzanej w piersi

ROZPOZNANIE
BIOPSJA ASPIRACYJNA CIENKOIGŁOWA
Wskazaniami do BAC jest
Badalna palpacyjnie (lub
widoczna w USG), podejrzana
klinicznie lub w badaniach
obrazowych zmiana w piersi.
Ujemny wynik BAC nie wyklucza
raka!
Wskazania do wykonania BAC
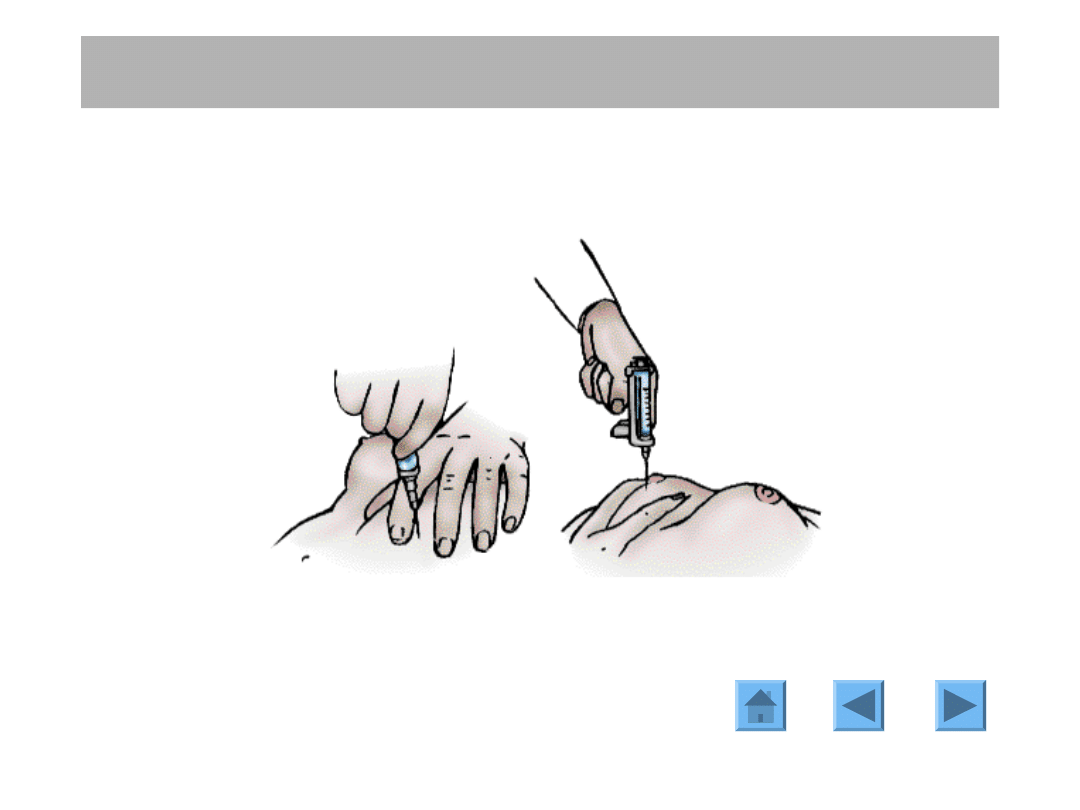
ROZPOZNANIE
BIOPSJA ASPIRACYJNA CIENKOIGŁOWA
Technika wykonania BAC
Z użyciem zwykłej
strzykawki
Strzykawka w specjalnym
uchwycie
Dla bardziej dokładnego
wkłucia BAC można wykona
pod kontrolą USG.

ROZPOZNANIE
BIOPSJA ASPIRACYJNA CIENKOIGŁOWA
Możliwymi powikłaniami BAC są:
- krwiak w miejscu wkłucia
- uszkodzenie opłucnej i odma
- rozsiew komórek nowotworowych w kanale wkłucia (powikłanie
teoretyczne, liczne badania doświadczalne nie potwierdziły ich obecności)
- zafałszowanie obrazu mammograficznego
Powikłania BAC

ROZPOZNANIE
BIOPSJA
Rozróżnia się
- biopsję gruboigłową (z ang. „core-needle biopsy”, „jet biopsy”)
- biopsję otwartą (z ang. „excisional biopsy”)
Wskazania
- biopsję gruboigłową stosuje się w przypadkach podejrzanych klinicznie
zmian w piersiach, w których BAC nie dała potwierdzenia raka.
Wynik ujemny
tego badania nie wyklucza raka!
Na podstawie pobranego w ten sposób
materiału tkankowego można określić typ nowotworu i obecność receptorów.
- biopsja otwarta (wycięcie podejrzanej zmiany w całości, tumorectomia) jest
jedyną metodą która może wykluczyć złośliwy charakter zmiany
. Wykonuje
się ją gdy BAC nie potwierdziła raka.
Rodzaje i wskazania
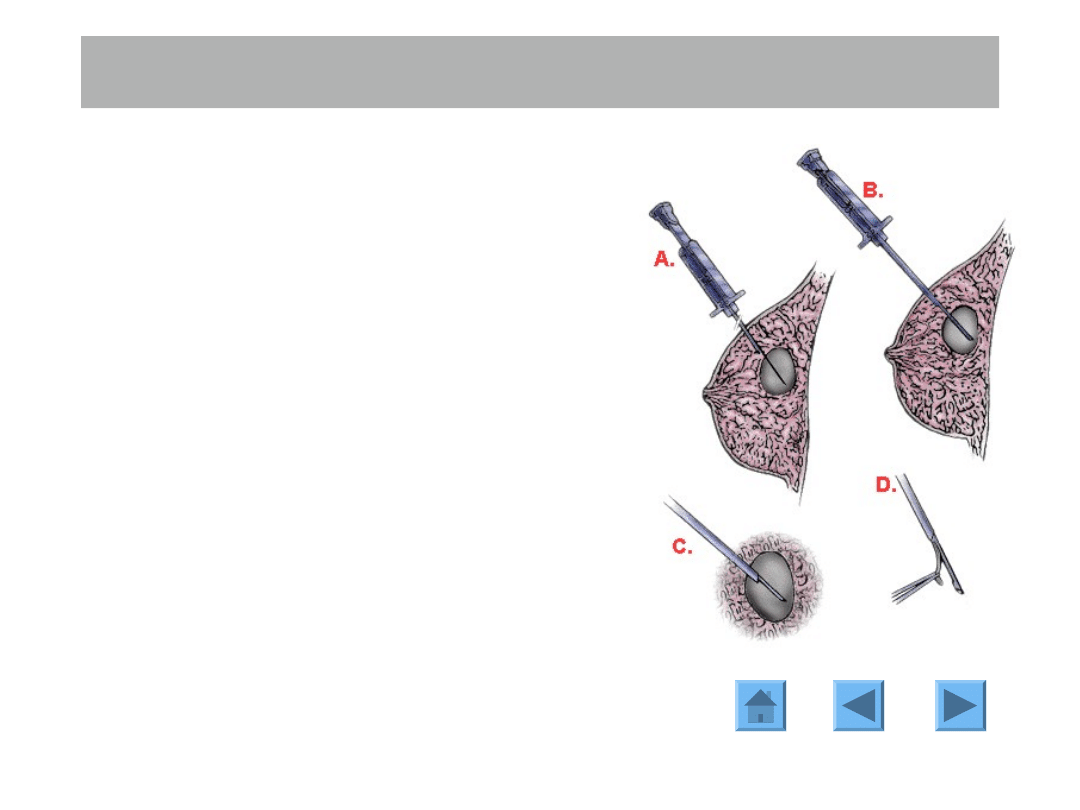
ROZPOZNANIE
BIOPSJA
Biopsję gruboigłową można
wykonywać pod kontrolą USG lub pod
kontrolą palpacyjną.
W jej wyniku otrzymuje się wałeczek
tkanki o średnicy ok. 1 mm i długości
ok. 2 cm.
Biopsja gruboigłowa - technika.
ROZPOZNANIE
BIOPSJA
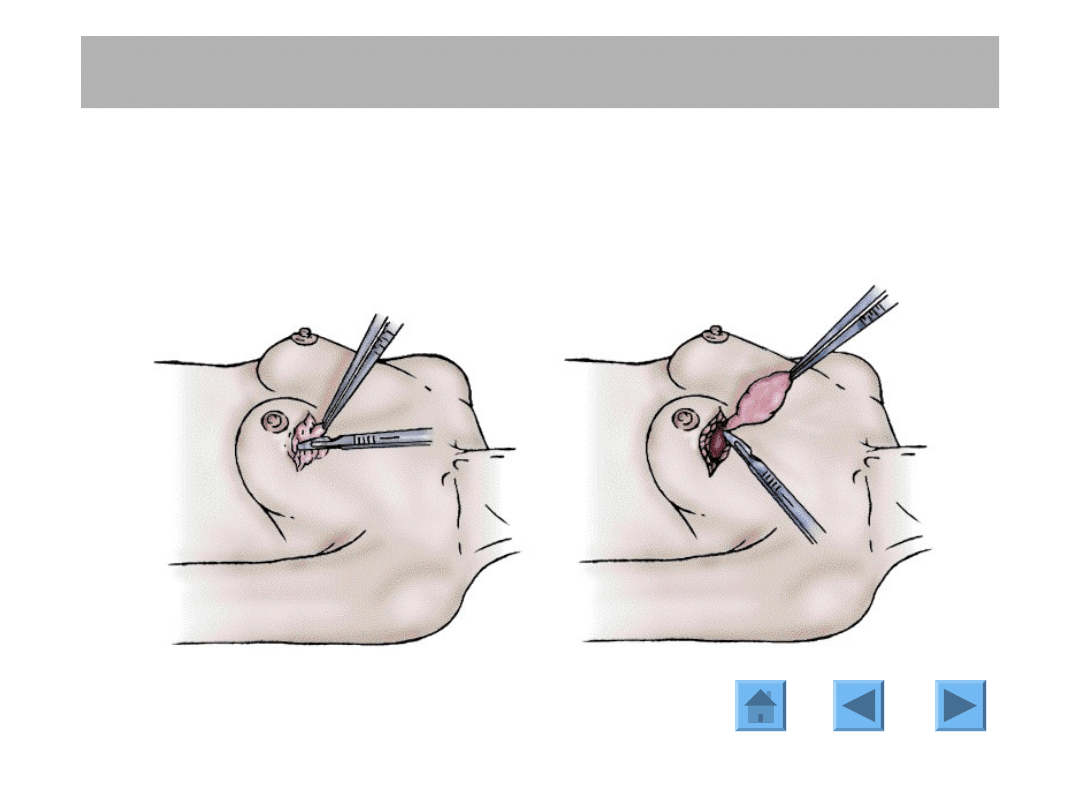
Biopsja otwarta - technika
ROZPOZNANIE
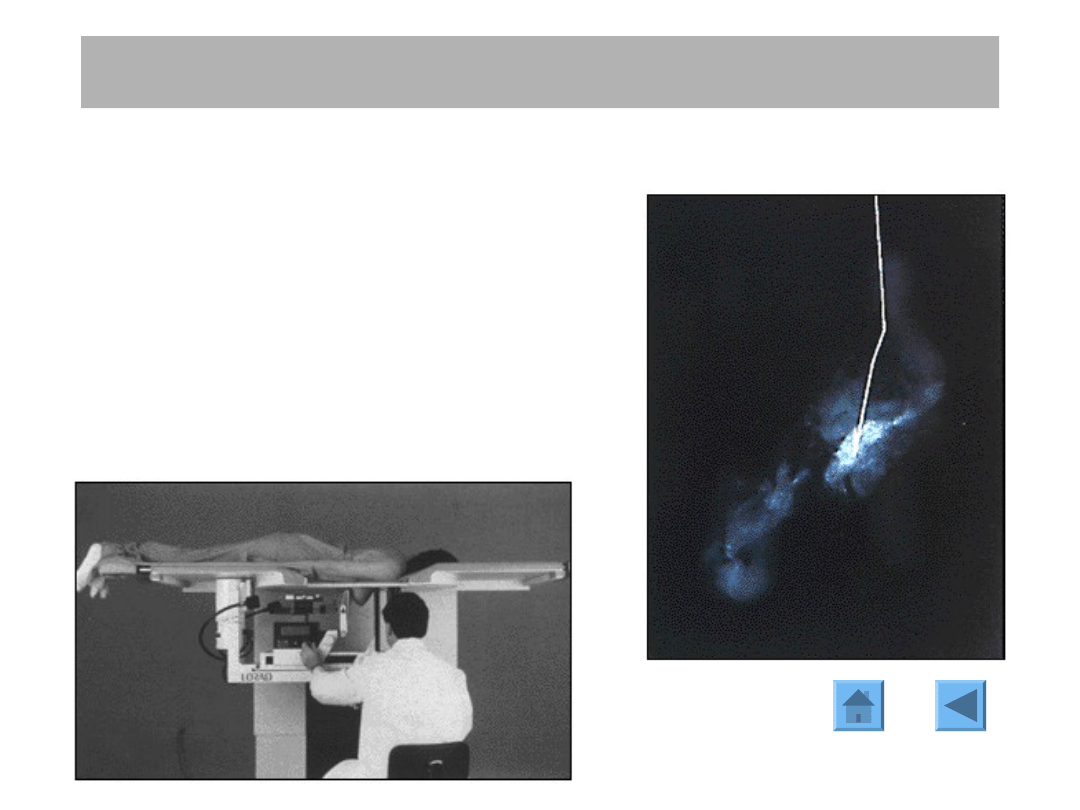
BIOPSJA
Zmiany
widoczne
w
mammografii
ale
niebadalne palpacyjnie oznacza się pod kontrolą
mammografii igłą lokalizacyjną („kotwiczką”)
lub podaje się do podejrzanego obszaru
barwnik, a następnie wycina.
Technika ABBI (Advanced Breast Biopsy
Instrumentation) - wycięcie fragmentu tkanki
pod stereotaktyczną kontrolą mammograficzną.
Biopsja zmian niebadalnych palpacyjnie

ROZPOZNANIE
NOWE TECHNIKI
Chociaż wciąż najlepszą techniką w skriningu i diagnostyce raka piersi jest
mammografia, to jednak i ta metoda ma swoje ograniczenia jeśli chodzi o
czułość i rozdzielczość.
W fazie testowania są nowe techniki obrazowania:
- mammografia cyfrowa
- diagnostyka wspomagana komputerowo (CAD Computer Aided Diagnosis)
- tomografia rezonansu magnetycznego
- pozytronowa tomografia emisyjna (PET)
Diagnostyczne techniki eksperymentalne w raku
piersi.

ROZPOZNANIE
NOWE TECHNIKI
Diagnostyka guzów piersi z użyciem tomografii rezonansu magnetycznego z
kontrastem (Gadolin) bywa stosowana u:
- kobiet z „gęstymi” radiologicznie, skrajnie nieprzeziernymi piersiami, w
połączeniu z USG
- pacjentek po leczeniu oszczędzającym raka piersi
- pacjentek po wszczepieniu protezy silikonowej
- dla bardzo dokładnej oceny naciekania raka
MRI
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 21
- Slide 22
- Slide 25
- Slide 26
- Slide 27
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
- Slide 99
- Slide 100
- Slide 101
- Slide 102
- Slide 103
- Slide 104
- Slide 105
- Slide 106
- Slide 107
- Slide 108
- Slide 109
- Slide 110
- Slide 111
- Slide 112
- Slide 113
Wyszukiwarka
Podobne podstrony:
GENETYKA 01 Dziedziczny rak sutka
GENETYKA 01. Dziedziczny rak sutka, GENETYKA ćwiczenie 1
pyt 18 rak sutka, Fizjoterapia
rak sutka
rak sutka (3)
Rak sutka leczenie oszczędzjące
rak sutka
GENETYKA 01. Dziedziczny rak sutka
Rak sutka ppt
Rak sutka, Chirurgia(1)
Rak sutka u kobiet w cišży, ustny
RAK SUTKA TARNOBRZEG
Rak sutka
GENETYKA 01 Dziedziczny rak sutka
Rak sutka rozsiany hormonoterapia
Rak sutka Agata
rak sutka
rak sutka (3)
więcej podobnych podstron