Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
CHROMATOGRAFIA GAZOWA ZE SPEKTROMETRIĄ MAS (GC-MS)
Analiza składu olejków eterycznych i aromatów spożywczych
Prowadzący ćwiczenie: dr Anna Sadowska-Rociek
Laboratorium 1.82, I piętro, III segment
Chromatografia gazowa jest jedną z najbardziej rozpowszechnionych metod instrumentalnych w
chemii analitycznej. Rozdzielenie składników analizowanych metodami chromatograficznymi mieszanin
jest wynikiem różnego ich podziału między fazę ruchomą i nieruchomą układu chromatograficznego.
Przy jej pomocy można analizować substancje mające w warunkach analizy postać gazów lub par.
Chromatografia gazowa obejmuje wszystkie metody chromatograficzne, w której fazą ruchomą jest
gaz. W zależności od typu stosowanej fazy nieruchomej (stacjonarnej) wyróżnia się:
• chromatografię adsorpcyjną (fazą nieruchomą jest adsorbent, rozdzielanie polega na różnej
adsorpcji składników próbki przez fazę stacjonarną, jest tzw. chromatografia w układzie gaz-ciało
stałe);
• chromatografię podziałową (fazą nieruchomą jest ciecz, która jest rozpuszczalnikiem dla
rozdzielanych substancji, rozdzielanie polega na podziale składników próbki pomiędzy fazę ciekłą i
gazową, jest to tzw. chromatografia w układzie gaz-ciecz).
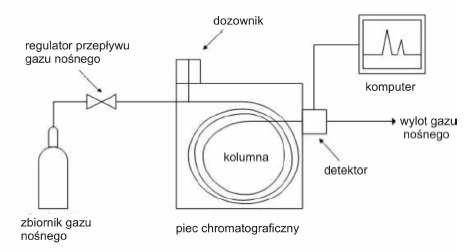
Rys.1. Schemat chromatografu gazowego
BUDOWA CHROMATOGRAFU GAZOWEGO
Jako gaz nośny (faza ruchoma) stosuje się najczęściej wodór, azot, argon lub hel. Rodzaj gazu
nośnego ma mały, zwykle pomijalny wpływ na wynik rozdzielania chromatograficznego i jest głównie
uzależniony od rodzaju użytego detektora. Jego czystość ma wpływ na pracę detektora i wypełnienie
kolumn, które może ulegać dezaktywacji. Gaz nośny nie może zawierać zanieczyszczeń, przede
wszystkim tlenu, pary wodnej i węglowodorów.
1
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
Dozownik (ang. injector)
Jest elementem umożliwiającym wprowadzenie próbki w strumień gazu nośnego, który przenosi ją
do kolumny. Wprowadzona do kolumny próbka musi mieć możliwie najmniejszą objętość. Sposób
wprowadzenia próbki zależy od jej stanu skupienia. Próbki ciekłe dozuje się za pomocą specjalnych
mikrostrzykawek. Próbka powinna odparować lub odsublimować w dozowniku w możliwie jak
najkrótszym czasie. W tym celu temperatura dozownika jest zwykle około 20 oC wyższa od temp.
wrzenia najwyżej wrzącego składnika próbki. Za wysoka temp. dozownika może powodować termiczny
rozkład próbki i pojawienie się na chromatogramie pików produktów tego rozkładu (pików duchów).
Natomiast za niska temp. dozownika powoduje długi czas wprowadzania próbki na kolumnę, co objawia
się pikami rozmytymi, niesymetrycznym lub ich złym rozdziałem.
Próbki ciał stałych wprowadza się przeważnie w postaci ich roztworów. Jeśli nie jest to możliwe,
próbkę wprowadza się specjalną strzykawką do dozowania substancji stałych. Gazy dozuje się bądź to
za pomocą specjalnych strzykawek bądź za pomocą specjalnych zaworów dozujących (popularny jest
tzw. zawór sześciodrożny).
Kolumna chromatograficzna
W kolumnie chromatograficznej zachodzi właściwy proces rozdziału analizowanych mieszanin.
Najczęściej stosowane są kolumny kapilarne i pakowane. Obecnie najpopularniejszymi kolumnami są
kolumny kapilarne tzn. kolumny o średnicy 0,2–0,6 mm i długości do kilkudziesięciu metrów.
Charakteryzują się one dużą zdolnością rozdzielczą. Mają one postać zwoju i wytwarzane są ze szkła
lub topionego kwarcu. W celu zwiększenia wytrzymałości i trwałości mechanicznej kolumny kwarcowe
pokrywa się z zewnątrz warstwą tworzywa sztucznego. Fazy stacjonarne w kolumnach kapilarnych
mogą być zarówno adsorbentami, jak i cieczami i są osadzone na ściankach w różny sposób. Dzieli się
je na kolumny z gładkimi ścianami pokrytymi ciekłą fazą stacjonarną (WCOT)- najczęściej stosowane,
kolumny z warstwą porowata na ściankach (PLOT) oraz kolumny na ścianki których naniesiono nośnik
nasycony ciekłą faza stacjonarna (SCOT). Grubość warstwy stacjonarnej wynosi zwykle 0,1-0,3 mm.
Cieńsza warstwa powoduje, że kolumna jest sprawniejsza i krótsze są czasy rozdzielania, grubsza
zapewnia większą pojemność sorpcyjną kolumny. Przy niektórych typach detektorów (GC-MS) kolumny
kapilarne są jedynymi możliwymi do zastosowania.
Kolumny pakowane wypełnia się cząstkami adsorbentu lub nośnika z osadzoną na nim fazą ciekłą.
Cząstki wypełnienia powinny mieć wąski zakres frakcji sitowej i kulisty kształt, gdyż zapewnia to małe
opory przepływu gazu przez kolumnę i małe rozmycie dyfuzyjne. Wypełnienie kolumny oraz własności
wypełnienia (polarność) mają ogromne znaczenie przy rozdziale substancji.
Detektor
Jego rolą jest wykrywane substancji rozdzielonych na kolumnie. Istota działania detektorów
stosowanych w chromatografii gazowej polega na tym, że reagują one na różnice we właściwościach
fizykochemicznych czystego gazu nośnego i gazu zawierającego substancję eluowaną z kolumny.
2
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
Zadaniem detektora jest przetworzenie stężenia substancji w fazie ruchomej w sygnały elektryczne.
Powstający sygnał często wymaga dodatkowego wzmocnienia. Detektor chromatograficzny powinien
charakteryzować się dużą czułością, niską granicą wykrywalności, dużą stabilnością, dużym zakresem
liniowości wskazań oraz dobrą odtwarzalnością. Poszczególne właściwości detektora nabierają
znaczenia w zależności od wymogów analizy. Niektóre detektory niszczą wykrywane substancje. W
zasadzie każda właściwość fizyczna lub fizykochemiczna substancji różniąca ją od gazu nośnego może
być stosowana jako podstawa detekcji, ograniczenia wynikają z wymagań stawianych detektorom.
Rozróżnia się detektory uniwersalne (do wykrywania wszystkich substancji) i selektywne (do wykrywania
tylko niektórych grup związków, np. halogenopochodnych lub zawierających siarkę).
Liczba typów detektorów znajdujących się dzisiaj w praktycznym użyciu wynosi przeszło 30.
Najczęściej wykorzystuje się następujące detektory:
Detektor płomieniowo-jonizacyjny - FID (ang. flame jonisation detector)
Jest detektorem uniwersalnym, przydatnym do wykrywania prawie każdego związku organicznego.
Ma szczególnie duże znaczenie przy analizie węglowodorów i ich pochodnych. Jego duża czułość,
stabilność oraz uniwersalność powoduje, że jest to najbardziej rozpowszechniony detektor. Do jego
działania potrzebny jest wodór i powietrze. Stosunek natężenia przepływu tych gazów wpływa na jego
czułość i specyficzność. W detektorze spalany jest wodór, przy czym płomień znajduje się między
dwiema elektrodami. Zasada pomiaru polega na zmianie przewodnictwa elektrycznego płomienia
wodoru w polu elektrycznym po wprowadzeniu substancji organicznej. Jeżeli do płomienia kolumny
dochodzi tylko gaz nośny, to wytwarzane są termojony tego gazu, które powodują pojawienie się w
układzie stałego prądu jonowego o bardzo małym natężeniu - prosta linia podstawowa na taśmie
rejestratora. Gdy do płomienia wodorowego wraz z gazem nośnym wprowadza się substancję
wymywaną z kolumny, wówczas jest ona spalana w detektorze i pojawia się większa liczba termojonów.
Tworzenie się termojonów następuje przez rozpad cząsteczek organicznych wychodzących z kolumny i
następujące po nim utlenianie produktów rozpadu tlenem doprowadzonym do płomienia z zewnątrz.
Prąd jonowy wzrasta i po wzmocnieniu zapisywany jest na taśmie w postaci piku przez czas
odpowiadający czasowi spalania się eluowanej substancji.
Detektor wychwytu elektronów - ECD (ang. electron capture detector)
Jest detektorem radiojonizacyjnym, w którym jonizacja analizowanych chromatograficznie
substancji następuje pod wpływem promieniowania jonizującego. Zasada działania tego detektora
polega na zdolności wszystkich substancji (z wyjątkiem gazów szlachetnych) do przyłączania wolnych
elektronów w fazie gazowej. Ta zdolność jest uzależniona od struktury wykrywanego związku i jest
szczególnie duża dla związków zawierających atomy fluorowców.
Cząstka promieniowania jonizującego b, pochodząca z wbudowanego radioaktywnego źródła
promieniowania zawierającego Ni-63, powoduje jonizacje gazu nośnego z uwolnieniem elektronu.
Cząstki b jonizują gaz nośny, przy czym powstają dodatnie jony gazu nośnego i powolne elektrony.
3
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
N2 + b = N2+ + e-
Wskutek powstawania w tej reakcji elektronów płynie prąd, który jest prądem podstawowym
detektora i na taśmie rejestratora otrzymuje się linie prostą. Jeżeli z kolumny eluowana jest substancja
mająca odpowiednie powinowactwo elektronowe, to wychwytuje ona powolne elektrony, tworząc jony
ujemne: M + e- = M-
Ten proces może zachodzić w połączeniu z dysocjacją lub bez niej. Ujemne jony wykrywanych
substancji rekombinują z dodatnimi jonami gazu nośnego, tworząc obojętne cząsteczki. Przez to zostają
usunięte z układu ostatnie elektrony i prąd zerowy w obecności substancji staje się słabszy - jest to
zapisywane w postaci piku na taśmie rejestratora. Gdy elucja danej substancji z kolumny zostaje
zakończona, natężenie prądu powraca do stanu początkowego - linia zerowa.
Do detektorów selektywnych (oprócz ECD) zaliczamy jeszcze detektor płomieniowo-fotometryczny
(FPD) (związki siarki i fosforu), detektor chemiluminescencyjny - SCD (związki siarki), detektor
termojonowy- TID (związki fosforu, azotu i halogenoorganiczne), detektor emisji atomowe - AED
(zanieczyszczenia środowiska, związki metaloorganiczne i produkty petrochemiczne).
Do detektorów uniwersalnych zaliczamy detektor fotojonizacyjny-PID (może on być również
stosowany jako selektywny), detektor jonizacyjno- wyładowczy.
Jako detektor w chromatografii gazowej bywa także stosowany olfaktometr (sprzężenie GC-O),
który pozwala na informację o stężeniu zapachu pochodzącym od konkretnego związku. Podczas
analizy, próbka wstrzykiwana jest do chromatografu gazowego, gdzie następuje jej rozdzielenie na
poszczególne substancje. Eluat z kolumny po jej opuszczeniu dzielony jest na dwa strumienie: pierwszy
trafia do tradycyjnego detektora (np. MS lub FID), drugi kierowany jest do olfaktometru. Grupa
oceniających ma za zadanie ocenić rodzaj zapachu oraz
oszacować jego intensywność. Wszystkie wskazania
grupy oceniających są rejestrowane (tworzony jest tzw.
aromagram) i następnie porównywane z wynikami
analizy GC-MS lub GC-FID. Porównanie sygnałów z
detektora MS lub FID (pik związku) z informacją z
olfaktometru (rodzaj i intensywność zapachu) pozwala
na ustalenie, które ze zidentyfikowanych związków
Rys.2. Chromatograf gazowy sprzężony z
olfaktometrem
charakteryzują się zapachem, jaki jest jego typ i
natężenie. Technika GC-O wykorzystywana jest do
badań mieszanin gazowych obdarzonych zapachami i znalazła zastosowanie przede wszystkim w
analizie żywności, środków zapachowych oraz próbek środowiskowych.
4
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
SPEKTOMETRIA MAS
Istota spektrometrii mas polega na otrzymaniu z obojętnych cząsteczek analizowanej próbki
naładowanych cząstek i rozdzieleniu ich według stosunku ich masy do ładunku (m/z).
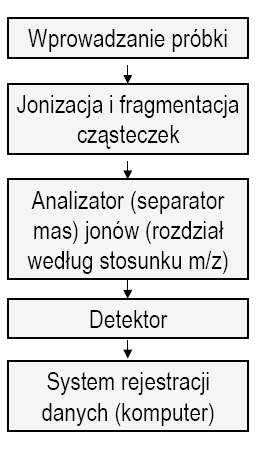
Schemat spektrometru mas przedstawiony został na Rys. 3.
Analizowaną próbkę wprowadza się do komory jonizacyjnej,
gdzie następuje jonizacja i fragmentacja analizowanych cząsteczek.
Jonizacja polega na oderwaniu od cząsteczki lub atomu jednego lub
kilku elektronów i utworzeniu jonu dodatniego. Jonizacji może
towarzyszyć proces rozpadu tego kationu na różne części
naładowane dodatnio lub obojętnie (fragmentacja). Jonizację
substancji
gazowych
prowadzi
się
najczęściej:
strumieniem
elektronów
emitowanych
przez
rozżarzoną
katodę,
polem
elektrycznym, stosuję się także jonizację chemiczną lub wyładowanie
iskrowe w próżni.
Rozdzielenie powstałych jonów według wartości stosunku m/z
następuje w analizatorach zwanych separatorami mas. Do najczęściej
stosowanych należą: pułapka jonowa, kwadrupol, analizator czasu
przelotu. Rozdzielone jony trafiają następnie do detektora, gdzie są
Rys. 3. Schemat spektrometru mas
rejestrowane. W spektrometrii mas jako detektory stosuje się
najczęściej powielacze elektronów.
Wykres wartości natężeń sygnałów odpowiadających kolejnym
wartościom m/z stanowi widmo masowe substancji, które jest charakterystyczne dla każdego związku.
W widmach masowych na osi x podaje się stosunek masy jonu m do ładunku z, na osi y – natężenie
danego piku m/z.
Spektrometria mas znalazła zastosowanie do określania wyznaczaniu masy molowej i wzoru
sumarycznego oznaczanych związków, do identyfikacji nieznanych substancji oraz do określania
struktury badanych związków organicznych.
Połączenie chromatografii gazowej ze spektrometrią masową (GC-MS) jest najczęściej
spotykanym połączeniem. Obie te metody analityczne bardzo dobrze nadają się do współpracy. Na
podstawie otrzymanego w wyniku rozdzielenia chromatograficznego i widma masowego można
zidentyfikować poszczególne substancje. We współczesnych przyrządach GC-MS prawie wyłącznie
stosuje się kolumny kapilarne. W spektrometrze masowym zachodzi jonizacja cząsteczek rozdzielonych
wcześniej chromatograficznie substancji i ich rozpad na charakterystyczne fragmenty. Charakteryzują
się one właściwym dla nich stosunkiem masy do ładunku (m/z) i są rozdzielane w polu magnetycznym.
Na podstawie chromatografu otrzymanego w wyniku rozdzielenia i widma masowego można
zidentyfikować poszczególne substancje. Najczęściej wykonuje się to przez porównanie widma
masowego zebranego dla analizowanego piku z widmami masowymi znajdującymi się w pamięci
5
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
komputera. Szybkość rejestracji widm masowych jest tak duża, że podczas rejestracji jednego piku
zwykłym detektorem można zarejestrować wiele widm masowych i stwierdzić np. koelucję dwóch lub
więcej analitów. Wykrywalność i czułość spektrometru masowego jest porównywalna z odpowiednimi
wielkościami dla detektora FID.
ANALIZA JAKOŚCIOWA I ILOŚCIOWA
Analiza jakościowa
Analiza jakościowa polega na porównaniu położenia piku na chromatogramie, czyli czasu retencji
rozdzielanych na kolumnie substancji z czasem retencji substancji wzorcowych. Czas retencji jest
wielkością stałą dla określonej substancji w danych warunkach chromatografowania (wypełnienie i
rodzaj kolumny, rodzaj i przepływ gazu nośnego oraz program temperaturowy). Wiele substancji może
mieć taki sam czas retencji, identyfikacje należy więc wykonywać na kilku różnych kolumnach,
modyfikując również program temperaturowy. Składniki chromatografowanej mieszaniny można
identyfikować innymi metodami analizy chemicznej lub fizykochemicznej (np. przy pomocy spektrometrii
mas, spektrometrii IR, spektrometrii UV–Vis).
Analiza ilościowa
Analiza jakościowa i ilościowa złożonych mieszanin jest wykonywana w jednym procesie.
O ilości substancji w mieszaninie można wnioskować na podstawie wysokości odpowiadającego jej
piku, gdyż wysokość i powierzchnia piku są proporcjonalne do ilości oznaczanego składnika. Wysokość
piku wykorzystuje się do oznaczeń ilościowych tylko, gdy pik jest symetryczny i wąski. Przy
wykorzystaniu tego parametru piku należy pamiętać, że jest on wrażliwy na czas trwania dozowania
próbki i na małe nawet zmiany prędkości gazu nośnego. Z punktu widzenia otrzymania powtarzalnych
wyników analizy korzystniejsze jest mierzenie powierzchni piku. Istota chromatograficznej analizy
ilościowej polega na porównaniu wielkości piku oznaczanego składnika z wielkością piku odpowiadającą
znanej ilości tego składnika w postaci substancji wzorcowej. Znając trzy wielkości oblicza się czwartą,
szukaną wielkość, tzn. masę lub stężenie oznaczanej substancji w próbce. Analizę ilościową
przeprowadza się metodą wzorca zewnętrznego (kalibracja bezwzględna), wzorca wewnętrznego,
dodatku substancji oznaczanej (wzorca) lub normalizacji wewnętrznej.
PARAMETRY WPŁYWAJĄCE NA ROZDZIAŁ SUBSTANCJI NA KOLUMNIE
CHROMATOGRAFICZNEJ
Znajomość składu próbki pozwala na wybór odpowiedniego detektora oraz kolumny (typu i
wypełnienia). Na rozdział substancji może również wpływać kontrola zmian temperatury w trakcie
procesu chromatografowania, co pozwala na poprawę oraz przyspieszenie tego procesu. Zaletą
chromatografii z programowaniem temperatury jest możliwość rozdziału mieszaniny o szerokim zakresie
6
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
temperatury wrzenia poszczególnych składników, niezależność detekcji od temperatury wrzenia,
niezależność dokładności oznaczeń od czasu retencji.
Zbyt wysoka temperatura kolumny powoduje zbyt szybkie pojawienie się pików oraz ich
niecałkowite rozdzielenie. Natomiast zbyt niska temperatura pracy kolumny powoduje wydłużenie czasu
analizy, wyżej wrzące substancje pojawiają się w postaci rozmytych, płaskich pików.
W
typowych
aparatach
istnieje
możliwość
zaprogramowania sekwencji kilku liniowych odcinków
narostu temperatury, z zadawanym współczynnikiem
szybkości zmian. Postępując w ten sposób, można
dobrać niską początkową temperaturę, odpowiednią do
rozdzielenia niskowrzących składników, a końcową
temperaturę - dostatecznie wysoką, aby można było
wyeluować wszystkie składniki próbki w racjonalnym
czasie. Zalety pracy z programowaną temperaturą
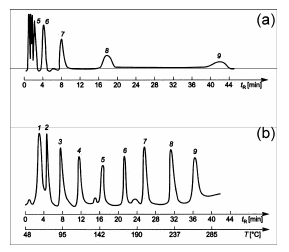
kolumny pokazano na Rys. 4.
Rys. 4. Chromatograf mieszaniny wykonany: a) w warunkach izotermicznych (temp. 60°C); b) w warunkach
programowania temperatury
ZWIĄZKI ZAPACHOWE W śYWNOŚCI – terpeny
Terpeny są składnikiem większości roślinnych substancji zapachowych: owoców cytrusowych, ziół,
przypraw, wchodzą w skład tzw. olejków eterycznych. Pomarańcze, grejpfruty, mandarynki, cytryny
zawierają powyżej 3% olejków eterycznych.
Terpeny składają się z jednostek izoprenowych, najczęściej spotykane są monoterpeny i
seskwiterpeny o 10 lub 15 atomach węgla. Ich tlenowe pochodne (aldehydy, ketony, estry i kwasy)
również obdarzone są silnym zapachem. Izomery stereochemiczne terpenów mogą mieć różne zapachy,
np. karwon.
O
O
limonen
α-pinen
β-pinen
kamfen
zapach cytrusów
zapach leśny
zapach sosnowy zapach kamfory (+)-karwon
(–)-karwon
p-cymen
zapach kminku zapach mięty zapach tymianku
Terpeny zawarte w olejkach eterycznych otrzymuje się najczęściej poprzez wytłaczanie, ekstrakcję
odpowiednim rozpuszczalnikiem organicznym lub destylację z parą wodną. Olejki eteryczne wytwarzane
z owoców cytrusowych zawierają głównie D-limonen, aldehydy, estry, alkohole i seskwiterpeny. Olejki
stosowane są jako środki aromatyzujące w przemyśle spożywczym (np. aromaty do ciast).
7
Analiza składu olejków eterycznych i aromatów spożywczych metodą GC-MS Chemiczna analiza instrumentalna
ZAGADNIENIA DO OPRACOWANIA:
• Zasada rozdziału chromatograficznego, podstawowe pojęcia i wielkości w chromatografii
• Budowa i zasada działania chromatografu gazowego; sposoby dozowania, podział kolumn i
detektorów; przykłady
• Analiza jakościowa i ilościowa w GC
• Spektrometria mas (MS) – podstawy teoretyczne, elementy składowe spektrometru i ich rola
• Przykłady zastosowań chromatografii gazowej oraz spektrometrii mas w analizie żywności
• Substancje zapachowe w żywności.
WYKONANIE ĆWICZENIA:
1.
Sporządzić roztwór wzorcowy mieszaniny terpenów o stężeniu podanym przez prowadzącą
ćwiczenie.
2.
Wykonać analizę chromatograficzną roztworu wzorcowego.
3.
Sporządzić roztwory rozcieńczone: olejku cytrynowego, pomarańczowego, aromatu cytrynowego
oraz pomarańczowego w heksanie. Proporcje zostaną podane przez prowadzącą ćwiczenie.
4.
Na tarce zetrzeć skórki z cytryny i pomarańczy. Zalać odpowiednią ilością heksanu, wytrząsać.
5.
Wykonać analizy chromatograficzne sporządzonych ekstraktów próbek w trybie full scan oraz SIM.
LITERATURA POMOCNICZA:
1. Szczepaniak W.: Metody instrumentalne w analizie chemicznej. Wyd. Nauk. PWN, Warszawa 2007.
2. Grabowska J.: Substancje zapachowe w żywności. [w:] Chemia żywności. Praca zbiorowa pod red.
Z. Sikorskiego, WNT, Warszawa 2007.
Inne materiały dotyczące chromatografii gazowej, spektrometrii mas oraz związków zapachowych w
żywności
8
Wyszukiwarka
Podobne podstrony:
K1 2011 12 zad 2
1 MSL temat 2011 12 zaoczneid 1 Nieznany
Pochodne funkcji, IB i IŚ, 2011 12
Calki, IB i IS, 2011 12 id 1073 Nieznany
dodatkowe8 analiza 2011 12 id 1 Nieznany
egz pol ETI EiT 2011 12
Lista zagadnien 2011-12, ! UR Towaroznawstwo, II ROK, chai
ćw 5 pdf przekształcenia użytkow, teren 2011 12
E1 2011 12 zad 3 id 149124
egz pol ETI AiR IBM 2011 12
Wykład 2011-12-20, psychologia drugi rok, psychologia ról
2011 12 02
gotowość szkolna przewodnik EK1 2011 12
2010 09 2011 12 Kalendarz żydowski 5770 5771 5772
IS 2011 12 wyklad 11 15 12 2011 MDW
Instrukcja GO 1 LABORATORIUM 2011 12 ćw2
lista nr5 EKONOMETRIA1 2011 12 Nieznany
Dynamika Budowli wyklad 4 2011 12
więcej podobnych podstron