ALICJA ggsgfgfs, JULIA gfvbbtds, MARIUSZ gfdsaI
KIERUNEK: BIOTECHNOLOGIA
GRUPA: 2B
ZESPÓŁ: 5
ĆWICZENIE NR 3
KINETYKA REAKCJI ENZYMATYCZNYCH
CEL ĆWICZENIA: W temperaturze pokojowej i bez katalizatora samorzutny rozkład nadtlenku wodoru zachodzi bardzo wolno. Reakcje tę katalizuje wiele substancji, w tym jony metali i enzymy. W przypadku katalizy za pomocą enzymów kinetyka rozkładu nadtlenku wodoru zależy od stosunku stężenia enzymu i stężenia substratu oraz temperatury. Celem ćwiczenia jest potwierdzenie słuszności równania Briggsa -Haldane'a oraz wyznaczenie wartości liczbowych stałych: Vmax i KM.
TABELE WYNIKÓW I OBLICZENIA:
TAB. 1
Czas reakcji, min |
Liczba cm3 0,02 mol/dm3 roztworu KMnO4 |
Stężenie roztworu H2O2 [S], mol/dm3 |
0 |
13,2 |
0,066 |
10 |
5,3 |
0,027 |
20 |
2,5 |
0,013 |
30 |
1,5 |
0,0075 |
40 |
0,9 |
0,0045 |
50 |
0,65 |
0,0033 |
60 |
0,6 |
0,003 |
Na podstawie wyników miareczkowania obliczamy stężenie molowe [S] nadtlenku wodoru:
5 H2O2 + 2 KMnO4 + 3 H2SO4→ 5 H2O2 + 2 KMnO4 + 3 H2SO4
1000 cm3 ∙ 5M H2O2 - 1000cm3 ∙ 2M KMnO4
10 cm3 ∙ Cx H2O2 - Vcm3 ∙ 0,02M KMnO4
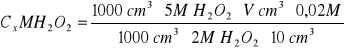
0 min 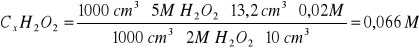
10 min 
20 min 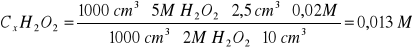
30 min 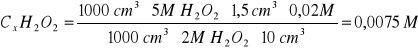
40 min 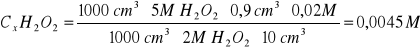
50 min 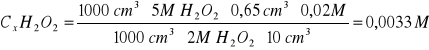
60 min 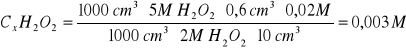
Obliczanie parametrów xi i zi:
![]()
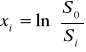
![]()
![]()
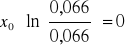
![]()
![]()
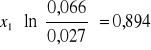
![]()
![]()
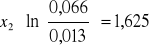
![]()
![]()
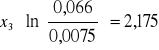
![]()
![]()
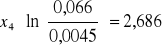
![]()
![]()
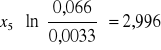
![]()
![]()
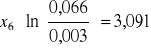
![]()
Lp. |
xiyi [min] |
zi2 [M2] |
yizi [min·M] |
xizi [M] |
xi2 |
(xizi)2 [M2] |
1 |
0,0000 |
0,0000 |
0,0000 |
0,0000 |
0,0000 |
0,0000 |
2 |
0,8940 |
0,0015 |
0,3900 |
0,0349 |
0,7992 |
0,0012 |
3 |
32,5000 |
0,0028 |
1,0600 |
0,0860 |
2,6406 |
0,0074 |
4 |
65,2500 |
0,0035 |
1,7700 |
0,1283 |
4,7306 |
0,0165 |
5 |
107,4400 |
0,0038 |
2,4800 |
0,1665 |
7,2146 |
0,0277 |
6 |
149,8000 |
0,0040 |
3,1500 |
0,1887 |
8,9760 |
0,0356 |
7 |
185,4600 |
0,0040 |
3,7800 |
0,1947 |
9,5543 |
0,0379 |
∑ |
541,3900 |
0,0196 |
12,6300 |
0,7991 |
33,9153 |
0,1263 |
Na podstawie powyższej tabeli, obliczanie parametrów a i b:
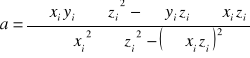
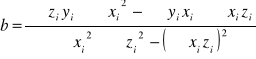
![]()
![]()
Obliczanie wartości stałych występujących w równaniu Briggsa-Haldene'a:
![]()
![]()
WNIOSKI:
Wysycanie enzymu substratem (zbliżanie się do szybkości maksymalnej) oznacza, że maleje liczba wolnych cząsteczek enzymu, gdyż rośnie ilość tych związanych w kompleksie z substratem (ES). Co można było zauważyć zmniejszającym się stężeniem nadtlenku wodoru (przy stałej temperaturze) wraz z upływem czasu.
Wyszukiwarka
Podobne podstrony:
113MOJA, Ochrona Środowiska pliki uczelniane, Fizyka
zgapy z fizyki, Ochrona Środowiska pliki uczelniane, Fizyka
LAB25, Ochrona Środowiska pliki uczelniane, Fizyka
NASZA52, Ochrona Środowiska pliki uczelniane, Fizyka
Lab82b, Ochrona Środowiska pliki uczelniane, Fizyka
NASZA61A, Ochrona Środowiska pliki uczelniane, Fizyka
Energia wodna na Fizykę, Ochrona Środowiska pliki uczelniane, Fizyka
61-obliczenia2, Ochrona Środowiska pliki uczelniane, Fizyka
113A, Ochrona Środowiska pliki uczelniane, Fizyka
nasza 9, Ochrona Środowiska pliki uczelniane, Fizyka
ENERGIA WODNA1, Ochrona Środowiska pliki uczelniane, Fizyka
Lab61, Ochrona Środowiska pliki uczelniane, Fizyka
NASZA51, Ochrona Środowiska pliki uczelniane, Fizyka
LAB51, Ochrona Środowiska pliki uczelniane, Fizyka
Pobieranie, Ochrona Środowiska pliki uczelniane, Fizyka
sprawozdanie 4 fizyka, Ochrona Środowiska pliki uczelniane, Fizyka
82MOJE, Ochrona Środowiska pliki uczelniane, Fizyka
lab121 wyn, Ochrona Środowiska pliki uczelniane, Fizyka
więcej podobnych podstron