skrypt wzory i prawa z objasnieniami62

122 Przemiany stanu gazu doskonałego
■ W trakcie przemiany i/obaryc/ncj spełniony jest warunek p const,a więc r równania stanu gazu doskonałego wynika zależność Y tT=const lub ry7*i = y^tTi (prawo Gay - Lussaca)
W cza>:c przemiany izobaryczncj gaz pobiera ciepło i wykonuje pracę Ilość ciepła potrzebna do ogrzania n moli gazu od temperatury Tdo temperatury T * aT w przemianie izobaryczncj wyraża się wzorem
Q — nCpAT,
gdzie zakładamy, że Cp - ciepło molowe pod stałym ciśnieniem jest stałe.
Praca W wykonana przez gaz w przemianie izobaryczncj wyraża się wzorem
'? yf
W= pĆV=-p | d v = y2 - V, )=p&r .
«-:l ‘'i
Pierwsza zasada termodynamiki dla tej przemiany ma więc postać nCp£s.T = A U~rpAV.
■ Przemiana i/.ucbnryczna gazu doskonałego zachodzi przy w-arunku I const, który jest równoważny warunkow i p!T- const lub p-JT\ ~P2'^2 (pniwn Charicsa)
W czasie przemiany izochoryczncj gaz nic wykonuje pracy dff/= pdV- 0.
Ilość ciepła potrzebna do ogrzania n moli gazu od temperatury T do temperatury T + A T wynosi Q - nCyAT* gdzie Cy jest ciepłem molowym przy stałej objętości P.erwsza zasada termodynamiki dla lej przemiany ma więc postać
nCyAT - AU.
■ Powyższy wzór w postaci różniczkowej diz = nCy&T wyraża zmianę energii wewnętrznej r. moli gazu przy zmianie temperatury o dT w dowolnym procesie termodynamicznym.
■ Równanie Mayera. Zastosujmy pierwszy zasadę termodynamiki do przemiany izobaryczncj n moli gazu doskonałego
nCpAT= AU-^pAY.
Ponieważ dla gazu doskonałego mamy A U = nC j/AT, więc otrzymujemy nCpAT =nCyAT+pAV 7. równania Clapeyrona mamy pAY = nRAT Zatem nCpAT-HRAT^nCytsT,
skąd dzieląc obie strony równania przez nAT otrzymujemy
Cp ~ Cy — R.
Dla każdego gazu ciepło molowe pod stałym ciśnieniem jest zawsze większe od ciepła molowego w stałej objętości o wielkość równą stałej gazowej Równanie Mayera można także zapisać dla cicpeł właściwych
gdzie M jest masą cząsteczkową gazu
objętość gazu doskonałego
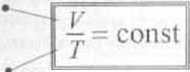
PA
temperatura bezwzględna gazu doskonałego
ciepło molowe
ciepło pobrane przez gaz przy stałym ciśnieniu
w czasie przemiany izobaryczncj
■
v
liczba mol gazu
Q = n CpAT= m CpAT
x
li gazu * /
masa gazu •
praca w przemianie izobaryczncj
ciepło właściwe przy stałym ciśnieniu
ciśnienie gazu doskonałego

ly = const
izochoru (V - const i
/
siała w artość dla danej masy gazu doskonałego
ciepło pobrane przez gaz w czasie przemiany izochoryczr.cj
ciepło molowe
przy stałej objętości •
Równanie Mayera
■ ciepło molowe przy stałym ciśnieniu <
»stała gazowa J
o.-K
i zmiana
temperatury gazu
ciepło właściwe przy stałej objętości
/
/ .» stała gazów?
/"■ = 8.
C p — L y = K | rao
• ciepło molowe przy stałej objętości
/
Wyszukiwarka
Podobne podstrony:
skrypt wzory i prawa z objasnieniami62 122 Przemiany stanu gazu doskonałego ■ W tr
skrypt wzory i prawa z objasnieniami63 124 Przemiany stanu gazu doskonałego ■ W pr
skrypt wzory i prawa z objasnieniami47 92 J 1 Małe drgania ■ Jeżeli energia potencjalna układu, któr
skrypt wzory i prawa z objasnieniami63 124Przemiany stanu gazu doskonałego ■ W prz
skrypt wzory i prawa z objasnieniami71 140 Średnia droga swobodna. Dyfuzja ■ Pomię
skrypt wzory i prawa z objasnieniami69 136Rozkład Boltzmanna T ■ Ko/Mud Boit/iminu
skrypt wzory i prawa z objasnieniami71 Średnia droga swobodna. Dyfuzja ■ Pomiędzy kornym; zderzeniam
skrypt wzory i prawa z objasnieniami03 4 Układy współrzędnych ■ Układem odniesienia nazywamy ciało,
skrypt wzory i prawa z objasnieniami05 8 Prędkość ■ Tor jest to krzywa opisywana w przestrzeni przez
skrypt wzory i prawa z objasnieniami24 46 Pole grawitacyjne ■ Pole grawitacyjne przy powierzchni Zie
skrypt wzory i prawa z objasnieniami25 Pole sił zachowawczych (potencjalnych) ■ Jeśli w każdym punkc
skrypt wzory i prawa z objasnieniami37 72Moment bezwładności ■ Moment bezwładności
skrypt wzory i prawa z objasnieniami38 74 Ruch obrotowy ciała ■ Jak wynika z własności iloczynu wekt
więcej podobnych podstron