skrypt wzory i prawa z objasnieniami63

124 Przemiany stanu gazu doskonałego
■ W przemianie izotermie/ncj gazu doskonałego warunek 7 - const jesi równoważny warunkowi pV= const lub P\V\ -P2^2 (prawo Boylc'a -Manoue'a). W przemianie izotcrmiczr.cj zmiana energii wewnętrznej jest równa zeru. gdyż temperatura gazu me zmienia sic dL/ = n CydT = 0. Gdy gaz pobiera Ciepło, 10 jest ono całe zużyte na wykonanie przez gaz pracy Q - W.
•‘racę wykonywaną przez gaz w przemianie izotermiczncj obliczamy ze wzoru
ti
IV = )póV. v\
Podstawiając ciśnienie p - nRTi'V otrzymujemy
V2 j/
W^nRT J ^=/»/?rin-r^
./ V v i
■ Przemiana adiabatyczna jest to proces, podczas którego nie zachodzi wymiana ciepła z otoczeniem Można to uzyskać poprzez oddzielenie układu od otoczenia dobrymi izolatorami cieplnymi lub jeżeli proces przeprowadzimy dostatecznie szybko.
/ pierwszej zasady termodynamiki d£-d(/*d#' wynika, że ponieważ dQ - O .tu dl'+ćH = 0. Czyli w’ przemianie adiabatycznej praca wykonywana przez uklar. równa est ubytkowi energii wewnętrznej układu, a więc dłf* = - dU
■ Przyrost energii wewnętrznej układu powoduje wzrost jego temperatury. Ten wzrost temperatury powoduje dodatkowy wzrost ciśnienia gazu. A wiec podczas adiabatycznego sprężania (rozprężania) gazu zmiany ciśnienia są większe niż podczas izotomucznego sprężania (rozprężania) gazu (wykres po prawej stronie).
■ Z równania utli.ih;<(> (rów nania Poisuina) dla zmiennychp i V{pVI -const ' można przejść do zmiennych T i V Skorzystamy w tym celu / równaniu Clapcyrona p - uRT>V Otrzymujemy pV- nRT\r*iV =nRTV'i~] = const. Stąd yyr-l - "ciist (stałe występujące w dwóch ostatnich równaniach są oczywiście •óżne). Ink więc równanie adiabaty może być w7rażone poprzez dowolne dwie wielkości spośród p. V. T
■ Przemianą politropową nazwy wainy przemianę, podczas której ciepło molowe C (ciepło właściwe c) jest stałe. Równanie politropy gazu doskonałego ma posiać
pV n = const, gdzie k - nazywamy wykładnikiem politropy
Wszystkie dotychczas omówione przemiany są szczególnymi przypadkami przemiany poi tropowej. W przemianie izoharyczncj C-Cp a więc n = 0. izochorycznęj C=C, czyli n-t, izotermiczncj n = / Przemiana adiabatyczna również jest przemianą pobtropową dlu n = y
Termodynamika
125
63.3 Przemiana izotermiczna

63.4. Przemiana adiabatyczna
ciepło molowe przy siałym ciśnieniu
objętość gazu doskonałego
• współczynnik Poissona
równanie Poissona
cinieme gazu doskonałego
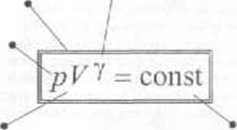
ciepło molowe przy stałej objętości
stała wartość dla danej masy gazu doskonałego
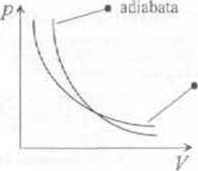
izoierrr.a {T= consri
Wyszukiwarka
Podobne podstrony:
skrypt wzory i prawa z objasnieniami62 122 Przemiany stanu gazu doskonałego ■ W tr
skrypt wzory i prawa z objasnieniami62 122 Przemiany stanu gazu doskonałego ■ W tr
skrypt wzory i prawa z objasnieniami63 124Przemiany stanu gazu doskonałego ■ W prz
skrypt wzory i prawa z objasnieniami71 140 Średnia droga swobodna. Dyfuzja ■ Pomię
skrypt wzory i prawa z objasnieniami69 136Rozkład Boltzmanna T ■ Ko/Mud Boit/iminu
skrypt wzory i prawa z objasnieniami71 Średnia droga swobodna. Dyfuzja ■ Pomiędzy kornym; zderzeniam
skrypt wzory i prawa z objasnieniami03 4 Układy współrzędnych ■ Układem odniesienia nazywamy ciało,
skrypt wzory i prawa z objasnieniami05 8 Prędkość ■ Tor jest to krzywa opisywana w przestrzeni przez
skrypt wzory i prawa z objasnieniami24 46 Pole grawitacyjne ■ Pole grawitacyjne przy powierzchni Zie
skrypt wzory i prawa z objasnieniami25 Pole sił zachowawczych (potencjalnych) ■ Jeśli w każdym punkc
skrypt wzory i prawa z objasnieniami37 72Moment bezwładności ■ Moment bezwładności
skrypt wzory i prawa z objasnieniami38 74 Ruch obrotowy ciała ■ Jak wynika z własności iloczynu wekt
skrypt wzory i prawa z objasnieniami49 96 Składanie drgań ■ Przy składaniu drgań o
więcej podobnych podstron