larsen0269

12. Gazy krwi 269
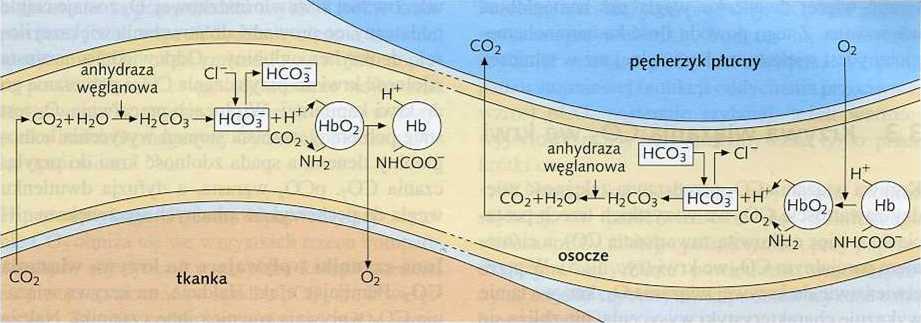
Ryc. 12.4 Chemiczne reakcje w erytrocytach podczas wymiany gazowej w tkankach (po stronie lewej) i w płucach (po stronie prawej; Schmidt i Thews, 1995; zmodyfikowano).
transportować do płuc jego duże ilości powstające w procesach przemiany materii.
3.2.1 Transport C02 fizycznie rozpuszczonego we krwi
Uwarunkowane ciągłą produkcją C02, cis'nienie parcjalne C02 jest w komórce większe niż w naczyniach włosowatych tkanek; dlatego cząsteczki C02 mogą dyfundować według gradientu cis'nień do krwi kapilarnej. Tylko bardzo niewielka część pozostaje fizycznie rozpuszczona w osoczu. Stężenie C02 fizycznie rozpuszczonego można wyliczyć na podstawie prawa Henry’ego-Daltona:
stężenie C02 w roztworze = a x pC02 (a - współczynnik rozpuszczalności, p - ciśnienie parcjalne).
Rozpuszczalność C02 zależy od temperatury ciała: wraz ze spadkiem temperatury ciała zwiększa się rozpuszczalność i odwrotnie. W 37°C rozpuszczalność C02 wynosi 0,0308 mmol/1/ mmHg
3.2.2 Przekształcanie C02 w wodorowęglan
Jedynie niewielka część znajdującego się w osoczu C02 ulega tam powolnemu uwodnieniu, ze względu na brak odpowiedniego enzymu. Duża część dyfunduje z osocza do erytrocytów. Tutaj reakcja z wodą ulega znacznemu przyspieszeniu, dzięki działaniu anhydrazy węglanowej (enzymu znajdującego się w erytrocytach i śródbłonku), co prowadzi do powstania kwasu węgłowego (uwodnienie). Kwas węglowy natychmiast dysocjuje do wodorowęglanu i jonu wodorowego:
C02 + H20 H2C03 -> HCOy + H+.
Reakcja ta prowadzi do wzrostu stężenia wodorowęglanów w erytrocytach. Powstaje różnica stężeń pomiędzy erytrocytem a osoczem. Ujemnie naładowany wodorowęglan może dyfundować z erytrocytu do osocza jednak tylko wtedy, gdy utrzymana zostanie równowaga ładunków elektrycznych i jakiś' anion przejdzie z osocza do erytrocytu (kationy nie mogą przechodzić przez błonę). Jonem tym jest jon chlorkowy, CP, który dyfunduje do erytrocytu, podczas gdy wodorowęglan dyfunduje na zewnątrz - proces ten nazywany jest przesunięciem chlorków (chłorid shift) lub przesunięciem Hamburgera.
Powstające w procesie tworzenia wodorowęglanów jony H+ zostają zbuforowane przez hemoglobinę tak, że wartos'ć pil nie zmienia się istotnie. W tkankach buforowanie to ułatwiane jest przez jednoczesne oddawanie 02 z hemoglobiny, ze względu na to, że dcoksyhemoglobina wykazuje mniejszą kwasowos'ć niż oksyhemoglobina. Może więc zostać wychwyconych odpowiednio więcej dodatkowych jonów H+ i więcej wodorowęglanów może utworzyć się z kwasu węglowego.
3.2.3 Połączenia karbaminowe C02
Niewielka ilość rozpuszczonego we krwi C02 (5%) reaguje bezpośrednio z grupami aminowymi hemoglobiny, tworząc połączenia karbaminowe, względnie karbaminohemoglobinę:
Hb x NH2 + C02 = Hb x NHCOCr + H+.
Do zajścia tej reakcji nie jest konieczna obecność anhydrazy węglanowej. Podobnie jak w przypadku wodorowęglanów, deoksyhemoglobina może przy-

Wyszukiwarka
Podobne podstrony:
0000037 (8) Ryc. 158. Położenie kończyny przy wysokim porażeniu nerwu kulszowego po stronie lewej (w
0000037 (8) Ryc. 158. Położenie kończyny przy wysokim porażeniu nerwu kulszowego po stronie lewej (w
larsen0088 88 I Podstawy farmakologiczne i fizjologiczne Ryc. 4.8 Budowa chemiczna droperidolu. Środ
wykłady z socjologii 13 2014 (101) 2013-12-06 Czynniki kryzysu na poziomie wiedzy profesjonalnej: Po
wstrzyknięcia 4 Ryc. 12b. Miejsce wkłucia według metody Sachtlebena po stronie lewej (pozycja przed
larsen0261 12. Gazy krwi 261 Wdechowe stężenie 02. Jeżeli zmieni się wdechowe stężenie 02, jednakowo
larsen0263 12. Gazy krwi 263 12. Gazy krwi 263 ps02 (%) = Hb + 4 02 = Hb (02)4. Teoretycznie 1 g hem
larsen0265 12. Gazy krwi 265 Przesunięcie krzywej wiązania 02 na skutek zmian stężenia H+ i pC02 jes
larsen0267 12. Gazy krwi 267 pojemności minutowej serca i odwrotnie - przy założeniu, że nie zmienił
larsen0271 12. Gazy krwi 271 12. Gazy krwi 271 Przebieg ten zależy od produkcji C02 i od pojemności
larsen0688 688 II Anestezjologia ogólna Ryc. 26.12 Trzepotanie przedsionków. ne. Naparstnica wzmaga
larsen1212 1212 III Anestezjologia specjalistyczna Ryc. 41.12 Schemat blokowy leczenia podwyższonego
larsen0012 12 I Podstawy farmakologiczne i fizjologiczne 12 I Podstawy farmakologiczne i fizjologicz
larsen0750 750 II Anestezjologia ogólna Tabela 27.12 Wyrównywanie strat płynów podczas różnych zab
DSC09387 Energia swobodna A + C-+B + D + Ciepło Ryc. 12-1. Sprzężenie reakcji egzoergicznej z
WIADOMOŚCI 2003,57, 11-12 chemiczne PL ISSN 0043-5104 ZASTOSOWANIE TRIETYLOAMINY W SYNTEZIE
WIADOMOŚCI 2003,57, 11-12 Chemiczne PL ISSN 0043-5104KIERUNKI BADAŃ I MOŻLIWOŚCI ANALITYCZNE W TECHN
więcej podobnych podstron