Blok d
2009-01-12
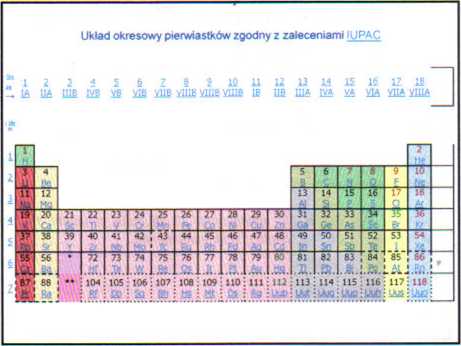
• Trzy okresy metali bloku d
• Określenie pierwiastki przejściowe (metale) nie jest zamienne z określeniem metale bloku d.
Pierwiastkiem przejściowym jest taki pierwiastek, którego atom ma niecałkowicie wypełniona powłokę d lub takie, których atom przechodząc do formy kationowej będzie posiadał niewypełnione orbitale d.
■ Stąd też pierwiastki grupy 12 (cynkowce) nie będą należały do pierwiastków przejściowych.
Pierwiastki bloku f są natomiast czasami nazywane pierwiastkami wewnętrzno-przejściowymi.
Żeby być spójnym z naszą klasyfikacją pierwiastków na blok s i blok p powinniśmy używać również i tu nazwy pierwiastki bloku d i f.
Powinniśmy zwrócić uwagę na trzy dalsze kwestie :
r Każda grupa metali bloku d składa się z trzech członków i nazywana jest triadą;
r Metale drugiego i trzeciego okresu są czasami nazywane ciężkim metalami bloku-d.
r Ru, Os, Rh, Ir, Pd i Pt są kolektywnie nazywane metalami grupy platynowców.
Konfiguracja elektronowa stanu podstawowego
I. W pierwszym przybliżeniu obserwowane konfiguracja elektronowa stanu podstawowego pierwszego, drugiego i trzeciego okresu bloku metali -d odpowiada progresywnemu wypełnianiu odpowiednich orbitali 3d, 4d, i Sd.
/. Istnieją drobne odstępstwa od tego szablonu jak np. w
pierwszym okresie: stan podstawowy chromu jest Ar[4s‘3d5j aniżeli ten który wynikałby z reguły afbau tzn. Ar[4s23d4].
|
21 Sc 3d’4s2 |
22 Tl 3d24s2 |
23 V 3dJ4s2 |
24 Cr 3d*4s1 |
25 Mn 3d54s2 |
26 Fe 3d«4s2 |
27 Co 3d74s2 |
28 Ni 3d84s2 |
29 Cu 3d'°4s' |
30 Zn 3d’°4s2 |
|
39 Y 4d<5s2 |
40 Zr 4d25s2 |
41 Nb 4d45s1 |
42 Mo 4d55s1 |
43 Tc 4ds4s’ |
44 Ru 4d75sł |
45 Rh 4d*5s1 |
46 Pd 4d105s° |
47 Ag 4d,05s1 |
48 Cd. 3d104s2 |
|
57 La 5d’6s2 |
72 Hf 5d26s2 |
73 Ta 5dJ6s2 |
74 W 5d46s2 |
75 Re 5d*6s2 |
76 Os 5d*6s2 |
77 Ir 5d;6s2 |
78 Pt Sd^s1 |
79 Au 5d,06s' |
80 Hg 5d106s2 |
Przyczyna tych odchyleń jest poza materiałem tego kursu:
powinniśmy znać zarówno różnicę energii pomiędzy orbitalami atomowymi 4s i 3d kiedy ładunek jądrowy wynosi 24 (liczbo atomowo Cr) jak I energie Inter- elektronowych oddziaływań dla każdej z powyższych konfigurocji.
Na szczęście wszystkie jony M2’ IM'* pierwszego okresu bloku-d posiadają konfigurację taką samą tzn. Ar[3d"j tak więc porównawcza chemia tych metali iest w większości związana z sukcesywnym wypełnianiem orbitali 3d.
II. Dla metali drugiego i trzeciego okresu ten obraz jest bardziej skomplikowany i systematyczne traktowanie ich chemii nie może być przedstawione jedynie na podstawie wypełniania poszczególnych pasm elektronowych.
III. Ważnym punktem, o którym nie możemy zapominać jest to, że atomy metali bloku d są wielo-elektronowymi indywiduami, i kiedy dyskutujemy np. na temat funkcji radialnego rozłożenia
orbitali nd, odnosimy się to atomów wodoropodobnych a stąd dyskusja jest w bardzo dużym stopniu przybliżona.
1
Wyszukiwarka
Podobne podstrony:
Blok d (6) 2009-01-12 Model Keperta tłumaczy kształt kompleksów metali bloku d [MLJ, czy [ML J"
Blok d (1) 2009-01-12Właściwości fizyczne Prawie wszystkie metale bloku -d są metalami: •
Blok d (2) 2009-01-12 [&<li]0śEp«M)Ś(§ BEfDdM Kilka uogólnień w odniesieniu do pierwiastków
Blok d (3) 2009-01-12 ---■.___—........4f, •* -f-r 4+4+. 4++r:.■H"*........4f C,
Blok d (5) 2009-01-12 Rysunek (a) przedstawia kompleks w który wyraźnie wskazane jest tworzenie się
Blok d (7) 2009-01-12licdabont}«acyjBa3 1. Przykłady kompleksów z liczbą koordynac
Blok d (8) 2009-01-12 wymienione należą do grupy kompleksów wysoko spinowych. W grupie kompleksów ok
Blok d (9) 2009-01-12 Określenie przeciw-jonów jest Istotne poniewai rótnice energetyczne pomiędzy 8
2009 01 02 2030 G W v.nl **.-« S I Dufly. (’A#«wvłv^*wU, W<ntwj itil? ISBN >-41-15324-3. C by
2009 01 02 2446 6 W almo. $ I Duffy. ( A-Ow vuA»vU, W.ofn»j JCKT ISBN *?ŁA>-OI I5)2-4 ?. O by ttN
2009 01 02 2514 G W v.nl **.-« S I Dufly. (’A#«wvłv^*wU, W<ntwj itil? ISBN >-41-15324-3. C by
img038 data zajęć w pracowni komp. 30.11.2009 7.12.2009 14.12.2009 4.01.2010 18.01.2009 nr grupy
więcej podobnych podstron