5806256273
Część III: Termodynamika układów biologicznych
Tak więc objętość jest funkcją stanu gazu doskonałego. W analogiczny sposób można wykazać, że temperatura i ciśnienie są również funkcjami stanu gazu doskonałego.
Sprawdźmy teraz czy praca mechaniczna wykonywana przez gaz doskonały jest funkcją stanu tego gazu. Najpierw musimy znać różniczkę pracy gazu doskonałego. Z fizyki i chemii fizycznej wiemy, że różniczka pracy równa jest:
dW = -pdV = -pf — dT - dpi = -RdT +—dp kP P ) P
Sprawdźmy teraz czy jest to różniczka zupełna:
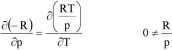
Wniosek: praca mechaniczna nie jest funkcja stanu gazu doskonałego, chociaż jest parametrem stanu.
I. zasada termodynamiki
Pierwsze sformułowanie tej zasady zawdzięczamy Juliuszowi Robertowi Mayerowi (1942). Uzupełnił ja Helmholtz w roku 1947. Mówi ona, że suma wszystkich rodzajów energii w układzie zamkniętym pozostaje stała. Po opublikowaniu teorii Einsteina Henri Poincare sformułował ja w 1908 roku w nieco przekorny sposób: „Istnieje coś, co jest stałe w układzie zamkniętym”.
Ale co to jest to „coś”? Jest ono stałe w układzie zamkniętym, tzn. nie wymieniającym materii z otoczeniem. Jest funkcja stanu, bo jej różniczka w układzie zamkniętym jest równa 0. Nie jest to praca, bo praca nie jest funkcja stanu, ale ma z pracą i energią coś wspólnego. Przyjęto nazywać to „coś” energia wewnętrzną i oznaczać symbolem U.
Współcześnie I zasadę termodynamiki zapisujemy w postaci: dU = dQ + dW,
a więc przyrost energii wewnętrznej jest sumą przyrostu ciepła i pracy wykonanej nad układem. W tej postaci nie można jeszcze wykazać, że różniczka energii wewnętrznej jest różniczką zupełną, ale wykażemy to w toku dalszego wykładu.
I. zasada termodynamiki była badana na gruncie biologii jeszcze przed jej precyzyjnym sformułowaniem. Już w roku 1777 Lavoisier zastanawiał się nad związkiem ilości wydzielanego przez zwierzą ciepła z ciepłem uzyskanym przy spalaniu pożywienia w trakcie oddychania. W kilka lat później Lavoisier i Laplace przeprowadzili pierwsze ilościowe badania kalorymetryczne na świnkach morskich. Potwierdziły one w pełni stosowalność zasady zachowania energii również w
4
Wyszukiwarka
Podobne podstrony:
Część III: Termodynamika układów biologicznych gdzie L, M, N są pochodnymi cząstkowymi funkcji g
Część III: Termodynamika układów biologicznych Materiały Pomocnicze do Wykładów z Podstaw
Część III: Termodynamika układów biologicznych ■ AG > O - reakcja przebiega spontanicznie, ale w
Część III: Termodynamika układów biologicznych 2N2 + 502 + 2H20 = 4H+ + 4N03 Standardowa zmiana ent
Część III: Termodynamika układów biologicznych Do opisu wymiany entropii z otoczeniem wygodnie jest
Część III: Termodynamika układów biologicznych Przez dłuższy czas poszukiwano wyjścia z tego problem
Część III: Termodynamika układów biologicznych W przypadku strumieni sprzężonych niektóre strumienie
Część III: Termodynamika układów biologicznych Ldv - współczynnik ultrafiltracji lub osmozy Z faktu
Część III: Termodynamika układów biologicznych dt Na uwagę zasługuje fakt, że występowanie
Część III: Termodynamika układów biologicznych ■ przyjęliśmy liniową
Część III: Termodynamika układów biologicznychPOMIARY KALORYMETRYCZNEWstęp Pomiary kalorymetryczne
Część III: Termodynamika układów biologicznych niższej niż zadana temperatura doświadczenia T°,
Część III: Termodynamika układów biologicznych układu na jednym poziomie może być traktowany jako ca
Część III: Termodynamika układów biologicznych roztworu składnika B i proces się powtarza. W miarę j
Część III: Termodynamika układów biologicznych układach biologicznych. Od tego czasu badania takie
Część III: Termodynamika układów biologicznych r - współrzędna pracy. Należy teraz dla każdego
Część III: Termodynamika układów biologicznych ■ energia swobodna (F) zwana także
Część III: Termodynamika układów biologicznych dH = TdS - Vdp + Pidiij + pjdn } Jeżeli założymy, że
Część III: Termodynamika układów biologicznych fj.i = H-RTlnrij lub m = +
więcej podobnych podstron