
2011-04-13
1
HEMOSTAZA
Zespół mechanizmów zapewniających płynność krwi krążącej
oraz
zdolność do tamowania wypływu krwi z łożyska
naczyniowego, przy jego uszkodzeniu.
Krzepnięcie krwi
naturalny, fizjologiczny proces zapobiegający
utracie krwi w wyniku uszkodzeń naczyń
krwionośnych.
Istotą krzepnięcia krwi jest przejście
rozpuszczonego w osoczu fibrynogenu
w sieć
przestrzenną skrzepu (► fibryny) pod
wpływem trombiny.
Krzepnięcie krwi jest jednym z mechanizmów
obronnych organizmu w wypadku przerwania
ciągłości tkanek.
Krzepnięcie krwi jest procesem enzymatycznym,
uwarunkowanym działaniem czynników
krzepnięcia krwi (enzymów, kofaktorów) oraz
płytek krwi.
Czynniki krzepnięcia można podzielić na 2 grupy:
- czynnik IV – Ca²+
- czynniki o charakterze białek:
•
czynniki zespołu protrombiny (II, VII, IX i X) –
zależne od witaminy K
•
czynniki wrażliwe na działanie trombiny (I, V, VIII,
XIII)
•
czynniki kontaktu (XI i XII)
Czynniki krzepnięcia krwi mogą występować w
postaci nieaktywnej lub aktywnej.
Czynnik VIII jest wytwarzany przez komórki
siateczkowo–śródbłonkowe występujące w
wątrobie i śledzionie oraz w śródbłonku naczyń,
pozostałe powstają w wątrobie i są wydzielane do
krwi.
Niedobór poszczególnych czynników krzepnięcia
krwi powoduje zwolnienie lub zahamowanie
procesu krzepnięcia i prowadzi do powstania skaz
krwotocznych.
Płytki krwi wykazują wielokierunkowe działanie w
procesie krzepnięcia krwi, zwłaszcza w przypadkach
uszkodzenia naczyń krwionośnych.
Są wytwarzane w szpiku kostnym przez megakariocyty.
U osoby zdrowej w 1 mm³ krwi występuje 150 000-
400 000 płytek krwi, a przeciętny okres ich życia
wynosi 8-12 dni.
Nie mają jądra komórkowego; wyróżnia się w nich:
- warstwę zewnętrzną nieziarnistą (hialomer) –
zawierającą wszystkie czynniki krzepnięcia krwi
- warstwę wewnętrzną ziarnistą (glanulomer) –
zawierającą czynniki płytkowe.

2011-04-13
2
Zaburzenia czynności płytek krwi - trombopatia
zmniejszenie ich ilości - trombocytopenia
– obydwa te zaburzenia upośledzają proces
krzepnięcia krwi i mogą powodować występowanie
skaz krwotocznych.
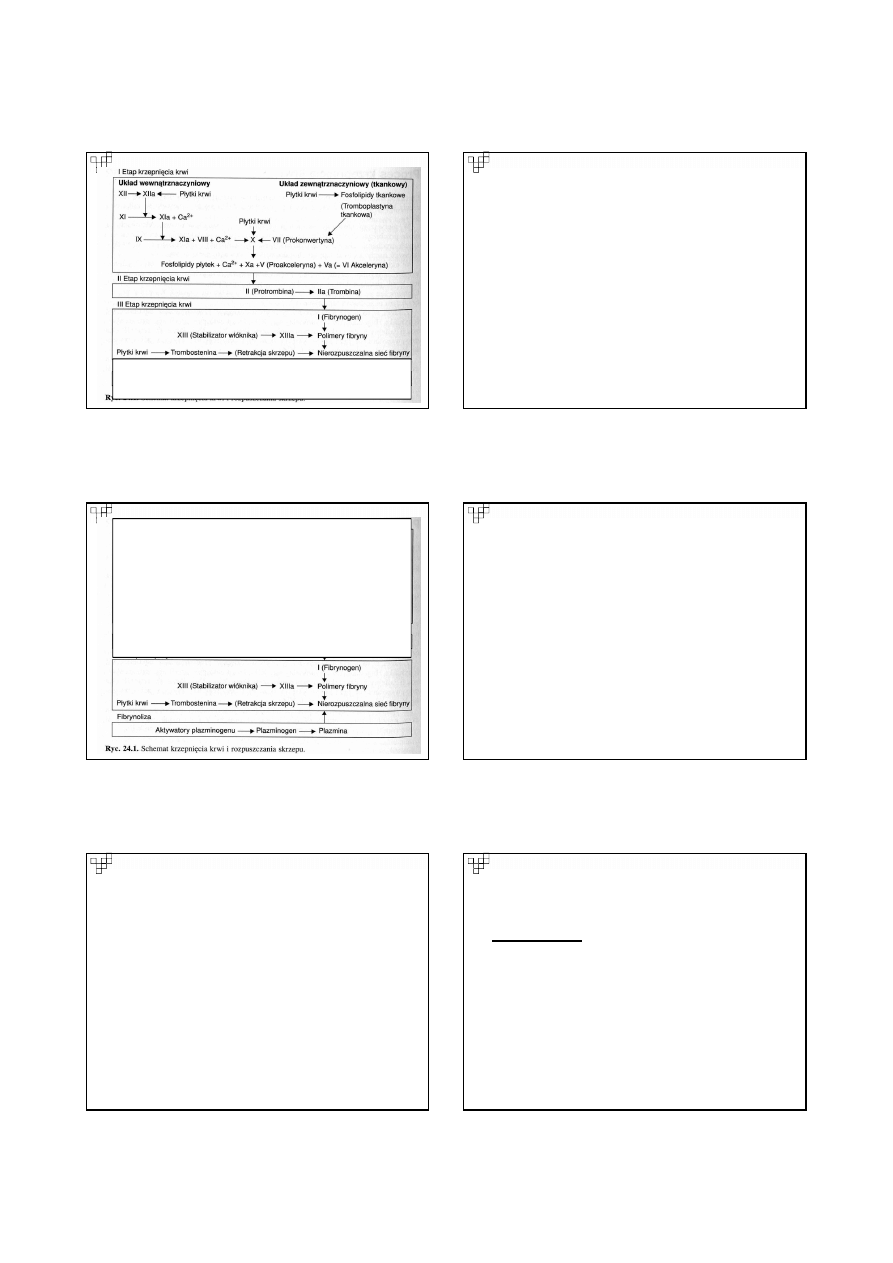
PROCES KRZEPNIĘCIA KRWI
polega na kaskadowej aktywacji czynników
krzepnięcia.
ETAPY:
I.
Aktywacja czynnika X.
Aktywacja ta może przebiegać dwiema różnymi
drogami: w przypadku uszkodzenia naczyń
krwionośnych uruchamia się układ
zewnątrznaczyniowy (tkankowy);
przy nieuszkodzonych naczyniach zostaje
uruchomiony układ wewnątrznaczyniowy.
W układzie zewnątrznaczyniowym na skutek
uszkodzenia naczyń krwionośnych następuje, w
wyniku zetknięcia się z fosfolipidami
uszkodzonych komórek i rozpadu płytek krwi,
przekształcenie czynnika VII –
prokonwertyny, w czynnik aktywny VIIa.
Czynnik ten przy współudziale czynnika IV
(Ca²+) aktywuje czynnik X do Xa.
W układzie wewnątrznaczyniowym następuje
przekształcenie czynnika XII w czynnik
aktywny XIIa, który następnie uruchamia
proces aktywacji kolejnych czynników i
powstanie czynników XIa i IXa. Powstały
czynnik IXa przy współudziale czynników:
VIII, IV (Ca²+) i V oraz jego aktywnej postaci
– aktywuje czynnik X do Xa.
II. W drugim etapie krzepnięcia krwi
wytwarzana jest trombina.
Aktywny czynnik Xa przy współudziale
czynnika IV (Ca²+) oraz czynników V i Va
działa na czynnik II – protrombinę, i
powoduje jego przekształcenie w aktywną
trombinę (czynnik IIa)
III. W trzecim etapie powstaje włóknik (fibryna).
Wytwarzanie włóknika następuje na skutek
rozkładu czynnika I – fibrynogenu, przez
czynnik IIa – trombinę.
W trzecim okresie następuje również stabilizacja
skrzepu na skutek przekształcenia przez
trombinę czynnika XIII w czynnik XIIIa.
Powstały czynnik jest aktywną transpeptydazą i
powoduje zmianę wiązań wodorowych w trwałe
wiązania międzypeptydowe.
Jednocześnie pod wpływem trombosteniny płytek
krwi następuje retrakcja (obkurczanie się)
skrzepu.
2011-04-13
3
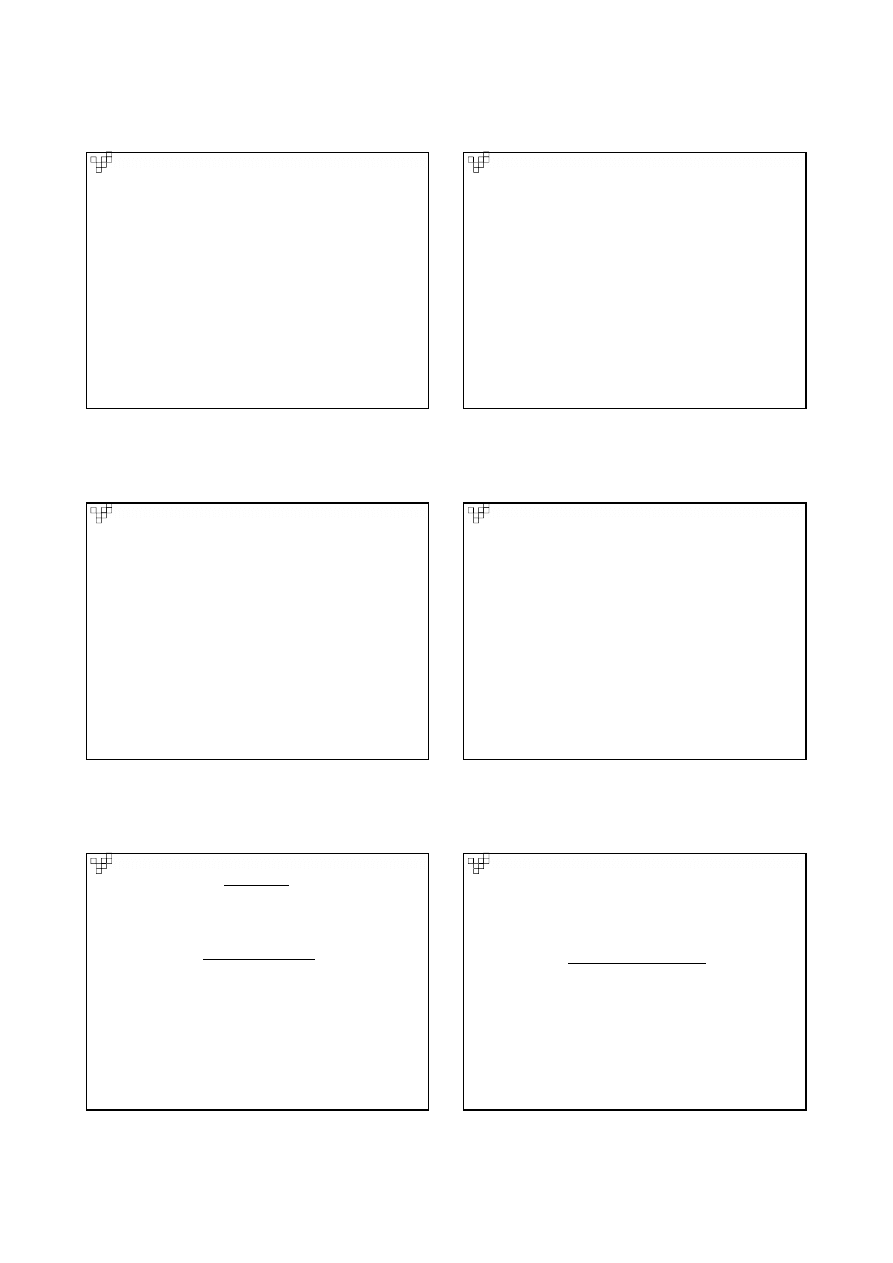
FIBRYNOLIZA
Wytworzony skrzep jest rozpuszczany w procesie
fibrynolizy (proteolityczy rozkład włóknika
skrzepu, zachodzący pod wpływem plazminy).
Plazmina powstaje z ►plazminogenu, który
występuje we krwi jako białko nieaktywne i jest
częściowo wiązany przez włóknik skrzepu.
Przekształcenie może się odbywać pod wpływem
aktywatorów endogennych (występujących w osoczu
krwi i tkankach) lub aktywatorów egzogennych (kinaz
bakteryjnych).
Leki hamujące krzepliwość krwi
(antykoagulanty)
1.
Zmniejszające zawartość składników krwi biorących udział
w procesie krzepnięcia
środki wytrącające jony wapnia (stosowane in vivo)
leki antytrombinowe (heparyna , heparyny
małocząsteczkowe i heparynoidy)
leki antyprotrombinowe (antagoniści witaminy K)
leki defibrynujące (fibrynogenolityczne)
Leki hamujące krzepliwość krwi
antykoagulanty
c.d.)
2.
Leki zwiększające zawartość czynników rozkładających
skrzep
■
leki trombolityczne
■
leki zwiększające fibrynolizę
3.
Leki hamujące agregację płytek krwi
■
leki hamujące aktywność cyklooksygenazy w płytkach krwi
■
leki hamujące agregację płytek krwi przez ADP
(tienopirydyny)
■
leki inaktywujące glikoproteinowe receptory IIb/IIIa
4.
Leki hamujące wytwarzanie płytek krwi
1) Heparyna i jej pochodne
Heparyna –
sulfonowany glikozoaminoglikan,
występujący w zasadochłonnych ziarnistościach
komórek tucznych i jest uwalniana do krwi przy
rozpadzie tych komórek.
Znaczenie heparyny polega na zapobieganiu
powstawaniu skrzepów krwi w łożysku
naczyniowym.
Ponadto przyspiesza rozkład lipoprotein oraz
zmniejsza odczynowość immunologiczną.
2011-04-13
4
Mechanizm hamowania krzepnięcia krwi przez
heparynę :
-
zwiększeniu we krwi aktywności antytrombiny III
-
hamowaniu aktywności czynnika Xa i w mniejszym
stopniu czynników VIIa, IXa, XIa, XIIa i kalikreiny
-
hamowaniu agregacji płytek krwi
Heparyna
jest rozkładana w przewodzie pokarmowym
(podaje się ją podskórnie, dożylnie lub drogą wziewną)
•
w wątrobie ulega biotransformacji do uroheparyny
•
po podaniu dożylnym część heparyny jest wydalana z
moczem w postaci niezmienionej
•
działa krótko, 2-4 godziny
•
efektem silnego hamowania procesu krzepnięcia krwi
mogą być krwawienia
•
w celu zniesienia działania heparyny stosuje się
siarczan protaminy
•
groźnym powikłaniem występującym przy
długotrwałym podawaniu heparyny jest zmniejszenie
liczby płytek krwi
(trombocytopenia)
•
Innym powikłaniem w trakcie terapii heparyną może być
wylew krwi do nadnerczy oraz wystąpienie ich niewydolności
•
Heparyna jest stosowana w postaci soli wapniowej lub
sodowej
WSKAZANIA do stosowania heparyny :
•
zapobieganie powstawaniu zakrzepów w tętnicach i żyłach
przed zabiegami chirurgicznymi i po ich wykonaniu,
•
ostra faza zawału mięśnia sercowego
•
dializa otrzewnowa i przy użyciu sztucznej nerki
•
przetaczanie wymienne krwi
•
plazmafereza
Heparyny małocząsteczkowe
-
otrzymuje się je przez chemiczną lub enzymatyczną
degradację heparyny otrzymanej z tkanek
zwierzęcych
-
Mechanizm działania polega głównie na hamowaniu
aktywności czynnika Xa, w wyniku czego następuje
zwolnienie procesu przekształcania protrombiny w
trombinę.
-
w małym stopniu zwiększają aktywność antytrombiny III
-
w małym stopniu inaktywują aktywną trombinę
-
słabo hamują agregację płytek krwi
Wskazania:
● zapobieganie powstawaniu zakrzepów w stanach
zatorowo-zakrzepowych
● przed i po zabiegach chirurgicznych
Przeciwwskazania:
◙
uczulenie na heparynę
◙
wylewy krwawe do mózgu
◙
zabiegi chirurgiczne na mózgu
◙
duże nadciśnienie krwi
◙
przewlekłe zapalenie wsierdzia
◙
owrzodzenie żołądka i jelit
◙
uszkodzenie wątroby
Działania niepożądane:
◙
trombocytopenia
◙
oraz powikłania, jak przy stosowaniu heparyny
2011-04-13
5
Enoksaparyna
Nadroparyna
Rewiparyna
Dalteparyna
Parnaparyna
Tinzaparyna
Heparynoidy
-
związki o budowie zbliżonej do występujących w organizmie
glikozoaminoglikanów
- mają podobne właściwości do heparyn małocząsteczkowych
i mogą zapobiegać powstawaniu zakrzepów krwi przez
hamowanie aktywności czynnika Xa
■ Sulodeksyd
(glikozoaminoglikan pochodzenia naturalnego)
o działaniu przeciwzakrzepowym, profibrynolitycznym, hipolipemicznym)
postać doustna
■ Danaparoid
(mieszanina glikozoaminoglikanów),
zwiększa hamowanie czynnika Xa przez antytrombinę III
Heparynoidy /Inne
Fondaparynuks
– syntetyczny pentasacharyd
wybiórczo hamuje czynnik Xa przez odwracalne połączenie z
cząsteczką antytrombiny.
* T
1/2 ok..
15 godzin, może być stosowany 1 raz dziennie.
* aktualnie uważa się, że jest skuteczniejszy od heparyn
drobnocząsteczkowych w zmniejszaniu ryzyka wystąpienia żylnej
choroby zakrzepowo-zatorowej u osób poddawanych dużym zabiegom
ortopedycznym, zmniejszając jednocześnie ryzyko małopłytkowości oraz
powikłań krwotocznych.
Leki hamujące aktywność trombiny
Trombina to serynowa proteinaza, odgrywająca
kluczową rolę w:
-
procesie tworzenia skrzepu przez rozkład
fibrynogenu do fibryny
-
aktywacji czynnika VIII do postaci VIIIa i czynnika V
do postaci Va
-
pobudzaniu agregacji płytek krwi
-
stabilizacji włóknika
Aktywność trombiny
in vivo
hamuje
endogenna
■ antytrombina III (AT III)
-
glikoproteid zawierający 425 aminokwasów i 2 mostki
disiarczkowe. Wytwarzana w wątrobie, a następnie
wydzielena do krwi. Jest inhibitorem seryny i zapobiega
powstawaniu skrzepów krwi przez hamowanie aktywności
czynnika IIa (trombiny) oraz czynnika Xa; w mniejszym
stopniu czynników IXa, XIa i XIIa.
Dla celów leczniczych AT III otrzymuje się z krwi ludzkiej.
oraz otrzymane syntetycznie:
■ argatroban
■ biwalirudyna
■ lepirudyna
■ Argatroban odwracalnie wiąże się z trombiną i hamuje
aktywność tego enzymu. Jest stosowany do zapobiegania
agregacji płytek krwi przed wykonywaniem plastyki naczyń
wieńcowych. Może powodować występowanie skazy
krwotocznej
■ Biwalirudyna jest syntetycznym peptydem hamującym
aktywność trombiny. Stosowana u pacjentów poddawanych
angioplastyce. Wykazuje właściwości antykoagulacyjne.
Działania niepożądane to: krwawienie, nudności, ból głowy,
obniżenie ciśnienia krwi
■ Lepirudyna hamuje aktywność trombiny i jest stosowana w
zakrzepowej trombocytopenii wywołanej heparyną
(Długotrwałe stosowanie heparyny prowadzi do zmniejszenia liczby płytek.
Trombocytopenia późna, pojawiająca się po tygodniu stosowania leku, polega
na wytwarzaniu przeciwciał przciwpłytkowych, które stymulują agregację płytek i
tworzą skrzepy w obrębie naczyń).
2011-04-13
6
Antagoniści witaminy K
• Pod wpływem witaminy K w powstających w
wątrobie czynnikach krzepnięcia krwi, wytwarzany
jest kwas γ-karboksyglutaminowy – jego
wytworzenie umożliwia wiązanie Ca²+ i
aktywowanie procesu krzepnięcia krwi.
• W przypadku braku witaminy K lub przy
zablokowaniu jej działania przez związki
antagonistyczne, powstające czynniki są
niepełnowartościowe, nie aktywują procesu
krzepnięcia krwi.
• Pochodne 4-hydroksykumaryny i indan-1,3-dionu.
• Związki te mają budowę chemiczną podobną do witaminy K
i blokują zależną od niej syntezę czynników II, VII, IX i X
Dikumarol
Warfaryna
Fenoprokumon
Acenokumarol
Fenindion
Anisyndion
•
Łatwo wchodzą w interakcje z innymi lekami
• Wąski wskaźnik terapeutyczny
Leki defibrynujące
Leki defibrynujące stosuje się w celu zmniejszenia
ilości fibrynogenu we krwi oraz zapobieżenia
powstawania zakrzepów krwi w obrębie naczyń
krwionośnych
Ankrod – enzym; po podaniu dożylnym rozkłada
fibrynogen na mniejsze cząsteczki, które nie
powodują powstawania zakrzepów, a następnie są
usuwane z krwi na drodze fagocytozy
Batroksobina – enzym zmniejszający stężenie
fibrynogenu we krwi
Leki trombolityczne
• Leki trombolityczne powodują fibrynolizę; rozpuszczają
skrzepy (zawał mięśnia sercowego, zator płucny)
• Wzmagają wytwarzanie plazminy
(plazmina jest endogennym czynnikiem fibrynolitycznym !)
w procesie fibrynolizy przez aktywacje plazminogenu.
■ Urokinaza
■ Streptokinaza
■ Alteplaza
■ Prourokinaza
■ Tenekteplaza
■ Drotrecogin a
postać rekombinowana białka C, regulatora krzepnięcia
■ t-PA
tkankowy aktywator plazminogenu
■
Leki hamujące agregację płytek krwi
Hamowanie agregacji płytek krwi ma na celu
zapobieganie zatorom i zakrzepom występującym
u osób ze zmianami miażdżycowymi w naczyniach
krwionośnych. Właściwe stosowanie leków
hamujących agregację płytek pozwala skutecznie
zapobiegać zawałom mięśnia sercowego, zatorom
mózgu lub zakrzepom w różnych miejscach łożyska
naczyniowego.
Leki hamujące aktywność COX w płytkach krwi
Kwas acetylosalicylowy hamuje cyklooksygenazę płytek
krwi, łącząc się z nią nieodwracalnie. Powoduje to
zablokowanie wytwarzania w płytkach tromboksanu i PGE2,
odpowiedzialnych za występowanie agregacji.
Indobufen ma złożony mechanizm działania.
• Lek blokuje uwalnianie stymulatorów płytkowych –
czynnika płytkowego 3 i 4, ADP, β-tromboglobuliby i
serotoniny
• Jest również odwracalnym COX płytkowej →
zahamowanie syntezy TXA
2

2011-04-13
7
Leki hamujące agregację płytek krwi przez ADP
(tienopirydyny)
ADP jest silnym aktywatorem agregacji płytek krwi
.
■ klopidogrel
■ tiklopidyna
- nieodwracalnie modyfikują strukturę płytkowego
receptora ADP o nazwie P2Y
12
, bezpośrednio i swoiście
hamując wiązanie ADP do receptora i wywoływaną przez
ADP aktywację kompleksu glikoprotein GPIIb/IIIa
-
proleki, z których w wątrobie przy udziale cytochromu
P450 powstają aktywne metabolity, blokujące receptory
ADP na powierzchni płytek.
Działania niepożądane:
- zmiany hematologiczne (agranulocytoza, trombocytopenia)
Leki inaktywujące glikoproteinowe receptory IIb/IIIa
Blokowanie receptora IIb/IIIa jest skuteczną metodą
hamowania agregacji płytek. W lecznictwie stosuje
się:
◘ Abciksimab
- jest monoklonalnym przeciwciałem chimerycznym
inaktywującym receptory IIb/IIIa; stosuje się go łącznie z heparyną i
kwasem acetylosalicylowym do zapobiegania występowaniu zakrzepów
przy wykonywaniu angioplastyki naczyń wieńcowych
◘ Eptifibatid
- wiąże się nietrwale z receptorem IIb/IIIa, po podaniu
dożylnym hamuje agregację płytek
◘ Tirofiban
- lek niepeptydowy, w połączeniu z heparyną jest stosowany
w ostrej niewydolności wieńcowej oraz przy wykonywaniu zabiegów na
naczyniach wieńcowych
Prostaglandyny
Epoprostenol – syntetyczna prostaglandyna
Hamuje agregację płytek krwi oraz rozszerza
naczynia krwionośne.
Jest stosowana w zaburzeniach krążenia
obwodowego, nadciśnieniu płucnym, a także do
zapobiegania krzepnięciu krwi.
Działania niepożądane:
-
krwawienia
-
suchość w jamie ustnej,
-
świąd
-
zaburzenia żołądkowo-jelitowe
-
drgawki, bóle w klatce piersiowej
Leki hamujące wytwarzanie płytek krwi
Anagrelid
• zmniejsza liczbę płytek krwi przez hamowanie dojrzewania
megakariocytów w fazie po wystąpieniu podziału
• nie wpływa na liczbę krwinek białych oraz biochemiczne
parametry krzepnięcia
• stosuje się u osób z nadpłytkowością, wynikającą wtórnie z
procesów rozrostowych w szpiku kostnym, w celu
zmniejszenia liczby płytek krwi i zapobieżenia występowaniu
zmian zakrzepowych
• zachować ostrożność u osób z chorobami serca ze względu
na wykazywane przez lek dodatnie działanie inotropowe
Wyszukiwarka
Podobne podstrony:
Leki układ krzepnięcia krwi cz II
4 LEKI WPŁYWAJĄCE NA UKŁAD KRZEPNIĘCIA KRWI, Ratownictwo medyczne, Farmakologia, Farmakologia
W05-SZ-W05 - Leki działające na układ równowagi krzepnięcia krwi (Krall), Naika, stomatologia, Farma
Leki wpływaj±ce na układ krzepnięcia
1 LEKI WPŁYWAJĄCE NA MECHANIZMY KRZEPNIĘCIA KRWI I HEMATOPOEZĘ
leki wpływające na krzepnięcie krwi, farmakologia(8)
Leki wpływające na układ krwiotworczy i uklad krzepnięcia
14 G07 H05 Pobieranie krwi cz 3 wersja IHiTid 15247 ppt
Krzepniecie krwi, Farmacja, Farmakologia(1), Hemostaza, Układ krwionośny
LEKI STOSOWANE W ZABURZENIACH KRZEPNIÄCIA KRWI, farmakologia
Leki wpływaj±ce na układ krzepnięcia
Leki wpływające na krzepnięcie krwi
Ocena wpływu transfuzji krwi autologicznej na układ krzepnięcia i krwawienie pooperacyjne u pacjentó
Układ oddechowy prezentacja cz 3
więcej podobnych podstron