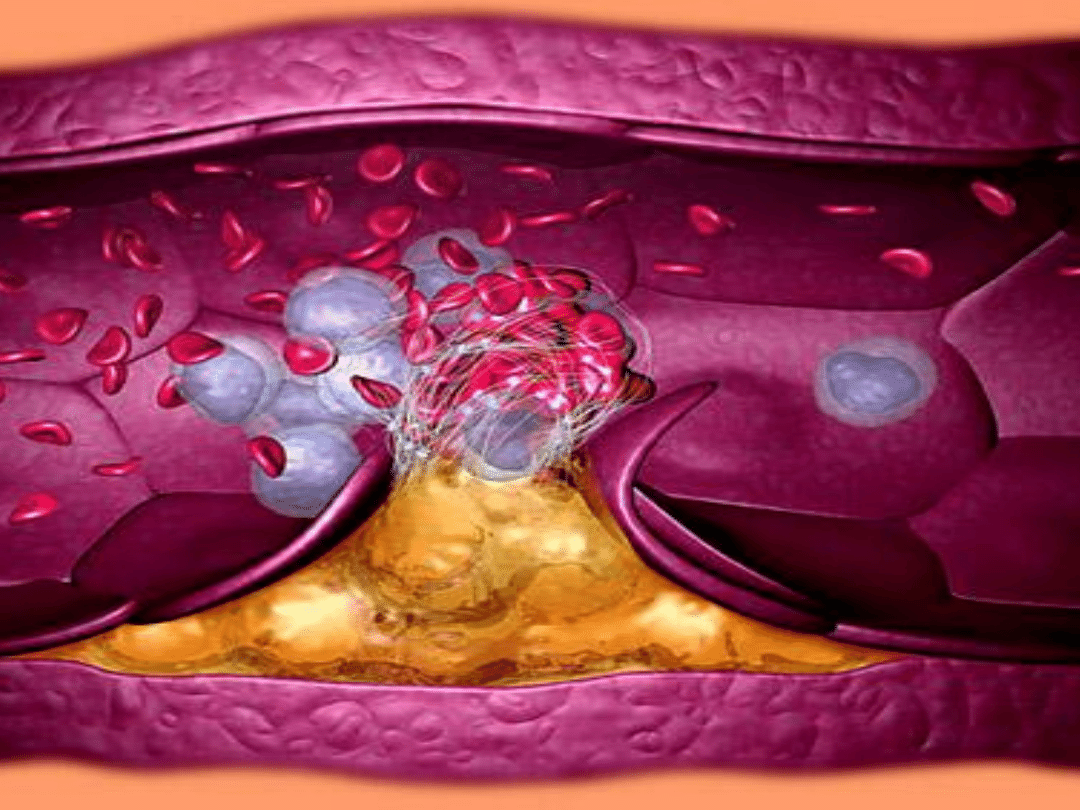
PATOGENEZA MIAŻDŻYCY
Zakład Nadciśnienia Tętniczego
Katedry Nefrologii i Nadciśnienia Tętniczego
Uniwersytetu Medycznego w Łodzi

• Miażdżyca tętnic (łac. atheromatosis, atherosclerosis) (potoczna
nazwa to "arterioskleroza") – przewlekła choroba, polegająca na
zmianach zwyrodnieniowo-wytwórczych w błonie wewnętrznej i
środkowej tętnic, głównie w aorcie, tętnicach wieocowych i
mózgowych, rzadziej w tętnicach kooczyn
• Przyczyną miażdżycy jest odkładanie się złogów cholesterolu w
ścianach naczyo krwionośnych, prowadzące do zmniejszenia lub
całkowitego blokowania światła naczynia.
• Utrudnienie przepływu krwi pociąga za sobą zaburzenia w
funkcjonowaniu wielu tkanek spowodowane ich
niedotlenieniem.
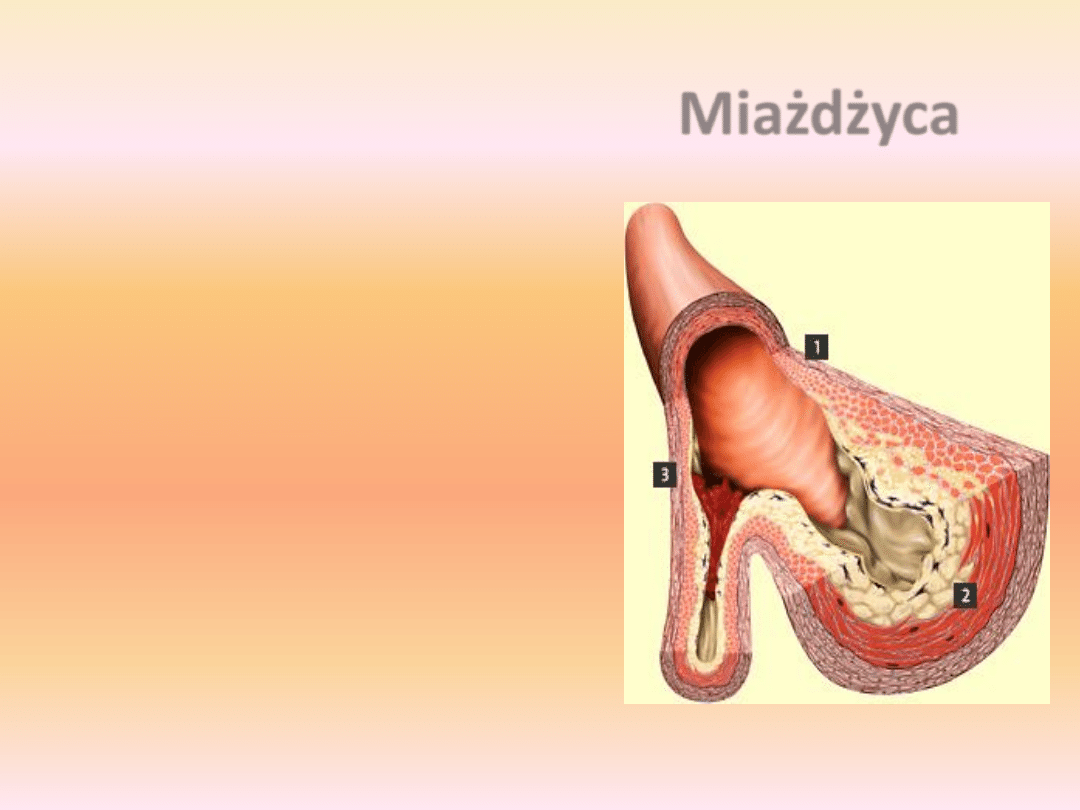
Miażdżyca
Ściana tętnicy składa się z 3 warstw:
•
tkanki łącznej (1)
•
warstwy składającej się z mięśni
gładkich i elastycznej tkanki
łącznej (2)
•
warstwy komórek śródbłonka
naczyniowego, bezpośrednio
kontaktującego się z krwią (3)
Powierzchnia śródbłonka
naczyniowego musi byd
nienaruszona. Bowiem tylko
wtedy możliwy jest przepływ
krwi bez turbulencji
zwiększających ryzyko powstania
zakrzepu krwi.
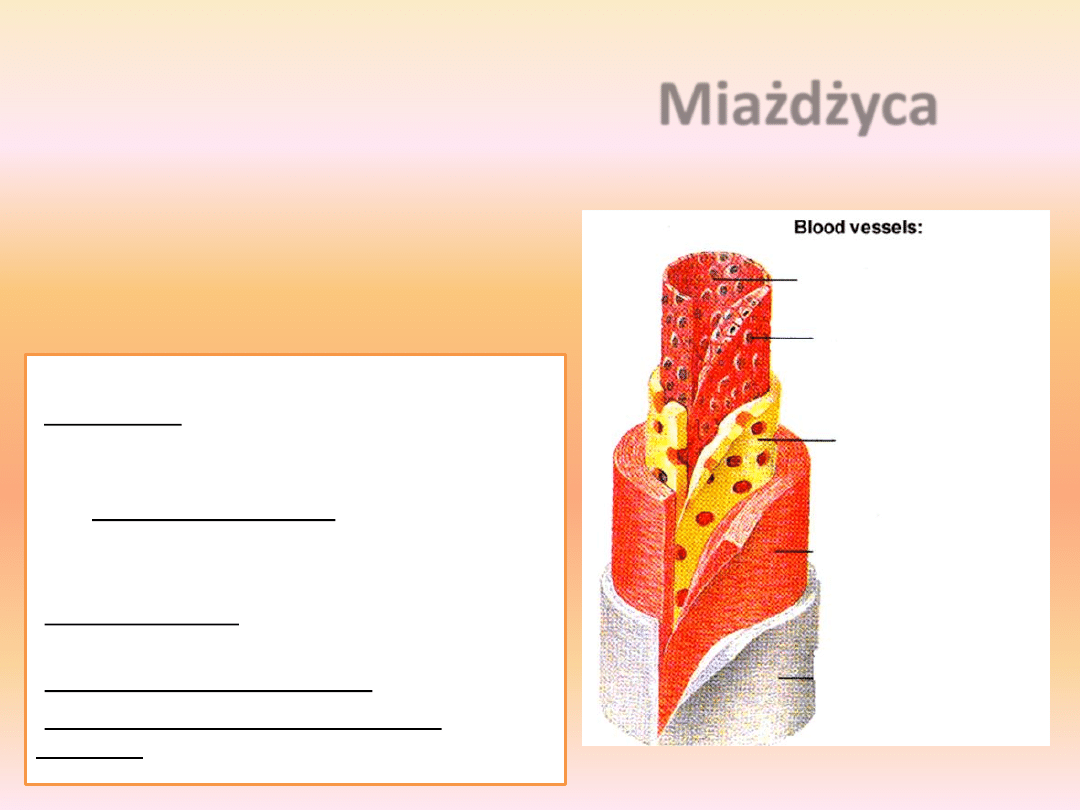
Miażdżyca
światło naczynia
komórki śródbłonka
tunica intima
warstwa komórek
mięśni gładkich
tunica adventitia
Podstawowym pierwotnym
procesem patologicznym leżącym u
podstaw rozwoju blaszek
miażdżycowych jest wywoływana
przez różne czynniki ryzyka
dysfunkcja
śródbłonka.
Należą do nich:
•siły nacisku prądu krwi na ścianę naczyniową
(shear stress
), działające w miejscach
rozdwojenia lub zwiększonej krzywizny tętnic
• towarzyszące hipercholesterolemii, krążące we
krwi lipoproteiny i monocyty
•produkty zaawansowanej glikacji białek
(cukrzyca)
•związki drażniące znajdujące się w dymie
tytoniowym
•noradrenalina i angiotensyna II
•kompleksy immunologiczne i czynniki
infekcyjne
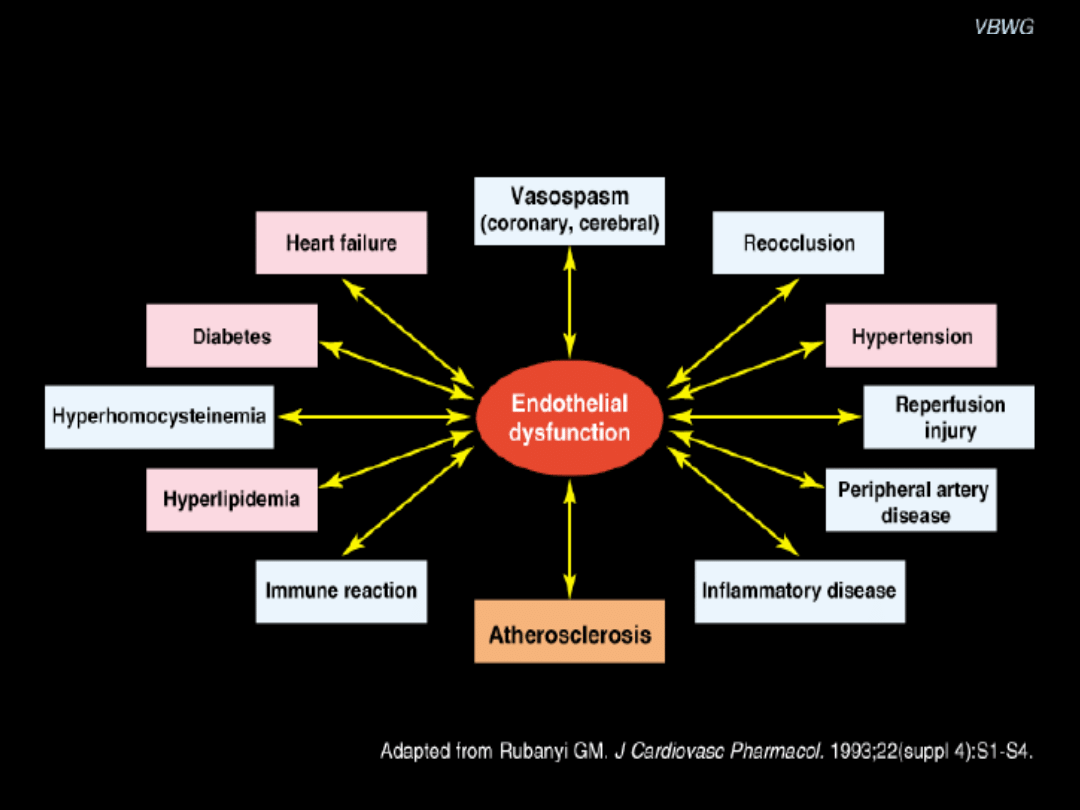
Przyczyny i konsekwencje dysfunkcji śródbłonka
naczyniowego
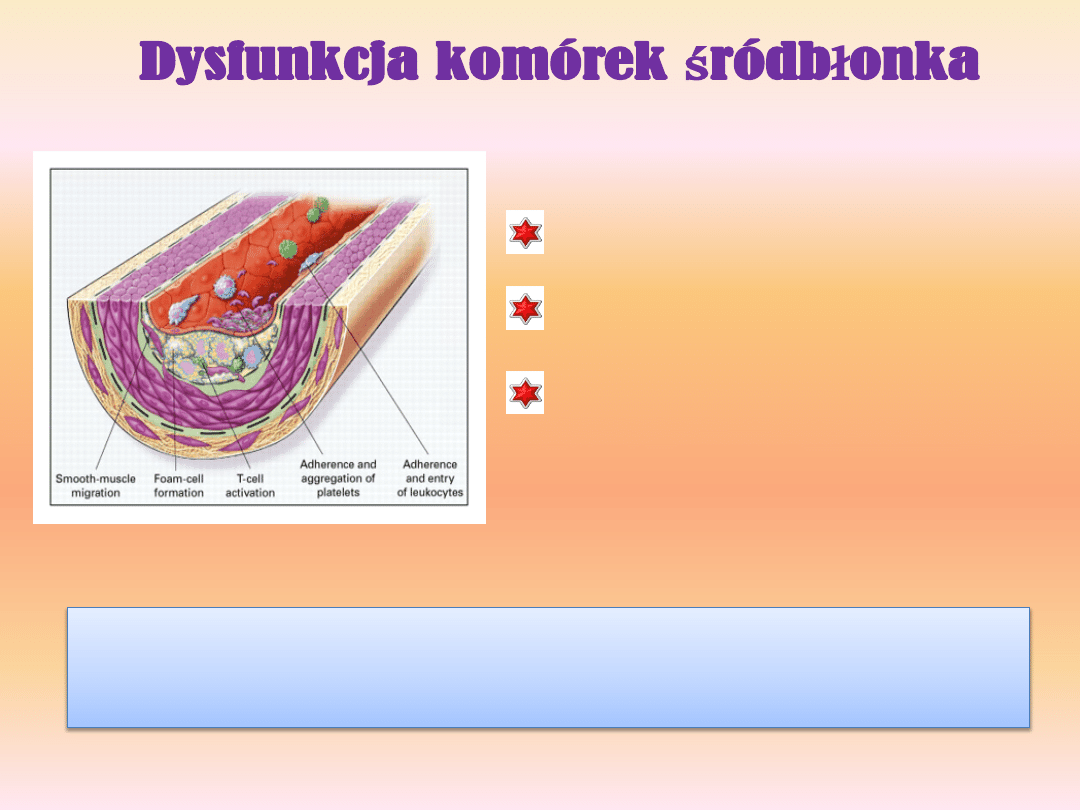
Dysfunkcja śródbłonka charakteryzuje
się
• zwiększoną przepuszczalnością błony
plazmatycznej,
• zmniejszoną syntezą i uwalnianiem
tlenku azotu (NO)
• wzmożoną ekspresją na powierzchni
śródbłonka chemoatraktantów
(substancji, które przyciągają komórki
zapalne) i cząsteczek adhezyjnych
(selektyna P i E, ICAM-1, VCAM-1).
Zmiany te ułatwiają rekrutowanie i późniejszą kumulację komórek zapalnych
w obrębie intimalnej warstwy ściany naczyniowej oraz proliferację komórek
naczyniowych mięśni gładkich.
Etapy rozwoju blaszki miażdżycowej
Oksydowane LDL (oxLDL)
nasilają adhezję
przepływających z
prądem krwi
monocytów do komórek
śródbłonka, zwiększając
tym samym skłonnośd
do rozwoju procesów
zakrzepowych.
Ścisły kontakt monocytów z
warstwą śródbłonka hamuje
sekrecję cząsteczek o
własnościach
fibrynolitycznych (np.
tkankowego aktywatora
plazminogenu [tPA]), a z
drugiej strony stymuluje
sekrecję inhibitora aktywatora
plazminogenu (PAI-1)].
Ponadto oxLDL wywierają
bezpośredni toksyczny
wpływ na komórki
śródbłonka – uszkadzając
go oraz zwiększając
przepuszczalnośd dla
komórek zapalnych i
kolejnych cząsteczek LDL.
Pierwsza faza rozwoju miażdżycy
obejmuje deponowanie, kumulację i
następnie utlenianie cząsteczek lipoprotein o niskiej gęstości (LDL cholesterolu)
w komórkach intimy.
Ogniskowo nagromadzone cząsteczki LDL tworzą
naciek tłuszczowy
, który
stanowi wstępną zmianę miażdżycową.
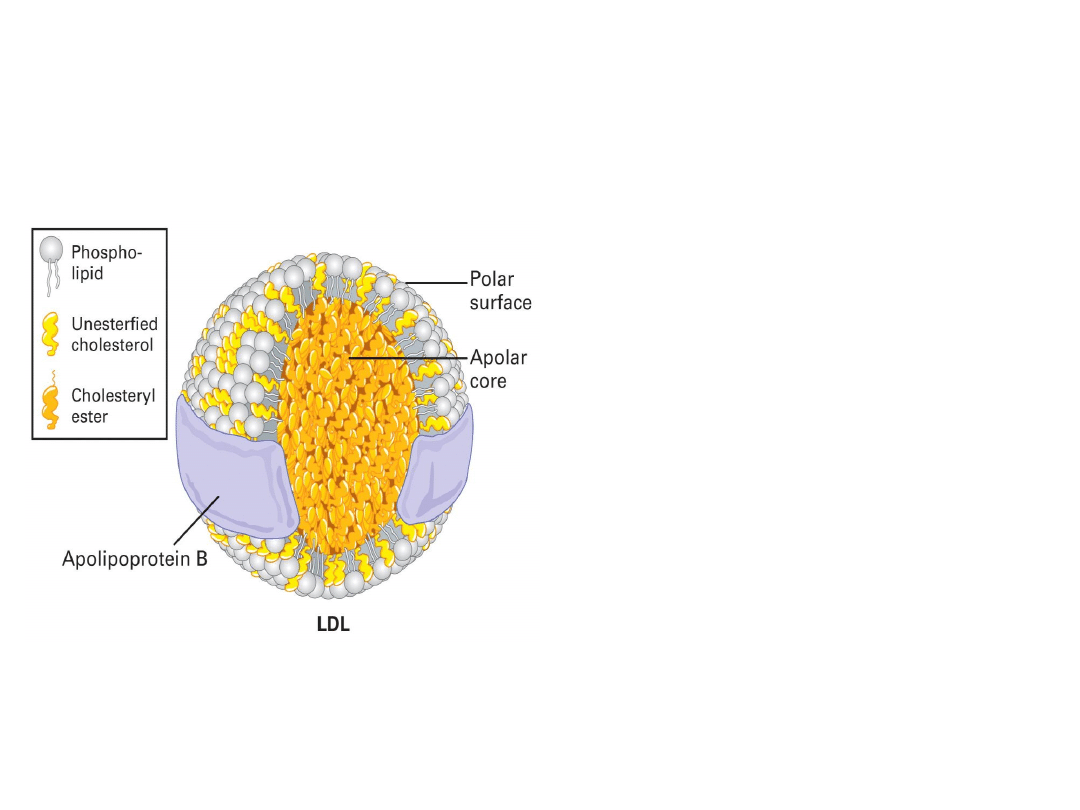
Lipoproteiny osocza są sferycznymi
cząstkami zbudowanymi z
hydrofobowego rdzenia, bogatego w
cholesterol i triglicerydy oraz z płaszcza
utworzonego z apolipoprotein (białka),
fosfolipidów i wolnego
(niezestryfikowanego) cholesterolu.
Gęstośd względna oraz średnica cząstki
zależą od składu chemicznego.
Im większa zawartośd apolipoprotein, tym
mniejsza średnica cząstki (białko
wykazuje duży stopieo upakowania)
oraz wyższa gęstośd względna (białko
posiada dużą masę cząsteczkową w
stosunku do lipidów). Najwyższą
zawartością apolipoprotein cechują się
lipoproteiny o dużej gęstości (HDL), a
najniższą chylomikrony.
LIPOPROTEINY
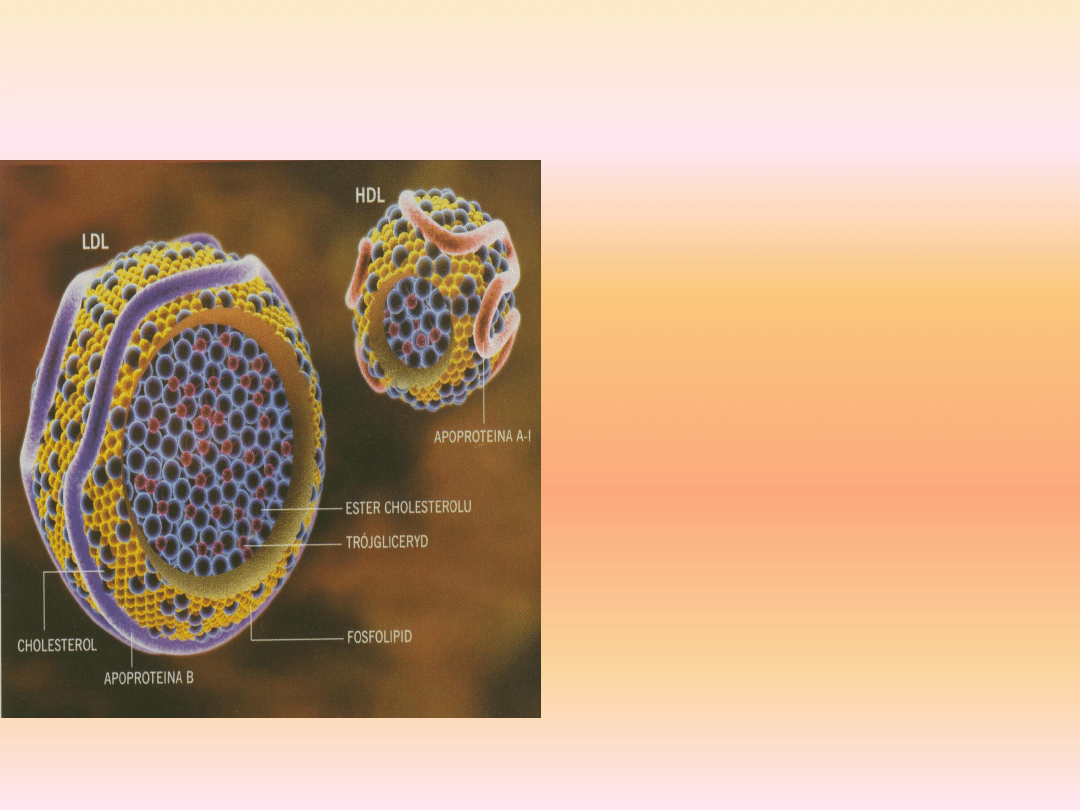
Głównym składnikiem lipidowym LDL jest
cholesterol w formie zestryfikowanej i
wolnej, który za ich pośrednictwem
przedostaje się do tkanek obwodowych,
służąc tam m.in. do syntezy błon,
prowitaminy D oraz hormonów
steroidowych.
Apolipoproteina B-100 pokonuje drogę od
wątroby, gdzie zostaje wbudowana do
VLDL, poprzez IDL i LDL do tkanek
obwodowych, w których jej interakcja z
receptorem dla apoB/E (receptor
wysokiego powinowactwa) warunkuje
prawidłowy klirens LDL.
Cholesterol LDL (low-density lipoprotein)
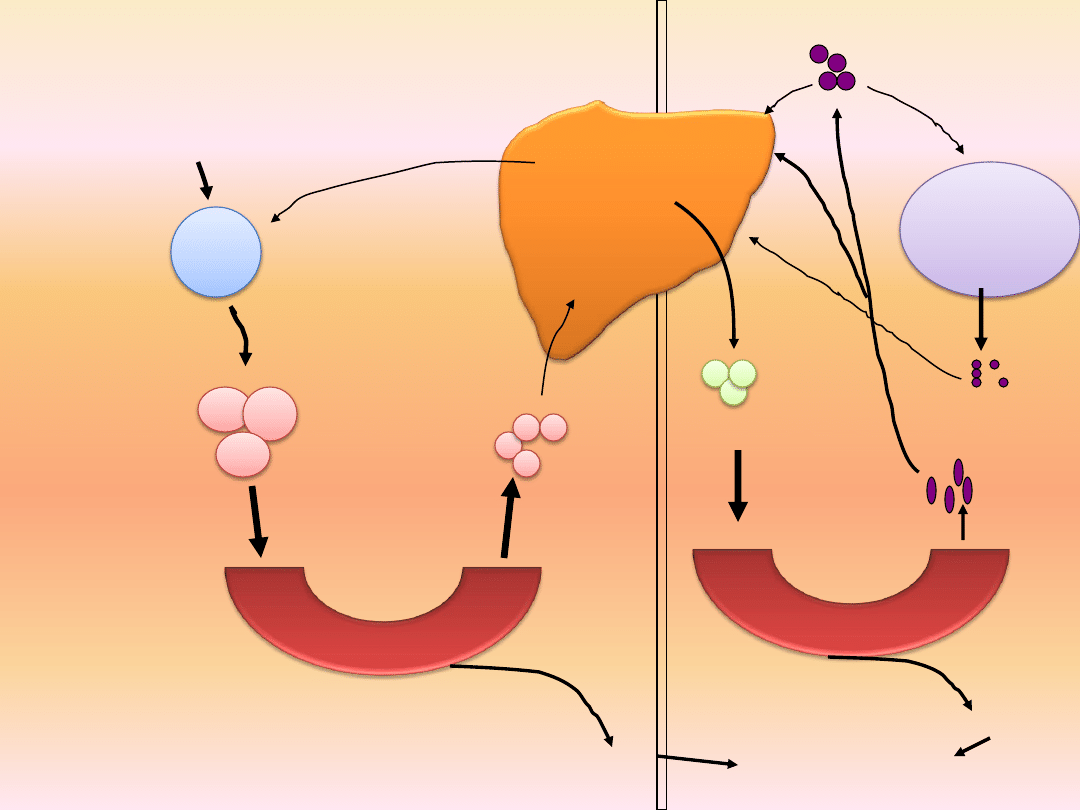
Tłuszcz
pokarmowy
Jelito
cienkie
Naczynia
Lipaza
Lipoproteinowa
WKT
Adipocyty,
mięśnie
chylomikrony
chylomikrony
resztkowe
VLDL
LPL
WKT
Tkanki
poza-
wątrobowe
IDL
HDL
LDL
Endogenny
cholesterol
Egzogenny
cholesterol
Kwasy
żółciowe
Wątroba
Y
Y
Y
Y
LDLR
LDLR
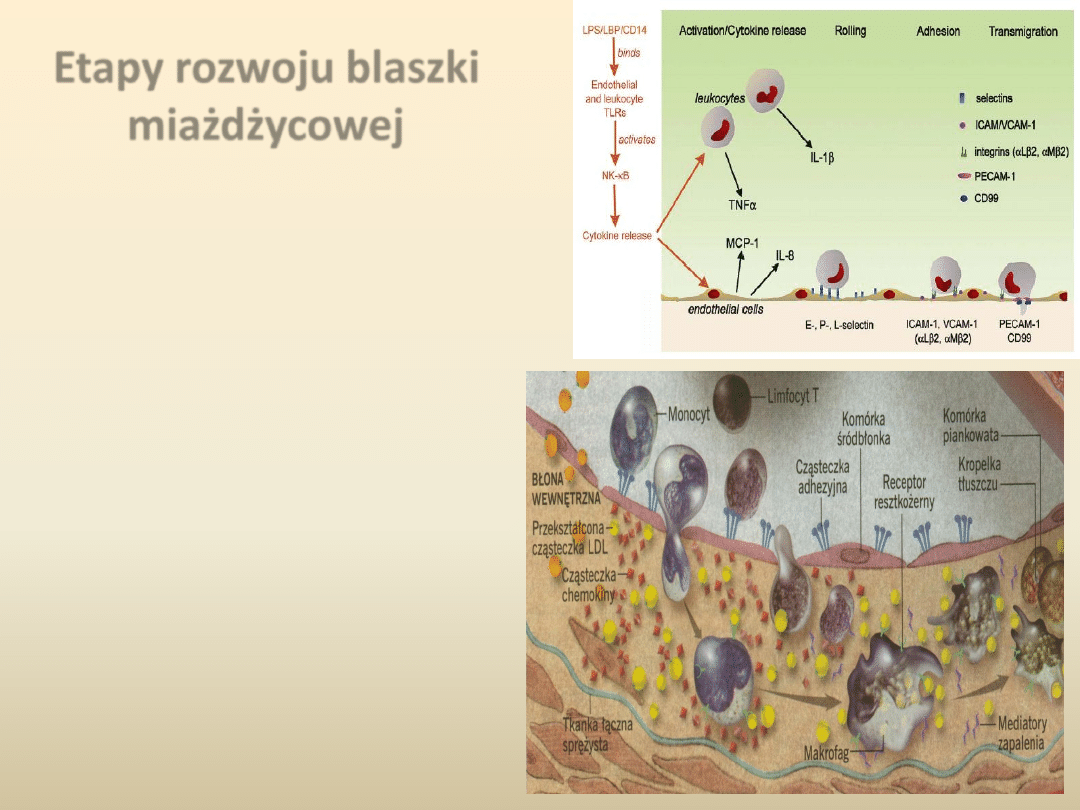
Etapy rozwoju blaszki
miażdżycowej
Druga fazę rozwoju miażdżycy stanowi
rekrutacja komórek zapalnych,
monocytów i limfocytów T, które
przyciągane są do śródbłonka przez
2 rodzaje cząsteczek adhezyjnych
VCAM-1 i ICAM-1. Struktury te
wywołują adhezję monocytów oraz
limfocytów T do warstwy naczynia.
Komórki te migrują następnie z
powierzchni śródbłonka do ściany
tętniczej w towarzystwie innego
zestawu białek, znanych jako
chemotaktyczne cytokiny lub
chemokiny, z których najlepiej
poznano białko chemotaktyczne dla
monocytów- 1 (MCP-1).
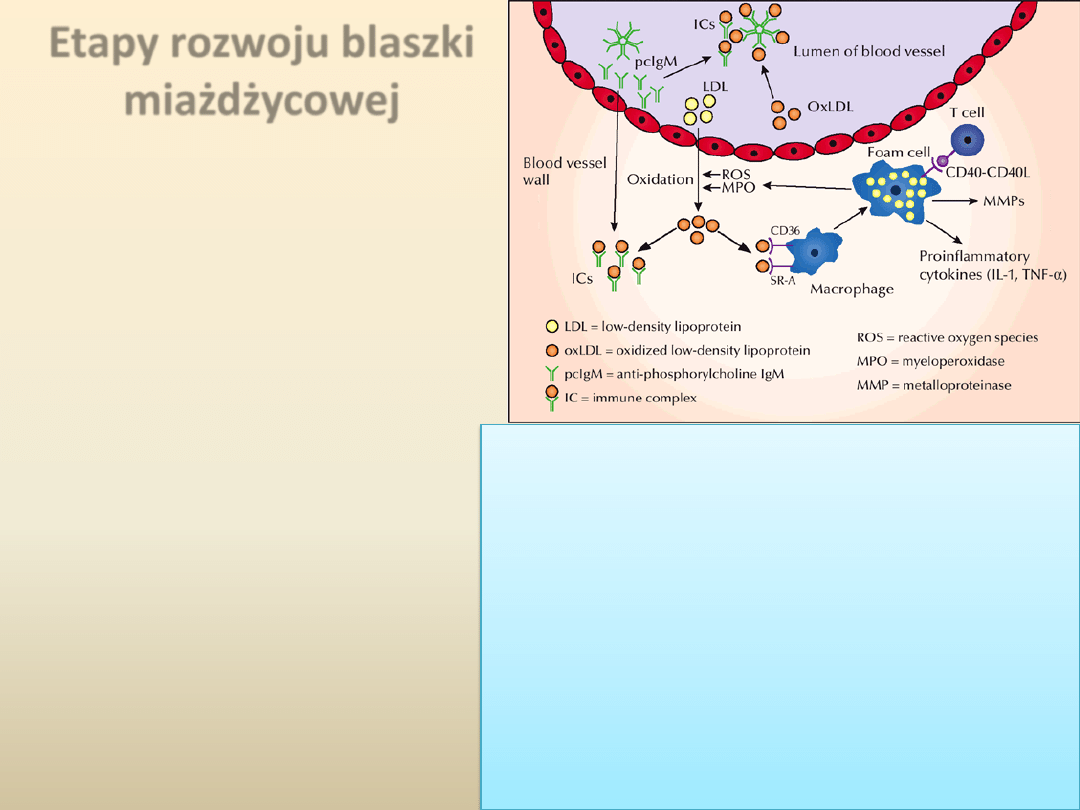
Etapy rozwoju blaszki
miażdżycowej
Trzecią fazę w rozwoju blaszki
miażdżycowej stanowi masywna
migracja monocytów do ściany tętnicy.
Komórki te wykazują ekspresję
receptora o charakterze
scavenger
(zmiatacz),
który wiąże oxLDL.
W następstwie komórki te
przekształcają się w makrofagi i
ulegają podziałom pod wpływem
makrofagowego CSF.
Związane z powierzchnią komórki
oxLDL
pochłaniane są przez
makrofagi, które pod mikroskopem
ujawniają się jako obładowane lipidami
komórki piankowate
, a ich skupienia
widoczne pod warstwą śródbłonka
określa się jako
nacieczenie
tłuszczowe
.
Zmodyfikowane LDL zwiększają następnie aktywność
powstałych komórek piankowatych, a także mogą
powodować rozszerzenie się procesu zapalnego poprzez:
•
stymulację replikacji makrofagów i migrację kolejnych
monocytów do blaszki miażdżycowej
•
wzrost ekspresji metaloproteinaz i hamowanie ekspresji
enzymu syntazy tlenku azotu, odpowiedzialnego za syntezę
tlenku azotu
Uwolnione przez makrofagi mediatory zapalne –
interleukina 1b (IL-1b), czynnik martwicy nowotworow –
TNF-α (
tumor necrosis factor α
) i
M-CSF(czynnik
aktywacji kolonii makrofagów
) nasilają wiązanie LDL do
śródbłonka i mięśniówki naczynia.
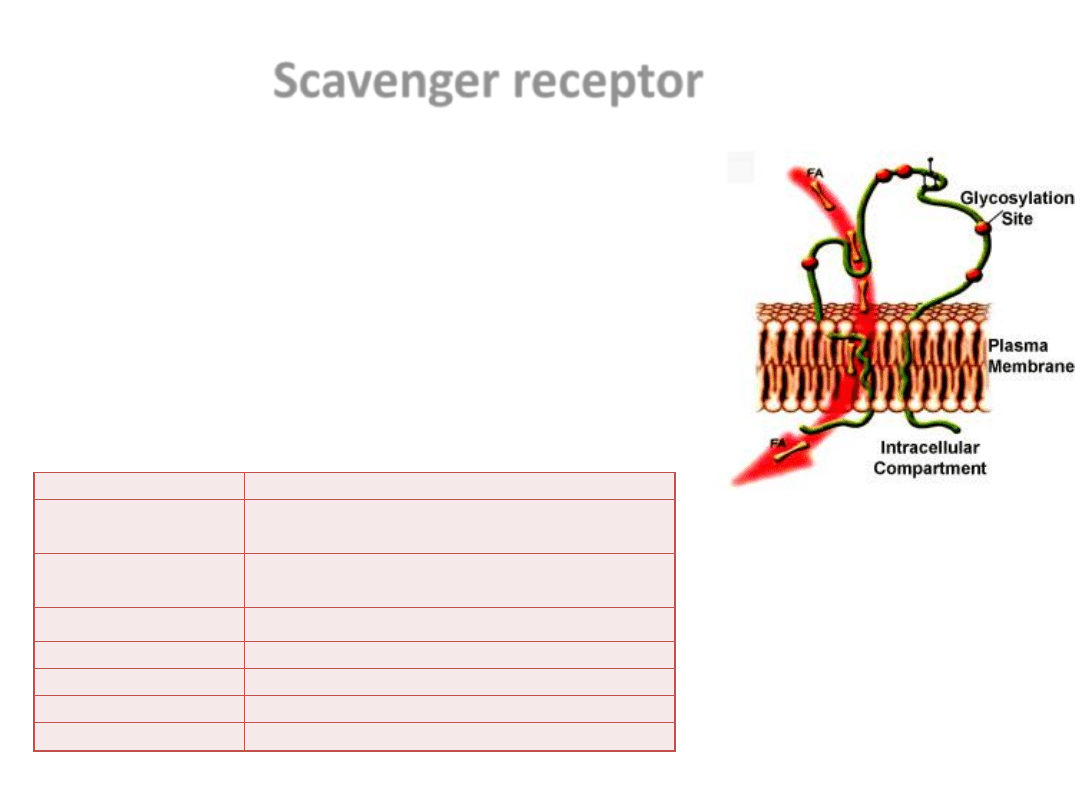
Scavenger receptor
Przyłączanie oxLDL przez makrofagi, poprzedzające ich
fagocytozę odbywa się z udziałem różnorodnych
receptorów znajdujących się na jednojądrowych
komórkach fagocytujących, w tym receptorów typu
scavenger.
Receptory te (SR – scavenger receptor) są grupą białek
wiążących chemicznie lub oksydacyjnie
zmodyfikowane lipoproteiny, polianiony i komórki
ulegające apoptozie.
Receptor CD36
Rodzaj receptora SR
Typ ligandu
SR-AI
SR-AII
acetylowane i utlenione
LDL, polianiony i martwe komórki
CD36
receptor fagocytujący wiąże m.in. acetylowane
i utlenione LDL, fosfatydyloserynę i komórki apoptotyczne
SR-BI
lipoproteiny o dużej gęstości HDL (high density lipoproteins)
SR-CI
acetylowane LDL i polianiony
CD68
(makrosialina) oxLDL
SR LOX-1
oxLDL i polianiony
SR-F
oxLDL, acetylowane LDL i polianiony
Tab.1. Rodzaje receptorów SR zaangażowanych w tworzenie „komórek piankowatych”
Etapy rozwoju blaszki miażdżycowej
Dalszy proces miażdżycowy przebiega z udziałem komórek linii monocytarno-makrofagowej.
Obecne w błonie wewnętrznej oprócz makrofagów liczne limfocyty T aktywują komórki
piankowate, które z kolei wytwarzają wolne rodniki tlenowe oraz czynniki wzrostowe;
•
czynnik wzrostu fibroblastów (FGF, fibroblast growth factor)
•
insulinopodobny czynnik wzrostu (IGF, insulin growth factor)
•
transformujący czynnik wzrostu (TGF, transforming growth factor)
•
interleukinę 1 (IL-1)
•
czynnik martwicy guza (TNF-α, tumor necrosis factor)
Mediatory te stymulują komórki mięśni gładkich do migracji z warstwy mięśniowej do ogniska
miażdżycowego.
Komórki ulęgają tam proliferacji i częściowemu przekształceniu w histiomiocyty produkujące
elementy włókniste tkanki łącznej (elastyna, kolagen).
Komórki m. gładkich naczyo i elementy włókniste tkanki łącznej stopniowo wrastają oraz
otaczają rdzeo lipidowy blaszki, tworząc utwardzony zrąb łącznotkankowy.

Blaszka miażdżycowa
Ukształtowana blaszka miażdżycowa jest zbudowana z włóknistej okrywy, która
zamyka centralnie położony rdzeo. Pokrywa zapewnia strukturalną
integralnośd zmiany miażdżycowej, natomiast rdzeo złożony z
pozakomórkowych lipidów jest miękki i silnie trombogenny.
Destabilizacja blaszki miażdżycowej
Aktywacja komórek zapalnych może w przeważającym stopniu destabilizowad ogniska
miażdżycowe, czego wyrazem są rozpoczynające się destrukcyjne procesy z udziałem
tych komórek, szczególnie w obszarze brzeżnym zmiany miażdżycowej, mogące
osłabiad pokrywę blaszki.
Destabilizacja blaszki
miażdżycowej
limfocyty T
INF-γ
kolagen
proliferacja
INF-γ, TNF-α, IL-1, MCSF, oxLDL,
makrofagi,
komórki mięśni
gładkich
MMP
aktywacja
uwalnianie
degradacja kolagenu, elastyny
Zwiększona aktywnośd
komórek zapalnych →
apoptoza komórek m.
gładkich → zmniejszona
mechaniczna odpornośd
pokrywy blaszki
Destabilizacja blaszki miażdżycowej
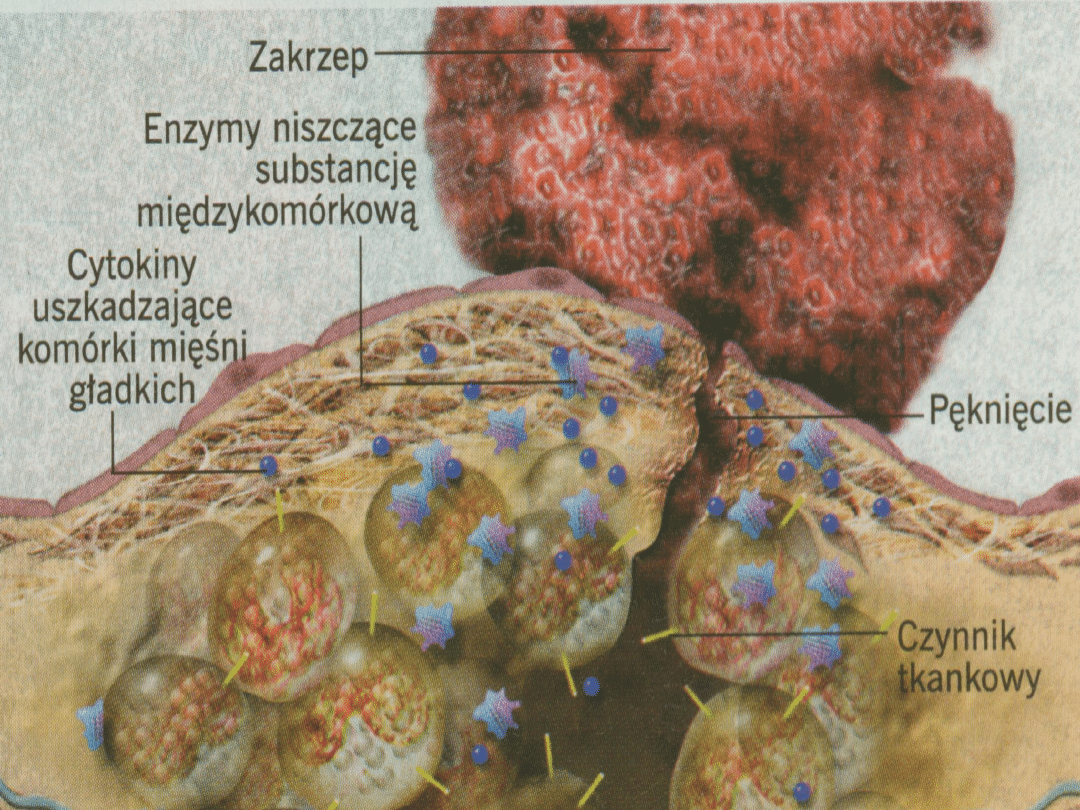
Pękanie blaszki miażdżycowej
Aktywny
proces działania
enzymów proteolitycznych
uwalnianych z makrofagów na
pokrywę włóknistą
Bierne
pękanie blaszki związane z
naprężeniami okrężnymi i podłużnymi,
działającymi na najcieosze miejsce otoczki
włóknistej, w punkcie przylegania do
„prawidłowej” ściany naczynia
Progresja blaszki miażdżycowej, związana z ewolucją od stabilnej blaszki do ostrego incydentu
wieocowego, zależy od lokalnych i systemowych czynników trombogennych i równowagi między układem
krzepnięcia i fibrynolizy.
Zasadniczymi trombogennymi składnikami blaszki miażdżycowej są kolagen i bogatolipidowy rdzeo z dużą
zawartością czynnika tkankowego. Kiedy włóknista pokrywa blaszki ulega rozerwaniu, ekspozycja
pochodzących z krążącej krwi czynników krzepnięcia (zwłaszcza VIIa i Xa) na czynnik tkankowy, zlokalizowany
w blaszce miażdżycowej, powoduje rozszczepienie protrombiny do trombiny.
Proces ten inicjuje krzepnięcie, deponowanie fibryny i aktywację płytek, prowadząc ostatecznie do
wytworzenia zakrzepu. Adhezja płytek i ich aktywacja powoduje uwalnianie tromboksanu A2, serotoniny,
ADP, PAF, trombiny i czynnika tkankowego, stymulujących dalsze gromadzenie się płytek, narastanie zakrzepu i
w koocu zamknięcie zwężonej tętnicy.
Procesy reparacyjne w stabilizacji blaszek
miażdżycowych
Komórki uszkodzonego śródbłonka, płytki krwi i makrofagi uwalniają
płytkopochodny czynnik wzrostu
(PDGF, platelet - derived growth factor )
wywołujący silne właściwości proliferacyjne. Wszystkie czynniki wzrostowe
rozpoczynają procesy naprawcze, które przeważają w tym okresie rozwoju
blaszki.
Zgodnie z obecnymi poglądami o stabilności blaszek miażdżycowych decyduje
przewaga procesów reparacyjnych nad zapalnymi
. W wyniku procesów
reparacyjnych blaszka zwiększa swoją całkowitą objętośd, ale dzięki
uzyskanej sztywności i stłumieniu odczynu zapalnego może wykazywad
mniejsza skłonnośd do pękania.
Wtórne zmiany blaszek miażdżycowych
Wraz z rozwojem zmian miażdżycowych w obrębie blaszki powstają liczne
siatki drobnych naczyo krwionośnych połączonych
z vasa vasorum tętnic.
Przez te naczynia leukocyty penetrują i opuszczają ogniska miażdżycowe.
Naczynia te są również źródłem krwotoków do wnętrza blaszki.
Utworzone blaszki miażdżycowe często gromadzą
wapo
. Za jego kumulacje
odpowiedzialne są wyspecjalizowane białka wiążące wapo np.:
osteokalcyna, osteopontyna i morfogenetyczne białka, które, podobnie jak
w kości, lokalizują się w zmianie miażdżycowej.
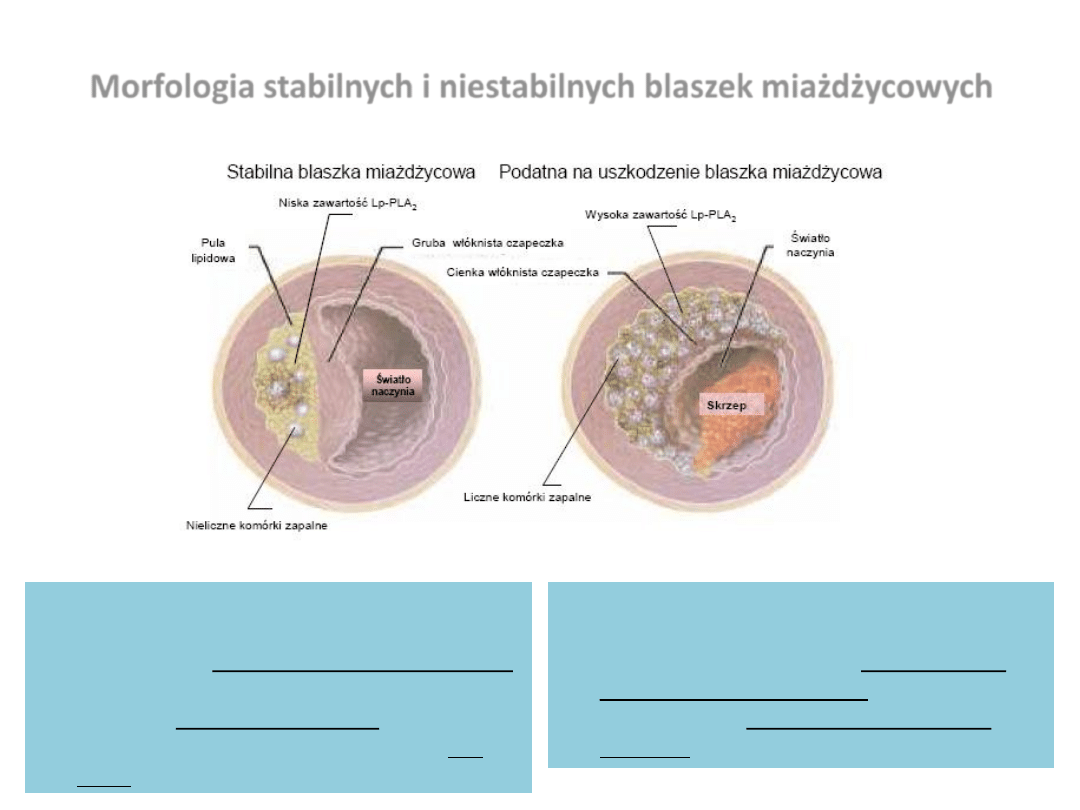
Morfologia stabilnych i niestabilnych blaszek miażdżycowych
Blaszki miażdżycowe u pacjentów ze stabilną
dławicą piersiową są zazwyczaj nieaktywne
biologicznie z przewagą komórek m. gładkich
nad makrofagami, limfocytami T i komórkami
tucznymi. Ryzyko ich pęknięcia bądź
owrzodzenia i wytworzenia skrzepliny jest
małe.
Blaszki miażdżycowe w ostrych zespołach
wieocowych cechują się zwiększoną
aktywnością biologiczną, z gromadzeniem
licznych komórek zapalnych i dużą
gotowością do gwałtownego zamknięcia
naczynia.
koncentryczne zwężanie naczynia
ekscentryczne zwężanie naczynia
Podłoże zapalne miażdżycy
W ostatnich latach wyniki wielu badao coraz wyraźniej wskazują, że miażdżyca
jest procesem o
charakterze zapalnym
.
Koncepcję roli przewlekłego procesu zapalnego w miażdżycy potwierdza
szereg obserwacji:
miażdżycy towarzyszą podwyższone poziomy parametrów zapalnych,
zwłaszcza białka C-reaktywnego (CRP)
miażdżycowe tętnice produkują szereg enzymów hydrolitycznych,
molekuły adhezyjne, cytokiny i czynniki wzrostu podobnie jak obserwuje
się to w innych przewlekłych stanach zapalnych
komórki stwierdzane we wczesnych zmianach miażdżycowych (monocyty,
makrofagi, limfocyty T) są komórkami typowo zapalnymi
Istnieją przekonujące kliniczne i eksperymentalne dowody, że podczas tego
przewlekłego procesu zapalnego nasila się produkcja reaktywnych
pochodnych tlenu (ROS), wynikająca z braku równowagi pomiędzy syntezą
ROS a neutralizującymi antyoksydatywnymi mechanizmami obronnymi.
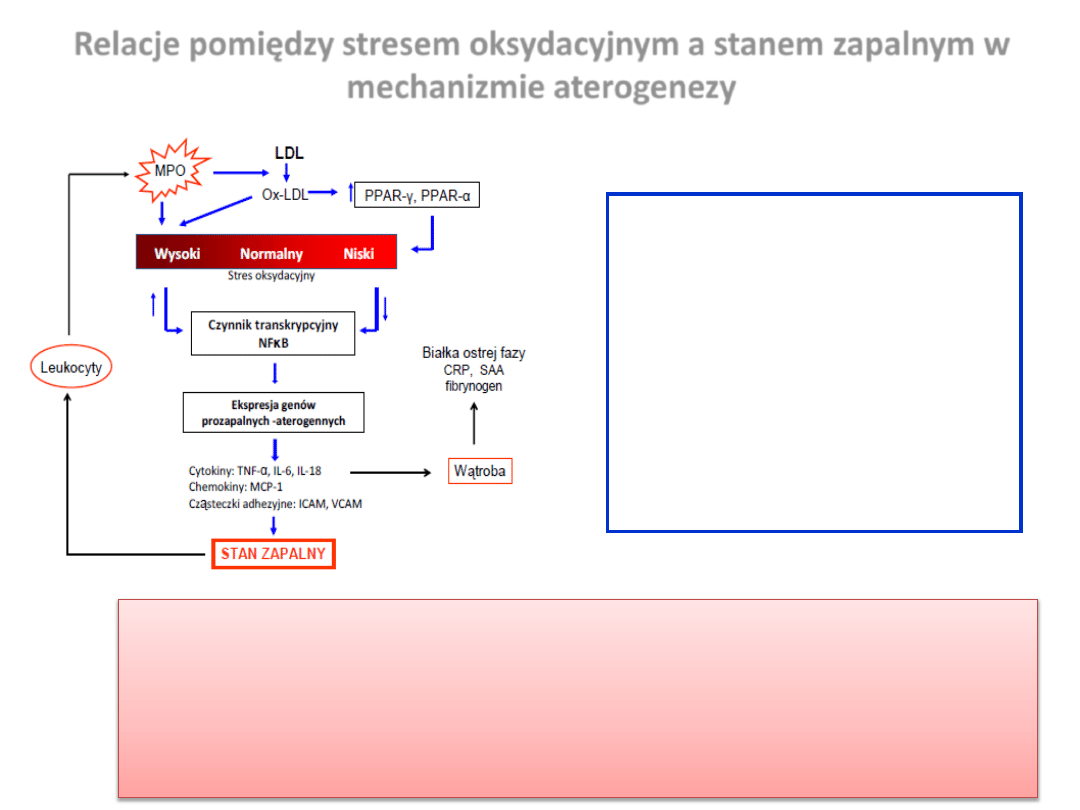
Relacje pomiędzy stresem oksydacyjnym a stanem zapalnym w
mechanizmie aterogenezy
Stres oksydacyjny i reaktywne formy tlenu
(RFT) stanowią drugorzędowy przekaźnik
sygnałów zaangażowanych w regulację
ekspresji prozapalnych genów i ich
produktów takich jak: cytokiny i
molekuły adhezyjne.
Zwiększona ekspresja tych genów promuje
infiltrację monocytów do ściany
naczynia.
Proces ten prowadzi do nasilenia lokalnego
stanu zapalnego i w konsekwencji do
dysfunkcji śródbłonka naczyniowego.
Kluczowym elementem tego mechanizmu wydaje się byd jądrowy czynnik transkrypcyjny NFκB , należący
do rodziny czynników transkrypcyjnych wrażliwych na stres oksydacyjny. Jest on aktywowany przez wiele
różnych czynników, wśród których najważniejsze wydają się koocowe produkty peroksydacji lipidów oraz
prozapalne cytokiny.
Z drugiej strony stymulacja receptorów aktywowanych przez proliferator peroksysomów (PPAR), hamuje
ekspresję prozapalnych genów kodujących cytokiny, metaloproteinazy macierzy (MMP) oraz białka ostrej
fazy poprzez regulację aktywności NFκB
Zakażenie w etiologii miażdżycy
Badania serologiczne, a także niektóre obserwacje epidemiologiczne sugerują, że w aterogenezie pewną rolę
odgrywad mogą rolę bakterie lub wirusy:
• Chlamydia pneumoniae
• Helicobacter pylori
• cytomegalowirusy
• wirusy Herpes simplex i wirusy Hepatitis A
W ludzkich blaszkach miażdżycowych wykrywano obecnośd tych mikroorganizmów, a w surowicy pacjentów z
chorobą wieocową stwierdzano skierowane przeciwko nim przeciwciała.
Możliwe mechanizmy aterogenne związane z zakażeniem obejmują, m.in.:
•
bezpośrednie patogenne inwazje komórek tętnic
•
przewlekłe zakażenia innych obszarów ustroju, prowadzące do produkcji mediatorów
aterogenezy
•
mechanizmy o charakterze autoimmunologicznym, wywołane przez wcześniejszą ekspozycję
patogenów na ustrojowe systemy odpornościowe
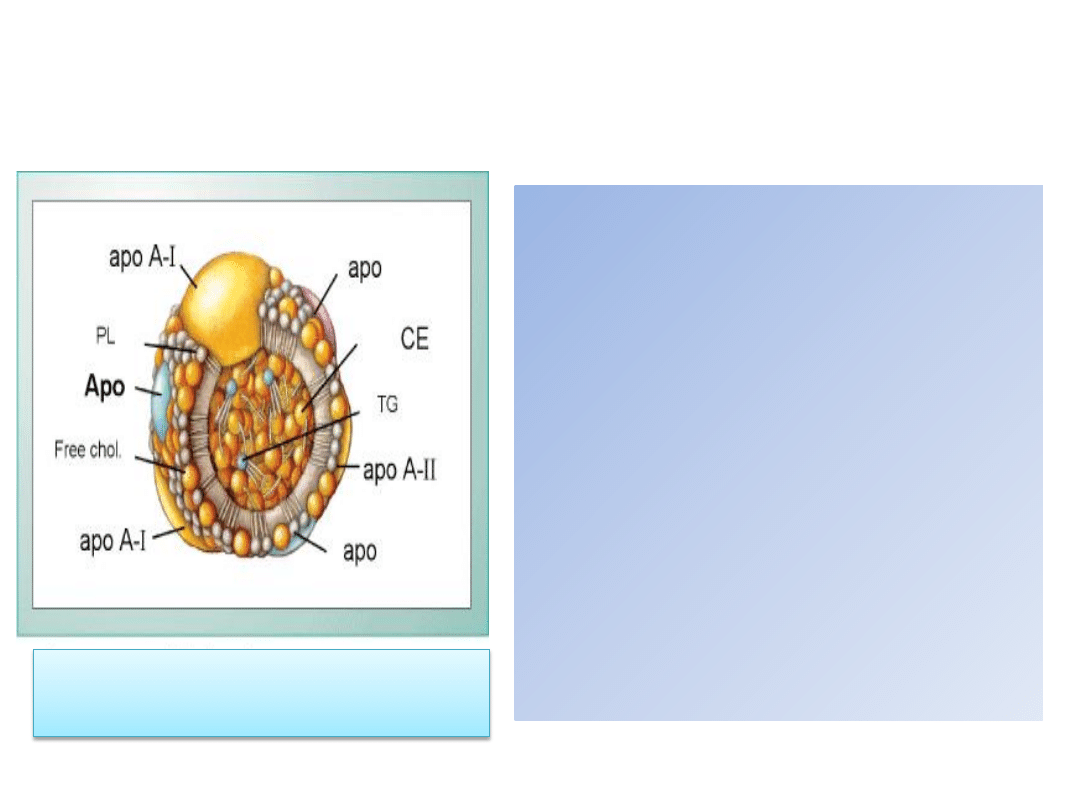
Cholesterol HDL (high-density lipoprotein)
Lipoproteiny o wysokiej gęstości stanowią
frakcję cholesterolu uzyskiwaną w wyniku
ultrawirowania lipoprotein surowicy.
Wysoka gęstośd HDL wiąże się ze znaczną
zawartością apolipoprotein (stanowiącą aż
55% całej cząsteczki), w skład których
wchodzą: apo A-I, apo A-II, apo C-III, apo
C-I, apo D.
Pozostała częśd cząsteczki HDL to lipidy (45%),
w tym: 25% to fosfolipidy, 20% —
cholesterol, a 5% — triglicerydy.
Obecnośd wolnego cholesterolu w rdzeniu
cząsteczek HDL zwiększa ich zdolnośd do
wiązania cholesterolu z innych lipoprotein.
Apo = apolipoproteina; PL =fosfolipidy; chol =
cholesterol; CE= cholesterol zestryfikowany; TG =
triglicerydy
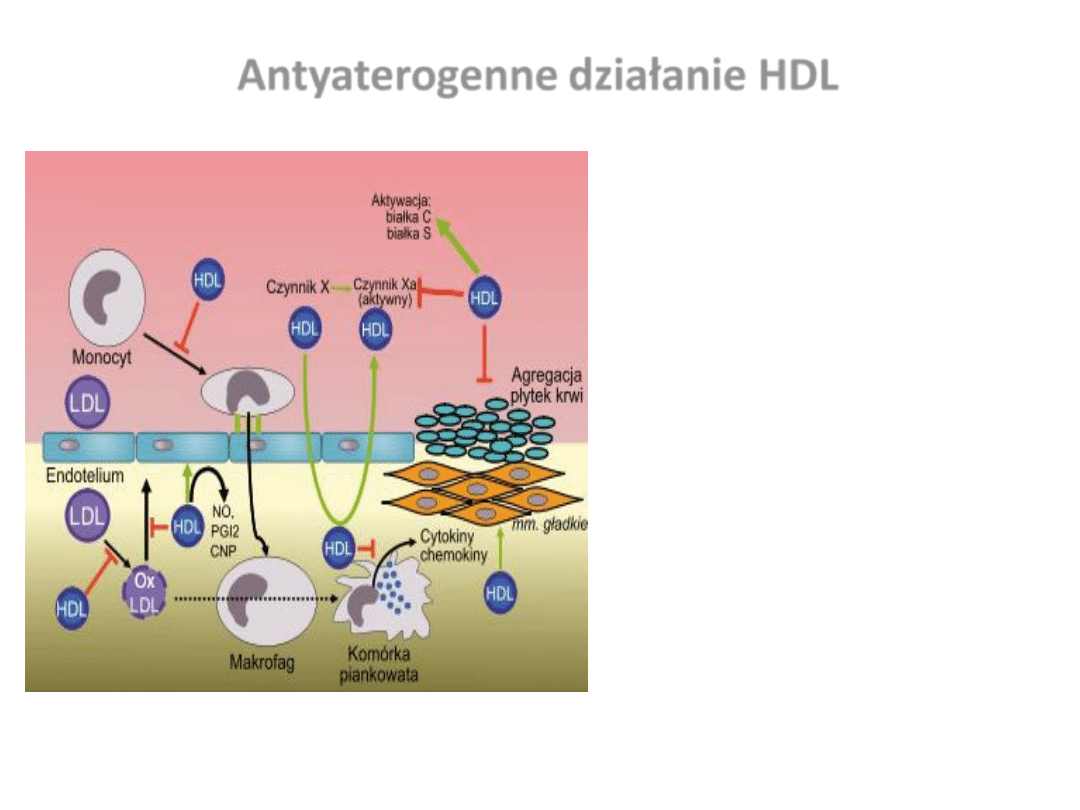
Antyaterogenne działanie HDL
•
Zwrotny transport cholesterolu z
tkanek obwodowych do wątroby
•
Działanie przeciwzapalne - inhibicja
adhezji i aktywacji monocytów (↓
ICAM-1,VCAM-1, selektyna E)
•
Działanie antyoksydacyjne (↓oxLDL)
•
Działanie ochronne i modulujące w
stosunku do śródbłonka (↑NO
2
, PGI
2
,
CNP, hamowanie apoptozy, układu
dopełniacza)
•
Działanie przeciwpłytkowe
(hamowanie wiązania Fg, hamowanie
uwalniania ziarnistości płytkowych,
↑NO
2
,)
•
Działanie fibrynolityczne i
przeciwzakrzepowe (↓ powstawania
kompleksu tenazy i protrombinazy,
↓czynnika X, ↑ białko C i S

• dieta
• palenie tytoniu
• aktywnośd fizyczna
Elementy stylu życia
• ciśnienie tętnicze
• stężenie cholesterolu całkowitego
• stężenie cholesterolu LDL
• stężenie cholesterolu HDL
• stężenie trójglicerydów
• stężenie glukozy/cukrzyca
• nadwaga/otyłośd
• czynniki prozakrzepowe
• markery przewlekłego procesu zapalnego
Czynniki biochemiczne i
fizjologiczne
• wiek
• płed
• wywiad rodzinny (przedwczesne występowanie chorób sercowo-
naczyniowych)
• choroba sercowo-naczyniowa w wywiadzie
• markery genetyczne
Czynniki indywidualne
Czynniki ryzyka miażdżycy
Wyszukiwarka
Podobne podstrony:
Rola uszkodzen srodblonka w patogenezie miazdzycy
PATOGENEZA MIAŻDŻYCY
Patogeneza miażdżycy i występowania zdarzeń wieńcowych, Pomoce naukowe, studia, medycyna
PATOGENEZA MIAŻDŻYCY
Miazdzyca patogeneza i nastepstwa
Jak patogeny z jamy ustnej przyczyniają się do miażdżycy, zawału i udaru
Miazdzyca
miażdżyca1b
PROCES MIAŻDZYCOWY A(1)
STRES A MIAŻDŻYCA
Miażdżyca 5
Patogeneza i objawy odwarstwienia siatkówki (RD)
Patogeneza raka płuc
Zapalenie w miażdżycy
Klasyfikacja bakterii i mechanizmy patogenezy bakteryjnej
więcej podobnych podstron