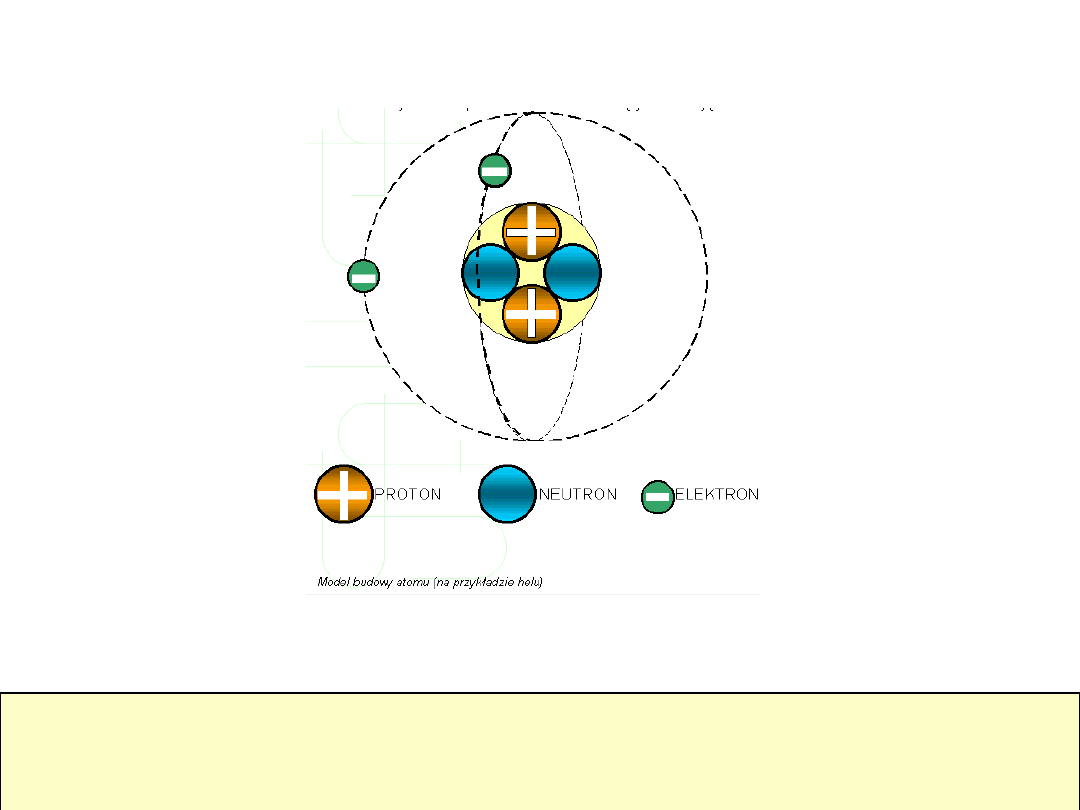
Atom -jego parametry
Średnica atomów n*10
-8
cm (nA), jądra n*10
-
12
cm
Średnica atomów n*10
-8
cm (nA), jądra n*10
-
12
cm
Prof.. J.Pietrzyk
02.2006p
Z=n
p
, =n
e
-liczba atomowa

Atom -jego parametry
• Z=n
p
, =n
e
-liczba atomowa
m=m
n
+ m
p
+m
e
-masa atomowa
m
e
=
1/1840*
m
n
(
m
n
=
m
p
), stąd
m=m
n
+ m
p
jeżeli przyjąć
m
n
=
m
p
=
1
to masa atomowa każdego
pierwiastka powinna być w przybliżeniu liczbą całkowitą,
tak nie jest gdyż większość pierwiastków występuje w
postaci izotopów np. Fe:
26Fe55.85= 26Fe54 (6%) +26Fe56 (91.6%)
+26Fe57 (2.1%) + 26Fe58 (0.3%)
po wybuchach jądrowych pojawia się izotop
promieniotwórczy o czasie półrozpadu 47.1 dni.
• Średnica
atomu zależna jest od ułożenia ich w sieci
krystalicznej np. Fe w sieci A2 (ferryt) 2.48A :A1 (austenit)
2.54A jeszcze inna (mniejsza) w związkach chemicznych.
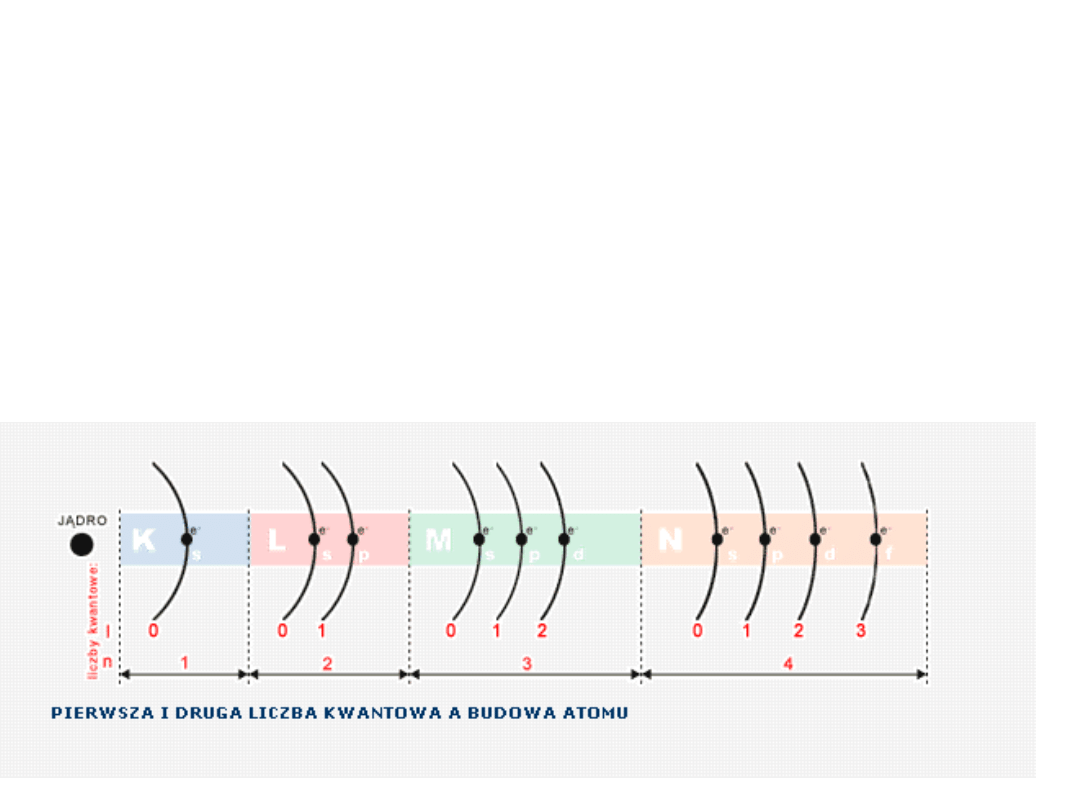
Atom -jego parametry
Własności pierwiastka określa jego liczba
atomowa Z ściśle związana z budową
jego zewnętrznych powłok
elektronowych. Łatwość oddawania i
przyłączania elektronów na zewnętrzne
powłoki określa typ i charakter wiązań w
ciałach stałych -geometrię przestrzenną
wiązań.
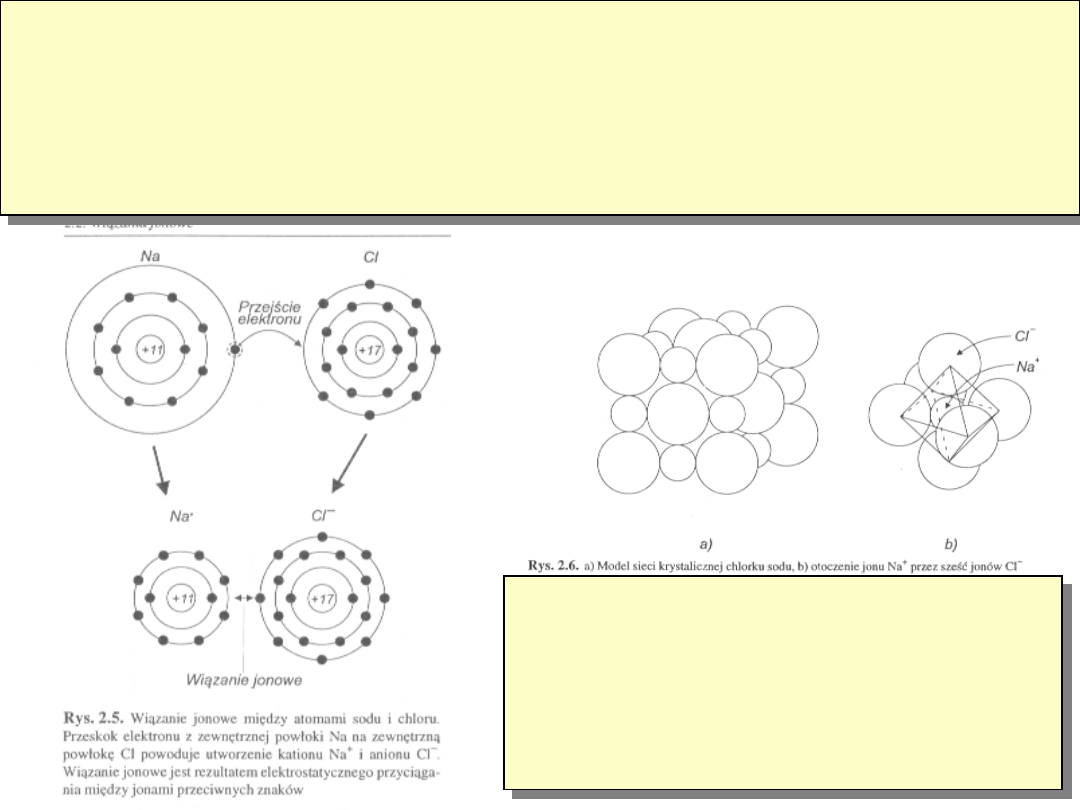
Wiązania międzyatomowe
Silne A.Jonowe
Wiązania międzyatomowe
Silne A.Jonowe
Charakteryzują je :Moduł sprężystości
E, G
Temperatura topnienia
Ts Energia wiązań 600 -1550 kJ/mol
:kierunkowość wiązań
Charakteryzują je :Moduł sprężystości
E, G
Temperatura topnienia
Ts Energia wiązań 600 -1550 kJ/mol
:kierunkowość wiązań
(10Ne
)
(18Ar
)
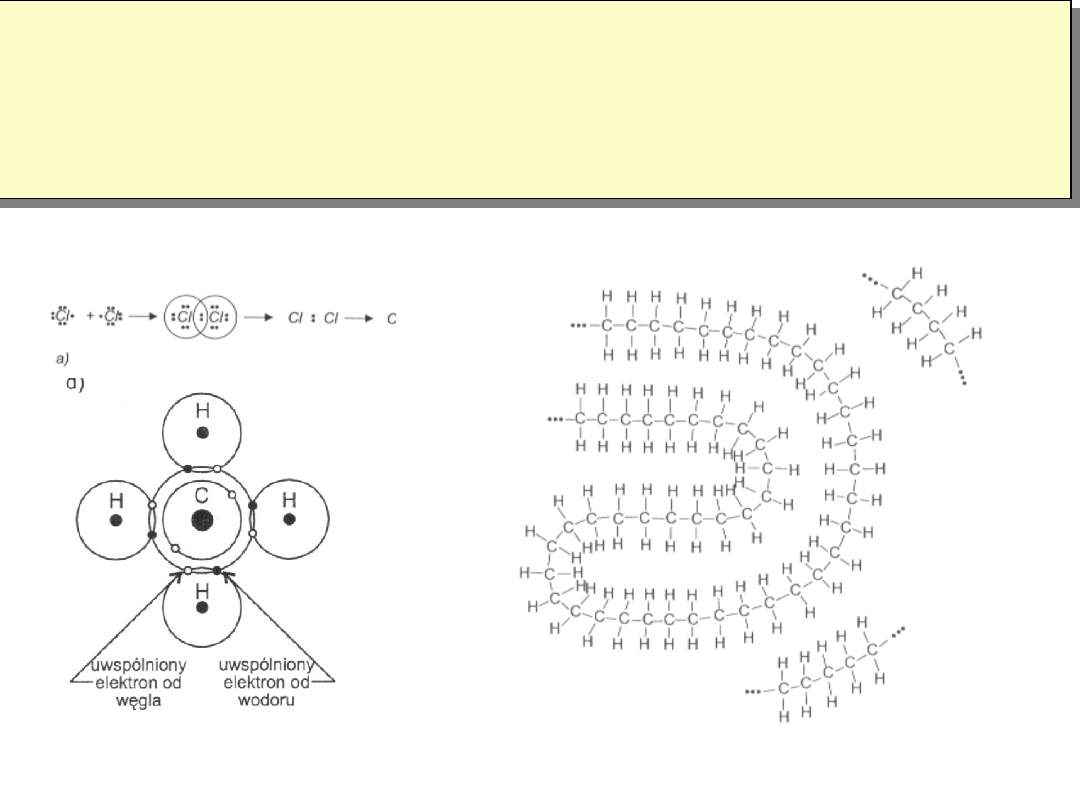
Wiązania międzyatomowe silne
B.Kowalencyjne
w molekułach gazu, polimerach, węgiel -diament
Energia wiązań 500 -1250 kJ/mol :kierunkowość wiązań
Wiązania międzyatomowe silne
B.Kowalencyjne
w molekułach gazu, polimerach, węgiel -diament
Energia wiązań 500 -1250 kJ/mol :kierunkowość wiązań
Cl
2
Etylen CH
4
Polietylen (CH)
n
n=1000 -100000
Wiązania silne C. Metaliczne
Energia wiązań 100
-850 kJ/mol
Duża plastyczność (walcowanie na zimno miedzi do 0.001mm), duża
przewodność elektryczna, mała kierunkowość wiązań
Wiązania silne C. Metaliczne
Energia wiązań 100
-850 kJ/mol
Duża plastyczność (walcowanie na zimno miedzi do 0.001mm), duża
przewodność elektryczna, mała kierunkowość wiązań
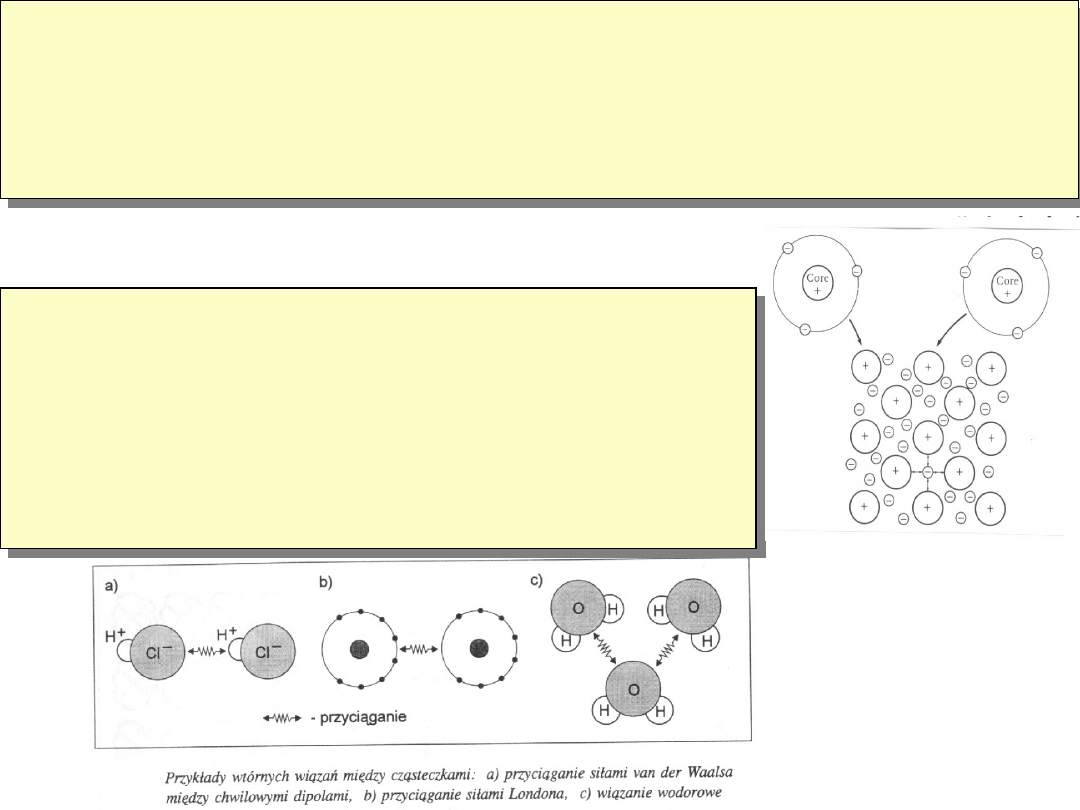
Wiązania słabe (wtórne)
wywołane
są asymetrią ładunku elektrycznego molekuł.
Asymetria może być wywołana kierunkowością
wiązań HCl, H
2
O, jak i wyindukowana zbliżeniem
molekół (gazy szlachetne). Energia wiązań <40 kJ/mol
Występują w polimerach, tkankach biologicznych.
Wiązania słabe (wtórne)
wywołane
są asymetrią ładunku elektrycznego molekuł.
Asymetria może być wywołana kierunkowością
wiązań HCl, H
2
O, jak i wyindukowana zbliżeniem
molekół (gazy szlachetne). Energia wiązań <40 kJ/mol
Występują w polimerach, tkankach biologicznych.
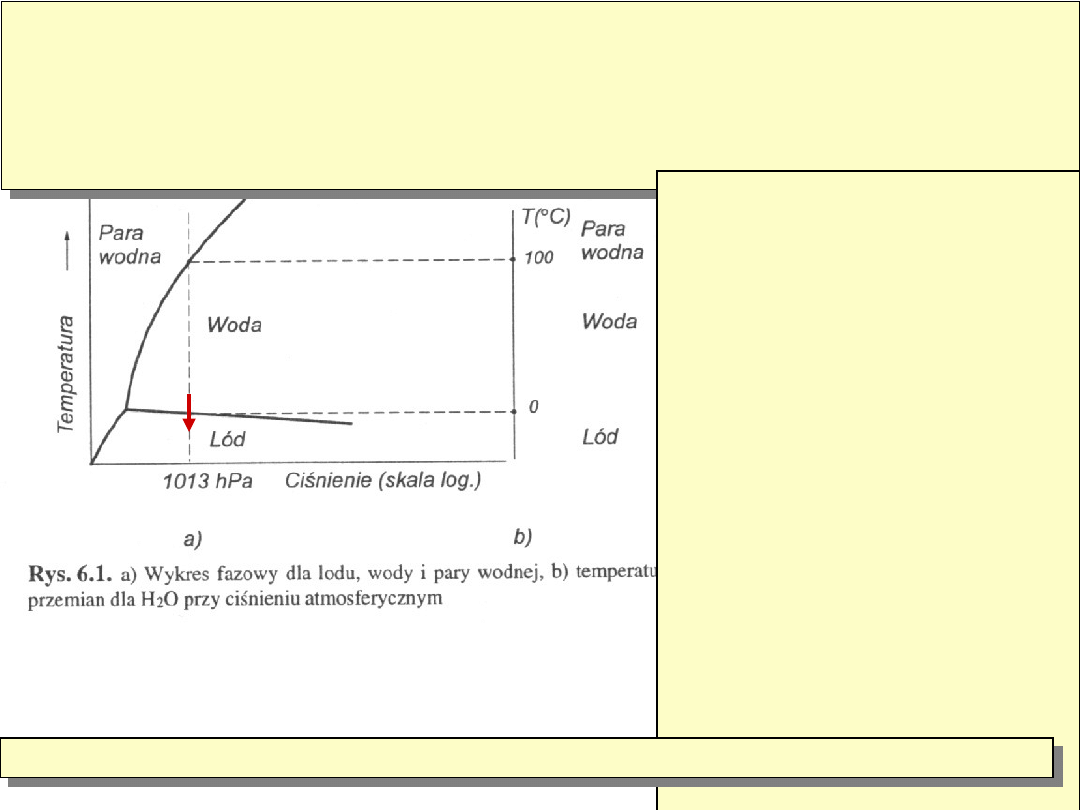
Stan stały
substancji pojawia się przy niskich temperaturach gdy siły
międzycząsteczkowe przewyższą energię kinetyczną cząsteczek -przy
temperaturze Ts. Podczas przejść międzyfazowych Ciecz -Ciało stałe, Gaz
-Ciecz wydziela (pochłania) się ciepło danego procesu. Dla H
2
O L-S 1.4
kcal/mol (c. krystalizacji); L -G 9.71 kcal/mol
Stan stały
substancji pojawia się przy niskich temperaturach gdy siły
międzycząsteczkowe przewyższą energię kinetyczną cząsteczek -przy
temperaturze Ts. Podczas przejść międzyfazowych Ciecz -Ciało stałe, Gaz
-Ciecz wydziela (pochłania) się ciepło danego procesu. Dla H
2
O L-S 1.4
kcal/mol (c. krystalizacji); L -G 9.71 kcal/mol
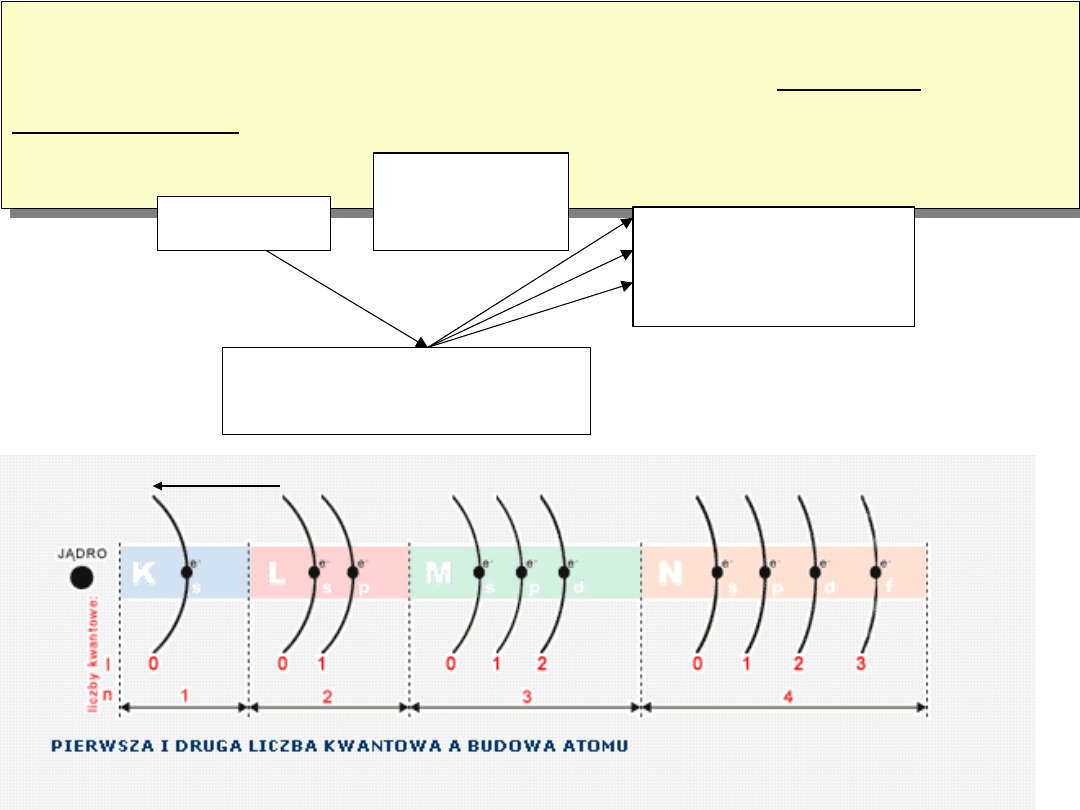
Stan stały
charakteryzuje się:
1.Oscylacjami wokół
położenia r. 2.Gęstym
ułożeniem cząsteczek
2a.Struktury uporządkowane
-kryształy.
2b. Struktury
nieuporządkowane -ciała
amorficzne -przechłodzone
ciecze
Określenie
rodzaju
powstającej podczas
krzepnięcia struktury
umożliwiło odkrycie w 1895
roku
Promieniowania
rentgenowskiego
Stan stały
charakteryzuje się:
1.Oscylacjami wokół
położenia r. 2.Gęstym
ułożeniem cząsteczek
2a.Struktury uporządkowane
-kryształy.
2b. Struktury
nieuporządkowane -ciała
amorficzne -przechłodzone
ciecze
Określenie
rodzaju
powstającej podczas
krzepnięcia struktury
umożliwiło odkrycie w 1895
roku
Promieniowania
rentgenowskiego
I zastosowanie go przez Bragga (1913r.) do badania struktury ciał stałych.
I zastosowanie go przez Bragga (1913r.) do badania struktury ciał stałych.
Ts
Wykorzystanie charakterystycznego Z)
promieniowania rentgenowskiego do analizy
chemicznej -sondy, mikrosondy
Wykorzystanie charakterystycznego Z)
promieniowania rentgenowskiego do analizy
chemicznej -sondy, mikrosondy
Elektrony E=1-
10KV
Promieniowanie
rentgenowskie
(Z)
01 10
Ciało stałe
Analizator I, (Z)
Komputer
Analiza ilościowa składu
chemicznego CS
k
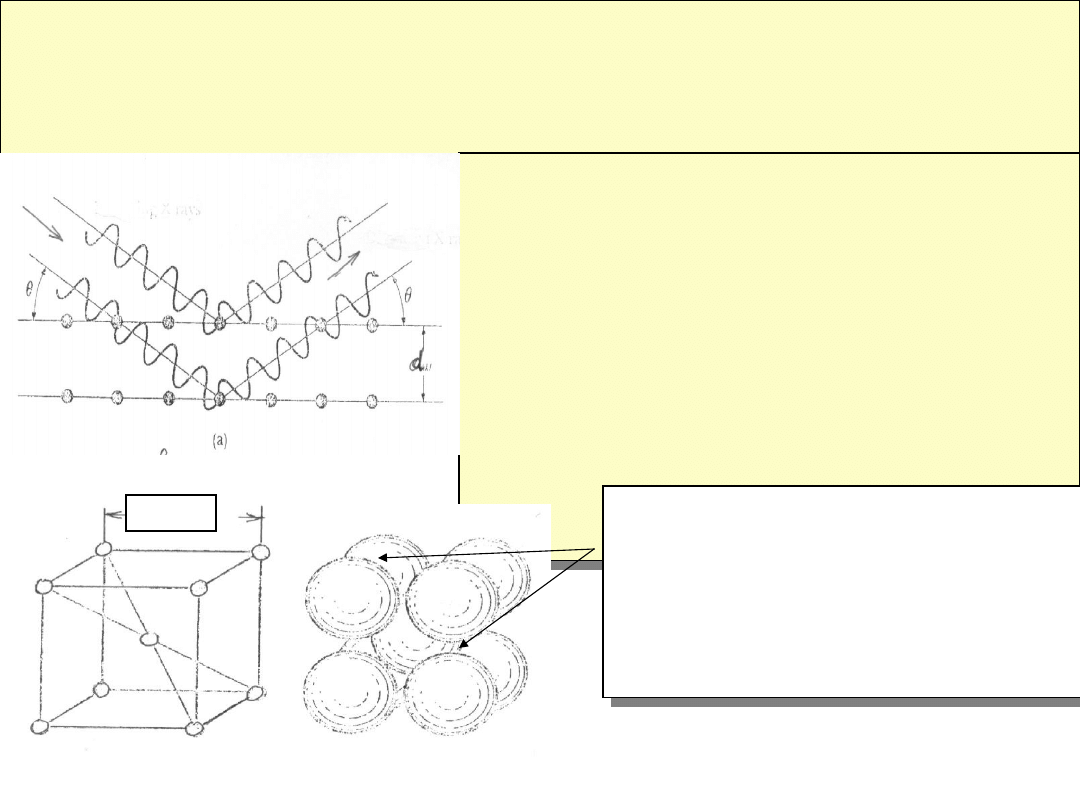
Wykorzystanie charakterystycznego
Z)
promieniowania rentgenowskiego do badania
struktury CS. Wykorzystanie prawa Bragga
2dsinn
Wykorzystanie charakterystycznego
Z)
promieniowania rentgenowskiego do badania
struktury CS. Wykorzystanie prawa Bragga
2dsinn
d -odległość
pomiędzy obsadzonymi
atomami odbijającymi płaszczyznami
krystalograficznymi
.
Określając je dla
wszystkich kierunków można określić
ułożenie przestrzenne atomów
-przestrzenną sieć krystaliczną -jej
najmniejszy element -
Komórkę
elementarną np. A1; A2; A3 i
inn.
d -odległość
pomiędzy obsadzonymi
atomami odbijającymi płaszczyznami
krystalograficznymi
.
Określając je dla
wszystkich kierunków można określić
ułożenie przestrzenne atomów
-przestrzenną sieć krystaliczną -jej
najmniejszy element -
Komórkę
elementarną np. A1; A2; A3 i
inn.
Komórka A2
np.Fe
Luki oktaedryczne
miejsca które zajmują
rozpuszczone atomy węgla i
azotu (0.00n%)
Komórka A2
np.Fe
Luki oktaedryczne
miejsca które zajmują
rozpuszczone atomy węgla i
azotu (0.00n%)
2.86A
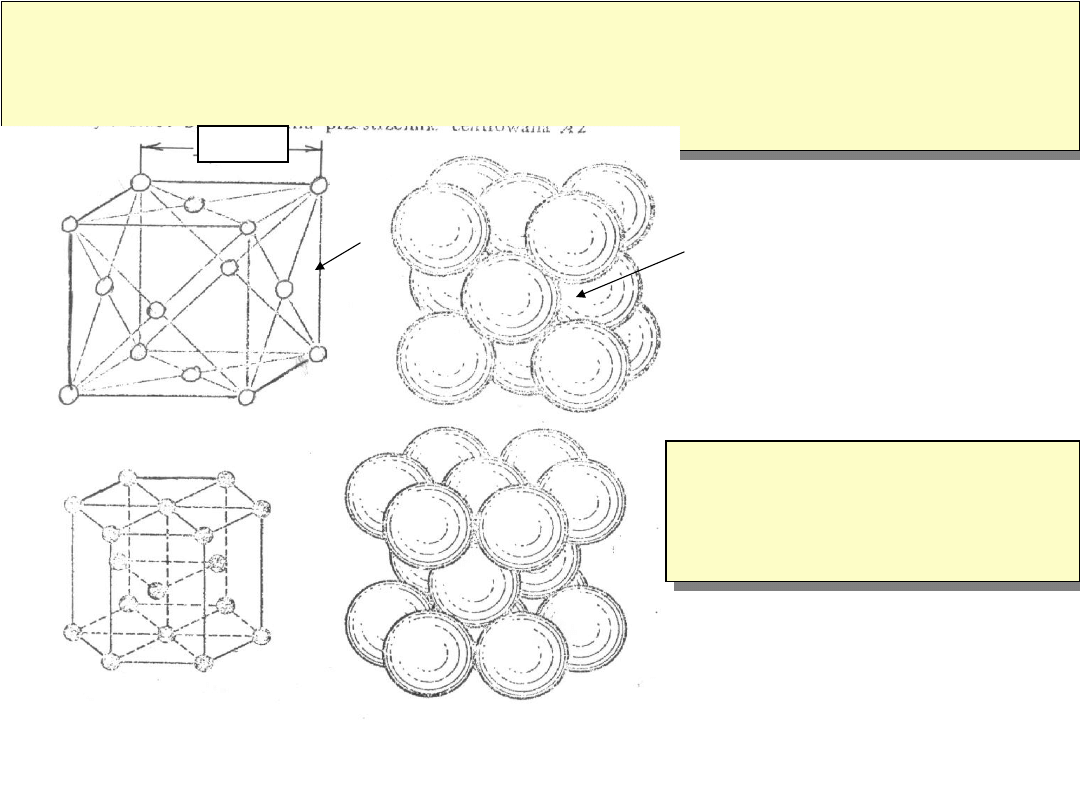
Komórki Elementarne A1 (Fe) Duże luki
rozpuszczalność C do 2.11%
Komórki Elementarne A1 (Fe) Duże luki
rozpuszczalność C do 2.11%
Komórka A3
Heksagonalna
zwarta
np.
Be ;Zn
Komórka A3
Heksagonalna
zwarta
np.
Be ;Zn
3.59A

W latach 30-tych ubiegłego wieku porównując
oszacowaną wytrzymałość teoretyczną
kryształów, z rzeczywistymi wynikami badań
wytrzymałości, stwierdzono znaczną rozbieżność,
sięgającą dwa, a nawet trzy rzędy wielkości.
Aby to wyjaśnić wprowadzono pojęcie wad
sieci krystalicznej. Obecność wad potwierdzono
eksperymentalnie wiele lat później gdy rozwinięto
nowe techniki badawcze m. inn mikroskopię
elektronową.
Obecnie wady dzielimy na trzy grupy:
Wady punktowe
Wady liniowe
Wady powierzchniowe
W latach 30-tych ubiegłego wieku porównując
oszacowaną wytrzymałość teoretyczną
kryształów, z rzeczywistymi wynikami badań
wytrzymałości, stwierdzono znaczną rozbieżność,
sięgającą dwa, a nawet trzy rzędy wielkości.
Aby to wyjaśnić wprowadzono pojęcie wad
sieci krystalicznej. Obecność wad potwierdzono
eksperymentalnie wiele lat później gdy rozwinięto
nowe techniki badawcze m. inn mikroskopię
elektronową.
Obecnie wady dzielimy na trzy grupy:
Wady punktowe
Wady liniowe
Wady powierzchniowe
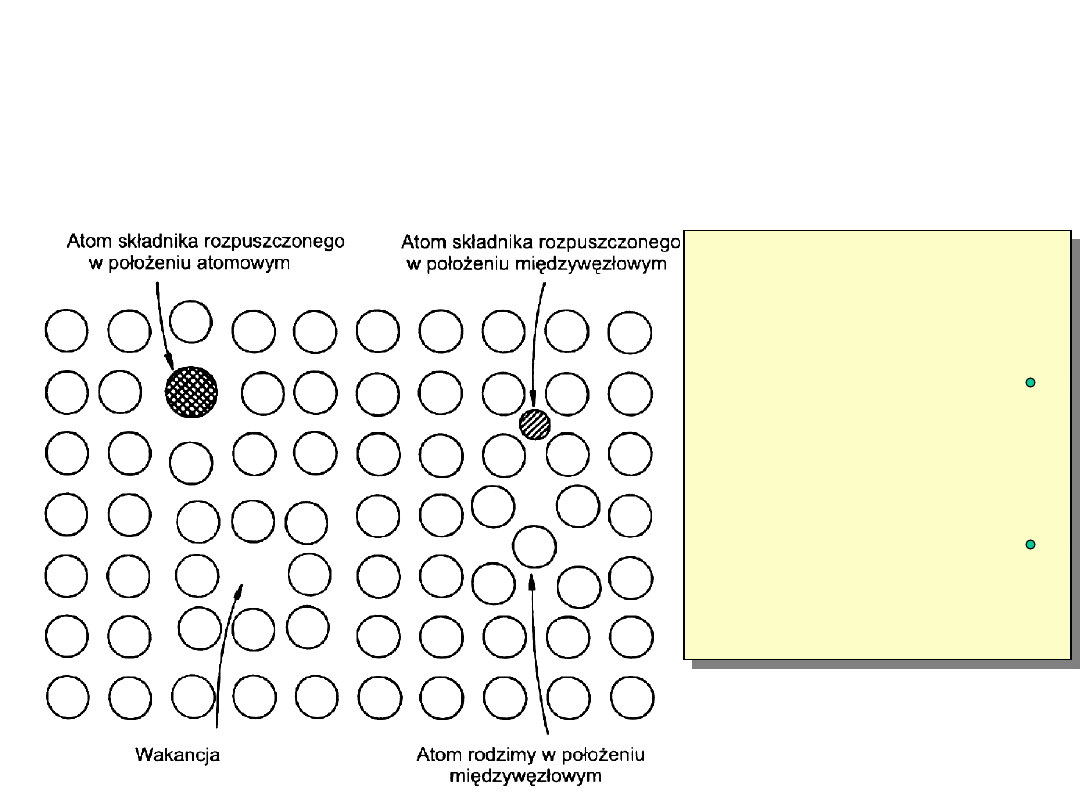
Wady punktowe
-wakancje ilość-n/N=10(-4) dla T
s
; dla Fe przy 20C n/N=10
-19
-atomy międzywęzłowe własne ilość-n/N=10
-40
dla T
s
- atomy międzywęzłowe obce ilość-n/N=0-0.0n%
-atomy różnowęzłowe (substytucyjne) ilość-n/N=0-50%
Szybkości dyfuzji-
czas osiadłego życia
1 sec. Przy
temperaturze:
-w. Dla Fe -60C
-a.m.wł. Dla Fe -200C
-a.m.o. C w Fe +40C
-a.r. V w Fe +350C
Szybkości dyfuzji-
czas osiadłego życia
1 sec. Przy
temperaturze:
-w. Dla Fe -60C
-a.m.wł. Dla Fe -200C
-a.m.o. C w Fe +40C
-a.r. V w Fe +350C
D
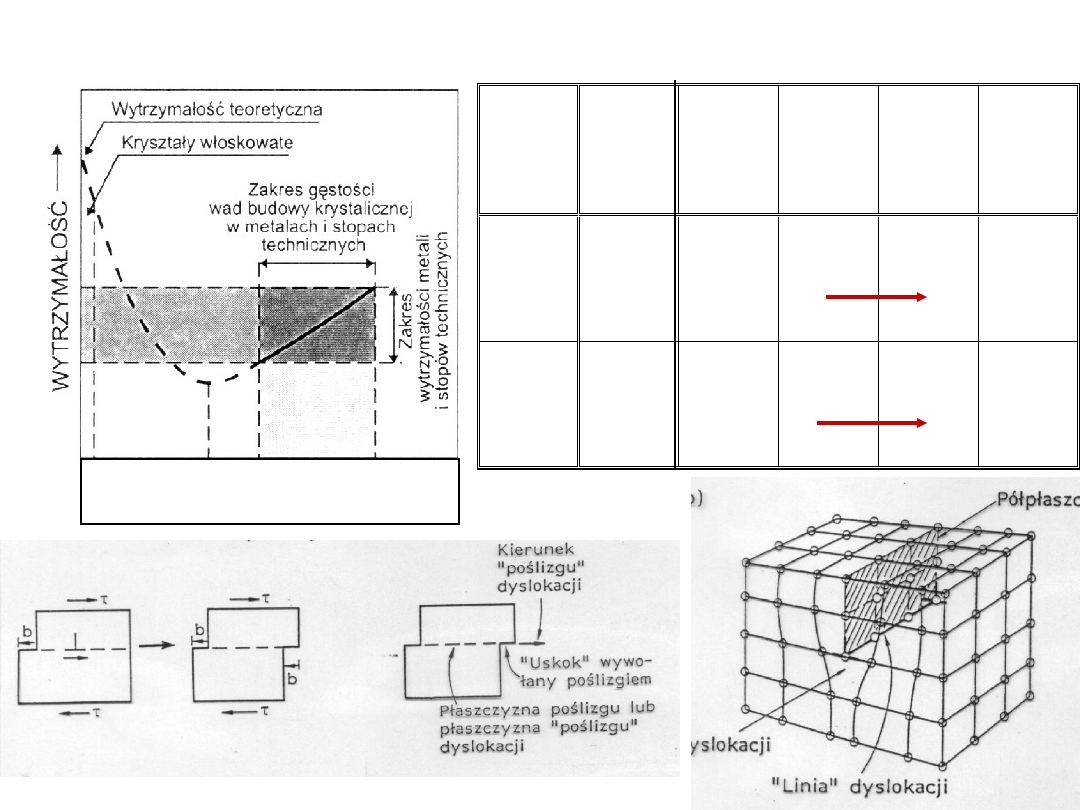
Wady liniowe
10
8
10
12
Gęstość dyslokacji cm/cm
3
Przykład:
Materiał
G [MPa]
max
[MPa]
max
[MPa]
R
e
[MPa]
max
/R
e
Cu
45 000
7 150
14 300
30
475
Fe
80 000
12 750
25 000
160
150
D. krawędziowa
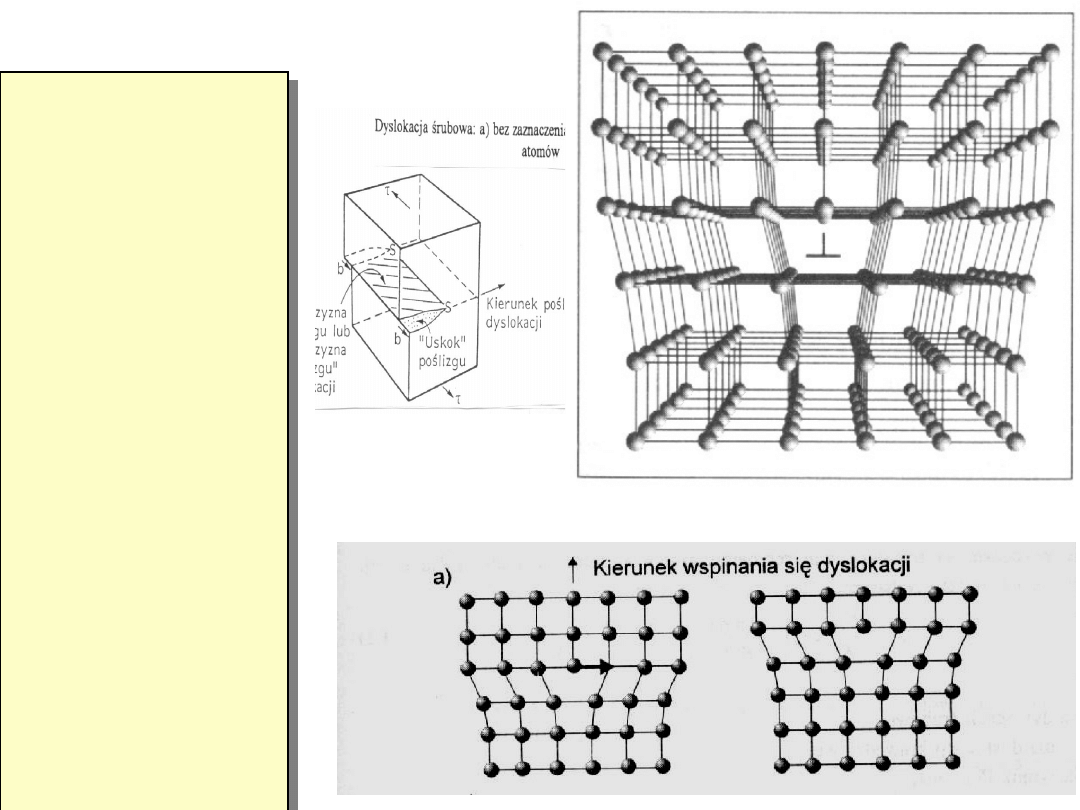
Wady liniowe
Odkształcenie
nieodwracalne
-plastyczne
materiałów
krystalicznych
odbywa się
najczęściej
poprzez poślizg
dyslokacji pod
wpływem
naprężeń
ścinających.
Przy wysokich
temperaturach
(dużo
wakancji) może
być
wspomagane
przez
wspinanie
dyslokacji.
Odkształcenie
nieodwracalne
-plastyczne
materiałów
krystalicznych
odbywa się
najczęściej
poprzez poślizg
dyslokacji pod
wpływem
naprężeń
ścinających.
Przy wysokich
temperaturach
(dużo
wakancji) może
być
wspomagane
przez
wspinanie
dyslokacji.
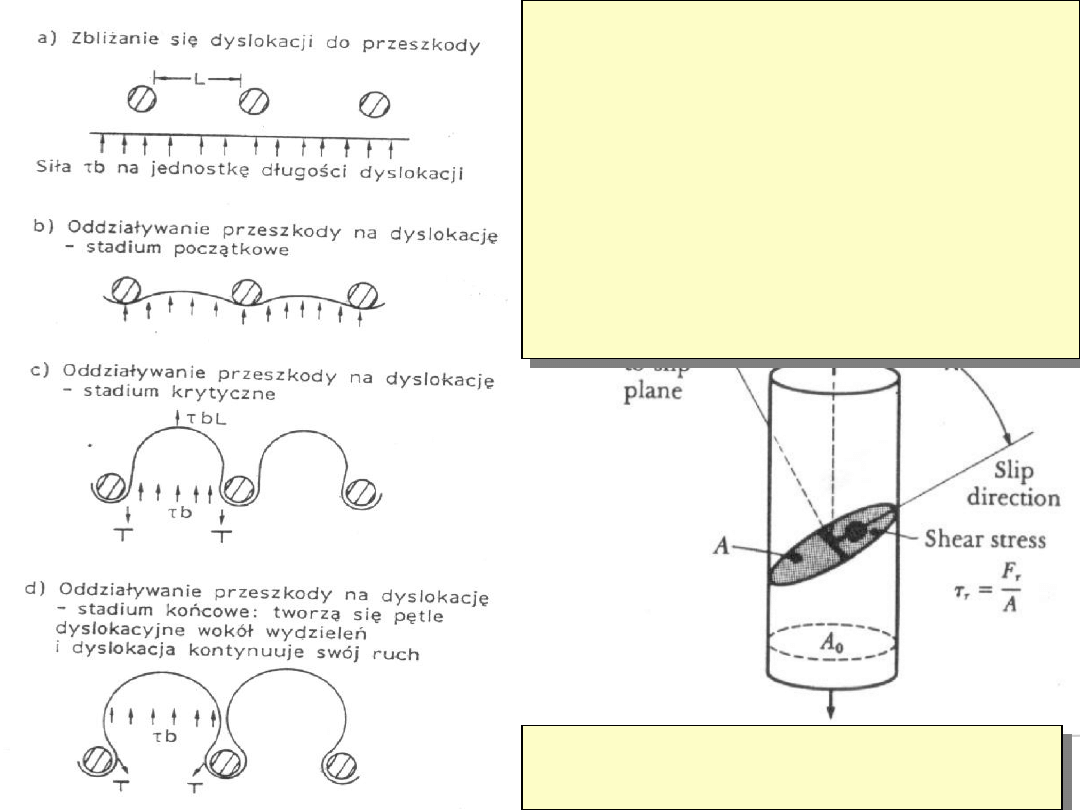
coscos 45
05
Wszelkie przeszkody na
drodze przemieszczającej
się linii dyslok. będą
umacniały materiał:
coscos
45
Wszelkie przeszkody na
drodze przemieszczającej
się linii dyslok. będą
umacniały
materiał:
A. Umocnienie przez wydzielenia
A. Umocnienie przez wydzielenia
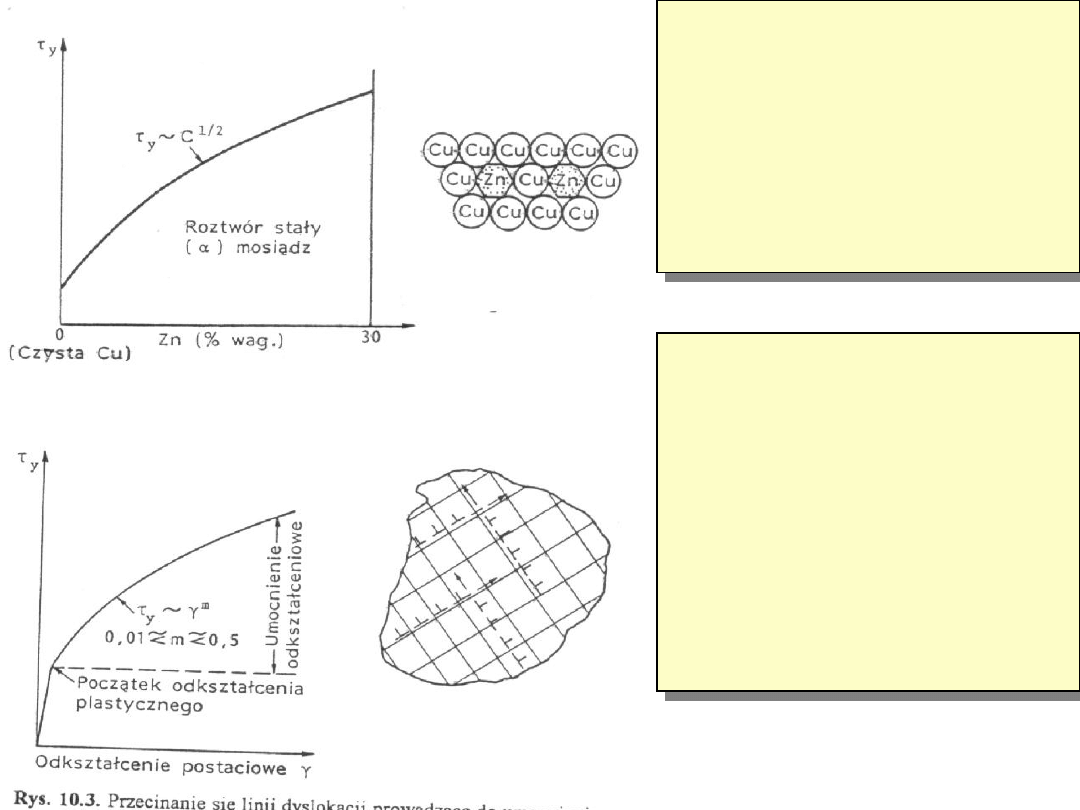
B. Umocnienie
przez atomy obce
-umocnienie
roztworowe
B. Umocnienie
przez atomy obce
-umocnienie
roztworowe
C. Umocnienie
przez defekty
liniowe.
- dyslokacje ulokowane na
innych płaszczyznach.
Ich gęstość rośnie z
odkształceniem od 10
8
do
10
12
cm/cm
3
C. Umocnienie
przez defekty
liniowe.
- dyslokacje ulokowane na
innych płaszczyznach.
Ich gęstość rośnie z
odkształceniem od 10
8
do
10
12
cm/cm
3
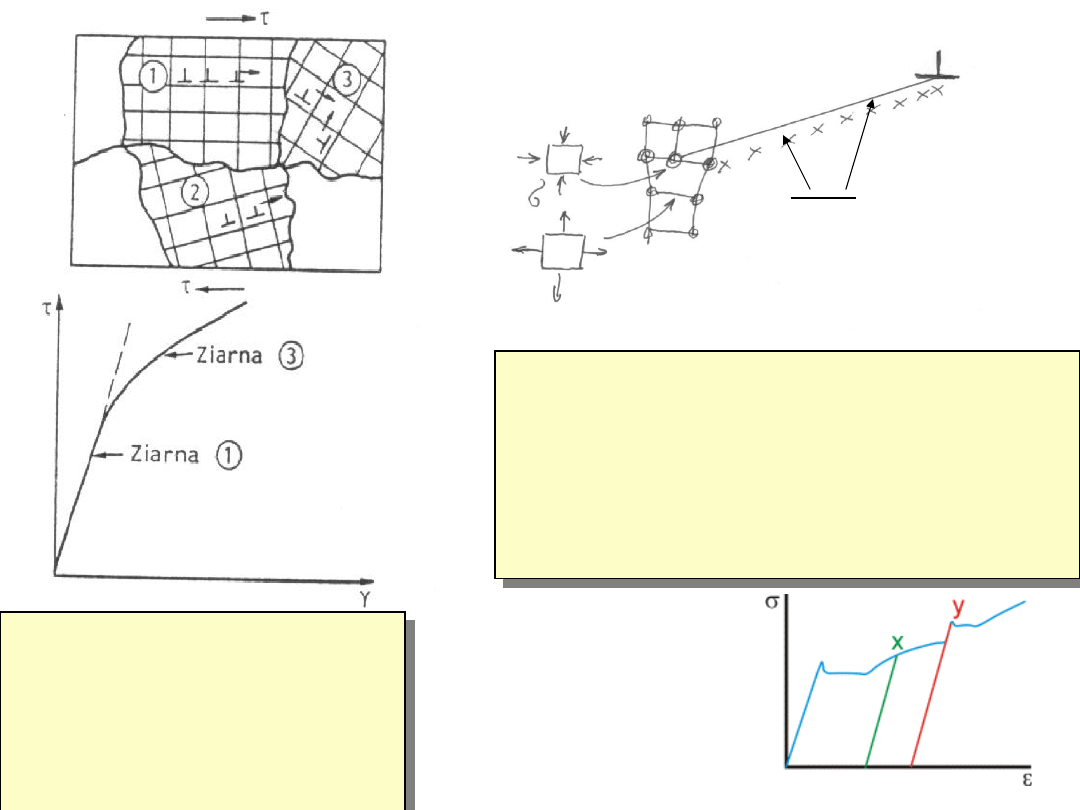
D. Umocnienie
przez granice
ziaren.
D. Umocnienie
przez granice
ziaren.
Atomy obce rozpuszczone w sieci
dyfundując do strefy naprężeń wokół linii
dyslokacji tworzą Atmosfery Cottrella.
Daje to efekty wyraźnej granicy
plastyczności i efekty starzenia po
zgniocie.
Atomy obce rozpuszczone w sieci
dyfundując do strefy naprężeń wokół linii
dyslokacji tworzą Atmosfery Cottrella.
Daje to efekty wyraźnej granicy
plastyczności i efekty starzenia po
zgniocie.
C, N w Fe

Metaliczne materiały konstrukcyjne są, prawie zawsze
polikryształami, składają się z dużej liczby kryształów całkowicie
wypełniających przestrzeń. W materiałach jednofazowych
sąsiadujące ze sobą kryształy różnią się jedynie orientacją sieci.
Kryształy te nazywamy ziarnami, a obszary styku kryształów
granicami ziaren. W obszarach granicy następuje zmiana
orientacji sieci. Granice umacniają materiał Re=Ro+kd
-1/2
, są
drogami szybkiej dyfuzji.
Defekty powierzchniowe (płaskie)
- granice ziaren
np.
Fe
Defekty powierzchniowe (płaskie)
- granice ziaren
np.
Fe
Charakterystyki ilościowe-
średnia średnica ziarna d
Nanoziarna d=3 -0.00n [m]
ziarna d=3 -50 [m]
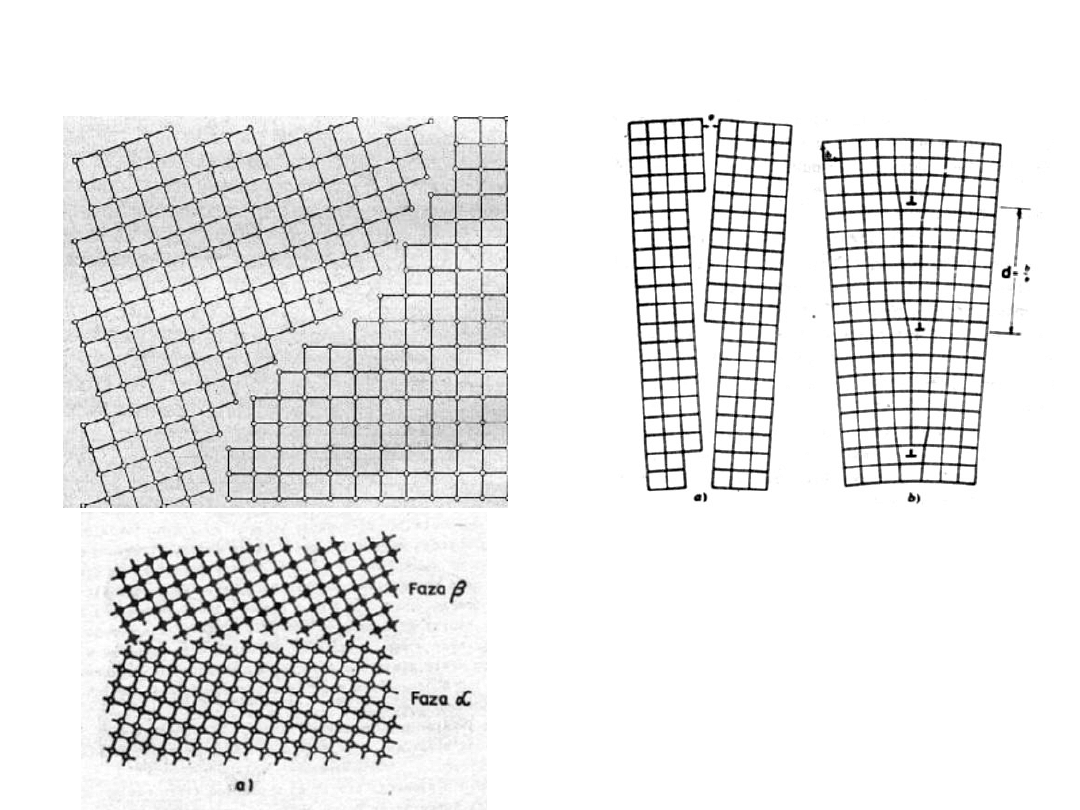
Granice między ziarnami jednej fazy
Granice między ziarnami
dwu faz i
Prof.. J.Pietrzyk
02.2006p
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
Wyszukiwarka
Podobne podstrony:
STRUKTURA TRENINGU
30 Struktury zaleznosci miedzy wskaznikami zrow rozw K Chmura
rodzaje struktur rynkowych 2
Struktura regionalna
struktura organizacyjna BTS [ www potrzebujegotowki pl ]
Struktura treningu sportowego (makrocykl) szkoła PZPN
Struktura podmiotowa i przedmiotowa gospodarki
STRUKTURA I FUNKCJONOWANIE GN
Strukturalizm i stylistyka (część II)
Struktura ludności w Polsce
wykład 7 struktura kryształów
Struktura 3
STRUKTURA ORGANIZACYJNA UKúAD I WZAJEMNE ZALE»NOŽCI MI¦DZY
STATUT I STRUKTURA ORGANIZACYJNA WOPR
strukturalnaMinuchina stud
więcej podobnych podstron