
Diagnostyka
laboratoryjna chorób
przewodu pokarmowego
cz.2
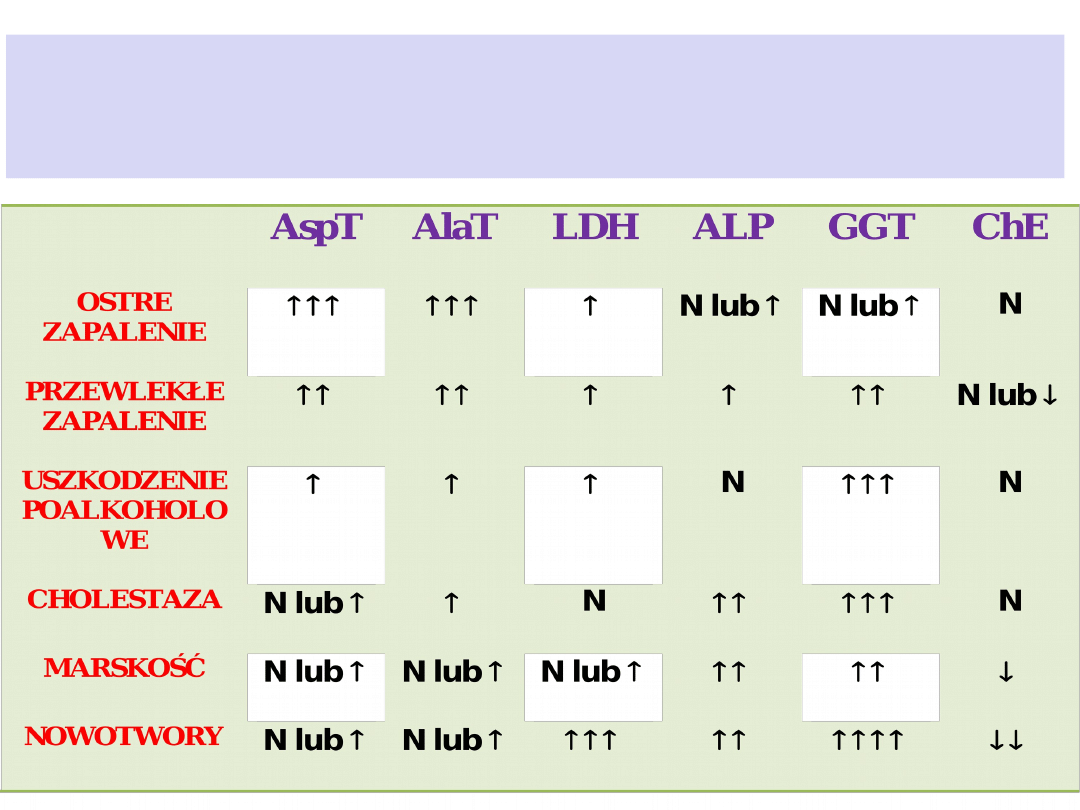
Zmiany aktywności enzymów w
wybranych schorzeniach wątroby

Żółtaczki
•Hiperbilirubinemia i żółtaczka mogą być
objawem chorób o różnej etiologii i samo stwierdzenie
hiperbilirubinemii
musi
być
rozpatrywane
w
kontekscie okoliczności jej wystepowania. Czasem dla
celów
dydaktycznych
dzieli
się
zółtaczki
na
przedwatrobowe,
wątrobowe
i
pozawątrobowe.
Podział ten nie jest ścisły ponieważ najczęściej
przyczyny żółtaczki są złożone i obejmują zarówno
mechanizmy poza wątrobą jak i w samej wątrobie.

Żółtaczki
*
A.
Żółtaczka hemolityczna
powstaje w
następstwie wzmożonej hemolizy erytrocytów co
prowadzi do uwolnienia dużych ilości bilirubiny.
Zmienia się równowaga pomiędzy wychwytem
bilirubiny i jej napływem drogą osocza. W
konsekwencji następuje wzrost stężenia bilirubiny
we krwi. Żółtaczki hemolityczne charakteryzują się
umiarkowanie zwiększonym stężeniem bilirubiny
wolnej we krwi i umiarkowanie zwiększonym
wydalaniem urobilinogenu z moczem przy znacznie
zwiększonym wydalaniu sterkobilinogenu z kałem.
Brak jest objawów uszkodzenia wątroby.
Żółtaczka noworodków
jest jednym z
przykładów żółtaczki hemolitycznej
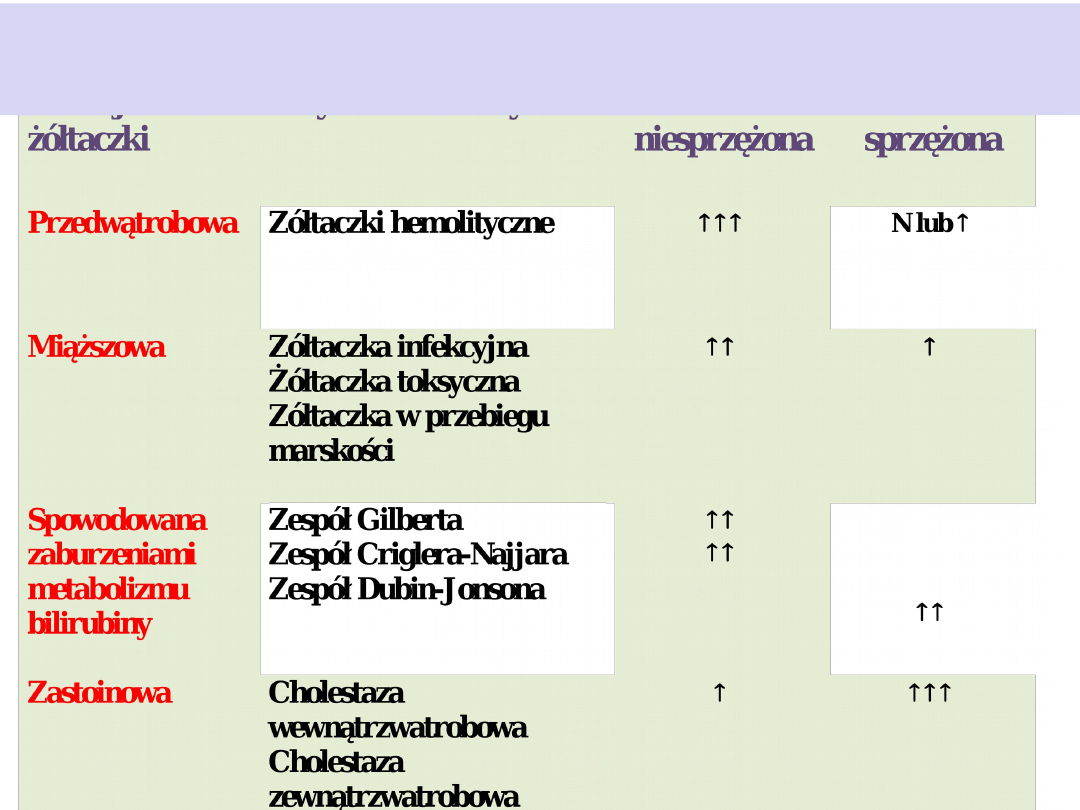
Zaburzenia metabolizmu bilirubiny w
różnych rodzajach żółtaczek
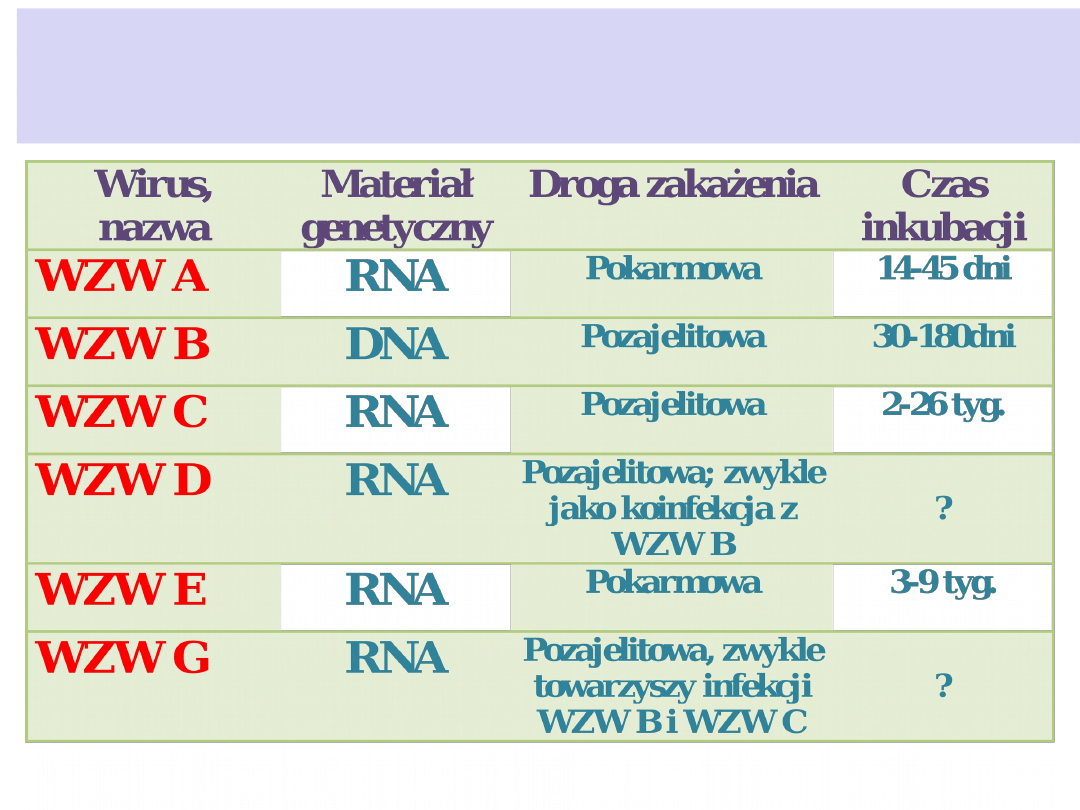
Charakterystyka wirusów
hepatotropowych

Wstępne testy diagnostyczne w
wirusowych zapaleniach wątroby
IgM anty HAV
wykrywa ostre WZW
typu A
HBsAg
wykrywa ostre lub przewlekłe
WZW typu B
Anty-HCV
wykrywa ostre lub
przewlekłe WZW typu C

WZW A
HAV wywołujacy WZW A jest wirusem RNA należącym do
rodziny Picornaviridae, rodzaju enterowirusów.
Zakażenie szerzy się drogą pokarmową.
HAV wykazuje bezpośrednie działanie hepatotoksyczne,
jednakże nie można wykluczyć uszkodzenia wątroby przez
immunologiczną odpowiedź gospodarza.
Okres wylęgania wynosi 15-49 dni (średnio 28 dni)
MARKERY ZAKAŻENIA HAV
Antygen wirusowy HAAg wykrywalny w kale na kilkanaście dni przed
wystąpieniem
klinicznych objawów choroby, utrzymuje się przez kilka dni w okresie
rozwiniętych objawów klinicznych.
Przeciwciała anty-HAV
·
anty-HAV-IgM
pojawiają się 18-41 dni po zakażeniu i
utrzymują się zwykle 2-3 miesięcy.
Są dowodem ostrej fazy zakażenia i świadczą o
zakaźności chorego.
· anty-HAV-IgG
Najwyższe miana stwierdza się w okresie
rekonwalescencji.
Utrzymują się latami, często przez całe życie. Są
dowodem odporności na
zakażenie HAV.

WZW B
Czynnikiem etiologicznym WZW typu B jest kompletny wirus, zwany
cząstką Dane‘a (
rdzeń DNA, polimeraza pDNA, białka nukleokapsydu
c, s, e
)
Zakażenie drogą parenteralną.
Okres wylegania wynosi 28-160 dni.
u 90 % pacjentów dorosłych rozwija się ostre zapalenie wątroby
kończące się pełnym
wyzdrowieniem.
u 10 % pacjentów dorosłych zakażenie z fazy ostrej przechodzi w
przewlekłą
Klinicznie przewlekłe zapalenie wątroby będące konsekwencją
niewyeliminowania wirusa
po fazie ostrej podejrzewa się gdy po upływie 6 miesięcy brak
normalizacji klinicznej i biochemicznej oraz utrzymują się znaczniki
HBV w surowicy.
W zapaleniu przewlekłym wyróżniamy:
fazę replikacji
pacjent zakaźny
wykrywalne markery replikacji DNA-HBV* oraz pDNA-HBV*
HBsAg(
+) HBeAg(+) anty-HBc(+)
Okrse serokonwersji zanik HBeAg i pojawienie się anty-Hbe,
replikacja nadal obecna* u 50% chorych
fazę integracji
pacjent niezakaźny
nie wykrywa się DNA-HBV oraz pDNA-HBV
HBsAg(+), anty HBe(+), anty
HBc(+)

MARKERY ZAKAŻENIA HBV
·
HBsAg
Pojawia się na 2-4 tyg przed wzrostem aktywności
transaminaz. Jeżeli dochodzi do całkowitej eliminacji wirusa z ustroju
HBsAg zanika 1-6 tyg (może przetrwać do 20 tygodni).
·
HBeAg
Pojawia się w surowicy kilka dni po HBsAg, utrzymuje się
przez 3-9 tygodni. Przetrwanie dłużej niż 10 tyg rokuje przejście
zakażenia ostrego w przewlekłe. HBeAg jest markerem zakaźności osób
zarażonych HBV. Jego obecność jest skorelowana z wystepowaniem
licznych cząstek Dane'a w surowicy, HBV-DNA, polimerazy DNA i HBcAg
w hepatocytach. Jest markerem replakcji HBV.
·
Anty-HBc IgM
Pojawiają sie w surowicy 3-5 tyg po antygenemii HBs, a
więc na krótko przed objawami klinicznymi lub równolegle z nimi.
Wysokie miana utrzymują się przez cały okres antygenemii HBs i są
wykrywalne także gdy HBsAg zanika, a anty-HBs jeszcze się nie pojawiły.
Anty-HBc IgM zanikają w okresie 3-24 miesięcy. Są najpewniejszym
dowodem trwającego zakażenia HBV. Ich niskie miana zmogą przetrwać
gdy rozwija się zapalenie przewlekłe.
·
Anty-HBc IgG
Pojawiaja się kilka tyg po Anty HBc IgM i utrzymują
latami jako dowód przebytego zakażenia HBV.
·
Anty-HBe
Pojawiaja się kilka-kilkunastu dni po zaniku HBeAg.
Utrzymuja się 1-2 lat. Są markerem przebytego stosunkowo niedawno
WZW typu B.
·
Anty-HBs
Pojawiaja się do kilku miesięcy po zaniku HBsAg. Ich
pojawienie się świadczy o
pełnej serokonwersji
i wyeliminowaniu wirusa z
ustroju. Utrzymują się kilkadziesiat miesiecy. Oznaczają odporność na
zakażenie HBV. Najczulsze znaczniki replikacji wirusa to DNA-HBV oraz
aktywność pDNA-HBV. Pojawiają się w surowicy w okresie poprzedzającym
objawy kliniczne i zanikaja wraz z HBeAg.
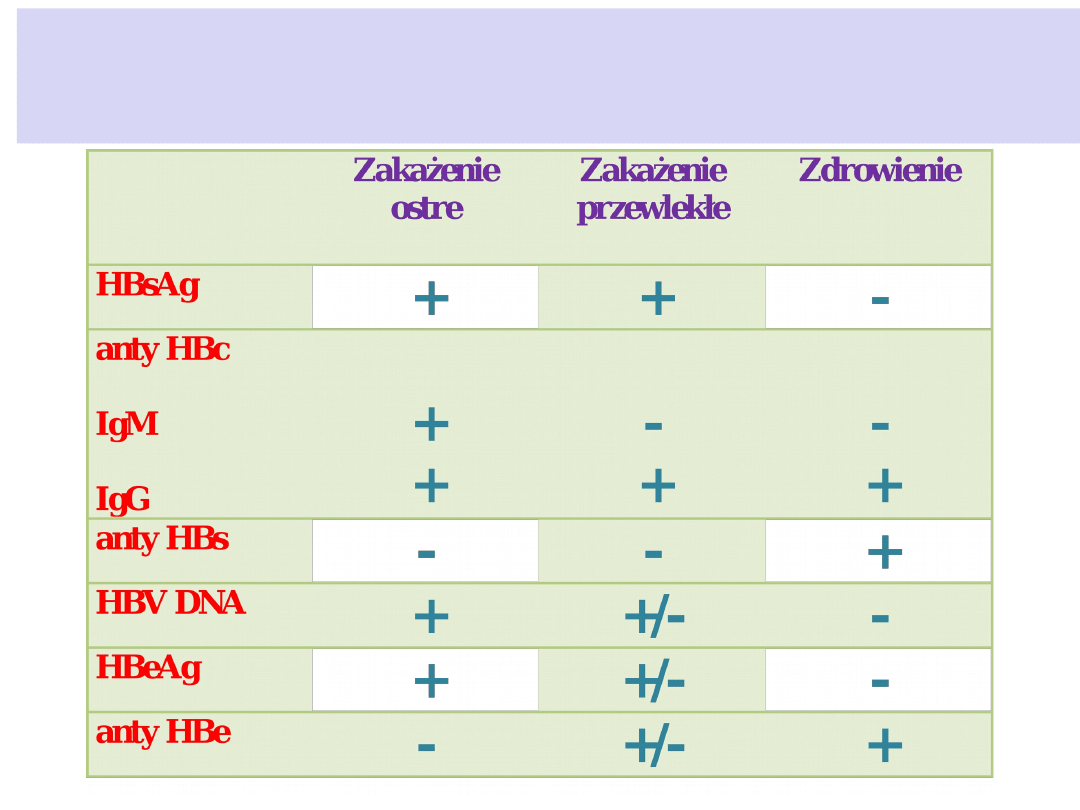
Badania molekularne i serologiczne
wykorzystywane w diagnostyce zakażenia wirusem
zapalenia wątroby typu B
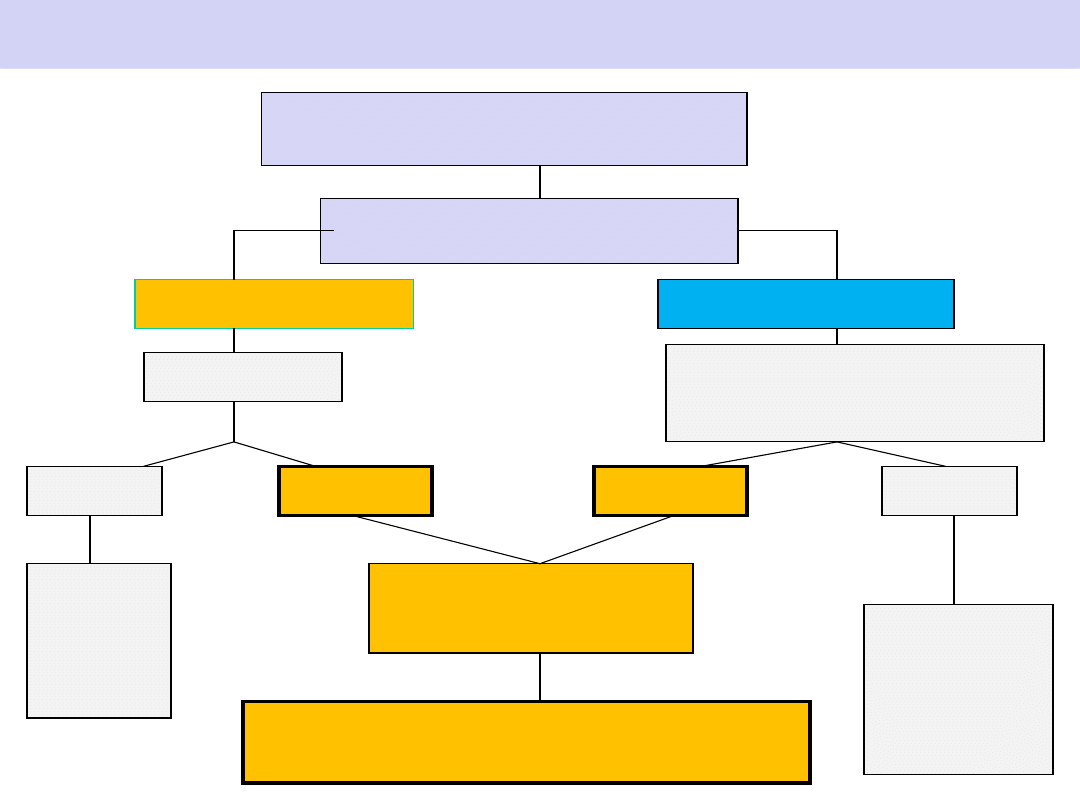
zwiększona aktywność ALAT
wykonać oznaczenie anty-HCV
anty- HCV obecne
anty HCV nieobecne
PCR
brak HCV
obecne HCV
PCR
gdy istnieje ryzyko zakażenia
lub pacjent w immunosupresji
okresowa
kontrola
ALAT
i HCV RNA
brak HCV
obecne HCV
Jeżeli ALAT
podwyższone >6 miesiecy
Przewlekłe zapalenie wątroby typu C
poszukiwanie
innych
przyczyn
choroby
wątroby
Algorytm diagnostyczny przy podejrzeniu przewlekłego
wirusowego zapalenia wątroby wywołanego przez
HCV

Diagnostyka molekularna zakażeń wirusami hepatotropowymi
Dotychczas zidentyfikowano sześć rodzajów
wirusów wywołujących zapalenie wątroby;
wirus A, B, C, D, E i niedawno odkryty wirus
G.
Diagnostyka molekularna dotyczy przede wszystkim
zakażeń wirusami typu B i C. Należy przypuszczać, iż
w najbliższym czasie pojawią się testy na wykrywanie
zakażeń wirusem G.
Metoda PCR ma duże znaczenie w wykrywaniu zakażeń
wirusem typu C. Wiadomo bowiem, że testy ELISA
wykrywają jedynie przeciwciała anty-wirusowe.
W przypadku tego wirusa okres okienka serologicznego
może być jednak bardzo długi. Ponadto nie u wszystkich
chorych powstają specyficzne przeciwciała, a testy ELISA
nie są wystarczająco pewne. Istnieje zatem znaczna liczba
pacjentów zakażonych, u których nie wykrywa się
przeciwciał anty-HCV. Dlatego istnieje potrzeba
potwierdzania zakażeń testem RT-PCR

Diagnostyka molekularna zakażeń wirusami hepatotropowymi
Test RT-PCR na obecność wirusa C polega na
amplifikacji fragmentu materiału genetycznego
wirusa. RNA wirusa jest izolowany z surowicy lub
bioptatu wątroby. Amplifikacji jest poddawany
najczęściej najmniej zmienny fragment RNA wirusa,
znajdujący się w tzw. niekodującym odcinku 5' RNA.
Na pierwszym etapie, podczas reakcji odwrotnej
transkrypcji (RT) jest syntetyzowany cDNA wirusa,
który następnie jest poddawany amplifikacji
podczas PCR. Z reguły po RT-PCR, obejmującej
około
30-40
cykli,
wykonuje
się
reakcję
wzmacniającą, tzw. wewnętrzny PCR. Reakcja taka
jest niezbędna, gdyż zawartość RNA wirusa C w
surowicy jest często niska i nie uzyskuje się po RT-
PCR wystarczającej ilości produktu, by można go
było zobaczyć po elektroforezie w żelu agarozowym.
Niektóre testy polegają na wykonaniu tylko jednej
tury amplifikacji, po której wykrywa się produkty,
wykonując
hybrydyzację
ze
znakowanymi
sondami.

Diagnostyka molekularna zakażeń wirusami hepatotropowymi
Dzięki testowi RT-PCR możliwe staje się wykrywanie zakażeń
HCV u osób, u których inne badania diagnostyczne nie dały
pewnych
wyników.
Test
RT-PCR
jest
niezbędny
do
diagnozowania wątpliwych przypadków zapalenia wątroby.
Test RT-PCR umożliwia również określenie,
jaki genotyp wirusa
występuje u badanego pacjenta. Opracowane zostały proste i
szybkie, aczkolwiek kosztowne testy pozwalające określić
sześć
głównych genotypów HCV
. Należy się jednak zastanowić nad
zasadnością wykonywania takich badań przed rozpoczęciem terapii
interferonem. Istnieją rzeczywiście pewne dane wskazujące, że
niektóre genotypy HCV są bardziej oporne na leczenie
interferonem. Nadal jednak nie wiadomo, czy efekt ten jest zależny
jedynie od genotypu wirusa, czy od ilości wirusa w organizmie
chorego, czy też ilość wirusa zależy od rodzaju genotypu. Pewna
grupa pacjentów zakażonych HCV o domniemanej wyższej
odporności na interferon poddaje się jednak leczeniu. Należy
zatem zalecać, by genotypowanie wirusa wykonywać dopiero po
kilku miesiącach terapii, równocześnie z testem ilościowej PCR,
który pozwoli ocenić, czy leczenie jest skuteczne.

Diagnostyka molekularna zakażeń wirusami hepatotropowymi
Zgodnie z najnowszymi zaleceniami w przypadku
rozważania
leczenia
przeciwwirusowego
obowiązkowymi testami jest poziom HCV surowicy,
ocena genotypu wirusa. Wynik tego badania, czyli
rodzaj genotypu, wpływa na czas terapii (24 lub 48
tyg.). Na przykład zakażeni HCV genotypem 1, 4, 5
lub 6 powinni mieć oznaczenie wielkości wiremii
przed włączeniem terapii przeciwwirusowej, gdyż
zalecana jest dłuższa 48-tygodniowa terapia.
Kolejne badanie ilościowe HCV-RNA wykonuje się do 12
i po 24 tygodniach leczenia. Jedynie w przypadkach
genotypu 2 i 3 oznaczenia ilościowe nie są
restrykcyjnie wymagane, a leczenie trwa 24
tygodnie, gdyż wirusa o tym genotypie łatwiej jest
wyeliminować.

Diagnostyka molekularna zakażeń wirusami hepatotropowymi
Mimo iż diagnostyka zakażeń HBV jest lepiej rozwinięta
niż HCV, to jednak stosowanie testów PCR jest przydatne ze
względu na ich wysoką czułość i specyficzność. Wykrywanie
HBV polega na amplifikacji fragmentu jego DNA i możliwe
jest dzięki tej metodzie określenie, z jakim szczepem wirusa
mamy do czynienia.
Nowością w zakresie diagnostyki genetycznej stosowanej
w zakresie infekcji wirusem HBV jest wykrywanie mutacji
wirusa odpornych na działanie leku przeciwwirusowego-
lamiwudyny. Ponieważ w wielu przypadkach po pewnym
czasie stosowania leku (po roku leczenia lamiwudyną u
około 16-32% zakażonych HBV-DNA rozwija mutację YMDD)
WZW B uodparnia się na jego istnienie stąd konieczne jest
wykonywanie do wykonywania badań mających na celu
wykrycie mutacji wirusa (genotypowanie) odpowiedzialnych
za rozwijającą się w trakcie leczenia lekooporność.

Niealkoholowe stłuszczeniowe
zapalenie wątroby (nonalkoholic
steatohepatitis – NASH)
NASH rozpoznajemy tylko u osób, które nie
nadużywają alkoholu.
Częstość występowania choroby alkoholowej wątroby wzrasta
dopiero przy częstym przekraczaniu pewnego „progu” spożycia
alkoholu (tj. 20 g etanolu na dobę u kobiet i 80 g etanolu na
dobę u mężczyzn).
Testy powszechnie stosowane w celu wykrycia nałogowego
picia alkoholu np.
wzrost aktywności aminotransferaz
wzrost aktywności GTP
zmiana średniej objętości krwinki czerwonej
mogą być zmienione przez samą chorobę wątroby i wówczas
oceniane spożycie alkoholu może być zawyżone.
1.Częściowo desialylowana transferyna (partially desialylated
transferrin, dTf)
2.Stosunek dTf/Tf (transferyna całkowita) prawdopodobnie
najlepiej odzwierciedla przewlekłe nadużywanie alkoholu
(czułość 81%, swoistość 98%).
Biopsja wątroby pozostaje najlepszym badaniem
diagnostycznym dla potwierdzenia klinicznego.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
Wyszukiwarka
Podobne podstrony:
Diagnostyka laboratoryjna chorób przewodu pokarmowego analityka
Diagnostyka laboratoryjna chorób przewodu pokarmowego (+)
Diagnostyka laboratoryjna chorob przewodu pokarmowego, Zaliczone, Diagnostyka, analityka
Laboratoryjna diagnostyka chorob przewodu pokarmowego IV L
Diagnostyka laboratoryjna chorób serca i mięśni poprzecz (2)
Choroby przewodu pokarmowego
Choroby przewodu pokarmowego 4
CHOROBY PRZEWODU POKARMOWEGO
Leki stosowane w chorobach przewodu pokarmowego, Farmakologia
Choroby przewodu pokarmowego, Kliniczny zarys chorób
Dieta w chorobach przewodu pokarmowego(1)
Diagnostyka laboratoryjna chorob trzustki oraz cukrzycy koni i bydla mlecznego
Choroby przewodu pokarmowego Ć TŁwi Ć TŁ
Nowotwory przewodu pokarmowego ppt
Choroby przewodu pokarmowego 2
Choroby przewodu pokarmowego
więcej podobnych podstron