
LECZENIE SZPICZAKA MNOGIEGO
Piotr Boguradzki
Klinika Hematologii, Onkologii i Chorób
Wewnętrznych
Akademii Medycznej w Warszawie

SZPICZAK PLAZMOCYTOWY
Istota choroby-klonalny, nowotworowy rozrost
plazmocytów syntetyzujących nadmierne ilości
nieprawidłowych immunoglobulin lub ich fragmentów
Wiek, >60 lat, mediana 65lat, M:K=3:2, zachorowalność
4/100000/rok
Etiologia:-czynniki fizyczne (promieniowanie),
- chemiczne (azbest, kadm, ołów, benzen),
- biologiczne (przewlekłe zakażenia, stymulacja
antygenowa)
Anomalie chromosomowe-35%-65%
- chromosomy-14,1,6

Diagnostyka
Cele:
1. Określenie stadium zaawansowania choroby
2. Wykrycie sytuacji wymagających szybkiej
interwencji
• hiperkalcemia
• zespół nadlepkości
• ciężka niewydolność nerek
• zagrażające złamania patologiczne

Diagnostyka
• β
2
-microglobulina, LDH, CRP
• Wapń w surowicy
(30% hiperkalcemia)
• Biopsja szpiku kostnego
• Zdjęcia RTG
–
czaszka, kręgosłup, żebra, k. ramienia
i staw łokciowy, miednica, k. Udowe
i staw kolanowy
• D
obowa
Z
biórka
M
oczu
–
oznaczenie wydalanego
białka, wapnia i fosforanów
• Immunoglobuliny
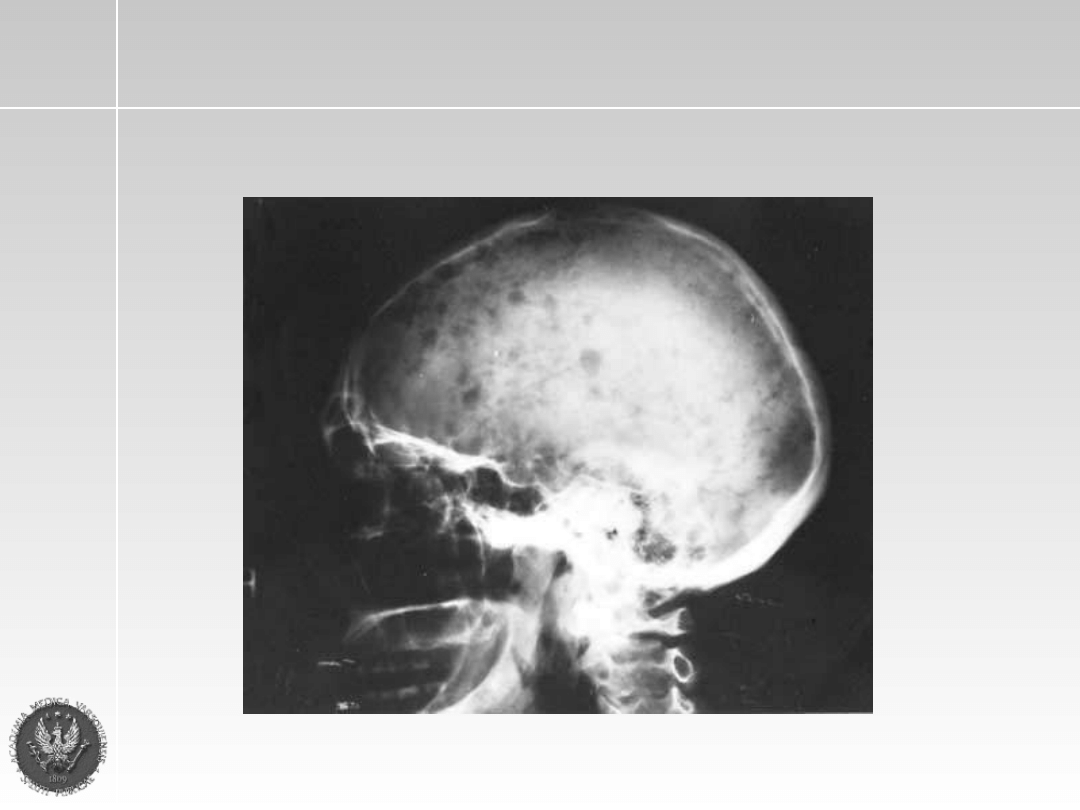
Zmiany osteolityczne
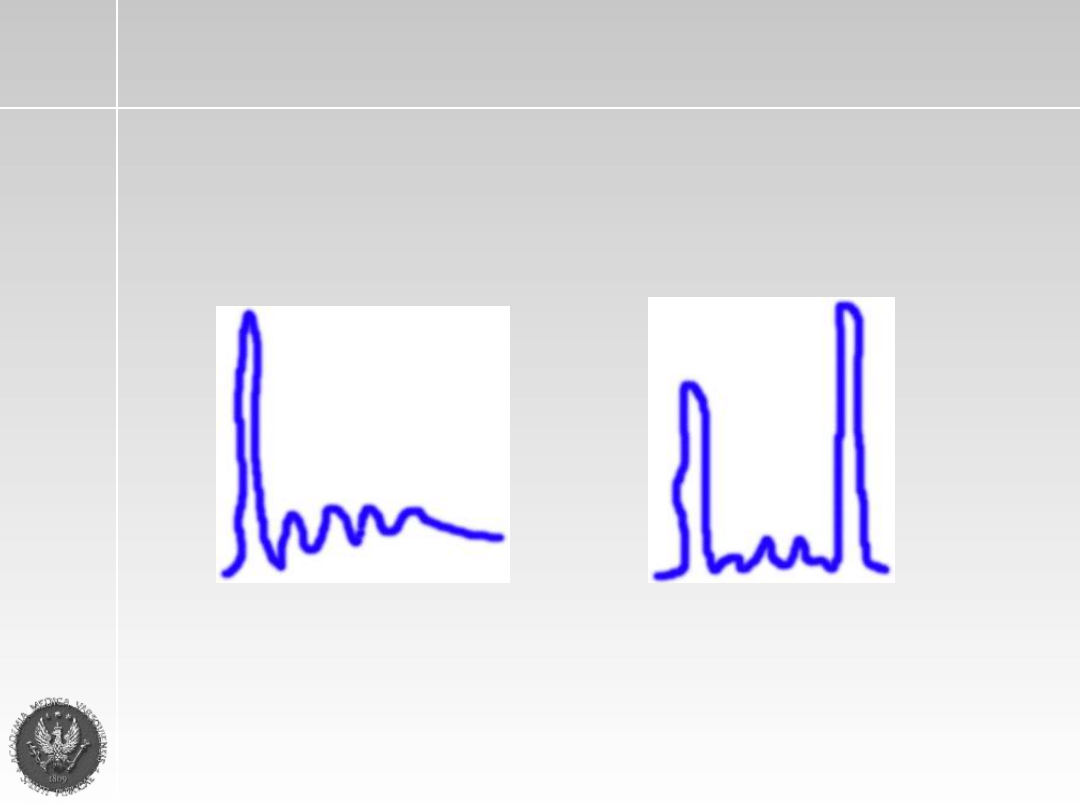
Diagnostyka
• Proteinogram – elektroforeza (krew i mocz)
Alb α
1
α
2
β γ
Prawidłowy
Alb α
1
α
2
β γ
„Szpiczakowy”

Rozpoznanie
Kryteria duże
• Obecność plazmocytów w biopsji
tkankowej
• Plazmocyty w szpiku 30%
• Białko monoklonalne:
3 500 mg% IgG
2 000 mg% IgA
1,0 g/24 h łańcuchy lekkie w
moczu
1 kryterium duże + 1 kryterium małe

Rozpoznanie
Kryteria małe
• Plazmocyty w szpiku 10-30%
*
• Białko monoklonalne w niższym stężeniu
niż w kategoriach dużych
*
• Ogniska osteolityczne w kościach
• IgM 50 mg% IgA 100 mg%
IgG 600 mg%
3 kryteria małe
Kliniczne zaawansowanie choroby
wg Durie i Salmona
Stadium I
Stadium III
>10g/dl
Hb
<8,5 g/dl
normalny
Wapń
podwyższony
bez zmian lub z
pojedynczą zmianą
Szkielet
mnogie zmiany
ostelityczne
IgG < 5g/dl
IgA < 3g/dl
Łańcuchy lekkie w
moczu < 4g/24h
Białko
monoklonalne
IgG > 7g/dl
IgA > 5g/dl
Łańcuchy lekkie w
moczu > 12g/24h
<0,6 x 10
12
/m
2
Masa
nowotworu
>1,2 x 10
12
/m
2
ISS
(Internatilal
s
taging
s
ystem)
(the International Myeloma Working Group 2003)
Stadium
β
2
-microglobulina
albuminy
Średnie
przeżycie
-miesiące
I
<3.5
>=3,5
62
II
<3.5
lub 3.5 do 5.5
<3.5
44
III
>=5.5
29

Leczenie
• Leczenie choroby podstawowej (MM)
• Leczenie wspomagające - powikłań choroby

Okresy choroby w zależności
od leczenia
indukcja remisji
faza stacjonarna “plateau”
progresja choroby
faza niekontrolowanego wzrostu

Kryteria remisji choroby
wg zasady Myeloma Task Force
Remisja całkowita:
całkowite zniknięcie białka monklonalnego w surowicy i
w moczu przez co najmniej 6 tyg.
< 5% pazmocytów w biopsji szpiku
stacjonarna faza choroby kostnej
zniknięcie guzów odosobnionych pozakostnych

Kryteria remisji choroby
wg zasady Myeloma Task Force
Remisja częsciowa
zmniejszenie o co najmniej 50% odsetka
plazmocytów w szpiku przez co najmniej 6 tyg.
zmniejszenie o co najmniej 50% stężenia białka M
i/lub zmniejszenie o 50% białka monoklonalnego w
moczu przez co najmniej 6 tyg.
normalizacja stężenia białka całkowitego w
surowicy krwi,
zmniejszenie≥ 50% rozmiarów guzów
odosobnionych pozakostnych
normalizacja obrazu krwi,
stacjonarna faza choroby kostnej

Kryteria progresji choroby:
progresywny wzrost stężenia białka M w
surowicy krwi, o co najmniej 10g/l w stosunku do
wartości przed leczeniem
zwiększenie ilości łańcucha lekkiego
immunoglobulin
w moczu o 100% w stosunku do wartości przed
leczeniem
wystąpienie hiperkalcemii ( powyżej 2,75mmol/l)
mimo leczenia przeciwnowotworowego.

Kryteria progresji choroby
progresywny wzrost stężenia białka M w surowicy
krwi, o co najmniej 10g/l w stosunku do wartości
przed leczeniem
zwiększenie ilości łańcucha lekkiego
immunoglobulin
w moczu o 100% w stosunku do wartości przed
leczeniem
wystąpienie hiperkalcemii( powyżej 2,75mmol/l)
mimo leczenia
przeciwnowotworowego.

Negatywne czynniki rokownicze
w szpiczaku plazmocytowym
zły stan ogólny chorego przed leczeniem
niewydolność nerek
zmniejszona liczba krwinek białych i
płytkowych
typ A lub/i lambda białka monoklonalnego
obecność białka Bence-Jonesa
III stadium kliniczne
wiek ≥ 65 r.ż

Negatywne czynniki rokownicze
w szpiczaku plazmocytowym
Genetyczne:
–delecja 13q,
- delecja 17p,
- t(11:14) (q13;q32)
- hipodiploidia DNA
- zwiększona ekspresja onkogenu H-ras
- mutacje onkogenu N/K-ras

Negatywne czynniki rokownicze
w szpiczaku plazmocytowym
Biochemiczne
podwyższony stężenie
2
mikroglobuliny
>6 mg/l
podwyższony stężenie IL6(>6 mg/l)
podwyższone stężenie CRP (>6 mg/l)
podwyższone stężenie LDH
duże stężenie rozpuszczalnej formy
CD56 (sCD56) w surowicy

Negatywne czynniki rokownicze
w szpiczaku plazmocytowym
Histopatologiczne
Plazmoblastyczny i niedojrzały typ rozrostu
Zajęcie szpiku kostnego w postaci „litego”
nacieku

Określenie celu terapii
Całkowita remisja-wyleczenie-
- przeszczepienie allogenicznych komórek
krwiotwórczych u chorych poniżej 60 roku
życia mających zgodnego dawcę w układzie HLA,
Długotrwała remisja-
- przeszczepienie autologicznych komórek
krwiotwórczych szpiku u chorych powyżej 65 roku
życia lub tych ,którzy nie mają zgodnego
dawcy
- klasyczna chemioterapia

Rodzaj terapii
• Leczenie indukcyjne I-Melfalan
• Leczenie indukcyjne II-VAD + PBSCT
• Leczenie indukcyjne III-klasyczna
chemioterapia
• Leczenie postaci opornych IV

Leczenie indukcyjne I
Melfalan wg programu M1
I stopień zaawansowania klinicznego wg D-S
z dobrymi czynnikami rokowniczym
Chorzy powyżej 70rż
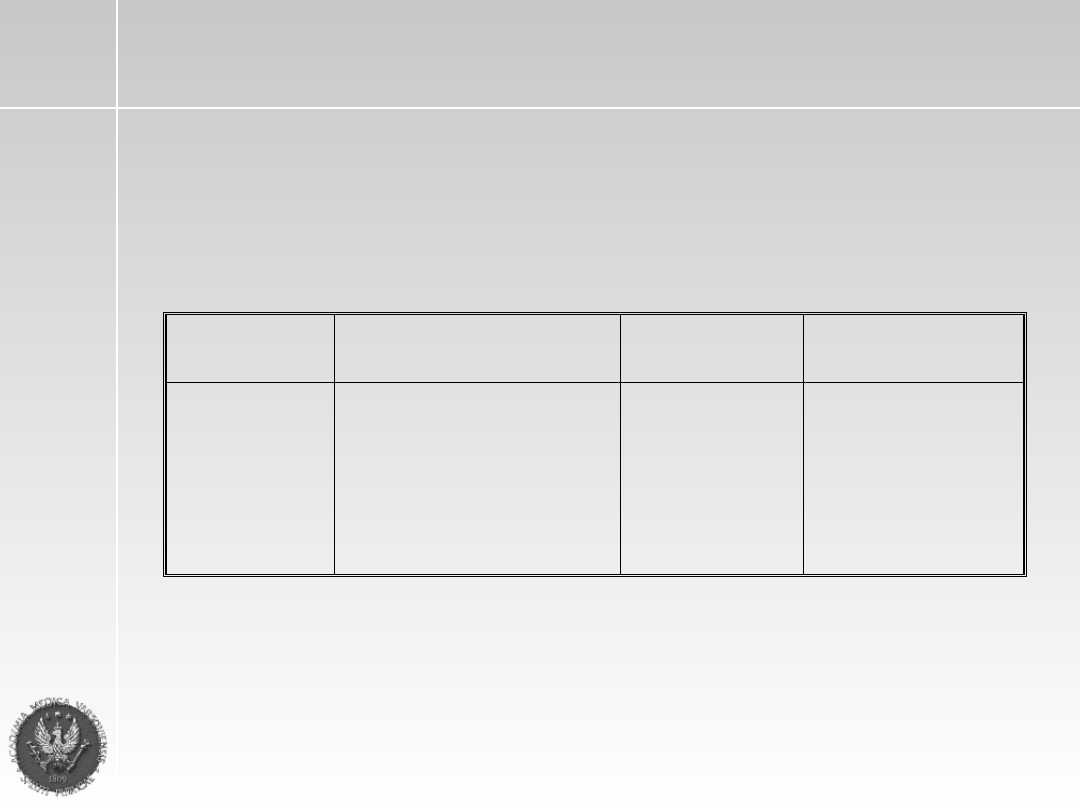
Leczenie indukujące
wg schematu M - 1
Lek
Dawkowanie dzienna,
droga podawania
Dni stosowania
Uwagi
Alkeran
Ewentualnie
+ Enkorton
0,15 mg/kg m.c. p.o.
1mg/kg wagi m.c. p.o.
1-7 dni
1-7 dni
Przerwa między
kuracjami wynosi
4 tygodnie.

Leczenie indukcyjne
wg schematu M - 1
Po 6 kuracjach tego typu, w przypadku uzyskania
regresji zmian chorobowych, wydłużamy przerwy
między kuracjami do 8 tygodni, leczenie
kontynuujemy do 12 – 18 miesięcy,
W przypadku uzyskania stabilnej fazy “plateau”
choroby zaprzestajemy leczenia cytostatycznego
U pacjentów z tendencją do przedłużającej się
cytopenii stosuje się duże dawki sterydów:
Metylprednizolon w dawce 2g i.v. 3 x w tygodniu -
przez 4 tygodnie,
a następnie po uzyskaniu poprawy: 2g i.v. 1 x w
tygodniu a la longue.

Wysokodawkowane kortykosterydy
Plusy
• Łatwość podania
• Brak znaczącego toksycznego wpływu na szpik
• Można stosować u osób starszych
• Ominięcie alkilujących chemioterapeutyków – można
je lepiej użyć w innym momencie.
• Polecane u chorych z niewydolnością nerek (DEX)
• Odpowiedź na takie leczenie w 60%-70%
nieleczonych dotąd przypadków (taka jak w
przypadku chemioterapii VAD) – II etap badań
klinicznych

Leczenie indukcyjne II
Wysokodawkowa polichemioterapia indukcyjna z
przeszczepianiem komórek krwiotwórczych
poniżej do 70 r.ż
w III okresie zaawansowania klinicznego choroby
z dużą masą nowotworową, z wybitnym
rozrostem plazmocytów w szpiku stanowiącym
70-100% komórek jądrzastych, o dużej
aktywności proliferacyjnej z dominującymi
komórkami w fazie syntezy DNA,

Leczenie indukcyjne II
a także z zaburzeniami chromosomalnymi
[del13,del 13q, 11q,t(4;14)]
z rozsiano-guzkową postacią rozrostu
z typem plazmoblastycznym rozrostu
chorzy z czynnikami złego rokowania (dużego
ryzyka), a zwłaszcza z głęboką
niedokrwistością uzależnioną od rozrostu
nowotworowego oraz hiperkalcemią,

Leczenie indukcyjne II c.d.
•
z bardzo wysokim stężeniem białka
monoklonalnego w surowicy powodującym
żelifikację surowicy i związane z tym objawy
kliniczne (IgG powyżej 70g/l lub IgA powyżej
50g/l)
• poronną postacią szpiczaka plazmocytowego
typu lambda,
• ze stężeniem beta
2
-mikroglobuliny w surowicy
krwi powyżej 6 mg/l.
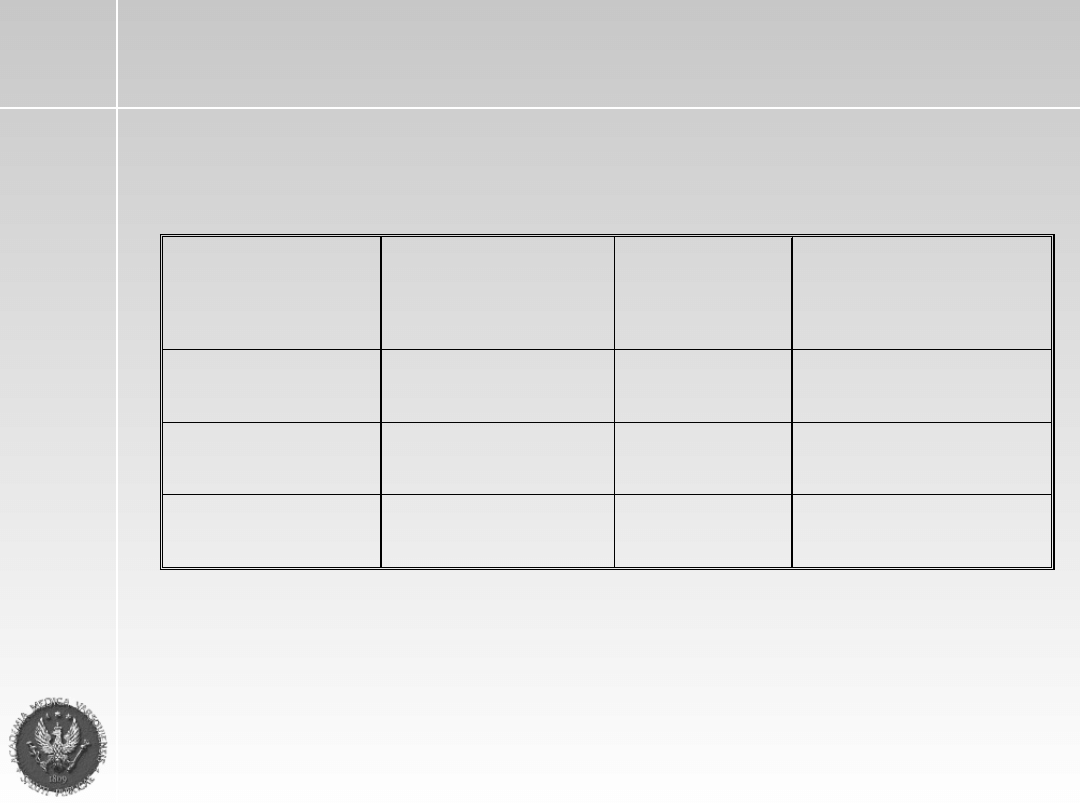
Leczenie indukcyjne II
Lek
Dawkowanie
dzienna, droga
podawania
Dni
stosowania
Uwagi
VCR
(winkrystyna)
0,5 mg i.v.
1-4 dzień
W ciągłej 24 h infuzji
ADM
(adriblastyna)
9mg/m2 i.v.
1-4 dzień
W ciągłej 24 h infuzji
DX
(deksametazon)
40mg/24 h p.o.
lub i.v.
1-4 dzień
9-12 dzień,
17-20 dzień
.

Leczenie indukcyjne II
Zmodyfikowany schemat zakłada podawanie DX
tylko pierwsze cztery dni w cyklu
przerwa między kuracjami wynosi 3- 4 tygodnie,
po 3 kuracjach VAD dokonujemy oceny wyników
dotychczasowego leczenia i w przypadku
uzyskania remisji kwalifikujemy chorego do
zabiegu transplantacji komórek krwi lub szpiku,

Leczenie indukcyjne II
w przypadku oporności na VAD, po 2-3
cyklach można dodać cyklosporynę A
(Neoral)-2x100mg przez 5 dni -
rozpoczynając jeden dzień przed podaniem
kuracji VAD,
w przypadku przeciwwskazań do stosowania
antracyklin (choroby serca, przebyty zawał)
można stosować preparat o mniejszej
kariotoksyczności (np. idarubicynę,
liposomalna doxorubicyna) lub podawać
antracykliny z osłoną dekstrazoxanu.

Leczenie indukcyjne II
• Schematy alternatywne do VAD
• VAMP (VCR, DOX, Methylprednisolon)
• C-VAMP (CTX,VCR,DOX,Methylprednisolon)
• DVD (DOXIL,VCR,DEX)
• Z-DEX (IDARUBICYNA,DEX)
• MOD (MITOXANTRON,VCR,DEX)

Autotransplantacja-PBSCT-
po podaniu submieloablacyjnej chemioterapii
Melfalanem(MEL200)
• Leczenie wstępne-3x VAD-redukcja masy
nowotworu
• Mobilizacja lecząca- wysokie dawki CTX-4g/m
2
-2x/24h+ forsowana diureza-3l/m
2
lub Mesna 4g/m
2
w 5 podzielonych dawkach
• GM-CSF 250mikrogramów/m
2
• Pobieranie komórek macierzystych (drogą
aferezy z krwi, gdy leukocytoza>2tyś./microL tj.
zwykle ok. 10 dni po podaniu CTX) i
przeszczepianie(3 zabiegi po co najmniej 2 x 10
6
/kg CD34+ komórek) poprzedzone trzykrotnym
podaniem Melfalanu 200mg/m
2
.
• (MEL100mg/m
2
, MEL140mg/m
2
)

Leczenie indukcyjne III
wg. schematu M- 2
II i III stopień zaawansowania klinicznego
MM wg D-S ; z dobrymi czynnikami
rokowniczymi
Chorzy powyżej 70rż lub młodsi z
obciążeniami kardiologicznymi
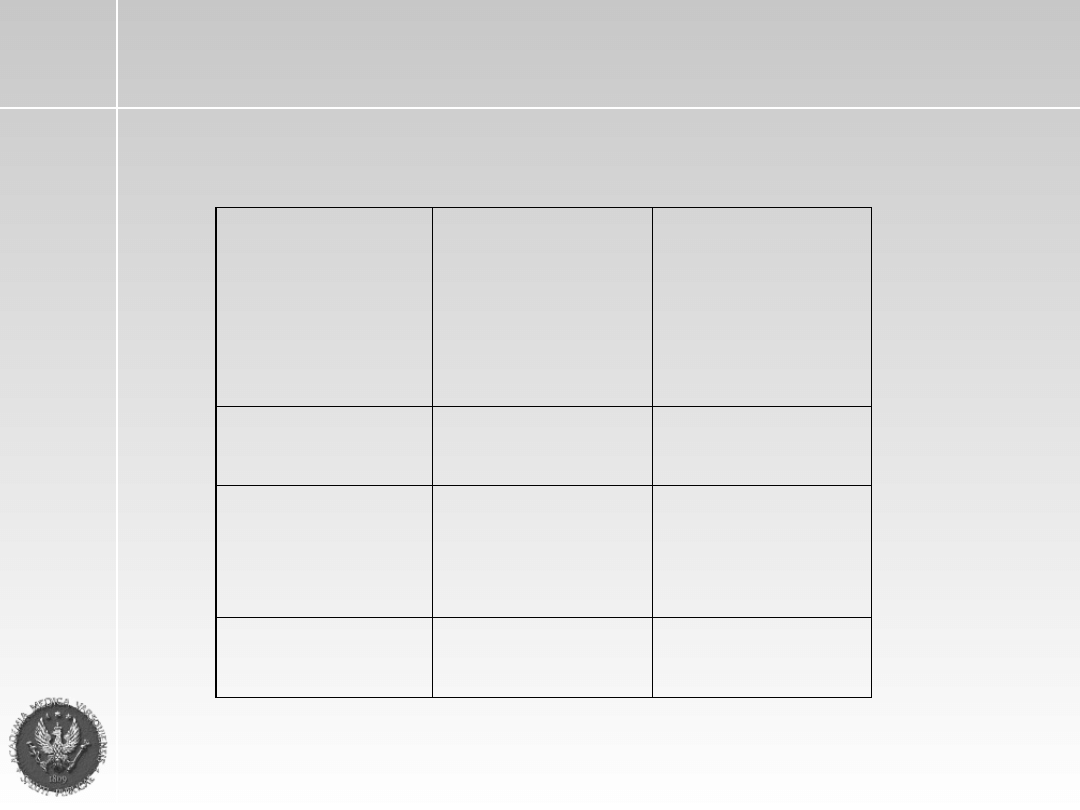
Leczenie indukcyjne III
wg. schematu M- 2
BCNU
Lub zamiennie
Lomustyna
1mg/kg m.c. iv.
w 250ml 0,9%
NaCl w 30-60 min.
wlewie
75mg/m2 p.o.
1 dnia kuracji
1 dnia kuracji
CPA (cyklofosfamid)
10 mg/kg m.c. i.v.
w 500ml 0,9% NaCl
1dnia kuracji
Anti-Uron
(MESNA)
250mg/m
2
i.v.
Przed- i po- CPA i.v.
1dnia kuracji
Enkorton
1mg/kg m.c. p.o.
1-5 lub 7 dni

Leczenie indukcyjne M2
W przypadku braku oczekiwanego efektu po
6 kursach leczenia schematem M-2, przy braku
progresji choroby, przeprowadzamy jeszcze 3
kursy leczenia tym samym schematem z
dodatkiem werapamilu (Isoptin) 3x80mg/dz
lub cyclosporyny A.
Werapamil stosujemy w celu przełamania
wielolekowej oporności na cytostatyki (MDR-
MultiDrug Resistance), z jednodniowym
wyprzedzeniem w stosunku do chemioterapii i
przez cały okres chemioterapii.

Leczenie indukcyjne M2
W przypadku remisji uzyskanej za pomocą
schematu M-2 rozpoczynamy leczenie
podtrzymujące samym interferonem alfa w
dawce 3mln j. trzy razy w tygodniu podskórnie,
lub zaprzestajemy chemioterapii stosując u
pacjenta bisfosfoniany

Leczenie progresji choroby
• DCEP (Dex, CTX, VP-16,cisplatin)
• DT-PACE
(Dex, Thal,cisplatin,adriamycin,CTX,VP-16)
• BLT-D (clarytromycyna, Thal-małe dawki,Dex)

Nowe metody leczenia
1. Związki antyangiogenne - Thalidomid i jego
analogi Revimid i Actimid
2. Ihibitory proteasomów – Bortezomib
3. Trójtlenek arsenu

Thalidomid
• Mechanizm działania:
• Zwiększa odsetek komórek MM w fazie G1 i
powoduje ich appoptozę
• Zmniejsza wiązanie komórek MM z
podścieliskiem szpiku
• Zmniejsza aktywność i produkcję cytokin(Il-6,
TNF-alfa)
• Zmniejsza angiogenezę (VEGF)
• Zwiększa odpowiedź immunologiczną chorego
przeciw MM (IL-2, INF-gamma, CD8+,NK)

Thalidomid
• Dawkowanie: 50-100mg/d p.o (200-800mg/d
p.os.)
• Łączony z dexamethasonem (2x200mg i.v 1-4
dnia) daje 70-80% remisji u nieleczonych
uprzednio chorych
• Brak oceny długotrwałej takiego leczenia
• Brak randomizowanych dużych badań
klinicznych
• Częste efekty uboczne: spowolnienie, zaparcia,
neuropatia obwodowa i zakrzepica żylna
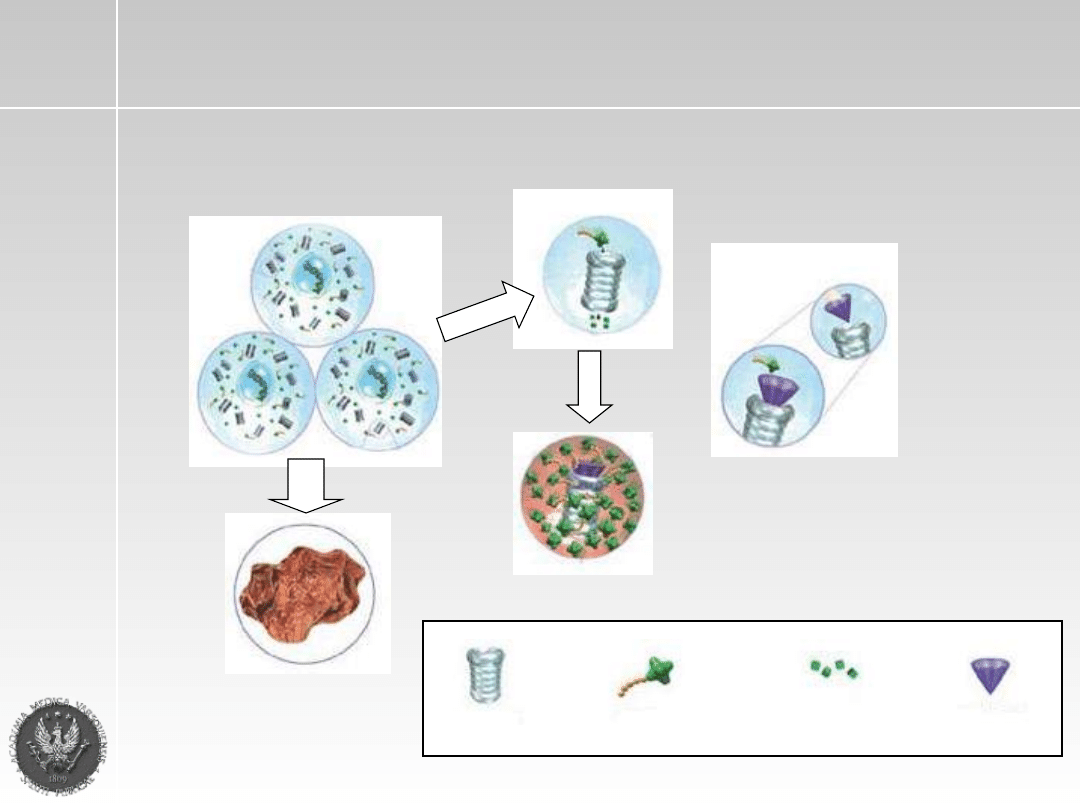
Bortezomib (Velcade)
Proteasom Białko Rozłożone białka Bortezomib
Rysunek zaadoptowany z Millennium Pharmaceuticals, Inc

Bortezomib (Velcade)
• U chorych którzy są oporni na inne leczenie –
35% odpowiedzi (badania kliniczne II fazy)
przy stosowaniu dawki 1,3mg/m2 i.v
1,4,8,11d ; cykle co 28 dni
• Działania nieporządane:
• Nudności
• Toksyczność dla szpiku (małopły tkowość,
leukopenia)
• Polineuropatia obwodowa
• Ortostatyczne spadki ciśnienia
• Wzrost męczliwości

Trójtlenek arsenu
• Punkt działania:
aktywacja apoptozy w komórkach
szpiczaka,
mechanizm działania taki jak
Thalidomidu
• Wskazania:
przypadki w których nie ma już
innych opcji terapeutycznych
• Skuteczność:
brak oceny długotrwałej takiego
leczenia
brak randomizowanych dużych badań
klinicznych

Trójtlenek arsenu (As
2
O
3
)Trisenox
• Dawkowanie:
• As
2
O
3
0,15 – 0,25mg/kg/dz. Iv 1-5, 8-12 dzień
(dwa tygodnie przerwy)
• Vit. C 1000mg/dz 1-5, 8-12 dzień(30 min. Po
As
2
O
3
, cykle powtórzyć 5-6 razy

Przeciwciała przeciwko VEGF
• Punkt działania
Przerywanie interakcji komórek szpiczka z
podścieliskiem szpiku (dodatnie sprzężenie zwrotne
Il6 - VEGF)
• Dawkowanie
• Wskazania
• Zalety
• Efekty uboczne

Leczenie wspomagające
Zapobieganie niewydolności nerek
:
odpowiednie nawodnienie pacjenta
zapewnienie diurezy ok.2 l/dz przez
infuzję 0,9%NaCl
unikanie antybiotyków nefrotoksycznych
zwłaszcza aminoglikozydów
stosowanie inhibitorów oksydazy
ksantynowej przed i w czasie kuracji
cytostatycznej (preparat Milurit
3x1tabl/dz doustnie).

Leki hamujące resorpcję kostną:
Pamidronat (Aredia) 90mg i.v. w 500ml
0,9% Na Cl w 4 godzinnym wlewie co 4
tygodnie,
Klodronat (Bonefos) 1600-2400mg/dz p.o.
a la longue
Leczenie wspomagające

Stymulacja tworzenia kości:
(stosowanie łącznie 4 leków)
Fluossen 3-6 tabl. a` 15mg/dz w czasie
posiłków,
Calcium carbonicum 4 g/dobę
Vit D
3
300 000 j raz na 2-3 tygodnie
Nerobolil (preparat anaboliczny) 50mg 1 raz
w tygodniu domięśniowo ( u chorych bez
zmian kostnych) lub 2 razy w tygodniu a`
50mg domięśniowo (u osób ze zmianami
kostnymi).
Leczenie wspomagające

Leczenie niedokrwistości:
Jeżeli poziom Hb jest mniejszy niż 11g/dl
wskazane jest zastosowanie
erytropoetyny w dawce 150 IU/kg 3 x w
tygodniu podskórnie przez okres 4-6
tygodni.
Leczenie wspomagające
Hb<11g/dl
L:Epo150IU/kg 3x/tydz.-2 tyg.
Epo end.<100mU/ml >100mU/ml
wzrost Hb>0.5g/dl <0.5g/dl
L:Epo jw przerywamy leczenie
wzrost: Hb<1g/dl >1g/dl >3g/dl Hb c.>14g/dl Hb c.>12g/dl
L:Epo 300IU/tydz. Epo jw.. Zmniejszyć przerwa do nie leczymy
dawkę o 25% <12g/dl
Leczenie wspomagające

Leczenie wspomagające
Zwalczanie hiperkalcemii:
wymuszanie diurezy przez podawanie
furosemidu po uprzednim nawodnieniu
0,9%NaCl
podawanie sterydów - Dexaven 2 - 3 amp/dz
i.v.
podawanie bisfosfonianów -
Bonefos 300mg (1 amp/dz i.v.)
w jednogodzinnym wlewie przez 5 dni lub
Kalcytonina łososiowa (Miacalcic, Calsynar,
Calcihexal) 100j s.c. 1 - 2 razy dziennie
Hemodializa

Zmniejszenie hiperproteinemii i objawów
nabytej koagulopatii
Plazmafereza powtarzana w miarę potrzeby
Leczenie wspomagające

Radioterapia:
miejscowa: w celu zmniejszenia bólów
opornych na farmakoterapię i
zabezpieczenia przed złamaniem
zagrożonych odcinków kości lub w
wypadku niebezpiecznego dla życia
ucisku tkanek przez masy
nowotworowe
ograniczone zmiany kostne -
radioterapia miejscowa 2000-3000
radów
Leczenie wspomagające

uogólnione bóle kostne i oporna na leczenie
hiperkalcemia - stosujemy napromienianie dawką
6 - 8 Gy (600-800radów) na każdą połowę ciała w
odstępach 4-6 tygodni
zajęcie centralnego układu nerwowego jest
wskazaniem do stosowania dokanałowego
metotreksatu 10-15 mg i prednisolonu 25 mg 1 x
w tygodniu, ale skuteczne jest też napromienianie
czaszki i kręgosłupa.
Leczenie wspomagające

Wysokodawkowana chemioterapia z
przeszczepieniem szpiku
• Wysokie dawki chemioterapeutyków
• Przeczepienie komórek krwiotwórczych
autologicznych (PBSC - częste) lub
allogenicznych
• W przypadku autologicznego przeszczepienia
szpiku – znaczna redukcja ryzyka powikłań

Konwencjonalna chemioterapia
• VAD
• Melfalan

Statyny
• Punkt działania
• Dawkowanie
• Wskazania
• Zalety
• Efekty uboczne
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
Wyszukiwarka
Podobne podstrony:
Szpiczak mnogi
Szpiczak mnogi 2
Szpiczak mnogi slajdy19
Szpiczak mnogi MELOMA MULTIPLEX?aaa
Szpiczak mnogi
Szpiczak mnogi
Szpiczak Mnogi poradnik pacjenta
Szpiczak mnogi – historia badań nad chorobą, epidemiologia, patofizjologia, objawy kliniczne oraz na
2 Objawy kliniczne w szpiczaku plazmocytowym – patomechanizm objawów 2id 19582 ppt
Szpiczak, interna
2 Objawy kliniczne w szpiczaku plazmocytowym – patomechanizm objawów 1
Szpiczak
Białka oporności wielolekowej w szpiczaku mnogim
najnowsze metody leczenia chorób hematologicznych, w tym szpiczaka mnogiego
CZYRAK MNOGI, ZDROWIE-Medycyna naturalna, 3-Medycyna chińska, MEDYCYNA CHIŃSKA-choroby
Szpiczak
03 0000 040 02 Leczenie opornych postaci szpiczaka mnogiego plazmocytowego
2 Objawy kliniczne w szpiczaku plazmocytowym – patomechanizm objawów 3
więcej podobnych podstron