
Nadciśnienie tętnicze
hormonalne
Jadwiga Słowińska-
Jadwiga Słowińska-
Srzednicka
Srzednicka
Centrum Medyczne
Centrum Medyczne
Kształcenia Podyplomowego
Kształcenia Podyplomowego
Klinika Endokrynologii
Klinika Endokrynologii
Warszawa
Warszawa

Nadciśnienie w
przebiegu chorób
nadnerczy
Choroby kory nadnerczy
aldosteronizm
zespół Cushinga
nadmiar DOC
Choroby rdzenia nadnerczy
guz chromochłonny
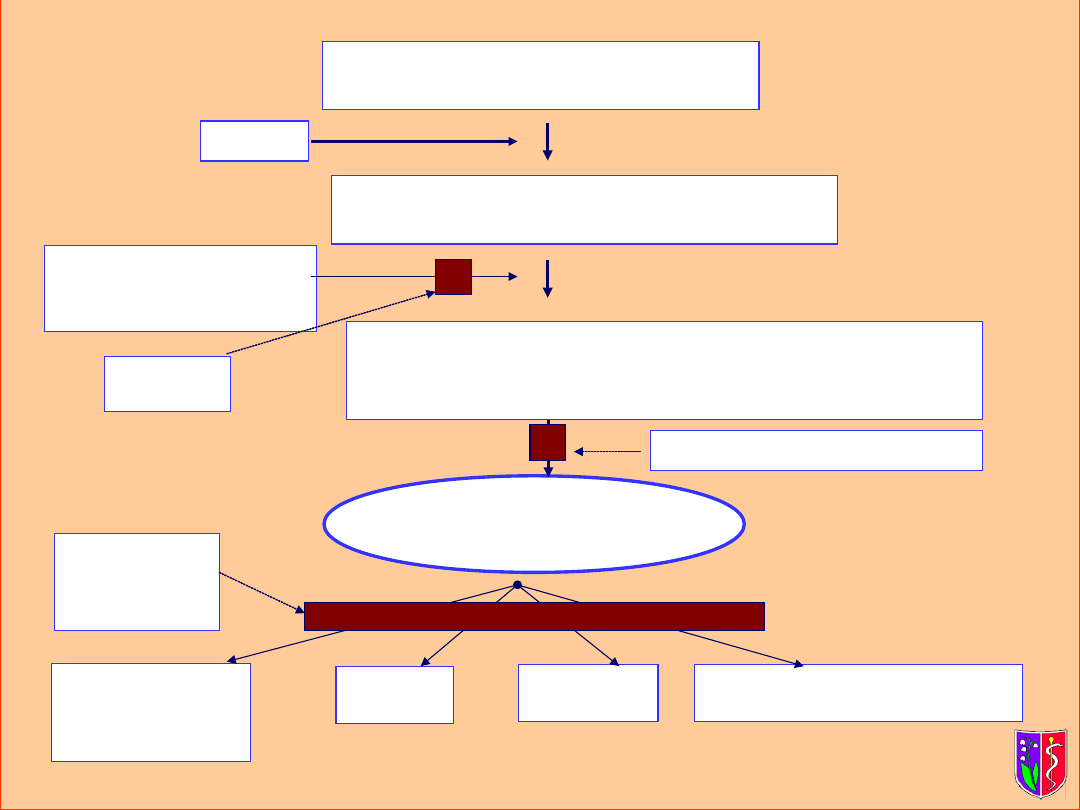
ALDOSTERON
angiotensynogen
renina
angiotensyna I(1-10
)
angiotensyna II
(1-8) działanie na AT1 i AT2 receptory )
Enzym konwertujący
angiotensynę (
ACE
)
Chymaza
. Katepsyny
blokery
aldostero
nu
nerki
ślinianki
jelito grube
serce
mózg
naczynia krwionośne
iACE
blokery angiotensyny
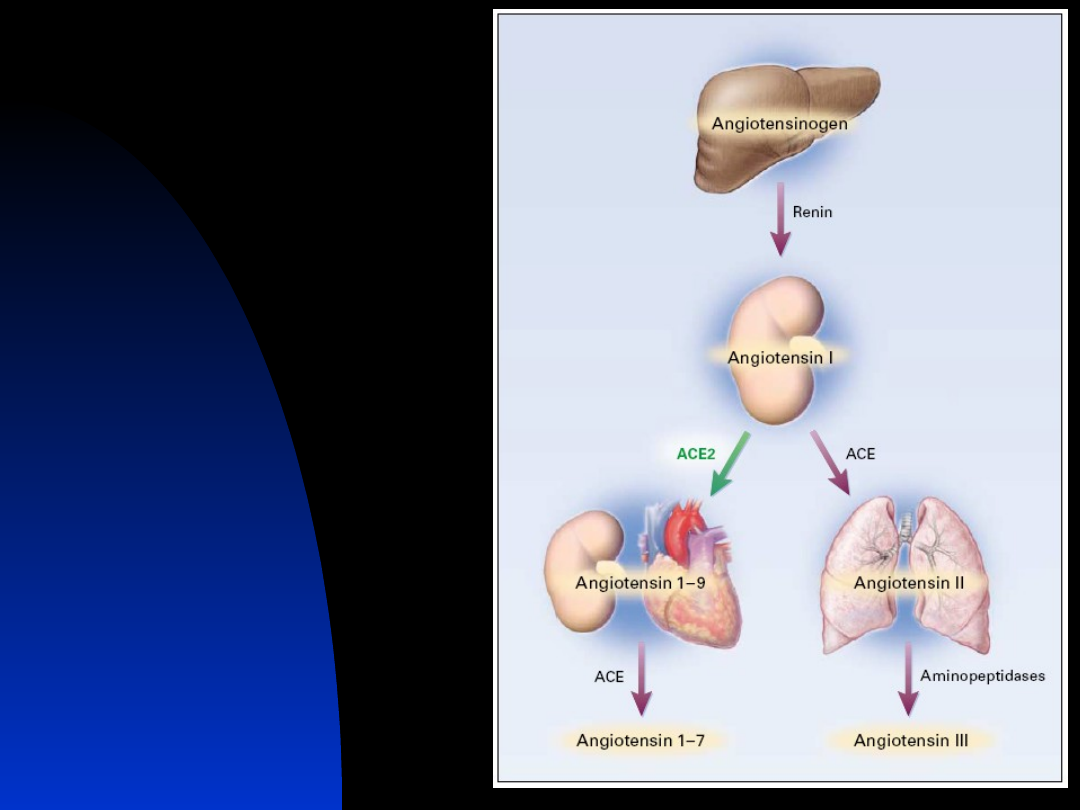
M. Boehm: NEJM 2002;347, 22:1795-
7
dod.

Układ RAA
Wytwarzanie angiotensyny I i II
zachodzi w krążeniu, w tkankach
w ścianie naczyń
W sercu ludzkim zidentyfikowano
chymazę -
główny enzym
wytwarzający angiotensynę II,
wysoka aktywność chymazy w
naczyniach wieńcowych i w
nerkach w cukrzycy

Angiotensyny
Angiotensyna I (1-10)
Angiotensyna II (1-8)
receptory AT1 i AT2
Angiotensyna III (2-8)
receptory AT1
Angiotensyna IV (3-8)
receptory AT4
Angiotensyna 1-9
Angiotensyna 1-7
onkogen mas (mas)

Receptory angiotensyny
AT
AT 1 – (ang II 1-8 i III 2-8)
Skurcz naczyń, wzrost aldo, wzrost
aktywności układu współczulnego, wzrost
komórek, zapalenia
AT2 (ang II 1-8)
działanie antagonistyczne w stosunku do AT1
pobudzenie apoptozy, ochrona tkanki
nerwowej
AT4 (ang IV 3-8)
rozszerzenie naczyń zmniejszenie transportu
sodu w nerkach
mas
(
ang 1-7
) działa antagonistycznie w
stosunku do efektów pobudzenia AT1,
hamuje wzrost komórek

Układ RAA
Stymulacja reniny i aldosteronu
dieta niskosodowa (20-30
mmol/d)
pionizacja
pionizacja + Furosemid 20-40 mg
Hamowanie reniny i aldosteronu
dieta wysokosodowa
Fludrokortyzon (Cortinef)
0,9% sól fizjologiczna

Układ RAA – wartości
prawidłowe
ARO do 1 ng/ml/h
po pionizacji: 0,7 do 3,3 ng/ml/h
Aldosteron we krwi
spoczynkowy (średnio): 77 pg/ml
po pionizacji: 50 do 200 pg/ml
Aldosteron w moczu:
5 - 19 μg/d

Aldosteron – regulacja
wydzielania
Aldosteron - warstwa kłębkowata
kortykosteron przechodzi w aldosteron
tylko w tej warstwie – 11 hydroksylaza
angiotensyna II
stężenie K
+
ACTH
dopamina i inne
warstwa kłębkowata
mała zawartość 17 hydroksylazy
koniecznej do syntezy androgenów
i kortyzolu

Mineralokortikoidy
Działanie mineralokortikoidowe
wykazują:
Aldosteron
DOC
Kortyzol
Receptory mineralokortikoidowe (MR)
- nie są selektywne
11-HSD2
dehydrogenaza 11-hydroksysteroidowa,
reguluje wiązanie sterydów z MR
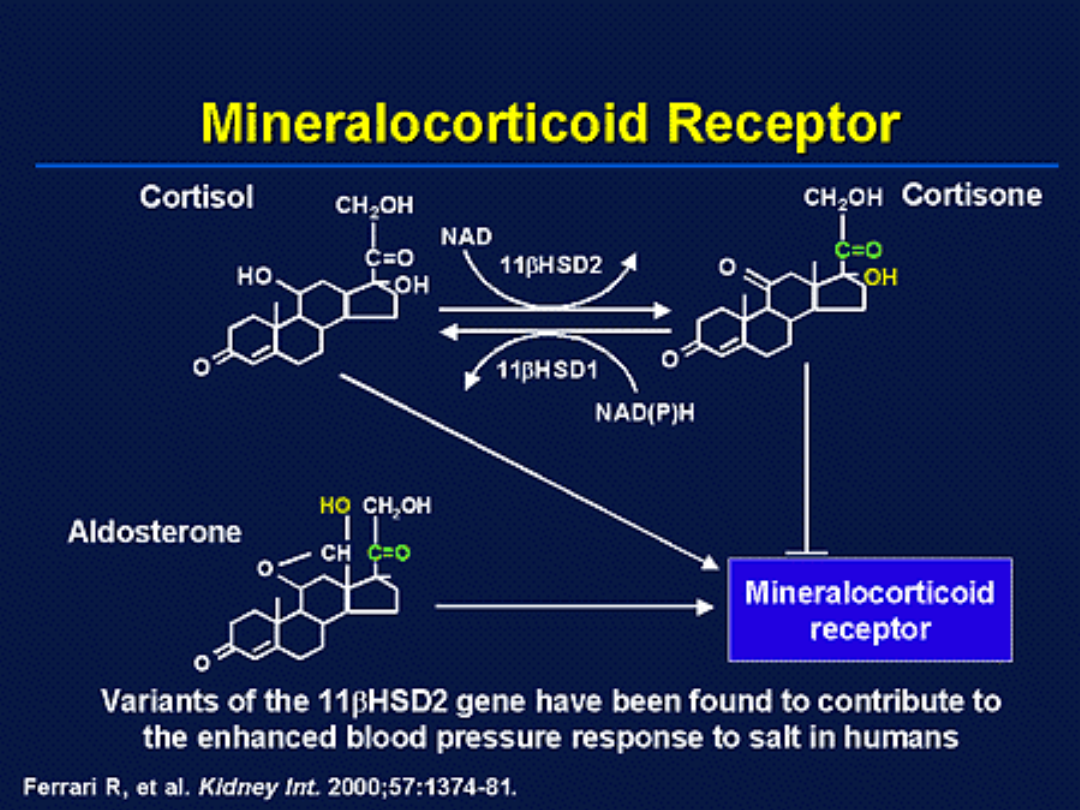

Obniżenie aktywności 11-
HSD2
Kortyzol
– receptory
mineralokortikodowe (MRI)
Sekrecja
Kortyzol
1 - 20 mg/d
Aldosteron
100 - 150 g/
d

Obniżenie aktywności 11-
HSD
2
(kortyzol- MR)
Preparaty i leki (lukrecja, carbenoxolon)
Zespół ektopowego wydzielania ACTH
Choroby wątroby (alkohol, marskość)
Choroby nerek (inhibitory ACE
zwiększają aktywność 11-HSD
2
)
Niedoczynność tarczycy

Obniżenie aktywności 11 B-
HSD2
A
pparent
M
ineralocrticoid
E
xcess
(
AME
)
Uwarunkowany genetycznie
pozorny nadmiar
mineralokrtikoidów
Leczenie DXA, antagoniści MR

Nadciśnienie tętnicze z
hipokaliemią
Hiperaldosteronizm pierwotny
Hiperaldosteronizm wtórny
Zespół Cushinga
Choroby nerek
Hipokaliemia polekowa u osoby
z nadciśnieniem tętniczym

nadciśnienie tętnicze, często o ciężkim
przebiegu
osłabienie mięśniowe, kurcze mięśni
wielomocz, wzmożone pragnienie,
parestezje, tężyczka
zaburzenia gospodarki węglowodanowej
Hiperaldosteronizm pierwotny
(zespół Conna)

Hiperaldosteronizm
pierwotny
Hipokaliemia
wydalanie K
+
z moczem (>30
mmol/l)
Hipernatremia (143-152 mmol/l)
Hipomagnezemia

Wykonywanie badań
przesiewowych
Wyrównać niedobór potasu
Odstawić spironolacton na 4 tygodni8e
Odstawić inne leki wpływające na układ
RAA na 2 tyg.
Stosować: -adrenolityki i ew. blokujace
kanał wapniowy
W badaniu ambulatoryjnymi – pozycja
pionowa przez 2-4 h przed badaniem
W badaniu szpitalnym – pobranie rano
krwi w pozycji leżącej i następnie po 2 h
pionizacji

Oznaczenie aldosteronu – leki
hipotensyjne
Verapamil 90-120 mg 2xdz.
Hydralazyna 10-12.5 mg 2xdz.
Prazosin 0.5-1.0 mg 3xdz.
Doxazosin 1-2 mg/d

Zespół Conna
A.R.O.:
<1ng/ml/h
zahamowana
aldosteronemia spoczynkowa:
>15
ng/dl
aldosteron w moczu:
>14 g/d
wskaźnik:
aldosteron (ng/dl)
ARO (ng/ml/h)
>20

ARO <1,0 ng/ml/h i brak
wzrostu po stymulacji
3 dniowa dieta ubogosolna
2-3 godziny pionizacji
poprzedzonej podaniem 20 - 40
mg furosemidu
Zespół Conna

Zespół Conna
Testy hamowania
(ostrożnie
)
3-dniowa dieta bogatosolna
ALDO w moczu: >14
g/d
0,9% roztwór soli 2,0 l i.v./4h
ALDO: >10 ng/dl lub
> 5 ng/dl
Test z fludrokortyzonem
0,2 mg 2 x dz. przez 3 dni
ALDO: >6 ng/dl lub >
5 ng/dl
Test z captoprilem
(25 mg) po 2h
ALDO 8,5-12 ng/dl (podejrzenie
Conna)
Klasyfikacja pierwotnego
hiperaldosteronizmu
Przyczyna
Częstość
występowania
Gruczolak kory
nadnerczy
65%
Przerost kory
nadnerczy
34%
Rak kory nadnerczy
<1%

Pierwotny
hiperaldosteronizm
Rodzinny hiperaldosteronizm typu 1 (1%)
Poddaje się leczeniu deksametazonem
Mutacja dwóch genów: CYP 11ß2-(syntazy
aldosteronu) + CYP-11ß1 (11ß-hydroksylazy)
występuje rodzinnie
wczesne incydenty naczyniowo-mózgowe

Pierwotny
hiperaldosteronizm
Rodzinny hiperaldosteronizm
typu 2
Mutacja genowa – nieokreślona
W nadnerczach przerost lub
gruczolak
Hiperaldosteronizm pierwotny co
najmniej u 2 krewnych

Zespół Conna
CT lub MRI nadnerczy
Jeżeli brak guza:
18 OH kortykosteron
Scyntygrafia nadnerczy
po DXA
8 mg przez 3 dni
Cewnikowanie żył nadnerczowych
(pobranie krwi na aldo i kortyzol
również z żyły głównej)

Leczenie zespołu
Conna
Gruczolak
–
operacja
normalizacja
poziomu K
+
, ale u 40% nadal nadciśnienie
tętnicze
Przerost nadnerczy
lub p/wskazania do
operacji
Spironolacton
100 - 500 mg
(hipogonadyzm, ginekomastia)
dawka podtrzymująca 75 - 100 mg
Eplerenon
25 mg 2 x
dz. (INSPRA tabl. 25 i 50 mg
Pfizer - selektywny antagonista receptora aldosteronu)
Amiloride
10 - 40 mg
Blokery kanału wapniowego
Inhibitory ACE

Pierwotny aldosteronizm
Objawy
Nadciśnienie tętnicze łagodne lub
ciężkie
Hipokaliemia (badanie przesiewowe)
Hipernatremia
Screenig test
ALDO / ARO (rano) wskaźnik >20
Aldosteronemia >15 ng/dl
Diagnoza pewna
Potwierdzenie, że guz nadnercza
wydziela aldosteron autonomicznie

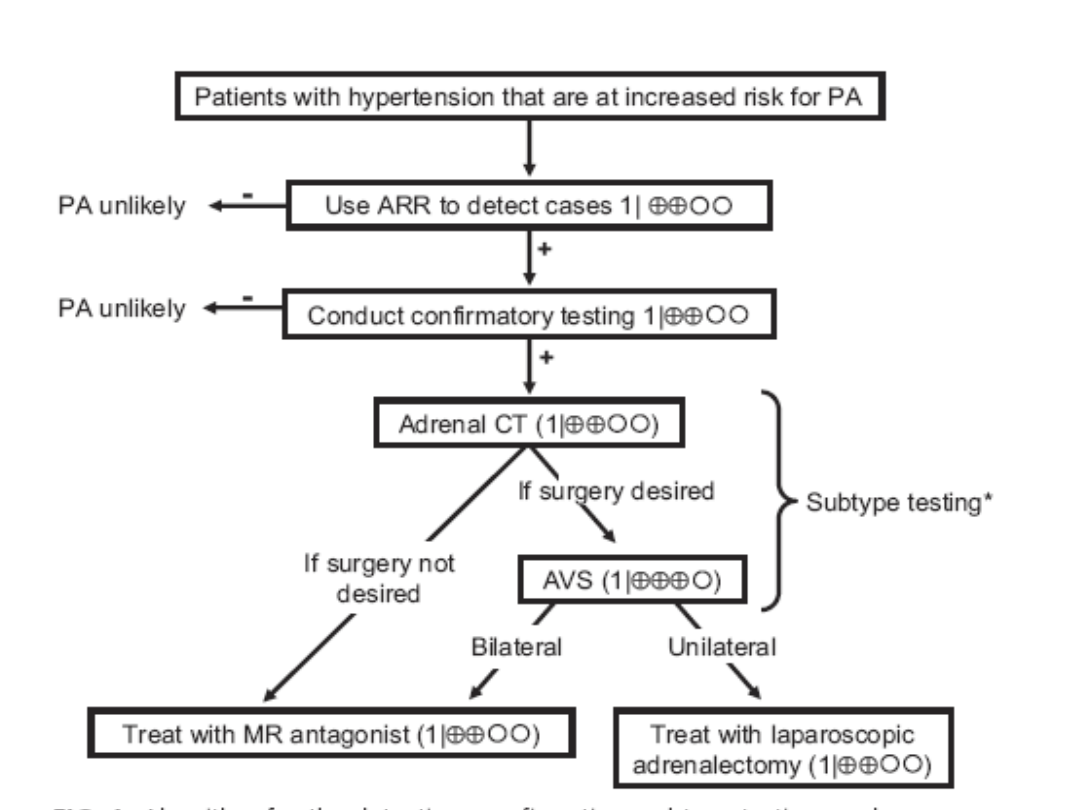
Hiperaldosteronizm pierwotny
Wytyczne 2007
Europejskiego Towarzystwa Nadciśnienia Tętniczego
Częstotliwość występowania 1-11%
Oznaczenie potasu we krwi – badanie przesiewowe
30% przypadków to gruczolaki nadnerczy
70% to przerost nadnerczy, rzadko rak lub
aldosteronizm hamowany glikokortykosterydami
Może współistnieć z guzem chromochłonnym,
nadczynnością przytarczyc i akromegalią
Często powoduje nadciśnienie oporne
Potwierdza -test z fludrokortyzonem, aro i aldo
Przydatność wskaźnika aro/aldo kontrowersyjna
Badania obrazowe MRI, TK i scyntygrafia z DXA
Dość często wyniki fałszywie dodatnie (przy
decyzji opartej tylko na TK - 25% niepotrzebnych
operacji)
N

Leki hamujące układ RAA
-blokujące
- hamują uwalnianie reniny
i wytwarzanie angiotensyny II
Inhibitory ACE:
hamują powstanie ang II z ang I
Inhibitory ARB:
znoszą efekty pobudzenia
receptorów AT1, pobudzają receptory AT2
zmniejszenie migotania przedsionków i udarów
mózgu
Opóźnienie rozwoju cukrzycy
Ochrona przed powikłaniami cukrzycy
Blokujące receptory aldosteronowe
spironolacton, eplerenon

Układ RAA a inhibitory ACE
I etap:
Obniżenie angiotensyny II
Wzrost ARO
Obniżenie aldosteronu
II etap
Wzrost stężenia potasu
Wzrost aldosteronu
Obniżenie ARO
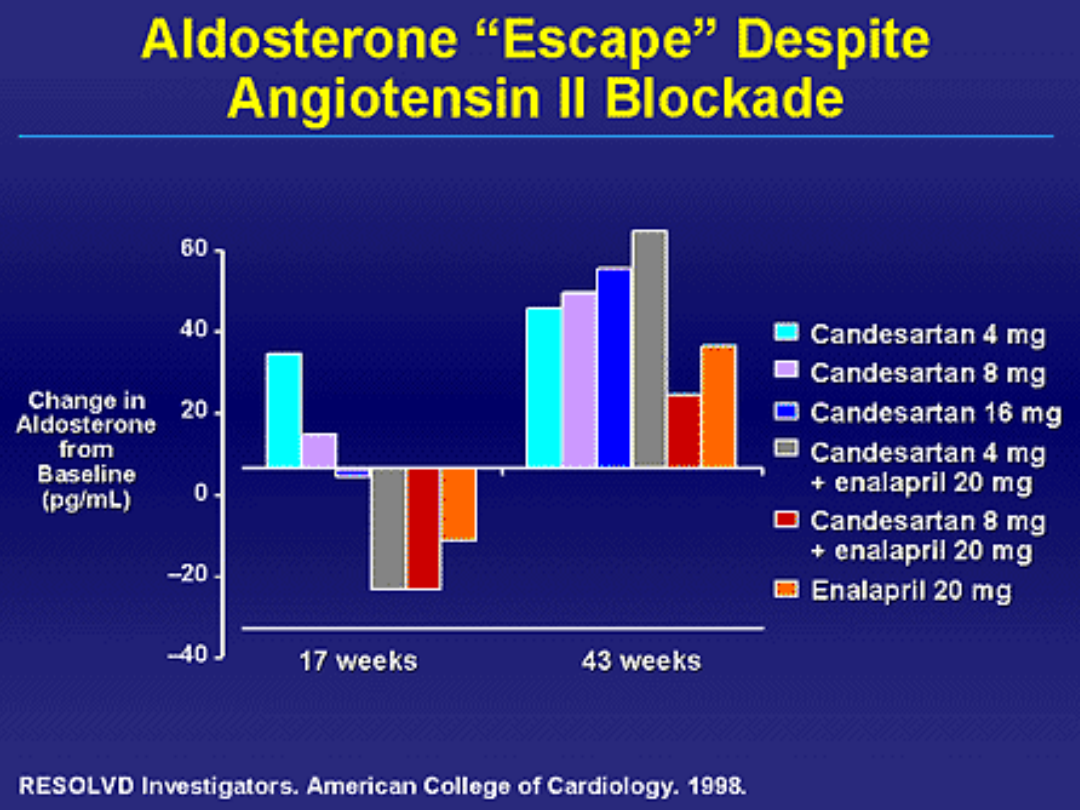
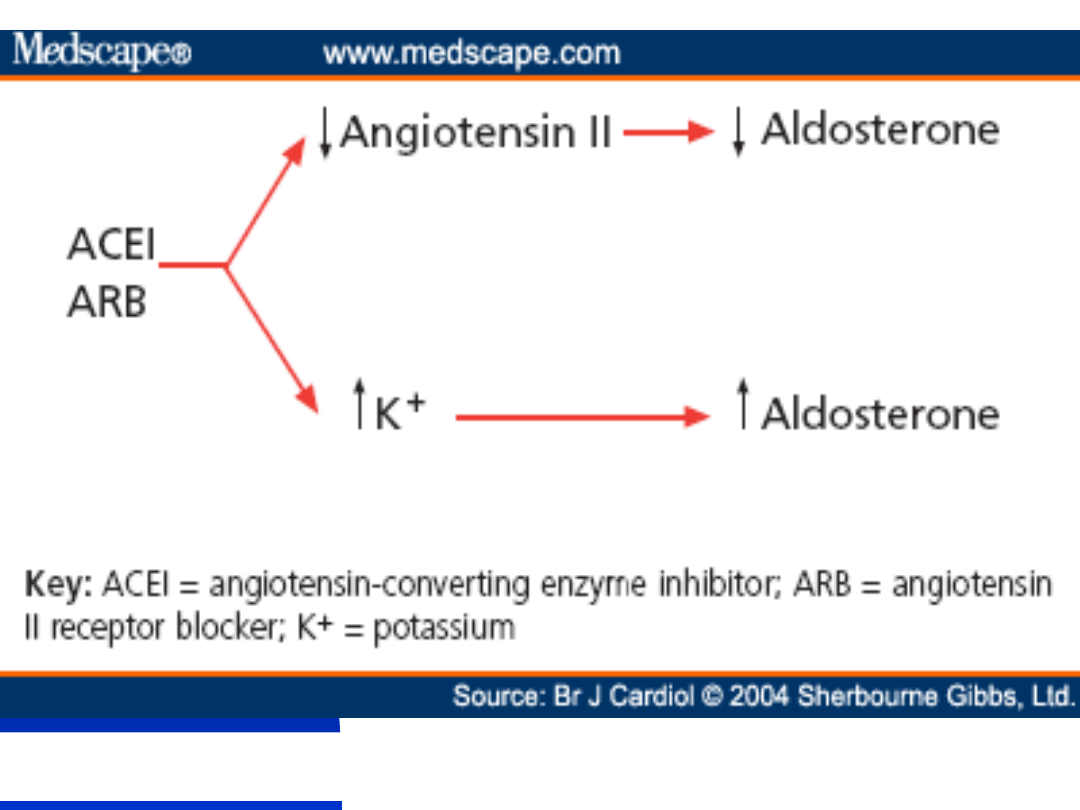
Mechanisms of aldosterone escape with ACE inhibitor
or angiotensin II receptor blocker therapy

Guz chromochłonny
nowotwór
rozwijający się z komórek
chromochłonnych
z nadmiernym
wydzielaniem katecholamin

Pheochromocytoma
wydzielane hormony
Noradrenalina
Adrenalina
Inne hormony:
ACTH
Somatotropina
Kalcytonina
PTH
VIP
Erytropoetyna
Serotonina
Interleukina 6

Guz chromochłonny
komórki układu współczulno-nadnerczowego
wydzielające KA
Klasyczne cechy kliniczne
nadciśnienie tętnicze ,napadowe bóle
głowy
poty, bladość skóry
kołatania serca, hipotonia ortostatyczna
nierozpoznany pheochromocytoma
przełomy nadciśnieniowe
zaburzenia rytmu serca
zawał serca
diagnostyka
potwierdzenie hormonalne
lokalizacja nadnerczowa lub
pozanadnerczowa (paraganglioma)

Pheochromocytoma
Objawy
Nadciśnienie tętnicze napadowe lub utrwalone,
hipotonia ortostatyczna, bladość
Screening test
Metoksykatecholaminy
Wyniki fałszywie dodatnie
Ciężkie choroby, trójcykliczne antydepresanty
i inne leki zwiększające produkcje KA
Diagnoza pewna
MRI, scyntygrafia z metajodobezyloguanidyną
131
I

Pheochromocytoma
90% to guzy chromochłonne występujące
sporadycznie, mogą być bezobjawowe
10% schorzenie dziedziczne związane z:
MEA-2A, MEA 2B
Zespół von Hippla-Lindaua
Rodzinne zespoły paraganglioma
Robert G. Dluphy: NEJM
2002;346:1486

Pheochromocytoma
Leki prowokujące Pheo
Aminy sympatykomimetyczne
Trójcykliczne antydepresanty
Silbutramina
Kokaina
Interferują z badaniami
biochemicznymi
Glukagon, sterydy, angiotensyna II,
wazopresyna, histamina
Tyramina (sery i wina)
Metoclopramid
Efedryna
Inhibitory MAO

Podstawy diagnostyki
genetycznej guzów
chromochłonnych
Germinalne mutacje genowe
protoonkogenu
RET
genu
VHL
genu
SDHD
podjednostka D dehydrogenazy
bursztynowej
genu
NF1

Guz chromochłonny
kwalifikacja do badań
genetycznych
Rejestracja chorych z pheochromocytoma
(Freiburg i Warszawa)
n = 271 (sporadyczny pheochromocytoma)
25% miało mutacje szlaku
germinalnego
w tym:
45% - mutacja VHL
20% - mutacja RET
17% - mutacja SDHD
18% - mutacja SDHB
Hartmut P.H. Neumann, Andrzej Januszewicz i inni.: NEJM
2002;346:1456

guzy chromochłonne mnogie
nowotwory w rodzinie
młody wiek
rak rdzeniasty, rak nerki, naczyniak
siatkówki, hemangioblastoma,
torbiel trzustki
neurofibroma (skóra, śluzówki)
screnning – gen RET nie
wystarczający
Guz chromochłonny
kwalifikacja do badań
genetycznych

Guz chromochłonny
Wolne metoksykatecholaminy
w osoczu
(badanie niedostępne w rutynowej pracy)
Wydalanie metoksykatecholamin
z moczem
(50-1000 mg/24h)
i
kwasu wanilinomigdałowego

Czynniki wpływające
na oznaczenia
katecholamin
methyldopa
labetalol
-adrenolityki
chinidyna
tetracykliny
erytromycyna
sulfonamidy
leki sedatywne
inhibitory MAO
chloropromazyn
a
imipramina
p/histaminowe
orzech
y
banany
cytrus
y
wanilia
herbat
a
kawa

Chromogranina A
Biologiczny marker pheochromocytoma i
guzów neuroendokrynnych
zwiększone stężenie – MEA
zespó
ł
von Hippla-Lindau, neurofibroma,
sporadyczne przypadki
pheochromocytoma
koreluje z wielkością guza
Pheochromocytoma:
188 ± 40,6 ng/ml
Pheochromo złośliwy:
2932 ± 900 ng/ml
Hypertension 2000;
36:1945

Paraganglioma
Guzy z komórek
chromochłonnych,
pozanadnerczowe (n = 236)
Lokalizacja:
69% szyja i głowa
9,5% serce, płuca, śródpiersie
21,5% w części brzusznej
Dana Erickson i wsp. - Mayo Clinic: JCEM 2001;
86:5210

Paraganglioma
lokalizacja i objawy kliniczne
Guzy szyi i głowy
nadciśnienie
nieprawidłowa masa w obrębie szyi
Poniżej szyi
nadciśnienie
hipotonia ortostatyczna,
bóle głowy
poty
Dana Erickson i wsp. – Mayo Clinic: JCEM 2001; 86:5210–5216

Guz chromochłonny
Biochemiczne potwierdzenie guza
metoksykatecholaminy w moczu/24h
kwas wanilinomigdałowy w moczu/24h
dopamina i chromogranina w osoczu
rzadko testy:
hamowania - z klonidyną
lub pobudzania - z glukagonem
CT/MRI
Scyntygrafia
z
metajodobezyloguanidyną
131
I
Trudności lokalizacyjne
diagnostyka obrazowa
PET
Badania genetyczne
w kierunku mutacji genów
VHL, RET, SDHD, SDHB - Krajowy Rejestr

Predyspozycja rodzinna
MEN 2 -
zespół gruczolakowatości
wewnątrzwydzielniczej typu 2
guz chromochłonny
rak rdzeniasty
PNP
NF1
– nerwiakowłókniakowatość typ 1
(choroba Recklinghausena) -
mutacja genu
NF1
zmiany skórne ( plamy kawa z mlekiem)
nerwiakowłókniaki
guzy o.u.n.
guz chromochłonny
rakowiak
mutacja
RET

Predyspozycja rodzinna
PPS
- zespół guza chromochłonnego
i przyzwojaków -
mutacja genu
SDHD
VHL
- zespół von Hippla-Lindaua
mutacja genu VHL
Naczyniak siatkówki
Hemangioblastoma o.u.n.
Rak jasnokomótkowy nerek
Guz chromochłonny

Lokalizacja
zmian
Tomografia komputerowa (CT
)
- gęstość
>+10 HU (jednostek Hounsfielda)
MRI
lokalizacja pozanadnerczowa
u dzieci
u kobiet w ciąży
Scyntygrafia z MIBG
123
I
Pozytronowa Scyntygrafia Emisyjna
z zastosowaniem
F18 DOPA
Scyntygrafia receptorów somatostatny
Octreoscan
-
analog somatostatyny
Endosonografia

Guz
chromochłonny
Operacja po przygotowaniu
przez 2-3 tygodnie -adrenolityki
Fenoksybenzamina
(Dibenzyran)
20 - 100 mg w dawkach podzielonych
a następnie dołączenie leku ß-adrenalitycznego
Doksazosyna
(Doxagen XL 4 mg Merck)
Cardura
1-8 mg lub Kamiren
+ lek ß-adrenalityczny
Labetalol
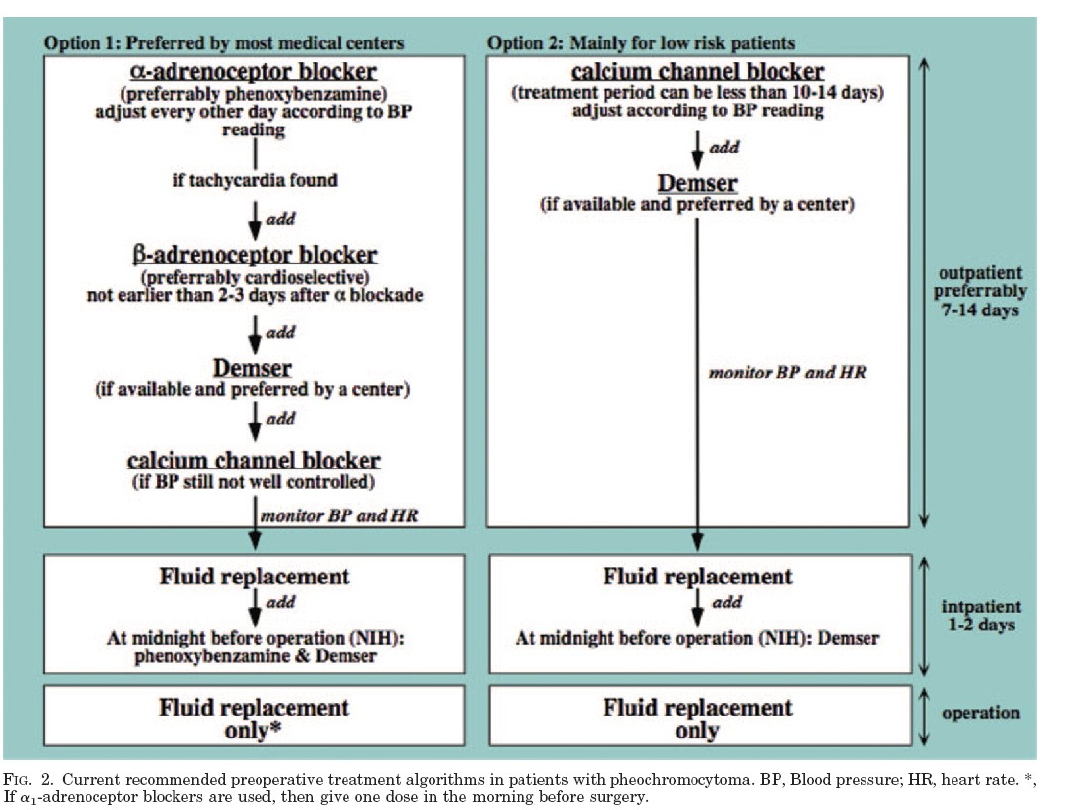

Demser
-methyl-L-thyrozyna
(analog tyrozyny) kompetycyjnie
hamuje syntezę, redukuje zapasy
katecholamin w komórkach guza
maksymalnie po 3 dobach.
Początkowo 250 mg 2-3 x /d i po 2-
3 dniach wzrost do dawki 1.5- 2.0
g

Pheochromocytoma
1/3 guzów pheochromocytoma
to guzy bezobjawowe
(traktowane jako incidentaloma)
Głównie sporadyczne
Pheochromocytoma obustronne
to głównie choroby dziedziczne
25% guzów sporadycznych ma
mutacje genowe germinalne
Guz chromochłonny
Wytyczne z 2007 r.
Europejskiego Towarzystwa Nadciśnienia Tętniczego
B. rzadka przyczyna nadciśnienia tętniczego – 0,4%
Nadciśnienie utrwalone lub napadowe
Największa czułość diagnostyczna (97-98%) wolne
metoksykatecholaminy w osoczu (mało dostępne
badanie) najbardziej polecane metoksykatecholaminy w
moczu
Testy hamowania i pobudzania po skutecznym leczeniu
antagonistą receptorów
95% guzów jest w nadnerczach
Najbardziej czułym jest TK i MRI
Scyntygrafia z MIBG- lokalizacja pozanadnerczowa
Badania genetyczne (zalecane)
Przygotowanie przed operacją (blokujące a potem
receptory)
Zespół Cushinga
ACTH zależny
%
Przyczyna
Choroba Cushinga 80 Mikro i makrogruczolak
przysadki
Ektopowe
wydzielanie
ACTH / CRF
10
Rak
owsianokomórkowy
Rakowiak
Guz chromochłonny
Rak sutka, jajnika,
prostaty, przyusznic
Grasiczak
ACTH - niezależny
10
Gruczolak nadnercza
Rak nadnercza
Guzkowy przerost
nadnercza

Objawy zespołu Cushinga
otyłość
androidalna
plethora
miopatie, zaniki
mięśni
nadciśnienie
tętnicze
czerwone rozstępy
zaburzenia
miesiączkowania
osteoporoza,
depresja
trądzik
impotencja
bezpłodność
zaburzenia
tolerancji
glukozy, cukrzyca
hipokaliemia


Nieprawidłowe:
wydalanie
wolnego kortyzolu z moczem
nocny test hamowania kortyzolu mała
dawka
DXM 1 mg
o 22:00 kortyzol
>5,0
μg/dl
Stężenie kortyzolu o 24.00
>7,5 μg/dl
Zespół Cushinga
Test hamowania DXA 2 mg/d przez dwa
dni lub hamowanie dużą dawką DXM
8
mg/d przez 4 dni

Hiperkortyzolemia (
F)
insulina,
oporność insulinowa
wrażliwość naczyń na substancje
presyjne (NA i Angiotensynę II)
Bezpośredni wpływ (F) na mięśnie
gładkie naczyń
Angiotensynogen,
A.R.O.
Zespół Cushinga
nadciśnienie tętnicze

Zespół Cushinga
Objawy
Otyłość centralna, czerwone rozstępy, miastenia,
zaniki mięśniowe, depresja, osteoporoza, cukrzyca
Screening test
Nocny test hamowania DXA (F <5 μg/dl,
<1.8 μg/dl )
Wyniki fałszywie dodatnie
Leki przyspieszające metabolizm DXA (p/padaczkowe)
Diagnoza pewna
ACTH. Kortyzol w ślinie i wolny kortyzol w moczu,
supresyjny test z DXA

Zespół Cushinga
Nadciśnienie tętnicze – leczenie
Usunięcie przyczyny zespołu Cushinga
guz: przysadki, nadnercza,
nowotworowy
Hamowanie wydzielania sterydów
nadnerczowych:
-
aminoglutetymid 0,5 do 2,0 g/d
-
ketokonazol 800 - 1000 mg/d
-
metyrapon, mitotan
Leki hipotensyjne

Zespół Cushinga
Wytyczne z 2007 r.
Europejskiego Towarzystwa Nadciśnienia
Tętniczego
Zespół Cushinga - <0,1% populacji
Nadciśnienie tętnicze u 80% chorych
Typowa budowa ciała
Ocena 24h wydalania kortyzolu z
moczem (>40 μg/d)
Dwudniowy test z DXA - wydalanie
wolnego kortyzolu >10 μg
W teście nocnym z DXA kortyzolu >5
μg/dl
N
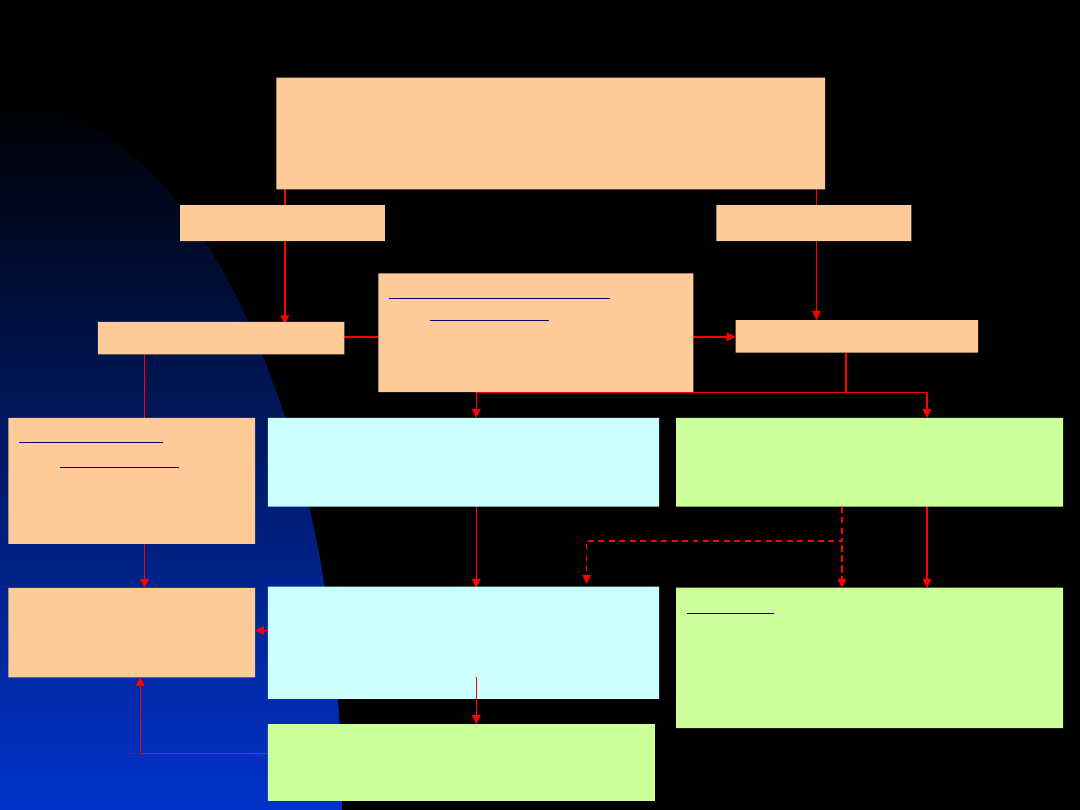
Nocny test hamowania z DXA (1 mg)
Stężenie metoksykatecholamin w moczu
dobowym
ALDO i ARO w osoczu
wynik (+)
wynik (-)
Testy potwierdzające
Brak autonomicznego
wydzielania
kortyzolu
aldosteronu
katecholamin
Obraz fenotypowy
Autonomiczne
wydzielanie
kortyzolu
aldosteronu
katecholamin
Gęstość w CT ≤10 j.H.
CT contrast-medium washout ≥50% at
10’
William F. Young, Jr.
N Engl J Med 2007; 356:601-10.
Gęstość w CT >40 j.H.
CT contrast-medium washout <50% at
10’
powtórzenie
CT po 6, 12 i 24 mies.
testy hormonalne corocznie, przez 4
lata
chirurgiczne usunięcie guza Ø ≥ 4 cm
Rozważyć
biopsja cienkoigłowa
(jeżeli przerzuty lub podejrzenie
infekcji)
leczenie chirurgiczne.
follow up z kontrolnymi CT co 3 m-ce
Guz Ø ≥ 1 cm
z autonomicznym wydzielaniem
hormonów
Leczenie
chirurgiczne
Algorytm badania chorego z nadnerczowym
„incidentaloma”

Doustne środki
antykoncepcyjne
Etynyloestradiol:
35, 30, 20 µg EE
+ progestagen (pochodna 19-nortestosteronu)
Działanie:
EE ~ 200 x silniejsze od E
2
obniżenie FSH i wzrost
angiotensynogenu)
zahamowanie osi podwzgórzowo-
przysadkowo-jajnikowej

OC
5-letnie stosowanie OC
RR >140/90 mm Hg u 5% ♀
przy NT odstawić OC
brak normalizacji RR po ½
roku diagnostyka
nadciśnienia

Przyczyna
NT hormonalne
Guz wydzielający
reninę
Pierwotny reninizm
Choroby tarczycy
Nadczynność
i niedoczynność
tarczycy
Choroby przytarczyc
Pierwotna
nadczynność
przytarczyc
Leczenie
estrogenami
Doustne środki
antykoncepcyjne
Inne
Akromegalia
Otyłość

Nadciśnienie zależne od
mineralokortikoidów
Przyczyna
Mineralokortikoi
d
Aldosteronizm pierwotny
aldosteron
Wrodzony przerost
nadnerczy (blok 11 i 17)
DOC
Guz wydzielający DOC
DOC
Deficyt 11-HSD
2
kortyzol
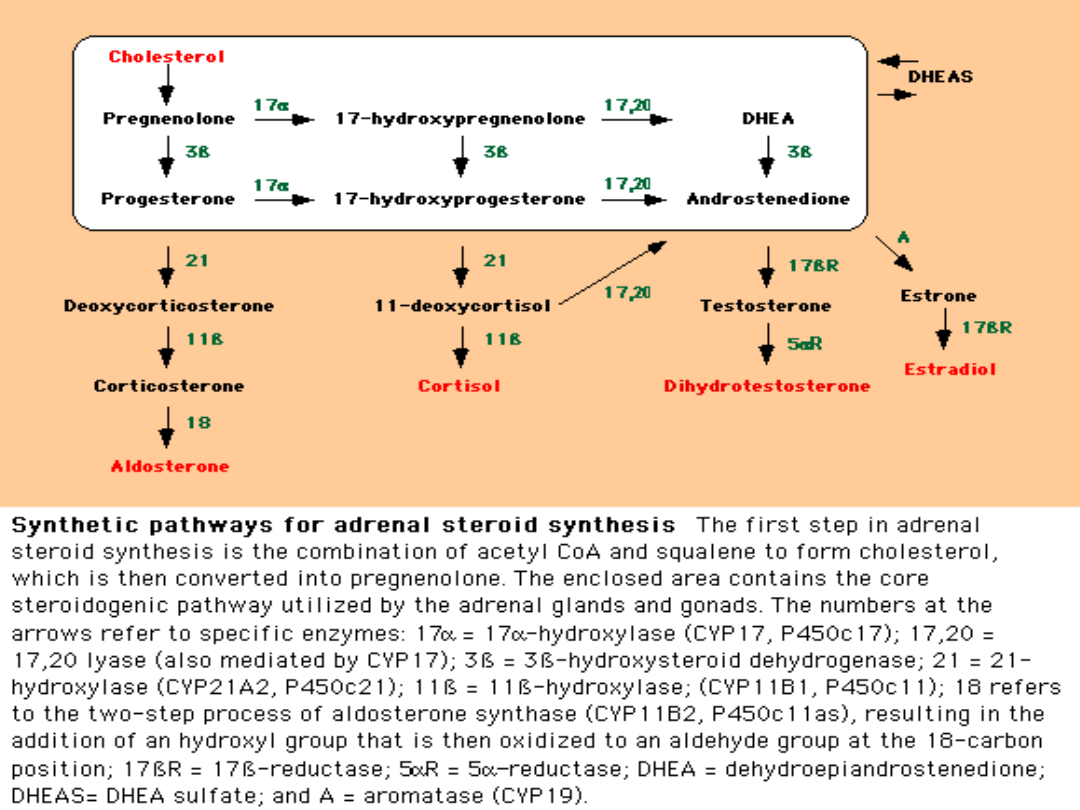
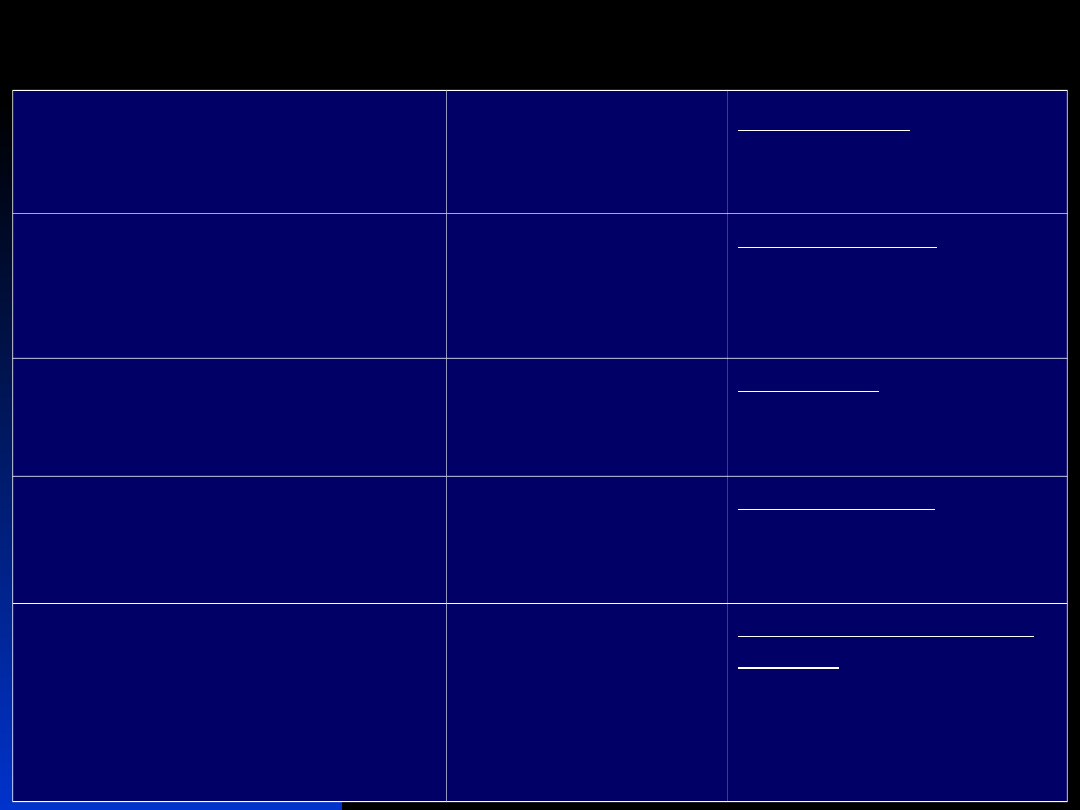
Nadciśnienie – nadmiar
mineralokortikoidów
Hiperalosteronizm
ALDOSTERO
N
hipokaliemia
ARO
ALDO
Blok 17α-
hydroksylazy
DOC
hipogonadyzm
ARO
ALDO
kortyzol
Blok 11β-
hydroksylazy
DOC
wirylizacja
ARO
ALDO (n lub )
Guzy nadnercza
wydzielające DOC
DOC
guz nadnercza
ARO
ALDO
Niedobór 11β-HSD2
(pozorny nadmiar
mineralokortikoidów)
KORTYZOL
wzmożone pragnienie
poliuria
ARO
ALDO
metabolity kortyzolu

Szczególnie częste
przyczyny
hiperaldosteronizmu
zastoinowa niewydolność serca
zawał serca
nadciśnienie tętnicze -
niskoreninowe
Nadciśnienie tętnicze
Hipokaliemia
Alkaloza metaboliczna
Nadciśnienie młodocianych
Niska waga urodzeniowa
Polidypsja
Poliuria
ARO
Aldosteron
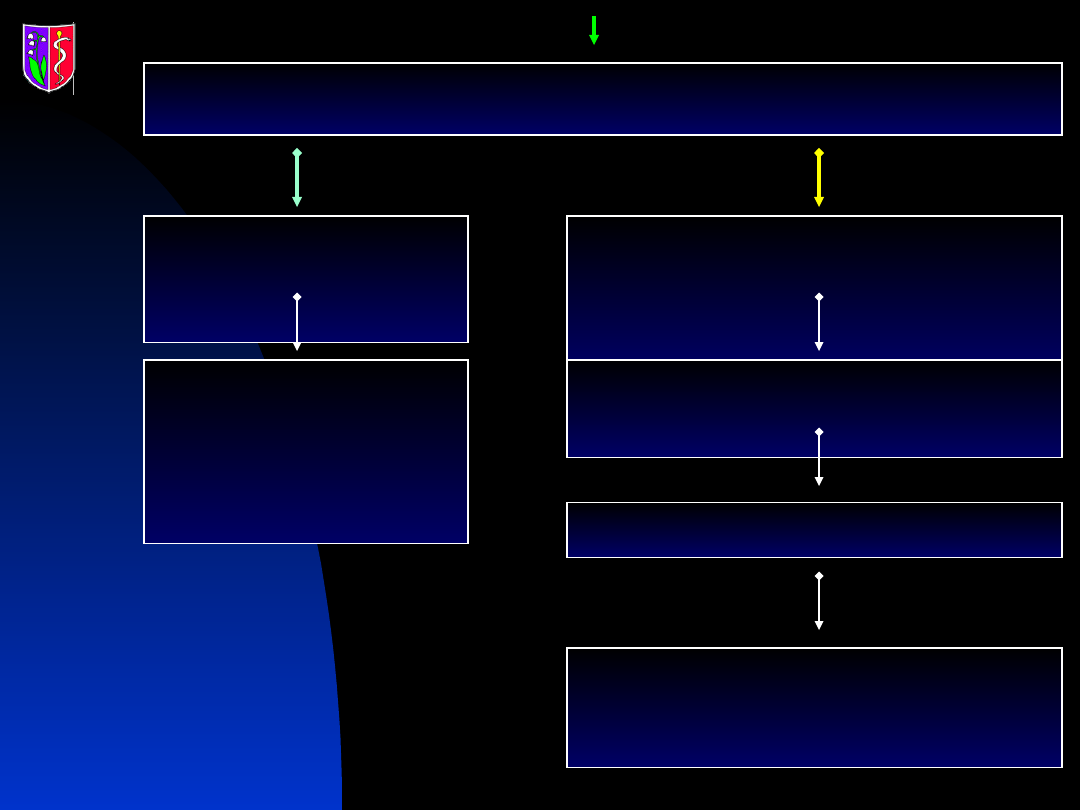
prawidłow
e
THF/THE
Pozorny nadmiar
mineral.
zespół
Liddle’a
mutacja MR
nadmiar DOC
zespół ektopowego
ACTH
Metabolity kortyzolu
lukrecja
zespół AME
(potwierdzony testem
genetycznym)
Marcus Quinkler i wsp.: JCEM 2003; 88:2384
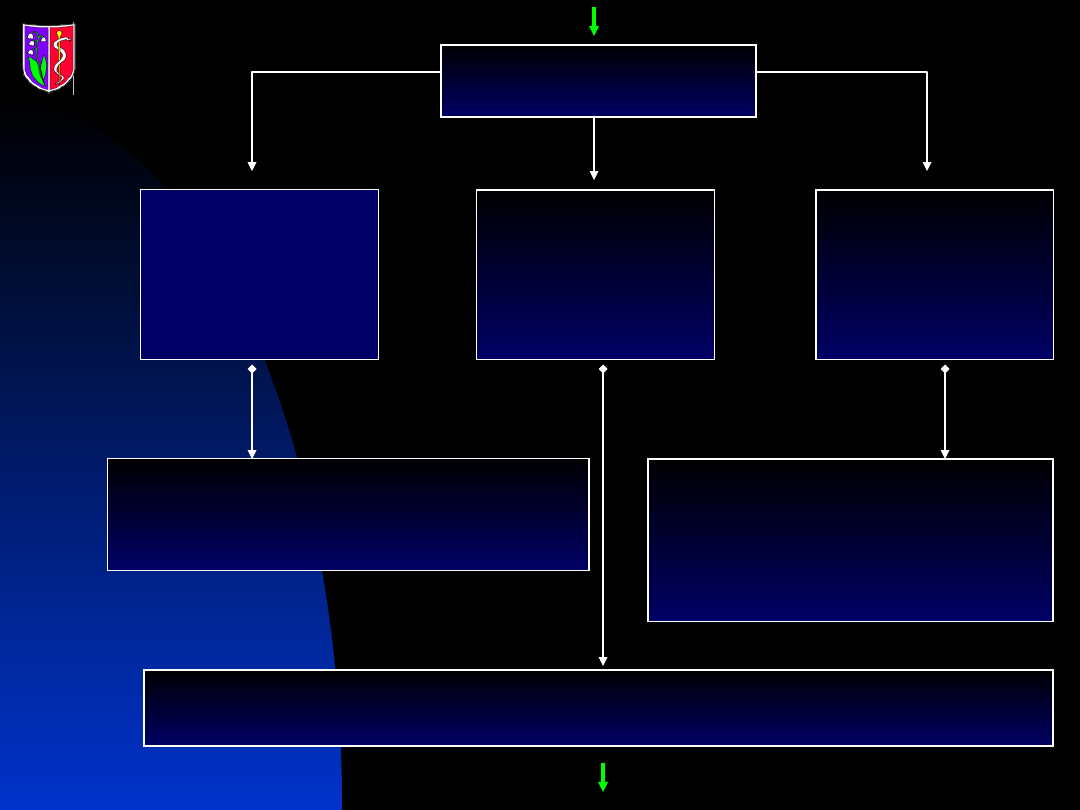
Aldo
ARO
Aldo
ARO
Aldo
ARO
pierwotny
hiperaldosteronizm
wtórny
hiperaldosteron
izm
metabolity kortyzolu
Aldo i ARO
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
Wyszukiwarka
Podobne podstrony:
Nadcisnienie tętnicze hormonalne
Nadciśnienie tętnicze hormonalne (2)
Nadciśnienie tętnicze hormonalne
NADCIŚNIENIE TĘTNICZE UWARUNKOWANE HORMONALNIE
NADCIŚNIENIE TĘTNICZE UWARUNKOWANE HORMONALNIE
WPŁYW STRESU NA NADCIŚNIENIE TETNICZE
Nadciśnienie tętnicze (3)
09 Nadciśnienie tętnicze
Nadcisnienie tetnicze 3
Leki stosowane w terapii nadciśnienia tętniczego
nadcisnienie tetnicze 2
Niewydolność serca i nadciśnienie tętnicze klinika i pielęgnowanie
Patomechanizm nadciśnienia tętniczego w niewydolności nerek Ż Chatys
Ostre stany kardiologiczne w przebiegu nadciśnienia tętniczego(1), różne, ►Medycyna-Fizykoterapia,Ps
Leki stosowane w nadciśnieniu tętniczym-powtórzenie (1), Szkoła
pacjent z nadcisnieniem tetniczym w wieku podeszlym
więcej podobnych podstron