307

A HibUl. IM1U.1 ,Vv»« r„, r ), buui :uO
ISBN D4H1II ł-7. © l>. »N TOS >«}
307
10 3 PRAWO DZIAŁANIA .MAS
10.3. PRAWO DZIAŁANIA MAS W ZASTOSOWANIU DO RÓWNOWAG CHEMICZNYCH W UKŁADACH HOMOGENICZNYCH
Rozumowanie, które przedstawiono w poprzednim paragrafie i które doprowadziło nas do wzoru <10.10). można zastosować także w przypadku każdej innej reakcji chemicznej dochodzącej do stanu równowagi, a nawet w przypadku przemian fazowych oraz równowag fazowych. W tym paragrafie zajmiemy się uogólnieniem równania (10.10). a więc podaniem prawa działania mas w bardziej ogólnej postaci. W tym celu rozważymy reakcję, w której a moli cząsteczek substancji A reaguje z b moli cząsteczek substancji B i powstaje r moli cząsteczek substancji C oraz <1 moli cząsteczek substancji D zgodnie z równaniem
flA + />B ł* rC t i/D
Zakładamy przy tym. ze rozpatrywana przez nas reakcja dochodzi do stanu równowagi, w którym substancje A. B, C, D obecne są w odpowiednich ilościach. Rozumując podobnie jak w poprzednim paragrafie, dochodzimy do wniosku, zc po osiągnięciu przez układ stanu równowagi musi być spełnione równanie
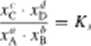
(10.11)
analogiczne do równ. (10.10). Stanowi ono ogólną postać prawa działania mas (Cato M. Guldbcrg i Peter Waagc. I867 r.). Stwierdza, zc w stanic równowagi iloczyn ułamków molowych produktów reakcji, podniesionych do odpowiednich potęg, podzielony przez iloczyn ułamków molowych substratów reakcji, również podniesionych do odpowiednich potęg, ma wartość stałą. Wykładnikami potęgowymi przy wartościach ułamków molowych poszczególnych substancji są wartości współczynników stcchiomctrycznych w równaniu chemicznym. Z równania (10.9) wynika, że stalą równowagi A', reakcji tworzenia się amoniaku możemy obliczyć, gdy znamy wartości poszczególnych substancji. Wartości tc zmieniają się w zależności od temperatury oraz (w przypadku gdy mamy do czynienia z fazą gazową) od całkowitego ciśnienia panującego w układzie. Wynika z tego. że wartość A', jest stała tylko wówczas, gdy rozpatrujemy ró/Jie stany równowagi dla tej samej temperatury oraz — w obecności fazy guzowej — dla lego samego całkowitego ciśnienia panującego w układzie.
Jeżeli substancje A. B. C i D są gazami (mamy wówczas do czynienia z układem jednofazowym. a więc z układem homogenicznym), to przez wykorzystanie wzoru (10.4a) wyrażającego potencjał chemiczny, fi,, składnika i fazy gazowej za pomocą jego ciśnienia cząstkowego, oraz zastosowanie takiego rozumowania jak przy wyprowadzaniu wzoru ( 10.10) możemy zamiast stałej równowagi A\ wyprowadzić stalą równowagi K^. wielkość niezależną od ciśnienia całkowitego:
Wyszukiwarka
Podobne podstrony:
A HibUl. IM1U.1 ,Vv»« rw, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 18
A HibUl. IM1U.1 ,Vv»« raa, r ), buui :uO ISBN D4H1II ł-7. © t>< WN TOS >«
A HibUl. IM1U.1 ,Vv». r.., r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 3
A HibUl. IM1U.1 ,Vv.« r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 14 10
A HibUl. IM1U.1 ,Vv»« :u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >*} 14
A HibUl. IM1U.1 .Vvu --u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS »*} 155 i
A HibUl. IM1U.1 .Vvu :u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 27S
A HibUl. IM1U.1 ,Vvu r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 325 10
A HibUl. IM1U.1 ,Vvu r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 15 10 W
A HibUl. IM1U.1 ,Vv»« :i>, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«
A HibUl. IM1U.1 .Vv»« r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >*} 6
A HibUl. IM1U.1 ,Vv»« :u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 1
A HibUl. IM1U.1 ,Vv». r ), buui :uO ISBN D4H1II t-7. © l>. »N TOS >*} 22 2 J
A HibUl. IM1U.1 ,Vv». -u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 26
A HibUl. IM1U.1 ,Vv»« .«»•»». :u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 33 2 7 PROST
A HibUl. IM1U.1 ,Vv»« --u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS »*} 2 JĄ
A HibUl. IM1U.1 ,Vv»« --u, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS >«} 3
A HibUl. IM1U.1 ,Vv»« r„, r ), buui :uO ISBN D4H1II ł-7. © l>. »N TOS »*} 44
więcej podobnych podstron