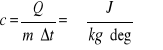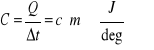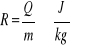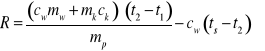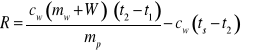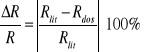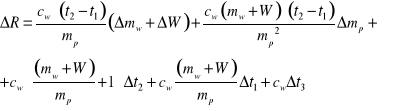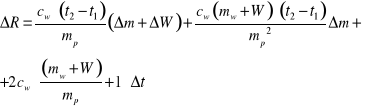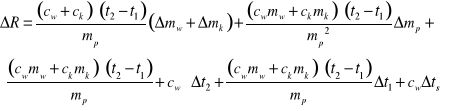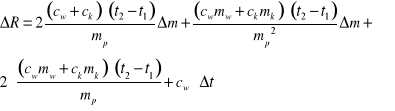Ćwiczenie nr 24
Wyznaczanie ciepła parowania wody
Cel ćwiczenia
Pomiar ciepła parowania wody w temperaturze wrzenia.
Wprowadzenie
Aby zwiększyć o Δt temperaturę ciała o masie m należy dostarczyć ciepło Q:
|
(24.1) |
gdzie: c oznacza ciepło właściwe, zmiana temperatury Δt=ΔT jest taka sama w przypadku gdy wyrazimy ją w stopniach Celsjusza lub Kelvina, m - masa ciała,
U podstaw kalorymetrii leży założenie spełnienia zasady zachowania energii. Przyjmujemy, że ilość ciepła Q1 oddana przez badane ciało jest równa ilości ciepła Q2 pobranej przez otoczenie Q1=Q2.Również zakładamy, że ilości ciepła potrzebne do uzyskania określonej zmiany temperatury Δt są inne dla różnych ciał.
Ciepłem właściwym nazywamy ilość ciepła Q potrzebną do ogrzania (oziębienia) jednostki masy m=1 kg danego ciała o jeden stopień.:
|
(24.2) |
gdzie: deg oznacza temperaturę w stopniach Celsjusza lub Kelvina
Pojemnością cieplną danego ciała nazywamy ilość ciepła potrzebną do ogrzania całej masy ciała m o jeden stopień:
|
(24.3) |
Ciepło dostarczone do układu termodynamicznego oprócz podgrzania ciała może posłużyć do zmiany jego stanu skupienia.
Ilość ciepła Q potrzebną do zamiany cieczy o masie m w parę o tej samej temperaturze wynosi:
|
(24.4) |
gdzie:
R - ciepło parowania.
Ciepłem parowania R nazywamy ilość ciepła potrzebną do zamiany jednostki masy m=1 kg cieczy w parę o tej samej temperaturze:
|
(24.5) |
Ciepło parowania zależy od temperatury, w której ciecz paruje i od ciśnienia Ćwiczenie dotyczy wyznaczenia ciepła parowania wody w temperaturze wrzenia pod ciśnieniem atmosferycznym. Zgodnie z regułami bilansu ciepłego ciepło skraplania, przebiegające w odwrotnym kierunku, jest dokładnie równe ciepłu parowania.
Aby wyznaczyć wartość ciepła parowania wodę w kolbie ogrzewamy do temperatury wrzenia ts. Para wodna przechodzi przez przewód do kalorymetru napełnionego wodą gdzie ulega skropleniu. Para wodna o masie mp skraplając się oddaje ciepło Q1:
|
(24.6) |
Następnie powstała z niej woda oziębiając się do temperatury końcowej t2 oddaje ciepło Q2:
|
(24.7) |
gdzie:
ts- temperatura skraplania pary (równą temperaturze wrzenia wody).
Kalorymetr i znajdująca się w nim woda ogrzewa się od temperatury początkowej t1 do temperatury końcowej t2 w wyniku pobrania ciepła Q3:
|
(24.8) |
Z bilansu cieplnego zakładając brak strat cieplnych otrzymujemy:
|
(24.9) |
Po przekształceniach otrzymujemy wzór na ciepło parowania R:
|
(24.10) |
Jeżeli uprzednio wyznaczono równoważnik wodny kalorymetru W można zapisać:
|
(24.11) |
Opis stanowiska laboratoryjnego
Rys. 24.1. Schemat układu pomiarowego
Na rysunku 24.1. przedstawiono schemat układu pomiarowego. Składa się on ze szklanej kolby, której ogrzewamy wodę, aby powstała para wodna, izolowanego termicznie przewodu łączącego kolbę z kalorymetrem. W pokrywie kubka termicznego pełniącego rolę kalorymetru wywiercono centralnie otwór do doprowadzenia pary. Rurka doprowadzająca parę powinna zostać umieszczona w wodzie Zestaw pomiarowy powinien również zawierać: elektroniczną wagę laboratoryjną lub kuchenną, termometr elektroniczny, rękawicę kuchenną, aby uniknąć oparzeń, palnik lub grzałkę elektryczną do podgrzewania wody.
Program ćwiczenia
Zważyć pusty kalorymetr wraz z termometrem i mieszadełkiem- masa mk.
Nalać wodę do kalorymetru do około połowy pojemności naczynia. Wyznaczyć temperaturę wody t1.
Zważyć ponownie kalorymetr wraz z termometrem i mieszadełkiem-masa m1, aby obliczyć masę wody mw:
Nalać wody do kolby. Podgrzewać naczynie aż woda zacznie wrzeć.
Parę do kalorymetru wprowadzić, gdy przewód doprowadzający nagrzeje się do temperatury wrzenia i para w przewodzie nie skrapla się, lecz wypływa strumieniem.
Gdy para intensywnie wydobywa się z rurki wkładamy rurkę do kalorymetru przez otwór w pokrywie tak, aby jej koniec był zanurzony w wodzie.
Po upływie 2-3 minut wyjmujemy rurkę z kalorymetru. Wyłączamy zasilanie kolby z wrzącą wodą.
Wyznaczyć temperaturę końcową układu t2.
Zważyć ponownie kalorymetr, aby ustalić masę skroplonej pary mp
Ustalić i zapisać niepewności pomiarów bezpośrednich masy i temperatury.
Sprawozdanie
Obliczyć wartość ciepła parowania R.
Znaleźć w tablicach wartość ciepła parowania i obliczyć względną różnicę tablicowych Rlit i mierzonych wartości Rdoś:
Jeżeli wcześniej wyznaczono równoważnik wodny kalorymetru W skorzystać ze wzoru na bezwzględną niepewność pomiarową ΔW.
Następnie wyznaczyć maksymalną niepewność systematyczną pomiaru ciepła parowania ΔR metodą różniczki zupełnej korzystając ze wzoru:
Jeżeli posługujemy się tą samą wagą i jednym termometrem wszystkie niepewności pomiaru masy będą jednakowe, dotyczy to również pomiaru temperatury. Wzór na ΔR uprości się:
Jeżeli nie wyznaczono równoważnika wodnego kalorymetru posłużyć się wzorem:
Jeżeli posługujemy się tą samą wagą i jednym termometrem wszystkie niepewności pomiaru masy będą jednakowe, dotyczy to również pomiaru temperatury. Wzór na ΔR uprości się:
Dyskusja wyników i wnioski.
Pytania kontrolne
Wzór na ciepło pobrane lub oddane.
Ciepło właściwe, ciepło molowe, pojemność cieplna.
Zasady układania bilansu ciepłego.
Sposoby przenoszenia ciepła.
Przemiany fazowe i ciepła przemian.
|
(24.12) |
|
(24.13) |
|
(24.14) |
|
(24.15) |
|
(24.16) |
|
(24.17) |
153
Wyszukiwarka
Podobne podstrony:
ćw.14, Fizyka, Skrypt do Laborek
ćw.27, Fizyka, Skrypt do Laborek
ćw.31, Fizyka, Skrypt do Laborek
ćw.20, Fizyka, Skrypt do Laborek
ćw.15, Fizyka, Skrypt do Laborek
ćw.12, Fizyka, Skrypt do Laborek
ćw.26, Fizyka, Skrypt do Laborek
ćw.23, Fizyka, Skrypt do Laborek
ćw.25, Fizyka, Skrypt do Laborek
ćw.13, Fizyka, Skrypt do Laborek
ćw.17, Fizyka, Skrypt do Laborek
ćw.11, Fizyka, Skrypt do Laborek
ćw.21, Fizyka, Skrypt do Laborek
ćw.30, Fizyka, Skrypt do Laborek
ćw.10, Fizyka, Skrypt do Laborek
ćw.16, Fizyka, Skrypt do Laborek
ćw.29, Fizyka, Skrypt do Laborek
ćw.28, Fizyka, Skrypt do Laborek
ćw.33, Fizyka, Skrypt do Laborek
więcej podobnych podstron