394 [1024x768]
OGNIWA GALWANICZNE 403
= (Wj. + WS.+//S-)-(w£,cl + y«”,j -9600 = (0+0+H?,.)-(-30 360 +0) skąd
= —39 960 cal/mol
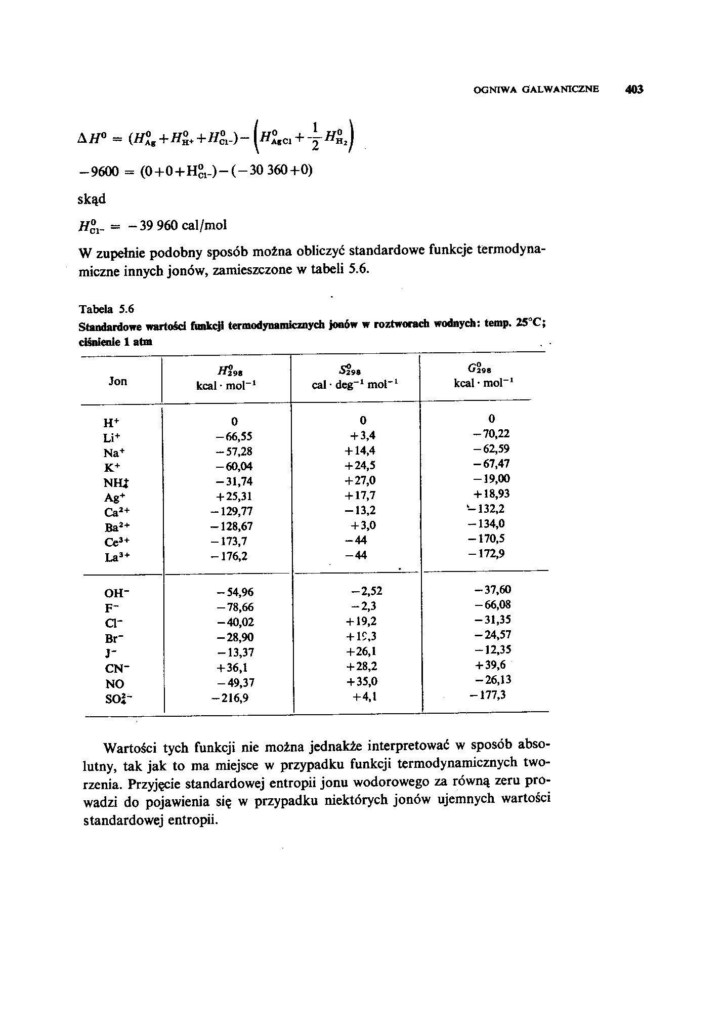
W zupełnie podobny sposób można obliczyć standardowe funkcje termodynamiczne innycb jonów, zamieszczone w tabeli 5.6.
Tabela 5.6
Standardowe wartości funkcji termodynamicznych jonów w roztworach wodnych: temp. 25’C;
|
Jon |
g°29. | ||
|
kcal • mol-1 |
cal • dcg-1 md'1 |
kcal • mol-1 | |
|
H* |
0 |
0 |
0 |
|
Li* |
-66,55 |
+ 3,4 |
-70,22 |
|
Na* |
-57,28 |
+ 14,4 |
-62,59 |
|
K* |
-60,04 |
+ 24,5 |
-67,47 |
|
NHi |
-31,74 |
+ 27,0 |
-19,00 |
|
Ag* |
+ 25,31 |
+ 17,7 |
+ 18,93 |
|
Ca3* |
-129,77 |
-13,2 |
‘-132,2 |
|
Ba3* |
-128,67 |
+ 3,0 |
-134,0 |
|
Ce3* |
-173,7 |
-44 |
-170,5 |
|
U3* |
-176,2 |
-44 |
-172,9 |
|
OH- |
-54,96 |
-2,52 |
-37,60 |
|
F" |
-78,66 |
-2.3 |
-66,08 |
|
ci- |
-40,02 |
+ 19,2 |
-31,35 |
|
Br" |
-28,90 |
+ 1C.3 |
-24,57 |
|
J* |
-13,37 |
+26,1 |
-12.35 |
|
CN“ |
+ 36,1 |
+ 28,2 |
+ 39,6 |
|
NO |
- 49,37 |
+ 35,0 |
-26,13 |
|
soi- |
-216,9 |
+4.1 |
-177,3 |
Wartości tych funkcji nie można jednakże interpretować w sposób absolutny, tak jak to ma miejsce w przypadku funkcji termodynamicznych tworzenia. Przyjęcie standardowej entropii jonu wodorowego za równą zeru prowadzi do pojawienia się w przypadku niektórych jonów ujemnych wartości standardowej entropii.
Wyszukiwarka
Podobne podstrony:
347 [1024x768] Ogniwa galwaniczneSilą elektromotoryczna ogniw galwanicznych W czasie elektrolizy wod
348 [1024x768] OGNIWA GALWANICZNE 357 Na zaciskach elektrod platynowych pojawi się teraz różnica pot
350 [1024x768] OGNIWA GALWANICZNE 359 Na elektrodzie ujemnej zachodzi proces utlenienia,
352 [1024x768] OGNIWA GALWANICZNE 361 Elektrochemiczny schemat elektrody wodorowej zapisujemy w post
354 [1024x768] OGNIWA GALWANICZNE 3^3 Jeżeli z drugiej strony, mówimy o SEM półogniw: Zn/Zn2 +Pt. ci
356 [1024x768] OGNIWA GALWANICZNE 365Rodzaje elektrod Elektrody gazowe Należą tu elektroda wodorowa,
358 [1024x768] OGNIWA GALWANICZNE 347 Elektrody oksydacyjno-redukcyjne Nazwa tego typu elektrod jest
360 [1024x768] OGNIWA GALWANICZNE 369 Zatem: . r. K crM- iQH=i [ +(fP)+-(irfH Ponieważ roztwór chinh
362 [1024x768] OGNIWA GALWANICZNE 371 Znaleźć aktywność oraz współczynnik aktywności UCI3 w roztworz
364 [1024x768] OGNIWA GALWANICZNE Klucz elektrolityczny eliminuje potencjał dyfuzyjny, występujący n
366 [1024x768] OGNIWA GALWANICZNE przepływowi przez ogniwo 1F towarzyszyć będzie przeniesienie t+ gr
370 [1024x768] OGNIWA GALWANICZNE 379£„ = (/♦-/-)RT. -Fh (5102) co wynika z równości r+ = J — Z równ
372 [1024x768] OGNIWA GALWANICZNE Różniczkując to równanie względem temperatury (przy stałym ciśnien
374 [1024x768] OGNIWA GALWANICZNE 383 SEM ogniw zalety na ogól znacznie od temperatury; zależność od
376 [1024x768] OGNIWA GALWANICZNE 385 w którym doświadczalnie mierzona wielkość £ jest liniową funk
378 [1024x768] OGNIWA GALWANICZNE 387 którego SEM zgodnie z reakcją ogniwa: 1/2 H2(ł, + 1/2 Hg.CI,,.
382 [1024x768] OGNIWA GALWANICZNE 391 zatem logyt = -0,5091 • j/cot - 2 log Yz - 2 0,5091
384 [1024x768] OGNIWA GALWANICZNE 393E°-~ !n(H*)! • (SOi-) = E°--2F In yl • y. ’
390 [1024x768] OGNIWA GALWANICZNE 399 Przyrównując równania (5.136) i (5.137) otrzymujemy: d In (y±
więcej podobnych podstron