skanuj0020(1) 2

Zakażenia szpitalne asteroides, Legionella, Pasteurella. Pseudomonas mallei. Salmonella sp., Yersinia sp., Chlamydia (Mandell, 1992).
Duże limfocyty o ziarnistość i ach w cytoplazmie, zwane też komórkami NK, wydają się ściśle przypominać limfocyty cytotoksyczne, jednak istotna różnica polega na braku swoistego receptora - TCR. Tak więc. brak tu cech swoistości, pamięci i ograniczenia zależnego od zestawu antygenów zgodności tkankowej i zjawiska odkrytego przez Dohcrty’ego i Zinkernagla. Zbliżenie komórki NK i zakażonej drobnoustrojem wynika z interakcji między ich powierzchniami, a dalej - uruchomienie perforyny i proces zabijania zakażonej komórki wyglądają podobnie. Jak wspomniano na wstępie tego rozdziału, komórki NK mogą być szybsze, choć mniej swoiste od innych, w kontroli zakażeń wewnątrzkomórkowych (ryc. 1.5).
Wspomniane wyżej bakterie, które rozwijają się wewnątrzkomórkowo, mogą przetrwać we wnętrzu monocytów po sfagocytowaniu. Komórki te mogą następnie roznosić chorobotwórczy drobnoustrój do różnych miejsc w organizmie. Eliminacja tych bakterii wymaga odrębnej strategii, w której uczestniczą makrofagi oraz limfo-
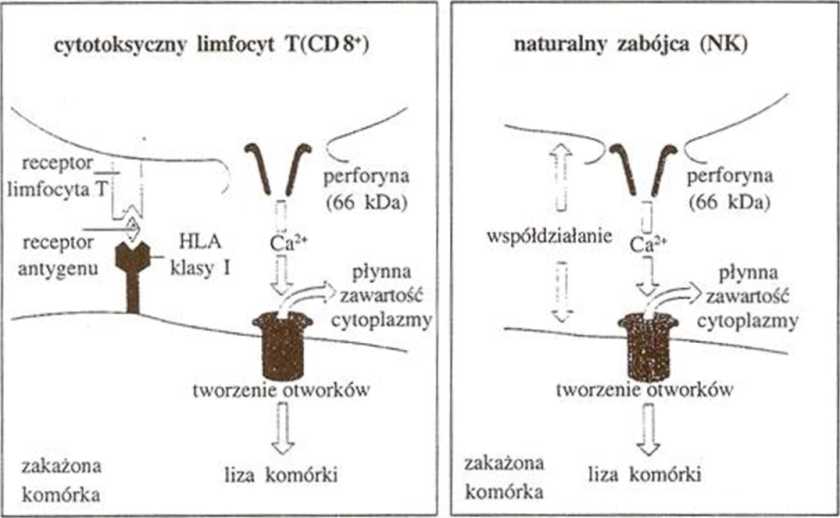
Rycina 1.4. Perforacja i zabijanie zakażonej komórki z udziałem limfocytów cytotoksycznych w porównaniu z tym samym procesem z udziałem komórek - naturalnych zabójców. Należy zwrócić uwagę na współdziałanie cząsteczki HLA klasy 1 z receptorem limfocyta CD8* w rozpoznaniu antygenu. Takiego rodzaju współdziałanie nie ma w przypadku komórek - naturalnych zabójców.
Liza
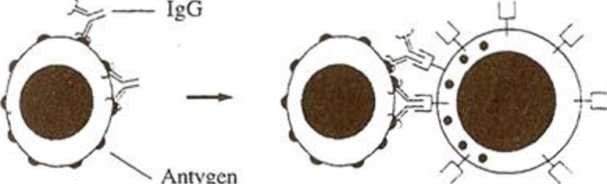
Antygen
powierzchniowy cząstki zakaźnej
Komórka NK
komórki
zakażonej
Rycina 1.5. Zabicie zakażonej komórki przez komórkę NK za pośrednictwem przeciwciała klasy IgG.
cyty T CD4* i CD8*. Gdy białka drobnoustroju przedostają się do cytoplazmy, zostają następnie, jako peptydy, prezentowane na powierzchni komórki w połączeniu z cząsteczkami HLA klasy I. W następnej kolejności dochodzi do aktywacji swoistych cytotoksycznych limfocytów T CD8\ Ich rola jest dwojaka: zabijają zakażone komórki, jak również wytwarzają IFN-a, aktywujący makrofagi w miejscu zakażenia (podobną rolę mogą także spełniać komórki NK). Zabicie zakażonych komórek jednojądrowych gospodarza powoduje uwolnienie drobnoustrojów, które są fagocytowane przez napływające makrofagi, a następnie zabijane.
Również limfocyty T CD4\ które rozpoznały antygeny namnażającego się wewnątrzkomórkowe drobnoustroju w połączeniu z cząsteczkami HLA klasy II, uwalniają cytokiny, np. IL-2, IL-4, IL-6, IFN-y, GM-CSF (czynnik krw iotwórczy granulocytów-makrofagów). Cytokiny te aktywują makrofagi, zwiększając ich zdolności bójcze.
Na podstawie rodzaju łańcuchów- białkowych tworzących receptor dla antygenu w-yróżnia się dwa typy limfocytów T: limfocyty Ta{5 i Tyó. Ich receptory składają się odpowiednio z łańcuchów a i p oraz y i ó. Większość limfocytów I (95% u zdrowych ludzi) wykazuje obecność heterodimeru cip. Jednakże limfocyty o ekspresji yó mają pew-ną szczególną rolę. Rozpoznają one preferencyjnie antygeny mykobakterii przypominające tzw. białka szoku termicznego (konserwatywne białka; HSP - lieat shock proteins). Na przykład, połowa spośród klonów limfocytów' T reagujących na antygeny prątka gruźlicy wiąże peptydy z grupy HSP60. Białka szoku termicznego są indukowane po ekspozycji na różne formy stresu, w- tym gorąco, pozbawienie tlenu, podstawowych jonów i składników odżywczych, a także w-ystawienie na wolne rodniki. Limfocyty T uczestniczą we wczesnej fazie odpowiedzi przcciw'bakteryjnej, do czego predysponuje je lokalizacja we wrotach zakażenia.
37
Wyszukiwarka
Podobne podstrony:
skanuj0009 7 Zakażenia szpitalne Ayliffe określa jako minimalną częstość występowania i szacuje na 5
skanuj0012(1) 3 Zakażenia szpitalne u pacjentów z immunosupresją lub z cukrzycą. Obecność enterokokó
skanuj0012 4 Zakażenia szpitalne Translokacji sprzyjają: - zaburzenie składu jakoś
skanuj0014 6 Zakażenia szpitalne Czynniki zjadliwości ułatwiające kolonizacje i inwazję Jeśli drobno
skanuj0016(1) 2 Zakażenia szpitalne dechów oraz czynności serca oraz pojawienie się leukocytozy we k
skanuj0018(1) Zakażenia szpitalne Mediator) procesu zapalnego - prostaglandyny i lcukotrieny - są p
skanuj0018 4 Zakażenia szpitalne Rycina 1.3. Struktura cząsteczek immunoglobulin: IgG i IgM. a.
skanuj0019(1) Zakażenia szpitalne Procesy zapalne mają za zadanie ograniczenie penetracji czynnika z
skanuj0019(2) Zakażenia szpitalnePiśmiennictwo Bates D.W. i wsp.: Projected impact of monoclonal ant
skanuj0020(2) Zakażenia szpitalne Rycina 5.8. Sposób pakowania tzw. ..równoległy”.Sterylizacja Sprzę
skanuj0021(1) Zakażenia szpitalne Relacje między odpornością wrodzoną i nabytą Czynnik zakaźny ataku
skanuj0027(1) Zakażenia szpitalne humoralnej, szczególnie syntezy IgE. Zarówno limfocyty Th 1. jak i
skanuj0028(2) Zakażenia szpitalne Tabela 5.4. Zależność pomiędzy zawartością powietrza w parze a cza
skanuj0029(1) Zakażenia szpitalne do zaburzeń funkcji życiowych drobnoustrojów. Produkty uboczne ste
skanuj0030(2) Zakażenia szpitalne Często dla celów praktycznych wyróżnia się walidację prospektywną,
skanuj0031 4 Zakażenia szpitalne Wiele badań eksperymentalnych in vivo wykazało, że wobec szczepów w
skanuj0032(2) Zakażenia szpitalne kierunek ruchu sprzętu kierunek ruchu powietrza Rycina 5.9b. Służb
skanuj0052 3 Zakażenia szpitalne i aseptyki przez personel oddziału. Dochodzi do nich podczas zabieg
skanuj0057 2 Zakażenia szpitalne padkach ostrych, masywnych infekcji. Wtedy w badaniu radiologicznym
więcej podobnych podstron