
Choroba Parkinsona
i jej leczenie farmakologiczne
dr hab. Przemysław Mikołajczak
Katedra i Zakład Farmakologii
Uniwersytet Medyczny im. K. Marcinkowskiego
w Poznaniu

Zespół Parkinsona
Choroba Parkinsona
Zespół parkinsonowsko-otępienny (wyspa Guam)
Zespół Parkinsona w dziedzicznych chorobach
zwyrodnieniowych (np. ataksja Friedricha, CJD)
Zespół Parkinsona po zapaleniu mózgu (śpiączkowe
zapalenie mózgu)
Miażdżycowy zespół Parkinsona

Postać zespołu Parkinsona
Częstość występowania
[%]
Endogenna
79-80
Miażdżycowa
15-30
Po zapaleniu mózgu
5
Pourazowa
0.6
Toksyczna (mangan, CO)
0.4
Związana z guzem
0.2-0.3
Polekowa (neuroleptyki)
5

Choroba Parkinsona
• określona przez Parkinsona w 1817 r.
(drżączka poraźna)
• jest jedną z najczęstszych chorób układu
nerwowego ok. 1,5/1000
• w Polsce ok. 50-55 tys. chorych, częstość
występowania wzrasta wraz z wiekiem
(osoby >65 r.ż. – 1,5% populacji)
• dziedziczona Autosomalnie Dominująco
(AD), rzadziej Autosomalnie Recesywnie
(AR) (10-20%)
• M>K, wiek: 50-60 lat

Typowy w
chorobie Parkinsona
wygląd:
chód
małymi
kroczkami,
pochylona
do przodu sylwetka
brak
ruchów towarzyszących ramion
brak
mimiki twarzy
każdy ruch zaczyna się bardzo
powoli
(ruch zamiarowy)
ruch jest z
trudnością
wyhamowywany

Objawy parkinsonizmu
1. Zaburzenia motoryczne
Stężenie (rigor)
Drżenie spoczynkowe (tremor)
Zaburzenia mowy
Hipo- i akinezja
2. Zaburzenia wegetatywne
Wzmożony ślinotok i łzawienie, podwyższone wydzielanie
łoju (
twarz jakby wysmarowana masłem
)
Zaburzona termoregulacja oraz wydzielanie potu
Obniżone ciśnienie tętnicze
Czynnościowe zaburzenia pęcherza i jelit
3. Zaburzenia psychiczne
Nastrój depresyjny
Przedłużony przebieg procesów myślenia
W późnych okresach spowolnienie myślenia (bradyfernia) i
otępienie

W
zespole Parkinsona
- niezależnie od przyczyn które go
wywołały – dochodzi do
bezwzględnego
lub względnego niedoboru dopaminy
w
jądrach podkorowych i przewagi układu
cholinergicznego
.

Przyczyny biochemiczno-neuroprzekaźnikowe
zaburzona równowaga
między przekaźnictwem:
dopaminergicznym
acetylocholinergicznym
glutaminergicznym
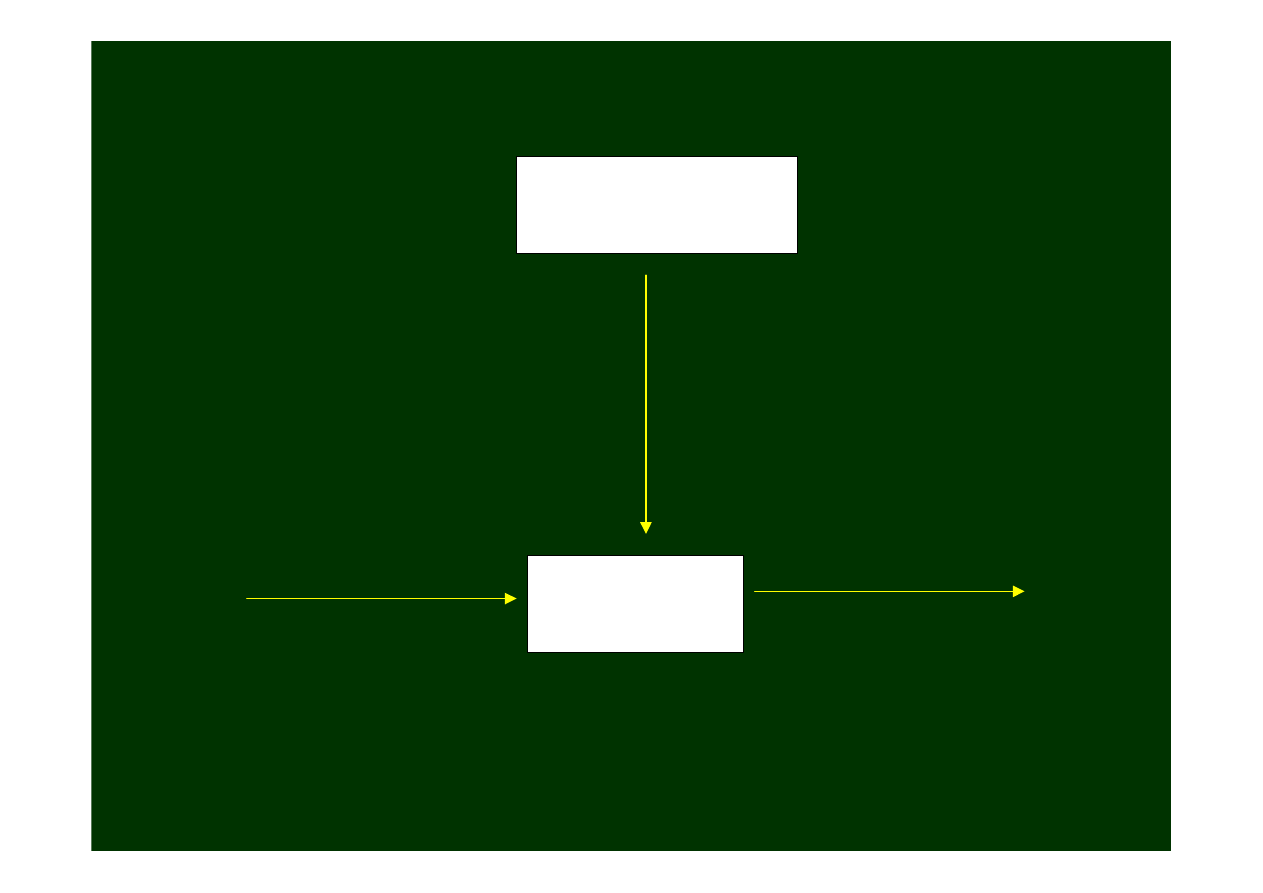
Dopamina
Acetylocholina
GABA
Istota czarna
Prążkowie
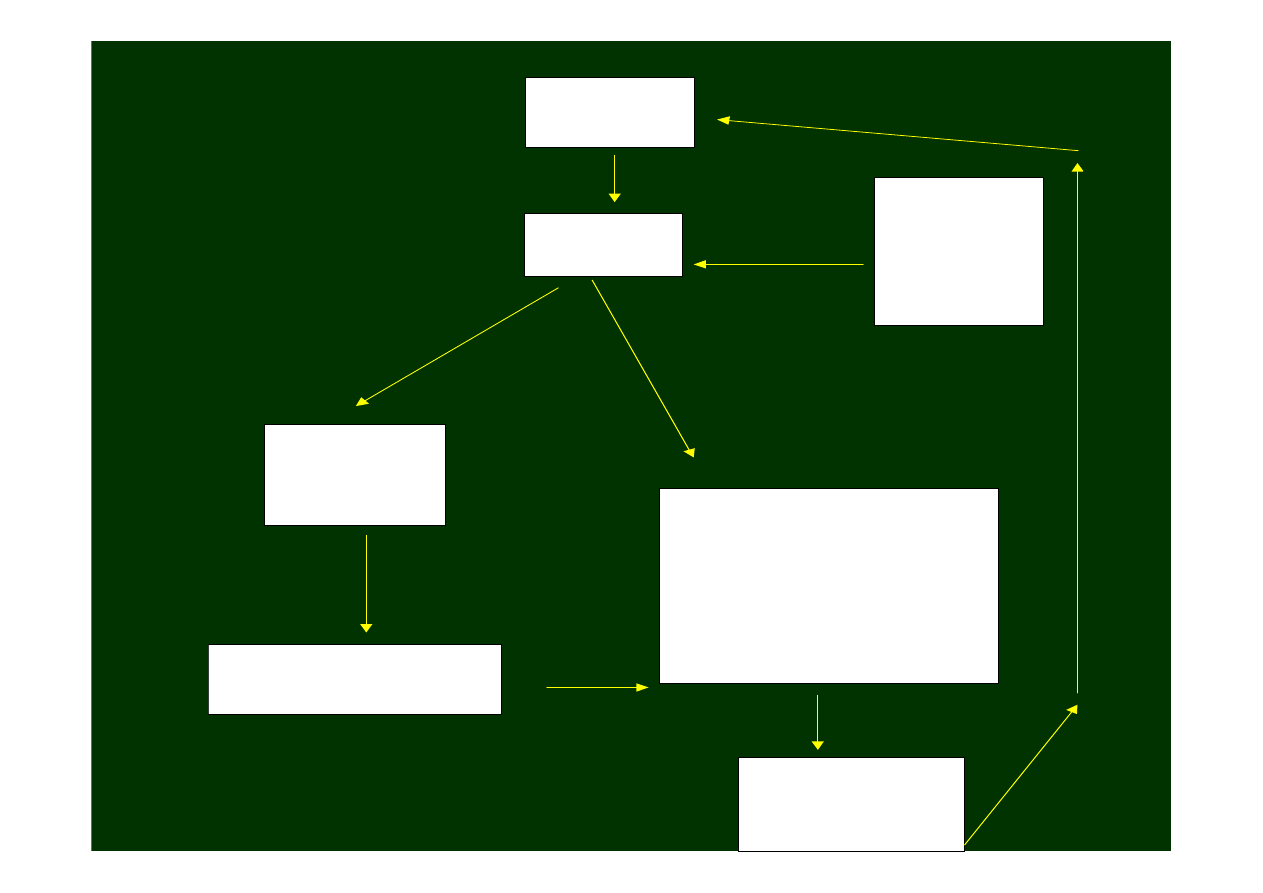
G l u
t a m i n i a n +
+
G l u
t a m i n i a n +
D o p a m i n a
+
G A B A _ _
E n k e f a l i n y D r o g a p o ś r e d n i a
D r o g a b e z p o ś r e d n i a
_ _
G A B A , s u b s t a n c j a P
G A B A
_ _
g l u t a m i n i a n
+
G A B A _ _
K o r a
c o r t e x
G a ł k a b l a d a
Z e w n e t r z n a
G l o b u s p a l l i d u s
( e x t e r n a l )
J ą d r o n i s k o w z g ó r z a
S u b t h a l a m i c n u c l e u s
W z g ó r z e
( J ą d r o b r z u s z n e
b o c z n e i i p r z e d n i e )
T h a l a m u s
G a ł k a b l a d a
W e w n ę t r z n a
G l o b u s p a l l i d u s ( i n t e r n a l )
I s t o t a c z a r n a w a r s t w a
s i a t k o w a t a ( c z e r w o n a )
S u b s t a n t i a n i g r a
( p a r s r e t i c u l a t a )
P r ą ż k o w i e
s t r i a t u m
I s t o t a
c z a r n a –
w a r s t w a
z b i t a
S u b s t a t i a n i g r a
( p a r s c o m p a c t a )
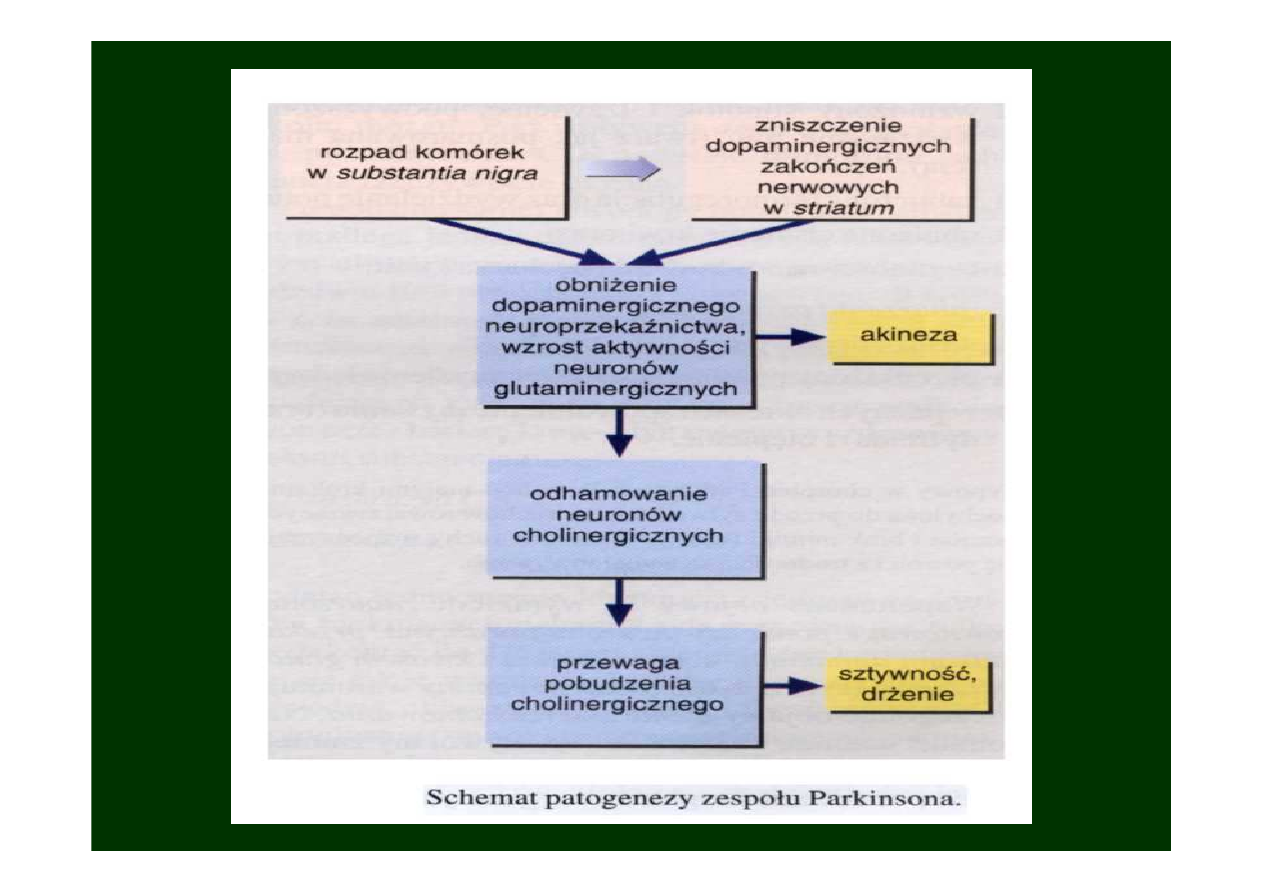

Niedobór
dopaminy
:
objawy o charakterze
hamowania
Nadmiar
acetylocholiny
:
objawy o charakterze
pobudzenia

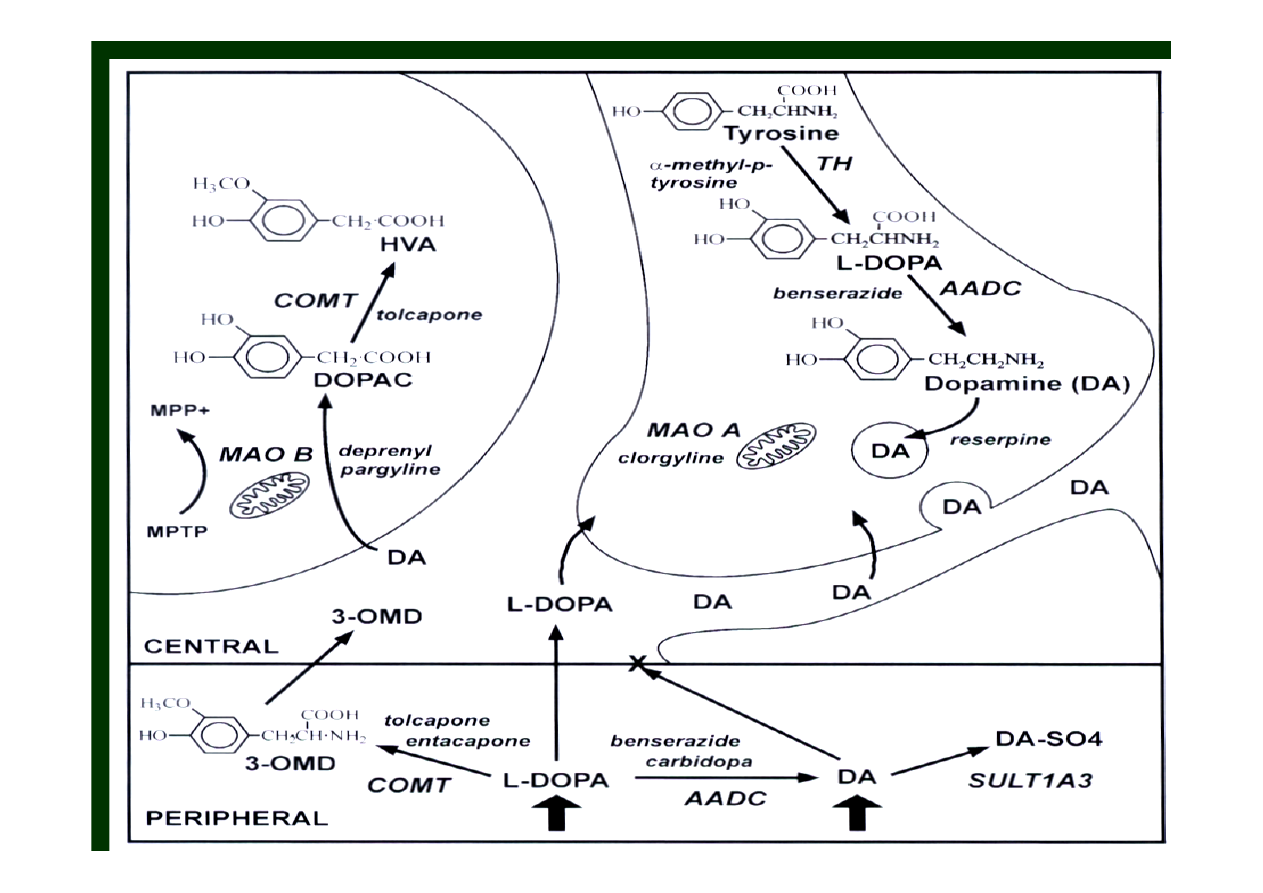
Farmakoterapia:
podanie
lewodopy
(prekursora dopaminy)
blokada na obwodzie dekarboksylacji lewodopy do
dopaminy (
obwodowe blokery
)
zahamowanie metylacji grupy -OH lewodopy (meta)
poprzez zastosowanie inhibitorów katecholo-O-
metylo-trasnferazy (
inhibitory COMT
)
zahamowanie rozkładu dopaminy przez zastoswanie
inhibitorów monoaminooksydazy typu B (MAO-B)
pobudzenie
ośrodkowych receptorów
dopaminergicznych za pomocą
agonistów
blokadę pochodnymi
adamantanu
receptorów
NMDA
w
prążkowiu
zahamowanie receptorów
muskarynowych
za pomocą
działających ośrodkowo
cholinolityków
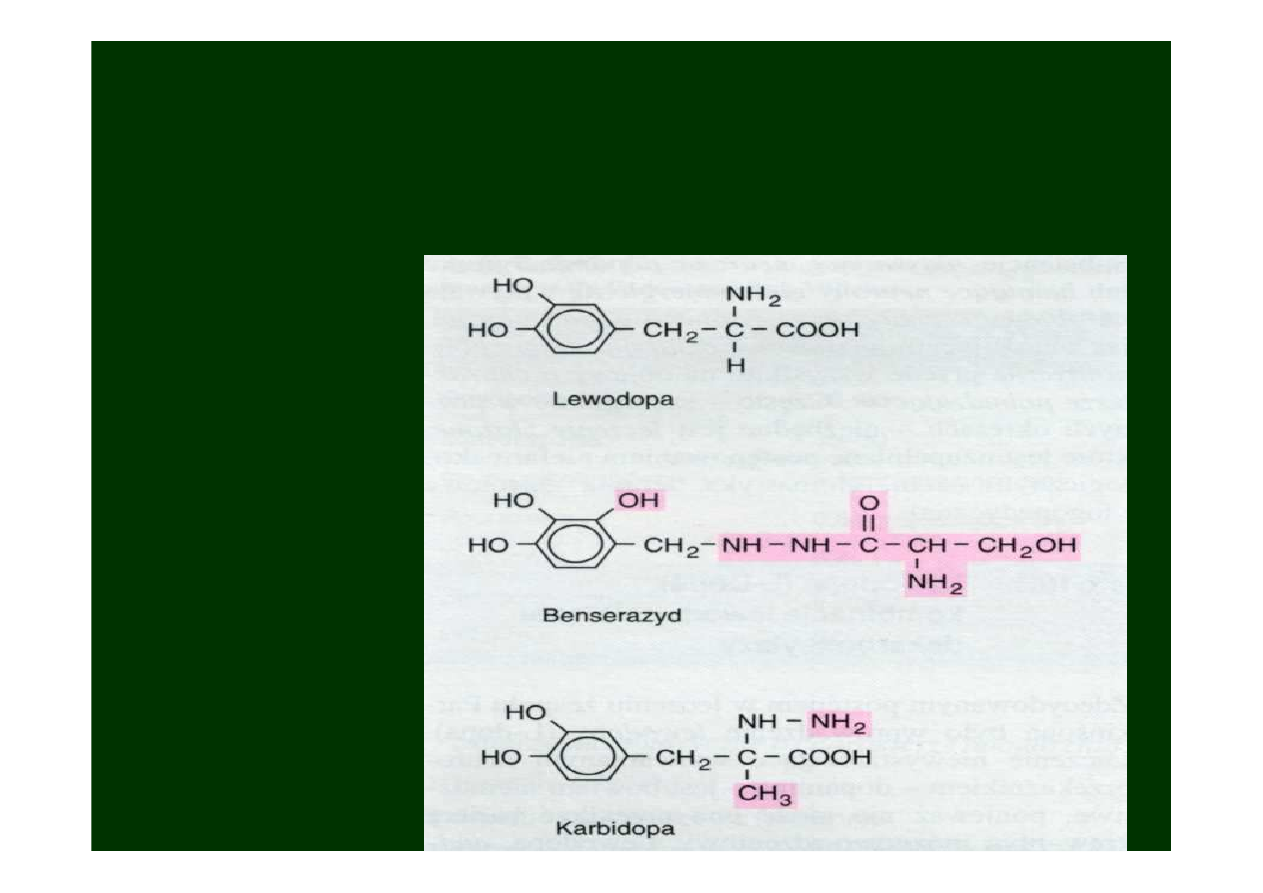
Lewodopa
W praktyce podaje się zawsze z
obwodowym inhibitorem
dekarboksylacji:
karbidopa
benserazyd
metaboliczne prekursory dopaminy – np. lewodopa (
L-dihydroksyfenyloalanina
)

Korzyści leczenia
Lewodopą:
Zmniejszenie wszystkich objawów zespołu
Parkinsona
(zwłaszcza na początku leczenia)
a przede wszystkim
akinezy i zaburzeń psychicznych
Dawkowanie: od 62,5 do 125 mg/dz.- 1 raz dziennie,
co tydzień o 125 mg, aż do 600-700 mg/dz.
(niekiedy nawet 2000 mg)
Poprawa
jakości
życia
i przewidywanej długości życia chorych

Jednakże:
po 3-5 latach leczenia - zespól „
On/off
”-
Fluktuacje
(wahania) działania
Lewodopy
prowadzące do tzw.
dyskinez
(
zmiany prawidłowej ruchliwości do akinezy
) -
nagły stan
bezruchu i sztywności u pacjenta, który wcześniej nie zdradzał
objawów choroby, ze względu na stosowanie agonistów
dopaminy - głównie młodsi chorzy
Być może spowodowane
desensytyzacją
receptorów
dopaminergicznych jak i zmienioną
farmkokinetyką
dopaminy

Objawy niepożądane
Lewodopy
:
objawy
motoryczne
(
hiperkinetyczne - bezbolesne,
powolne dyskinezje - bolesne
)
zaburzenia
wegetatywne
(
np. żołądkowo-jelitowe
)
zaburzenia
sercowo-naczyniowe
(
tachyarytmie, hipotonia
ortostatyczna
)
zmiany
psychiczne
(bezsenność, niepokój, pobudzenie, omamy)
u ¼ chorych, głównie starszych (>70 r.ż)
Interakcje :
neuroleptyki i rezepina -
↓↓↓↓
działania
Lewodopy
witamina B6 -
↓↓↓↓
działania
Lewodopy
(
pobudzenie dekarboksylazy
)
Lewodopa
↑↑↑↑
działanie norepineryny i epinefryny
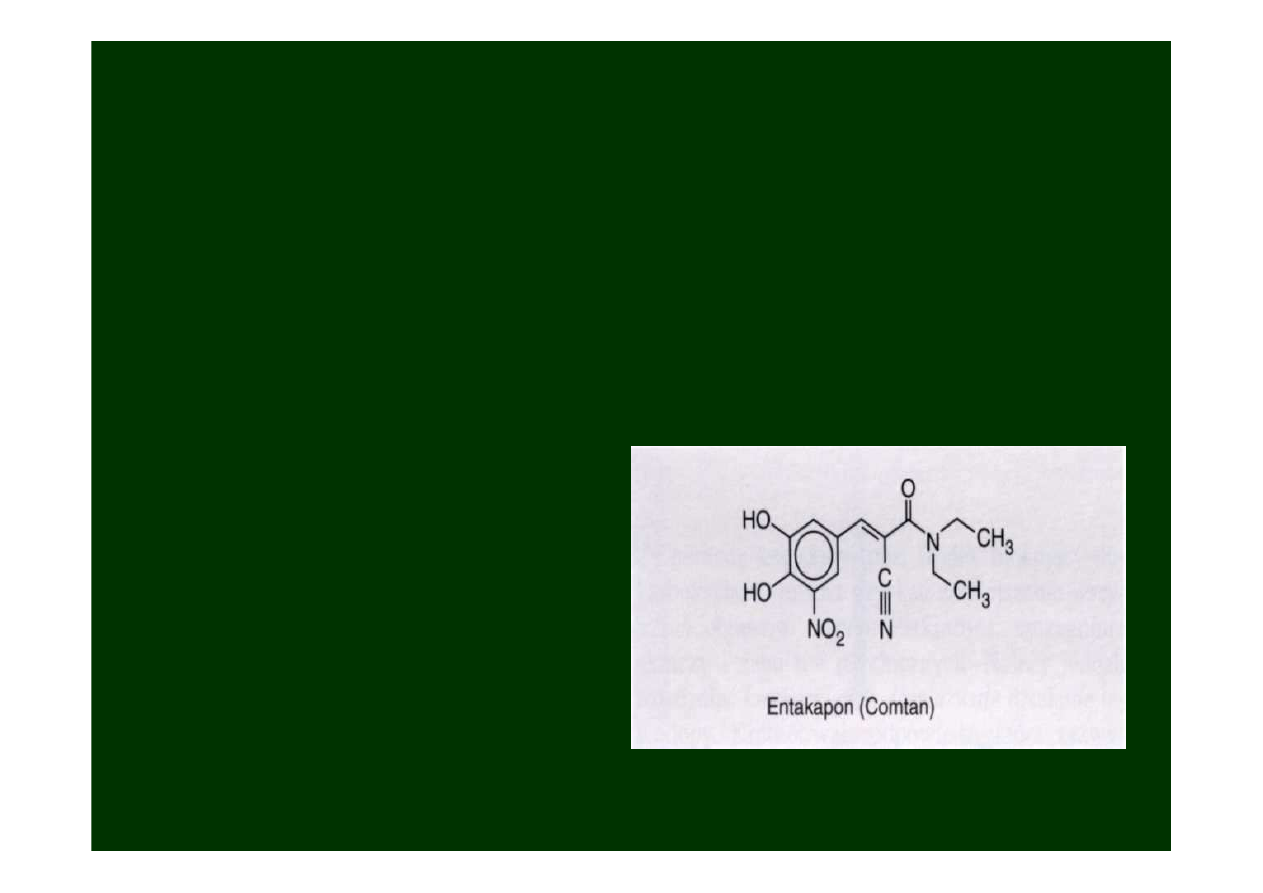
Entakapon
(inhibitor COMT)
Podaje się zawsze z
Lewodopą
(sam nie wywołuje efektu leczniczego).
Objawy niepożądane
:
(
większość ze względu na podwyższenie stężenia dopaminy w osoczu
)
dyskinezje
nudności
bóle w jamie brzudsznej
zaburzenia motoryki jelit
suchość w jamie ustnej
Przeciwwskazania:
niewydolność wątroby
złośliwy zespól neuroleptyczny
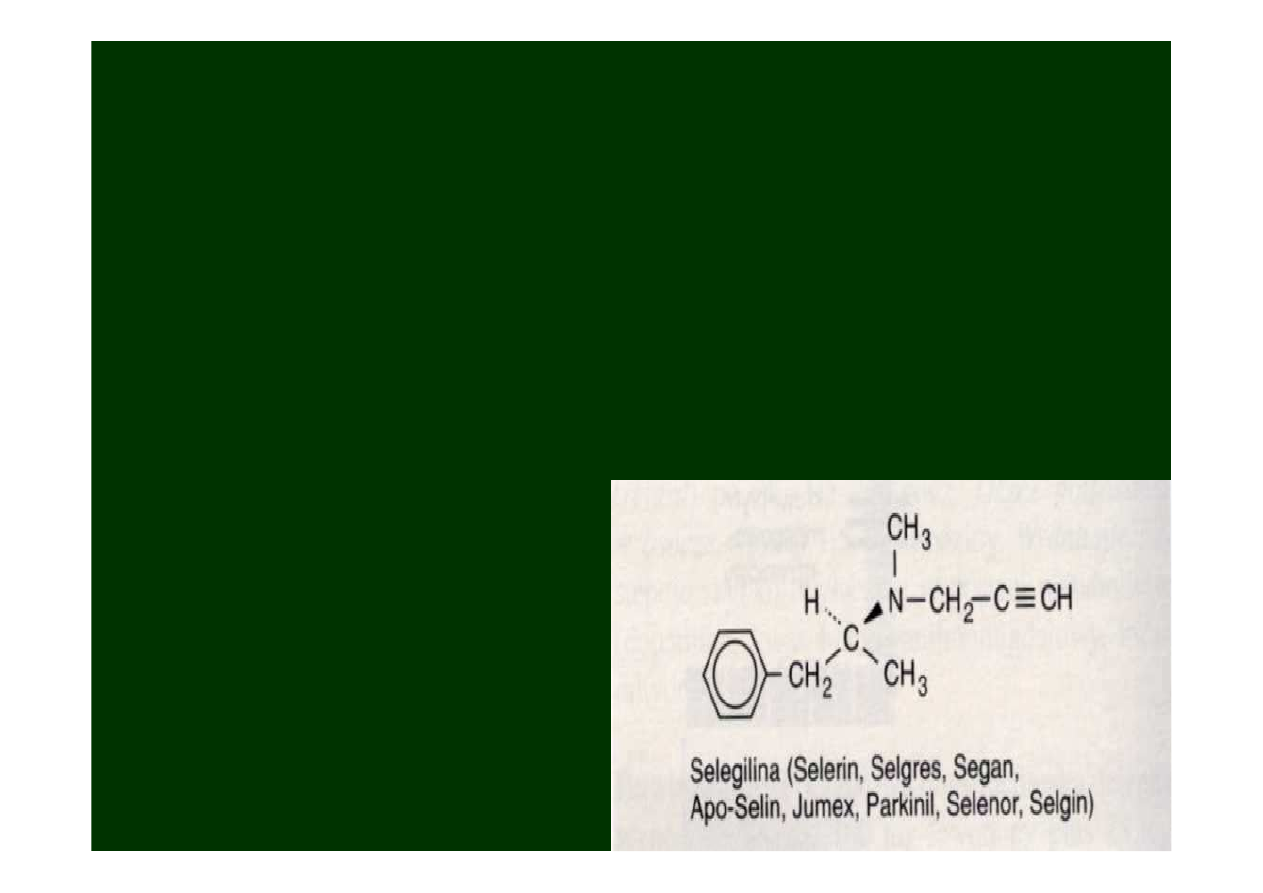
Selegilina
(
inhibitor MAO B
)
Podaje się przeważnie z
Lewodopą i blokerem dekarboksylazy.
Ma mieć również działanie neuroprotekcyjne .
Leczenie wczesnego okresu choroby, pomocniczo w standardowym leczeniu
(umożliwia obniżenie stężeń dopaminy) Dawkowanie: 10 mg/dz.
Objawy niepożądane
:
nudności
spadek
ciśnienia krwi
nasilanie wywołanych przez
lewodopę
objawów niepożądanych
Przeciwwskazania:
nadciśnienie
jaskra
prostata
angina pectoris
arytmiach
postępujące otępienie

Bromokryptyna
(poch. sporyszu, grupa ergoliny)
Działa jako niewybiórczy agonista receptorów dopaminergicznych.
Efekty wywołuje podobne do
Lewodopy
, ale słabsze i szybciej
przemijające .
Objawy niepożądane
:
zaburzenia psychiczne (omamy)
spadek
ciśnienia krwi (hipotonia ortostatyczna)
parestezje
zwłóknienia płuc i przestrzeni pozaotrzewnowej
Analogicznie działają:
dihydroergokryptyna, lisuryd
(agoniści D2),
pergolid
(agonista D1 i D2) (
wycofany?),
pramipeksol
(agonista
wybiórczy D3) (ma zdolność skracania trwania zespołu “On/off”)
Stosuje się gdy:
-pacjent nie reaguje już na lewodopę, pojawiają się objawy nietolerancji lewodopy
-
Dawkowanie: 1.tydz.-1x1,25mg/dz., 2.tydz.- 2x1,25mg/dz., co 1, 2 lub 4 tygodnie zwiększać
o 2,5mg/dz., aż do 15-30mg/dz. (obecnie 2-20mg/dz.), przy stos. razem z lewodopą- 5-15 mg/dz.

Zwalczanie objawów psychotycznych po poch. ergoliny leczymy:
najpierw odstawiamy agonistów, potem wprowadzamy zmniejszoną
dawkę, jeżeli nie pomaga-
klozapina
Klozapina
(Klozapol) – tzw. neuroleptyk atypowy, pochodna
dibenzepiny, blokuje silnie rec. D4,
umiarkowane powinowactwo do D1, D2,
D3, D5.
stosuje się gdy :
nasilone drżenie
objawy psychotyczne po
lewodopie
Dawkowanie: 12,5 lub 25mg, 1 do kilku razy na dzień
Objawy uboczne:
-
zaburzenia hemopezy,
-
objawy cholinolityczne

Amantadyna
(niekompetytywny bloker receptorów NMDA )
Wskazania:
W
monoterapii
niezbyt nasilonych przypadków z hipokinezją,
częściej razem z
Lewodopą
.
Stosowna w
przełomach akinetycznych
.
Objawy niepożądane:
wewnętrzny niepokój
zaburzenia żołądkowo-jelitowe
Przeciwwskazania:
ciężkie stany hipotonii
Dawkowanie:
do 200mg/dz. (nawet 500-600 mg/dz.)

Triheksyfenidyl
(cholinolityk łatwo przechodzący przez
barierę krew-mózg)
Wskazany zwłaszcza na:
drżenia, akinezy, pocenie się i ślinotok
Objawy uboczne:
jak większość cholinolityków
Przeciwwskazania:
wcześniej zdiagnozowane (innego pochodzenia) zaburzenia
psychoorganiczne
objawy psychotyczne
Dawkowanie:
2-6 mg/dz
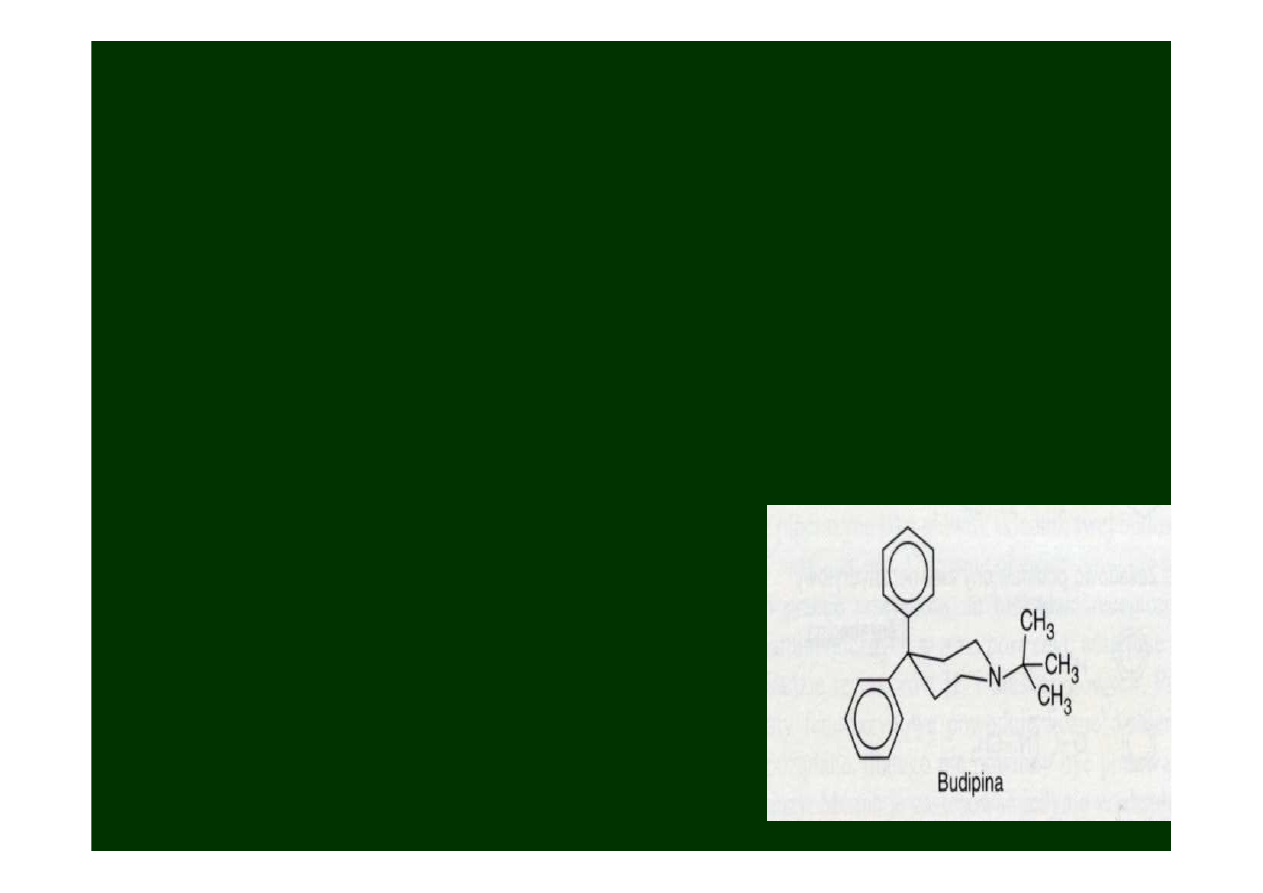
Budypina
(
antagonista receptora NMDA i słaby cholinolityk
)
Stosowana przeważnie z
Lewodopą
-
zmniejszając
drżenia
Objawy uboczne:
cholinolityczne
(
suchość w jamie ustnej, nudności, zaburzenia
akomodacji, omamy
)
Przeciwwskazania:
myasthenia gravis
niewyrównana niewydolność krążenia
w hipokalemii i hipomagnezemii
zmianach rytmu serca

Choroba Parkinsona
-
rokowanie
Skuteczne początkowo leczenie
opóźnia
ostatnie
stadia choroby (inwalidztwo) tylko o kilka lat.
Średni okres trwania choroby wynosi 7,4 lat.
Główne przyczyny zgonu (ok. 70 r.ż.):
choroby serca
zapalenie płuc

Rozwoju
choroby Parkinsona
, nie można wyraźnie
spowolnić, zatrzymać ani mu zapobiec.
Dwie standardowe metody leczenia,
farmakoterapia i
zabiegi chirurgiczne
, mogą jedynie
łagodzić
objawy.
Ostatnio dokonane odkrycia nieprawidłowego
funkcjonowania niektórych białek oraz genetycznych
uwarunkowań choroby podsyciły
nadzieję
na
opracowanie skutecznych metod leczenia..

Kluczowymi zjawiskami w
chorobie Parkinsona
są
zaburzenia zwijania łańcuchów białkowych
oraz
upośledzenie systemu eliminacji nieprawidłowych białek.
Genetyczne podłoże tych problemów zostało już
częściowo poznane.

Skupiska
niewłaściwie zwiniętych białek
, zwane
ciałkami Lewy’ego
, od dziesiątek lat uznawane
są za znak rozpoznawczy
choroby Parkinsona
.
Nie wiadomo jeszcze, czy te zlepki białkowe mają:
działanie ochronne
(uniemożliwiając toksycznym
białkom wyrządzanie szkód),
one same ostatecznie
wyzwalają
proces obumierania
komórek nerwowych.
Oczywiste jest jednak, że to właśnie
źle zwinięte białka
są
podłożem
choroby Parkinsona
.

Loci
Typ Chromosom Gen lub białko Zwi
ą
zek z wyst
ę
powaniem
PARK1
AD
4q21-23
αααα
-synukleina
wczesne wyst
ę
powanie (<50)
PARK2
AR
6q25.2-27 parkina
ró
ż
ne genotypy (#1)
PARK3
AD
2p13
nieznany
pó
ź
ne wyst
ę
powanie (>50)
PARK4
AD
4p15
αααα
-synuc: 3X
zwi
ą
zane z dr
ż
eniem
samoistnym?
PARK5
AD
4p14
UchL1
1 family of 2 (<50 yrs)
PARK6 AR
1p36
PINK1
wczesne wyst
ę
powanie (<50)
PARK7
AR
1p36
DJ-1
rzadkie wczesne
wyst
ę
powanie(<50)
PARK8
AD
12p11q13.1 dardarin
pó
ź
ne wyst
ę
powanie (LRKK2)
PARK9
AR
1p36
nieznany
PARK10
1p32
nieznany
pó
ź
ne wyst
ę
powanie
PARK11 2q36-37 nieznany
pó
ź
ne wyst
ę
powanie
Genetyczne wskaźniki choroby Parkinsona
(10-20% pacjentów )

Nowe komórki
nie zdołałyby
odtworzyć
w całości
uszkodzonych struktur ani też przywrócić utraconych
wspomnień.
Produkowałyby jednak wystarczające ilości
dopaminy
lub
innej potrzebnej w danym obszarze substancji.
Teoretyczne leczenie przy pomocy stosowania komórek macierzystych

Dziękuję
Wyszukiwarka
Podobne podstrony:
choroby afektywne1 prof Mikołajczak
farmakokinetyka ćw prof Mikołajczak
antybiotyki i chemioterapeutyki prof Mikołajczak
AUN1 prof Mikołajczak
Choroby afektywne2 prof Mikołajczak
AIDS prof Mikołajczak
przeciwdrgawkowe prof Mikołajczak
znieczulenie ogólne prof Mikołajczak
ch wrzodowa prof T Starzyńska
derivation flow equation prof J Kleppe
mikolaj2 www prezentacje org
CHOROBA PARKINSONA 4
Reh amb w ch Parkinsona
Choroba Parkinsona
Prof J Chmura(1)
Interakcje wyklad Pani Prof czesc pierwsza i druga 2
więcej podobnych podstron