92723

Chemia fizyczna - termodynamika molekularna 2009/2010 43
M(xlel roztworu doskonałego jest stosowany do opisu rzeczywistych mieszanin, złożonych z podobnych składników (np. 1-butanol + 1-propanol).
4. Roztwór a termalny.
Założenia:
1) Mieszanina złożona jest ze składników zbudowanych z różnej liczby takich samych segmentów.
2) Energia wymiany pomiędzy segmentami wynosi zero.
Składniki tworzące mieszaninę różnią się zatem kształtem i są równoważne energetycznie. Model może być stosowany do opisu mieszanin substancji pochodzących z tego samego łańcucha homologicznego lub polimerów.
Różnica w stosunku do roztworu doskonałego dotyczy udziału kombinatorycznego. Wyraża on liczbę sposobów' na jaką można rozmieścić w węzłach sieci cząsteczki wielosegmentowe.
Zagadnienia tego nic da się rozwiązać w sposób ścisły. Najczęściej używane uproszczenie pochodzi od P. J. Flory’ego (szczegóły w skrypcie).
W w yniku otrzymuje się następujące wyrażenie na potencjał chemiczny p4(7\p,.tł) = pJ(7\/?) + /?7'(ln<p4 -<pt /xk + 1)
gdzie <{>k jest ułamkiem segmentowym składnika k. Dla układu dwuskładnikowego ułamki segmentowe wynoszą
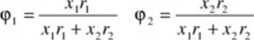
Ponieważ liczba segmentów jest proporcjonalna do objętości molowej, ułamek segmentowy może być zastąpiony przez ułamek objętościowy. Wtedy powyższe równania będą miały postać
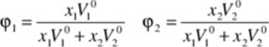
Mianownik ułamków jest molową objętością mieszaniny, a sam ułamek objętościowy określa jaką część objętości roztworu zajmuje dany składnik.
Ze wzoru
n, =n” + R7-|n(.t,v,)
wynika współczynnik aktywności, który równa się
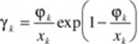
Można wykazać, że współczynniki aktywności są nie większe od jedności, a zatem roztwór aternialny wykazuje ujemne odchylenia od doskonałości.
Mające duże znaczenie praktyczne współczynniki aktywności w rozcieńczeniu nieskończenie wielkim, równają się
Wyszukiwarka
Podobne podstrony:
Chemia fizyczna - termodynamika molekularna 2009/2010 37 Wykład 10 11.12.2009 1. Równania stanu w te
Chemia fizyczna - termodynamika molekularna 2009/2010 52 Wykład 13 15.01.2010 1. O
Chemia fizyczna - termodynamika molekularna 2009/2010 32 Wykład 9 4.12.2009 1. Uogólniona funkcja po
Chemia fizyczna - termodynamika molekularna 2009/2010 7 6. Przykład z życia. Chcemy znaleźć temperat
Chemia fizyczna - termodynamika molekularna 2009/2010 38 Chemia fizyczna - termodynamika molekularna
Chemia fizyczna - termodynamika molekularna 2009/2010 48 ln(? = ln#- kT ^ i Wyrażenie na potencjał
Chemia fizyczna - termodynamika molekularna 2009/2010 53 poprawki i często bywają w ogóle pomijane.
Chemia fizyczna - termodynamika molekularna 2009/2010 8 wnętrze Słońca - 2 000 000 K Czy istnieje sz
Chemia fizyczna • termodynamika molekularna 2009/2010 12 4. W stanic rozważanej równowagi, wszystkie
Chemia fizyczna - termodynamika molekularna 2009/2010 16 występujący w róźnic/cc zupełnej energii
Chemia fizyczna - termodynamika molekularna 2009/2010 20 4. Sprawdzamy ekstensywno
Chemia fizyczna - termodynamika molekularna 2009/2010 25 ć)H dH —— = q.
Chemia fizyczna - termodynamika molekularna 2009/2010 29 Chemia fizyczna - termodynamika molekularna
Chemia fizyczna • termodynamika molekularna 2009/2010 33 Konfiguracyjna funkcja podziału będzie równ
Chemia fizyczna - termodynamika molekularna 2009/2010 1 Wykład 1. 2.10.2009 1. Pla
Chemia fizyczna - termodynamika molekularna 2009/2010 42 Wykładll 18.12.2008 1. Roztwór doskonały w
Chemia fizyczna - termodynamika molekularna 2009/2010 11 Wykład 4 23.10.2009 1.
Chemia fizyczna - termodynamika molekularna 2009/2010 15 Wykład 5 30.10.2009 1. Wa
Chemia fizyczna - termodynamika molekularna 2009/2010 19 Wykład 6 5.11.2009 1. Wątpliwość (wyrażona
więcej podobnych podstron